Низкий ттг при беременности последствия для плода: Аптека Ригла – забронировать лекарства в аптеке и забрать самовывозом по низкой цене в Москва г.
Заболевания щитовидной железы при беременности
Крайне важно раннее выявление и своевременная коррекция заболеваний ЩЖ у женщин с бесплодием, планирующих проведение программ ВРТ (вспомогательных репродуктивных технологий), т.к. это позволит минимизировать неблагоприятное влияние на фертильность (способность производить жизнеспособное потомство), состояние оравиального резерва (фолликулярный запас — число яйцеклеток, потенциально готовых к оплодотворению в данное время) и качество ооцитов, позволит повысить результативность программ ВРТ, снизить риск ранних репродуктивных потерь (самопроизвольные аборты, невынашивание беременности и др.).
Сегодня в эпоху совершенствования методов планирования семьи, развития информационных технологий, важным фактором является повышение знаний женщин планирующих беременность о возможных заболеваниях щитовидной железы и последствиях, которые они могут оказывать в отношении развития беременности, ее течения и непосредственного влияния на плод. Своевременное обращение за медицинской помощью в высококвалифицированные медицинские учреждения еще на этапе планирования беременности позволит вовремя скорректировать имеющиеся нарушения, улучшить показатели фертильности и исходы будущей беременности.
Своевременное обращение за медицинской помощью в высококвалифицированные медицинские учреждения еще на этапе планирования беременности позволит вовремя скорректировать имеющиеся нарушения, улучшить показатели фертильности и исходы будущей беременности.
Следует знать, что уже с первых недель беременности происходят значительные изменения в работе щитовидной железы (повышение продукции тиреоидных гормонов на 30-50%) под воздействием разных эндогенных стимулирующих факторов. Этот физиологический механизм «повышенной работы» ЩЖ во время беременности вполне понятен и оправдан, т.к. до того момента когда у плода начнет функционировать собственная щитовидная железа, весь эмбриогенез (физиологический процесс, в ходе которого происходит образование и развитие эмбриона), в т.ч. формирование центральной нервной системы, происходит при участии тиреоидных гормонов матери!
Так, наиболее мощным стимулятором ЩЖ в I триместре беременности является ХГ (хорионический гонадотропин).
- Гормон начинает вырабатываться тканью хориона после имплантации эмбриона уже на 6-8 день после оплодотворения яйцеклетки и является одним из важнейших показателей наличия и благополучного развития беременности.
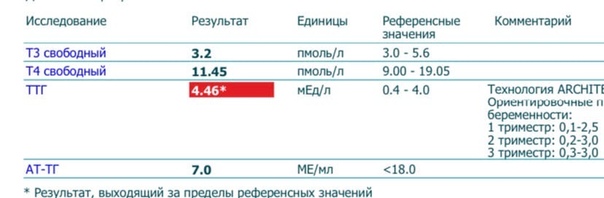
- За счет эффектов ХГ происходит существенное увеличение продукции тиреоидных гормонов ЩЖ. К 18-20-й неделе беременности при участии ряда других механизмов происходит значительное увеличение общего содержания тиреоидных гормонов в организме беременной.
- У 20-30% женщин наблюдается даже развитие так называемого состояния «транзиторного гестационного гипертиреоза» (не требует медикаментозной коррекции).
- Во II-III триместрах беременности тиреоидные гормоны возвращаются к нормальному уровню.
Йод является уникальным и единственным микроэлементом который участвует в образовании гормонов ЩЖ: входит в состав тиреоидных гормонов — три-йод-тиронин (ТЗ) и тетра (=четрые)-йод-тиронин, Т4).
Щитовидная железа плода созревает только к 16-17 недели беременности и начинает функционировать самостоятельно. Для полноценной работы щ/железы плода и образования собственных тиреоидных гормонов, ему необходим йод, который он получает только от матери! Путем трансплацентарного переноса или с молоком матери в период лактации. Тиреоидные гормоны необходимы плоду для полноценного развития и созревания всех его органов (прежде всего на ранних этапах эмбриогенеза), а так же для адекватного формирования центральной нервной системы и правильной адаптации новорожденного к внеутробной жизни.
Тиреоидные гормоны необходимы плоду для полноценного развития и созревания всех его органов (прежде всего на ранних этапах эмбриогенеза), а так же для адекватного формирования центральной нервной системы и правильной адаптации новорожденного к внеутробной жизни.
Во время беременности увеличивается выведение йода с мочой и перенос через плаценту, что обуславливает дополнительную косвенную стимуляцию ЩЖ женщины. Однако в условиях йоддефицита (вся территория РФ!) у беременной на фоне повышенной потери в йоде подключение мощных компенсаторных механизмов может не хватить для обеспечения значительного увеличения продукции тиреоидных гормонов ЩЖ, что часто приводит к развитию у беременной зоба (увеличение размеров щ/железы выше нормальных показателей — 18 смЗ).
Дефицит йода на фоне беременности может отразиться на развитии плода и привести к перинатальным осложнениям (патологические состояния и заболевания плода после 28-недели и в периода новорожденности) — самопроизвольные аборты, мертворождения, врожденные аномалии развития, эндемический кретинизм (слабоумие), зоб/врожденное снижение функции ЩЖ (гипотиреоз) у новорожденного, в последующей жизни — эндемический зоб, необратимое снижение умственных способностей (интеллектуальное и неврологическое развитие), снижение фертильности.
С учетом вышеизложенного становится понятным, что потребность в йоде у беременной женщины возрастает, и ей требуется адекватное потребление йода во время беременности (в дозе не менее 250 мкг/сутки в составе препаратов йода по рекомендациям ВОЗ) для полноценного функционирования собственной щитовидной железы, а так же (с увеличение сроков гестации) сформировавшейся щитовидной железы плода.
Следует еще раз подчеркнуть, что при наличии адекватных количеств основного компонента синтеза тиреоидных гормонов — йода — не будет наблюдаться каких-либо неблагоприятных последствий со стороны течения беременности и развития плода!
Уже на этапе планирования беременности женщинам целесообразно назначение индивидуальной йодной профилактики физиологическими дозами йода (200 мкг/сут. — например, одна таблетка препарата «Иодомарин» или «ЙодБаланс» ежедневно). Профилактика дефицита йода у детей до 1 года — грудное вскармливание и прием матерью препаратов йода в дозе 250 мкг/сути весь период кормления или смеси для доношенных детей с содержанием йода 100 мкг/л.
Заболевания ЩЖ у женщин приводящие либо к снижению функции (ГИПОТИРЕОЗ) либо повышению ее функции (ТИРЕОТОКСИКОЗ) могут приводить к нарушению фертильности и являться фактором риска осложнений течения беременности и нарушений развития плода.
Гипотиреоз
В ситуации, когда у женщины еще до беременности имеет место заболевание ЩЖ, приводящее к снижению ее функции (гипотиреоз), физиологическая гиперстимуляция ЩЖ во время наступившей беременности (самостоятельно или в программах ЭКО) в той или иной степени затрагивает ее резервные возможности, и даже использование мощных компенсаторных механизмов оказывается недостаточной для обеспечения столь значительного увеличения продукции тиреоидных гормонов во время беременности.
Гипотиреоз во время беременности наиболее опасен для развития плода и в первую очередь поражением центральной нервной системы, внутриутробной гибелью, формированием врожденных пороков развития, а так же рождением ребенка с малым весом, неврологическими заболеваниями у новорожденного. Состояние гипотиреоза у матери повышает риск самопроизвольных абортов, послеродовых кровотечений, преэклампсии (нарушение мозгового кровообращения, что может привести к отеку мозга, повышению внутричерепного давления, функциональным нарушениям нервной системы).
Состояние гипотиреоза у матери повышает риск самопроизвольных абортов, послеродовых кровотечений, преэклампсии (нарушение мозгового кровообращения, что может привести к отеку мозга, повышению внутричерепного давления, функциональным нарушениям нервной системы).
Оценка функции ЩЖ проводится всем женщинам с нарушениями репродуктивной функции (бесплодием, невынашиванием беременности и др.). Своевременная коррекция нарушений функции щитовидной железы осуществляется эндокринологом на этапе подготовки к программам ВРТ!
Компенсированный гипотиреоз не является противопоказанием для планирования беременности в т.ч. в программах ВРТ! (у женщин с компенсированным гипотиреозом при наступлении беременности и возрастанием потребности в тиреоидных гормонах доза левотироксина (L-Т4), которую они принимали до беременности, сразу увеличивают примерно на 30-50%).
Оценка функции щитовидной железы проводится только по уровню тиреотропного гормона («ТТГ») крови (гормон, выделяемый передней долей гипофиза — железы, находящейся на нижней поверхности мозга, и оказывающей непосредственное стимулирующее влияние на работу ЩЖ).
Как упоминалось выше, в норме на ранних сроках беременности характерен высоконормальный или даже повышенный уровень тиреоидных гормонов, в связи с чем «по принципу отрицательной обратной связи» будет отмечаться низкий или даже подавленный (у 20-30% женщин) уровень ТТГ: < 2,5 мЕд/л.
Скрининг на нарушения функции ЩЖ целесообразно проводить в самые ранние сроки: лучше во время определения (β-субъединицы ХГ для констатации беременности!
Если уровень ТТГ превышает 2,5 мМЕ/л, женщине показана заместительная терапия препаратами левотироксина (L-Т4). Контроль уровня ТТГ и Т4 крови целесообразно проводить каждые 4 недели в I триместре, и далее по необходимости. Адекватной заместительной терапией считается поддержание уровня ТТГ на нижней границе референсных значений для соответствующего срока беременности.
Тиреотоксикоз
Тиреотоксикоз (повышенная функция щитовидной железы) во время беременности развивается относительно редко (в 1-2 на 1000 беременностей). Практически все случаи тиреотоксикоза у беременных женщин связаны с болезнью Грейвса (БГ или токсический диффузный зоб, хроническое аутоиммунное нарушение, при котором наблюдается увеличение и гиперфункция щитовидной железы) развитием гипертиреоза на фоне стимулирующего влияния ХГЧ. Если у женщины до беременности была болезнь Грейвса, то риск обострения (рецидива) заболевания высокий в ранний период беременности.
Практически все случаи тиреотоксикоза у беременных женщин связаны с болезнью Грейвса (БГ или токсический диффузный зоб, хроническое аутоиммунное нарушение, при котором наблюдается увеличение и гиперфункция щитовидной железы) развитием гипертиреоза на фоне стимулирующего влияния ХГЧ. Если у женщины до беременности была болезнь Грейвса, то риск обострения (рецидива) заболевания высокий в ранний период беременности.
Неадекватное лечение тиреотоксикоза связано с развитием осложнений: самопроизвольный аборт, замедленное внутриутробное развитие плода, мертворождение, преждевременные роды, преэклампсия, сердечная недостаточность.
Если женщина с болезнью Грейвса планирует проведение программ ВРТ, то только на фоне стойкой нормализации функции щитовидной железы (минимум через 24 месяца т.е. 18 месяцев лечение + нормальные показатели тиреоидных гормонов в течение минимум 6 месяцев без лечения!). Неадекватно пролеченная Болезнь Грейвас четко связана с неблагоприятными исходами беременности, в частности риском невынашивания, в программах ВРТ!
Оценка функции щитовидной железы проводится по уровню тиреотропного гормона (ТТГ), тиреоидных гормонов крови (Т4, ТЗ) с оценкой титра «тиреоидстимулирующих» АТ в крови (АТ к рТТГ, должны быть значимо повышены!).
Согласно современным представлениям, тиреотоксикоз на фоне болезни Грейвса не является показанием для прерывания беременности, поскольку в настоящее время разработаны эффективные и относительно безопасные методы консервативного лечения данного заболевания.
В случае, если у беременной женщины (в т.ч. молодой с сохраненным овариальным резервом и планирующей ВРТ) имеет место тиреотоксикоз, то основной целью лечения является назначение тиреостатиков (лекарственные препараты, которые подавляют синтез гормонов щитовидной железы) в минимально эффективной дозе для поддержания уровня Т4 на верхней границе нормы или несколько выше нормы. Препаратом выбора (с учетом безопасности для плода) в I триместре считается пропилтиоурацил (ПТУ), со второго триместра — используется тиамазол (тирозол) в эквивалентной дозе. Контроль уровня Т4, ТЗ проводится каждые 4 недели.
С увеличением срока беременности закономерно происходит уменьшение тяжести тиреотоксикоза и снижение потребности в препаратах, которые у большинства женщин в III триместре беременности, как правило, полностью отменяют. При приеме малых доз ПТУ (100 мг/сут) или тирозола (5-10 мг) грудное вскармливание достаточно безопасно для ребенка. Однако через 2-3 месяца после родов в большинстве случаев развивается рецидив (утяжеление) тиреотоксикоза, требующий увеличения дозы тиреостатика.
При приеме малых доз ПТУ (100 мг/сут) или тирозола (5-10 мг) грудное вскармливание достаточно безопасно для ребенка. Однако через 2-3 месяца после родов в большинстве случаев развивается рецидив (утяжеление) тиреотоксикоза, требующий увеличения дозы тиреостатика.
Альтернативным методом лечения тиреотоксикоза у женщины вне беременности (в т.ч. молодой с сохраненным овариальным резервом и планирующей ВРТ) на фоне болезни Грейвса (или его рецидива после терапии тиреостатиками) может быть терапия радиоактивным йодом (I-131). После терапии радиоактивным йодом планирование самостоятельной беременности или проведение программ ВРТ возможно только через 12 месяцев после окончания лечения, в течение всего периода лечения (12 мес.) необходимо использовать эффективные методы контрацепции — терапия радиоактивным йодом в период беременности и лактации противопоказана!
Следует знать, что у женщин старшего репродуктивного возраста (старше 35 лет) со сниженным овариальным резервом методом выбора лечения болезни Грейвса является хирургическое — удаление щитовидной железы (тиреоидэктомия). Такая тактика лечения признана наиболее эффективной и безопасной и дает возможность планировать проведение ВРТ в максимально короткие сроки! Тактика длительного лечения тиреостатиками (более 1,5 лет) и последующее наблюдение (6 месяцев) для подтверждения стойкой нормализации функции ЩЖ, а так же высокая вероятность рецидива тиреотоксикоза во время беременности в программах ВРТ не оправдана у женщин позднего репродуктивного возраста.
Такая тактика лечения признана наиболее эффективной и безопасной и дает возможность планировать проведение ВРТ в максимально короткие сроки! Тактика длительного лечения тиреостатиками (более 1,5 лет) и последующее наблюдение (6 месяцев) для подтверждения стойкой нормализации функции ЩЖ, а так же высокая вероятность рецидива тиреотоксикоза во время беременности в программах ВРТ не оправдана у женщин позднего репродуктивного возраста.
Нередко в послеродовом периоде происходит обострение заболевания ЩЖ (у 5-9% всех женщин), которое имело место у матери до зачатия. Поэтому после родов такие женщины должны продолжать наблюдаться у эндокринолога.
Послеродовой тиреоидит
Данное состояние характеризуется временным нарушением функции ЩЖ, возникающим на протяжении первого года после родов. В патогенезе (механизм зарождения и развития болезни) послеродового тиреоидита лежит аутоиммунное воспаление ЩЖ развивающееся на фоне генетической предрасположенности (установлена четкая взаимосвязь с генами НЬА-А26/ ВW46/ВW67/А1/В8 у женщин с данным заболеванием). Основное значение в развитии послеродового тиреоидита отводится иммунной реакции, или феномену «рикошета», который заключается в резком увеличении активности иммунной системы после ее долгого как известно физиологического подавления во время беременности, что у предрасположенных лиц может спровоцировать развитие аутоиммунного заболевания ЩЖ.
Основное значение в развитии послеродового тиреоидита отводится иммунной реакции, или феномену «рикошета», который заключается в резком увеличении активности иммунной системы после ее долгого как известно физиологического подавления во время беременности, что у предрасположенных лиц может спровоцировать развитие аутоиммунного заболевания ЩЖ.
Классическая клиническая картина включает в себя трехфазный процесс.
Вначале через 8-12 недель после родов развивается транзиторный гипертиреоз (повышенный уровень тиреоидных гормонов в крови), обусловленный высвобождением в кровь готовых тиреоидных гормонов, запасенных в ЩЖ, продолжается в среднем 1-2 месяцев, специфического лечения не требуется.
Затем следует фаза восстановления функции ЩЖ, завершающаяся фазой гипотиреоза (снижением функции ЩЖ), при которой уже необходимо назначение заместительной терапии препаратами тиреоидных гормонов (L-Т4).
Гипотиреоидная фаза имеет большое количество симптомов: депрессия, раздражительность, сухость кожи, астения, повышенная утомляемость, головная боль, снижение способности, концентрации внимания, склонность к запорам, мышечные и суставные боли.
Контроль гормонов крови (ТТГ, Т4) проводится каждые 4 недели. Через 6-8 месяцев функция ЩЖ, как правило, восстанавливается.
Автор статьи Татьяна Юрьевна Голицына, врач-эндокринолог Института репродуктивной медицины REMEDI
Низкий ТТГ при беременности: состояние нормы или угроза?
Низкий ТТГ при беременности является нормой у здоровых женщин. Однако бывает, что снижение гормона сильно сказывается на самочувствии будущей мамы. В этом случае говорят о патологических изменениях в организме. Именно по этой причине во время беременности необходим контроль за гормонами, оказывающими влияние на деятельность щитовидной железы.
Что такое тиреотропный гормон
Тиреотропный гормон (тиротропин или ТТГ) – гормон гипофиза, контролирующий правильное развитие и работу щитовидной железы, а также выработку основных гормонов – трийодтиронина (Т3) и тироксина (Т4). Эти гормоны отвечают за состояние сердечно-сосудистой, половой, нервной систем и регулируют обмен веществ./113/113.jpg)
Регуляция выработки гормона осуществляется нейрогормонами гипоталамо-гипофизарной системы. Важность трех перечисленных элементов трудно переоценить, поскольку они регулируют практически все процессы, происходящие в организме: уровень артериального давления, частоту сердцебиения, уровень кислорода в крови и т.д. Гормоны поддерживают нормальный гомеостаз и температуру тела.
Общий тиротропин зависит от величин Т3 и Т4. Они подавляют его чрезмерную выработку. Нормативное значение тиреотропина находится в диапазоне 0,4-4 мЕд/л у небеременных женщин, и 0,2-3,5 у беременных. Т4 в норме составляет от 110 до 130 нМ/л, а Т3 – от 2,5 до 5,8 пмоль/л. Небольшие отклонения в ту или иную сторону допускаются, но только если остальные показатели и самочувствие в норме.
Влияние низкого ТТГ
Поскольку ТТГ регулирует процессы клеточного размножения, он влияет и на желтое тело, способствуя сохранению беременности в первом триместре. Под контролем тиротропина закладываются органы плода и осуществляется его развитие.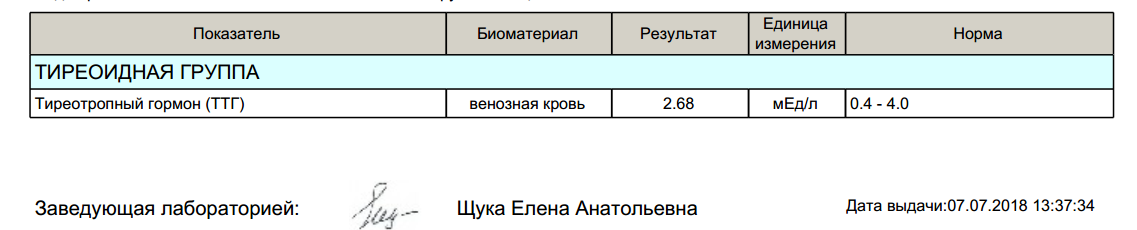 По этой причине при планировании беременности желательно в список исследований включить анализ на Т3, Т4 и ТТГ.
По этой причине при планировании беременности желательно в список исследований включить анализ на Т3, Т4 и ТТГ.
При беременности пониженный ТТГ является достаточно частым явлением. Особенно это касается многоплодной беременности. Если ТТГ слишком низкий, то показать его наличие может только высокочувствительный тест. При некачественном анализе уровень будет нулевым.
Лучше всего измерять тиреотропин в середине каждого триместра. Но особенно проблемным является первый период. Уровень ТТГ в это время постоянно меняется и его достаточно трудно определить. Но это необходимо, поскольку иногда недостаточность сохраняется всю беременность и не приходит в норму даже после родов. Если в первом триместре выявлен гормональный недостаток, то сдавать кровь на гормоны щитовидной железы нужно постоянно.
Наши читатели рекомендуют!Для профилактики и лечения заболеваний щитовидной железы наши читатели советуют «Монастырский Чай». Он состоит из 16 самых полезных лекарственных трав, которые обладают крайне высокой эффективностью при профилактике и в лечении щитовидной железы, а также при очищении организма в целом. Эффективность и безопасность Монастырского чая неоднократно доказана клиническими исследованиями и многолетним терапевтическим опытом. Мнение врачей… »
Эффективность и безопасность Монастырского чая неоднократно доказана клиническими исследованиями и многолетним терапевтическим опытом. Мнение врачей… »
Таким образом, влияние тиреотропина на развитие плода и сохранение беременности значительно. Поэтому необходимо следить, чтобы его уровень и на этапе планирования, и во время беременности сохранялся в рамках нормальных значений.
Почему снижается ТТГ во время беременности
Чтобы вовремя выявить дисфункцию щитовидной железы необходимо знать, от чего снижается ТТГ. С первых недель беременности значительно увеличивается нагрузка на железу. Главным стимулятором является ХГЧ – главный гормон беременности. Он увеличивает производство Т3 и Т4.
Благодаря увеличению гормонального уровня, уровень ТТГ опускается ниже нормы. В первом триместре небольшое снижение является нормой, но если речь идет о нулевом уровне, то стоит найти причину и устранить ее.
Выработка ХГЧ снижается к 13 неделе, и щитовидная железа стабилизируется. Поэтому при нормальном функционировании органа, уровень ТТГ во втором триместре должен прийти в норму.
Поэтому при нормальном функционировании органа, уровень ТТГ во втором триместре должен прийти в норму.
Основными причинами того, что тиротропин имеет низкий уровень, помимо первого триместра беременности, являются:
- гормональный дисбаланс, при котором снижается выработка ХГЧ;
- тиреотоксикоз;
- вторичный гипотиреоз;
- синдром эутиреоидной патологии.
Помимо этого, к снижению уровня ТТГ ведет длительный психологический стресс и неполноценное питание.
Таким образом, если до беременности были выявлены проблемы со щитовидкой, то необходимо тщательно следить за показателями, и если ТТГ понижен, то принимать соответствующую терапию.
Симптомы низкого уровня ТТГ
Основными симптомами низкого ТТГ у беременной являются:
- усиленная рвота в любом из триместров;
- депрессия, эмоциональные перепады;
- бледность и сухость кожных покровов;
- боль в суставах.
Кроме этого, может наблюдаться двоение в глазах, повышенная потливость и нестабильность артериального давления. Данные симптомы неприятны сами по себе и опасны для будущей мамы. При обнаружении 2-3 признаков из списка необходимо сдать анализ на ТТГ даже если ранее не было проблем.
Данные симптомы неприятны сами по себе и опасны для будущей мамы. При обнаружении 2-3 признаков из списка необходимо сдать анализ на ТТГ даже если ранее не было проблем.
Врач должен провести дифференциальную диагностику, поскольку снижение уровня гормона возможно и при тиреотоксикозе. Основным симптомом при этой болезни является потеря массы тела, что нехарактерно для беременных. Дифференциальная диагностика проводится посредством УЗИ. Если ультразвуковое исследование не выявило проблему в щитовидной железе, то, возможно, она заключается в сбое работы гипофиза. В этом случае врач назначает дополнительные исследования – УЗИ головного мозга и МРТ.
Таким образом, низкий ТТГ во время беременности имеет достаточно серьезные последствия, и оказывает влияние и на маму, и на будущего ребенка. При обнаружении симптомов недостаточности нужно незамедлительно обратиться к врачу. В случае, если будет выявлена патология специалист назначит лечение, которое отлично сочетается с беременностью.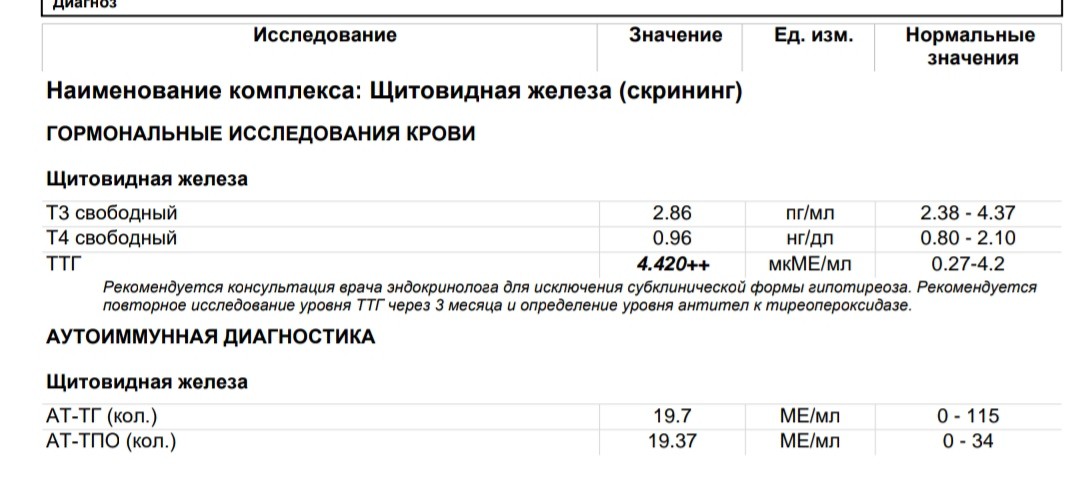
Все равно кажется, что вылечить щитовидку непросто?
Учитывая, что Вы сейчас читаете эту статью, можно сделать вывод, что этот недуг до сих пор не дает Вам покоя.
Вас наверняка также посещали мысли о хирургическом вмешательстве. Оно и ясно, ведь щитовидная железа — один из важнейших органов, от которого зависит Ваше хорошее самочувствие и здоровье. А отдышка, постоянная усталость, раздражительность и прочие симптомы явно мешают наслаждаться Вам жизнью…
Но, согласитесь, правильнее лечить причину, а не следствие. Рекомендуем прочесть историю Ирины Савенковой о том как ей удалось вылечить щитовидную железу…
Читать далее »
загрузка…
Заболевания щитовидной железы и беременность | Бурумкулова
В своей практике как эндокринологи, так и акушеры-гинекологи часто встречаются с различными заболеваниями щитовидной железы (ЩЖ) у беременных, что представляет собой значительный клинический и научный интерес как для изучения патологии этих нарушений, так и в плане их лечения.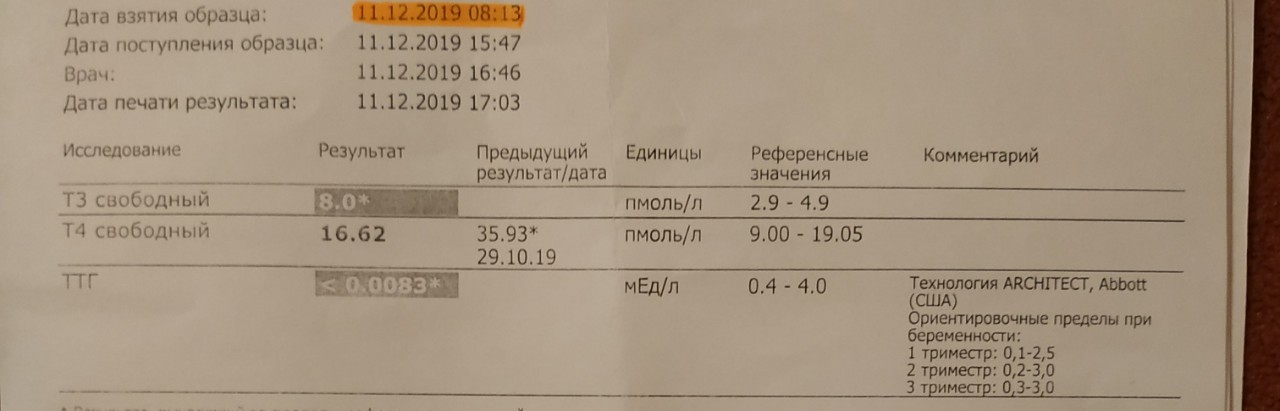
Как известно, беременность часто ведет к возникновению зоба. Увеличение размеров и объема ЩЖ во время беременности наблюдается вследствие как более интенсивного кровоснабжения ткани ЩЖ, так и увеличения массы ткани ЩЖ. Стимулировать функцию ЩЖ во время беременности могут 3 фактора: возрастание степени связывания тиреоидных гормонов (ТГ) с белками крови, повышение уровня хорионического гонадотропина (ХГ) в крови беременных и недостаточное снабжение ЩЖ йодом в связи с повышенной экскрецией йода с мочой во время беременности (см. рисунок).
Возрастание связывания ТГ с белками крови. Более 99% циркулирующих в крови ТГ связано с белками плазмы: тироксинсвязывающим глобулином (ТСГ), тироксинсвязывающим преальбуми- ном и альбумином. Относительное распределение величины связывания ТГ с различными связывающими белками напрямую зависит от степени их сродства и концентрации. 80% ТГ связано с ТСГ. Связанная и неактивная фракции ТГ находятся в равновесии со «свободной» несвязанной фракцией, которая представляет собой лишь небольшую долю всех циркулирующих ТГ: 0,03—0,04% для свободного тироксина (свТ4) и 0,3—0,5% для свободного трийодтиронина (свТ3).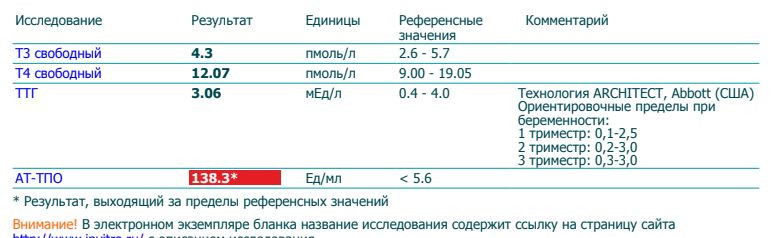 Однако именно эта фракция обеспечивает всю метаболическую и биологическую активность ТГ.
Однако именно эта фракция обеспечивает всю метаболическую и биологическую активность ТГ.
При беременности, уже через несколько недель после зачатия сывороточный уровень ТСГ прогрессивно повышается в результате стимуляции значительным количеством эстрогенов, вырабатываемых плацентой. Затем уровень ТСГ достигает плато, которое поддерживается до момента родов. И, напротив, уровень 2 других циркулирующих связывающих белков имеет тенденцию к снижению, главным образом в результате пассивного
Схема стимуляции ЩЖ при беременности
разведения вследствие увеличенного сосудистого пула (кровяного депо).
Результатом повышения при беременности продукции ТСГ является повышение общего уровня ТГ. Уровни общих Т4 (обТ4) и Т3 (обТ3) -значительно повышаются в течение первой половины беременности и достигают плато к 20-й неделе, оставаясь в дальнейшем на том же уровне. Транзи- торное снижение количества свТ4 и свТз по принципу обратной связи стимулирует высвобождение тиреотропного гормона (ТТГ) и восстановление гомеостаза уровня свободных форм ТГ.
Адекватное поддержание тиреоидного гомеостаза нарушено примерно у 1/3 беременных женщин, что приводит к развитию состояния относительной гипотироксинемии.
Стимуляция функции ЩЖ во время беременности ХГ. ХГ секретируется плацентой только у приматов. Он вырабатывается в больших количествах синцитиотрофобластом плаценты, особенно в первой четверти беременности. Важнейшая функция ХГ — стимуляция стероидогенеза сначала в желтом теле, затем в плаценте.
Значение ХГ для стимуляции ЩЖ женщин во время беременности не до конца изучено. Известно, что существует корреляция между подавлением секреции ТТГ и повышением концентрации ХГ, а также между уровнем ХГ и уровнем свТ4. ХГ способен оказывать прямое стимулирующее действие на ЩЖ матери (причем это влияние наиболее выражено в конце I триместра беременности) благодаря молекулярному сходству ХГ с ТТГ. Действуя на ранних сроках беременности как слабый ’’аналог” ТТГ, ХГ ответствен за небольшое повышение сывороточных уровней свТ4 и свТ3 и как следствие за снижение сывороточного уровня ТТГ. У подавляющего большинства здоровых беременных сти- муляторный эффект ХГ на ЩЖ является коротким и незначительным. Однако у 1—2% всех беременных во время I триместра беременности отмечается снижение концентрации ТТГ и повышение уровня свТ3, что сопровождается клиникой тиреотоксикоза. Этот синдром получил название ’’гестационный транзиторный тиреотоксикоз” (ГТТ).
У подавляющего большинства здоровых беременных сти- муляторный эффект ХГ на ЩЖ является коротким и незначительным. Однако у 1—2% всех беременных во время I триместра беременности отмечается снижение концентрации ТТГ и повышение уровня свТ3, что сопровождается клиникой тиреотоксикоза. Этот синдром получил название ’’гестационный транзиторный тиреотоксикоз” (ГТТ).
Возможными причинами повышения уровня ХГ и развития ГТТ могут быть следующие: 1) несбалансированная продукция ХГ вследствие тран- зиторной суперэкспрессии гена, кодирующего Р-субъединицу ХГ; 2) изменения в степени гликозилирования молекулы ХГ, что в свою очередь приводит к удлинению периода его полувыведения; 3) увеличение массы синцитиальных клеток трофобласта плаценты у некоторых женщин (например, при многоплодной беременности). При многоплодной беременности концентрация ХГ возрастает пропорционально числу плацент.
ГТТ нередко сопровождается неукротимой рвотой беременных (hyperemesis gravidatum), что затрудняет его диагностику из-за того, что на ранних сроках беременности в принципе характерны тошнота и рвота. Это состояние обычно носит транзиторный характер и разрешается ко II триместру беременности. Диагноз ГТТ ставят на основании повышенного уровня ХГ, незначительно подавленной концентрации ТТГ, увеличения сывороточных уровней свТ4 и свТ3 до показателей, характерных для гипертиреоза. Лечение тиреостатиками ГТТ не показано; при выраженных клинических симптомах достаточно только короткого курса р-адреноб- локаторов.
Это состояние обычно носит транзиторный характер и разрешается ко II триместру беременности. Диагноз ГТТ ставят на основании повышенного уровня ХГ, незначительно подавленной концентрации ТТГ, увеличения сывороточных уровней свТ4 и свТ3 до показателей, характерных для гипертиреоза. Лечение тиреостатиками ГТТ не показано; при выраженных клинических симптомах достаточно только короткого курса р-адреноб- локаторов.
Таким образом, клиницистам важно знать, что симптоматика тиреотоксикоза при беременности имеет специфические отличия и может являться следствием не только аутоиммунного процесса в ЩЖ, но и гормональных изменений, присущих собственно беременности.
Понижение доступности йода при одновременном повышении потребности в нем при беременности. Повышение потребности в йоде во время беременности связано с двумя факторами. С одной стороны, при беременности наблюдается дополнительная потеря йода из организма матери за счет усиленного почечного клиренса йодида, с другой — потеря йодида во второй половине беременности усиливается из-за того, что часть материнского пула неорганического йодида потребляется фето- плацентарным комплексом и идет на синтез ТГ ЩЖ плода.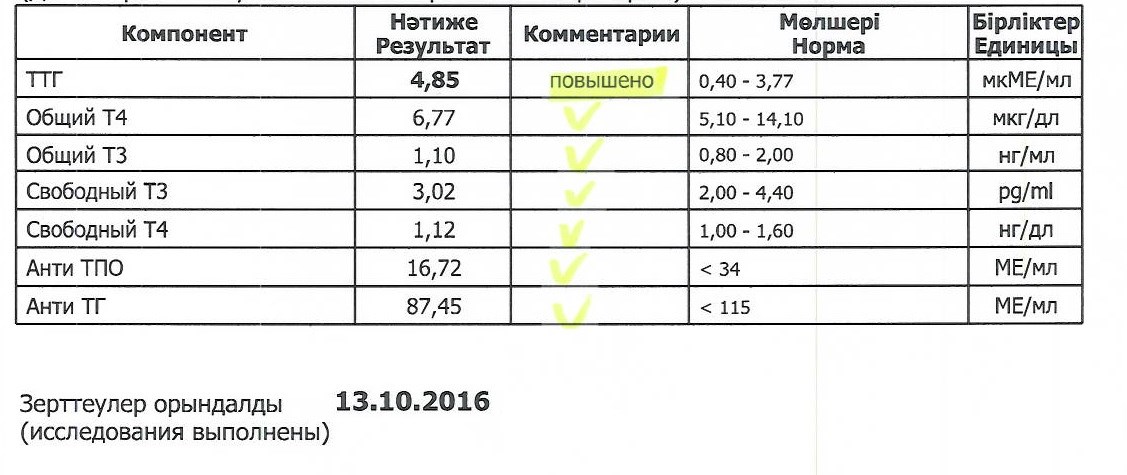
Для женщин, проживающих в странах с достаточным уровнем потребления йода (таких, как Япония, США или Скандинавия), потеря йода во время беременности не имеет существенного значения, поскольку суточное потребление йода составляет больше 150—200 мкг/сут и остается удовлетворительном в течение всей беременности.
В то же время в регионах с умеренной и тяжелой степенью йодного дефицита в биосфере, к которым относится подавляющая часть территории России, пониженное потребление йода (менее 100 мкг/сут) является довольно жестким фактором стимуляции ЩЖ во время беременности.
Риск развития заболевания ЩЖ во время беременности выше у женщин с наличием в анамнезе зоба (диффузного или узлового), причем количество и размер узлов могут увеличиваться во время беременности. Повторная беременность приводит к дальнейшему увеличению размеров ЩЖ и усилению узлообразования.
В 1989 г. D. Glinoer и соавт. предложили гипотезу, согласно которой усиленная тиреоидная стимуляция во время беременности может вести к образованию диффузного нетоксического зоба (ДНЗ), а беременность представляет собой один из факторов, вызывающих патологические изменения в ЩЖ.
В клинической практике для выявления повышенной тиреоидной стимуляции во время беременности было предложено использовать следующие биохимические показатели.
— Наличие относительной гипотироксинемии, наблюдаемой примерно у 1/3 всех беременных. Для ее диагностики рекомендуются определенные отношения Т4/ТСГ.
— Увеличение секреции Т3, проявляющееся в повышении отношения Т3/Т4 более 0,025 и отражающее стимуляцию ЩЖ в условиях йодного дефицита.
— Изменение концентрации ТТГ в крови. После начальной фазы подавления уровня ТТГ вследствие высокой секреции ХГ в конце I триместра беременности уровень ТТГ прогрессивно повышается и его концентрация к моменту родов удваивается по отношению к исходной. Повышение уровня ТТГ обычно остается в пределах нормы (<4 мЕД/л).
— Изменение концентрации тиреоглобулина (Тг) в сыворотке крови. Сывороточный уровень Тг представляет собой чувствительный индикатор стимуляции ЩЖ, который часто повышается во время беременности : его увеличение наблюдается уже в I триместре, однако наиболее явно выражено в III триместре и к моменту родов. К моменту родов 60% беременных имеют повышенный уровень Тг в крови.
К моменту родов 60% беременных имеют повышенный уровень Тг в крови.
Увеличение концентрации Тг коррелирует с другими показателями тиреоидной стимуляции, такими как небольшое повышение уровня ТТГ и увеличение отношения Т3/Т4 более 0,025. Наличие кореляции между уровнем Тг и объемом ЩЖ (по данным ультразвукового исследования — УЗИ подтверждает, что уровень Тг в крови представляет собой достаточно надежный биохимический маркер зобогенного действия беременности.
Недостаточное потребление йода во время беременности оказывает отрицательное влияние на ЩЖ плода и в дальнейшем на интеллектуальное и физическое развитие ребенка. Как известно, ЩЖ плода приобретает способность концентрировать йод и синтезировать йодтиронины на 10—12-й неделе внутриутробного развития. Средние показатели концентрации свТ4, обТ4 и ТСГ достигают уровня, характерного для взрослых, примерно на 36-й неделе беременности.
Вопрос о проницаемости плаценты для ТГ длительное время остается дискуссионным. В настоящее время предполагается, что ЩЖ матери и плода регулируются автономно, однако не независимо друг от друга. По-видимому, трансплацентарный переход ТГ из организма матери к плоду наблюдается только на ранней стадии внутриутробного развития.
В настоящее время предполагается, что ЩЖ матери и плода регулируются автономно, однако не независимо друг от друга. По-видимому, трансплацентарный переход ТГ из организма матери к плоду наблюдается только на ранней стадии внутриутробного развития.
Кроме того, активность ЩЖ плода полностью зависит от поступления йода из материнского организма. В результате как недостаточного поступления йода в организм матери, так и низкого собственного интратиреоидного запаса йода происходит стимуляция ЩЖ плода, что находит отражение в значительном повышении (по сравнению с аналогичными показателями матери) уровней неонатального ТТГ и Тг, а также развитии зоба у плода. Развитие гипотиреоза во внутриутробном и неонатальном периодах может привести к необратимому снижению умственного развития ребенка вплоть до эндемического кретинизма.
Для лечения ДНЗ при беременности в регионах с недостаточным потреблением йода целесообразно рекомендовать прием йода из расчета 150—250 мкг/сут. Для этого можно использовать имеющийся в аптечной сети препарат «Антиструмин» (1000 мкг калия йодида в 1 таблетке) по 1 таблетке 1—2 раза в неделю.
Другим препаратом йода являются таблетки ’’Калия йодид-200″, выпускаемые фирмой «Бер- лин-Хеми». Их надо принимать ежедневно. Альтернативой могут служить импортные поливитамины, содержащие суточную дозу йода (150 мкг). Как правило, этих назначений будет достаточно, чтобы предотвратить дальнейший рост зоба и даже достигнуть уменьшения его объема.
При наличии большого зоба до беременности или при его быстром росте в начале беременности оправдано назначение комбинации йода и тиреоидных гормонов: либо препарат «Тиреокомб», содержащий 70 мкг Т4, 10 мкг Т3 и 150 мкг йода, либо 50—100 мкг Т4 ежедневно и дополнительно 1 таблетку антиструмина 2—3 раза в неделю. Это позволяет быстро и эффективно восстановить нормальную функцию ЩЖ матери и предупредить зобогенный эффект беременности.
Развитие гипертиреоза во время беременности встречается относительно редко и наблюдается у 0,05—3% беременных женщин. В большинстве случаев его причиной является диффузный токсический зоб (ДТЗ), в то время как токсическая аденома или многоузловой токсический зоб встречаются гораздо реже.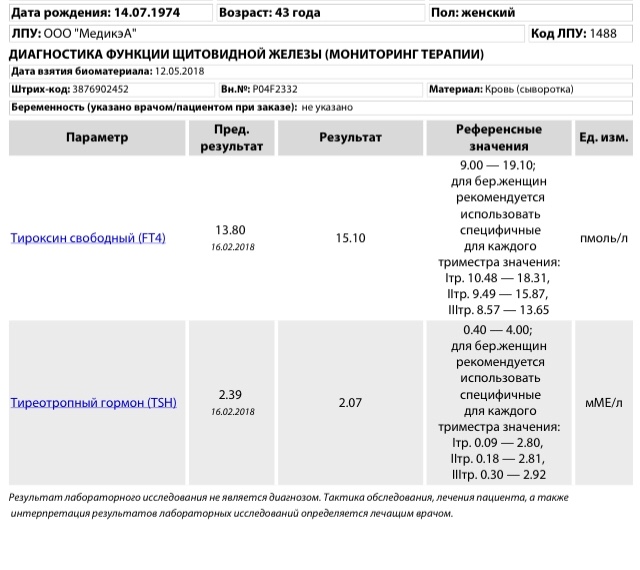 обТ4 и обТ3, что не отражает истинного функционального состояния ЩЖ.
обТ4 и обТ3, что не отражает истинного функционального состояния ЩЖ.
Для лечения ДТЗ у беременных во всех странах предпочтение отдается тиреостатическим препаратам (мерказолил, метимазол, пропилтиоурацил). Хирургическое лечение рекомендуется только в исключительных случаях, таких как выраженные побочные эффекты, зоб очень большого размера, подозрение на малигнизацию или необходимость использовать высокие дозы тиреостатиков для поддержания эутиреоза у матери. Оптимальным сроком для проведения субтотальной резекции ЩЖ считается II триместр беременности. Назна-‘ чение йодидов во время беременности противопоказано из-за риска развития гипотиреоза у плода и — зоба вследствие эффекта Вольфа—Чайкова.
Каких же принципов следует придерживаться при лечении беременной с ДТЗ?
- Выбор конкретного тиреостатика определяется как личным опытом врача, так и доступностью того или иного препарата. В нашей стране для лечения ДТЗ на фоне беременности чаще применяют мерказолил (1 -метил-2-меркаптоимидазол) или его аналоги (метимазол, тиамазол).
 За рубежом в аналогичной ситуации предпочтение отдается пропилтиоурацилу (6-пропил-2-тиоурацил). В настоящее время в России зарегистрирован и стал доступен препарат этой группы под названием «Пропи- цил» (фирма «Кали-Хеми).
За рубежом в аналогичной ситуации предпочтение отдается пропилтиоурацилу (6-пропил-2-тиоурацил). В настоящее время в России зарегистрирован и стал доступен препарат этой группы под названием «Пропи- цил» (фирма «Кали-Хеми).
Частота побочных эффектов терапии одинакова для пропилтиоурацила и мерказолила. Оба препарата проникают через плаценту, и чрезмерные их дозы могут вызвать развитие гипотиреоза и зоба во внутриутробном и неонатальном периодах.
Назначение пропилтиоурацила при беременности тем не менее имеет ряд преимуществ. Во-первых, кинетика пропилтиоурацила не меняется при беременности, во-вторых, период полувыведения пропилтиоурацила из крови не зависит от наличия печеночной или почечной недостаточности, в- третьих, пропилтиоурацил в большей степени по сравнению с мерказолилом связывается с белками и обладает ограниченной липофильностью, что затрудняет его проникновение через биологические мембраны, такие как плацента и эпителий молочной железы.
- Клиническое улучшение при лечении тиона- мидами проявляется уже к концу 1-й недели терапии, а эутиреоз достигается через 4—6 нед.
 В результате хорошо известного иммуносупрессивного действия беременности, проявляющегося повышением числа Т-супрессоров и снижением количества Т-хелперов, ДТЗ при беременности имеет тенденцию к спонтанной ремиссии. Знание этой особенности течения тиреотоксикоза при беременности позволяет контролировать функцию ЩЖ матери с помощью относительно низких начальных, так и поддерживающих доз тиреостатиков. Препараты необходимо назначать в минимальной возможной начальной дозировке (не выше, чем 10— 15 мг мерказолила или 100 мг пропилтиоурацила в сутки) с переходом на поддерживающую дозу (2,5 мг/сут для мерказолила и 50 мг/сут для пропилтиоурацила) .
В результате хорошо известного иммуносупрессивного действия беременности, проявляющегося повышением числа Т-супрессоров и снижением количества Т-хелперов, ДТЗ при беременности имеет тенденцию к спонтанной ремиссии. Знание этой особенности течения тиреотоксикоза при беременности позволяет контролировать функцию ЩЖ матери с помощью относительно низких начальных, так и поддерживающих доз тиреостатиков. Препараты необходимо назначать в минимальной возможной начальной дозировке (не выше, чем 10— 15 мг мерказолила или 100 мг пропилтиоурацила в сутки) с переходом на поддерживающую дозу (2,5 мг/сут для мерказолила и 50 мг/сут для пропилтиоурацила) . - Лечение по методу ’’блокируй и замещай» высокими дозами тионамидов в сочетании с заместительной терапией Т4 при беременности противопоказано. При данном режиме терапии Т4 обеспечивает сохранение эутиреоза только у матери, в то же время это может вызвать гипотиреоз у плода, так как высокие дозы тиреостатиков в противоположность Т4 легко проходят через плаценту.

- Использование p-адренергических антагонистов при беременности, осложнившейся развитием тиреотоксикоза, нежелательно, так как они могут вызвать уменьшение массы плаценты, задержку внутриутробного развития плода, постнатальную брадикардию и гипогликемию, а также ослабить реакцию на гипоксию, р—блокаторы могут быть использованы только на короткий период для подготовки к оперативному лечению или при развитии тиреотоксического криза.
- Оптимальным методом контроля эффективности лечения тиреотоксикоза при беременности является определение концентрации свТз и свТ4 в крови. Уровни свТ4 и свТ3 в сыворотке крови матери при лечении тиреостатиками следует поддерживать на верхней границе нормы во избежание гипотиреоза у плода.
Вследствие физиологических изменений секреции ТТГ во время различных фаз беременности уровень ТТГ в крови не является надежным критерием для суждения об адекватности лечения. Вместе с тем очень высокий уровень ТТГ указывает на развитие медикаментозного гипотиреоза и требует немедленной отмены или снижения дозы тионамидов. Рекомендуемые рядом авторов ультразвуковое определение размеров ЩЖ плода и исследование уровня ТТГ, Т3 Т4 в крови плода, к сожалению, доступны только небольшому кругу высокоспециализированных медицинских учреждений и пока не могут широко применяться.
Рекомендуемые рядом авторов ультразвуковое определение размеров ЩЖ плода и исследование уровня ТТГ, Т3 Т4 в крови плода, к сожалению, доступны только небольшому кругу высокоспециализированных медицинских учреждений и пока не могут широко применяться.
- При наличии стойкой компенсации в последние месяцы беременности тиреостатические препараты могут быть отменены. В то же время следует помнить о частом рецидиве тиреотоксикоза в послеродовом периоде.
- При лактации тионамиды могут проникать в грудное молоко, причем мерказолил в большей степени, чем пропилтиоурацил. Однако, по существующим данным, низкие дозы тионамидов (до 15 мг мерказолила и 150 мг пропилтиоурацила), принимаемые женщиной во время кормления груч дью, по-видимому, не влияют на функцию ЩЖ ребенка.
Почему так важно лечить тиреотоксикоз на фоне беременности?
Заболевание беременных тиреотоксикозом повышает риск рождения мертвого ребенка, наступления преждевременных родов или развития преэклампсии.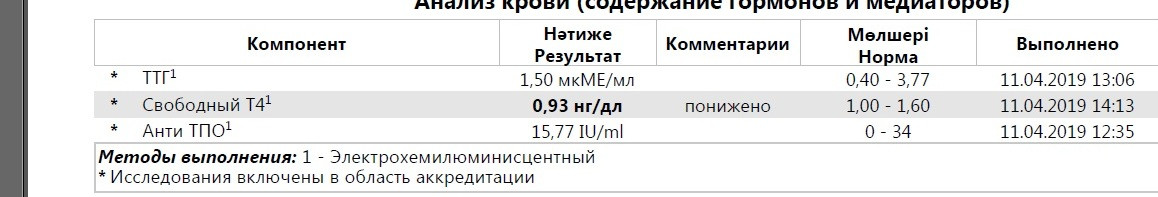 Также отмечается повышение частоты неонатальной смертности и вероятности рождения ребенка с дефицитом массы тела. Декомпенсированный тиреотоксикоз может вызвать и усугубить сердечно-сосудистую недостаточность у матери, а также способствовать развитию тиреотоксического криза во время родовых схваток и потуг.
Также отмечается повышение частоты неонатальной смертности и вероятности рождения ребенка с дефицитом массы тела. Декомпенсированный тиреотоксикоз может вызвать и усугубить сердечно-сосудистую недостаточность у матери, а также способствовать развитию тиреотоксического криза во время родовых схваток и потуг.
Следует отметить, что вышеперечисленные осложнения чаще наблюдаются при развитии тиреотоксикоза во время беременности, чем в случае наступления беременности у женщин с ранее леченным ДТЗ. Несомненно, что адекватный контроль р лечение тиреотоксикоза у матери являются главным фактором улучшения прогноза беременное™ и родов.
У детей, рожденных от матерей с декомпенсированным ДТЗ, отмечено повышение риска врожденных пороков развития и других фетальных нарушений (6%). В то же время у детей, чьи матер] во время беременности находились в состояни] медикаментозного эутиреоза на фоне лечения ме тимазолом, частота фетальных нарушений анало гична таковой среди детей здоровых эутиреоидны матерей (< 1%).
В литературе отсутствуют сведения о тератоген ных воздействиях пропилтиоурацила, тогда ка: прием метимазола крайне редко сопровождаете врожденным нарушением развития кожи (aplasi cutis). Исследования интеллектуального развити детей, подвергшихся воздействию тиреостатико во время внутриутробного развития, также не вы явили отклонения от нормальных показателей.
Все эти данные подтверждают, что нелечены] тиреотоксикоз у матери может быть причиной вро жденных пороков развития плода и других ослож нений беременности и что преимущества лечени тиреостатиками превышают какие-либо возмож ные тератогенные эффекты, связанные с этим] препаратами.
У детей, матери которых во время беременност страдали аутоиммунным тиреотоксикозом, може развиться фетальный или неонатальный гипертирео:
Внутриутробный тиреотоксикоз развивается то гда, когда функция зрелой ЩЖ плода стимулиру ется большим количеством иммуноглобулинов и крови матери. Это состояние может развитье только примерно после 25-й недели беременности Фетальный тиреотоксикоз можно установить из мерением частоты сердечных сокращений (выш 160 в минуту), определением уровня ТТГ или ин тегрального уровня ТГ, полученных методом ам ниоцентеза или кордоцентеза, а также УЗИ, позво ляющим установить наличие зоба у плода. длится 2—3 мес, может являться трансплацента! ный пассаж стимулирующих ЩЖ иммуноглобулинов. Клиническими симптомами неонатального тиреотоксикоза являются тахикардия, гиперчувствительность, задержка роста, увеличение костного возраста, зоб (не всегда), преждевременный, краниостеноз, повышенная смертность и заболеваемость.
длится 2—3 мес, может являться трансплацента! ный пассаж стимулирующих ЩЖ иммуноглобулинов. Клиническими симптомами неонатального тиреотоксикоза являются тахикардия, гиперчувствительность, задержка роста, увеличение костного возраста, зоб (не всегда), преждевременный, краниостеноз, повышенная смертность и заболеваемость.
Неонатальный гипертиреоз требует как можно более раннего и активного лечения тионамидами. Новорожденным назначают метимазол (0,5—1 мг/кг массы тела в день) или пропилтиоурацил (5— 10 мг/кг массы тела в день) в 3 приема. Возможно назначение пропранолола для урежения частоты сердечных сокращений и снижения катехоламиновой активности. При тяжелом заболевании можно давать насыщенный раствор йодида (1 капля раствора в день на протяжении не более 3 нед) для ингибирования высвобождения ранее синтезированных ТГ.
В тяжелых случаях необходимо добавление глюкокортикоидов, которые, помимо общего воздействия, также обладают способностью блокировать конверсию Т4вТ3.
Причинами первичного гипотиреоза у беременных женщин наиболее часто являются хронический аутоиммунный тиреоидит (АИТ) и состояние после резекции ЩЖ по поводу ДТЗ и разных форм зоба. Гипотиреоз вследствие АИТ в большинстве случаев выявляется и компенсируется до наступления беременности, однако иногда его дебют совпадает с беременностью.
С целью выявления АИТ во время беременности необходимо в ранние сроки обследовать беременных с подозрением на дисфункцию ЩЖ на наличие в сыворотке крови антител к тиреоглобулину и тиреоидной пероксидазе.
Как уже описывалось ранее, вследствие иммуносупрессивного действия беременности ранее диагностированный АИТ может иметь тенденцию к ремиссии во время беременности с рецидивом в послеродовом периоде.
Наиболее типичными симптомами гипотиреоза при беременности являются слабость, повышенная сухость кожи, быстрая утомляемость и запоры, однако следует помнить, что эти симптомы могут быть также проявлениями самой беременности в отсутствие понижения функции ЩЖ. Диагноз гипотиреоза при беременности ставят на основании снижения уровня свТ4 и повышения концентрации ТТГ в сыворотке крови.
Диагноз гипотиреоза при беременности ставят на основании снижения уровня свТ4 и повышения концентрации ТТГ в сыворотке крови.
Подбор адекватной дозы Т4 проводят под контролем уровня ТТГ и свТ4 в сыворотке крови (100—150 мкг Т4 в сутки). До недавнего времени считалось, что беременные женщины с ранее леченным гипотиреозом не нуждаются в повышении дозы Т4 на основании того, что повышенная потребность в гормонах ЩЖ компенсируется увеличением их концентрации в сыворотке крови и уменьшением метаболической конверсии Т4. Однако в настоящее время стало ясно, что женщинам, болеющим гипотиреозом и получающим заместительную терапию Т4, нередко во время беременности необходимо увеличивать дозу Т4.
Вероятными причинами повышения потребности в тг во время беременности могут быть как повышение массы тела с увеличением срока беременности, так и адаптационная регуляция оси гипоталамус—гипофиз—ЩЖ, а также возможные изменения периферического метаболизма Т4 из-за наличия фето-плацентарного комплекса.
Неадекватное лечение материнского гипотиреоза может привести к таким осложенениям беременности, как анемия, преэклампсия, отслойка плаценты, послеродовые кровотечения и нарушения функции сердечно-сосудистой системы. Кроме того, у плода и новорожденного с врожденным гипотиреозом трансплацентарный пассаж материнского Т4 на ранних стадиях беременности может играть критическую роль в нормальном развитии мозга.
Блокирующие антитела к рецепторам ТТГ, переходящие через плаценту к плоду, могут вызывать фетальный и неонатальный гипотиреоз (по аналогии с фетальным и неонатальным гипертиреозом). Важно отметить, что у детей матерей, болеющих гипотиреозом с присутствием антител, блокирующих рецептор ТТГ, имеется повышенный риск заболеть внутриутробным или послеродовым гипотиреозом даже при достижении эутиреоидного состояния матери после проведения заместительной терапии Т4.
Фетальный гипотиреоз сопровождается внутриутробным замедлением роста, брадикардией, запоздалым развитием ядер окостенения, а также нарушением процессов развития центральной нервной системы плода.
Неонатальный гипотиреоз обычно длится в течение 1—4 мес (период полувыведения материнских антител из крови ребенка в среднем составляет 3 нед). Наиболее типичными признаками гипотиреоза в ранний постнатальный период являются переношенная беременность (гестационный возраст > 42 нед), большая масса тела при рождении (> 4 кг), макроглоссия, периферический цианоз и отеки, затруднение дыхания, низкий грубый голос при плаче и крике. Диаметр затылочного родничка превышает 5 мм, период желтухи удлиняется (> 3 дней). В дальнейшем могут отмечаться сонливость, снижение аппетита, пониженная активность, гипотермия, сухость и бледность кожных покровов.
Другими причинами транзиторного гипотиреоза могут быть функциональная незрелость гипота- ламо-гипофизарной системы у недоношенных детей, а также тяжелый йодный дефицит у матери во время беременности и назначение высоких доз тиреостатиков по поводу ДТЗ. Доказанная роль ТТГ в развитии плода, а также влияние ТГ на рост и развитие в неонатальном периоде (особенно в течение 1-го года жизни) обусловливают необходимость проведения скрининга на врожденный (в том числе и транзиторный) гипотиреоз.
Транзиторная гипотироксинемия в большинстве случаев проходит самостоятельно при исчезновении причины, ее вызвавшей. В ряде случаев показано назначение новорожденному Т4 в дозе 10—15 мкг/кг массы тела в день коротким курсом (3—4 нед).
В послеродовом периоде у 4—16,7% женщин с отсутствием в анамнезе заболеваний ЩЖ может развиться послеродовой тиреоидит (ПТ). Этиология этого заболевания до сих пор до конца неясна. Выявленная взаимосвязь между ПТ и выявлением аутоантител к ткани ЩЖ (к тиреоидной пероксидазе и микросомальным антигенам), наличием определенных HLA-маркеров и лимфоцитарной инфильтрации ткани ЩЖ позволяет рассматривать ПТ как разновидность АИТ.
В течение ПТ отмечается определенная фазо- вость. После необязательной фазы деструктивного гипертиреоза, протекающей в виде безболевого асимптомного тиреоидита (1—4-й месяц послеродового периода), примерно в 23% случаев наступает фаза стойкого гипотиреоза (5—7-й месяц послеродового периода).
Клинические проявления гипотиреоза при ПТ обычно типичны (слабость, сухость кожи, склонность к запорам и т. д.). При сканировании ЩЖ отмечается пониженное поглощение радиоактивного изотопа йода. Для ультразвуковой картины ПТ характерны диффузное или мультифокальное снижение эхогенности ЩЖ и структурные изменения, характерные для лимфоцитарной инфильтрации ЩЖ и нарушения тиреоидной морфологии.
д.). При сканировании ЩЖ отмечается пониженное поглощение радиоактивного изотопа йода. Для ультразвуковой картины ПТ характерны диффузное или мультифокальное снижение эхогенности ЩЖ и структурные изменения, характерные для лимфоцитарной инфильтрации ЩЖ и нарушения тиреоидной морфологии.
При развитии стойкого гипотиреоза назначается заместительная терапия Т4 по обычной схеме.
В настоящее время исследуется взаимосвязь между наличием в послеродовом периоде повышенного титра антител к ткани ЩЖ и послеродовой депрессией. Предполагается, что эти антитела могут модулировать функцию нейротрансмиттеров, а также воздействовать на цитокиновые рецепторы мозга.
В заключение хотелось бы отметить, что своевременное и адекватное лечение заболеваний ЩЖ у беременных женщин способствует как нормальному течению беременности, так и правильному физическому и интеллектуальному развитию ребенка.
Особенности обследования и лечения заболеваний щитовидной железы во время беременности.
 Современное состояние проблемы (обзор литературы) | Шестакова Т.П.
Современное состояние проблемы (обзор литературы) | Шестакова Т.П.
Обзор литературы посвящен вопросам диагностики и лечения заболеваний щитовидной железы во время беременности. При обследовании и лечении беременных женщин необходимо учитывать физиологические изменения, свойственные беременности. Подробно обсуждается проблема определения нормы тиреотропного гормона (ТТГ) для беременных. В настоящее время увеличилась распространенность субклинического гипотиреоза. Вопрос о целесообразности лечения субклинического гипотиреоза, диагностированного по новым нормам ТТГ, не решен. Доказано положительное влияние левотироксина натрия у беременных с субклиническим гипотиреозом и положительными антителами к тиреоидной пероксидазе. Не подтверждается влияние субклинического гипотиреоза на психоневрологическое развитие плода. В настоящее время уделяется большое внимание вопросам безопасности антитиреоидных препаратов при беременности.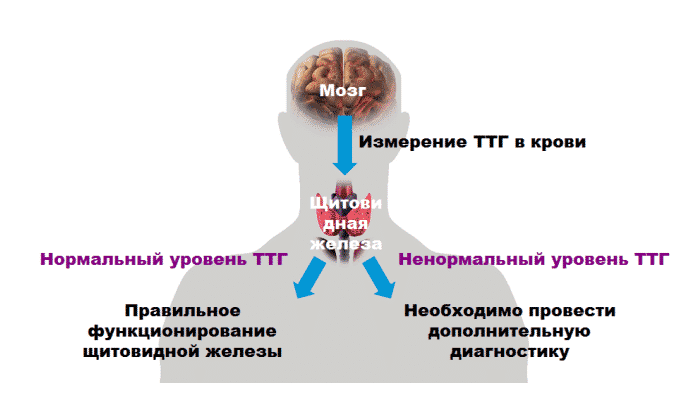 Выявлено тератогенное влияние на плод пропилтиоурацила, поэтому рекомендуется ограничить применение этого препарата I триместром. Затрагиваются вопросы обследования и лечения беременных с узловыми образованиями щитовидной железы.
Выявлено тератогенное влияние на плод пропилтиоурацила, поэтому рекомендуется ограничить применение этого препарата I триместром. Затрагиваются вопросы обследования и лечения беременных с узловыми образованиями щитовидной железы.
Ключевые слова: щитовидная железа, беременность, гипотиреоз, тиреотоксикоз, узлы щитовидной железы.
Для цитирования: Шестакова Т.П. Особенности обследования и лечения заболеваний щитовидной железы во время беременности. Современное состояние проблемы (обзор литературы). РМЖ. 2017;1:37-40.
Diagnosis and treatment of thyroid gland disorders in pregnancy: current conception (a review)
Shestakova T.P.
M.F. Vladimirskiy Moscow Regional Research and Clinical Institute, Moscow
The paper reviews the issues regarded diagnosis and treatment of thyroid gland disorders in pregnancy. Physiological changes that are typical of pregnancy should be considered when examining and treating pregnant women.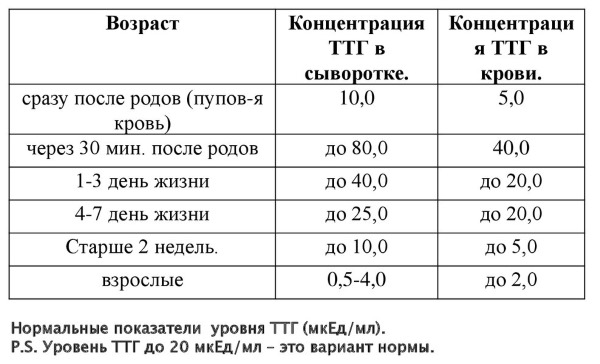 The estimation of TSH normal ranges in pregnancy is discussed. Currently, the occurrence of subclinical hypothyroidism is raising. The indications to the treatment of subclinical hypothyroidism diagnosed by novel TSH normal ranges are not determined yet. Sodium levothyroxin provides beneficial effects in pregnant women with subclinical hypothyroidism and anti-TPO antibodies. The influence of subclinical hypothyroidism on fetal psychoneurological development is not evident. Currently, the safety of anti-thyroid agents in pregnancy is of special importance. Previously unrecognized effect of propylthiouracil on the fetus was demonstrated. Additionally, the risk of liver failure due to propylthiouracil is an issue. Therefore, this agent should be used in the first trimester of pregnancy only. Finally, the paper addresses examination algorithms and treatment approaches to nodular thyroid gland disorders in pregnant women.
The estimation of TSH normal ranges in pregnancy is discussed. Currently, the occurrence of subclinical hypothyroidism is raising. The indications to the treatment of subclinical hypothyroidism diagnosed by novel TSH normal ranges are not determined yet. Sodium levothyroxin provides beneficial effects in pregnant women with subclinical hypothyroidism and anti-TPO antibodies. The influence of subclinical hypothyroidism on fetal psychoneurological development is not evident. Currently, the safety of anti-thyroid agents in pregnancy is of special importance. Previously unrecognized effect of propylthiouracil on the fetus was demonstrated. Additionally, the risk of liver failure due to propylthiouracil is an issue. Therefore, this agent should be used in the first trimester of pregnancy only. Finally, the paper addresses examination algorithms and treatment approaches to nodular thyroid gland disorders in pregnant women.
Key words: thyroid gland, pregnancy, hypothyroidism, thyrotoxicosis, thyroid gland nodules.
For citation: Shestakova T.P. Diagnosis and treatment of thyroid gland disorders in pregnancy: current conception (a review) // RMJ. 2017. № 1. P. 37–40.
Обзор литературы посвящен вопросам диагностики и лечения заболеваний щитовидной железы во время беременности
В настоящее время накоплены новые данные, которые меняют тактику лечения беременных женщин с гипотиреозом, тиреотоксикозом и узловыми образованиями щитовидной железы.
Особенности диагностики и лечения заболеваний щитовидной железы у беременных связаны с физиологическими изменениями, свойственными беременности. Эти изменения касаются метаболизма йода, связывающей способности сыворотки крови относительно тиреоидных гормонов, появления и функционирования плаценты, а также активности иммунной системы.
Физиологические изменения тиреоидной функции во время беременности
При обследовании и лечении беременных с заболеваниями щитовидной железы необходимо учитывать физиологические изменения, свойственные беременности.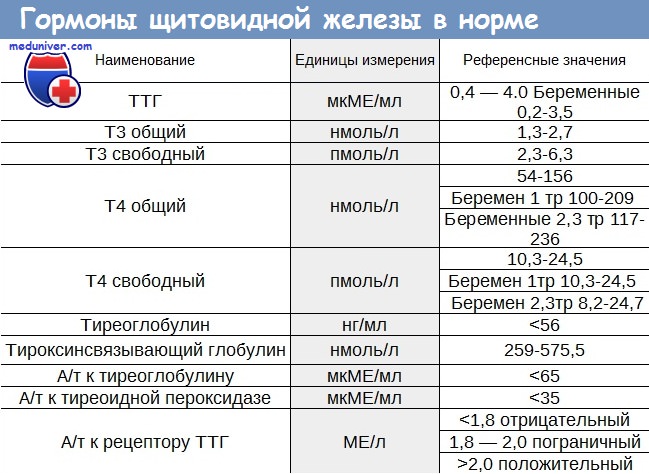 Во время беременности увеличиваются потери йода из кровотока за счет повышения фильтрации в почках и потребления йода плацентой. Кроме этого потребность в йоде увеличивается за счет повышения синтеза тиреоидных гормонов. Начиная с 5–7-й недели и до 20-й недели беременности увеличивается концентрация тиреоидсвязывающего глобулина (ТСГ), которая остается повышенной до завершения беременности. В результате ТСГ связывает больше тиреоидных гормонов, что проявляется увеличением общей фракции Т3 и Т4. Свободные фракции тиреоидных гормонов менее подвержены изменениям, но и их уровень не остается постоянным на протяжении беременности. В I триместре свободные фракции Т3 и Т4 увеличиваются в результате стимулирующего влияния хорионического гонадотропина на щитовидную железу, а в III триместре уровень Т3 и Т4 снижается [1]. Это происходит не столько за счет реального уменьшения уровня гормонов, сколько за счет колебаний его значений при определении наиболее часто используемым хемилюминесцентным методом.
Во время беременности увеличиваются потери йода из кровотока за счет повышения фильтрации в почках и потребления йода плацентой. Кроме этого потребность в йоде увеличивается за счет повышения синтеза тиреоидных гормонов. Начиная с 5–7-й недели и до 20-й недели беременности увеличивается концентрация тиреоидсвязывающего глобулина (ТСГ), которая остается повышенной до завершения беременности. В результате ТСГ связывает больше тиреоидных гормонов, что проявляется увеличением общей фракции Т3 и Т4. Свободные фракции тиреоидных гормонов менее подвержены изменениям, но и их уровень не остается постоянным на протяжении беременности. В I триместре свободные фракции Т3 и Т4 увеличиваются в результате стимулирующего влияния хорионического гонадотропина на щитовидную железу, а в III триместре уровень Т3 и Т4 снижается [1]. Это происходит не столько за счет реального уменьшения уровня гормонов, сколько за счет колебаний его значений при определении наиболее часто используемым хемилюминесцентным методом. Точность определения концентрации гормонов этим методом снижается в случае нарушения равновесия между свободной и связанной фракциями. Во время беременности изменяется количество не только тиреоидсвязывающего глобулина, но и альбумина, что изменяет соотношение свободной и связанной фракций тиреоидных гормонов [2]. В связи с этим некоторые исследователи рекомендуют использовать общую фракцию гормонов, которая более точно коррелирует с уровнем тиреотропного гормона (ТТГ). При этом необходимо учитывать, что нормальные показатели общего Т3 и Т4 отличаются у беременных. Начиная с середины беременности уровень общего Т4 на 50% превышает уровень, имевшийся до беременности. Сложнее определить нормальный уровень на сроках беременности между 7-й и 16-й неделями, когда уровень общего Т4 динамично изменяется. Считается, что начиная с 7-й недели каждую последующую неделю уровень свободного Т4 увеличивается на 5%; исходя из этого можно рассчитать верхнюю границу нормы для общей фракции Т4 по формуле: (неделя беременности от 8-й до 16-й – 7) × 5 [3].
Точность определения концентрации гормонов этим методом снижается в случае нарушения равновесия между свободной и связанной фракциями. Во время беременности изменяется количество не только тиреоидсвязывающего глобулина, но и альбумина, что изменяет соотношение свободной и связанной фракций тиреоидных гормонов [2]. В связи с этим некоторые исследователи рекомендуют использовать общую фракцию гормонов, которая более точно коррелирует с уровнем тиреотропного гормона (ТТГ). При этом необходимо учитывать, что нормальные показатели общего Т3 и Т4 отличаются у беременных. Начиная с середины беременности уровень общего Т4 на 50% превышает уровень, имевшийся до беременности. Сложнее определить нормальный уровень на сроках беременности между 7-й и 16-й неделями, когда уровень общего Т4 динамично изменяется. Считается, что начиная с 7-й недели каждую последующую неделю уровень свободного Т4 увеличивается на 5%; исходя из этого можно рассчитать верхнюю границу нормы для общей фракции Т4 по формуле: (неделя беременности от 8-й до 16-й – 7) × 5 [3].
Если же использовать значения свободных фракций, то необходимо учитывать, что у беременных нормы для тиреоидных гормонов значительно различаются при разных методиках определения гормонов. Поэтому рекомендуется в каждой лаборатории, которая выполняет гормональные анализы для беременных, определить свой референсный интервал не только для каждого триместра беременности, но и для каждого применяемого метода исследования [4].
Хорионический гонадотропин (ХГЧ), вырабатываемый плацентой, оказывает стимулирующее воздействие на щитовидную железу вследствие его способности взаимодействовать с рецептором ТТГ. В результате этого в I триместре, на пике секреции ХГЧ, повышается выработка тиреоидных гормонов, причем увеличивается не только общая, но и свободная фракция Т3 и Т4. При этом по механизму обратной отрицательной связи снижается уровень ТТГ. У большинства беременных изменения происходят в пределах референсных значений, но у 1–3% беременных ТТГ и свободный Т4 выходят за пределы нормы и тогда развивается транзиторный гестационный тиреотоксикоз, требующий дифференциальной диагностики с диффузным токсическим зобом и другими заболеваниями, сопровождающимися тиреотоксикозом. Изменения уровня гормонов, возникающие вследствие стимуляции ХГЧ, обычно исчезают к 18–20-й неделе беременности, но в редких случаях ТТГ остается подавленным во II и даже III триместрах [5].
Изменения уровня гормонов, возникающие вследствие стимуляции ХГЧ, обычно исчезают к 18–20-й неделе беременности, но в редких случаях ТТГ остается подавленным во II и даже III триместрах [5].
Йод и беременность
Йод – микроэлемент, необходимый для синтеза тиреоидных гормонов. Потребность в йоде увеличивается во время беременности примерно на 50%. По мнению ВОЗ, йодурия у беременных должна быть в пределах 150–249 мкг/л [6]. Рекомендации в отношении дополнительного потребления йода беременными не меняются: 250 мкг йода ежедневно на протяжении всей беременности. В регионе легкого йодного дефицита это достигается добавлением к пище 200 мкг йода в виде калия йодида. Даже в таких регионах, как США, где дефицит йода полностью восполняется, во время беременности рекомендуется дополнительное потребление 150 мкг йода в сутки. Положительными эффектами восполнения дефицита йода является уменьшение перинатальной смертности, увеличение окружности головы новорожденных, а также повышение IQ, и особенно уменьшение проблем с чтением и восприятием прочитанного [6].
Гипотиреоз и беременность
В последние годы увеличилась распространенность гипотиреоза среди беременных до 15% за счет субклинических форм, тогда как распространенность манифестного гипотиреоза не изменяется и составляет 2,0–2,5%. В крупном исследовании в США выявлена распространенность гипотиреоза на уровне 2,5% [7]. В Италии частота гипотиреоза, с учетом субклинического, составила 12,5% [8].
Увеличение количества беременных с субклиническим гипотиреозом в большой мере связано с изменением нормы для ТТГ во время беременности.
В 2011 г. Американской ассоциацией тиреоидологов (АТА) было рекомендовано применение у беременных специфичных для каждого триместра норм ТТГ, определяемых для каждой этнической группы, либо использование предложенных: для I триместра – 0,1–2,5 мЕд/л, для II триместра – 0,2–3,0 мЕд/л, для III триместра – 0,3–3,0 мЕд/л [9]. Предложенные референсные нормы основывались на результатах шести исследований, в которых приняли участие в общей сложности 5500 беременных. Использование рекомендованных значений ТТГ привело к закономерному увеличению частоты субклинического гипотиреоза. Например, в Китае при переходе на новые нормативы распространенность субклинического гипотиреоза достигла 28% [10]. В связи с этим во многих странах были проведены собственные исследования для определения нормальных показателей ТТГ у беременных.
Использование рекомендованных значений ТТГ привело к закономерному увеличению частоты субклинического гипотиреоза. Например, в Китае при переходе на новые нормативы распространенность субклинического гипотиреоза достигла 28% [10]. В связи с этим во многих странах были проведены собственные исследования для определения нормальных показателей ТТГ у беременных.
В настоящее время общее количество беременных, принявших участие в исследовании тиреоидного статуса, превышает 60 тыс. Вновь проведенные исследования показали, что нормы ТТГ различаются в зависимости от обеспеченности региона йодом, индекса массы тела и этнической принадлежности [10–13].
Так, в Китае установлено нормальное cодержание ТТГ для I триместра в пределах 0,14–4,87 мЕд/л, при переходе на эти показатели частота субклинического гипотиреоза составила 4% [10]. Схожие данные были получены в Корее, где верхняя граница референсных значений ТТГ cоставила от 4,1 мЕд/л в I триместре до 4,57 мЕд/л в III триместре [14]. Подобные результаты были получены при обследовании беременных в Европе. Так, в Чехии нормой для I триместра беременности признан уровень ТТГ 0,06–3,67 мЕд/л. При применении таких показателей распространенность гипотиреоза среди беременных составила 4,48% [15]. Суммарные данные нескольких исследований показывают, что в I триместре беременности верхняя граница нормы ТТГ находится в интервале от 2,15 до 4,68 мЕд/л [16].
Подобные результаты были получены при обследовании беременных в Европе. Так, в Чехии нормой для I триместра беременности признан уровень ТТГ 0,06–3,67 мЕд/л. При применении таких показателей распространенность гипотиреоза среди беременных составила 4,48% [15]. Суммарные данные нескольких исследований показывают, что в I триместре беременности верхняя граница нормы ТТГ находится в интервале от 2,15 до 4,68 мЕд/л [16].
На основании последних исследований АТА рекомендует в случае отсутствия собственного референсного интервала использовать в качестве верхней границы нормы ТТГ обычно применяемый критерий – 4 мЕд/л либо, учи-тывая физиологические особенности беременной, снизить этот верхний порог на 0,5 мЕд/л [4].
Манифестный гипотиреоз не только снижает фертильность женщины, но и неблагоприятно влияет на течение беременности и здоровье плода. Некомпенсированный гипотиреоз увеличивает риск гибели плода (OR 1,26; 95% CI 1,1–1,44; р=0,0008), преждевременных родов (OR 1,96; 95% CI 1,4–2,73; p=0,0008), преэклампсии и гестационного сахарного диабета (OR 1,69; 95% CI 1,27–2,43; p=0,002), оказывает негативное влияние на психоневрологическое развитие плода [17]. При этом в многочисленных исследованиях показано, что компенсация гипотиреоза уменьшает риск осложнений беременности до общепопуляционного [18].
При гипотиреозе, диагностированном до наступления беременности, необходима коррекция дозы левотироксина натрия во время беременности. Повышение дозы диктуется физиологическими изменениями, свойственными беременности, но зависит от многих факторов, в частности от уровня ТТГ на момент наступления беременности и причины гипотиреоза. Опрос врачей из Европейского общества эндокринологов выявил, что около половины врачей (48%) коррекцию дозы левотироксина натрия проводят после контроля ТТГ на фоне беременности [19]. Такой подход приемлем у комплаентных женщин, когда коррекцию дозы можно проводить по результатам гормонального исследования крови. Однако у женщин, которые нерегулярно посещают врача и редко контролируют гормональный статус, рекомендуется превентивное увеличение дозы левотироксина натрия на 50% сразу после наступления беременности.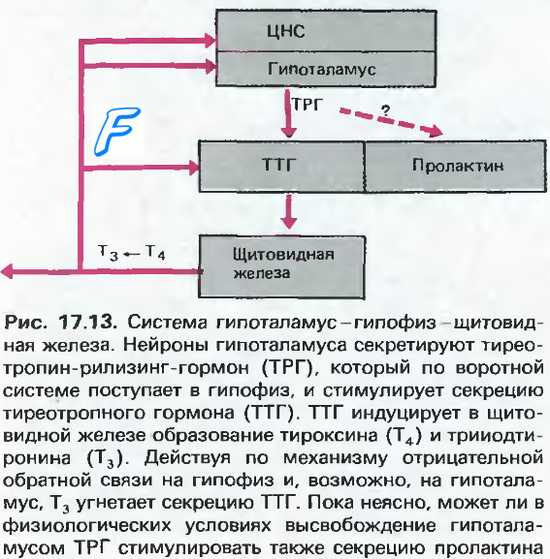
В настоящее время не решен вопрос о влиянии на течение беременности и здоровье плода субклинического гипотиреоза, т. е. изолированного повышения ТТГ, или изолированной гипотироксинемии во время беременности.
Для того чтобы решить, необходимо ли активное лечение беременных с субклиническим гипотиреозом, особенно при незначительном повышении ТТГ в пределах 2,5–5,0 мЕд/л, нужно определить влияние этого состояния на вынашивание, течение беременности и здоровье плода. Ранее исследования показывали, что субклинический гипотиреоз увеличивает частоту выкидышей в той же мере, что и манифестный гипотиреоз [20, 21]. Но подобные исследования были немногочисленными, часто в ходе их объединялись беременные с субклиническим и манифестным гипотиреозом. Исследование, проведенное в Австралии, не выявило зависимости осложнений беременности от повышенного в пределах 10 мЕд/л ТТГ и изолированного снижения свободного Т4 [22]. В другом крупном исследовании с участием более 5000 беременных, 3/4 которых имели субклинический гипотиреоз, было показано, что выкидыш чаще, чем у эутиреоидных женщин, происходил в группах с содержанием ТТГ от 5 до 10 мЕд/л в сочетании с антитиреоидными антителами или без такового, тогда как при более низких значениях ТТГ (2,5–5,22 мЕд/л) повышение частоты выкидышей отмечалось только при наличии антител к ТПО. При субклиническом гипотиреозе выкидыши случались на более ранних сроках беременности по сравнению с беременными с эутиреозом [23]. Это исследование подтвердило результаты более ранних исследований, показывающих, что влияние на вынашивание беременности оказывает снижение функции щитовидной железы при аутоиммунном тиреоидите. В случае отсутствия повышенного титра антитиреоидных антител влияние повышенного ТТГ на вынашивание беременности недостаточно доказано.
При субклиническом гипотиреозе выкидыши случались на более ранних сроках беременности по сравнению с беременными с эутиреозом [23]. Это исследование подтвердило результаты более ранних исследований, показывающих, что влияние на вынашивание беременности оказывает снижение функции щитовидной железы при аутоиммунном тиреоидите. В случае отсутствия повышенного титра антитиреоидных антител влияние повышенного ТТГ на вынашивание беременности недостаточно доказано.
Другой важный аспект – это влияние субклинического гипотиреоза на течение беременности и здоровье плода. При обследовании более 8000 беременных выявлена повышенная частота гестационной гипертензии (OR 2,2) и внутриутробной задержки развития плода (OR 3,3), низкий вес плода (OR 2,9) у беременных с субклиническим гипотиреозом по сравнению с эутиреоидными беременными [24]. Схожие данные были получены в другом исследовании, которое подтвердило, что суммарный риск неблагоприятных исходов (преждевременные роды или выкидыш, низкий вес плода, преэклампсия) был повышен в 2 раза у беременных с субклиническим гипотиреозом [25].
Влияние некомпенсированного гипотиреоза на психоневрологическое развитие плода, имеющее отдаленные последствия, хорошо известно. Проведенные за последние 5 лет исследования беременных с субклиническим гипотиреозом, особенно с незначительным повышением ТТГ, не подтвердило негативного воздействия на плод. Интервенционные исследования также не показали положительного эффекта лечения. Возможно, это объясняется включением в исследование беременных с ТТГ от 2,5 мЕд/л, что может являться вариантом нормы для данной популяции. Второй ограничивающий фактор – срок начала лечения. В нескольких исследованиях, которые не подтвердили положительного эффекта лечения, оно было начато во II триместре, что, вероятно, следует считать поздним началом [26].
Суммарные данные 21 исследования по изучению влияния субклинического гипотиреоза на течение и исход беременности и здоровье плода подтвердили негативное влияние дефицита тиреоидных гормонов на течение и исход беременности, особенно в группах, где субклинический гипотиреоз сочетался с высоким титром антитиреоидных антител. При этом необходимо заметить, что данных о влиянии субклинического гипотиреоза на психоневрологическое состояние плода на сегодня недостаточно [4].
При этом необходимо заметить, что данных о влиянии субклинического гипотиреоза на психоневрологическое состояние плода на сегодня недостаточно [4].
Влияние изолированной гипотироксинемии на течение беременности и здоровье плода также вызывает интерес. V. Рор в ранних исследованиях показал, что снижение свободного Т4 у беременных в I триместре влияет на психоневрологическое развитие плода [27]. Высокий риск преждевременных родов, в т. ч. ранее 34-й недели беременности, выявлен у женщин с гипотироксинемией на ранних сроках беременности и позитивными антителами к ТПО на ранних сроках [28]. Однако рандомизированные исследования не доказали положительного влияния лечения изолированной гипотироксинемии на исходы беременности [29]. Учитывая отсутствие убедительных данных о положительном влиянии коррекции изолированной гипотироксинемии, в настоящее время не рекомендуется проведение лечения беременных с такими лабораторными отклонениями. Кроме того, необходимо учитывать частые лабораторные погрешности при определении уровня свободного Т4 у беременных.
Тиреотоксикоз и беременность
Основной причиной тиреотоксикоза у беременных является диффузный токсический зоб (ДТЗ), который необходимо дифференцировать с транзиторным гестационным тиреотоксикозом (ТГТ). ТГТ – это состояние, обусловленное избыточной стимуляцией щитовидной железы со стороны ХГЧ. Распространенность ТГТ составляет 1–3% и превышает распространенность ДТЗ, частота которого составляет не более 0,2%. ТГТ ассоциирован с многоплодной беременностью и тошнотой и рвотой беременных [30, 31]. Дифференциальная диагностика основывается на анамнезе, осмотре с целью выявления характерных для ДТЗ симптомов (зоб, эндокринная офтальмопатия, претибиальная микседема), определении антител к рецепторам ТТГ, исследовании соотношения Т3/Т4 и ТТГ и тиреоидных гормонов в динамике. Исследование ХГЧ не позволяет определенно дифференцировать ТГТ и ДТЗ [32].
Основной метод лечения ДТЗ во время беременности – консервативный. В последние годы изменение подходов к лечению беременных связано с вопросами безопасности применения тиреостатиков.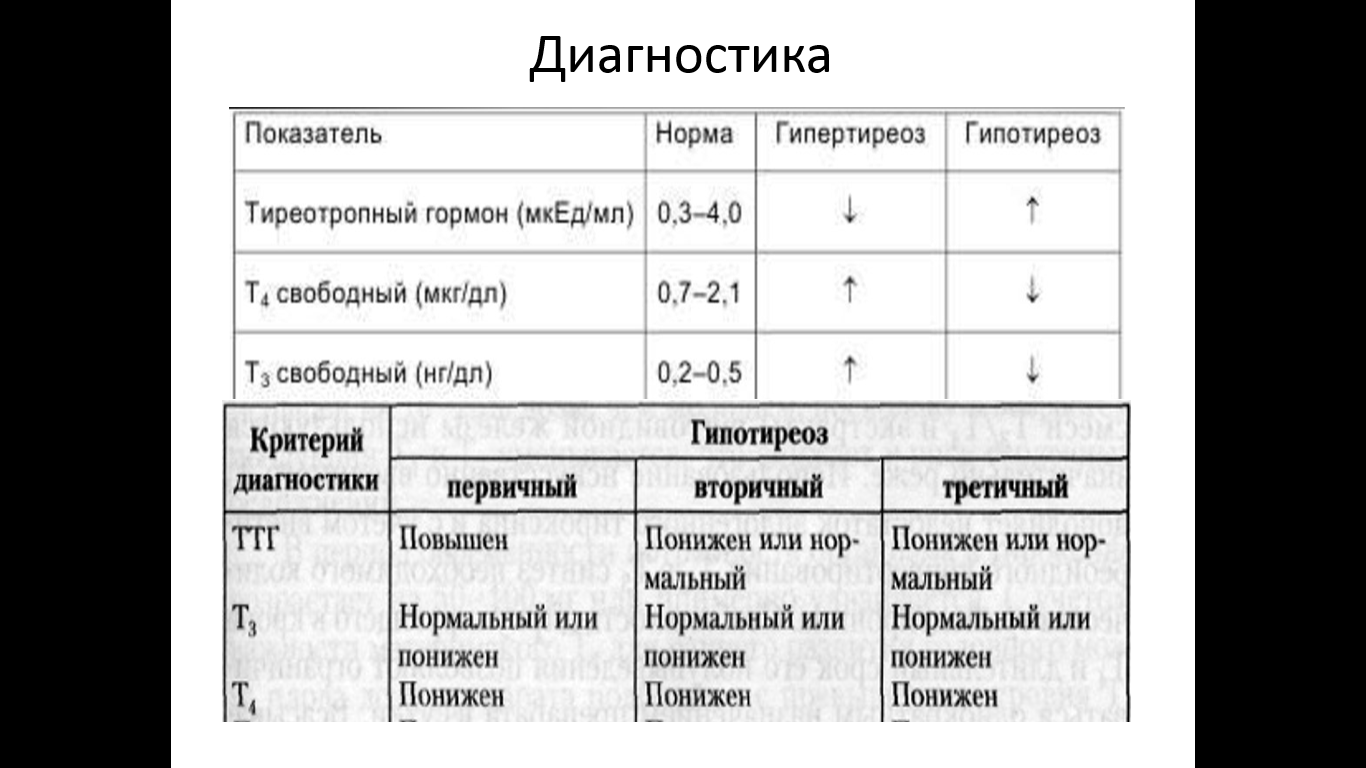 Одним из опасных побочных эффектов тиреостатиков является развитие агранулоцитоза или панцитопении. Это осложнение может развиться в любые сроки лечения, но более характерно для первых 90 дней [33]. При обследовании беременных, получавших тиреостатики, выявлено, что агранулоцитоз и поражение печени встречались гораздо реже, чем в общей популяции (примерно по 1 случаю на 2500 беременных). Самый частый побочный эффект применения тиреостатиков беременными – врожденные патологии плода, причем, по данным S. Anderson, они встречались с одинаковой частотой на фоне приема пропилтиоурацила и метимазола [34]. Однако в другом исследовании частота врожденных аномалий на фоне пропилтиоурацила не отличалась от таковой в контрольной группе, тогда как метимазол вызывал малые эмбриопатии (аплазию кожи на волосистой части головы, атрезию пищевода и др.) [35]. Ранее полагали, что пропилтиоурацил не обладает тератогенным эффектом, но опубликованные недавно результаты исследования датских ученых показали, что это не так.
Одним из опасных побочных эффектов тиреостатиков является развитие агранулоцитоза или панцитопении. Это осложнение может развиться в любые сроки лечения, но более характерно для первых 90 дней [33]. При обследовании беременных, получавших тиреостатики, выявлено, что агранулоцитоз и поражение печени встречались гораздо реже, чем в общей популяции (примерно по 1 случаю на 2500 беременных). Самый частый побочный эффект применения тиреостатиков беременными – врожденные патологии плода, причем, по данным S. Anderson, они встречались с одинаковой частотой на фоне приема пропилтиоурацила и метимазола [34]. Однако в другом исследовании частота врожденных аномалий на фоне пропилтиоурацила не отличалась от таковой в контрольной группе, тогда как метимазол вызывал малые эмбриопатии (аплазию кожи на волосистой части головы, атрезию пищевода и др.) [35]. Ранее полагали, что пропилтиоурацил не обладает тератогенным эффектом, но опубликованные недавно результаты исследования датских ученых показали, что это не так. Выявлено, что у 2–3% детей, внутриутробное развитие которых проходило на фоне приема пропилтиоурацила, развиваются кисты лица и шеи, а также патология мочевыводящих путей (киста почки, гидронефроз). Эта патология не диагностируется в большинстве случаев сразу после родов, а проявляется клинически гораздо позже, поэтому ранее отсутствовала информация о тератогенном эффекте пропилтиоурацила [36–38]. Учитывая, что пропилтиоурацил вызывает менее тяжелые аномалии развития, в настоящее время в целях минимизации побочных эффектов рекомендуется для лечения тиреотоксикоза в I триместре беременности применять пропилтиоурацил, а во II и III триместрах – метимазол.
Выявлено, что у 2–3% детей, внутриутробное развитие которых проходило на фоне приема пропилтиоурацила, развиваются кисты лица и шеи, а также патология мочевыводящих путей (киста почки, гидронефроз). Эта патология не диагностируется в большинстве случаев сразу после родов, а проявляется клинически гораздо позже, поэтому ранее отсутствовала информация о тератогенном эффекте пропилтиоурацила [36–38]. Учитывая, что пропилтиоурацил вызывает менее тяжелые аномалии развития, в настоящее время в целях минимизации побочных эффектов рекомендуется для лечения тиреотоксикоза в I триместре беременности применять пропилтиоурацил, а во II и III триместрах – метимазол.
Узлы щитовидной железы и беременность
Обследование беременных с узловыми образованиями щитовидной железы не отличается от общепринятого. Однако необходимо учитывать некоторые особенности.
Хорошо известно, что во время беременности увеличивается объем щитовидной железы. Информация о росте узлов и их количестве противоречива. В недавнем исследовании S. Sahin показал, что размер узлов увеличивался одновременно с ростом общего объема щитовидной железы, без изменения количества узлов. У 6,6% беременных, по данным пункционной биопсии, был выявлен рак щитовидной железы (РЩЖ) [39].
В недавнем исследовании S. Sahin показал, что размер узлов увеличивался одновременно с ростом общего объема щитовидной железы, без изменения количества узлов. У 6,6% беременных, по данным пункционной биопсии, был выявлен рак щитовидной железы (РЩЖ) [39].
Данные о распространенности РЩЖ у беременных различаются в исследованиях, достигая высоких показателей – 15–34% [40, 41]. Более того, по некоторым данным, дифференцированные РЩЖ оказались более агрессивными, склонными к прогрессированию и рецидивам, если они выявлялись во время беременности или сразу после нее. Это объяснялось наличием рецепторов к эстрогенам в опухоли [42]. Однако в более позднем исследовании хотя и была подтверждена повышенная агрессивность дифференцированных РЩЖ, обнаруженных во время беременности, но причина этого не была установлена. Не было обнаружено ни BRAF-мутации, ни рецепторов эстрогенов [43].
Оперативное лечение во время беременности по поводу РЩЖ сопряжено с повышенной частотой осложнений и представляет угрозу для плода. По последним данным, отложенное до окончания беременности оперативное лечение не приводило к уменьшению продолжительности жизни по сравнению с оперированными во время беременности и не влияло на частоту рецидива и персистенцию заболевания [44]. Таким образом, если РЩЖ выявлен в первой половине беременности, то целесообразно проведение оперативного лечения во II триместре. Если же узел обнаружен во второй половине беременности, то оперативное лечение может быть отложено до послеродового периода.
По последним данным, отложенное до окончания беременности оперативное лечение не приводило к уменьшению продолжительности жизни по сравнению с оперированными во время беременности и не влияло на частоту рецидива и персистенцию заболевания [44]. Таким образом, если РЩЖ выявлен в первой половине беременности, то целесообразно проведение оперативного лечения во II триместре. Если же узел обнаружен во второй половине беременности, то оперативное лечение может быть отложено до послеродового периода.
Скрининг на заболевания щитовидной железы во время беременности
Проводить ли скрининг на заболевания щитовидной железы у всех беременных или только в группах риска – этот вопрос остается предметом дискуссии. Главным образом при избирательном обследовании пропускаются случаи гипотиреоза у беременных. При опросе американских врачей 42% респондентов сообщили, что проводят тотальный скрининг беременных женщин на заболевания щитовидной железы, 43% – только в группах риска и 17% – не проводят вообще. Европейские врачи в основном проводят скрининг в группах риска [45].
Европейские врачи в основном проводят скрининг в группах риска [45].
Таким образом, в настоящее время продолжаются исследования для уточнения нормального уровня ТТГ во время беременности и определения патологического значения незначительно повышенного ТТГ. Учитывая накопленные данные по безопасности тиреостатиков, изменились рекомендации по их применению во время беременности.
Литература
1. Андреева Е.Н., Григорян О.Р., Ларина А.А., Лесникова С.В. Эндокринные заболевания и беременность в вопросах и ответах под ред. Дедова И.И., Бурумкуловой Ф.Ф. // Москва. Е-ното. 2015. 272 с. [Andreeva E.N., Grigorjan O.R., Larina A.A., Lesnikova S.V. Jendokrinnye zabolevanija i beremennost’ v voprosah i otvetah pod red. Dedova I.I., Burumkulovoj F.F. // Moskva. E-noto. 2015. 272 s. (in Russian)].
2. Soldin O.P., Tractenberg R. E., Hollowell J.G. et al. Trimesterspecificchanges in maternal thyroid hormone, thyrotropin, and thyroglobulin concentrations during gestation: trends and associations across trimesters in iodine sufficiency // Thyroid. 2004. Vol. 14. Р. 1084–1090
E., Hollowell J.G. et al. Trimesterspecificchanges in maternal thyroid hormone, thyrotropin, and thyroglobulin concentrations during gestation: trends and associations across trimesters in iodine sufficiency // Thyroid. 2004. Vol. 14. Р. 1084–1090
3. Weeke J., Dybkjaer L., Granlie K. et al. A longitudinal study of serum TSH, and total and free iodothyronines during normal pregnancy // Acta Endocrinologica. 1982. Vol. 101. Р. 531.
4. Alexander E., Pearce E., Brent G. et al. Guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease during Pregnancy and the Postpartum // Thyroid. 2016. doi: 10.1089/thy.2016.0457.
5. Древаль А.В., Шестакова Т.П., Нечаева О.А. Заболевания щитовидной железы и беременность // М.: Медицина. 2007. 80 с. [Dreval’ A.V., Shestakova T.P., Nechaeva O.A. Zabolevanija shhitovidnoj zhelezy i beremennost’ // M.: Medicina. 2007. 80 s. (in Russian)].
6. Zimmermann M.B. The effects of iodine deficiency in pregnancy and infancy // Paediatr Perinat Epidemiol. 2012. Vol. 26 (Suppl 1). Р. 108–117.
2012. Vol. 26 (Suppl 1). Р. 108–117.
7. Blatt A.J., Nakamoto J.M., Kaufman H.W. National status of testing for hypothyroidism during pregnancy and postpartum // Jl of Clinical Endocrinology and Metabolism. 2012. Vol. 97. Р. 777–784.
8. Altomare M., La Vignera S., Asero P. et al. High prevalence of thyroid dysfunction in pregnant women // Jo of Endocrinological Investigation. 2013. Vol. 36. Р. 407–411.
9. Stagnaro-Green D., Abalovich M., Alexander E. et al. Guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease During Pregnancy and Postpartum // Thyroid. 2011. Vol. 21. doi: 10.1089/thy.2011.0087.
10. Li C., Shan Z., Mao J., Wang W. et al. Assessment of thyroid function during first trimester pregnancy: what is the rational upper limit of serum TSH during the first trimester in Chinese pregnant women? // J Clin Endocrinol Metab. 2014. Vol. 99. Р. 73–79.
11. Bestwick J.P., John R., Maina A. et al. Thyroid stimulating hormone and free thyroxine in pregnancy: expressing concentrations as multiples of the median (MoMs) // Clin Chim Acta. 2014. Vol. 430. Р. 33–37.
Thyroid stimulating hormone and free thyroxine in pregnancy: expressing concentrations as multiples of the median (MoMs) // Clin Chim Acta. 2014. Vol. 430. Р. 33–37.
12. La’ulu S.L., Roberts W.L. Ethnic differences in firsttrimester thyroid reference intervals // Clin Chem. 2011. Vol. 57. Р. 913–915.
13. Medici M., Korevaar T.I., Visser W.E. et al. Thyroid function in pregnancy: what is normal? // Clin Chem. 2015. Vol. 61(5). Р. 704–713.
14. Moon H.W., Chung H.J., Park C.M. et al. Establishment of trimester-specific reference intervals for thyroid hormones in Korean pregnant women // Ann Lab Med. 2015. Vol. 35(2). Р. 198–204.
15. Springer D., Zima T., Limanova Z. Reference intervals in evaluation of maternal thyroid function during the first trimester of pregnancy // Eur J Endocrinol. 2009. Vol. 160. Р. 791–797.
16. Medici M., Korevaar T.I., Visser W.E. et al. Thyroid function in pregnancy: what is normal? // Clin Chem. 2015. Vol.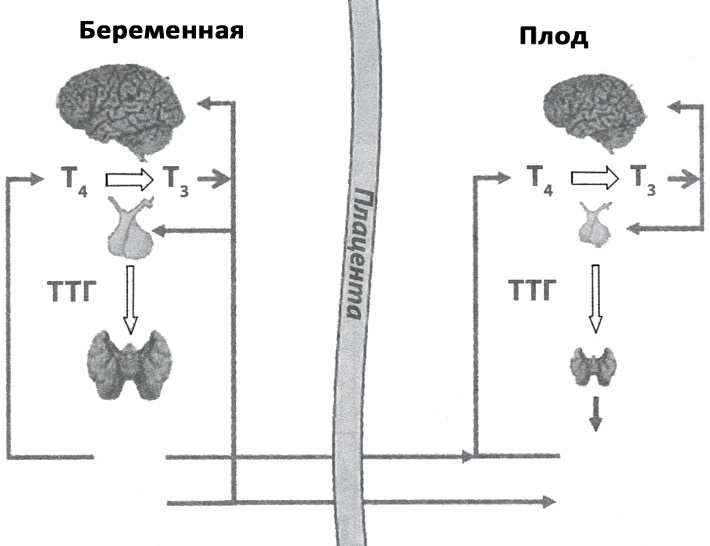 61(5). Р. 704–713.
61(5). Р. 704–713.
17. Taylor P, Lazarus J. Summary of adverse maternal and offspring outcomes associated with SCH in pregnancy //Thyroid international. 2014. Vol. 2. Р. 4–8.
18. Taylor P.N., Minassian C., Rehman A. et al. TSH Levels and Risk of Miscarriage in Women on Long-Term Levothyroxine: A Community-Based Study // JCEM. 2014. Vol. 99. Р. 3895–3902.
19. Vaidya B., Hubalewska-Dydejczyk A., Laurberg P. et al. Treatment and screening of hypothyroidism in pregnancy: results of a European survey // Eur J Endocrinol. 2012. Vol. 166(1). Р. 49–54.
20. Negro R., Schwartz A., Gismondi R. et al. Increased pregnancy loss rate in thyroid antibody negative women with TSH levels between 2.5 and 5.0 in the first trimester of pregnancy // J Clin Endocrinol Metab/ 2010. Vol. 95. Р. 44–48.
21. Benhadi N., Wiersinga W.M., Reitsma J.B. et al. Higher maternal TSH levels in pregnancy are associated with increased risk for miscarriage, fetal or neonatal death //Eur J Endocrinol.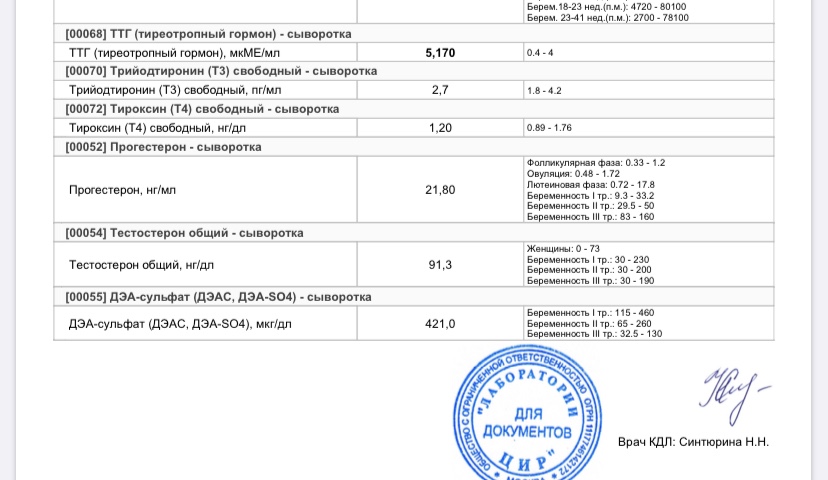 2009. Vol. 160. Р. 985–991.
2009. Vol. 160. Р. 985–991.
22. Ong G.S., Hadlow N.C., Brown S.J. et al. Does the thyroid-stimulating hormone measured concurrently with first trimester biochemical screening tests predict adverse pregnancy outcomes occurring after 20 weeks gestation? // J Clin Endocrinol Metab. 2014. Vol. 99(12). P. 2668–2672.
23. Liu H., Shan Z., Li C. et al. Maternal subclinical hypothyroidism, thyroid autoimmunity, and the risk of miscarriage: a prospective cohort study // Thyroid. 2014. Vol. 24(11). Р. 1642–1649.
24. Chen L.M., Du W.J., Dai J. et al. Effects of subclinical hypothyroidism on maternal and perinatal outcomes during pregnancy: a single-center cohort study of a Chinese population // PLoS. 2014. Vol. 9(10). Р. 1093–1094.
25. Schneuer F.J., Nassar N., Tasevski V. et al. Association and predictive accuracy of high TSH serum levels in first trimester and adverse pregnancy outcomes //J Clin Endocrinol Metab. 2012. Vol. 97. Р. 3115–3122.
26. Henrichs J., Ghassabian A., Peeters R.P., Tiemeier H. Maternal hypothyroxinemia and effects on cognitive functioning in childhood: how and why? //Clin Endocrinol (Oxf). 2013. Vol. 79. Р. 152–162.
27. Pop V.J., Brouwers E.P., Vader H.L. et al. Maternal hypothyroxinaemia during early pregnancy and subsequent child development: a 3-year followup study //Clin Endocrinol (Oxf). 2003. Vol. 59. Р. 282–288.
28. Korevaar T.I., Schalekamp-Timmermans S., de Rijke Y.B. et al. Hypothyroxinemia and TPOantibody positivity are risk factors for premature delivery: the generation R study // J Clin Endocrinol Metab. 2013. Vol. 98(11). Р. 4382–4390.
29. Lazarus J.H., Bestwick J.P., Channon S. et al. Antenatal thyroid screening and childhood cognitive function // N Engl J Med. 2012. Vol. 366(6). Р. 493–501.
30. Ashoor G., Muto O., Poon L.C. et al. Maternal thyroid function at gestational weeks 11–13 in twin pregnancies //Thyroid. 2013. Vol. 23(9). Р. 1165–1171.
31. Tan J.Y., Loh K.C., Yeo G.S., Chee Y.C. Transient hyperthyroidism of hyperemesis gravidarum // BJOG. 2002. Vol. 109. Р. 683–688.
32. Yoshihara A., Noh J.Y., Mukasa K. et al. Serum human chorionic gonadotropin levels and thyroid hormone levels in gestational transient thyrotoxicosis: Is the serum hCG level useful for differentiating between active Graves’ disease and GTT? // Endocr J. 2015. Vol. 62(6). Р. 557–560.
33. Nakamura H., Miyauchi A., Miyawaki N., Imagawa J. Analysis of 754 cases of antithyroid drug-induced agranulocytosis over 30 years in Japan // J Clin Endocrinol Metab. 2013. Vol. 12. Р. 4776–4783.
34. Anderson S., Olsen J., Laurberg P. Antithyroid Drug Side Effects in the Population and in Pregnancy // JCEM. 2016. Vol. 101(4). Р. 1606–1614.
35. Yoshihara A., Noh J., Yamaguchi T. et al. Treatment of Graves’ disease with antithyroid drugs in the first trimester of pregnancy and the prevalence of congenital malformation //J Clin Endocrinol Metab. 2012. Vol. 97(7). Р. 2396–2403.
36. Andersen S.L., Olsen J., Wu C.S., Laurberg P. Birth defects after early pregnancy use of antithyroid drugs: a Danish nationwide study //J Clin Endocrinol Metab. 2013. Vol. 98(11). Р. 4373–4381.
37. Laurberg P., Andersen S.L. Therapy of endocrine disease: antithyroid drug use in early pregnancy and birth defects: time windows of relative safety and high risk? // Eur J Endocrinol. 2014. Vol. 171(1). Р. 13–20.
38. Andersen S.L., Olsen J., Wu C.S., Laurberg P. Severity of birth defects after propylthiouracil exposure in early pregnancy //Thyroid. 2014. Vol. 10. Р. 1533–1540.
39. Sahin S.B., Ogullar S., Ural U.M. et al. Alterations of thyroid volume and nodular size during and after pregnancy in a severe iodine-deficient area //Clin Endocrinol (Oxf). 2014. Vol. 81(5). Р. 762–768.
40. Marley E.F., Oertel Y.C. Fine-needle aspiration of thyroid lesions in 57 pregnant and postpartum women // Diagn Cytopathol. 1997. Vol. 16. Р. 122–125.
41. Kung A.W., Chau M.T., Lao T.T. et al. The effect of pregnancy on thyroid nodule formation // J Clin Endocrinol Metab. 2002. Vol. 87. Р. 1010–1014.
42. Vannucchi G., Perrino M., Rossi S. et al. Clinical and molecular features of differentiated thyroid cancer diagnosed during pregnancy // Eur J Endocrinol. 2010. Vol. 162. Р. 145–151.
43. Messuti I., Corvisieri S., Bardesono F. et al. Impact of pregnancy on prognosis of differentiated thyroid cancer: clinical and molecular features //Eur J Endocrinol. 2014. Vol. 170(5). Р. 659–666.
44. Uruno T., Shibuya H., Kitagawa W. et al. Optimal Timing of Surgery for Differentiated Thyroid Cancer in Pregnant Women // World J Surg. 2014. Vol. 38. Р. 704–708.
45. Vaidya B., Hubalewska-Dydejczyk A., Laurberg P. et al. Treatment and screening of hypothyroidism in pregnancy: results of a European survey // European Journal of Endocrinology. 2012. Vol. 16. Р. 649–54.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам
последствия пониженного уровня тиреотропного гормона для плода, при планировании беременности
Поддержание оптимального уровня гормонов щитовидной железы при беременности очень важно. Это необходимо для того, чтобы малыш полноценно рос и развивался в материнской утробе. Низкий уровень ТТГ по время беременности является опасным состоянием, требующим проведения обязательной коррекции.
Что это такое?
Между щитовидной железой и гипофизом существует довольно сильное взаимодействие. Оба этих органа выбрасывают гормоны в кровоток, которые необходимы для осуществления многих реакций и жизненно важных процессов в организме.
Гипофиз — это структура головного мозга. Он выбрасывает в системный кровоток гормон, который называется тиреотропным. Его появление в крови приводит к тому, что щитовидная железа начинает вырабатывать свои гормональные вещества.
Пониженный уровень ТТГ в крови способствует тому, что начинают возникать разнообразные патологии как в организме будущей мамочки, так и ее развивающего малыша.
Сохранение баланса между тиреоидными и тиреотропным гормонами очень важно при планировании беременности. Эта ситуация необходима для того, чтобы успешно произошло зачатие, и началось внутриутробное развитие малыша.
ТТГ непосредственно не оказывает существенного действия на женский организм. Влияют на протекающие в нем процессы тиреоидные гормоны Т3 и Т4. Именно они оказывают воздействие на работу сердечно-сосудистой, нервной системы, а также на функционирование желудочно-кишечного тракта.
Снижение ТТГ способствует повышению в крови тиреоидных гормонов, что и приводит к тому, что у будущей мамы начинают возникать определенные неблагоприятные клинические проявления.
Симптомы
Выраженность клинических признаков сниженного ТТГ в крови бывает разной. Во многом она зависит от того, насколько стали повышены тиреоидные гормоны Т3 и Т4. При их существенном повышении у будущей мамы и начинают проявляться неблагоприятные симптомы, которые существенно ухудшают качество ее жизни.
Такая ситуация приводит к тому, что женщина начинает терять в весе. В некоторых случаях масса ее тела остается нормальной, но существенных прибавок, положенных по срокам беременности, врачи у нее не отмечают.
Женщина начинает худеть на фоне повышенного аппетита. Некоторые мамочки отмечают, что при таком состоянии они испытывают «волчий» голод и начинают употреблять огромное количество пищи. При этом им бывает довольно трудно насытиться.
У женщины появляется сильная потливость. Причем она, как правило, жалуется на появление большого количества пота практически на всех участках своего тела. Такой системный гипергидроз беспокоит будущую маму как в дневное время, так и ночью.
Повышение в крови Т3 и Т4 способствует нарушениям в работе сердечно-сосудистой системы. Это обычно проявляется изменениями и сбоями сердечного ритма.
Частое проявление такой ситуации — развитие аритмии. В этом случае женщина может чувствовать «перебои» в работе сердца или сбивчивый сердечный ритм. Особенно неблагоприятно, если на фоне такой ситуации у будущей мамы появляется выраженное головокружение.
Скачки артериального давления — еще один возможный признак, который встречается при снижении ТТГ в крови. Часто женщина жалуется на стойкое повышение АД. В этом случае, как правило, повышается «верхнее» или систолическое артериальное давление. При неблагоприятном течении патологии его цифры могут достигать даже 160-180 мм. рт. ст. и выше.
Возрастающая в крови концентрация тиреоидных гормонов приводит к неврологическим нарушениям. Это обычно проявляется появлением сильного патологического дрожания (тремора) рук.
Данный симптом приводит к тому, что женщине бывает трудно вставить нитку в иголку или даже писать ручкой по бумаге.
Некоторые будущие мамы, имеющие сниженную концентрацию в крови ТТГ, жалуются своим врачам на то, что у них появляется постоянное ощущение «жара». Это приводит к тому, что женщина выбирает неподходящую одежду для прогулок на улице и простужается. Развитию простуды также способствует сильное потоотделение.
Изменение поведения — один из самых характерных симптомов, которые возникают при этой патологии. Оно проявляется тем, что у будущей мамочки появляется сильная тревожность, нервозность.
У многих женщин, имеющих данные нарушения, усиливается агрессивность. Они могут «вспылить» по пустякам, часто ссорятся со своим мужем и близкими родственниками, могут «срываться» на детей.
Чрезмерная активность и стремление к бурной деятельности — также характерный признак данной патологии. Несмотря на свое положение, женщина старается вести очень активный образ жизни, постоянно находится в движении. Ее день, буквально, расписан по минутам. На фоне такой активной деятельности она не чувствует никакой усталости.
Нарастание в крови Т3 и Т4 способствует тому, что женщина начинает быстрее говорить. Довольно часто это проявляется тем, что она начинает «заговариваться» и даже путать слова. Важно отметить, что данные возникшие нарушения в своем поведении будущая мама не замечает.
Если об этом ей говорят ее близкие, то реакция на критику бывает крайне агрессивной.
Нормы
Концентрация в крови тиреоидного гормона во время всей беременности меняется. Это обусловлено тем, что гормональный фон у будущей мамочки претерпевает постоянные изменения. Скачки показателей концентрации в ее крови ХГЧ, пролактина и других специфичных гормонов беременности приводит к тому, что и уровень ТТГ изменяется.
В самые первые дни с момента зачатия малыша концентрация в крови тиреотропного гормона его мамы очень низкая. Затем она начинает постепенно возрастать. В первую половину беременности средняя концентрация в крови этого гормона, как правило, составляет от 0,1 до 3 мМЕ/мл. В дальнейшем уровень ТТГ только растет. Во второй половине беременности его нормальные значения составляют от 0,2 до 4 мМЕ/мл.
Важно отметить, что референтные границы данного показателя могут несколько отличаться в разных лабораториях.
Это зависит от того, на какой аппаратуре проводятся анализы, а также какие единицы измерения использует конкретное медицинское учреждение. Сдать такой лабораторный тест можно по направлению эндокринолога женской консультации или самостоятельно.
Последствия для плода
Если в крови у будущей мамы существенно и длительно снижен ТТГ, это может привести к довольно опасным осложнениям для ее ребенка. Довольно часто такая ситуация приводит к тому, что у малыша нарушаются естественные процессы внутриутробного развития. Опасна данная патология также развитием нежелательных аномалий и пороков, которые могут сформироваться у плода в разных периодах его роста.
Самая критическая ситуация – самопроизвольный выкидыш. Обычно она развивается на самых ранних сроках беременности. Сопровождается такая ситуация, как правило, развитием сильного кровотечения и появлением выраженного болевого синдрома в животе у будущей маме. В этом случае требуется экстренная госпитализация женщины в стационар для проведения ей интенсивного лечения.
Стойкое снижение ТТГ в крови на поздних сроках беременности может способствовать формированию различных патологий плаценты. Это приводит к нарушению течения крови по маточно-плацентарной системе кровотока, что опасно для плода развитием стойкой и выраженной гипоксии.
Лечение
Выявление снижения в крови тиреоидного гормона — обязательный повод для направления будущей мамы на консультацию к эндокринологу. Этот доктор проведет пальпацию щитовидной железы, а также полноценный клинический осмотр.
При необходимости специалист может назначить дополнительные анализы, а также проведение ультразвукового обследования щитовидной железы. Эти тесты необходимы для установления верного диагноза.
Существенное снижение ТТГ в крови будущей мамы — показание для назначения ей антитиреодных лекарственных средств. Эти препараты снижают уровень Т3 и Т4, помогая уменьшить возникшие неблагоприятные симптомы у женщины.
Подбор данных лекарственных средств проводится строго индивидуально. Для этого оценивается исходное состояние женщины, ее вес, характер течения беременности, а также потенциальный риск, который могут оказать такие препараты на плод.
Для устранения нежелательных симптомов со стороны сердечно-сосудистой системы будущей маме назначаются лекарственные средства, направленные на коррекцию возникших нарушений.
Устранить аритмию можно с помощью бета-блокаторов. Использовать такие препараты следует по потребности.
Постоянно употреблять их можно только с разрешением кардиолога.
Контроль за назначенной терапией проводится с помощью проведения регулярных ЭКГ. Такие исследования помогают врачам оценить, насколько изменился сердечный ритм и остались ли какие-либо нарушения на фоне использования лекарственных средств.
Консервативная терапия с применением лекарственных препаратов — базовая мера, которая применяется у беременных женщин. При ее неэффективности обычно требуется проведение хирургического лечения. Однако, при беременности к такому методу терапии врачи стараются не прибегать.
Данные операции проводятся только под общим наркозом. Все наркотические средства являются крайне токсическими для плода. Хирургическое лечение патологий щитовидной железы проводится только по строгим медицинским показаниям и при угрозе жизни беременной женщины.
Следит за состоянием пациентки во время беременности эндокринолог. Именно этот специалист, а не акушер-гинеколог, может проводить подбор лекарственных препаратов, а также выбор их необходимой дозировки.
При необходимости женщину направляют на консультацию к эндокринологу — хирургу для определения дальнейшей тактики ее наблюдения.
О том, что делать при низком ТТГ, смотрите в следующем видео.
Низкий ТТГ при беременности — причины и возможные последствия
Тиреотропин, известный также как тиреотропный гормон – специфическое вещество, которое продуцируется гипофизом, а именно передней долей. Основная функция гормона – влияние на функционирование щитовидки. Дефицит тиреотропина, прежде всего, отражается на деятельности щитовидки.
В период беременности в женском организме происходят разные процессы, изменяется концентрация гормонов. Давайте разберемся – чем грозит маме, будущему ребенку нехватка тиреотропного гормона.
Информация о тиреотропине
Гормон тиреотропин продуцируется головным мозгом, а именно – передней долей гипофиза. Процесс синтеза регулируется гипоталамусом. Рецепторы, которые особенно остро реагируют на изменение количества тиреотропина, расположены в щитовидке.
Тиреотропный гормон регулирует образование двух основных гормонов щитовидки:
- Тироксина – Т4;
- Трийодтиронина – Т3.
Вещества регулируют рост клеток, кроме этого, выполняют следующие задачи:
- Активизируют процесс насыщения клеток кислородами;
- Контролируют уровень давления;
- Регулируют настроение;
- Принимают активное участие в обменных процессах;
- Отвечают за терморегуляцию.
На протяжении суток уровень ТТГ меняется. Максимальный уровень фиксируется ночью – с 2 до 4 часов, к 8 часам утра концентрация снижается. Минимальное содержание гормона в крови с 17 до 19 часов. Если человек ведет ночной образ жизни, синтез тиреотропина нарушается.
Наибольшее значение вещество приобретает в период беременности, так как контролирует деятельность эндокринной системы мамы, будущего малыша. Чтобы отследить работу щитовидки, необходимо, прежде всего, сдать анализ на гормон тиреотропин. Специалисты рекомендуют пройти обследование до момента зачатия – на этапе планирования беременности. Это позволит своевременно выявить нарушения в функционировании щитовидки, устранить их. Необходимо понимать, что низкий уровень гормона никак не отразится на способности к зачатию, но может негативно повлиять на развитие ребенка.
Проблема дефицита ТТГ возникает чаще всего в период беременности, это обусловлено тем, что щитовидная железа не в состоянии синтезировать необходимый объем гормона. Выявить нарушения можно на основании результатов одного анализа. Направление на анализ должен выдать врач. Если специалист по каким-то причинам не выдал направление, можно посетить любую лабораторию и сдать кровь самостоятельно.
Показания ТТГ для женщины в положении в первом триместре должны быть следующими – от 0,1 до 2,5 мЕд/л. Консультация эндокринолога потребуется, если концентрация ТТГ ниже установленной нормы.
Как меняется количество ТТГ после зачатия
В первом триместре концентрация тиреотропина бывает ниже нормы. Как правило, подобное явление бывает у женщин, которых мучает токсикоз. Уже к 14 неделе уровень гормона выравнивается, приходит в норму. Вплоть до родов уровень ТТГ остается практически неизменным.
Нормы тиреотропина по триместрам беременности:
- Первый – от 01, до 2,5 мЕд/л;
- Второй – от 0,2 до 3,0 мЕд/л;
- Третий – от 0,3 до 3,0 мЕд/л.
Результаты диагностики должен трактовать и оценивать только врач.
Как проходить диагностику:
- Забор биологического вещества проводится из вены;
- Кровь нужно сдавать натощак, последний прием пищи за 8-14 часов до диагностики;
- Непосредственно перед анализом можно выпить обычную воду;
- Если требуется оценить динамику гормона ТТГ, его сдают несколько раз, желательно в одинаковое время.
Если нарушена техника обследования, результаты могут быть искажены. Также не стоит проходить диагностику в первом триместре, оптимальный период – с 16 по 18 неделю беременности.
Признаки сниженного ТТГ при беременности
Следует отметить, что сниженный уровень тиреотропина у пациенток проявляется по-разному. Симптомы зависят от того, насколько повышено количество гормонов щитовидки.
Прежде всего, гормональный сбой отражается на весе – отмечается снижение массы тела. Бывают ситуации, когда вес остается нормальным, но необходимого при беременности набора веса не фиксируется. При этом вес уменьшается или остается стабильным даже на фоне увеличивающегося аппетита. По отзывам некоторых пациенток, они испытывают сильнейший голод, кушают часто и много, но не насыщаются.
Еще один симптом – потливость. Избыточное потоотделение фиксируется во всех участках тела, независимо от времени суток и времени года.
Изменения уровня гормона может спровоцировать нарушения в функционировании сердечно-сосудистой системы, женщина ощущает изменения сердечного цикла. На фоне гормонального фона проявляется аритмия, ощущаются перебои в работе сердца. Особое внимание необходимо обратить на состояние, когда у женщина аритмия дополнительно осложняется головокружением.
Заподозрить снижение уровня ТТГ можно частым и резким скачкам артериального давления. Часто женщины обращаются к специалисту с жалобой на стабильно высокое систолическое (верхнее) давление.
Следует обратить внимание на неврологические факторы. Дрожь в руках, нервозность могут стать признаком низкого содержания тиреотропина. Ситуация может осложниться настолько, что женщина даже не сможет писать на бумаге текст.
Наиболее выраженный симптом снижения концентрации ТТГ – резкие изменения настроения. Женщина становится нервозной, испытывает тревогу, агрессию. При таком диагнозе женщина может вспылить, часто ссорится с родственниками и друзьями. Также женщина становится чрезмерно активной, начинает очень быстро говорить, постоянно находится в движении и не испытывает усталости. Опасный признак, когда женщина начинает заговариваться.
Норма тиреотропина при беременности
Прежде всего, расшифровкой анализов должен заниматься только врач. Специалист проверяет значения, указанные лабораторией. Дело в том, что условная норма по гормону тиреотропину варьируется в широком диапазоне – от 0,4 до 4 мЕд/л. Данные меняются в зависимости от срока беременности. На протяжении 12 недель показания остаются максимально низкими, затем уровень гормона постепенно повышается.
В большинстве случаев в первом триместре концентрация гормона сохраняется на уровне 0,1 до 2 мЕд/л. Не стоит пугаться, ели показания тиреотропина на нулевом уровне, при многоплодной беременности это произойдет со стопроцентной вероятностью.
Следует учитывать, что результаты и точность результатов зависят от степени чувствительности тест-системы, которую использует лаборатория. Специалисты настоятельно рекомендуют не паниковать, если результат оказался нулевым. Прежде всего, нужно сдать анализ на ТТГ в другой лаборатории. Если результаты повторились, потребуется консультация врача-эндокринолога.
На первых сроках беременности щитовидная железа работает очень интенсивно, вырабатывает повышенное количество гормонов, в связи с этим анализ на ТТГ может показать нулевой результат. Врачи рекомендуют не переживать, дело в том, что организм перестраивается, в том числе, меняется гормональный фон. В большинстве случаев гормональный «перекос» проходит самостоятельно, без медикаментозной терапии. Существует ли необходимость назначать лечение – определит только врач, изучив анализы.
Если врач при сниженном уровне ТТГ рекомендует прерывать беременность – сразу меняйте врача и не слушайте подобные советы.
В каких случаях снижается тиреотропин:
- Индивидуальные особенности организма, обусловленные беременностью;
- Токсический зоб;
- Травма гипофиза;
- Стрессовые ситуации;
- Голодание;
- Лекарственная терапия, которая снижает уровень тиреотропина.
Если результаты анализа показывают резкое снижение уровня гормона, потребуется консультация эндокринолога, поскольку потребуется исключить патологии щитовидки.
Следует учесть – не все женщины должны проходить диагностику на ТТГ. Показания следующие:
- Патологии эндокринной системы в анамнезе;
- Постоянный контроль гормона при существующих заболеваниях щитовидки;
- Характерные признаки сердечных заболеваний – аритмия, отдышка.
Кроме этого, абсолютным показанием к диагностике является обследование женщина в случае бесплодия.
Последствия резкого снижения гормона ТТГ для будущего ребенка
Снижение концентрации гормона в первом триместре беременности не опасно для мамы и ее ребенка. Подобное явление является нормальным и не требует лечения, только наблюдения. Снижение концентрации наблюдается при выраженном токсикозе. Если к 15-16 неделе уровень гормона не восстанавливается, требуется дополнительное обследование, поскольку на данном этапе важно своевременно выявить возможные заболевания щитовидки.
Один из опасных патологических симптомов – увеличение щитовидки. В медицине подобное состояние называют гипертиреоз или тиреотоксикоз. Данное патологическое состояние диагностируется только у 2%-4% беременных.
У небеременных женщин гипертиреоз сопровождается отсутствием менструации (аменореей).
К слову, именно гипертиреоз – частая причина бесплодия, на фоне этого заболевания развиваются подобные осложнения:
- Выкидыш;
- Гестоз;
- Преждевременные роды;
- Отслойка плаценты;
- Анемия;
- Гипоксия;
- Задержка в развитии плода.
У 3% беременных на фоне тиреоксикоза происходит заражение плода агрессивными антителами. Выявить заболевание можно по таким признакам:
- Чрезмерная возбудимость;
- Резкое увеличение частоты сердечных сокращений;
- Снижение веса;
- Ухудшение зрения.
При врожденном тиреотоксикозе в большинстве случаев ребенку не нужно специального лечения – все симптомы исчезают к шести месяцам. Если состояние новорожденного тяжелое, терапию назначает эндокринолог.
К сожалению, на фоне уменьшения концентрации тиреотропина, осложненного тиреотоксикозом, беременность под угрозой и сохранит ее вряд ли получится. Если состояние пациентки тяжелое, единственным решение проблемы станет прерывание беременности. Если беременность удается сохранить, женщина требует постоянного наблюдения у врача-эндокринолога. Что касается родоразрешения, вероятнее всего, будет показано кесарево сечение. Естественные роды возможны только при удовлетворительном состоянии беременной.
Причины снижения тиреотропина при беременности
Прежде всего, причиной снижений ТТГ может стать многоплодная беременность. Некоторые врачи считают, что снижение гормона до нулевой отметки указывает на беременность двойней или даже тройней и организм тратит ресурсы на развитие младенцев. Если многоплодная беременность не подтверждается, необходимо искать другие причины. Снижение уровня ТТГ может указывать на такие патологии:
- Доброкачественная опухоль щитовидки;
- Лечение гормональными препаратами;
- Болезнь Пламмера.
Не стоит паниковать раньше времени, чтобы установить диагноз, потребуется дополнительная диагностика. Только на основании полученных результатов врач принимает решение о дальнейших действиях.
Если ТТГ снижен, но уровень Т4 нормальный
Ситуация с синтезом гормонов следующая – если щитовидная железа продуцирует недостаточное количество гормона роста Т4, гипофиз, чтобы сбалансировать ситуацию, начинает синтезировать больше тиреотропина. Если гормон Т4 образуется в большом количестве, соответственно, концентрация тиреотропина снижается.
В организме беременной женщины ситуация, когда уровень Т4 нормальный, а уровень ТТГ снижен, предварительно указывает следующее:
- Развивающаяся патология Грейвса-Базедова;
- Прием лекарств определенных групп.
Главное при таких показателях анализа не отчаиваться, а своевременно начать терапию. Чтобы нежелательные результаты диагностики не застали вас врасплох, пройдите полное обследование в период планирования беременности.
Влияние уровня йода женщины во время беременности на IQ будущего ребенка
Йод дефицитные заболевания объединяют не только патологию Щитовидной железы, резвившуюся вследствие дефицита йода, но и патологические состояния, обусловленные дефицитом Тиреоидных гормонов.
Влияние щитовидной железы на становление интеллектуальных функций человека начинается на самых ранних этапах развития нервной системы.
В первом триместре беременности под действием гормонов щитовидной железы происходит миграция нервных клеток, образование коры головного мозга и других функциональных центров нервной системы будущего ребенка.
Также в это время закладывается внутреннее ухо (улитка и нервный аппарат) и двигательные зоны мозга, которые в будущем станут управлять движениями ребенка. Важно заметить, что в первом триместре беременности щитовидная железа плода еще не работает и потому потребность плода в гормонах щитовидной железы покрывается исключительно за счет работы щитовидной железы матери.
Если щитовидная железа матери работает нормально, то и мозг ребенка развивается хорошо. А что если еще до начала беременности будущая мама страдала скрытым зобом (скажем по причине недостатка йода в воде и пищевых продуктах)? Во время беременности дефицит йода становится еще более выраженным, а результирующий из этого дефицит гормонов щитовидной железы начинает тормозить развитие мозга ребенка, который затем рождается с более или менее выраженным психомоторным отставанием. Клинические исследования последнего времени показывают, что дети, рожденные матерями с гипотиреозом (скрытым или выраженным) чаще других страдают врожденной тугоухостью, двигательными нарушениями, хуже учатся и склонны к развитию различных расстройств поведения. Нужно заметить, что эти и другие нарушения, вызванные недостатком йода и гормонов щитовидной железы в течение первого триместра беременности невозможно исправить при помощи более позднего введения этих веществ.
Во втором триместре беременности начинает работать щитовидная железа плода, поэтому организм будущего ребенка становится более или менее независимым от работы щитовидной железы матери. Однако и в конце беременности более 20% общей потребности плода в гормонах щитовидной железы покрывается за счет гормонов материнского происхождения.
В течение второго и третьего триместров беременности гормоны щитовидной железы обеспечивают процессы синаптогенеза (образование контактов между нервными клетками) и миелинизации (покрытие нервных волокон особым жировым слоем, необходимым для проведения нервных импульсов).
После рождения гормоны щитовидной железы влияют на протекание синтетических и строительных процессов мозга, что в значительной степени определяет интеллект растущего ребенка. Показано, что в географических регионах с недостатком йода показатель интеллекта детей (IQ) ниже в среднем на 10-15 баллов, чем в зонах с достаточным содержанием йода в окружающей среде. Таким образом, можно говорить о социальной значимости заболеваний щитовидной железы и дефицита гормонов щитовидной железы во время беременности, ведь снижение показателя интеллекта большей части популяции региона, влияет на его экономику и культуру.
Для предотвращения дефицита йода и гормонов щитовидной железы во время беременности рекомендуется:
- На этапе планирования беременности:
А) осуществить контроль ТТГ, АткТПО, в случае гипотиреоза обратится к эндокринологу с целью коррекции функции щитовидной железы.
Б) Принимать Калия йодид 250 мкрг в сутки.
- Во время беременности:
А) контроль ТТГ, Атк ТПО при возникновении беременности
Б) для профилактики йододефицита, рекомендуется принимать витаминно-минеральные препараты, содержащие йод ( суточная потребность 250мкрг).
Беременных женщин с высоким уровнем антител к целиакии подвержены риску рождения детей с низкой массой тела — ScienceDaily
Беременные женщины со средним и высоким уровнем антител, характерными для пациентов с целиакией, подвержены риску рождения детей с пониженной массой плода и массой тела при рождении согласно новому исследованию, опубликованному в Gastroenterology , официальном журнале Американской гастроэнтерологической ассоциации. Антитела к тканевой трансглутаминазе (анти-tTG) чаще всего обнаруживаются у пациентов с глютеновой болезнью.
«Хотя несколько наблюдательных исследований показали, что целиакия связана с различными исходами беременности, это исследование учитывает фактические уровни тканевой трансглутаминазы, которые отражают степень повреждения слизистой оболочки, связанного с недиагностированной глютеновой болезнью или ограниченным соблюдением безглютеновой диеты. «Эта дифференциация имеет решающее значение, поскольку большинство случаев целиакии остаются невыявленными», — сказала Джессика Кифте-де Йонг, магистр медицинских наук, Медицинский центр Университета Эразма и ведущий автор исследования.
Исследователи провели популяционное перспективное когортное исследование 7046 беременных женщин и разделили субъектов на три группы: отрицательные анти-tTG (контроль), промежуточные анти-tTG (чуть ниже клинической пороговой точки, используемой для диагностики пациентов с глютеновой болезнью). болезнь) и положительный анти-tTG (пациенты с высокой вероятностью целиакии). Плоды женщин с положительным уровнем антител к ТТГ во втором триместре весили на 16 граммов меньше, чем у женщин с отрицательными уровнями антител к ТТГ, и на 74 грамма меньше в течение третьего триместра.
Людей с промежуточным уровнем антител к тТГ обычно не считают потенциальными пациентами с целиакией, однако исходы родов у этих людей также были затронуты. Младенцы от женщин с промежуточным и положительным анти-tTG весили при рождении на 53 грамма и 159 граммов меньше, соответственно, чем у женщин с отрицательными анти-tTG.
«Исследователям необходимо изучить естественную историю и долгосрочные последствия промежуточных уровней анти-tTG, чтобы определить, вызваны ли эти уровни беременностью или отражают субклиническое состояние целиакии, требующее последующего наблюдения», — добавил Джонг.
Кроме того, помогая определить связь между уровнями антител к тТГ и целиакией, исследование Clinical Gastroenterology and Hepatology подтверждает недавние рекомендации Европейского общества детской гастроэнтерологии, гепатологии и питания (ESPGHAN), в которых признается вероятность возникновения целиакии. увеличивается с увеличением концентрации антител.
В исследовании, проведенном университетскими больницами Лёвена, Бельгия, подчеркивается важность мониторинга соответствующих симптомов, таких как потеря веса, недостаточное развитие, анемия, дефицит железа или усталость, при диагностике пациентов, и отмечается, что врачи не должны полагаться исключительно на анти- Тестирование tTG для постановки диагноза.
Исследование показало, что существует от 50 до 75 процентов вероятности того, что люди без симптомов, но с уровнем анти-tTG более чем в 10 раз превышающим пороговое значение, определенное в рекомендациях ESPGHAN, будут иметь целиакию. Вероятность того, что у пациента глютеновая болезнь, возрастает до 95 процентов или выше, когда, помимо высоких уровней анти-tTG, пациент выражает жалобы, которые могут быть связаны с глютеновой болезнью.
История Источник:
Материалы предоставлены Американской гастроэнтерологической ассоциацией . Примечание. Содержимое можно редактировать по стилю и длине.
Целиакия во время беременности: что нужно знать, когда вы ждете
При глютеновой болезни важно соблюдать особые меры предосторожности. Вот что вам следует знать.
Когда вы ждете рождения ребенка, важно сделать упор на здоровье и питание. Это может быть проблемой само по себе, когда вы боретесь с утренним недомоганием и боретесь с тягой к нездоровой пище.Глютеновая болезнь добавляет дополнительные трудности к этому уравнению, а также делает сбалансированное питание еще более важным приоритетом.
Вообще говоря, безглютеновая диета может содержать мало основных питательных веществ, включая кальций, железо, витамины группы B, клетчатку, цинк, витамин D и магний. Чтобы гарантировать, что ваш развивающийся ребенок получает питательные вещества, необходимые ему для роста, вам, возможно, придется более внимательно относиться к своей диете во время беременности.
Продолжайте читать, чтобы узнать больше о том, как управлять глютеновой болезнью во время беременности, включая обзор того, как глютеновая болезнь влияет на беременность, какие проблемы вам следует ожидать, а также несколько простых советов по сохранению здоровья как вас, так и вашего ребенка.
Как целиакия влияет на беременность?
Целиакия — одно из самых распространенных аутоиммунных заболеваний в мире, но исследователи все еще не могут полностью его понять. Поскольку глютеновая болезнь проявляется по-разному, ее часто не диагностируют в течение месяцев или лет, что может привести к довольно серьезным проблемам со здоровьем, включая хроническую усталость и недоедание. Даже при правильном лечении глютеновая болезнь может вызвать некоторые проблемы со здоровьем, особенно когда вы беременны.
Глютеновая болезнь, которую когда-то считали мальабсорбционным заболеванием у детей, вызывает симптомы, которые выходят далеко за рамки желудочно-кишечных заболеваний, таких как диарея и рвота. Фактически, новое исследование предполагает, что между глютеновой болезнью и репродуктивными нарушениями у женщин может быть связь. Нелеченная целиакия связана с более короткой продолжительностью фертильной жизни, более короткими периодами грудного вскармливания и низким уровнем фертильности. Большинство из этих проблем были решены, когда пациент перешел на безглютеновую диету, но есть некоторые опасения, что глютеновая болезнь может повлиять на беременность, даже если пациент ест без глютена.
В обзоре литературы, опубликованном в выпуске Human Reproduction Update в марте или 2014 г., ведущий автор доктор Кьяра Терсинги выделяет два механизма, посредством которых глютеновая болезнь влияет на беременность: дефицит питания и аутоиммунные механизмы.
Что касается дефицита питательных веществ, глютеновая болезнь может вызывать дефицит селена, цинка и фолиевой кислоты — все они являются важными питательными веществами для здоровой беременности. Когда дело доходит до аутоиммунных механизмов и их влияния на беременность, есть две возможности.Первая возможность заключается в том, что антитела против трансглутаминазы (tTG) связываются с эмбрионом и вызывают повреждение плаценты. Вторая возможность состоит в том, что антитела против tTG повреждают эндотелиальные клетки эндометрия матери.
Требуются дополнительные исследования для всех этих возможностей, но исследования показывают, что правильное питание во время беременности имеет особое значение для женщин с глютеновой болезнью.
Какие проблемы вам следует ожидать во время беременности?
Любая беременная женщина подвержена риску различных осложнений.Выкидыш, железодефицитная анемия и преждевременные роды — все это риски, о которых должна знать любая беременная женщина. Однако вы можете быть удивлены, узнав, что женщины с глютеновой болезнью испытывают проблемы с беременностью и осложнения гораздо чаще — примерно в два-четыре раза чаще, чем женщины без целиакии.
В итальянском исследовании, опубликованном в 2010 году, собраны данные о частоте репродуктивных нарушений и осложнений беременности у женщин с целиакией. Из всех участников 65% женщин с глютеновой болезнью сообщили по крайней мере об одном гестационном расстройстве во время беременности по сравнению с 31% женщин без глютеновой болезни.На момент беременности у 85% женщин диагноз не был поставлен.
Вот обзор некоторых проблем и осложнений беременности, выявленных в этом исследовании:
- Примерно 41% женщин с глютеновой болезнью страдали тяжелой анемией во время беременности по сравнению с 2% контрольных субъектов.
- Только 9% женщин без целиакии испытали угрозу прерывания беременности или выкидыша по сравнению с 39% женщин с глютеновой болезнью.
- Отслойка плаценты, состояние, при котором плацента отделяется от стенки матки, затронула 1% женщин контрольной группы, но 18% женщин с целиакией.
- Ни одна из контрольных женщин не страдала гестационной гипертензией по сравнению с 10% женщин с глютеновой болезнью.
- Аномальная активность мышц матки, известная как гиперкинез матки, затронула 10% женщин с глютеновой болезнью и никого из контрольных субъектов.
- Неправильная скорость роста, известная как ограничение внутриутробного развития, затронула более 6% женщин с глютеновой болезнью, но ни одного из контрольных субъектов.
Другое исследование показало связь между глютеновой болезнью и низкой массой тела при рождении.Риск низкой массы тела при рождении, по-видимому, выше у женщин с недиагностированной глютеновой болезнью, и у этих женщин также обычно бывает более короткая беременность — до двух недель короче. Женщинам с глютеновой болезнью также требуется кесарево сечение чаще, чем женщинам, не страдающим глютеновой болезнью. Есть также некоторые свидетельства того, что дети, рожденные в результате кесарева сечения, имеют более высокий риск развития глютеновой болезни в дальнейшем.
Имейте в виду, что многие проблемы и осложнения беременности у женщин с глютеновой болезнью либо полностью исчезают, либо значительно уменьшаются, когда женщина переходит на безглютеновую диету.Серьезные осложнения, такие как бесплодие и выкидыш, гораздо более вероятны у женщин с недиагностированной глютеновой болезнью, чем у женщин с глютеновой болезнью, соблюдающих безглютеновую диету.
Продолжайте читать, чтобы получить несколько советов по сохранению здоровья вас и вашего ребенка во время беременности.
Простые советы по сохранению здоровья вас и вашего ребенка
Здоровье вашего ребенка напрямую связано с вашим собственным, поэтому вам нужно позаботиться о себе, если вы хотите позаботиться о своем ребенке.Если вы беременны и у вас уже были проблемы с беременностью, вы можете пройти тест на целиакию, особенно если у вас также были симптомы пищеварения, хроническая усталость или другие проблемы со здоровьем.
Если вам уже поставили диагноз целиакия, вот несколько простых вещей, которые вы можете сделать, чтобы сохранить здоровье себе и своему ребенку на протяжении всей беременности:
- Чтобы предотвратить анемию, ешьте много продуктов, богатых железом . К ним относятся темные листовые овощи, говядина, баранина, сладкий картофель, брокколи и горох.
- Убедитесь, что вы получаете достаточно фолиевой кислоты для здорового развития мозга вашего ребенка. . Источники питания включают фасоль пегую, черную фасоль, чечевицу, темную листовую зелень, цитрусовые, брокколи и арахис.
- Поддерживайте здоровое развитие костей, получая большое количество кальция, витамина D и магния . Если у вас также непереносимость лактозы, ищите немолочные источники, такие как рыбные консервы, листовая зелень и напитки, обогащенные кальцием.
- Увеличьте потребление омега-3 жирных кислот или принимайте добавки с рыбьим жиром .Природные источники омега-3 включают тунец, лосось, сардины и озерную форель.
- Получите дневную дозу активности, совершив прогулку . Поговорите со своим врачом о том, какой уровень физической активности соответствует вашему здоровью и физической форме.
- Подумайте о том, чтобы сдать кровь . Если вам недавно поставили диагноз целиакия, возможно, у вас уже есть дефицит питательных веществ. Анализ крови поможет вашему врачу определить, каких питательных веществ вам не хватает, и как лучше всего устранить этот недостаток.
- Обязательно включайте в свой рацион цельнозерновые . Многие беременные женщины испытывают запор во втором или третьем триместре. Вы можете бороться с этим, увеличивая потребление цельнозерновых продуктов без глютена, таких как теф и киноа.
Поскольку нелеченная глютеновая болезнь значительно увеличивает риск осложнений при беременности, вам необходимо как можно строже придерживаться безглютеновой диеты. Запаситесь закусками без глютена, такими как хлеб и крекеры, в те дни, когда вы испытываете тягу к углеводам, и старайтесь есть разнообразные продукты без глютена, чтобы обеспечить баланс питательных веществ в своем рационе.Вы также можете поговорить со своим врачом о пищевых добавках, чтобы убедиться, что вы соблюдаете рекомендуемую дневную норму.
Тело каждой женщины уникально, поэтому беременность будет полностью вашей. Лучшее, что вы можете сделать, — это придерживаться безглютеновой диеты и постараться получить правильный баланс питательных веществ. Обязательно поговорите со своим врачом о способах обеспечения сбалансированного питания и предотвращения любых проблем с беременностью, которые могут у вас возникнуть.
Как глютеновая болезнь влияет на беременность
Глютеновая болезнь (ЦБ), одно из самых распространенных аутоиммунных заболеваний в мире, также является одним из наиболее недиагностируемых, в немалой степени благодаря множеству различных способов ее проявления в клинике. В прошлом БК считали детским мальабсорбционным заболеванием и характеризовались хронической диареей, вздутием живота, утомляемостью и рвотой. Но пациенты с БК могут испытывать многие симптомы, не связанные с желудочно-кишечным трактом, и в недавней статье из Италии сделана попытка проанализировать, как БК может влиять на репродуктивное здоровье женщин.
Статья была опубликована на сайте Human Reproduction Update 11 марта 2014 г. и озаглавлена «Целиакия и репродуктивные расстройства: метаанализ эпидемиологических ассоциаций и потенциальных патогенных механизмов». Первая часть статьи представляла собой мета-обзор других статей в литературе, в которых исследовалась связь между CD и различными репродуктивными расстройствами. Во второй части были рассмотрены возможные механизмы того, как БК влияет на репродуктивное здоровье женщин.
В обзоре литературы авторы, во главе с первым автором доктором Кьярой Терсиньи, обнаружили, что нелеченый CD был связан с различными репродуктивными расстройствами, но эта взаимосвязь исчезла после того, как пациенты перешли на безглютеновую диету. Например, авторы обнаружили, что женщины с нелеченым CD имели как более короткую продолжительность фертильной жизни, так и более короткий период грудного вскармливания, но после лечения безглютеновой диетой пациенты вернулись к нормальному состоянию. Также было показано, что невылеченная БК влияет на фертильность.В крупном шведском исследовании ученые обнаружили, что в целом показатели фертильности между пациентами с CD и контрольной группой были одинаковыми, но за 2 года до постановки диагноза, когда CD, скорее всего, был активен, но не лечился, фертильность была значительно снижена у женщин с CD.
Доктор Терсиньи и другие авторы затем определили отношения шансов (OR) и их 95% доверительный интервал (95% CI) для того, насколько вероятно, что у пациента есть CD, на основе того, есть ли у них различные репродуктивные расстройства, используя «обширный поиск литературы» отдельные базы данных.Они обнаружили, что недиагностированная CD была связана с необъяснимым бесплодием (OR = 5,06, 95% CI 2,13-11,35), повторным выкидышем (OR = 5,82, 95% CI 2,30-14,74) и задержкой внутриутробного развития (IUGR) (OR = 8,73, 95% ДИ 3,23–23,58), но не было обнаружено никакой связи для преждевременных родов и маленьких детей для гестационного возраста (SGA).
Исследователи также использовали свой литературный поиск, чтобы определить относительный риск (ОР) этих состояний для пациентов с БК по сравнению с контрольной группой. ОР составил 1,39 для выкидыша (95% ДИ 1.15-1,67), 1,54 для ЗВУР (95% ДИ 1,22-1,95), 1,75 для детей, рожденных с низкой массой тела при рождении (НМТ) (95% ДИ 1,23-2,49) и 1,37 для преждевременных родов (95% ДИ 1,19-1,57). . Не было обнаружено увеличения RR для повторного выкидыша, необъяснимого мертворождения или преэклампсии. Повышенный риск IUGR, LBW и преждевременных родов исчез после того, как пациенты прошли лечение от CD с помощью безглютеновой диеты.
Обратите внимание, что отношение шансов и относительный риск — это две разные, но взаимосвязанные концепции. OR основывается на шансах, а RR — на вероятности.В случае этой статьи авторы предполагают, что OR по сути совпадает с RR из-за «предположения о редком заболевании». Однако, когда предположение о редком заболевании не выполняется, OR обычно переоценивает ОР.
Вторая часть статьи была обзором того, что известно о возможных механизмах воздействия CD на беременность. Эти механизмы делятся на две основные категории: недостаточность питания и аутоиммунные механизмы. CD может вызвать дефицит цинка, селена и фолиевой кислоты, которые являются важными соединениями для беременности.Однако, несмотря на то, что имеются лишь ограниченные исследования беременных женщин с CD, есть исследования, которые показывают, что женщины, страдающие бесплодием, связанным с атрофией ворсинок, вызванной CD, не имели признаков дефицита микроэлементов, что означает отсутствие дефицита питательных веществ. отвечает за влияние CD на репродуктивное здоровье.
Авторы изучали, как иммунная система пациенток с CD может повлиять на их беременность. Они предложили две возможности: первая, что антитела против трансглютаминазы (tTG) связываются со слоем трофобласта эмбриона, вызывая повреждение будущей плаценты, и вторая, что антитела против tTG могут повредить цитоскелет эндотелиальных клеток эндометрия мама.Антитела против tTG обычно обнаруживаются только у пациентов, у которых CD активен, что объясняет, почему безглютеновая диета устраняет большинство осложнений беременности, обнаруженных исследователями. Необходимы дополнительные исследования для дальнейшего выяснения механизма между невылеченными БК и репродуктивным здоровьем.
Авторы признают некоторые ограничения в своем исследовании. Поскольку это мета-обзор других исследовательских работ, любая предвзятость в исследованиях может проявиться в их обзоре. Эта статья по-прежнему показывает, что CD имеет серьезные последствия для беременных женщин, но, к счастью, лечение безглютеновой диетой должно облегчить большинство их беспокойств.
Исследование, на котором основана эта статья, можно найти здесь.
Влияние вмешательств во время беременности на вес матери и акушерские исходы: метаанализ рандомизированных данных
Резюме
Цель Оценить влияние диетических вмешательств и изменений образа жизни во время беременности на вес матери и плода и количественно оценить их влияние вмешательства по родовспоможению.
Дизайн Систематический обзор и метаанализ.
Источники данных Основные базы данных с момента создания до января 2012 года без языковых ограничений.
Выбор исследования Рандомизированные контролируемые испытания, в которых оценивали любые изменения в питании или образе жизни, которые могут повлиять на вес матери во время беременности и исходы беременности.
Синтез данных Результаты представлены в виде относительных рисков для дихотомических данных и средних различий для непрерывных данных.
Результаты Мы выявили 44 соответствующих рандомизированных контролируемых испытания (7278 женщин), оценивающих три категории вмешательств: диета, физическая активность и смешанный подход.В целом, при любом вмешательстве наблюдалось снижение на 1,42 кг (95% доверительный интервал от 0,95 до 1,89 кг) гестационного веса при любом вмешательстве по сравнению с контролем. При объединении всех вмешательств не было значительных различий в массе тела при рождении (средняя разница -50 г, от -100 до 0 г) и частоте встречаемости больших для гестационного возраста (относительный риск 0,85, 0,66 до 1,09) или малых для гестационного возраста (1,00 0,78–1,28) между группами, хотя физическая активность сама по себе была связана с пониженной массой тела при рождении (средняя разница от –60 г, от –120 до –10 г).Вмешательства были связаны со снижением риска преэклампсии (0,74, 0,60–0,92) и дистоции плеча (0,39, 0,22–0,70) без значительного влияния на другие критически важные исходы. Диетическое вмешательство привело к значительному снижению прибавки в весе матери во время беременности (3,84 кг, 2,45–5,22 кг) с улучшением исходов беременности по сравнению с другими вмешательствами. Общий рейтинг доказательств был от низкого до очень низкого для важных исходов, таких как преэклампсия, гестационный диабет, гестационная гипертензия и преждевременные роды.
Выводы Вмешательства в диету и образ жизни во время беременности могут снизить прибавку в весе во время беременности и улучшить результаты как для матери, так и для ребенка. Среди вмешательств те, которые основаны на диете, являются наиболее эффективными и связаны с уменьшением прибавки в весе во время беременности и улучшением акушерских исходов.
Введение
Ожирение представляет собой растущую угрозу для женщин детородного возраста. Половина населения имеет избыточный вес (индекс массы тела (ИМТ) 25.0-29,9) или ожирением (ИМТ ≥30) .1 В Европе и Соединенных Штатах 20-40% женщин набирают во время беременности вес больше рекомендованного 2. Повышенный вес матери или чрезмерное увеличение веса во время беременности связаны с неблагоприятным течением беременности. исходы.3 Половина женщин, которые умирают во время беременности, родов или послеродового периода в Соединенном Королевстве, страдают ожирением или избыточным весом.4 Для потомства материнское ожирение является основным фактором риска детского ожирения, которое сохраняется в зрелом возрасте независимо от других факторов.5 Ожирение обходится Национальной службе здравоохранения Великобритании (NHS) примерно в 0,5 миллиарда фунтов стерлингов в год, а экономика Великобритании — еще на 2,3 миллиарда фунтов стерлингов в виде косвенных затрат6
Дородовой период с возможностью регулярного контакта с медицинскими работниками считается идеальным время вмешаться, поскольку у матерей есть мотивация для внесения изменений, которые могут оптимизировать их исход и исход ребенка7. Необходимо определить соответствующие меры по контролю веса, которые являются эффективными и безопасными во время беременности. Существующие обзоры и руководящие принципы ограничены в своих рекомендациях из-за небольшого количества включенных исследований.8 9 Они не смогли определить наилучшее вмешательство, которое оптимизирует результаты для матери и ребенка.9 10 Также отсутствует консенсус в отношении того, что считать важными результатами. Рекомендации Института медицины (IOM) предоставляют контрольные диапазоны для оптимального набора веса во время беременности для женщин с нормальным весом, избыточным весом и ожирением на основе данных наблюдений.11 Учитывая потенциальную важность вмешательств по контролю веса во время беременности, мы систематически анализировали влияние влияние диет и образа жизни на различные результаты оценивалось по степени их важности.
Методы
Мы провели систематические обзоры в соответствии с протоколами, разработанными с использованием рекомендованных в настоящее время методов обзора12 13 14, и ранжировали результаты по важности с помощью двухэтапного опроса Delphi.15
Идентификация исследований
Мы провели поиск в Medline, Embase, BIOSIS, LILACS , Индекс научного цитирования, Кокрановская база данных систематических обзоров (CDSR), Кокрановский центральный регистр контролируемых исследований (CENTRAL), База данных рефератов обзоров эффектов (DARE), База данных оценки технологий здравоохранения (HTA) и PsychInfo с момента создания до января 2012 г. для определения релевантных цитат.Мы провели поиск соответствующих неопубликованных исследований и исследований, опубликованных в «серой» литературе, в таких базах данных, как «Inside Conferences», «Системы информации в« серой литературе »» (SIGLE), «Тезисы диссертаций» и «Clinical Trials.gov». Интернет-поиск также проводился с помощью специализированных поисковых шлюзов (таких как OMNI: www.omni.ac.uk), общих поисковых систем (таких как Google) и метапоисковых систем (таких как Copernic: www.copernic.com). Комбинация поисковых слов охватывала понятие «беременность и вес», включая MeSH, произвольный текст и варианты слов.Языковые ограничения не применялись.
Выбор исследования
Электронный поиск был тщательно изучен, и были отобраны полные рукописи всех цитат, которые могли бы соответствовать заранее определенным критериям отбора. Независимые рецензенты (ER и SG) изучили эти рукописи и приняли окончательные решения относительно включения или исключения. Когда возникали разногласия, они разрешались путем консенсуса или арбитража с третьим рецензентом (ST). В случае дублирования публикаций мы выбирали самые свежие и полные версии.Были включены рандомизированные контролируемые испытания, в которых оценивались любые изменения в питании или образе жизни, которые могут повлиять на исходы для матери и плода, связанные с весом. Два независимых обозревателя (ER, SG) классифицировали вмешательства как подход, основанный в основном на диете, физической активности или смешанный (с компонентами диеты и физической активности, которые могут или не могут быть подкреплены поведенческой теорией). Любые разногласия разрешались путем обсуждения с третьим рецензентом (ST). Мы исключили исследования беременных женщин с недостаточным весом (ИМТ <18.5).
Оценка качества исследования и извлечение данных
Качество, определяемое как степень, в которой оценка эффекта могла быть правильной или беспристрастной, оценивалось в соответствии с принятыми современными стандартами.16 17 Риск систематической ошибки в отдельных исследованиях оценивался с учетом шесть пунктов: генерация последовательности, сокрытие распределения, ослепление, неполные данные о результатах, выборочная отчетность по результатам и другие потенциальные источники систематической ошибки. Эта информация предоставила данные для одного из доменов, используемых в рейтинге доказательств (см. Ниже).Два независимых эксперта (ER и SG) извлекали данные в двух экземплярах, используя заранее разработанные и апробированные формы извлечения данных. Мы попытались получить недостающую информацию, связавшись со следователями.
Синтез данных
Мы рассчитали относительные риски с 95% доверительным интервалом для дихотомических данных. Непрерывные данные были суммированы как средние различия со стандартными отклонениями. Мы использовали статистику I 2 для оценки статистической неоднородности между испытаниями и исследовали возможные причины, если мы обнаружили существенную неоднородность (I 2 > 50%).Были выполнены мета-анализы подгрупп по основным исходам. Для каждого результата в подгруппах, определенных априори, были клинические характеристики, такие как ИМТ и диабет во время беременности; вид вмешательства; респонденты, определяемые как женщины со значительным снижением прибавки в весе во время беременности после вмешательства; и качество обучения. Считалось, что истинный эффект подгруппы присутствует, когда разница в оценках между подгруппами была значимой при P <0,005. Когда какая-либо неоднородность не была объяснена анализом подгрупп, мы выполнили метаанализ с использованием модели случайных эффектов.Вес при рождении измерялся в килограммах и указывается в граммах. Графики-воронки использовались для отображения небольших эффектов исследования, когда эффекты вмешательства в небольших исследованиях отличались от эффектов, отображаемых в более крупных исследованиях. Мы использовали тест Эггера для проверки асимметрии воронкообразной кривой.18 Все анализы проводились с помощью статистического программного обеспечения Revman19 и Stata.20
Приоритизация и рейтинг доказательств
Нашими первичными результатами были изменения веса матери и ребенка в зависимости от веса. Мы отдали приоритет другим исходам для матери и плода, связанным с беременностью, и оценили их по важности с помощью двух раундов опроса врачей Delphi, обладающих опытом в этой области.15 Девятнадцать врачей (19/20, процент ответивших 95%) приняли участие в первом раунде и 16 (84%) во втором. Список исходов, оцениваемых как критически важные для контроля веса во время беременности, представлен в Приложении 1 на сайте bmj.com.
Мы суммировали силу доказательств для ключевых результатов, используя методы GRADE (классификация рекомендаций, оценка, разработка и оценка) .21 Эта система классифицирует достоверность наблюдаемой оценки на один из четырех уровней (высокий, средний, низкий, и очень низкая) оценка пяти областей (риск систематической ошибки (см. выше), (непоследовательность) результатов (неоднородность), (непрямость) доказательств, (не) точность результатов и систематическая ошибка публикации) .Первоначально мы присвоили доказательствам рандомизированных исследований высокое качество и скорректировали уровень с учетом недостатков в вышеуказанных областях. Это снизило рейтинг доказательств с высокого до умеренного до низкого или даже очень низкого, в зависимости от серьезности дефицита. В сносках в Приложении 2 на сайте bmj.com объясняется, как мы снизили оценку доказательств в свете различных недостатков.
Безопасность вмешательств при беременности
Мы провели обзор безопасности вмешательств на основе рекомендованных методов, включая методы подгруппы Кокрановских побочных эффектов.22 23 Мы разработали отдельную стратегию поиска для оценки безопасности путем включения текстовых слов и терминов индексации для выявления побочных эффектов. Мы ограничили поиск, включив поисковые фильтры для «побочных эффектов», «исследований на людях» и «типа исследования» (исключая редакционные статьи и письма). Мы проводили поиск в Medline и Embase с момента создания до марта 2011 года. Мы включили все релевантные рандомизированные исследования, обсервационные исследования, серии случаев или отчеты о случаях без каких-либо языковых ограничений. Количество нежелательных явлений, зарегистрированных у беременных женщин и детей, было получено для каждого вмешательства, чтобы вычислить процент от общего числа женщин и детей, у которых было сообщено о возникновении этого конкретного нежелательного явления или подтверждении его отсутствия.Неблагоприятные события были количественно определены как относительный риск и 95% доверительный интервал.
Результаты
Выбор исследований
Из 19 593 цитирований мы отобрали 215 полных статей для оценки (рис. 1⇓). В сорока четырех рандомизированных испытаниях (7278 женщин) сообщалось о влиянии изменения диеты и образа жизни на беременность. Вмешательства в исследованиях в целом были разделены на три группы: в основном на основе диеты (13 рандомизированных испытаний) 24 25 26 27 28 29 30 31 32 33 34 35 36 или физической активности (18 рандомизированных испытаний) 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 и смешанный подход с компонентами диеты и физической активности, которые могут или не могут быть подкреплены поведенческим консультированием (13 рандомизированных испытаний).7 56 57 58 59 60 61 62 63 64 65 66 67
Рис.1 Выявление исследований в систематическом обзоре влияния диетических вмешательств и изменений образа жизни во время беременности на исходы для матери и плода
Характеристики включенных исследований и вмешательств
Включенные испытания изучали влияние вмешательств на женщин с любым ИМТ, 7 25 26 27 28 29 30 32 37 38 39 40 42 43 44 45 46 47 48 49 50 52 54 55 56 57 58 59 60 61 62 63 64 65 66 в основном женщины с ожирением и избыточным весом 31 33 53 или только женщины с ожирением 24 29 34 35 36 51 59 67 (клинические характеристики всех выявленных исследований приведены в приложении 3 по bmj.com). Пять рандомизированных испытаний включали беременных женщин с диагнозом гестационный сахарный диабет28 31 34 57 58 и одно — женщин с ранее существовавшим диабетом.32 Типичные диетические вмешательства включали сбалансированную диету, состоящую из углеводов, белков и жиров, и ведение дневника питания. Типичные вмешательства, основанные на физической активности, включали тренировки с отягощениями легкой интенсивности, упражнения с весовой нагрузкой и ходьбу в течение 30 минут. Вмешательства при смешанном подходе включали консультации, обучение относительно потенциальной пользы диеты и физической активности, а также отзывы о прибавке в весе во время беременности.В смешанном подходе использовались техники модификации поведения, чтобы дать женщинам понимание того, как контролировать периоды эмоционального переедания и предотвращать сеансы переедания. Качество исследований было разным (рис. 2⇓). Одно исследование было доступно только в виде резюме, и данные не были включены в метаанализ. 24
Рис. 2 Качество рандомизированных контролируемых исследований, включенных в систематический обзор диетических вмешательств и изменений образа жизни во время беременности на исходы для матери и плода
Влияние вмешательства на вес матери
Тридцать четыре рандомизированных испытания (5481 женщина) оценивали влияние вмешательств на прибавку в весе матери во время беременности.7 25 26 27 28 31 32 33 34 35 36 37 38 39 42 43 45 46 47 48 50 51 52 53 54 56 59 60 61 62 63 65 66 67 По сравнению с контрольными женщинами наблюдалось снижение прибавки в весе на 1,42 кг с вмешательства (95% доверительный интервал от 0,95 до 1,89 кг; P <0,001, I 2 = 80%) (рис. 3⇓). Наибольшее снижение веса наблюдалось при диетическом вмешательстве (3,84 кг, 2,45–5,22 кг; P <0,001, I 2 = 92%) (таблица 1⇓, рис. 3⇓). Не было существенной разницы между двумя группами в их приверженности рекомендациям Института медицины (IOM) по целевому увеличению массы тела во время беременности (относительный риск 0.85, от 0,66 до 1,1).
Рис. 3 Средняя разница в прибавке в весе во время беременности (кг) при изменении диеты и образа жизни во время беременности
Таблица 1
Влияние диетических вмешательств и изменений образа жизни во время беременности на первичные исходы (прибавка в весе во время беременности и масса тела при рождении) и вторичные связанные с весом результаты оцениваются как критически важные по данным исследования Delphi (за исключением превышения рекомендаций IOM)
Влияние вмешательства на массу плода
В 31 рандомизированном исследовании (5278 новорожденных) оценивалось влияние вмешательств на массу тела при рождении.26 27 28 30 31 32 33 34 35 36 37 38 39 40 42 44 45 46 47 48 49 50 52 53 57 59 61 62 63 65 66 По сравнению с контрольной группой, было минимальное снижение массы тела при рождении, которое не было значимым (средняя разница –50 г, 95% доверительный интервал –100–0 г) для всех вмешательств (таблица 1⇑, рис 4⇓). Наблюдалась тенденция к снижению риска рождения крупных детей для гестационного возраста (определяемого как масса тела при рождении выше 90-го центиля или 4000 г) (относительный риск 0,85, 0,66–1,09) с помощью вмешательств (рис. 5⇓. Возраст младенцев (определяемый как масса тела при рождении ниже 10-го центиля или 2500 г) не изменился (1.00, от 0,78 до 1,28) с вмешательствами (рис. 5⇓).
Рис. 4 Средняя разница в массе тела при рождении (г) при изменении диеты и образа жизни во время беременности
Рис. 5 Относительный риск влияния на размер гестационного возраста при изменении диеты и образа жизни во время беременности
Влияние вмешательства на акушерство исходы для матерей
Тридцать шесть рандомизированных исследований (n = 6543 женщины) изучали влияние вмешательств на исходы акушерства для матерей.24 26 28 29 30 31 32 33 34 35 36 37 38 39 42 44 45 46 47 48 49 50 52 53 54 55 56 57 59 61 62 63 64 65 66 67 Рис. исходы беременности. Общий эффект вмешательств привел к снижению преэклампсии на 26% (относительный риск 0,74, 0,60–0,92; P = 0,006, I 2 = 31%). Сводная оценка вмешательств выявила тенденции к снижению гестационного диабета (0,78, 0,57 до 1,08), гестационной гипертензии (0,89, 0,08).От 64 до 1,25) и преждевременных родов (0,78, 0,60 до 1,02), которые не были значимыми. Мета-анализ исследований показал отсутствие различий между группами по сроку беременности на момент родов (средняя разница 0,02 недели, от -0,08 до 0,11 недели) и частоте кесарева сечения (0,93, 0,85 до 1,01), индукции родов (1,12, от 1 до 1,26) и послеродовое кровотечение (0,90, 0,57–1,42).
Рис.6 Относительный риск влияния вмешательств по контролю веса во время беременности на исходы для матери
По сравнению с контролем, диетические вмешательства во время беременности были связаны со снижением риска преэклампсии на 33% (0.67, от 0,53 до 0,85; P <0,001, I 2 = 0%) и снижение риска гестационного диабета на 61% (0,39, 0,23-0,69; P = 0,001, I 2 = 21%) (рис. 6⇑). Они также были связаны со значительным снижением гестационной гипертензии (0,30, 0,10 до 0,88; P = 0,03, I 2 = 0%) и преждевременными родами (0,68, 0,48 до 0,96; P = 0,03, I 2 = 35 %) (таблица 2⇓). Не было различий в этих результатах при вмешательствах, основанных на физической активности и смешанном подходе, по сравнению с контролем.Визуальный анализ графиков воронки не показал никаких доказательств влияния небольших исследований на результаты, связанные с весом. Были некоторые доказательства асимметрии воронки для исходов беременности, таких как гестационный диабет (P = 0,034) и кесарево сечение (P = 0,002), и ни одного доказательства для других.
Таблица 2
Влияние диетических вмешательств и изменений образа жизни во время беременности на вторичные материнские исходы (оценены как критически важные по результатам исследования Delphi, за исключением вагинальных родов и гестационного возраста при рождении). Суммарные оценки представляют собой относительные риски, если не указано иное.
Влияние вмешательств на исходы плода и новорожденного
В пятнадцати рандомизированных испытаниях (n = 3905 новорожденных) изучалось влияние вмешательств на заболеваемость и смертность плода и новорожденного.28 29 30 31 34 35 37 38 39 46 50 53 57 63 67 Мета-анализ эффекта вмешательств показал тенденции к снижению внутриутробной смертности (относительный риск 0,15, 0,02 до 1,20, I 2 = 0%), родовых травм (0,36, 0,11–1,23, I 2 = 0%) (рис. 7⇓) и гипербилирубинемия (0,84, 0,64–1,10; таблица 3⇓). Общий риск дистоции плеча снизился на 61% при всех вмешательствах по сравнению с контрольной группой (0,39, 0,22–0,70; P = 0,002, I 2 = 0%; таблица 3⇓). Различий между группами по респираторному дистресс-синдрому не было (1.05, 0,48–2,28), поступление в отделение интенсивной терапии новорожденных (1,00, 0,75–1,33) или детская гипогликемия (1,07, 0,85–1,35) (рис. 7⇓).
Рис. 7 Относительный риск влияния вмешательств по контролю веса во время беременности на исходы плода и новорожденного
Таблица 3
Влияние вмешательств в диету и образ жизни во время беременности * на вторичные исходы для плода и новорожденного (оценены как критически важные по результатам исследования Delphi, за исключением для детской гипербилирубинемии). Сводные оценки представляют собой относительные риски, если не указано иное.
Анализ подгрупп и чувствительности
В таблицах 4 и 5⇓ представлены оценки результатов анализа подгрупп клинических характеристик и качества включенных исследований исходов для матери и плода.Наблюдалась значительная разница между подгруппами по прибавке в весе во время беременности в зависимости от типа вмешательства (P <0,001). Респонденты, определяемые как женщины со значительным снижением прибавки в гестационном весе после вмешательства, показали разницу в снижении преэклампсии (P = 0,009) и веса при рождении (P = 0,002) по сравнению с не ответившими на лечение. Не было значительных различий между подгруппами по ИМТ, диабетическому статусу во время беременности и риску систематической ошибки для сокрытия распределения.
Таблица 4
Анализ подгрупп методов исследования и клинических характеристик исходов для матери при оценке диетических вмешательств и изменений образа жизни во время беременности
Таблица 5
Анализ подгрупп методов исследований и клинических характеристик исходов для плода при оценке диетических вмешательств и изменений образа жизни во время беременности
Когда мы исключили исследования женщин с диабетом во время беременности28 31 32 34 57 58, анализ чувствительности последовательно показал общее снижение прибавки в весе во время беременности с помощью вмешательств (средняя разница -1.4 кг, 95% доверительный интервал от −2,09 до −0,71 кг, P <0,001), включая диету (−5,53 кг, от −8,54 до −2,53 кг; P <0,001), физическую активность (от −0,72 кг, от −1,2 до −0,25 кг, P = 0,003) и смешанный подход (-1,06 кг, -1,67 до -0,46 кг; P <0,001). Не было значительного снижения веса при рождении с помощью вмешательства (-40 г, -100 до 10 г) 26 27 30 33 35 36 37 38 39 40 42 44 45 46 47 48 49 50 52 53 59 61 62 63 65 66 после исключения женщин с диабетом различий между группами в частоте рождения детей, которые были маленькими или большими для гестационного возраста, или детей с дистоцией плечевого пояса, не было.Диетические вмешательства у женщин без диабета привели к значительному снижению преждевременных родов (относительный риск 0,26, 0,09–0,74) и гестационной гипертензии (0,30, 0,10–0,88). Наблюдалась незначительная тенденция к снижению преэклампсии (0,82, 0,43 до 1,42) у этих женщин с диетой.
Вмешательства у беременных женщин с ожирением и избыточной массой тела показали снижение прибавки в весе во время беременности (средняя разница от −2,1 кг, от −3,46 до −0,75 кг; P <0,002, I 2 = 88%).Не было значительного снижения веса плода или других клинических исходов. Диетическое вмешательство у женщин с ожирением и избыточным весом значительно снизило риск преэклампсии (относительный риск 0,63, 0,42–0,96), гестационного диабета (0,39, 0,23–0,69) и гестационной гипертензии (0,30, 0,10–0,88). Это преимущество не наблюдалось для других исходов или с другими вмешательствами. После того, как мы исключили женщин с диабетом, положительный эффект, наблюдаемый с помощью диеты, сохранился в отношении прибавки в весе во время беременности (средняя разница -7.73 кг, от −6,05 до −9,40 кг; P <0,001, I 2 = 41%) и гестационная гипертензия (относительный риск 0,30, от 0,10 до 0,88). Не наблюдалось увеличения риска рождения маленьких для гестационного возраста детей, и не было никакого влияния на какие-либо другие исходы для матери или плода.
Оценка доказательств
Опрос практикующих врачей, проведенный Delphi, определил важность исходов для матери и плода.15 Общая оценка доказательств была умеренной для снижения прибавки в весе во время беременности (см. Приложение 2 о bmj.com). Оценка была умеренной, что свидетельствовало об отсутствии эффекта вмешательств на риск рождения детей, не достигших гестационного возраста. Оценка клинических исходов, таких как преэклампсия, гестационный диабет, преждевременные роды, гестационная гипертензия, госпитализация в неонатальное отделение и неонатальная гипогликемия, была низкой или очень низкой. Оценка доказательности положительного эффекта диеты была высокой для гестационной гипертензии, умеренной — для гестационного диабета, низкой — для преэклампсии и очень низкой — для преждевременных родов.Хотя клиницисты оценили тромбоэмболию, госпитализацию матери в отделение интенсивной терапии или интенсивной терапии, а также долгосрочные неврологические последствия для плода как критически важные исходы, мы не выявили доказательств для этих исходов.15
Безопасность вмешательств
Мы включили 26 исследований после просмотра 14 832 ссылок для оценки безопасности вмешательств во время беременности. Из включенных исследований два были рандомизированными контролируемыми (277 женщин) 40, 64 и 24 были наблюдательными (19 когортных исследований и пять исследований случай-контроль, 468 581 женщина).68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 В исследованиях оценивалось влияние диеты, физической активности и других изменений образа жизни во время беременности на исходы для матери и плода.
Два включенных рандомизированных исследования оценивали физическую активность и не показали увеличения окрашивания меконием околоплодных вод (относительный риск 0,62, 0,20 до 1,90), атонии матки (0,93, 0,22 до 3,89) или хориоамнионита (3,69, 0,15 до 88,13). ). Восемнадцать исследований наблюдали влияние диеты на исходы для матери и плода.Большинство включенных исследований оценивали эффект резкого снижения потребления энергии в экстремальных условиях, таких как война или голод. Отмечалось увеличение частоты дефектов нервной трубки, расщелины губы и неба у детей, рожденных женщинами с экстремальными формами диеты и на диетах с высоким гликемическим индексом во время беременности (см. Приложение 4 на bmj.com) 89. Риск коронарного заболевания. Заболевания артерий, метаболический синдром, рак груди и диабет увеличивались у младенцев, рожденных от матерей, диета которых была строго ограничена из-за голода.72 При физической активности во время беременности не наблюдалось серьезных побочных эффектов для матери или плода, таких как аномалии пуповины, угроза выкидыша, жидкость, окрашенная меконием, патология сердечного ритма плода, сепсис матери или хориоамнионит.
Обсуждение
Резюме результатов
Вмешательства в диету и образ жизни во время беременности эффективны в снижении гестационной прибавки в весе без какого-либо неблагоприятного воздействия на риск рождения детей с малым для гестационного возраста возрастом.По сравнению с физической активностью и смешанным подходом, диетические вмешательства были связаны с наибольшим снижением прибавки в весе во время беременности. Вмешательства также привели к значительному снижению риска преэклампсии. Наблюдалась общая тенденция к снижению гестационного диабета, гестационной гипертензии, преждевременных родов и внутриутробной смерти при вмешательстве по сравнению с контролем. В частности, диета значительно снизила риск преэклампсии, гестационного диабета, гестационной гипертензии и преждевременных родов по сравнению с любым другим вмешательством.Вмешательства оказали меньшее влияние на исходы, связанные с массой плода, другими заболеваниями и смертностью. Более того, не было доказательств того, что вмешательства снижали частоту кесарева сечения или индукции родов. Оценка качества доказательств была умеренной (см. Приложение 2 на сайте bmj.com) из-за отсутствия эффекта, наблюдаемого при вмешательствах в отношении размера для гестационного возраста. Качество доказательств преимущества, наблюдаемого при вмешательстве по увеличению массы тела во время беременности, было умеренным, но низким для клинических исходов.
Сильные стороны и ограничения
Наш систематический обзор был всеобъемлющим по своему охвату и поиску. Мы провели обзор в соответствии с современными рекомендациями и выполнили заявление PRISMA (предпочтительные элементы отчетности для систематических обзоров и метаанализов ).92 Наш поиск литературы был направлен на минимизацию риска выбора и систематической ошибки публикации. Большинство опубликованных обзоров о влиянии диетических вмешательств и изменений образа жизни на исходы для матери и плода были ограничены конкретными группами женщин или типами вмешательств.Не было формального определения приоритетов важности клинических исходов, и лишь немногие оценивали качество доказательств по важным исходам. Мы провели тщательную оценку качества и официально установили приоритет клинической значимости результатов. С помощью исследования Delphi были получены достоверные данные о клинически важных исходах, связанных с весом и беременностью. При необходимости мы исследовали источники неоднородности.
Соответствующие анализы подгрупп и анализы чувствительности, запланированные априори, были предприняты для важных факторов, таких как ИМТ, диабетический статус, изменение веса матери в результате вмешательства и качество исследования, которые могли повлиять на результаты.Мы официально оценили силу доказательств для ключевых результатов, выявленных в ходе исследования Delphi. Это дало нам уверенность в оценках наблюдаемых важных эффектов. Наше тщательное изучение и представление профилей доказательств обеспечивает столь необходимую ясность, необходимую для вынесения суждений о последствиях.
Достоверность метаанализа зависит от качества исследований компонентов, наблюдаемой неоднородности и риска систематической ошибки публикации. Качество различных исходов, оцененных по шкале GRADE, было умеренным в отношении пользы, наблюдаемой при гестационной прибавке в весе, но низким для других важных акушерских исходов, таких как преэклампсия, гестационный диабет, гестационная гипертензия и преждевременные роды.Это ослабляет выводы об этих результатах. Причины низкого рейтинга доказательств заключались в значительной неоднородности, наблюдаемой в величине эффекта, недостатках качества отдельных исследований, а также в риске публикации и связанных с ними систематических ошибках.
Мы наблюдали неоднородность положительного воздействия вмешательств на прибавку в весе матери, которая сохранялась после учета типа вмешательства, ИМТ и диабетического статуса. Необходима дополнительная информация о характеристиках включенных женщин, таких как возраст, этническая принадлежность, социально-экономический статус, равенство и основные медицинские состояния, а также о характеристиках вмешательств, таких как частота, продолжительность и интенсивность, которые могут повлиять на результаты.Мы были ограничены в наших возможностях определить оптимальное изменение веса во время беременности с помощью вмешательств, которые минимизировали бы осложнения для матери и плода. Кроме того, ограничения в доступных данных ограничили оценку исходных прогностических факторов эффективности результатов. На такие вопросы было трудно ответить с извлеченными результатами из публикаций испытаний, потому что информация на уровне пациентов была недоступна, а эффекты подгруппы («лечебно-ковариантные взаимодействия») редко сообщались достаточно подробно.Хотя группа клиницистов Delphi выявила долгосрочные неврологические последствия и метаболический синдром плодов, подвергшихся вмешательству, о них не сообщалось ни в одном из исследований.
Безопасность вмешательств
Благоприятные эффекты, наблюдаемые в нашем обзоре, требуют уравновешивания потенциальных побочных эффектов при оценке клинических последствий. Доказательства каких-либо побочных эффектов от диеты во время беременности обычно были получены из наблюдательных исследований крайних диет для снижения веса или приема пищи с очень высоким или низким гликемическим индексом.89 Эти результаты не применимы к рассмотренным нами вмешательствам. Мы также заметили, что снижение прибавки в весе во время беременности не было связано с увеличением числа детей, которые были маленькими для гестационного возраста. Наблюдательные исследования физической активности во время беременности не показали каких-либо значительных неблагоприятных исходов для матери или плода при занятиях различной интенсивностью.
Клинические и практические последствия
Наши результаты показывают, что вмешательства, основанные на диете во время беременности, снизят прибавку в весе во время беременности в среднем на 4 кг по сравнению с 0.7 кг и 1,0 кг при физической нагрузке и смешанном подходе соответственно. Диетические вмешательства были наиболее эффективны в снижении таких осложнений, как преэклампсия, гестационный диабет, гестационная гипертензия и преждевременные роды. Одной из основных проблем матерей является влияние изменений в питании и образе жизни на вес плода. Нет никаких доказательств того, что вмешательства, оцененные в нашем обзоре или рекомендованные в текущей клинической практике, связаны с неблагоприятными исходами для матери или плода.
Диеты, эффективные для снижения прибавки в весе во время беременности, включали сбалансированную диету 18-24 кДж / кг, диету с низким гликемическим индексом с необработанными цельнозерновыми, фруктами, бобами и овощами, а также здоровую диету с максимальным содержанием 30%. жира, 15-20% белка и 50-55% углеводов, с индивидуальным потреблением энергии в соответствии с потребностями матери. Предоставление регулярного вклада в планирование рациона питания на ранних сроках беременности через специальные бригады диетологов первичного и вторичного звена может улучшить результаты.Больше всего от этого выигрывают женщины с избыточным весом и ожирением, которые могут быть целевыми в клинической практике.
Текущее исследование в основном сосредоточено на смешанных вмешательствах с компонентами диеты и физической активности. Но вмешательства, основанные преимущественно на диете, оказались более эффективными в отношении связанных с весом и клинических исходов. Из-за отсутствия индивидуальных данных о важных факторах, таких как возраст, этническая принадлежность, социально-экономический статус, комплаентность и другие факторы риска, мы ограничены в нашем объяснении пользы, наблюдаемой при диете по сравнению с другими методами.Это могло быть связано с разными причинами. Во-первых, при комплексном вмешательстве полученная чистая выгода может быть связана с энергией, с которой выполняются компоненты вмешательства. В «смешанных подходах» отдельные компоненты могут не соответствовать тем же стандартам, что и в исследованиях, посвященных только диете. Во-вторых, соблюдение режима лечения могло быть лучше в исследованиях с вмешательством только в диете, чем с другими методами, из-за их относительной простоты и предполагаемой безопасности по сравнению с физической активностью во время беременности.93 94 В-третьих, определенные компоненты диеты, такие как клетчатка, могут иметь преимущества, которые не проявляются при других вмешательствах. Повышенные концентрации триглицеридов во время беременности связаны с риском преэклампсии.95 Известно снижение заболеваемости преэклампсией до 70%, связанное с падением концентрации триглицеридов у женщин с самым высоким уровнем рациона питания. потребление клетчатки по сравнению с самой низкой четвертью после поправки на факторы, влияющие на факторы.96 Высокое содержание клетчатки в диетическом вмешательстве во включенных исследованиях могло повлиять на положительный эффект, наблюдаемый при снижении частоты преэклампсии.
Экономическая оценка нефармакологических вмешательств для контроля веса вне беременности, проведенная Национальным институтом здравоохранения и клинического совершенства, показала, что диетические вмешательства были дешевле, чем вмешательства, основанные на физической активности.97 диетических вмешательств во время беременности, эта стратегия также может быть рентабельной по сравнению с другими методами.
Рекомендации для будущих исследований
Синтез данных на уровне пациентов с помощью метаанализа индивидуальных данных пациента необходим для оценки любого дифференциального эффекта преимуществ, наблюдаемых при вмешательствах в различных группах, на основе ИМТ, возраста, этнической принадлежности, социально-экономического статуса, паритета и статус риска при беременности.Доступность исходных данных существенно повысит возможности выявления исходных факторов, которые действительно изменяют эффект вмешательства98, и позволит количественно оценить эффекты вмешательства для клинически значимых групп.99 Кроме того, метаанализ индивидуальных данных пациента сможет оценить, насколько Улучшение клинических исходов связано только с уменьшением прибавки в весе во время беременности или если есть какие-либо дополнительные преимущества от типа вмешательства, приводящего к изменению веса. Это также позволит количественно оценить пользу от изменения веса во время беременности как для матери, так и для ребенка.Это позволит нам применять те меры по контролю веса, которые демонстрируют явную пользу с конкретными целевыми показателями набора веса во время беременности. Этот подход также обеспечит адекватные возможности для получения достоверных, надежных ответов и заполнения модели для аналитического моделирования решений для экономической оценки здравоохранения.
Нехватка описательной информации об интенсивности и продолжительности вмешательства, способах оказания помощи и соблюдении пациентом требований является факторами, которые потенциально могут способствовать или препятствовать реализации.Эти пробелы определяют проблемы для дальнейшего исследования. Существует потребность в крупных проспективных исследованиях хорошего качества для выявления важных клинических исходов, включая долгосрочное воздействие на мать и плод.
Заключение
До сих пор рекомендации по контролю веса во время беременности в основном касались женщин с ожирением и избыточным весом без акцента на конкретном типе вмешательства. Диетическое вмешательство является эффективным, безопасным и потенциально рентабельным и преобладает над вмешательством, основанным на физической активности.Доводы в пользу его введения с оценкой услуг подкреплены нашим обзором. Текущие испытания эффективности должны быть сосредоточены на клинически значимых результатах, зафиксированных в нашем исследовании Delphi. Они должны собирать данные для определения наиболее эффективных средств улучшения результатов с помощью стратегий управления весом во время беременности.
Что уже известно по этой теме
Чрезмерная прибавка в весе во время беременности связана с неблагоприятными исходами для матери и плода
Вмешательства по контролю веса во время беременности могут снизить неблагоприятные исходы для матери и ребенка
Вмешательства, основанные на диете или физической активности, или и том и другом, во время беременности могут повлиять на вес матери и плода и акушерские исходы
Что добавляет это исследование
Вмешательства в диету и образ жизни во время беременности могут снизить прибавку в весе матери во время беременности
Нет значительного общего влияния на исходы, связанные с массой плода
Диетические вмешательства являются наиболее эффективными в снижении прибавки в весе во время беременности у матери по сравнению с другими методами
Малярия продолжает угрожать беременным женщинам и детям — Справочная информация о населении Бюро 900 01
(декабрь 2001 г.) Малярия ежегодно угрожает по меньшей мере 24 миллионам беременностей в Африке, континенте, наиболее пораженном этой болезнью по данным Всемирной организации здравоохранения (ВОЗ).Малярия вызывает анемию и может привести к выкидышу и рождению недоношенных детей с низкой массой тела.
По данным Всемирного банка, более 1 миллиона человек ежегодно умирают от малярии, в основном дети младшего возраста. Защита групп населения, подверженных риску заболевания малярией, находится в центре глобальных усилий по «борьбе с малярией». В то время как использование эффективных лекарств и защитных сеток для кроватей сокращает число жертв малярии в нескольких африканских странах, необходимы постоянные и расширенные усилия для защиты здоровья беременных женщин и детей.
Беременные в группе риска
Большинство из 300–500 миллионов случаев малярии ежегодно происходит в странах Африки к югу от Сахары. Хотя у большинства людей, живущих в районах, где широко распространена малярия, вырабатывается иммунитет к этой болезни, риск инфицирования беременной женщины увеличивается из-за изменений в ее уровне гормонов и иммунной системы. Особенно уязвимы матери, которые впервые рожают. Беременные женщины, страдающие малярией, подвергаются повышенному риску анемии и выкидыша, а их дети подвергаются риску мертворождения, недоношенности, задержки внутриутробного развития и низкой массы тела при рождении.
По данным Сети по малярии и беременности (группа, созданная для обмена информацией о малярии и беременности среди тех, кто занимается исследованиями малярии и борьбой с ней, а также в сфере охраны материнского и репродуктивного здоровья), малярия вызывает до 15 процентов материнских анемий и около 35 процентов предотвратимая низкая масса тела при рождении. Низкая масса тела при рождении — основная причина неонатальной смертности. По оценкам исследователей из Центров США по контролю и профилактике заболеваний, во всем мире от 75000 до 200000 младенческих смертей ежегодно связаны с инфекцией малярии во время беременности.
Малярия также способствует материнской смертности. Беременные женщины более подвержены осложнениям от малярии. Осложнения могут включать церебральную малярию, почечную недостаточность и гемолиз (разрушение эритроцитов). Этот повышенный риск сохраняется и в ранний послеродовой период. Беременные женщины с ВИЧ подвергаются еще большему риску плацентарной малярии (размножение малярийных паразитов в плаценте, которое блокирует обмен кислорода и питательных веществ с плодом), имеют более тяжелые малярийные инфекции и не развивают такую же устойчивость к малярии, как женщины без ВИЧ. .
Помощь беременным женщинам: временное презумптивное лечение и прикроватные сетки
Особые усилия прилагаются для профилактики и лечения малярии у беременных женщин. Осуществляются программы по обеспечению того, чтобы все женщины и дети спали под обработанными инсектицидами противомоскитными сетками. Многие страны снижают налоги и тарифы на товары, связанные с профилактикой (например, сетки, лекарства и инсектициды), чтобы сделать их более доступными.
Обзор 15 исследований противомалярийных вмешательств у беременных женщин за 2000 год, проведенный исследователями Полом Гарнером и А.Метин Гульмезоглу обнаружил, что предоставление эффективных лекарств во время беременности снижает заболеваемость матери и снижает частоту младенцев с низкой массой тела при рождении и анемии, особенно у женщин, родивших одного или двух детей. Прерывистое лечение предполагаемой малярии (ПЛИ) для беременных женщин оказалось эффективным и экономичным способом улучшения здоровья матери и ребенка, особенно для впервые родившихся матерей, живущих в эндемичных районах Африки. Исследования специалистов по малярии из двух британских школ тропической медицины показывают, что IPT с противомалярийным препаратом сульфадоксин-пириметамин (SP, также известный как Fansidar) во время беременности может снизить тяжелую анемию у матерей и частоту младенцев с низкой массой тела при рождении в регионах с устойчивостью к хлорохину. .В Малави IPT с SP является стандартной политикой профилактики малярии у беременных женщин с 1993 года. Одно исследование показало, что введение беременным женщинам двух или более доз SP снижает распространенность младенцев с низкой массой тела при рождении более чем наполовину (10,3 процента). против 23 процентов). По оценкам Сети по малярии и беременности, можно получить здоровый год жизни за 12 долларов США за две дозы СП для беременных женщин в районах, где отсутствует резистентность к СП.
В настоящее время ВОЗ рекомендует женщинам в районах, где широко распространена малярия, получать ПТИ с эффективным, предпочтительно однократным, противомалярийным препаратом в рамках рутинной дородовой помощи во время их первой и второй беременностей.Хотя SP часто является препаратом выбора для периодического лечения в регионах, устойчивых к хлорохину, он менее эффективен для женщин, инфицированных ВИЧ, и для тех, кто не вернулся для приема второй дозы. Устойчивость к SP наблюдается в некоторых районах Восточной Африки, поэтому потребность в новых эффективных лекарствах сохраняется.
Другие тропические болезни и беременность
Помимо малярии, другие тропические болезни могут влиять на репродуктивное здоровье, снижая фертильность, затрудняя использование противозачаточных средств или нанося вред беременной матери или ее плоду.Наиболее распространенными из этих заболеваний являются шистосомоз, кишечные гельминты и филяриатоз. Шистосомоз и кишечные гельминты, которыми заражено от 200 до 250 миллионов человек во всем мире, вызываются паразитическими червями, передаваемыми через зараженную воду и пищу. Филяриоз, которым страдают около 120 миллионов человек во всем мире, возникает в результате длинных нитевидных червей, передаваемых комарами, клещами или мухами. Последствия этих заболеваний во время беременности зависят от тяжести инфекции и стадии беременности.Все эти распространенные тропические болезни могут вызывать анемию или недоедание, что может иметь серьезные последствия для беременной женщины и ее плода.
Международные усилия по сокращению заболеваемости малярией среди беременных женщин и детей
Партнерство по сокращению заболеваемости малярией, инициированное в 1998 году ВОЗ, Программой развития Организации Объединенных Наций (ПРООН), Детским фондом Организации Объединенных Наций (ЮНИСЕФ) и Всемирным банком, направлено на сокращение вдвое глобальной заболеваемости малярией. Его цели включают лечение малярии у беременных женщин, обработанные инсектицидами противомоскитные сетки, борьбу с переносчиками болезней, раннюю диагностику, быстрое лечение, а также профилактику эпидемий и реагирование на них.
В Абуджийской декларации, подписанной африканскими лидерами в 1998 году, содержится призыв к правительствам принять конкретные меры по профилактике и лечению малярии среди беременных женщин и детей в возрасте до 5 лет. К 2005 году Декларация призывает охватить не менее 60 процентов групп риска, особенно беременных. женщинам и детям до 5 лет — обработанные противомоскитные сетки или другие профилактические меры. Кроме того, по крайней мере 60 процентов всех беременных женщин, подверженных риску малярии, должны иметь доступ к противомалярийным препаратам и профилактическому периодическому лечению, и по крайней мере 60 процентов жертв малярии должны иметь доступ к эффективному лечению в течение 24 часов после появления симптомов.
Вызовы для политиков
Необходимы постоянные усилия для уменьшения ущерба, наносимого малярией здоровью матери и ребенка. Конкретные действия, которые могут предпринять лица, определяющие политику, и руководители программ, включают:
- Разработать и внедрить новые национальные протоколы, основанные на фактических данных, по применению противомалярийных препаратов во время беременности.
- Разработайте меры вмешательства, которые будут безопасными, эффективными, приемлемыми и доступными.
- Интегрировать новые программы с существующими службами здравоохранения, включая дородовое наблюдение и другие программы репродуктивного здоровья.
- Обучайте и общайтесь с целью более широкого использования обработанных инсектицидами противомоскитных сеток.
- Сделайте надкроватные сетки и их повторную обработку доступными.
- Оценить эффективность периодического лечения как части повседневной дородовой помощи в регионах с высокой, средней и низкой степенью передачи малярии.
- Сделать лечение малярии подходящим и доступным на местном уровне путем обучения сельских медицинских работников, матерей и поставщиков лекарств.
Барбара Шейн — независимый консультант в области общественного здравоохранения.Она разработала и руководила программами репродуктивного здоровья за рубежом; письменные и подготовленные учебные материалы; и работал в клиниках репродуктивного здоровья.
Список литературы
Боаз Отиено-Ньюня, «Тропические болезни могут нанести вред беременности», Сеть 19 (2).
Пол Гарнер и А. Метин Гулмезоглу, «Профилактика и лечение малярии у беременных женщин» (Кокрановский обзор) в Кокрановская библиотека , выпуск 4 (Оксфорд: Обновление программного обеспечения, 2000).
Сеть по малярии и беременности, «Жизнь в опасности: малярия и беременность» (Вашингтон, округ Колумбия: Проект поддержки анализа и исследований в Африке (SARA), ноябрь 2000 г.).
S.J. Роджерсон и др., «Прерывистый сульфадоксин-пириметамин при беременности: эффективность против заболеваемости малярией в Блантайре, Малави, в 1997-99», Стенограмма Королевского общества тропической медицины и гигиены 94 (5): 549-553.
C.E. Shulman et al., «Малярия во время беременности: ее значение для программ безопасного материнства», Annals of Tropical Medicine and Parasitology 93 (Suppl.1): С59-66.
R.W. Steketee et al., «Бремя малярии при беременности в районах, эндемичных по малярии», Американский журнал тропической медицины и гигиены 63 (Дополнение 1-2): 28-35.
FH Verhoeff et al., «Оценка эффектов прерывистого лечения сульфадоксином-пириметамином во время беременности на устранение паразитов и риск низкой массы тела при рождении в сельских районах Малави», Annals of Tropical Medicine and Parasitology 92 (2): 141-150 .
Комитет экспертов ВОЗ по малярии, Серия технических отчетов Всемирной организации здравоохранения 892 (2000): i-v, 1-74.
Для получения дополнительной информации
Обратить малярию вспять: www.rbm.who.int
ВОЗ: www.who.int/inf-fs/en/fact094.html
Международный фонд борьбы с малярией: www.malaria.org
ЮНИСЕФ: www.unicef.org/programme/health/focus/community/malaria/overview.htm
Малярия и инфекционные заболевания в Африке: www.chez.com/malaria
ПУТЬ: www.path.org и http://malariavaccines.org
Проект
NetMark: www.netmarkafrica.org
Употребление опиоидов и расстройства, связанные с употреблением опиоидов во время беременности
Номер 711 (заменяет заключение Комитета № 524, май 2012 г.)
Комитет по акушерской практике
Американское общество наркологической медицины
Общество медицины матери и плода одобряет этот документ. Это заключение комитета было разработано Комитетом акушерской практики Американского колледжа акушеров и гинекологов в сотрудничестве с членами комитета Марией А.Маскола, доктор медицины, магистр здравоохранения; Энн Э. Бордерс, доктор медицины, магистр наук, магистр здравоохранения; и член Американского общества наркологической медицины Мишка Терплан, доктор медицины, магистр здравоохранения.
РЕЗЮМЕ. В последние годы резко возросло употребление опиоидов во время беременности, что соответствует эпидемии, наблюдаемой среди населения в целом. В борьбе с опиоидной эпидемией все поставщики медицинских услуг должны играть активную роль. Беременность дает важную возможность выявлять и лечить женщин с расстройствами, связанными с употреблением психоактивных веществ.Расстройства, связанные с употреблением психоактивных веществ, затрагивают женщин всех расовых и этнических групп и всех социально-экономических групп, а также затрагивают женщин в сельских, городских и пригородных районах. Поэтому важно, чтобы скрининг был универсальным. Скрининг на употребление психоактивных веществ должен быть частью комплексной акушерской помощи и проводиться при первом дородовом посещении совместно с беременной женщиной. Пациенты, употребляющие опиоиды во время беременности, представляют собой разнообразную группу, и важно распознавать и различать употребление опиоидов в контексте медицинской помощи, злоупотребление опиоидами и нелеченное расстройство, связанное с употреблением опиоидов.Многопрофильное долгосрочное наблюдение должно включать медицинскую, психологическую и социальную поддержку. Младенцы, рожденные женщинами, употреблявшими опиоиды во время беременности, должны находиться под наблюдением педиатра на предмет неонатального абстинентного синдрома. Ранний всеобщий скрининг, кратковременное вмешательство (например, привлечение пациента к короткой беседе, предоставление отзывов и рекомендаций) и направление на лечение беременных женщин с употреблением опиоидов и расстройством, связанным с употреблением опиоидов, улучшают исходы для матери и ребенка. В целом, скоординированный междисциплинарный подход без уголовных санкций имеет наилучшие шансы помочь младенцам и их семьям.
Рекомендации и выводы
Американский колледж акушеров и гинекологов (ACOG) делает следующие рекомендации и выводы:
Ранний всеобщий скрининг, краткое вмешательство (например, вовлечение пациента в короткий разговор, предоставление отзывов и советов) , а также направление на лечение беременных женщин с употреблением опиоидов и расстройствами, связанными с употреблением опиоидов, улучшают исходы для матери и ребенка.
Скрининг на употребление психоактивных веществ должен быть частью комплексной акушерской помощи и проводиться при первом дородовом посещении совместно с беременной женщиной.Скрининг, основанный только на таких факторах, как плохая приверженность к дородовой помощи или предшествующий неблагоприятный исход беременности, может привести к пропущенным случаям и может усилить стереотипы и стигму. Поэтому важно, чтобы скрининг был универсальным.
Регулярный скрининг должен опираться на проверенные инструменты скрининга, такие как анкеты, включая 4P, NIDA Quick Screen и CRAFFT (для женщин 26 лет и младше).
При хронической боли практические цели включают стратегии, позволяющие избегать или минимизировать использование опиоидов для лечения боли, выделяя альтернативные методы лечения боли, такие как нефармакологические (например, упражнения, физиотерапия, поведенческие подходы) и неопиоидные фармакологические методы лечения.
Для беременных женщин с расстройствами, связанными с употреблением опиоидов, фармакотерапия опиоидными агонистами является рекомендуемой терапией и предпочтительнее отмены под медицинским наблюдением, поскольку синдром отмены связан с высокой частотой рецидивов, что приводит к худшим исходам. Необходимы дополнительные исследования для оценки безопасности (особенно в отношении рецидива у матери), эффективности и долгосрочных результатов отмены под медицинским наблюдением.
Младенцы, рожденные женщинами, которые употребляли опиоиды во время беременности, должны находиться под наблюдением педиатра на предмет неонатального абстинентного синдрома, синдрома отмены лекарств, который новорожденные, подвергшиеся воздействию опиоидов, могут испытывать вскоре после рождения.
Учитывая уникальные потребности беременных женщин с расстройствами, связанными с употреблением опиоидов, поставщикам медицинских услуг необходимо будет рассмотреть возможность изменения некоторых элементов дородового ухода (таких как расширенное тестирование на инфекции, передаваемые половым путем [ИППП], дополнительные ультразвуковые исследования для оценки веса плода существуют опасения по поводу аномалий роста плода и консультации с различными поставщиками медицинских услуг) для удовлетворения клинических потребностей конкретной ситуации пациента.
Перед назначением опиоидов своим пациентам акушеры-гинекологи и другие поставщики медицинских услуг должны убедиться, что опиоиды указаны надлежащим образом; обсудить риски и преимущества употребления опиоидов и пересмотреть цели лечения; и составьте подробный анамнез употребления психоактивных веществ и просмотрите Программу мониторинга рецептурных препаратов, чтобы определить, получали ли пациенты ранее рецепты на опиоиды.
Следует поощрять грудное вскармливание у женщин, которые стабильны на своих опиоидных агонистах, не употребляют запрещенные препараты и не имеют других противопоказаний, таких как инфекция вируса иммунодефицита человека (ВИЧ). Женщин следует проинформировать о необходимости приостановить грудное вскармливание в случае рецидива.
Должен быть обеспечен доступ к адекватным службам послеродовой психосоциальной поддержки, включая программы лечения наркозависимости и профилактики рецидивов.
Консультации по вопросам контрацепции и доступ к услугам по контрацепции должны быть рутинной частью лечения расстройств, связанных с употреблением психоактивных веществ, среди женщин репродуктивного возраста, чтобы минимизировать риск незапланированной беременности.
Предпосылки
Употребление опиоидов во время беременности резко возросло в последние годы, параллельно с эпидемией, наблюдаемой среди населения в целом. В 2012 году медицинские работники США выписали более 259 миллионов рецептов на опиоиды, что в два раза больше, чем в 1998 году 1.Показатели допуска к программам лечения наркозависимости из-за злоупотребления рецептурными опиоидами выросли более чем в четыре раза в период с 2002 по 2012 год 2 3, а уровень смертности, связанной с опиоидными анальгетиками, вырос почти на 400% в период с 2000 по 2014 год 4. Наряду с увеличением злоупотребления рецептурными препаратами опиоидов, резко возросло потребление героина. Смертность от передозировки героином увеличилась более чем на 300% менее чем за 5 лет, с чуть более 3000 в 2010 г. до более 10 500 в 2014 г. 5.
В 2007 г. 22.8% женщин, участвовавших в программах Medicaid в 46 штатах, получали рецепт на опиоиды во время беременности 6. В исследовании, посвященном диагностическим кодам при выписке из больницы, с 2000 по 2009 год потребление опиоидов матерями в дородовой период увеличилось почти в пять раз. 7. Растущая распространенность употребления опиоидов. во время беременности привело к резкому увеличению неонатального абстинентного синдрома с 1,5 случаев на 1000 родов в больнице в 1999 году до 6,0 на 1000 родов в 2013 году, с соответствующими ежегодными больничными расходами на 1,5 миллиарда долларов.В штатах с самым высоким уровнем назначения опиоидов также наблюдается самый высокий уровень неонатального абстинентного синдрома 8. Кроме того, обзоры материнской смертности в нескольких штатах выявили употребление психоактивных веществ в качестве основного фактора риска смертей, связанных с беременностью 9 10.
Определение опиоидов Расстройство, связанное с употреблением опиоидов
Расстройство, связанное с употреблением опиоидов, — это модель употребления опиоидов, характеризующаяся толерантностью, желанием, неспособностью контролировать употребление и продолжением использования, несмотря на неблагоприятные последствия. Расстройство, связанное с употреблением опиоидов, является хроническим заболеванием, которое поддается лечению, с которым можно успешно справиться путем сочетания лекарств с поведенческой терапией и поддержкой восстановления 5, что позволяет людям с расстройством, связанным с употреблением опиоидов, восстановить контроль над своим здоровьем и своей жизнью.Краткосрочные программы лечения, направленные на воздержание, связаны с высокой частотой рецидивов 11 и, как правило, не способствуют стабильному долгосрочному выздоровлению пациентов 5. Это подчеркивает важность наличия и доступа к постоянному уходу в программах лечения опиоидами.
Диагноз ставится на основании определенных критериев, таких как безуспешные попытки сократить или контролировать потребление, а также употребление, приводящее к социальным проблемам и невыполнению обязательств на работе, в школе или дома 12. Диагностическое и статистическое руководство Психические расстройства , пятое издание (DSM-5), заменили термины злоупотребление опиоидами и опиоидная зависимость термином расстройство, связанное с употреблением опиоидов.В DSM-5 выделяются 11 основных симптомов расстройства, связанного с употреблением опиоидов, и определяется тяжесть расстройства на основе количества повторяющихся симптомов в течение 12-месячного периода. Степень тяжести классифицируется как легкая (два-три симптома), средняя (четыре-пять симптомов) и тяжелая (шесть или более симптомов). 13. Терминология злоупотребления и зависимости не соответствует точно новым категориям легкой, средней и тяжелой степени. расстройство, связанное с употреблением опиоидов. Хотя эта диагностическая терминология изменилась, большая часть предыдущих исследований, рекомендаций и нормативных требований в этой области основывается на предыдущей терминологии, такой как злоупотребление и зависимость; поэтому эти термины все еще используются при ссылке на эти источники.
Роль акушера-гинеколога и других поставщиков акушерской помощи
Пациенты, употребляющие опиоиды во время беременности, представляют собой разнородную группу, и важно распознавать и различать употребление опиоидов в контексте медицинской помощи (при хронической боли или при зависимости ), злоупотребление опиоидами и нелеченное расстройство, связанное с употреблением опиоидов. В борьбе с опиоидной эпидемией все поставщики медицинских услуг должны играть активную роль. Правильное назначение опиоидных препаратов жизненно важно.Перед назначением опиоидов своим пациентам акушеры-гинекологи и другие поставщики медицинских услуг должны сделать следующее:
Убедитесь, что опиоиды указаны надлежащим образом. Для женщин, в том числе беременных, с расстройством, вызванным употреблением опиоидов, рекомендуется фармакотерапия опиоидными агонистами. В отношении хронической боли практические цели включают стратегии, позволяющие избегать или минимизировать использование опиоидов для лечения боли, выделяя альтернативные методы лечения боли, такие как нефармакологические (например, упражнения, физиотерапия, поведенческие подходы) и неопиоидные фармакологические методы лечения.
Обсудите риски и преимущества употребления опиоидов и обсудите цели лечения с пациентом с самого начала. Это обсуждение должно включать риск возникновения физиологической зависимости от опиоидов и, в случае беременных женщин, возможность развития у ребенка неонатального абстинентного синдрома (НАС) secRef. Тем не менее, медицинские работники должны без колебаний назначать опиоиды только из-за опасений по поводу неонатального абстинентного синдрома.
Подробно изучите историю употребления психоактивных веществ и ознакомьтесь с Программой мониторинга рецептурных лекарств, которая в настоящее время действует в 49 штатах и округе Колумбия.Программа мониторинга лекарств, отпускаемых по рецепту, является ценным ресурсом для определения того, получали ли пациенты ранее рецепты на опиоиды или другие лекарства высокого риска, такие как бензодиазепины, и с ней следует консультироваться, когда пациенты запрашивают опиоидные обезболивающие или при подозрении на злоупотребление опиоидами. Этот ресурс (доступный по адресу www.pdmpassist.org/content/state-profiles) может дать рекомендации по безопасному назначению и помочь выявить пациентов, страдающих от злоупотребления опиоидами или расстройствами, связанными с употреблением опиоидов, и которым будет полезно лечение.Некоторые штаты теперь требуют, чтобы поставщики медицинских услуг использовали программы мониторинга рецептурных препаратов перед назначением определенных контролируемых веществ.
Перед тем, как начать опиоидную терапию при хронической боли у женщин репродуктивного возраста, клиницисты должны обсудить планирование семьи и то, как длительное употребление опиоидов может повлиять на уход во время будущей беременности.
Наконец, осторожный подход к назначению опиоидов должен быть сбалансирован с необходимостью устранения боли у беременной женщины.Беременность не должна быть причиной для отказа от лечения острой боли из-за опасений злоупотребления опиоидами или НАС.
Поставщики акушерских услуг должны быть осведомлены о медицинских, социальных и юридических последствиях, которые могут сопровождать употребление опиоидов беременными женщинами. Беременность дает важную возможность выявлять и лечить женщин с расстройствами, связанными с употреблением психоактивных веществ. Выявление пациентов с расстройствами, связанными с употреблением психоактивных веществ, с использованием проверенных инструментов скрининга, предложение краткосрочных вмешательств (таких как привлечение пациента к короткой беседе, предоставление отзывов и рекомендаций) и направление при необходимости за специализированной помощью, являются важными элементами медицинской помощи 14 Вставка 1.Кроме того, важно защищать эту часто маргинализированную группу пациентов, особенно с точки зрения работы над улучшением доступности лечения и обеспечения того, чтобы беременные женщины с расстройствами, связанными с употреблением опиоидов, которые обращаются за дородовой помощью, не подвергались уголовной ответственности. Наконец, поставщики акушерских услуг несут этическую ответственность перед своими беременными и родителями с расстройствами, связанными с употреблением психоактивных веществ, не поощрять разлучение родителей с их детьми исключительно на основании подозреваемого или подтвержденного расстройства, связанного с употреблением психоактивных веществ 15.В штатах, которые требуют отчетности, лица, определяющие политику, законодатели и врачи должны работать вместе, чтобы отменить карательное законодательство и определить и реализовать научно обоснованные стратегии вне правовой системы для удовлетворения потребностей женщин с зависимостями 16.
SBIRT: Скрининг, краткое вмешательство и направление на лечение
Скрининг, кратковременное вмешательство и направление на лечение (SBIRT) — это научно обоснованная практика, используемая для выявления, снижения и предотвращения проблемного употребления алкоголя и других веществ и зависимости от них.Модель SBIRT была продиктована рекомендацией Института медицины (теперь известной как Отдел здравоохранения и медицины Национальной академии наук, инженерии и медицины), которая призвала к скринингу на уровне сообществ на предмет поведения, связанного с риском для здоровья, включая употребление психоактивных веществ.
Скрининг — Медицинский работник оценивает пациента на предмет опасного поведения, связанного с употреблением психоактивных веществ, используя стандартные инструменты скрининга. Скрининг может проводиться в любом учреждении здравоохранения.
Краткое вмешательство — Медицинский работник вовлекает пациента, демонстрирующего опасное поведение, связанное с употреблением психоактивных веществ, в короткой беседе, предоставляя обратную связь и совет.
Направление на лечение — Медицинский работник направляет на краткую терапию или дополнительное лечение пациентов, которые проходят обследование и нуждаются в дополнительных услугах.
Данные центра комплексных решений для здравоохранения SAMHSA-HRSA. SBIRT: скрининг, краткое вмешательство и направление на лечение. Доступно по адресу: http://www.integration.samhsa.gov/clinical-practice/SBIRT. Проверено 20 марта 2017 года.
Физиология и фармакология употребления опиоидов
Опиоиды уменьшают интенсивность болевых сигналов и обычно назначаются для лечения боли, хотя кашель и диарея являются другими показаниями к их применению.Опиоиды обладают дополнительным эффектом, вызывая чувство эйфории, которое может привести к их неправильному употреблению. 17. Расстройство, связанное с употреблением опиоидов, может развиться при повторном употреблении любого опиоида, особенно у людей с лежащей в основе генетической уязвимостью. Героин — это быстродействующий опиоид, который можно вводить инъекционно, курить или вдыхать через нос. 18. Героин имеет короткий период полураспада, и чтобы избежать симптомов отмены опиоидов, физически зависимый героин должен принимать несколько доз в день. Назначенные опиоиды, такие как кодеин, фентанил, морфин, метадон, оксикодон, меперидин, гидроморфон, гидрокодон, пропоксифен и бупренорфин, потенциально могут быть использованы не по назначению.Эти продукты можно глотать, вводить путем инъекций, вдыхать через нос, курить, жевать или использовать в качестве суппозиториев 19. Начало и интенсивность эффекта будут варьироваться в зависимости от того, как было принято лекарство, и от состава; однако все они могут вызвать угнетение дыхания, передозировку и смерть. Риск угнетения дыхания, передозировки и смерти выше для полных агонистов опиоидов (таких как фентанил), чем для частичных агонистов (таких как бупренорфин). Инъекция опиоидов также сопряжена с риском целлюлита и образования абсцесса в месте инъекции, сепсиса, эндокардита, остеомиелита, гепатита B, гепатита C и ВИЧ-инфекции.Совместное использование приспособлений для нюхания также было определено как фактор риска передачи гепатита С и других вирусов в группе беременных женщин с гепатитом С 20.
Регулярное долгосрочное употребление любого опиоида приводит к предсказуемой физиологической зависимости, что приводит к симптомы отмены при отмене препарата. Типичные симптомы отмены опиоидов включают общую боль, мышечную боль, тошноту, диарею, потливость, ринорею, слезотечение, расширение зрачков, тремор, мурашки по коже, беспокойство и беспокойство.При употреблении опиоидов короткого действия, таких как героин, симптомы отмены могут развиваться в течение 4–6 часов после употребления, достигать максимума через 1–3 дня и постепенно уменьшаться в течение 5–7 дней. Для опиоидов длительного действия, таких как метадон, симптомы отмены обычно начинаются в течение 24–36 часов после употребления и могут длиться несколько недель. В отличие от алкогольной абстиненции, абстиненция от опиоидов редко связана с тяжелыми заболеваниями и легко поддается лечению.
Влияние употребления опиоидов на беременность и исход беременности
Безопасность опиоидов на ранних сроках беременности оценивалась в ряде обсервационных исследований.Более ранние отчеты не показали увеличения риска врожденных дефектов после пренатального воздействия оксикодона, пропоксифена или меперидина 21 22. Связь между использованием кодеина в первом триместре беременности и врожденными аномалиями была обнаружена в некоторых исследованиях 23 24 25, но не в других. 26 27. Авторы одного ретроспективного исследования наблюдали повышенный риск нескольких врожденных дефектов при использовании назначенных женщинами опиоидов за месяц до беременности или в течение первого триместра 25. Другое недавнее обсервационное исследование обнаружило возможную связь между употреблением опиоидов в первый триместр и дефекты нервной трубки, хотя и не при использовании кодеина специально 28.Однако существуют методологические проблемы с этими исследованиями, которые могут привести к смещению и ошибочности воспоминаний. Наблюдаемые врожденные дефекты остаются редкими и представляют собой незначительное увеличение абсолютного риска. Недавний метаанализ, сравнивавший метадон и бупренорфин, не обнаружил различий между группами в отношении врожденных пороков развития. Кроме того, частота аномалий, о которых сообщалось, была аналогична той, которую можно было бы ожидать в общей популяции 29. В целом беспокойство по поводу потенциально небольшого повышенного риска врожденных дефектов, связанного с фармакотерапией опиоидными агонистами во время беременности, следует сопоставить с явными рисками, связанными с продолжающееся злоупотребление опиоидами беременной женщиной.
Во время беременности хроническая нелеченая зависимость от героина связана с отсутствием дородового ухода, повышенным риском задержки роста плода, отслойкой плаценты, гибелью плода, преждевременными родами и внутриутробным переходом мекония 30. Кроме того, нелеченная зависимость связана с вовлечением виды деятельности с высоким риском, такие как проституция, торговля сексом в обмен на наркотики и преступная деятельность. Такое поведение подвергает женщин риску ИППП, насилию и правовым последствиям, включая потерю опеки над детьми, уголовное преследование или тюремное заключение.
Беременные женщины с расстройством, вызванным употреблением опиоидов, часто страдают сопутствующими психическими расстройствами, особенно депрессией, травмами в анамнезе, посттравматическим стрессовым расстройством и тревогой. Более 30% беременных женщин, включенных в программу лечения наркозависимости, дали положительный результат скрининга на умеренную и тяжелую депрессию, и более 40% сообщили о симптомах послеродовой депрессии 31. Кроме того, они подвергаются повышенному риску употребления других веществ, включая табак. , марихуана и кокаин 32.Эти женщины также часто страдают от плохого питания, и многие из них нарушили систему поддержки, что привело к потребности в социальных услугах. Выявление этих проблем во время беременности с направлением для получения специализированной многопрофильной помощи важно для достижения оптимального ухода за этими женщинами.
Скрининг на употребление опиоидов и расстройства, связанные с употреблением опиоидов во время беременности
Скрининг на употребление психоактивных веществ должен быть частью комплексной акушерской помощи и должен проводиться при первом дородовом посещении совместно с беременной женщиной.Расстройства, связанные с употреблением психоактивных веществ, затрагивают женщин всех расовых и этнических групп и всех социально-экономических групп, а также затрагивают женщин в сельских, городских и пригородных районах. Скрининг, основанный только на таких факторах, как плохая приверженность к дородовой помощи или предшествующий неблагоприятный исход беременности, может привести к пропущенным случаям и может усилить стереотипы и стигму 33. Поэтому важно, чтобы скрининг был универсальным. Перед беременностью и на ранних сроках беременности всех женщин следует регулярно спрашивать об употреблении ими алкоголя и наркотиков, в том числе рецептурных опиоидов и других лекарств, используемых в немедицинских целях.В начале разговора пациентку следует проинформировать о том, что эти вопросы задают всем беременным женщинам, чтобы убедиться, что они получают необходимую помощь. Сохранение заботливого и непредвзятого подхода, а также скрининг, когда пациент один, важны и обеспечат наиболее полное раскрытие информации. Поставщики акушерской помощи должны защищать автономию пациента, конфиденциальность и целостность взаимоотношений между пациентом и врачом в той мере, в какой это разрешено законами, касающимися раскрытия информации о расстройстве, вызванном употреблением психоактивных веществ (доступно на сайте www.guttmacher.org/state-policy/explore/substance-abuse-during-pregnancy. Врачи должны знать, что требования к отчетности сильно различаются и должны быть знакомы с законодательными требованиями в своем штате или сообществе 15. Регулярный скрининг должен опираться на проверенные инструменты скрининга, такие как анкеты, включающие 4P, NIDA Quick Screen и CRAFFT (для женщин 26 лет. или моложе) Вставка 2 34 35 36. Эти инструменты хорошо изучены и демонстрируют высокую чувствительность для выявления употребления психоактивных веществ и злоупотребления ими.Они могут использоваться в формате прямого интервью как врачами, так и нефизиками, и могут быть внедрены в клиническую практику с использованием компьютерных подходов 33.
Инструменты клинического скрининга пренатального употребления психоактивных веществ и злоупотребления ими
4 Ps *
P arents: Были ли у кого-либо из ваших родителей проблемы с употреблением алкоголя или других наркотиков?
P artner: Есть ли у вашего партнера проблемы с употреблением алкоголя или наркотиков?
P ast: Были ли у вас в прошлом трудности в жизни из-за алкоголя или других наркотиков, включая лекарства, отпускаемые по рецепту?
P возмущено: Употребляли ли вы в прошлом месяце алкоголь или другие наркотики?
Подсчет баллов: любое «да» должно вызывать дополнительные вопросы.
NIDA Quick Screen †
Просмотрите своих пациентов
Шаг 1. Спросите пациента об употреблении наркотиков в прошлом году — NIDA Quick Screen
Шаг 2. Начните работу с модифицированной NIDA ASSIST
Шаг 3. Определите уровень риска
Проведите краткое вмешательство
CRAFFT — тест на злоупотребление психоактивными веществами для подростков и молодых взрослых ‡
C Вы когда-нибудь ездили в автомобиле, за рулем которого вы сами) кто был под кайфом или употреблял алкоголь или наркотики?
R Вы когда-нибудь употребляли алкоголь или наркотики, чтобы РАССЛАБИТЬСЯ, почувствовать себя лучше или приспособиться?
A Употребляете ли вы когда-нибудь алкоголь или наркотики, находясь в одиночестве или ОДИН?
F ЗАБЫВАЕТЕ ли вы когда-нибудь о вещах, которые вы делали, употребляя алкоголь или наркотики?
F Ваша СЕМЬЯ или друзья когда-нибудь говорили вам, что вам следует сократить употребление алкоголя или наркотиков?
T Были ли у вас ПРОБЛЕМЫ, когда вы употребляли алкоголь или наркотики?
Подсчет баллов: два или более положительных пункта указывают на необходимость дальнейшей оценки.
Джон Р. Найт, доктор медицины, Детская больница Бостона, 2016. Все права защищены. Воспроизведено с разрешения. Для получения дополнительной информации свяжитесь с [email protected].
* Юинг Х. Практическое руководство по оказанию медицинских и социальных услуг беременным и послеродовым наркоманам и алкоголикам: теоретические основы, инструмент краткого скрининга, ключевые вопросы интервью и стратегии направления к ресурсам по выздоровлению. Мартинес (Калифорния): Проект «Рожденные свободными», Департамент здравоохранения округа Контра-Коста; 1990 г.
† Национальный институт по борьбе со злоупотреблением наркотиками. Справочник ресурсов: скрининг на употребление наркотиков в медицинских учреждениях общего профиля. Доступно по адресу: https://www.drugabuse.gov/publications/resource-guide-screeningdrug-use-in-general-medical-settings/nida-quick-screen. Проверено 8 марта 2017 г.
‡ Центр исследований подростковой токсикомании, Детская больница Бостона. Отборочное интервью CRAFFT. Бостон (Массачусетс): CeSAR; 2009 г. Доступно по адресу: http://www.ceasar.org/CRAFFT/pdf/CRAFFT_English.pdf. Проверено 28 апреля, 2017 г.
Тест на наркотики в моче также использовался для выявления или подтверждения подозрения на употребление психоактивных веществ, но его следует проводить только с согласия пациента и в соответствии с законами штата. Беременные женщины должны быть проинформированы о возможных последствиях положительного результата теста, в том числе о любых обязательных требованиях к отчетности. 15 16. Регулярный скрининг мочи на наркотики является спорным по нескольким причинам. Положительный результат теста на наркотики сам по себе не является признаком расстройства, связанного с употреблением опиоидов, или его тяжести.Тестирование мочи на наркотики позволяет оценить только текущее или недавнее употребление психоактивных веществ; таким образом, отрицательный результат теста не исключает спорадического употребления психоактивных веществ. Кроме того, токсикологический анализ мочи может не выявить многие вещества, включая синтетические опиоиды, некоторые бензодиазепины и дизайнерские наркотики. Ложноположительные результаты тестов могут быть получены при иммунном тестировании, и юридические последствия могут быть разрушительными для пациента и ее семьи. Поставщики медицинских услуг должны быть осведомлены о характеристиках тестов своей лаборатории и требовать проведения подтверждающего тестирования с помощью масс-спектрометрии и жидкостной или газовой хроматографии, если это необходимо.Некоторые центры внедрили универсальный токсикологический скрининг мочи для беременных пациенток, при этом одно исследование показало более высокие показатели выявления употребления психоактивных веществ матерями по сравнению со стандартными методами 37. Однако в этом исследовании не использовались проверенные вербальные инструменты скрининга в группе сравнения, что ограничивает полезность этих результатов. Необходимы дополнительные исследования, чтобы лучше понять влияние универсального скрининга мочи на исходы у матери и новорожденного. По этим причинам утвержденные инструменты вербального скрининга, такие как те, что обсуждались ранее, являются предпочтительным методом для первоначального скрининга.Инструменты для сбора анамнеза и устного скрининга дают возможность поставщику услуг дородового ухода предложить краткое вмешательство (например, вовлечь пациента в короткий разговор, дать обратную связь и дать совет), обучить пациентов и использовать принципы мотивационного собеседования, чтобы вызвать желание при необходимости изменить поведение, сопряженное с повышенным риском 33. Более тяжелые расстройства, связанные с употреблением психоактивных веществ, требуют направления на специализированное лечение.
Поставщики акушерских услуг должны быть осведомлены о местных ресурсах для лечения наркозависимости.Заручившись помощью социальных служб, чтобы облегчить направление пациентов к специалистам, и общение с поставщиками медицинских услуг, оказывающих услуги по лечению наркозависимости, оптимизирует уход за пациентами.
Лечение
Фармакотерапия опиоидными агонистами
С 1970-х годов фармакотерапия опиоидными агонистами (также называемая медикаментозным лечением) метадоном в сочетании с консультированием и поведенческой терапией была стандартным лечением героиновой зависимости во время беременности 30 В последующие годы фармакотерапия метадоном или бупренорфином использовалась для лечения расстройства, связанного с употреблением опиоидов 30 38 у беременных женщин.
Фармакотерапия опиоидными агонистами во время беременности имеет множество причин. Фармакотерапия опиоидными агонистами предотвращает симптомы отмены опиоидов и, как показано, предотвращает осложнения немедицинского употребления опиоидов за счет снижения риска рецидива и связанных с ним последствий. Это также улучшает приверженность к программам дородовой помощи и лечения зависимостей. Было продемонстрировано, что фармакотерапия опиоидными агонистами в сочетании с пренатальным уходом снижает риск акушерских осложнений 30 39. Абстинентный синдром новорожденных является ожидаемым и поддающимся лечению состоянием, которое может следовать за пренатальным воздействием опиоидных агонистов и требует сотрудничества с педиатрической бригадой для оказания помощи младенец.
Медицинские работники, занимающиеся лечением наркозависимости, должны быть знакомы с федеральными правилами, касающимися конфиденциальности записей пациентов, злоупотребляющих алкоголем и наркотиками. Эти правила требуют наличия определенных элементов 42 CFR Часть 2 для письменного согласия на раскрытие информации о пациенте 40. Список местных программ лечения расстройства, связанного с употреблением опиоидов, можно найти на веб-сайте Управления служб психического здоровья и злоупотребления психоактивными веществами http://dpt2.samhsa.gov /treatment/directory.aspx 41.
Метадон
Метадон отпускается ежедневно по зарегистрированной программе лечения опиоидов и должен быть частью комплексного лечения, включая консультирование по вопросам зависимости, семейную терапию, обучение питанию и другие медицинские и психосоциальные услуги как показано беременным женщинам с расстройством, связанным с употреблением опиоидов.Дозировка метадона для матери регулируется специалистами по лечению наркозависимости в рамках зарегистрированных программ лечения опиоидов, а общение между акушерской бригадой и программой лечения опиоидов способствует качественному уходу. Дозировку метадона, возможно, придется корректировать на протяжении всей беременности, чтобы избежать симптомов отмены, которые включают тягу к наркотикам, спазмы в животе, тошноту, бессонницу, раздражительность и беспокойство. Метадон имеет значительные фармакокинетические взаимодействия со многими другими лекарствами, такими как антиретровирусные средства, и может увеличивать интервал QTc в зависимости от дозы, что следует учитывать перед введением новых лекарств.
Если женщина получала стабильную дозу метадона до беременности, фармакокинетические и физиологические изменения, которые происходят во время беременности, могут потребовать корректировки дозы, особенно в третьем триместре 42. Из-за метаболических изменений во время беременности однократная суточная доза может не контролировать симптомы отмены в течение 24-часового периода. Быстрый метаболизм часто развивается во время беременности, особенно в третьем триместре, и в этих случаях раздельные дозы могут быть оптимальными 43. Не всем женщинам требуется увеличение дозы во время беременности, и корректировку доз следует проводить на клинической основе.
Если женщина начинает лечение метадоном во время беременности, ее дозу следует титровать до тех пор, пока у нее не исчезнут симптомы, в соответствии с протоколами безопасной индукции. Неадекватная дозировка метадона для матери может привести к появлению признаков и симптомов отмены опиоидов от легкой до умеренной, которые могут вызывать стресс у плода и тягу матери к наркотикам 43, что увеличивает вероятность рецидива и прекращения лечения.
В нескольких исследованиях изучали, в какой степени материнская доза метадона связана с тяжестью неонатального абстинентного синдрома.Систематический обзор литературы и метаанализ показали, что частота и продолжительность неонатального абстинентного синдрома не различаются в зависимости от дозировки метадона для матери 44; поэтому попытки минимизировать дозу метадона не показаны, поскольку низкие дозы не всегда связаны с более легкими или более короткими симптомами НАС. Интересно, что некоторые исследования показывают более низкие показатели НАС при использовании раздельных схем дозирования метадона 43.
В большинстве ситуаций беременные женщины начинают индукцию метадоном в рамках лицензированной амбулаторной программы лечения опиоидами.Некоторые акушерские службы начинают терапию опиоидными агонистами метадоном или бупренорфином в стационарных условиях. Хотя это может позволить более тщательно контролировать реакцию на лекарства, это не всегда необходимо или доступно. В случаях, когда беременная женщина начинает лечение метадоном в стационаре, перед выпиской следует договориться о приеме на следующий день для прохождения программы лечения опиоидами, чтобы не было пропущенных дней. Пациенты, которые начали принимать бупренорфин в стационаре, могут получать рецепт до их назначения лицензированным врачом, выписывающим бупренорфин.Перед выпиской необходимо установить постоянного поставщика бупренорфина и записаться на прием.
За исключением бупренорфина, в настоящее время для врача незаконно выписывать рецепт на любые другие опиоиды, включая метадон, для лечения расстройства, связанного с употреблением опиоидов, помимо лицензированной программы лечения опиоидами (где лекарства отпускаются) 45. Бупренорфин является единственным агонистом опиоидов, одобренным в настоящее время для лечения расстройства, связанного с употреблением опиоидов, по рецепту в офисных условиях 46.Однако врачи могут отпускать метадон и бупренорфин в условиях больницы без исключения. Лица, выписывающие рецепты, должны быть знакомы с федеральными постановлениями (доступны по адресу www.gpo.gov/fdsys/pkg/CFR-2016-title21-vol9/xml/CFR-2016-title21-vol9-sec1306-07.xml и постановлениями штата относительно назначения лекарств. для лечения расстройства, связанного с употреблением опиоидов
Бупренорфин
Последние данные подтверждают использование бупренорфина для лечения расстройства, связанного с употреблением опиоидов, во время беременности.Бупренорфин действует на те же мю-опиоидные рецепторы, что и героин и морфин 47, но действует как частичный, а не полный агонист, что снижает вероятность передозировки 48. Другие преимущества бупренорфина перед метадоном включают меньшее количество лекарственных взаимодействий, возможность лечения в амбулаторных условиях. без необходимости ежедневного посещения программы лечения опиоидами и свидетельств меньшей необходимости в корректировке дозировки на протяжении всей беременности. Кроме того, несколько исследований демонстрируют доказательства менее тяжелой неонатальной абстиненции 49.К недостаткам по сравнению с метадоном относятся редкие сообщения о печеночной дисфункции, отсутствие долгосрочных данных о последствиях для младенцев и детей, потенциально больший риск, связанный с индукцией из-за риска ускоренной абстиненции, и повышенный риск утечки (т. Е. совместное использование или продажа) прописанного бупренорфина 50.
Бупренорфин доступен в виде монопродукта или в виде комбинированного препарата с налоксоном, антагонистом опиоидов, который используется для уменьшения утечки, поскольку бупренорфин в сочетании с налоксоном вызывает тяжелые симптомы отмены при инъекции.Однако налоксон не является активным при пероральном приеме, поэтому при сублингвальном применении в соответствии с указаниями 47 симптомов отмены не возникает. 47. Монопродукт бупренорфина рекомендован во время беременности, чтобы избежать любого потенциального пренатального воздействия налоксона, особенно при введении 50. Тем не менее, недавние исследования, в которых оценивалась эффективность Использование комбинированного препарата бупренорфин с налоксоном не выявило побочных эффектов, и результаты были аналогичными по сравнению с одним бупренорфином 51 52. Использование комбинированного препарата во время беременности, вероятно, будет расширяться по мере накопления большего количества данных о безопасности.
Монопродукт бупренорфина имеет более высокий потенциал для неправильного использования, например, для внутривенных инъекций и утечки, и более высокую уличную ценность по сравнению с комбинированным продуктом. Таким образом, все пациенты должны находиться под наблюдением на предмет риска утечки их лекарства, особенно если прописан монопродукт. В отличие от метадона, который можно вводить только через строго контролируемые программы, бупренорфин может быть назначен для лечения расстройства, связанного с употреблением опиоидов, обученными и U.S. Утвержденные Управлением по борьбе с наркотиками поставщики медицинских услуг в медицинских учреждениях, что потенциально увеличивает доступность лечения и снижает стигму 47. Управление по борьбе с наркотиками и психическим здоровьем публикует каталог поставщиков медицинских услуг, зарегистрированных для прописывания бупренорфина www. samhsa.gov/medication-assisted-treatment/physician-program-data/treatment-physician-locator. В настоящее время в Соединенных Штатах насчитывается более 37 000 медицинских работников различных специальностей, которые прошли обучение и могут назначать бупренорфин 53.
Пациенты, которым назначено лечение бупренорфином вместо метадона, должны иметь возможность безопасно принимать препарат самостоятельно и соблюдать режим лечения. По сравнению с программами лечения опиоидами менее строгая структура стационарного лечения бупренорфином может сделать его неподходящим для некоторых пациентов, которым требуется более интенсивная структура и наблюдение 54.
Если беременная женщина уже получает терапию метадоном, ей не следует переходить к бупренорфину из-за значительного риска ускоренной отмены.Подобного риска отмены при переходе с бупренорфина на метадон нет. Всегда следует учитывать потенциальный риск нераспознанных неблагоприятных долгосрочных исходов при использовании бупренорфина, который присущ при использовании любых относительно новых лекарств во время беременности. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США недавно одобрило имплантат бупренорфина длительного действия, который обеспечивает низкие или умеренные дозы бупренорфина на срок до 6 месяцев для лечения расстройства, связанного с употреблением опиоидов, у пациентов, стабильно принимающих сублингвальную форму.На сегодняшний день нет данных об использовании имплантата у беременных.
Отмена под медицинским наблюдением
Для беременных женщин с расстройством, связанным с употреблением опиоидов, фармакотерапия опиоидными агонистами является рекомендуемой терапией и предпочтительнее отмены под медицинским наблюдением, поскольку отмена связана с высокой частотой рецидивов 55 56 57, варьирующейся от 59% до более 90 % 58 и более низкие результаты. Рецидив представляет собой серьезный риск, включая передачу инфекционных заболеваний, случайную передозировку из-за потери толерантности, акушерские осложнения и отсутствие дородовой помощи.Если женщина не принимает лечение опиоидным агонистом или лечение недоступно, можно рассмотреть возможность отмены под медицинским наблюдением под наблюдением врача, имеющего опыт лечения перинатальной зависимости, и с информированного согласия; однако для достижения успеха часто требуется длительное стационарное лечение и интенсивное амбулаторное наблюдение за поведенческим здоровьем. В некоторых районах доступ к фармакотерапии опиоидными агонистами ограничен, и следует предпринять усилия для улучшения доступности местных ресурсов.В ранних сообщениях о случаях было высказано беспокойство по поводу того, что отказ от опиоидов во время беременности может привести к стрессу плода и смерти плода 59 60. Более поздние исследования не находят четких доказательств связи между отменой под медицинским наблюдением и смертью плода или преждевременными родами, но долгосрочное наблюдение данные об этих женщинах отсутствуют 61 62 63, особенно с точки зрения частоты рецидивов. Необходимы дополнительные исследования для оценки безопасности (особенно в отношении рецидива у матери), эффективности и долгосрочных результатов отмены под медицинским наблюдением.
Налтрексон
Налтрексон — неселективный антагонист опиоидных рецепторов, который в терапевтических дозах блокирует эйфорические эффекты опиоидов и используется для помощи небеременным пациентам с расстройством, связанным с употреблением опиоидов, в их усилиях по поддержанию абстиненции. Хотя пероральная форма демонстрирует плохое соблюдение режима лечения, недавно одобренная инъекционная форма длительного действия более эффективна, чем плацебо в поддержании воздержания 64. На сегодняшний день информация о ее применении во время беременности ограничена небольшими сериями случаев и отчетами о случаях с нормальными исходами родов. сообщил 58.Однако существуют серьезные опасения относительно неизвестных эффектов на плод, а также риска рецидива и прекращения лечения с последующим возвращением к употреблению опиоидов и риском передозировки 64. Исследования лечения налтрексоном во время беременности создают этические и логистические проблемы, но необходимы для информирования об использовании это лечение у беременных. Недавний опрос среди беременных женщин, включенных в комплексную программу лечения наркозависимости, продемонстрировал большой интерес к рассмотрению возможности лечения антагонистами во время беременности 65.Решение о продолжении лечения налтрексоном для женщины, уже принимавшей налтрексон до беременности, должно включать тщательное обсуждение с пациенткой, которое сравнивает ограниченные данные по безопасности с потенциальным риском рецидива при прекращении лечения.
Налоксон
Налоксон — антагонист опиоидов короткого действия, который может быстро обратить вспять эффекты опиоидов и может спасти жизнь в условиях передозировки опиоидов. Хотя индуцированная абстиненция может способствовать стрессу плода, налоксон следует применять беременным женщинам в случае передозировки у матери, чтобы спасти жизнь женщины.
Налоксон может вводиться внутривенно или подкожно специалистами здравоохранения или неотложной медицинской помощи. Кроме того, при подозрении на передозировку форму для автоинъекций и предварительно упакованный назальный спрей могут вводить члены семьи или другие посторонние лица. 66. Пациентам с риском передозировки, например, при длительном применении или высоких дозах опиоидов, может помочь налоксон. комплект доступен в любое время. Во многих штатах разрешается выписывать налоксон третьему лицу, например члену семьи или опекуну, который может помочь в случае передозировки www.drugabuse.gov/related-topics/naloxone; www.prescribetoprevent.org.
Дородовой, интранатальный и послеродовой уход
Дородовой уход
Элементы дородового ухода за женщинами, употребляющими или употребляющими опиоиды, будут зависеть от ситуации каждого пациента и сопутствующих заболеваний. Следует рассмотреть ряд вопросов, включая следующие:
Следует рассмотреть возможность тестирования на ИППП и другие инфекционные агенты, такие как ВИЧ, гепатиты B и C, хламидийная инфекция, гонорея, сифилис и туберкулез.Если женщина относится к группе повышенного риска, может быть показано повторное тестирование в третьем триместре. Вакцинация против гепатита В рекомендуется беременным женщинам с отрицательным результатом на HBsAg, но с высоким риском заражения гепатитом В.
Необходимо проводить скрининг на депрессию и другие нарушения психического здоровья.
В дополнение к ультразвуковому обследованию для оценки состояния плода в середине второго триместра следует рассмотреть возможность проведения ультразвукового исследования в первом триместре для наилучшего определения предполагаемой даты родов и интервальной ультразвуковой оценки веса плода на более поздних сроках беременности, если есть беспокойство по поводу аномалий роста плода.
Консультации с анестезиологами, наркологами, специалистами по обезболиванию, педиатрами, медициной матери и плода, поведенческим здоровьем, питанием и социальными службами должны проводиться по мере необходимости.
Поскольку грудное вскармливание следует поощрять у женщин, которые стабильно принимают свои опиоидные агонисты, не принимают запрещенные препараты и не имеют других противопоказаний (см. Послеродовой уход), акушеры-гинекологи и другие акушерские работники должны обеспечивать опережающее грудное вскармливание. руководство в дородовой период 67.
Тесное общение между акушером и педиатрической бригадой перед родами необходимо для оптимального ведения новорожденного. Неонатальная консультация, если таковая доступна, может быть рассмотрена во время беременности, чтобы обсудить уход за младенцем после родов.
Употребление других веществ, особенно табака, часто встречается у женщин с расстройствами, связанными с употреблением опиоидов. Обследование и обсуждение этого и других веществ имеет важное значение, и необходимо предлагать услуги по прекращению употребления табака.
Уход во время родов
Роженицам, принимающим метадон или бупренорфин, следует продолжить прием поддерживающей дозы опиоидного агониста и получить дополнительное обезболивающее 68 69. При необходимости следует предложить эпидуральную или спинальную анестезию для купирования боли в труда или для доставки. Следует избегать приема таких опиоидных агонистов-антагонистов, как буторфанол, налбуфин и пентазоцин, поскольку они могут спровоцировать острую отмену у пациентов, принимающих опиоидные агонисты.Некоторые пациенты, которые физиологически зависимы от опиоидов, могут не раскрывать информацию о своем употреблении психоактивных веществ, и поэтому медицинские работники могут не знать об их употреблении опиоидами. Из-за этого некоторые подразделения решили удалить эти лекарства из своих формуляров из-за непреднамеренного ускорения отмены. Бупренорфин не следует назначать пациенту, принимающему метадон. Педиатрический персонал должен быть уведомлен обо всех младенцах, подвергшихся воздействию опиоидов, чтобы обеспечить надлежащий скрининг на неонатальный абстинентный синдром.
Как правило, пациентам, принимающим метадон или бупренорфин, для достижения обезболивания требуются более высокие дозы опиоидов, чем другим пациентам, поскольку они толерантны к поддерживающей дозе. Одно исследование показало, что после кесарева сечения женщинам, принимавшим бупренорфин, требовалось на 47% больше опиоидных анальгетиков, чем женщинам, которые не принимали бупренорфин, но адекватное обезболивание было достигнуто с помощью опиоидов короткого действия и противовоспалительных препаратов 70. Инъекционные нестероидные противовоспалительные средства, такие как кеторолак , также очень эффективны для снятия боли в послеродовом периоде и после кесарева сечения.Ежедневные дозы метадона или бупренорфина должны поддерживаться во время родов и послеродового пребывания женщины в больнице, чтобы предотвратить абстинентный синдром, и пациенты должны быть предупреждены об этом плане заранее, чтобы уменьшить беспокойство. Разделение обычной суточной лечебной дозы бупренорфина или метадона на три или четыре приема каждые 6–8 часов может обеспечить частичное облегчение боли; однако потребуется дополнительная анальгезия. 68. Обезболивание во время родов и в послеродовом периоде у пациентов, получающих терапию опиоидными агонистами, может быть сложной задачей из-за их повышенной переносимости лекарств и повышенной чувствительности к боли.При наличии ресурсов консультация анестезиолога может быть полезна беременным женщинам с расстройством, связанным с употреблением психоактивных веществ или хроническим употреблением опиоидов, для разработки плана обезболивания, адаптированного к конкретному пациенту. Мультимодальный подход к обезболиванию с нейроаксиальной анальгезией и нестероидными противовоспалительными препаратами и ацетаминофеном обычно необходим для эффективного обезболивания во время родов и в послеродовом периоде. симптомов неонатального абстинентного синдрома, меньшей потребности в фармакотерапии и более короткого пребывания ребенка в больнице 72.Кроме того, грудное вскармливание способствует установлению привязанности между женщиной и ее младенцем, облегчает уход кожа к коже и обеспечивает ребенку иммунитет. Следует поощрять грудное вскармливание у женщин, которые стабильны на своем опиоидном агонисте, не принимают запрещенные препараты и не имеют других противопоказаний, таких как ВИЧ-инфекция 73 74. Женщин следует проконсультировать о необходимости приостановить грудное вскармливание в случае рецидив. Американская академия педиатрии рекомендует кормить грудью женщин, принимающих метадон и бупренорфин, независимо от дозы для матери, поскольку перенос этих лекарств в грудное молоко минимален 75.У кормящих женщин сверхбыстрое превращение кодеина в морфин может привести к высоким и небезопасным уровням морфина в крови и грудном молоке. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США усилило этикетку с предупреждением о том, что грудное вскармливание не рекомендуется при использовании лекарств, содержащих кодеин или трамадол, из-за возможности серьезных побочных эффектов у ребенка из-за передозировки опиоидов 76. Однако, если кодеинсодержащие лекарства считается предпочтительным выбором, риски и преимущества этого препарата, а также причины предупреждения FDA следует обсудить с каждой семьей.
Хотя у большинства беременных женщин, принимающих метадон, дозировка увеличивается во время беременности, и в послеродовом периоде можно ожидать снижения дозировки, одно исследование продемонстрировало небольшую потребность в снижении дозировки метадона в послеродовом периоде 77. Значительное снижение дозы в послеродовом периоде не следует проводить рутинно, но следует титровать до признаков и симптомов седативного эффекта, особенно на пике дозы (2–6 часов). Большинство женщин, принимающих бупренорфин, не будут испытывать больших корректировок дозировки во время беременности, и большинство из них могут продолжать принимать те же дозы после родов 77.Другие лекарства, которые могут вызывать седативный эффект (например, бензодиазепины, золпидем, антигистаминные препараты), следует использовать с осторожностью, поскольку они могут повысить риск угнетения дыхания у матери 78.
Женщинам с расстройством, вызванным употреблением психоактивных веществ, следует продолжать фармакотерапию опиоидными агонистами в послеродовом периоде. Послеродовой период представляет собой время повышенной уязвимости, и у женщин с расстройством, вызванным употреблением опиоидов, рецидивы гораздо чаще возникают в послеродовом периоде по сравнению с периодом беременности 79. Причинами рецидива могут быть потеря страховки и доступа к лечению, необходимость ухода за новорожденным , недосыпание и угроза потери опеки над ребенком.Психиатрические расстройства, такие как депрессия, тревога, биполярное расстройство и посттравматическое стрессовое расстройство, распространены среди женщин с расстройством, связанным с употреблением опиоидов. Скрининг послеродовой депрессии должен быть рутинным, и следует рассмотреть возможность оценки других сопутствующих психических расстройств, если имеется предшествующий анамнез или есть опасения 78 80. Употребление психоактивных веществ и передозировка все чаще оказываются основными факторами, способствующими смертности в результате беременности в Соединенные Штаты Америки 9 10. Должен быть обеспечен доступ к адекватным службам послеродовой психосоциальной поддержки, включая программы лечения наркозависимости и профилактики рецидивов 81.Кроме того, послеродовые женщины с расстройствами, связанными с употреблением опиоидов, должны пройти обучение передозировке и, предпочтительно, назначить налоксон для профилактики передозировки 82.
Частота нежелательной беременности среди женщин с расстройствами, связанными с употреблением психоактивных веществ, составляет примерно 80%, что значительно выше, чем в общей популяции. Использование надежных противозачаточных средств среди этой группы женщин также ниже по сравнению с группой сравнения, не употребляющей наркотики 83. Таким образом, обсуждение полного спектра вариантов контрацепции следует начинать с этих пациенток пренатально.В частности, акушерские работники должны проконсультировать женщин о возможности немедленного послеродового лечения обратимой контрацепции длительного действия, которая имеет мало противопоказаний и является высокоэффективной и удобной 84.
Синдром неонатальной абстиненции
Неонатальный абстинентный синдром — это синдром отмены лекарств, который является синдромом отмены наркотиков, который является синдромом абстиненции у новорожденных. может быть результатом хронического употребления опиоидов матерью во время беременности и является ожидаемым и поддающимся лечению состоянием, наблюдаемым у 30–80% младенцев, рожденных женщинами, принимающими терапию опиоидными агонистами 43 85.Синдром неонатальной абстиненции характеризуется нарушениями в желудочно-кишечной, вегетативной и центральной нервной системах, что приводит к ряду симптомов, включая раздражительность, пронзительный крик, плохой сон и несогласованные сосательные рефлексы, которые приводят к плохому питанию. У младенцев, подвергшихся воздействию метадона, симптомы отмены могут начаться в любое время в течение первых 2 недель жизни, но обычно появляются в течение 72 часов после рождения и могут длиться от нескольких дней до 30 недель. У младенцев, подвергшихся воздействию бупренорфина, у которых развивается неонатальный абстинентный синдром, симптомы обычно развиваются в течение 12–48 часов после рождения, пик которых приходится на 72–96 часов и исчезает к 7 дням 50.Последние данные показывают, что другие вещества, такие как никотин, селективные ингибиторы обратного захвата серотонина и бензодиазепины, могут увеличивать частоту и тяжесть неонатального абстинентного синдрома 72. Использование проверенных скрининговых оценок, таких как шкала Финнегана, для диагностики неонатального абстинентного синдрома и протоколов, стандартизирующих лечение с использованием метадон или морфин были связаны с улучшением исходов для этих младенцев 72. Каждый детский сад должен разработать основанную на фактических данных письменную политику для оценки и лечения младенца с неонатальным абстинентным синдромом, а женщины должны быть проинформированы об основных компонентах этой политики (например, о любых задержка выписки младенца или требования к отчетности).Следует поощрять семьи к посещению и уходу за своими младенцами, а женщинам следует поддерживать их усилия по кормлению грудью своих младенцев, если это уместно. Несколько перинатальных совместных инициатив по обеспечению качества позволили получить ценные ресурсы для поставщиков медицинских услуг и пациентов, чтобы оптимизировать диагностику и лечение неонатального абстинентного синдрома и способствовать сотрудничеству между поставщиками акушерской и неонатальной помощи www.opqc.net/patients-providers/%20NAS; https://public.vtoxford.org/quality-education/nas-universal-training-program/ 86.
Долгосрочные исходы у младенцев
Долгосрочные исходы у младенцев, подвергшихся внутриутробному воздействию опиоидов, оценивались в нескольких обсервационных исследованиях. Основная проблема при оценке этих результатов — изолировать эффекты опиоидных агонистов от других мешающих факторов, таких как употребление других веществ (табак, алкоголь, немедицинские препараты) и воздействие факторов окружающей среды и других медицинских факторов риска (например, низкий социально-экономический статус, плохое пренатальное состояние). по уходу) 87. По большей части исследования не выявили значительных различий в когнитивном развитии между детьми в возрасте до 5 лет, подвергавшимися воздействию метадона в утробе матери, и контрольной группой, сопоставимой по возрасту, расе и социально-экономическому статусу, хотя оценки часто были ниже в обе группы по сравнению с данными населения 88.Профилактические вмешательства, направленные на поддержку женщины и других лиц, осуществляющих уход в раннем и текущем родительских годах, обогащение раннего опыта детей и улучшение качества домашней среды, вероятно, будут полезными 89.
Заключение
Раннее всеобщее обследование краткое вмешательство (например, вовлечение пациента в короткий разговор, предоставление отзывов и рекомендаций) и направление на лечение беременных женщин с употреблением опиоидов и расстройством, связанным с употреблением опиоидов, улучшают исходы для матери и ребенка.Консультации по вопросам контрацепции и доступ к услугам по контрацепции должны быть рутинной частью лечения расстройства, связанного с употреблением психоактивных веществ, среди женщин репродуктивного возраста, чтобы минимизировать риск незапланированной беременности. Беременность у женщин с расстройствами, связанными с употреблением опиоидов, должна проходить под совместным ведением акушерского врача и медицинского работника, обладающего опытом лечения наркозависимости, и от пациентки должно быть получено соответствующее согласие в соответствии с 42 CFR Part 2 на разглашение информации, чтобы можно было обменяться информацией. информация между поставщиками медицинских услуг.Учитывая уникальные потребности беременных женщин с расстройствами, связанными с употреблением опиоидов, медицинским работникам необходимо будет рассмотреть возможность изменения некоторых элементов дородового ухода (таких как расширенное тестирование на ИППП, дополнительные ультразвуковые исследования для оценки веса плода, если есть опасения по поводу аномалий роста плода, и консультации с различными поставщиками медицинских услуг) для удовлетворения клинических потребностей конкретной ситуации пациента. Непрерывность лечения, включая обеспечение постоянного ежедневного приема бупренорфина или метадона, имеет решающее значение для успеха.Для женщин, в том числе беременных, с расстройствами, связанными с употреблением опиоидов, фармакотерапия опиоидными агонистами является рекомендуемой терапией и предпочтительнее отмены под медицинским наблюдением, поскольку отмена связана с более высокой частотой рецидивов, что приводит к худшим исходам. Необходимы дополнительные исследования для оценки безопасности (особенно в отношении рецидива у матери), эффективности и долгосрочных результатов отмены под медицинским наблюдением. Младенцы, рожденные женщинами, которые принимали опиоиды во время беременности, должны находиться под наблюдением педиатра на предмет неонатального абстинентного синдрома.Многопрофильное долгосрочное наблюдение должно включать медицинскую, психологическую и социальную поддержку. В целом, скоординированный междисциплинарный подход без уголовных санкций имеет наилучшие шансы помочь младенцам и их семьям. Поставщики акушерской помощи несут этическую ответственность перед своими беременными и родителями с расстройствами, связанными с употреблением психоактивных веществ, не поощрять разлучение родителей с их детьми исключительно на основании подозреваемого или подтвержденного расстройства, связанного с употреблением психоактивных веществ.
Дополнительная информация
Американский колледж акушеров и гинекологов обнаружил дополнительные ресурсы по темам, связанным с этим документом, которые могут быть полезны акушерам-гинекологам, другим поставщикам медицинских услуг и пациентам.Вы можете просмотреть эти ресурсы на сайте www.acog.org/More-Info/OpioidUseinPregnancy.
Эти ресурсы предназначены только для информации и не могут быть исчерпывающими. Обращение к этим ресурсам не означает одобрения Американским колледжем акушеров и гинекологов организации, веб-сайта организации или содержания ресурса. Ресурсы могут быть изменены без предварительного уведомления.
Авторские права, август 2017 г., Американская коллегия акушеров и гинекологов.Все права защищены. Никакая часть этой публикации не может быть воспроизведена, сохранена в поисковой системе, размещена в Интернете или передана в любой форме и любыми средствами, электронными, механическими, путем фотокопирования, записи или иными способами, без предварительного письменного разрешения издателя.
Запросы на разрешение на изготовление фотокопий следует направлять в Центр защиты авторских прав, 222 Rosewood Drive, Danvers, MA 01923, (978) 750-8400.
ISSN 1074-861X
Американский колледж акушеров и гинекологов 409 12th Street, SW, PO Box 96920, Вашингтон, округ Колумбия 20090-6920
Употребление опиоидов и расстройство, связанное с употреблением опиоидов во время беременности.Заключение Комитета № 711. Американский колледж акушеров и гинекологов. Obstet Gynecol 2017; 130: e81–94.
Эта информация разработана как образовательный ресурс, чтобы помочь клиницистам в оказании акушерской и гинекологической помощи, и использование этой информации является добровольным. Эта информация не должна рассматриваться как исчерпывающая информация обо всех надлежащих процедурах или методах ухода или как изложение стандарта ухода. Он не предназначен для замены независимого профессионального суждения лечащего врача.Вариации на практике могут быть оправданы, когда, по разумному мнению лечащего врача, такой курс действий определяется состоянием пациента, ограниченностью доступных ресурсов или достижениями в знаниях или технологиях. Американский колледж акушеров и гинекологов регулярно проверяет свои публикации; однако его публикации могут не отражать самые последние свидетельства. Любые обновления этого документа можно найти на сайте www.acog.org или позвонив в ресурсный центр ACOG.
Хотя ACOG прилагает все усилия для предоставления точной и надежной информации, данная публикация предоставляется «как есть», без каких-либо явных или подразумеваемых гарантий точности, надежности или иного характера. ACOG не гарантирует, не гарантирует и не поддерживает продукты или услуги какой-либо фирмы, организации или лица. Ни ACOG, ни его должностные лица, директора, члены, сотрудники или агенты не несут ответственности за любые убытки, ущерб или претензии в отношении любых обязательств, включая прямые, особые, косвенные или косвенные убытки, понесенные в связи с этой публикацией или доверием. по представленной информации.
Инфекции мочевыводящих путей во время беременности
1. Паттерсон Т.Ф.,
Андриоле В.Т.
Бактериурия при беременности. Инфекция Dis Clin North Am .
1987; 1: 807–22 ….
2. Михаил М.С.,
Аняегбунам А.
Дисфункция нижних мочевыводящих путей при беременности: обзор. Наблюдение за акушерскими гинеколами .
1995; 50: 675–83.
3. Лукас М.Дж.,
Каннингем Ф.Г.
Инфекция мочевыводящих путей при беременности. Clin Obstet Gynecol .1993; 36: 855–68.
4. Барр Дж. Г.,
Ричи Дж. В.,
Генри О,
Эль-Шейх М,
Эль Диб К.
Микроаэрофильные / анаэробные бактерии как причина инфекции мочевыводящих путей во время беременности. Br J Obstet Gynaecol .
1985; 92: 506–10.
5. McDowall DR,
Бьюкенен Дж. Д.,
Фэрли К.Ф.,
Гилберт ГЛ.
Анаэробные и другие привередливые микроорганизмы при бессимптомной бактериурии у беременных. J Заразить Dis .
1981; 144: 114–22.
6. Kass EH.
Беременность, пиелонефрит и недоношенность. Clin Obstet Gynecol .
1970; 13: 239–54.
7. Штамм В.Е.,
Hooton TM.
Лечение инфекций мочевыводящих путей у взрослых. N Engl J Med .
1993; 329: 1328–34.
8. Gratacos E,
Торрес П.Дж.,
Вила J,
Алонсо ПЛ,
Карарах В.
Скрининг и лечение бессимптомной бактериурии при беременности предотвращают пиелонефрит. J Заразить Dis .1994; 169: 1390–2.
9. Harris RE,
Томас В.Л.,
Щелоков А.
Бессимптомная бактериурия при беременности: бактерии, покрытые антителами, функция почек и задержка внутриутробного развития. Am J Obstet Gynecol .
1976; 126: 20–5.
10. Антимикробная терапия акушерских больных. Образовательный бюллетень ACOG No. 245. Вашингтон, округ Колумбия: Американский колледж акушеров и гинекологов, март 1998 г., 245: 8–10.
11. Целевая группа превентивных служб США.Руководство по клиническим профилактическим услугам: отчет Целевой группы США по профилактическим услугам. 2-е изд. Балтимор: Williams & Wilkins, 1996.
12. Harris RE.
Значение искоренения бактериурии во время беременности. Акушерский гинекол .
1979; 53: 71–3.
13. Ромеро Р.,
Оярзун Э,
Мазор М,
Сиртори М,
Хоббинс JC,
Бракен М.
Метаанализ взаимосвязи между бессимптомной бактериурией и преждевременными родами / низкой массой тела при рождении. Акушерский гинекол .
1989. 73: 576–82.
14. Роуз DJ,
Эндрюс WW,
Гольденберг Р.Л.,
Оуэн Дж.
Скрининг и лечение бессимптомной бактериурии беременности для профилактики пиелонефрита: анализ экономической эффективности и затрат-выгод. Акушерский гинекол .
1995; 86: 119–23.
15. WC Wadland,
Plante DA.
Скрининг на бессимптомную бактериурию при беременности. Решение и анализ затрат. Дж. Фам Прак .1989. 29: 372–6.
16. Бахман Ю.В.,
Heise RH,
Naessens JM,
Тиммерман МГ.
Изучение различных тестов для выявления бессимптомных инфекций мочевыводящих путей в акушерской популяции. ДЖАМА .
1993; 270: 1971–4.
17. Дафф П.
Подбор антибиотиков при инфекциях у акушерских больных. Семин Перинатол .
1993; 17: 367–78.
18. Krieger JN.
Осложнения и лечение инфекций мочевыводящих путей во время беременности. Урол Клин Норт Ам .
1986; 13: 685–93.
19. Педди Б.А.,
Бейли Р.Р.,
Wells JE.
Устойчивость изолятов кишечной палочки мочевыводящих путей к котримоксазолу, сульфонамиду, триметоприму и ампициллину: 11-летнее исследование. N Z Med J .
1987; 100: 341–2.
20. Сандерс С.К.,
Сандерс В.Е. Младший
Устойчивость к бета-лактамам у грамотрицательных бактерий: глобальные тенденции и клиническое влияние. Клиническая инфекция .
1992; 15: 824–39.
21. Мастертон Р.Г.,
Эванс, округ Колумбия,
Strike PW.
Однократная доза амоксициллина при лечении бактериурии у беременных и в послеродовом периоде — контролируемое клиническое испытание. Br J Obstet Gynaecol .
1985. 92: 498–505.
22. Harris RE,
Gilstrap LC 3d,
Симпатичная А.
Разовая антимикробная терапия бессимптомной бактериурии во время беременности. Акушерский гинекол .
1982; 59: 546–9.
23. Кэмпбелл-Браун М.,
McFadyen IR.Бактериурия при беременности лечится однократным приемом цефалексина. Br J Obstet Gynaecol .
1983; 90: 1054–9.
24. Якоби П.,
Нейгер Р,
Мерцбах Д,
Палди Э.
Однодозная антимикробная терапия в лечении бессимптомной бактериурии у беременных. Am J Obstet Gynecol .
1987; 156: 1148–52.
25. Харрис RE,
Gilstrap LC 3d.
Цистит при беременности: отдельная клиническая картина. Акушерский гинекол .1981; 57: 578–80.
26. Gilstrap LC 3d, Cunningham FG, Whalley PJ. Острый пиелонефрит при беременности: антероспективное исследование. Акушер Гинеколь 1981; 57: 409–13.
27. Ангел JL,
О’Брайен В.Ф.,
Финан М.А.,
Моралес WJ,
Озеро М,
Кнуппель Р.А.
Острый пиелонефрит у беременных: проспективное исследование пероральной и внутривенной антибиотикотерапии. Акушерский гинекол .
1990; 76: 28–32.
28. Миллар Л.К.,
Крыло DA,
Пол RH,
Граймс Д.А.Амбулаторное лечение пиелонефрита при беременности: рандомизированное контролируемое исследование. Акушерский гинекол .
1995; 864 пт 1560–4.
29. Крыло DA,
Хендершотт CM,
Debuque L,
Миллар LK.
Рандомизированное испытание трех схем приема антибиотиков для лечения пиелонефрита у беременных. Акушерский гинекол .
1998. 92: 249–53.
30. Loughlin KR.
Управление урологическими проблемами во время беременности. Урология .1994; 44: 159–69.
31. Мид П.Дж.,
Харрис RE.
Заболеваемость бета-гемолитическим стрептококком группы В при инфекциях мочевыводящих путей в дородовом периоде. Акушерский гинекол .
1978; 51: 412–4.
32. Пройти MA,
Серый БМ,
Диллон ХК младший
Послеродовые и перинатальные инфекции, вызванные стрептококками группы B. Am J Obstet Gynecol .
1982; 143: 147–52.
33. Моллер М,
Томсен AC,
Борч К,
Динесен К,
Здравкович М.Разрыв плодных оболочек и преждевременные роды, связанные со стрептококками группы B в моче беременных. Ланцет .
1984; 2839469–70.
34. McKenzie H,
Доннет М.Л.,
Хауи П.В.,
Пател Н.Б.,
Бенви Д.Т.
Риск преждевременных родов у беременных со стрептококковыми инфекциями мочевыводящих путей группы B или мочевыми антителами к антигенам стрептококков группы B и E. coli. Br J Obstet Gynaecol .
1994; 101: 107–13.
35.Томсен AC,
Morup L,
Hansen KB.
Удаление антибиотиков стрептококков группы B с мочой для предотвращения преждевременных родов. Ланцет .
1987; 18533591–3.
36. Профилактика перинатальной стрептококковой болезни группы B: перспективы общественного здравоохранения. Центры по контролю и профилактике заболеваний . MMWR Morb Mortal Wkly Rep .
1996; 45: 1–24 [опечатка опубликована в MMWR Morb Mortal Wkly Rep 1996; 45 (31): 679].
37. Пфау А,
Мешки ТГ.Эффективная профилактика рецидивирующих инфекций мочевыводящих путей во время беременности. Клиническая инфекция .
1992; 14: 810–4.
38. Диокно АЦ,
Комптон А,
Сески Дж.,
Винсон Р.
Урологическая оценка инфекции мочевыводящих путей во время беременности. J Репрод Мед .
1986; 31: 23–6.
39. Шьеве Л.А.,
Обработчик A,
Хершоу Р,
Перский В,
Дэвис Ф.
Инфекция мочевыводящих путей во время беременности: ее связь с материнской заболеваемостью и перинатальным исходом.
