Кандидоз новорожденных: Молочница у грудных детей во рту
Молочница у грудных детей. Что такое Молочница у грудных детей?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Молочница – это одна из клинических вариаций грибковых заболеваний, вызванных дрожжеподобными грибами из рода Candida. У грудных детей чаще всего встречается оральная форма – кандидозный стоматит. Клинические проявления включают в себя белый творожистый налет на слизистых оболочках щек, языка и неба. В тяжелых случаях поражается вся ротовая полость, нарушается общее состояние ребенка. Диагностика предполагает выявление специфических симптомов при осмотре, подтверждение диагноза микроскопическим, бактериологическим и культуральным методами. Лечение проводится при помощи местного и системного применения антимикотических препаратов.
- Причины молочницы у грудных детей
- Симптомы молочницы у грудных детей
- Осложнения молочницы у грудных детей
- Диагностика молочницы у грудных детей
- Лечение молочницы у грудных детей
- Прогноз и профилактика молочницы у грудных детей
- Цены на лечение
Общие сведения
Кандидоз или молочница у грудных детей – грибковая патология, которая обусловлена условно-патогенными или патогенными штаммами грибов рода Candida. В 80-90% ее случаев возбудителем является C. albicans. Для новорожденных и младенцев наиболее характерен кандидоз полости рта. Впервые кандидозный стоматит был описан Гиппократом в примерно 400 году д.н.э. Название «молочница» патология получила из-за белого налета на слизистых оболочках, который внешне напоминает створоженное молоко, а также из-за творожистых выделений. Заболеваемость зависит от снижения иммунитета на фоне основных патологий или внешних обстоятельств: кандидоз развивается у 20-25% детей с сахарным диабетом I типа, у 25-30% онкологических больных и у 70-90% младенцев со СПИД.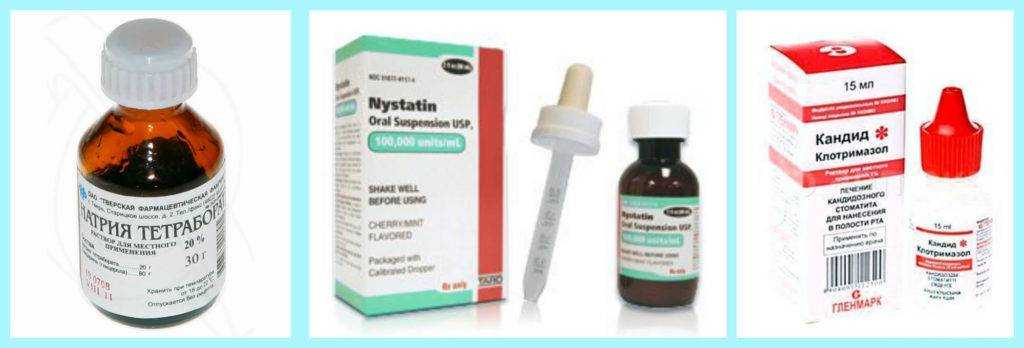
Молочница у грудных детей
Причины молочницы у грудных детей
Причиной молочницы у грудных детей, как и у взрослых, являются грибы из рода Candida. Чаще всего в роли возбудителя выступает C. albicans, реже – C. tropicalis, C. parapsilosis, C. glabrata, C. krusei. Данные дрожжеподобные грибы входят список условно-патогенных агентов, поскольку содержатся в нормальной микрофлоре полости рта и тонкой кишки. При полноценной работе иммунной системы негативного влияния они не оказывают. На фоне снижения резистентности организма грибы начинают интенсивно расти и размножаться, повреждая при этом слизистую оболочку и подлежащие ткани.
Способствовать развитию молочницы у грудных детей могут многие экзо- и эндогенные факторы. К внутренним факторам относятся недоношенность, вскармливание смесями, перенесенные операции, гипо- и авитаминозы, алиментарные дистрофии, анемии, рахит, нарушение нормальной кишечной микрофлоры, ОРВИ, хронические вирусные заболевания (в т. ч. ВИЧ), нарушения обмена белков, жиров и углеводов, эндокринные патологии (в т. ч. сахарный диабет), злокачественные новообразования, частые срыгивание и рвота. Внешними факторами, провоцирующими развитие кандидоза, являются химическое или физическое повреждение слизистой оболочки, длительная антибактериальная терапия, прием иммуносупрессивных препаратов, гормональных средств и цитостатиков, кандидозный вульвовагинит во время беременности и/или родов у матери, контакт с больными кандидозом или носителями патогенных штаммов, проведение ИВЛ и нахождение в условиях отделения РИТ.
ч. ВИЧ), нарушения обмена белков, жиров и углеводов, эндокринные патологии (в т. ч. сахарный диабет), злокачественные новообразования, частые срыгивание и рвота. Внешними факторами, провоцирующими развитие кандидоза, являются химическое или физическое повреждение слизистой оболочки, длительная антибактериальная терапия, прием иммуносупрессивных препаратов, гормональных средств и цитостатиков, кандидозный вульвовагинит во время беременности и/или родов у матери, контакт с больными кандидозом или носителями патогенных штаммов, проведение ИВЛ и нахождение в условиях отделения РИТ.
Симптомы молочницы у грудных детей
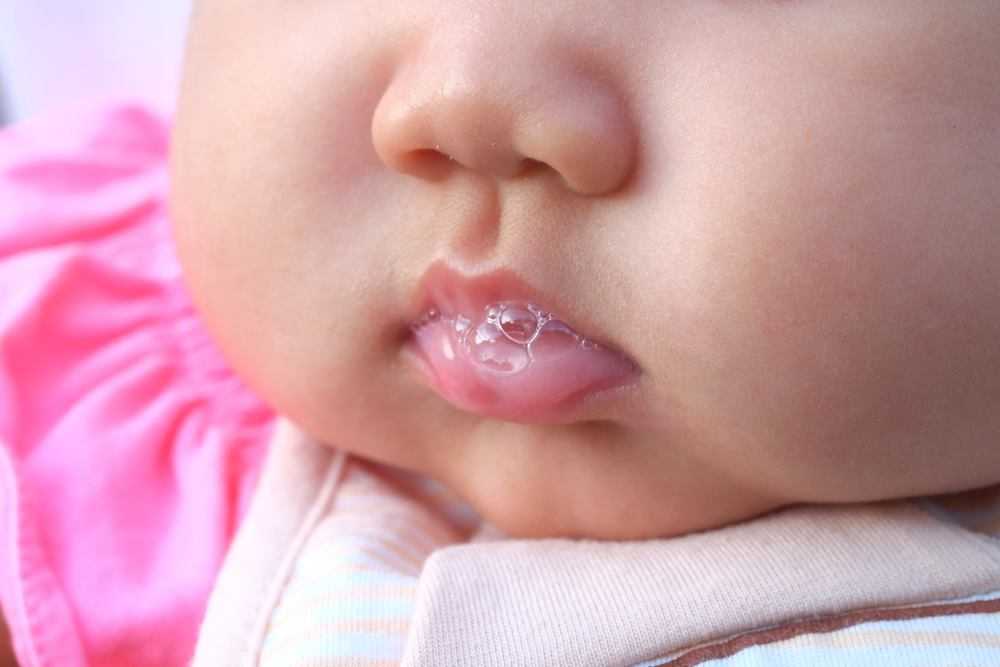
Инкубационный период молочницы у грудных детей колеблется от 2 дней до 2 месяцев, в среднем составляет 3-6 дней. Клиническая картина зависит от тяжести поражения. Выделяют легкую, среднетяжелую и тяжелую формы кандидозного стоматита. Легкая форма встречается чаще всего. Она характеризуется поражением ротовой полости в виде очагов творожистого налета. Наиболее частая локализация – внутренняя поверхность щек, верхняя часть языка, реже – твердое и мягкое небо. Образования без усилий отделяются при соскабливании. Общее состояние ребенка не нарушается, дискомфорта не возникает, специфического запаха не наблюдается.
Наиболее частая локализация – внутренняя поверхность щек, верхняя часть языка, реже – твердое и мягкое небо. Образования без усилий отделяются при соскабливании. Общее состояние ребенка не нарушается, дискомфорта не возникает, специфического запаха не наблюдается.
Среднетяжелая и тяжелая формы молочницы грудных детей менее распространены, поскольку развиваются только при отсутствии регулярных профилактических осмотров педиатром или сознательном отказе родителей от лечения. Кандидозный стоматит средней степени тяжести проявляется налетом творожистого или пленкоподобного характера, диффузно распространяющимся по всем типичным местам поражения. Прилегающие ткани резко гиперемированы. При попытке отделить налет от слизистой оболочки снимаются только некоторые его части, на месте которых остаются капли крови. Несколько нарушается общее состояние: сон неспокойный, ребенок капризничает.
При тяжелой форме молочницы у грудных детей выявляется тотальное поражение всех слизистых оболочек ротовой полости, в том числе задней стенки глотки, десен, губ. Налет плотно спаян с подлежащими тканями, поэтому при соскабливании удается отделить только небольшие участки, под которыми остается беловатая пленка. При осмотре изо рта определяется сильный неприятный запах. Резко нарушается общее состояние ребенка: он беспокоен, плохо спит, часто плачет, отказывается от груди матери.
Налет плотно спаян с подлежащими тканями, поэтому при соскабливании удается отделить только небольшие участки, под которыми остается беловатая пленка. При осмотре изо рта определяется сильный неприятный запах. Резко нарушается общее состояние ребенка: он беспокоен, плохо спит, часто плачет, отказывается от груди матери.
Осложнения молочницы у грудных детей
У детей, в отличие от взрослых, отмечается тенденция к быстрому развитию и распространению патологических процессов. Из-за этого кандидозный стоматит достаточно часто сопровождается поражением других участков тела – возникают кандидозы промежности, кишечника, межъягодичной и пахово-бедренной складки, кандидозный вульвовагинит. При тяжелых формах молочницы у грудных детей зачастую происходит гематогенная и лимфогенная диссеминация грибов – развивается сепсис. Неэффективное лечение острого кандидоза может привести к его переходу в хроническую форму. Помимо постоянных обострений и нарушений общего состояния ребенка, данное состояние становится причиной дальнейшего снижения иммунитета, склонности к аллергическим реакциям и атопическим заболеваниям, например – бронхиальной астме.
У девочек на фоне молочницы ротовой полости очень часто развивается кандидозный вульвовагинит. Клинически он проявляется гиперемией, отечностью и сухостью внешних половых органов с эрозиями слизистых оболочек. В педиатрии и неонатологии данная патология представляет большую опасность, поскольку в грудном возрасте из-за особой нежности тканей существует высокий риск срастания половых губ и стенок влагалища между собой. Подобное осложнение, помимо массивной фармакотерапии, требует хирургического вмешательства.
Диагностика молочницы у грудных детей
Диагностика молочницы у грудных детей основывается на полноценном сборе анамнестических данных, проведении объективного и лабораторного обследования ребенка. Инструментальные исследования, как правило, не требуются. При сборе анамнеза педиатр устанавливает этиологические и способствующие факторы, определяет время дебюта заболевания, оценивает особенности состояния ребенка. Специалист обязательно обращает внимание на грибковые патологии матери во время беременности и родов. Физикальное обследование включает в себя тщательный осмотр ротовой полости, выявление характерных налетов, определение степени тяжести процесса и осмотр других частей тела, на которых потенциально может развиться кандидоз. Ведущую роль играет лабораторная диагностика, заключающаяся в проведении микроскопии, бактериологического и серологического исследования.
Физикальное обследование включает в себя тщательный осмотр ротовой полости, выявление характерных налетов, определение степени тяжести процесса и осмотр других частей тела, на которых потенциально может развиться кандидоз. Ведущую роль играет лабораторная диагностика, заключающаяся в проведении микроскопии, бактериологического и серологического исследования.
Микроскопическая диагностика является первым этапом, на котором полученный при соскобе материал исследуют под световым или электронным микроскопом. Она дает возможность выявить характерные нити мицелия и дрожжеподобные клетки. Культуральный метод позволяет определить разновидность гриба и его чувствительность к конкретным антимикотическим препаратам. Этот метод также используется при неэффективности стартового эмпирического лечения распространенными средствами. Серологические реакции (чаще всего – РСК) показаны при отсутствии четкой клинической картины и низкой информативности других исследований. На основе вышеупомянутых исследований проводится дифференциальная диагностика кандидозного стоматита с острым тонзиллитом, дифтерией и острым герпетическим стоматитом у детей.
Лечение молочницы у грудных детей
Лечение молочницы у грудных детей зависит от распространенности патологического процесса. На ранних стадиях, при локальном поражении показана местная терапия – выполняется орошение ротовой полости противокандидозными (клотримазол, нистатин) ощелачивающими (2% раствор пищевой соды, 0,25% борный раствор) и дезинфицирующими (анилиновые красители – раствор Люголя, метиленовый синий) средствами. При грудном вскармливании показана обработка груди матери 2% содовым раствором и травяными настоями (дуб, календула и другие). Подобное лечение проводится до полного выздоровления ребенка, но сроком не менее 14 суток.
При среднетяжелых и тяжелых формах рекомендуется системная терапия путем перорального или парентерального введения антимикотических препаратов. При применении противокандидозных препаратов через рот отдается предпочтение порошкам для инъекций (флуконазол), так как приготовленный раствор оказывает не только общее, но и местное воздействие на слизистые оболочки ротовой полости.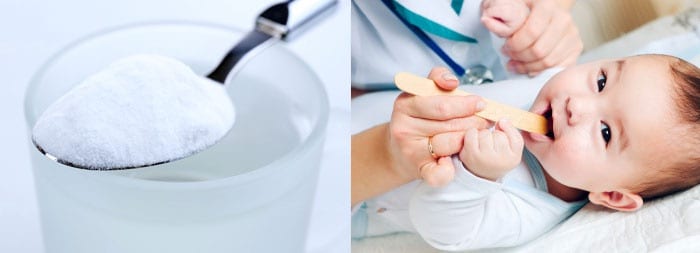 Параллельно в полном объеме осуществляется лечение сопутствующих заболеваний и симптоматическая терапия по показаниям. Согласно современным рекомендациям, такой подход следует использовать и при легких формах, поскольку он позволяет сократить сроки лечения до 3-6 суток.
Параллельно в полном объеме осуществляется лечение сопутствующих заболеваний и симптоматическая терапия по показаниям. Согласно современным рекомендациям, такой подход следует использовать и при легких формах, поскольку он позволяет сократить сроки лечения до 3-6 суток.
Прогноз и профилактика молочницы у грудных детей
Прогноз при молочнице у грудных детей благоприятный. При своевременной рациональной терапии полное выздоровление наступает на протяжении 7-10 дней. Тяжелые формы и развитие осложнений наблюдаются только на фоне полного отсутствия противогрибкового лечения. Неспецифическая профилактика кандидозного стоматита заключается в полноценном уходе за кожей и слизистыми оболочками ребенка, особенно – на фоне тяжелых патологий, снижающих иммунитет. Важная роль отводится рациональному приему антибактериальных средств и лечению грибковых заболеваний у матери в период вынашивания ребенка.
Специфическая профилактика молочницы у грудных детей необходима при наличии показаний, которые включают в себя отягощенный акушерский и гинекологический анамнез матери, недоношенность и внутриутробные пороки развития ребенка, дыхательные расстройства, родовые травмы новорожденных, патологии ЦНС. Новорожденным, входящим в эту группу, первые 7 дней жизни проводится микроскопия и бактериология образцов слизистых оболочек и кала. Для младенцев, находящихся на антибактериальной терапии, назначается профилактический курс противогрибкового препарата, как правило – флуконазола.
Новорожденным, входящим в эту группу, первые 7 дней жизни проводится микроскопия и бактериология образцов слизистых оболочек и кала. Для младенцев, находящихся на антибактериальной терапии, назначается профилактический курс противогрибкового препарата, как правило – флуконазола.
Вы можете поделиться своей историей болезни, что Вам помогло при лечении молочницы у грудных детей.
Источники
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Кандидоз у новорождённых с очень низкой массой тела при рождении
Аннотация
На базе данных Medline и Cochrane проанализирована литература по проблеме кандидоза у новорождённых с очень низкой массой тела при рождении (<1500 г). В анализ не вошли исследования по кандидозу у доношенных новорождённых и детей старше периода новорождённости, а также данные по колонизации Candida spp. слизистых оболочек. В статье приводятся наиболее распространённые классификации кандидоза в неонатологии, данные по его частоте и эпидемиологии. Указаны достоверные факторы риска для основных клинических форм кандидоза: врождённого, кандидоза кожи и слизистых и острого диссеминированного кандидоза. С позиций клинической фармакологии и доказательной медицины проведён анализ применения системных антимикотиков для лечения и профилактики инвазивного кандидоза.
В анализ не вошли исследования по кандидозу у доношенных новорождённых и детей старше периода новорождённости, а также данные по колонизации Candida spp. слизистых оболочек. В статье приводятся наиболее распространённые классификации кандидоза в неонатологии, данные по его частоте и эпидемиологии. Указаны достоверные факторы риска для основных клинических форм кандидоза: врождённого, кандидоза кожи и слизистых и острого диссеминированного кандидоза. С позиций клинической фармакологии и доказательной медицины проведён анализ применения системных антимикотиков для лечения и профилактики инвазивного кандидоза.
Колбин Алексей Сергеевич
Шабалов Н.П.
Климко Николай Николаевич
0000-0001-6095-7531
1.
Groll A.H., Walsh T.J. Fungal infections in the pediatric patient. In: Anaissie E.
 J., McGinnis M.R., Pfaller M.A, editors. Clinical mycology. – 1st ed. New York: Churchill Livingstone; 2003. p. 417-42.
J., McGinnis M.R., Pfaller M.A, editors. Clinical mycology. – 1st ed. New York: Churchill Livingstone; 2003. p. 417-42.2.
Самсыгина Г.А., Буслаева Г.Н. Кандидоз новорожденных и детей первого года жизни. Пособие для врачей. — М.: Изд-во «Печатный город»; 2004. — 63 с.
3.
Kaufman D., Fairchild K.D. Clinical microbiology of bacterial and fungal sepsis in very-low-birth-weight infants. Clin Microbiol Rev 2004; 17:638-80.
4.
Lee B.E., Cheung P., Robinson J.L., et al. Comparative study of mortality and morbidity in premature infants (<1250 g) with candidemia or candidal meningitis. Clin Infect Dis 1998; 27:559-65.
5.

Романюк Ф.П., Шабалов Н.П. Неонатальный кандидоз. Педиатрия. 1995; 3:77-81.
6.
Ascioglu S., Rex J.H., Pauw B., et al. Defining opportunistic invasive fungal infections in immunocompromised patients with cancer and hematopoietic stem cell transplant: an international consensus. Clin Infect Dis 2002; 34:7-14.
7.
Whyte R.K.Z., Hussain D. Antenatal infections with Candida species. Arch Dis Child 1982; 57:528-35.
8.
Романюк Ф.П. Микозы у детей, вызываемые условнопатогенными грибами: Автореф. дис. …. д-ра мед. наук. СПб, 1998. 44с.
9.
Johnson D.
 E., Thompson T.R., Ferrieri P. Congenital candidiasis. Am J Dis Child 1981; 135:273-5.
E., Thompson T.R., Ferrieri P. Congenital candidiasis. Am J Dis Child 1981; 135:273-5.10.
Darmstadt G.L., Dinulos J.G., Miller Z. Congenital cutaneous candidiasis: clinical presentation, pathogenesis, and management guidelines. Pediatrics 2000; 105:438- 44.
11.
Faix R.G., Kovarik S.M., Shaw T.R., et al. Mucocutaneuous and invasive candidiasis among very low birth weight infants in intensive care nurseries: a prospective study. Pediatrics 1989; 83:101-7.
12.
Baley J.E., Silverman R.A. Systemic candidiasis: cutaneous manifestations in low birth weight infants. Pediatrics 1988; 82:211-5.
13.

Baley I.E., Kliegman R.M., Fanaroff A.A. Disseminated fungal infections in very low-birth-weight infants: therapeutic toxicity. Pediatrics 1984; 73:153-7.
14.
Juster-Reicher A., Leibovitz E., Linder N., et al. Liposomal amphotericin B (AmBisome) in very low birth weight infants. Infection 2000; 28: 223-6.
15.
Saiman L., Ludington E., Pfaller M., et al. Risk factors for candidemia in Neonatal Intensive Care Unit patients. The National Epidemiology of Mycosis Survey study group. Pediatr Infect Dis J 2000; 19:319-24.
16.
Melviller C., Kempley S., Graham J., et al. Early onset systemic Candida infection in extremely preterm neonates.
 Eur J Pediatr 1996; 155:904-6.
Eur J Pediatr 1996; 155:904-6.17.
Baley J.E. Kliegman R.M., Boxerbaum B., et al. Fungal colonization in the very low birth weight infant. Pediatrics 1986; 78:225-32.
18.
Hageman J.R., Stenskle J., Keuler H., et al. Candida colonization and infection in very low birth weight infants. J Perinatol 1985; 6:251-4.
19.
Kaufman D., Boyle R., Hazen K.C., et al. Fluconazole prophylaxis against fungal colonization and infection in preterm infants. N Engl J Med 2001; 345:1660-6.
20.
Kicklighter S.D., Springer S.C., Cox T., et al. Fluconazole for prophylaxis against candidal rectal colonization in the very low birth weight infant.
 Pediatrics 2001 Feb; 107:293-8.
Pediatrics 2001 Feb; 107:293-8.21.
Kossoff E., Buescher E.S., Karlowicz M.G. Candidemia in a neonatal intensive care unit: trends fifteen years and clinical features of 111 cases. Pediatr Infect Dis J 1998; 17:504-8.
22.
Stoll B.J., Gordon T., Korones S.B. Late-onset sepsis in very low birht weight neonates: a report from the National Institute of Child Health and Human Development neonatal research network. J Pediatr 1996; 129:63-71.
23.
Stoll B.J., Hansen N., Fanaroff L., et al. Late-onset sepsis in very low birht weight neonates: the experience of the NICHD Neonatal Research Network. Pediatrics 2002; 110:285-91.
24.

Stoll B.J., Hansen N., Fanaroff A.A., et al. To tap or not to tap: high likelihood of meningitis without sepsis among very low birth weight infants. Pediatrics 2004; 113:1181-6.
25.
Makhoul I.R., Sujov P., Smolkin T., et al. Epidemiological, clinical, and microbiological characteristics of late-onset sepsis among very low birth weight infants in Israel: a national survey. Pediatrics 2002; 109:34-9.
26.
Benjamin D.K. Jr, Poole C., Steinbach W.J., et al. Neonatal candidemia and end-organ damage: a critical appraisal of the literature using meta-analytic techniques. Pediatrics 2003; 112:634-40.
27.
Колбин А.С., Шабалов Н.
 П., Любименко В.А., Климко Н.Н. Факторы риска развития кандидемии у недоношенных со сроком гестации менее 32 недель. Клиническая Микробиология и Антимикробная Химиотерапия 2005; 7:97-102.
П., Любименко В.А., Климко Н.Н. Факторы риска развития кандидемии у недоношенных со сроком гестации менее 32 недель. Клиническая Микробиология и Антимикробная Химиотерапия 2005; 7:97-102.28.
Kaufman D., Boyle R., Hazen K.C., et al. Fluconazole prophylaxis against fungal colonization and infection in preterm infants. N Engl J Med 2001; 345:1660-6.
29.
Pappu-Katikaneni L.D., Rao K.P., Banister E. Gastrointestinal colonization with yeast species and Candida septicemia in very low birth weight infants. Mycoses 1990; 33:20-3.
30.
Rowen J.L., Rench M.A., Kozinetz C.A., et al. Endotracheal colonization with Candida enhances risk of systemic candidiasis in very low birth weight neonates.
 J Pediatr 1994; 124:789-94.
J Pediatr 1994; 124:789-94.31.
Sherertz R.J., Gledhill K.S., Hampton K.D., et al. Outbreak of Candida bloodstream infections associated with retrograde medication administration in a neonatal intensive care unit. J Pediatr 1992; 120:455-61.
32.
Gustafson K.S., Vercellotti G.M., Bendel C.M., et al. Molecular mimicry in Candida albicans. Role of an integrin analogue in adhesion of the yeast to human endothelium. J Clin Invest 1991; 87:1896-902.
33.
Jourdain B., Novara A., Joly-Guillou M.L., et al. Role of quantitative cultures of endotracheal aspirates in the diagnosis of nosocomial pneumonia. Am J Respir Crit Care Med 1995; 152:241-6.
34.

Faix R.G. Invasive neonatal candidiasis: comparison of albicans and parapsilosis infection. Pediatr Infect Dis J 1992; 11:88-93.
35.
Pfaller M.A. Nosocomial candidiasis: emerging species, reservoirs, and modes of transmission. Clin Infect Dis 1996; 22(Suppl. 2):S89-94.
36.
Fairchild K.D., Tomkoria S., Sharp E.C., et al. Neonatal Candida glabrata sepsis: clinical and laboratory features compared with other Candida species. Pediatr Infect Dis J 2002; 21:39-43.
37.
Guida J.D., Kunig A.M., Leef K.H., et al. Platelet count and sepsis in very low birth weight neonates: is there an organism-specific response? Pediatrics 2003; 111:1411-5.

38.
Chapman R.L. Candida infections in the neonate. Curr Opin Pediatr 2003; 15:97-102.
39.
Fanaroff A.A., Korones S.B., Wright L.L. Incidence, presenting features, risk factors and significance of late onset septicemia in very low birth weight infants. Pediatr Infect Dis J 1998; 17:593-8.
40.
Колбин А.С., Шабалов Н.П., Климко Н.Н. Эффективность и безопасность применения системных противогрибковых препаратов у новорожденных. Российский вестник перинатологии и педиатрии 2005; 1:42-48.
41.
Frattarelli D.A.C., Reed M.D., Giacoia G.P., et al.
 Antifungals in systemic neonatal candidiasis. Drugs 2004; 64:949- 68.
Antifungals in systemic neonatal candidiasis. Drugs 2004; 64:949- 68.42.
Red Book: 2003 Report of the Committee on Infectious Diseases. 26th ed. Elk Grove Village, IL: American Academy of Pediatrics. Candidiasis. In: Pickering L.K., editor. 2003:229-32.
43.
Современная терапия в неонатологии. Под редакцией Н.П. Шабалова. Справочник. Перевод с английского. М.: МЕДпресс; 2000. 262 с.
44.
Driessen M., Ellis J., Cooper P., et al. Fluconazole vs. Amphotericin B for the treatment of neonatal fungal septicemia: a prospective randomized trial. Pediatr Infect Dis J 1996; 15:1107-12.
45.

da Silva L.P., Amaral J.M., Ferreira N.C. Which is most appropriate dosage of liposomsl amphotericin B (AmBisome) for the treatment of fungal infectionsin infants of very low birth weight? Pediatrics 1993; 91:1217-8.
46.
Lopez Sastre J.B., Coto Cotallo G.D., et al. Neonatal invasive candidiasis: a prospective multicenter stusy of 118 cases. Am J Perinatol 2003; 20:153-63.
47.
Isacson M., Faber N.J., Herishano Y., et al. Use of 5-fluorocytosine in systemic candidiasis in infancy. Arch Dis Child 1972; 47:954-9.
48.
Faix R.G. Systemic Candida infections in infants in intensive care nurseries: high incidence of central nervous system involvement.
 J Pediatr 1984; 105:616-22.
J Pediatr 1984; 105:616-22.49.
Wyble L.E., Gal P., Ransom J.L., et al. Fluconazole use and pharmacokinetics in three premature neonates. Pharmacotherapy 1991; 11:269-70.
50.
Krzeska I., Yeats R.A., Pfaff G. Single dose intravenous pharmacokinetics of fluconazole in infants. Drugs Exp Clin Res 1993; 19:267-71.
51.
Saxen H., Hoppu K., Pohjavuori M. Pharmacokinetics of fluconazole in very low birth weight infants during the first two weeks of life. Clin Pharmacol Ther 1993; 54:269- 77.
52.
Wong S.F., Leung M.P., Chan M.Y. Pharmacokinetics of fluconazole in children requiring peritoneal dialysis.
 Clin Ther 1997; 19:1039-47.
Clin Ther 1997; 19:1039-47.53.
Wenzl T.G., Schefels J., Hornchen H., et al. Pharmacokinetics of oral fluconazole in premature infants. Eur J Pediatr 1998; 157:661-2
54.
Kicklighter S.D. Antifungal agents and fungal prophylaxis in the neonat. NeoReviews 2002; 3:249-55.
55.
McGuire W., Clerihew L., Austin N. Prophylactic intravenous antifungal agents to prevent mortality and morbidity in very low birth weight infants (Cochrane Review). In: The Cochrane Library, Issue 1 2003. Oxford: Update Software.
56.
Колбин А.С., Иванов Д.О., Любименко В.
 А. Карпов О.И., Климко Н.Н. Профилактическое и эмпирическое использование антифунгальных препаратов у новорожденных. Клин микроб антимикроб химиотер 2003; 5:354-9.
А. Карпов О.И., Климко Н.Н. Профилактическое и эмпирическое использование антифунгальных препаратов у новорожденных. Клин микроб антимикроб химиотер 2003; 5:354-9.57.
Sims M.E., Yoo Y., You H., et al. Prophylactic oral nystatin and fungal infections in very-low-birthweight infants. Am J Perinatol 1988; 5:33-6.
58.
Wainer S., Cooper P.A., Funk E., et al. Prophylactic miconazole oral gel for the prevention of neonatal fungal rectal colonization and systemic infection. Pediatr Infect Dis J 1992; 11:713-6.
2023 Код диагноза по МКБ-10 P37.5: Кандидоз новорожденных
- Коды МКБ-10-СМ
- Р00-Р96
- П35-П39
- Р37-
- 2023 Код диагноза по МКБ-10-CM P37.
 5
5
›
›
›
›
Кандидоз новорожденных
- 2016 2017 2018 2019 2020 2021 2022 2023 Оплачиваемый/конкретный код Код в записи о новорожденном
- P37.5 — это оплачиваемый/специфический код МКБ-10-CM, который можно использовать для обозначения диагноза в целях возмещения расходов.
- Редакция МКБ-10-КМ P37.5 2023 г. вступила в силу 1 октября 2022 г.
- Это американская версия P37.5 ICD-10-CM. Другие международные версии P37.5 ICD-10 могут отличаться.
Правила кодирования МКБ-10-КМ
- P37.5 следует использовать в карте новорожденного, а не в карте матери.
Следующие коды выше P37.5 содержат обратные ссылки на аннотации
Обратная ссылка на аннотацию
В этом контексте обратные ссылки на аннотацию относятся к кодам, которые содержат:
- Применимо к аннотациям или
- Код Также аннотации , или
- Code First аннотации, или
- Exclude1 аннотации, или
- Исключает2 аннотации, или
- Включает аннотации, или
- Примечания к примечаниям, или
- Используйте дополнительные аннотации
, которые могут быть применимы к P37. 5:
5:
- P00-P96
2023 ICD-10-CM Диапазон P00-P96
Определенные состояния, возникающие в перинатальном периоде
Включает
- состояния, возникающие во внутриутробном или перинатальном периоде (до рождения в течение первых 28 дней) после рождения), даже если заболеваемость возникает позже
Примечание
- Коды из этой главы предназначены только для записей новорожденных, никогда не используются для записей матерей
Тип 2 Исключает
- врожденные пороки развития, деформации питания и хромосомные аномалии (Q00-Q004) 90-Q904 болезни обмена веществ (E00-E88)
- травмы, отравления и некоторые другие последствия внешних причин (S00-T88)
- новообразования (C00-D49)
- столбняк новорожденных (A33)
Определенные состояния, возникающие в перинатальном периоде
- P35-P39
2023 ICD-10-CM Диапазон P35-P39
Инфекции, специфичные для перинатального периода
Применимо к
- Инфекции, приобретенные через пупок, во время родов или в течение первых 28 дней после рождения
Тип 2 Исключая
- бессимптомный статус инфекции вирусом иммунодефицита человека [ВИЧ] (Z21)
- врожденная гонококковая инфекция (A54.
 -)
-) - врожденная пневмония (P23.-)
- врожденный сифилис (A50.-)
- болезнь, вызванная вирусом иммунодефицита человека [ВИЧ] (B20)
- младенческий ботулизм (A48.51)
- инфекционные болезни, неспецифические для перинатального периода ( A00-B99, J09, J10.-)
- кишечные инфекционные заболевания (A00-A09)
- лабораторные признаки вируса иммунодефицита человека [ВИЧ] (R75)
- столбняк новорожденных (A33)
Инфекции, специфичные для перинатального периода
- P37
ICD-10-CM Diagnosis Code P37
Other congenital infectious and parasitic diseases
- 2016 2017 2018 2019 2020 2021 2022 2023 Non-Billable/Non-Specific Code
Type 2 Excludes
- congenital syphilis (A50 .-)
- инфекционная диарея новорожденных (А00-А09)
- некротизирующий энтероколит новорожденных (Р77.-)
- неинфекционная диарея новорожденных (Р78.
 3)
3) - офтальмия новорожденных, вызванная гонококком (А54.31)
- Столбняк новорожденных (А33)
Другие врожденные инфекционные и паразитарные болезни
Примерные синонимы
- Монилиоз новорожденных
- Молочница новорожденных
ICD-10-CM P37.5 сгруппирован в группу (группы), связанные с диагностикой (MS-DRG v40.0):
- 794 Новорожденный с другими серьезными проблемами
Преобразовать P37.5 в МКБ-9-СМ
История кода
- 2016 (действует с 01.10.2015) : Новый код (первый год непроектной МКБ-10-КМ)
- 2017 (действует с 01.10.2016) : Без изменений
- 2018 (действует с 01.10.2017) : без изменений
- 2019 (действует с 01.
 10.2018) : без изменений
10.2018) : без изменений - 2020 (действует с 01.10.2019)) : Без изменений
- 2021 (действует с 01.10.2020) : Без изменений
- 2022 (действует с 01.10.2021) : Без изменений
- 2023 (действует с 01.10.2022) : Без изменений
Кодовые аннотации, содержащие обратные ссылки на P37.5:
Записи указателя диагнозов, содержащие обратные ссылки на P37.5:
- Кандидоз, кандидозный B37.9
Код диагноза по МКБ-10 B37.9
Candidiasis, unspecified
- 2016 2017 2018 2019 2020 2021 2022 2023 Billable/Specific Code
Applicable To
- Thrush NOS
- congenital P37.5
- neonatal P37.5
- Infection, infected, инфекционная (оппортунистическая) B99.9
Код диагноза по МКБ-10 B99.
 9
9Инфекционная болезнь неуточненная
- 2016 2017 2018 2019 2020 2021 2022 2023 Платежный/специфический код
- Moniliasis B37.9-См. Также Candidiasis
ICD-10-CM Код диагностики B37.9
Candidiasis, неопределенное
- 2016 2017 2018 2019 2020 2021 2022 2023 Billable/Special Code
Применимый к
- 9
- 40004 40004 40004 40004.ship.
- неонатальный P37.5
- Новорожденный (младенец) (живорожденный) (одноплодный) Z38.2
Код диагноза по МКБ-10 Z38.2
Одинокий живорожденный, место рождения не указано
7 2018 20192020 2021 2022 2023 Billable/Specific Code Newborn/Neonate Dx (0 years) POA Exempt
Applicable To
- Single liveborn infant NOS
- 40004 40004 40004 40004.ship.
- Thrush — see also Candidiasis
- newborn P37.5
Коды МКБ-10-СМ, соседние с P37. 5
5
P36.4 Сепсис новорожденного, вызванный Escherichia coli
P36.5 Сепсис новорожденного, вызванный анаэробами
P36.8 Другие бактериальные сепсисы новорожденных
P36.9 Бактериальный сепсис новорожденного неуточненный
P37 Другие врожденные инфекционные и паразитарные болезни
P37. 0 Врожденный туберкулез
0 Врожденный туберкулез
P37.1 Врожденный токсоплазмоз
P37.2 Неонатальный (диссеминированный) листериоз
P37.3 Врожденная малярия falciparum
P37.4 Другая врожденная малярия
P37.5
Неонатальный кандидоз
P37. 8 Другие уточненные врожденные инфекционные и паразитарные болезни
8 Другие уточненные врожденные инфекционные и паразитарные болезни
P37.9 Врожденная инфекционная или паразитарная болезнь неуточненная
P38 Омфалит новорожденных
P38.1 Омфалит со слабым кровоизлиянием
P38.9 Омфалит без кровоизлияний0028
P39 Другие инфекции, специфичные для перинатального периода
P39. 0 Инфекционный мастит новорожденных
0 Инфекционный мастит новорожденных
Р39.1 Неонатальный конъюнктивит и дакриоцистит
P39.2 Внутриамниотическая инфекция новорожденного, не классифицированная в других рубриках
P39.3 Неонатальная инфекция мочевыводящих путей0028
Требования о возмещении с датой вручения 1 октября 2015 г. или после этой даты требуют использования кодов МКБ-10-CM.
Кандидоз новорожденных — Doctor Fungus
Обзор
Инвазивный кандидоз у новорожденных является серьезной и относительно частой причиной позднего сепсиса, связанного с высокой смертностью. Обзор первых 26 случаев, описанных в английской литературе до 1984 г., показал уровень смертности 54{64e6c1a1710838655cc965f0e1ea13052e86759.7ac43370498029d1bc5831201} [1128]. Более свежие данные из (A): NICHD Центры неонатальной исследовательской сети сообщили о смертности 28,1 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} у новорожденных с фунгемией [2170].
Обзор первых 26 случаев, описанных в английской литературе до 1984 г., показал уровень смертности 54{64e6c1a1710838655cc965f0e1ea13052e86759.7ac43370498029d1bc5831201} [1128]. Более свежие данные из (A): NICHD Центры неонатальной исследовательской сети сообщили о смертности 28,1 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} у новорожденных с фунгемией [2170].
Недоношенные новорожденные и особенно младенцы с низкой массой тела при рождении нуждаются в инвазивных диагностических и агрессивных терапевтических вмешательствах, многие из которых повышают факторы риска развития инфекции Candida (см. ниже). Кроме того, незрелость иммунной системы, особенно у недоношенных новорожденных, которая в основном включает Т-клетки и нейтрофилы, еще больше предрасполагает эту популяцию к инфекциям [24–39].]. Действительно, было показано, что анти- Candida активность легочных макрофагов у новорожденных снижена [211, 770].
Кандидоз новорожденных можно разделить на две категории:
- Катетер-ассоциированная кандидемия
- Диссеминированный или инвазивный кандидоз
Кандидемия, связанная с катетером, относится к младенцам с установленными центральными сосудистыми катетерами и кандидемией, которая быстро разрешается после удаления катетера и начала терапии. Диссеминированный или инвазивный кандидоз относится к персистирующей кандидемии, если катетер был установлен и удален, и/или выделение Candida из других обычно стерильных участков тела. Однако, как и у взрослых, отсутствуют клинические критерии или диагностические тесты, позволяющие дифференцировать эти две группы при поступлении [351].
Диссеминированный или инвазивный кандидоз относится к персистирующей кандидемии, если катетер был установлен и удален, и/или выделение Candida из других обычно стерильных участков тела. Однако, как и у взрослых, отсутствуют клинические критерии или диагностические тесты, позволяющие дифференцировать эти две группы при поступлении [351].
До 75 случаев кандидоза новорожденных с инфекцией двух или более органов. Унифокальный остеомиелит, менингит и почечный кандидоз являются наиболее распространенными проявлениями, в противном случае инфекция любой комбинации крови, почек, мозговых оболочек, сердца, глаз, костей или суставов [1128].
Особая форма кожного кандидоза, которая может стать инвазивной и известна как (А): врожденный кандидоз, обсуждается отдельно ниже.
Эпидемиология
Частота инвазивного кандидоза в отделениях неонатальной помощи колеблется от 1,6 до 4,5 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} [164, 178]. Более свежие данные Центров неонатальных исследований NICHD по позднему сепсису у новорожденных с очень низкой массой тела при рождении показали, что грибковые патогены объясняют 9{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} всех инфекций кровотока [2170].
Новорожденные могут заразиться Candida путем вертикальной или нозокомиальной передачи [1885, 2346]. При вертикальной передаче заражение может произойти либо во время беременности, либо во время родов. В обоих случаях задействован восходящий путь из влагалища матери. Вагинальный кандидоз часто возникает у беременных, особенно в последнем триместре. Ставки до 56{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} [771].
Частота носительства Candida среди новорожденных колеблется от 30 до 60 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} [1720]. Интересно, что по мере снижения гестационного возраста частота кандидозной колонизации увеличивается [2088]. Приобретение Candida не всегда приводит к системной инфекции, но предшествующая колонизация является необходимым шагом перед возникновением инвазивного кандидоза.
Кандидозное нозокомиальное заражение признано очень важной формой передачи в отделении интенсивной терапии новорожденных (NICU) [1885]. Действительно, были выявлены важные вспышки кандидемии в отделениях интенсивной терапии [709, 731, 1880]. Такая колонизация на самом деле является общим явлением: было обнаружено, что частота ношения рук среди медицинских работников в семи отделениях интенсивной терапии интенсивной терапии в США составляет около 30 [1871].
Действительно, были выявлены важные вспышки кандидемии в отделениях интенсивной терапии [709, 731, 1880]. Такая колонизация на самом деле является общим явлением: было обнаружено, что частота ношения рук среди медицинских работников в семи отделениях интенсивной терапии интенсивной терапии в США составляет около 30 [1871].
Факторы риска неонатального кандидоза
| Факторы риска | Комментарии | Ссылки |
|---|---|---|
| Классический (также описан для взрослых) | ||
| Использование нескольких антибиотиков | Продолжительность лечения антибиотиками так же важна, как и спектр используемой схемы | [2392] |
| Центральные венозные катетеры | [2392] | |
| Парентеральное переедание и внутривенная жировая эмульсия | [2392] | |
| Колонизация Candida и/или предыдущий эпизод кожно-слизистого кандидоза | [710, 1720, 1978] | |
| Факторы риска, присущие только этой возрастной группе | ||
| Низкая масса тела при рождении | ~ 90{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} новорожденных с очень низкой массой тела при рождении (<1500 г) | [710] |
| Эндотрахеальные трубки и трахеостомии | У многих новорожденных имеется дыхательная недостаточность того или иного типа | [2392] |
| Периферийные венозные катетеры | Лейбовиц, 1992 № 512] | |
| Наиболее часто встречаются врожденные пороки развития, пороки развития ЖКТ и врожденные пороки сердца | Наиболее часто наблюдается у младенцев с массой тела > 2500 г при рождении с длительной госпитализацией в ОИТН | [1862] |
| Болезни желудочно-кишечного тракта | Некротический энтероколит и анатомические аномалии, требующие хирургического вмешательства | [710] |
Кандидоз новорожденных и
виды Candida
В первоначальных отчетах о кандидозе новорожденных постоянно указывалось, что Candida albicans ответственны за большинство случаев [351, 710]. Однако, подобно изменению эпидемиологических моделей, наблюдаемых у взрослых, среди новорожденных отмечается изменение спектра видов. Это изменение характеризуется прогрессирующим снижением скорости выделения Candida albicans и появление не- albicans видов [731, 1871]. Однако, в отличие от ситуации со взрослыми, именно Candida parapsilosis становится наиболее распространенным видом. В некоторых центрах он заменил C. albicans как наиболее часто встречающийся вид [1327].
Однако, подобно изменению эпидемиологических моделей, наблюдаемых у взрослых, среди новорожденных отмечается изменение спектра видов. Это изменение характеризуется прогрессирующим снижением скорости выделения Candida albicans и появление не- albicans видов [731, 1871]. Однако, в отличие от ситуации со взрослыми, именно Candida parapsilosis становится наиболее распространенным видом. В некоторых центрах он заменил C. albicans как наиболее часто встречающийся вид [1327].
| Артикул | Место | Н | Частота ({64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201}) для каждого вида Candida | ||||
|---|---|---|---|---|---|---|---|
| С. albicans | C. тропический | C. glabrata | C. parapsilosis | Другие | |||
| [710] | США | 16 | 88 | 0 | 0 | 12 | 0 |
| [351] | США | 30 | 73 | 13 | О | 10 | 1 (1) |
| [1315] | Израиль | 25 | 71 | 0 | 0 | 4 | 25 (2) |
| [1327] | США 1 центр | 35 | 26 | 3 | 0 | 68 | 3 |
| [1871] | США | 35 | 63 | – | 6 | 29 | 3 |
- Один случай C.
 lusitaniae
lusitaniae - Один ящик C.krusei
Клинические проявления
Классическая клиническая картина системного кандидоза у новорожденных неотличима от бактериального сепсиса [164]. Могут быть видны все следующие признаки:
- Нестабильность температуры
- Гипотония
- Ухудшение дыхания и апноэ
- Вздутие живота
- Положительный кал на гваяковую кислоту
- Непереносимость углеводов
Среди них дыхательная дисфункция и апноэ были наиболее частыми признаками в больших сериях, они присутствовали примерно в 70 случаях [2284].
У значительной части новорожденных одновременно проявляются локальные признаки кандидозной инфекции в одной или нескольких других локализациях:
- Кожа и слизистые оболочки Кожно-слизистый кандидоз у новорожденных может проявляться классической молочницей, опрелостями и/или любой разновидностью этой эритематозной сыпи с папулами и/или пустулами, поражающими обычно влажные кожные поверхности [710].
 Описаны также кожные абсцессы [13–15]. Однако наиболее частым проявлением является перинеальный кандидоз [7–10]. Важно подчеркнуть, что даже когда любая из этих форм кожно-слизистого кандидоза может предшествовать возникновению системного заболевания, это не является патогномоничным или обязательным состоянием. Проспективная оценка этой ассоциации показала, что 44{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} у новорожденных с инвазивным кандидозом никогда не развивались поражения кожи [710]. Однако тот же анализ показал, что у новорожденных, у которых развился кожно-слизистый кандидоз, был более высокий риск развития более поздней кандидозной инфекции глубоких органов [710].
Описаны также кожные абсцессы [13–15]. Однако наиболее частым проявлением является перинеальный кандидоз [7–10]. Важно подчеркнуть, что даже когда любая из этих форм кожно-слизистого кандидоза может предшествовать возникновению системного заболевания, это не является патогномоничным или обязательным состоянием. Проспективная оценка этой ассоциации показала, что 44{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} у новорожденных с инвазивным кандидозом никогда не развивались поражения кожи [710]. Однако тот же анализ показал, что у новорожденных, у которых развился кожно-слизистый кандидоз, был более высокий риск развития более поздней кандидозной инфекции глубоких органов [710].Две уникальные разновидности неонатальных кандидозных кожных заболеваний:
- (A): Врожденный кандидоз кожи
- Инвазивный грибковый дерматит . Это недавно описанное кожное заболевание [1977] влияет на новорожденных с экстремально низкой массой тела при рождении.
 Видны характерные язвенные и эрозивные поражения с обширными корками. Даже если в эту сущность вовлечены другие грибковые патогены, Candida spp. ответственны примерно за 70 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} случаев [1977]. Более половины из этих инфекций кожи, связанных с Candida , были связаны с возникновением инвазивного кандидоза. Авторы, описывающие эту и другие картины, постулируют, что незрелая кожа становится в этих случаях входными воротами для Candida [1516, 1977].
Видны характерные язвенные и эрозивные поражения с обширными корками. Даже если в эту сущность вовлечены другие грибковые патогены, Candida spp. ответственны примерно за 70 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} случаев [1977]. Более половины из этих инфекций кожи, связанных с Candida , были связаны с возникновением инвазивного кандидоза. Авторы, описывающие эту и другие картины, постулируют, что незрелая кожа становится в этих случаях входными воротами для Candida [1516, 1977].
- Центральная нервная система Среди новорожденных Кандидозный менингит — одно из наиболее частых проявлений инвазивного кандидоза [164, 433, 708]. До 64% новорожденных, умирающих от инвазивного кандидоза, имеют поражение ЦНС, и более 2/3 этих детей имеют положительные (A):культуры ЦСЖ в какой-то момент заболевания [708].
Неврологические клинические проявления в этой конкретной популяции немногочисленны и связаны с повышенным внутричерепным давлением (выбухание родничка и расхождение швов).
 Вместо этого обычно обнаруживаются общие признаки сепсиса и прогрессирующее клиническое ухудшение [708]. Другими словами, Candida менингит обычно проявляется как часть синдрома инвазивного или диссеминированного кандидоза. Таким образом, врач, лечащий сепсис у новорожденных из группы высокого риска, должен заподозрить Candida менингит, если Candida spp. выделяют из крови, мочи или других мест, свидетельствующих о сильной колонизации [708].
Вместо этого обычно обнаруживаются общие признаки сепсиса и прогрессирующее клиническое ухудшение [708]. Другими словами, Candida менингит обычно проявляется как часть синдрома инвазивного или диссеминированного кандидоза. Таким образом, врач, лечащий сепсис у новорожденных из группы высокого риска, должен заподозрить Candida менингит, если Candida spp. выделяют из крови, мочи или других мест, свидетельствующих о сильной колонизации [708].Candida менингит вызывает высокий уровень смертности, а у выживших высокая частота тяжелых последствий (гидроцефалия, задержка психомоторного развития и стеноз водопровода) [433].
- Глаза В качестве инструмента ранней диагностики инвазивных заболеваний рекомендуется использовать осмотр глазного дна. Единственное проспективное исследование, в котором оценивали новорожденных с кандидемией или ликвором, положительным на Candida , выявило заболеваемость Candida эндофтальмитом 50 {64e6c1a1710838655cc965f0e1ea13052e867597ac423370498029d1bc1}.

- Сердце Кандидозный эндокардит оказался второй наиболее распространенной формой эндокардита в этой возрастной группе [506, 1662]. Клинически ожидаются классические проявления, включая сердечные шумы, петехии, кожные абсцессы, артрит, гепатомегалию и спленомегалию [506]. Правосторонние внутрисердечные грибковые образования могут проявляться сердечной недостаточностью или даже легочной грибковой эмболией [1128] [867, 1472].
- Почки Кандидозная ИМП является наиболее частой причиной инфекции мочевыводящих путей в (A):ОИТН [1787]. Около половины этих детей имеют сопутствующую кандидемию [1787]. Кроме того, эта популяция особенно предрасположена к почечному кандидозу, который относится к почечным (А): грибковым шарикам или почечным грибковым абсцессам. От 35 до 42 новорожденных, госпитализированных в ОИТН с кандидурией, будут иметь почечный кандидоз, и подавляющее большинство этих случаев действительно являются грибковыми шариками [330, 1787]. Может возникать односторонняя или двусторонняя обструкция почек [330, 1787].
 Почечная недостаточность может быть первым клиническим проявлением инвазивного кандидоза [23–36].
Почечная недостаточность может быть первым клиническим проявлением инвазивного кандидоза [23–36]. - Кости и суставы Candida spp. неоднократно входили в тройку наиболее частых агентов, вызывающих неонатальный артрит [507, 1689, 1807]. Теплота и веретенообразный отек нижних конечностей в сочетании с рентгенологическими признаками остеолиза и эрозии кортикального слоя кости являются ожидаемыми находками в случаях кандидозного остеомиелита и/или артрита у новорожденных [2375, 2396].
Специальные диагностические стратегии
Общие сведения о диагностических процедурах см. в нашем (A):общем обсуждении диагностики инвазивного кандидоза. Однако по большей части концепции, обсуждаемые на этой странице, основаны на данных о взрослом населении.
Инвазивный кандидоз у новорожденных отличается более высокой скоростью восстановления посевов и более частыми локализованными проявлениями [1128]. Джонсон и др. al проанализировали 31 случай инвазивного кандидоза у младенцев и сообщили о следующих наиболее частых локализациях, из которых Candida был выделен [1128]:
| Сайты | Скорость восстановления |
|---|---|
| ФГОС | 52 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Моча | 48 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Кровь | 45 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Кости/Соединения | 26 {64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Глаз | 23{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Легкое | 13{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
| Брюшина | 13{64e6c1a1710838655cc965f0e1ea13052e867597ac43370498029d1bc5831201} |
Несмотря на эти данные, не менее 20{64e6c1a1710838655cc9В одном исследовании 65f0e1ea13052e867597ac43370498029d1bc5831201} детей с признаками кандидозной инфекции глубоких органов при вскрытии были отрицательными при жизни [1128].
В заключение, положительная культура на Candida spp. , полученный от ребенка с высоким риском развития инвазивного кандидоза, никогда не следует игнорировать. Кроме того, Candida spp. всегда следует учитывать при дифференциальной диагностике сепсиса у новорожденных, особенно сепсиса с поздним началом [473]. Тщательная оценка для исключения диссеминированной кандидозной инфекции у младенцев с этим синдромом должна проводиться в плановом порядке:
- завершение микробиологического исследования крови, мочи и спинномозговой жидкости
- клиническая оценка состояния сетчатки [162]
- эхокардиографическая оценка сердца
- УЗИ почек [644, 1264]
Некоторые авторы выступают за серийное УЗИ. Брайант и др. др. изучили 41 ребенка с кандидурией, госпитализированных в ОИТН, и обнаружили, что время до развития аномалий, обнаруживаемых с помощью УЗИ, составляло от 8 до 39 дней с момента обнаружения кандидурии [330]. Если имеются клинические признаки артрита или остеомиелита, то в оценку следует включить полное обследование скелета и аспирацию синовиальной оболочки или кости [320].
Терапия
Общие концепции терапевтических стратегий см. в обсуждении (A): терапия инвазивного кандидоза. Большинство данных по лечению любой формы инвазивного кандидоза у детей и новорожденных были экстраполированы из исследований пожилых пациентов.
Все большее внимание уделяется различиям новорожденных с точки зрения соответствующих стратегий. Были продемонстрированы важные различия в фармакокинетике, но особенно в профиле токсичности доступных противогрибковых средств. Как мы обсудим, оба классических, но токсичных противогрибковых агента, амфотерицин В и 5-фторцитозин, вызывают минимальные побочные эффекты у новорожденных, и комбинация этих двух агентов для лечения неонатального кандидоза широко используется и пропагандируется [164, 630, 708, 1128, 1315, 2392].
- Амфотерицин В
Первоначальные сообщения об использовании амфотерицина В у новорожденных были несколько тревожными. В частности, отчет Baley et al. увязали этот агент с высокой смертностью у 10 младенцев с инвазивным кандидозом и вызвали скептицизм у неонатологов [163, 2284]. Однако такие сопутствующие факторы, как почечная недостаточность в анамнезе и одновременное применение других нефротоксичных средств, не учитывались [22–84]. Johnson et al. не обнаружили ни одного случая значительной почечной токсичности амфотерицина В в группе из 21 ребенка (масса тела при рождении <1500 г) с кандидозом новорожденных, получавших лечение этим препаратом [1128]. Кроме того, в этой популяции особенно часто наблюдаются классические побочные эффекты, связанные с инфузией, лихорадка, озноб, тошнота и рвота [630, 1128, 2376]. И даже несмотря на то, что известно, что амфотерицин В ингибирует выработку эритропоэтина, анемия не была описана как значимое явление у детей, получавших этот препарат [351, 1346].
Однако такие сопутствующие факторы, как почечная недостаточность в анамнезе и одновременное применение других нефротоксичных средств, не учитывались [22–84]. Johnson et al. не обнаружили ни одного случая значительной почечной токсичности амфотерицина В в группе из 21 ребенка (масса тела при рождении <1500 г) с кандидозом новорожденных, получавших лечение этим препаратом [1128]. Кроме того, в этой популяции особенно часто наблюдаются классические побочные эффекты, связанные с инфузией, лихорадка, озноб, тошнота и рвота [630, 1128, 2376]. И даже несмотря на то, что известно, что амфотерицин В ингибирует выработку эритропоэтина, анемия не была описана как значимое явление у детей, получавших этот препарат [351, 1346].Действительно, некоторые авторы поддерживают использование только амфотерицина В для лечения неонатального кандидоза ввиду отсутствия внутривенной формы 5-фторцитозина и незрелости (А):ЖКТ у новорожденных [351]. ]. Ретроспективный анализ такого подхода показал, что транзиторная азотемия, повышение уровня креатинина сыворотки и гипоалкемия встречались примерно в половине случаев, но все эти осложнения удовлетворительно купировались короткими перерывами в терапии или коррекцией интервалов дозирования.
.jpg) Кроме того, сравнение уровня смертности этих детей, получавших лечение без 5-фторцитозина, с уровнем смертности, о котором сообщают авторы при использовании классической комбинации, показало, что они были одинаковыми или даже ниже [351].
Кроме того, сравнение уровня смертности этих детей, получавших лечение без 5-фторцитозина, с уровнем смертности, о котором сообщают авторы при использовании классической комбинации, показало, что они были одинаковыми или даже ниже [351]. - 5-фторцитозин
Johnson et al. также подчеркнули отсутствие случаев токсичности костного мозга или печени при использовании 5-фторцитозина для лечения кандидоза новорожденных. Они использовали дозы от 20 до 200 мг/кг/день [1128]. Во многих других отчетах, посвященных этой теме, предпочтение отдавалось сочетанному использованию этого препарата с амфотерицином В [164, 708, 1128, 1315, 2392]. - Флуконазол
Опубликованы ограниченные данные об использовании флуконазола у этой группы пациентов. Большая часть данных взята из отдельных отчетов [245, 1078, 1258, 1521, 1617, 2329]., 2330, 2348]. Совсем недавно в одном рандомизированном исследовании флуконазол сравнивали с амфотерицином В при лечении 23 детей с неонатальным кандидозом [619]. Однако была включена неоднородная группа младенцев. Однократная положительная культура кала на Candida учитывалась как критерий инвазивного кандидоза в одном случае. Таким образом, из этого исследования нельзя сделать серьезных выводов [619]. Нет сомнений в том, что флуконазол заслуживает дальнейшего изучения.
Однако была включена неоднородная группа младенцев. Однократная положительная культура кала на Candida учитывалась как критерий инвазивного кандидоза в одном случае. Таким образом, из этого исследования нельзя сделать серьезных выводов [619]. Нет сомнений в том, что флуконазол заслуживает дальнейшего изучения.
В заключение, амфотерицин В отдельно или в комбинации с 5-фторцитозином остается стандартом лечения неонатального кандидоза. Оптимальная продолжительность терапии неизвестна. Тем не менее, рекомендуется принимать амфотерицин В в дозе от 10 до 15 мг/кг в случаях неосложненной кандидемии, связанной с катетером, и от 25 до 30 мг/кг в целом для пациентов с инвазивным заболеванием. При использовании 5-фторцитозина рекомендуется 100 мг/кг/день в четырех равных дозах [351].
Врожденный кандидоз
Врожденный кандидоз является редкой клинической формой, при которой внутриутробная инфекция Candida проявляется при рождении. Врожденный кандидоз не связан с родами через естественные родовые пути, преждевременным излитием плодных оболочек, недоношенностью, возрастом матери, продолжительностью родов или паритетом [639, 1985]. Использование внутриматочных контрацептивов часто ассоциировалось с этим состоянием [513, 563, 24–26]. Описаны две формы болезни [1842]:
Использование внутриматочных контрацептивов часто ассоциировалось с этим состоянием [513, 563, 24–26]. Описаны две формы болезни [1842]:
- Врожденный кожный кандидоз
В этом случае в первые 12 часов жизни проявляется обширная кожная сыпь [1985]. Макулярная эритема, которая может развиться из пустулезной, папулезной или везикулярной фазы, в конечном итоге приводит к обширному шелушению [851, 1985]. Описаны также паронихия и дистрофия ногтевых пластин [112, 1877]. Наиболее часто поражаемые области включают туловище, шею, лицо и конечности [1985]. Эти кожные поражения обычно исчезают спонтанно или после коротких курсов перорального приема нистатина [50, 19].85]. - Врожденный системный кандидоз
В некоторых случаях картина может развиться до инвазивной инфекции и смерти, особенно у младенцев с очень низкой массой тела при рождении [1127]. Эта форма заболевания отличается высокой летальностью. Важно отметить, что по крайней мере в половине случаев кожная фаза, описанная ранее, не развивается [1124].
