Гемолитическая желтуха новорожденных: Гемолитическая болезнь новорожденных — «Наша Радость»
Гемолитическая болезнь новорожденных — «Наша Радость»
Гемолитическая болезнь новорождённого. Звучит страшно, пугающе — особенно в сочетании с трогательным словом «новорожденный». И это действительно тяжелая патология, которая требует срочного медицинского вмешательства. По прогнозам более 90 % детей, получивших своевременное лечение, впоследствии не имеют неврологических нарушений. Поэтому медлить нельзя, нужно вовремя диагностировать и принимать меры.
Поскольку, как правило, ГБН проявляется в первые дни жизни ребёнка, лечение назначают сразу, пожалуйста, доверяйте и не препятствуйте действиям врачей!
Итак, что же это за заболевание — ГБН? Это разрушение эритроцитов новорожденного ребенка антителами его матери. И причина его — несовместимость материнской и детской крови по антигенам красных кровяных клеток (эритроцитов), как правило, по резус-фактору и системе групп крови, и, иногда, по другим факторам крови.
В чем же причина?
Если у матери резус-отрицательная кровь, а у ребёнка резус-положительная, то возникает резус-несовместимость. Из-за этого иммунная система матери эритроциты плода может определить как потенциально опасные, инородные, и начнет вырабатывать антитела против резус-фактора, расположенного на них. Прикрепившись к эритроцитам ребёнка, антитела разрушают их. Причем начинается этот процесс еще в период внутриутробного развития плода и после рождения ребенка продолжается. Если же у плода кровь резус-отрицательная, а у мамы — резус-положительная, то это ситуации не возникает.
Из-за этого иммунная система матери эритроциты плода может определить как потенциально опасные, инородные, и начнет вырабатывать антитела против резус-фактора, расположенного на них. Прикрепившись к эритроцитам ребёнка, антитела разрушают их. Причем начинается этот процесс еще в период внутриутробного развития плода и после рождения ребенка продолжается. Если же у плода кровь резус-отрицательная, а у мамы — резус-положительная, то это ситуации не возникает.
Как не пропустить симптомы гемолитической болезни
Пока мама беременна, признаки несовместимости крови никак себя не проявляют ни у матери, ни у плода. А уже после рождения ГБН клинически проявляется по-разному, в зависимости от того, какую форму примет: анемическую, желтушную и отёчную. Бывают также случаи сочетания этих форм. Давайте рассмотрим их отдельно.
1. Анемическая форма. Считается наиболее лёгкой. Ее проявления — бледность кожных покровов, неврологические нарушения, например, слишком продолжительный сон, вялость, апатичность, плохой аппетит, вялый сосательный рефлекс.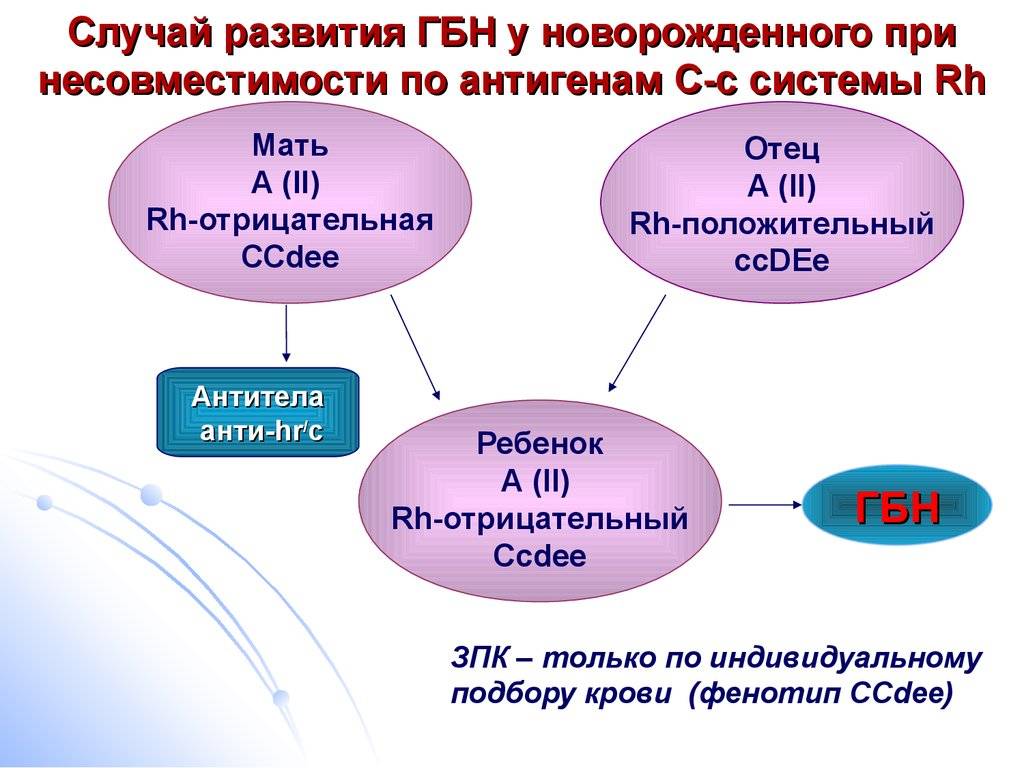 Кроме того, присутствуют признаки увеличения селезёнки и печени, наблюдающиеся в динамике.
Кроме того, присутствуют признаки увеличения селезёнки и печени, наблюдающиеся в динамике.
2. Желтушная форма. Наиболее часто встречающаяся форма. Она диагностируется почти в 90 % случаев. При этой форме желтуха самый главный симптом. Желтый оттенок буквально в первые часы жизни приобретает кожа, слизистые оболочки, возможны увеличения печени и селезёнки. От распространенности по телу и интенсивности желтухи определяют степень тяжести желтушной формы. Это определяется визуально по шкале Крамера. Всего степеней пять, при первой поражены лицо и шея, при пятой — уже все тело. Зависит интенсивность желтухи от уровня билирубина, который придает коже жёлтый. Критический уровень этого фермента способен поразить нейроны головного мозга, его структуры, и вызвать серьезного грозного осложнения, биллирубиновой энцефалопатии.
3. Отёчная форма («водянка плода»). Это наиболее тяжёлая форма, чаще всего диагностируемая ещё внутриутробно. Желтушная окраска плодных оболочек, околоплодных вод, пуповины не остался врачами незамеченными. У ребенка с момента рождения отеки по всему телу — подкожные, брюшной полости, грудной клетки. Состояние новорожденного тяжелое. Детям, у которых диагностируется именно эта форма заболевания, требуется интенсивное лечение, в том числе переливание крови.
У ребенка с момента рождения отеки по всему телу — подкожные, брюшной полости, грудной клетки. Состояние новорожденного тяжелое. Детям, у которых диагностируется именно эта форма заболевания, требуется интенсивное лечение, в том числе переливание крови.
Сразу после рождения детям, особенно из группы риска, важно определить группу крови. Дети, у которых не совпали группы крови или резус-принадлежности с мамой, первые сутки жизни должны быть осмотрены врачом несколько раз.
Мама может и сама заметить желтушность, также как и чрезмерную бледность слизистых и кожи. В этом случае необходимо незамедлительно сообщить врачу.
ГБН нельзя путать с другими заболеваниями новорождённых:
- наследственные гемолитические или постгеморрагические анемии;
- неиммунная водянка плода;
- различные инфекции и др.
Точную диагностику может провести только врач, не пытайтесь сами поставить диагноз или преуменьшить его важность.
Как лечат ГБН?
В лечении используются два подхода — консервативный и оперативный. К первому относят фототерапию и инфузионную терапию с внутривенными иммуноглобулинами, ко второму — заменное переливание крови. Формы лечения в зависимости от степени тяжести определяют врачи.
Конечно, фототерапия самый эффективный и безопасный метод лечения. В его основе — лечебное воздействие ультрафиолетовых лучей с определенной длиной волны, проникающих через кожу малыша и помогающих образовываться нетоксичной водорастворимой форме билирубина, которая в последствии легко выводится из организма. Как следствие, уровень билирубина в крови ребёнка падает, и организм не страдает от его токсического воздействия.
После постановки диагноза фототерапия проводится «нон-стоп». При этом ребенок теряет много жидкости, и восполняют ее как раз за счет внутривенного введения, частого прикладывания к груди и восполнения питьем.
В качестве побочных эффектов от лечения могут наблюдаться мелкоточечная сыпь и окрашивание мочи, кала и кожи в бронзовый цвет, все это не требует специального лечения, и проходят через некоторое время.
Операция заменного переливания крови проводится при тяжёлых формах гемолитической болезни новорождённых, и выполняется в условиях реанимационного отделения.
Поскольку средняя форма тяжести ГБН встречается довольно часто, мамам необходимо не только полагаться на врачей, но и самим быть внимательным к малышу, наблюдать за ним, особенно если ребенок относится к группе риска по группе крови и резусу. Нельзя списывать все проблемы на «желтушку новорожденных», как ее называют, и игнорировать эти серьезные симптомы.
Гемолитическая болезнь новорожденных: токсическое воздействие на организм
Содержимое
- 1 Гемолитическая болезнь новорожденных: Как она токсично влияет на организм?
- 1.1 Токсическое воздействие на организм при гемолитической болезни новорожденных
- 1.1.1 Гемолитическая болезнь новорожденных
- 1.1.2 Токсическое воздействие
- 1.2 Гемолитическая болезнь новорожденных: что это такое?
- 1.3 Развитие гемолитической болезни новорожденных
- 1.
 4 Почему гемолитическая болезнь новорожденных опасна
4 Почему гемолитическая болезнь новорожденных опасна - 1.5 Диагностирование гемолитической болезни новорожденных
- 1.5.1 Причины возникновения
- 1.5.2 Симптомы
- 1.5.3 Диагностирование
- 1.5.4 Лечение
- 1.6 Лечение гемолитической болезни новорожденных
- 1.6.1 Фототерапия
- 1.6.2 Плазменная эксфузия
- 1.6.3 Переливание крови
- 1.6.4 Курс лечения
- 1.7 Последствия гемолитической болезни новорожденных
- 1.7.1 Нарушение функционирования органов и систем
- 1.7.2 Вероятность развития осложнений
- 1.7.3 Необходимость стационарного лечения
- 1.8 Как меняется организм при гемолитической болезни новорожденных
- 1.8.1 Патологические изменения в кровеносной системе
- 1.8.2 Нарушения в функционировании органов и систем
- 1.8.3 Риск осложнений в будущем
- 1.9 Пострадавшие органы при гемолитической болезни новорожденных
- 1.10 Как противостоять гемолитической болезни новорожденных
- 1.
 11 Какие симптомы может показать ребенок в период гемолитической болезни новорожденных?
11 Какие симптомы может показать ребенок в период гемолитической болезни новорожденных? - 1.12 Видео по теме:
- 1.13 Вопрос-ответ:
- 1.13.0.1 Какие органы и системы наиболее часто подвергаются токсическому действию при гемолитической болезни новорожденных?
- 1.13.0.2 Какие симптомы токсического действия могут наблюдаться при гемолитической болезни новорожденных?
- 1.13.0.3 Как влияет токсическое действие на сердечно-сосудистую систему при гемолитической болезни новорожденных?
- 1.13.0.4 Как снизить токсическое действие при гемолитической болезни новорожденных?
- 1.13.0.5 Какие причины лежат в основе гемолитической болезни новорожденных?
- 1.13.0.6 Могут ли последствия токсического действия быть смертельными?
- 1.1 Токсическое воздействие на организм при гемолитической болезни новорожденных
Гемолитическая болезнь новорожденных оказывает токсическое действие на организм, вызывая разрушение красных кровяных клеток и возникающие при этом проблемы со здоровьем младенца. Узнайте, какие меры необходимо принимать для предотвращения этой опасной болезни.
Гемолитическая болезнь новорожденных характеризуется разрушением красных кровяных клеток, что может привести к серьезным осложнениям у ребенка. Одним из наиболее опасных последствий является токсическое действие на организм младенца, которое может привести к перитониту, острой почечной недостаточности и даже смертельному исходу.
Важно отметить, что существуют способы профилактики гемолитической болезни новорожденных, которые связаны с диагностикой заболевания до рождения и своевременным лечением после рождения. Однако, в случае развития токсического действия на организм ребенка, необходимо немедленно обратиться к врачам и проводить комплексное лечение.
Токсическое воздействие на организм при гемолитической болезни новорожденных
Гемолитическая болезнь новорожденных
Гемолитическая болезнь новорожденных (ГБН) – это редкое заболевание, которое возникает по причине несовместимости крови матери и её ребенка. Это происходит, когда кровь ребенка имеет другую группу крови или резус-фактор, чем кровь матери.
Токсическое воздействие
В результате разрушения красных кровяных клеток у детей с ГБН могут развиваться различные проблемы, связанные с токсическим воздействием на организм.
Анемия. Из-за высокого уровня определенных веществ, выделяющихся в результате разрушения красных кровяных клеток, у детей с ГБН может развиться анемия. Это состояние, при котором в крови отсутствует достаточное количество красных кровяных клеток.
Желтушность. В результате разрушения красных кровяных клеток могут высвобождаться вещества, которые могут вызвать желтушность. Желтушность – это состояние, при котором кожа и слизистые оболочки приобретают желтый оттенок.
Отек. Чрезмерное разрушение красных кровяных клеток может привести к увеличению уровня билирубина в крови. Это в свою очередь может вызвать отек и другие проблемы.
Симптомы гемолитической болезни новорожденныхСимптомыОписание
| Желтушность | Желтый оттенок кожи и слизистых оболочек |
| Анемия | Отсутствие достаточного количества красных кровяных клеток |
| Отек | Увеличение уровня билирубина может вызвать отек и другие проблемы |
Гемолитическая болезнь новорожденных: что это такое?
Гемолитическая болезнь новорожденных (ГБН) – это заболевание, возникающее в результате несовместимости крови матери и ребенка. Главная причина ГБН – различия в группах крови и резус-факторе между матерью и плодом. Если материнские антитела попадают в плодовую кровь и нападают на эритроциты ребенка, то ГБН может привести к различным осложнениям.
Главная причина ГБН – различия в группах крови и резус-факторе между матерью и плодом. Если материнские антитела попадают в плодовую кровь и нападают на эритроциты ребенка, то ГБН может привести к различным осложнениям.
Симптомы ГБН могут быть различными, включая желтуху, анемию, увеличение селезенки и печени, задержку роста и развития ребенка. Проявление и тяжесть симптомов зависит от многих факторов, включая степень несовместимости крови и резус-фактора, а также время начала лечения.
Одним из наиболее эффективных методов лечения ГБН является трансфузия крови или проведение фототерапии. В некоторых случаях может потребоваться экстренное вмешательство. Поэтому важно знать о возможности развития ГБН и проводить своевременную профилактику и лечение.
Развитие гемолитической болезни новорожденных
Гемолитическая болезнь новорожденных — это заболевание, которое развивается в результате резус-конфликта между матерью и плодом. Конфликт возникает, если резус-фактор плода не совпадает с резус-фактором матери.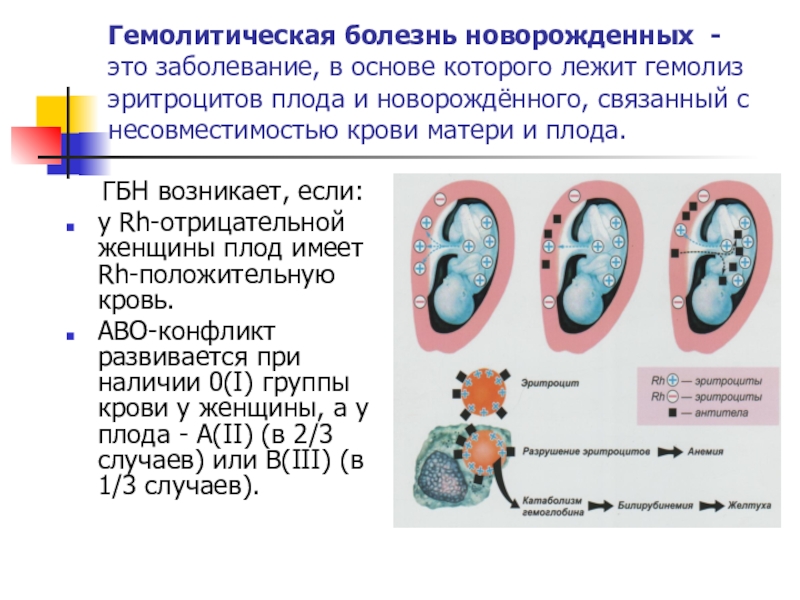
Когда антитела матери начинают атаковать эритроциты плода, происходит их разрушение — гемолиз. Разрушение эритроцитов приводит к высвобождению гемоглобина в кровь. Гемоглобин разлагается на биллирубин, который не может быть связан с белками крови и накапливается в тканях, вызывая желтушность.
- При легкой болезни новорожденный может не проявлять явных симптомов, или же они будут слабо выражены;
- Средней степени проявляется желтушность, увеличение печени и селезенки;
- В тяжелых случаях возможны осложнения, такие как повышенное кровотечение, повреждение ЦНС, анемия и даже смерть.
Гемолитическая болезнь новорожденных является серьезным заболеванием, но при своевременной диагностике и лечении может быть успешно излечена. Для предотвращения развития болезни необходимо диагностировать резус-конфликт во время беременности и принимать меры по его предотвращению или лечению.
Почему гемолитическая болезнь новорожденных опасна
Гемолитическая болезнь новорожденных (ГБН) является серьезным заболеванием, которое возникает при несовместимости кровей матери и ребенка. При этом антитела матери нападают на эритроциты плода, разрушая их стенки и вызывая нарушение кровотока.
При этом антитела матери нападают на эритроциты плода, разрушая их стенки и вызывая нарушение кровотока.
Главной причиной возникновения ГБН является несоответствие резус-фактора матери и ребенка. Несоответствие AB0-системы также может привести к развитию болезни. Однако, благодаря современным методам профилактики и лечения, риск возникновения ГБН уменьшен, и болезнь можно успешно обнаружить и лечить еще до рождения ребенка.
- Подводя итог, гемолитическая болезнь новорожденных является серьезной угрозой для здоровья и жизни маленьких детей. Однако, правильная диагностика и своевременное лечение позволяют уменьшить риск возникновения осложнений и обеспечить полноценное и здоровое развитие ребенка.
Диагностирование гемолитической болезни новорожденных
Причины возникновения
Гемолитическая болезнь новорожденных (ГБН) – это заболевание, которое возникает из-за несовместимости крови матери и плода по группе крови или резус-фактору. При перенесении первой беременности женщина не производит достаточное количество антител, которые могут проникнуть через плаценту и атаковать кровь плода.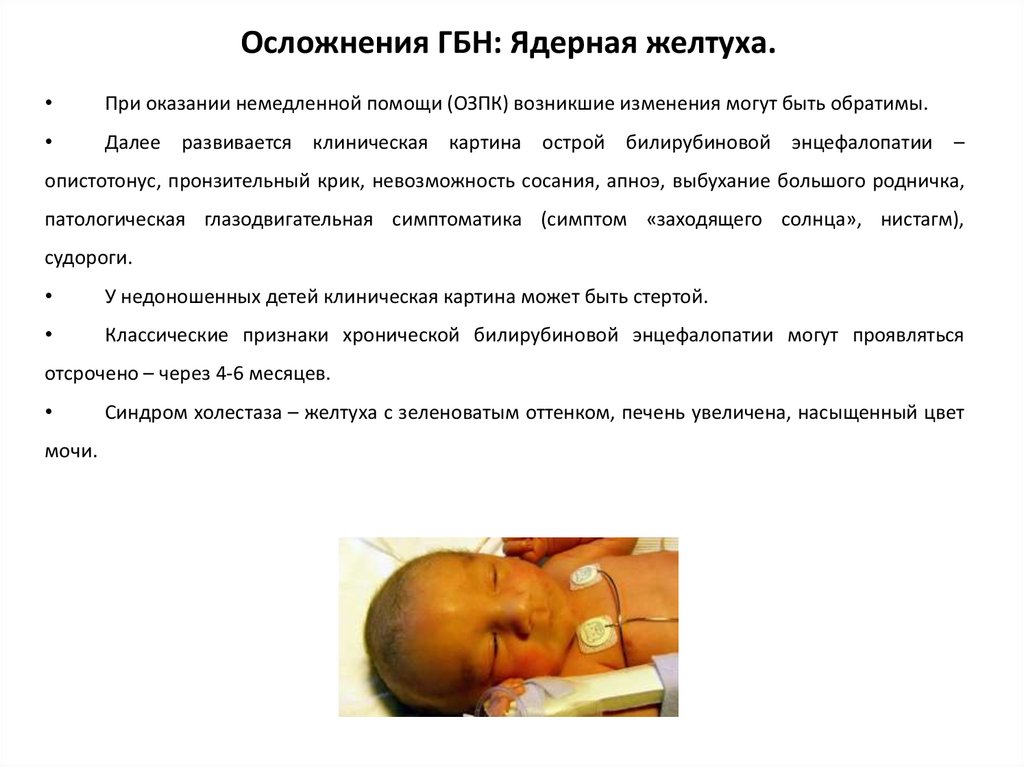 В следующих беременностях женщина реагирует быстрее, что может привести к развитию ГБН.
В следующих беременностях женщина реагирует быстрее, что может привести к развитию ГБН.
Симптомы
Самым ярким симптомом ГБН является желтуха у новорожденного. Кожа и склеры глаз набухают жёлтым оттенком. Может наблюдаться повышенная температура тела, задержка мочеиспускания, слабость, сонливость, увеличение печени и селезенки.
Диагностирование
Диагностика ГБН проходит в несколько этапов. Сначала измеряется концентрация билирубина в крови новорожденного. Если его уровень очень высокий, то это первый признак возможной ГБН. Затем проводятся дополнительные исследования, такие как анализ группы крови и резус-фактора матери и ребёнка. В некоторых случаях может потребоваться пункция пуповины.
Лечение
Лечение ГБН должно быть врачебным, и только он может определить, какой метод лечения подойдет в каждом отдельном случае. Прежде всего, врачи используют фототерапию – излучение кожи новорожденного специальными лампами, которые уменьшают уровень билирубина в крови. В более сложных случаях может понадобиться переливание крови новорожденного, чтобы пополнить красные кровяные тельца и убрать антитела из кровотока, а также предотвратить повторную атаку на кровь ребёнка.
В более сложных случаях может понадобиться переливание крови новорожденного, чтобы пополнить красные кровяные тельца и убрать антитела из кровотока, а также предотвратить повторную атаку на кровь ребёнка.
В заключении: регулярное планирование беременности и своевременное обращение к врачам помогут предотвратить появление ГБН у новорожденного.
Лечение гемолитической болезни новорожденных
Фототерапия
Одним из наиболее распространенных методов лечения гемолитической болезни новорожденных является фототерапия. Этот метод заключается в расположении ребенка под специальной лампой, которая испускает синий свет и позволяет превратить билирубин в биливердин, который легко выводится из организма.
Плазменная эксфузия
Если фототерапия не дает достаточных результатов, то может назначаться плазменная эксфузия. Это специальная процедура, в ходе которой кровь ребенка проходит через фильтр, который удаляет из крови антитела, вызывающие гемолитическую болезнь.
Переливание крови
Если уровень гемоглобина в крови новорожденного слишком низкий, то может быть назначено переливание крови. Этот метод позволяет увеличить количество эритроцитов в крови и предотвратить развитие анемии.
Курс лечения
Курс лечения гемолитической болезни новорожденных зависит от степени тяжести заболевания. В большинстве случаев, после фототерапии и плазменной эксфузии, дети восстанавливаются и могут выписываться домой. Однако, в некоторых случаях может потребоваться продолжительное лечение и госпитализация ребенка.
Последствия гемолитической болезни новорожденных
Нарушение функционирования органов и систем
Гемолитическая болезнь новорожденных, вызванная несовместимостью групп крови матери и ребенка, может привести к серьезным нарушениям функционирования органов и систем организма.
Процесс разрушения эритроцитов, который происходит при гемолитической болезни, приводит к повышенной концентрации билирубина в крови. Это может вызвать желтуху новорожденных, нарушения в работе печени, почек, сердечно-сосудистой системы и нервной системы.
Кроме того, токсическое действие на организм может привести к анемии, повышенной утомляемости, нарушению обмена веществ, что приведет к нарушению клинических показателей и замедлению физиологического развития ребенка.
Вероятность развития осложнений
Вероятность развития осложнений у ребенка с гемолитической болезнью новорожденных напрямую зависит от степени тяжести заболевания и срока его выявления. Чем больше время до начала лечения, тем выше вероятность того, что организм ребенка будет испытывать тяжелое токсическое воздействие. В некоторых случаях гемолитическая болезнь может привести к летальному исходу.
Необходимость стационарного лечения
Лечение гемолитической болезни новорожденных является сложным и требует серьезного подхода. В большинстве случаев для лечения требуется стационарное наблюдение и вмешательство специалистов. Лечение может включать введение иммуноглобулинов, переливание крови и использование специальных препаратов для связывания и вывода из организма билирубина.
При выявлении несовместимости групп крови у матери и ребенка необходимо незамедлительно обратиться за медицинской помощью и пройти необходимое лечение, чтобы избежать тяжелых последствий для здоровья и жизни ребенка.
Как меняется организм при гемолитической болезни новорожденных
Патологические изменения в кровеносной системе
Гемолитическая болезнь новорожденных (ГБН) вызывает серьезные нарушения в работе кровеносной системы ребенка. Из-за конфликта резус-факторов между кровью матери и плода у младенца начинают разрушаться красные кровяные клетки (эритроциты). Обычно печень и селезенка принимают на себя задачу удаления поврежденных клеток, но при ГБН они не справляются с таким объемом работы. Это приводит к тому, что поврежденные эритроциты могут окрашивать кожу, склеры и слизистые оболочки ребенка в ярко-желтый цвет (желтуха).
Нарушения в функционировании органов и систем
Из-за повышения количества свободного билирубина в крови ребенка может возникать энцефалопатия — нарушение функционирования мозга. Это может проявляться в виде задержки развития, нарушения сна, снижения аппетита и различных отклонений в поведении ребенка. Также у младенца может возникать водянка (накопление жидкости в тканях), что приводит к тяжелым нарушениям работы органов и систем.
Это может проявляться в виде задержки развития, нарушения сна, снижения аппетита и различных отклонений в поведении ребенка. Также у младенца может возникать водянка (накопление жидкости в тканях), что приводит к тяжелым нарушениям работы органов и систем.
Риск осложнений в будущем
При отсутствии своевременного лечения ГБН может привести к серьезным осложнениям в будущем. У детей, перенесших ГБН, наблюдается повышенный риск развития заболеваний печени, желчевыводящих путей, сердца и других органов. Также у них может возникнуть анемия — недостаток красных кровяных клеток в крови. Все это подчеркивает значимость своевременной диагностики и лечения гемолитической болезни новорожденных.
Некоторые признаки, которые могут указывать на ГБН:СимптомыПояснения
| Желтуха | Окрашивание кожи, склер и слизистых оболочек в желтый цвет |
| Бледность | Низкий уровень гемоглобина в крови |
| Опухоли на теле | Накопление жидкости в тканях (водянка) |
| Отсутствие аппетита | Связано с нарушением работы желудочно-кишечного тракта |
Пострадавшие органы при гемолитической болезни новорожденных
Гемолитическая болезнь новорожденных (ГБН) — это повреждение организма ребенка, которое возникает из-за несовместимости крови матери и ребенка. Когда кровь матери и ребенка не совпадает по группе и резус-фактору, у ребенка может произойти гемолиз крови, что приводит к токсическому воздействию на организм.
Когда кровь матери и ребенка не совпадает по группе и резус-фактору, у ребенка может произойти гемолиз крови, что приводит к токсическому воздействию на организм.
Органы, которые могут пострадать при ГБН, — это кранеальные нервы, печень, селезенка, сердце, легкие и почки. Кранеальные нервы отвечают за органы чувств, проблемы с ними могут привести к нарушениям слуха, зрения и дыхания. Печень и селезенка играют важную роль в очистке крови, поэтому их поражение приводит к нарушению работы иммунной системы и нарушению обмена веществ. Сердце и легкие важны для обеспечения тканей кислородом, поэтому их повреждение приводит к нарушению регуляции кислорода в организме. Почки служат для очистки отходов и избытка жидкости в организме, поэтому их поражение может привести к нарушению работы почечных клеток.
Без своевременного лечения ГБН может привести к серьезным осложнением и даже смерти ребенка. Поэтому при первых признаках ГБН необходимо обратиться к врачу и пройти соответствующее лечение.
Как противостоять гемолитической болезни новорожденных
1. Предупреждение заболевания. Для уменьшения вероятности развития гемолитической болезни новорожденных необходимо учитывать состояние родителей до беременности. Если один из родителей имеет резус-отрицательную кровь, а второй — резус-положительную, то ребенок может унаследовать положительный резус-фактор и вызвать у матери заболевание.
2. Обследование и лечение беременных женщин. В случае выявления у беременной женщины резус-отрицательной крови необходимо начать лечение в третьем триместре беременности, чтобы уменьшить количество антител, которые могут проникнуть в плодовую воду и привести к заболеванию новорожденного.
3. Введение иммуноглобулина. После рождения ребенка резус-отрицательной матери необходимо ввести иммуноглобулин, который свяжется с резус-положительными эритроцитами ребенка и предотвратит развитие заболевания.
4. Наблюдение за новорожденным. После рождения необходимо обследовать ребенка на наличие гемолитических анемий и проводить лечение в соответствии с медицинскими рекомендациями.
После рождения необходимо обследовать ребенка на наличие гемолитических анемий и проводить лечение в соответствии с медицинскими рекомендациями.
5. Назначение лечения при развитии заболевания. При развитии гемолитической болезни новорожденных необходимо назначить соответствующее лечение, которое будет направлено на снижение уровня билирубина в крови и повышение уровня гемоглобина.
Какие симптомы может показать ребенок в период гемолитической болезни новорожденных?
Гемолитическая болезнь новорожденных – это заболевание, которое проявляется в тех случаях, когда группа крови новорожденного не совпадает с группой крови матери. Данное заболевание может вызывать токсическое действие на организм ребенка, что приводит к нарушению функционирования внутренних органов и систем.
Симптомы гемолитической болезни новорожденных могут проявляться на разных уровнях. К примеру, у ребенка может появиться желтуха, наличие крови в моче, нарушение функционирования печени, анемия и т. д.
д.
Ребенок может чувствовать себя слабым, накладываться ограничения на физические нагрузки, а также может потерять аппетит и сонлив.
- Желтуха – ненормальная желтая окраска кожи и белков глаза. Она происходит из-за того, что продукты разложения красных кровяных телец можно отследить в круге системы кровообращения ребенка.
- Кровь в моче – это может быть еще одним симптомом гемолитической болезни новорожденных. Это может происходить из-за того, что почки работают на пределе своих возможностей в попытке удалить избыток продуктов разложения красных кровяных телец из крови ребенка.
- Нарушение функционирования печени – это может произойти в результате загрузки избытком продуктов разложения красных кровяных телец. В этом случае мочеиспускание становится частым, и кожа может стать желтой.
Все эти симптомы должны быть обратимыми в случае своевременного выявления и лечения гемолитической болезни новорожденных. Важно проконсультироваться с врачом при появлении любых подозрительных симптомов.
Видео по теме:
Вопрос-ответ:
Какие органы и системы наиболее часто подвергаются токсическому действию при гемолитической болезни новорожденных?
Токсическое действие при гемолитической болезни новорожденных оказывает наибольший вред на сердечно-сосудистую систему, почки, печень и нервную систему.
Какие симптомы токсического действия могут наблюдаться при гемолитической болезни новорожденных?
Симптомы токсического действия могут проявляться в виде желтухи, бледности кожи, повышенной утомляемости, задержки в физическом развитии, задержки в росте, изменения в поведении и нарушениях в работе системы крови.
Как влияет токсическое действие на сердечно-сосудистую систему при гемолитической болезни новорожденных?
Токсическое действие ведет к изменениям в работе сердечно-сосудистой системы, таким как увеличение размера сердца, нарушение ритма сердца, увеличение или уменьшение кровяного давления.
Как снизить токсическое действие при гемолитической болезни новорожденных?
Для снижения токсического действия можно использовать методы плазмафереза и масштабированной переливания крови, которые позволяют удалить лишнее количество антител и токсинов из кровотока ребенка.
Какие причины лежат в основе гемолитической болезни новорожденных?
Гемолитическая болезнь новорожденных возникает из-за несовпадения кровнных групп матери и ребенка, когда антитела матери нападают на эритроциты ребенка.
Могут ли последствия токсического действия быть смертельными?
Да, в некоторых случаях токсическое действие может привести к тяжелым осложнениям и даже смерти новорожденного.
Гемолитические болезни новорожденных — StatPearls
Непрерывное обучение
Гемолитическая болезнь плода и новорожденного — это несоответствие эритроцитов между матерями и их плодами, которое может вызвать значительную заболеваемость и смертность. К счастью, фатальные последствия этого расстройства стали редкостью при соответствующем применении иммунопрофилактики. Однако, чтобы избежать фатальных последствий этого расстройства, жизненно важны своевременная диагностика и лечение. Это мероприятие рассматривает оценку, лечение и профилактику гемолитической болезни плода и новорожденного межпрофессиональной командой.
Однако, чтобы избежать фатальных последствий этого расстройства, жизненно важны своевременная диагностика и лечение. Это мероприятие рассматривает оценку, лечение и профилактику гемолитической болезни плода и новорожденного межпрофессиональной командой.
Цели:
Опишите этиологию и эпидемиологию гемолитической болезни плода и новорожденного.
Обзор патофизиологии гемолитической болезни плода и новорожденного.
Схема лечения гемолитической болезни плода и новорожденного.
Обобщение межпрофессиональных командных стратегий по улучшению координации оказания медицинской помощи и коммуникации для улучшения лечения гемолитической болезни плода и новорожденного и улучшения исходов.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Гемолитическая болезнь плода и новорожденного (HDFN) представляет собой иммуноопосредованное заболевание эритроцитов (эритроцитов), при котором материнские антитела атакуют эритроциты плода или новорожденного. [1][2] HDFN может вызвать значительную заболеваемость и смертность, особенно в условиях ограниченных ресурсов здравоохранения. Эффекты HDFN варьируются от легкой анемии до водянки плода у плода и гипербилирубинемии и ядерной желтухи у новорожденных. Благодаря раннему выявлению, лечению и профилактике этого заболевания заболеваемость и распространенность ГБПН за последние 50 лет снизились в геометрической прогрессии.[1] 9[4] И наоборот, аллоиммунизация из-за фетоматеринского кровотечения (FMH) представляет собой приобретенный иммунно-опосредованный механизм, который обычно влияет на последующие беременности, а не на беременность, при которой происходит FMH.
[1][2] HDFN может вызвать значительную заболеваемость и смертность, особенно в условиях ограниченных ресурсов здравоохранения. Эффекты HDFN варьируются от легкой анемии до водянки плода у плода и гипербилирубинемии и ядерной желтухи у новорожденных. Благодаря раннему выявлению, лечению и профилактике этого заболевания заболеваемость и распространенность ГБПН за последние 50 лет снизились в геометрической прогрессии.[1] 9[4] И наоборот, аллоиммунизация из-за фетоматеринского кровотечения (FMH) представляет собой приобретенный иммунно-опосредованный механизм, который обычно влияет на последующие беременности, а не на беременность, при которой происходит FMH.
Эпидемиология
Гемолитическая болезнь плода и новорожденного впервые была описана доктором Луисом К. Даймондом в 1932, когда он написал об эритробластозе плода у новорожденных на основании мазков периферической крови.[6] Иммунопрофилактика резус-отрицательных (RhD) впервые была введена в 1968 году, благодаря чему заболеваемость ГБПН снизилась с 1% всех новорожденных во всем мире (с 50% смертностью) до 0,5% [1]. Заболеваемость HDFN снизилась еще больше до 0,1% при проведении дородовой иммунопрофилактики RhD [2]. Однако, несмотря на адекватную иммунопрофилактику RhD, по оценкам, от 1 до 3 из 1000 резус-отрицательных женщин все еще получают аллоиммунизацию. Таким образом, важно сохранять бдительность в отношении развития ГБПН.[1]
Заболеваемость HDFN снизилась еще больше до 0,1% при проведении дородовой иммунопрофилактики RhD [2]. Однако, несмотря на адекватную иммунопрофилактику RhD, по оценкам, от 1 до 3 из 1000 резус-отрицательных женщин все еще получают аллоиммунизацию. Таким образом, важно сохранять бдительность в отношении развития ГБПН.[1]
Резус-несовместимость зависит от расы, этнической принадлежности и факторов риска. Резус-отрицательная группа крови наиболее преобладает у белых рас (15%) по сравнению с афроамериканцами (от 5% до 8%) или азиатами и коренными американцами (от 1% до 2%). Среди белых женщин резус-отрицательная женщина имеет 85% шанс спаривания с резус-положительным мужчиной.[1] Эта часто встречающаяся резус-несовместимость увеличивает риск ГБПН при любом событии СМГ.
Всего 0,1 мл крови плода, попадающей в кровоток матери, достаточно для аллоиммунизации.[7] Фактически, от 15 до 50 % беременных имеют достаточно фетально-материнских кровотечений, чтобы вызвать аллоиммунизацию, и только от 1 до 2 % всех резус-аллоиммунизаций вызваны дородовой FMH. [7] Таким образом, важно учитывать ГБПН на всех стадиях беременности, когда может возникнуть ЗМГ.
[7] Таким образом, важно учитывать ГБПН на всех стадиях беременности, когда может возникнуть ЗМГ.
Патофизиология
Как уже упоминалось, существует два механизма, вызывающих гемолитическую болезнь плода и новорожденного. Во-первых, фето-материнская пара может иметь врожденную несовместимость по системе АВО, которая возникает в 15 – 25 % беременностей.[8] Только около 1% этих пар с высокими титрами IgG разовьют HDFN из-за несовместимости по системе ABO [8]. При несовместимости по системе ABO у матерей с группой крови O присутствуют естественные антигены против групп крови A или B. Если плод матери имеет группу крови A или B (или AB), материнские антитела анти-A и/или анти-B соответственно будут атаковать чужеродную группу крови плода. Антитела анти-А и анти-В представляют собой IgG, которые могут проникать через плаценту и воздействовать на развивающийся плод.[9]] По сравнению с FMH, несовместимость по системе ABO обычно вызывает менее тяжелую форму HDFN. Постулированные теории для этого включают в себя фетальные эритроциты экспрессируют меньше антигенов группы крови ABO, чем взрослые, и что антигены группы крови ABO экспрессируются многими тканями, что снижает вероятность того, что антитела специфически нацелены на антигены на фетальных эритроцитах.
Вторым механизмом, наиболее часто вызывающим ГБПН, является фетоматеринское кровотечение (ФМК), при котором материнские антитела вырабатываются после контакта с кровью плода. Когда эритроциты плода попадают в кровоток матери, материнские антитела могут вырабатываться к антигену, представленному на поверхности эритроцитов плода. Наиболее распространенным антигеном, участвующим в этом механизме, является антиген резуса D.[10] По оценкам, у 1,5–2,5% акушерских пациенток вырабатываются антитела к другим «второстепенным» антигенам. Хотя в большинстве этих случаев аллоиммунизация не вызывает значимой гемолитической болезни новорожденных, некоторые могут вызывать тяжелую анемию при низком пороге титра. Антитела против антигенов группы крови Келла, например, связаны с повышенным риском тяжелой анемии и/или гибели плода. Эти пациенты должны находиться под очень пристальным наблюдением на протяжении всей беременности.[3][7]
Антигены крови плода, чужеродные материнской крови, наследуются от отцовских генов. Например, у резус-отрицательной женщины может быть резус-положительный плод из-за того, что ее партнер является резус-положительным. Антитела, которые развиваются из-за FMH, подвергают последующие беременности риску HDFN, поскольку первые вырабатываемые антитела относятся к типу IgM, которые не могут проникать через плаценту. При последующих контактах с антигеном Rh-D материнские антитела быстро вырабатывают антитела IgG, которые проникают через плаценту.[11]
Например, у резус-отрицательной женщины может быть резус-положительный плод из-за того, что ее партнер является резус-положительным. Антитела, которые развиваются из-за FMH, подвергают последующие беременности риску HDFN, поскольку первые вырабатываемые антитела относятся к типу IgM, которые не могут проникать через плаценту. При последующих контактах с антигеном Rh-D материнские антитела быстро вырабатывают антитела IgG, которые проникают через плаценту.[11]
Когда эритроциты младенцев подвергаются атаке и разрушаются, у младенцев развивается гемолитическая анемия. Расщепление гема приводит к образованию билирубина, который выводится плацентой внутриутробно. При рождении печень начинает обрабатывать билирубин. Непрямой билирубин или неконъюгированный билирубин конъюгируют с прямым билирубином с помощью фермента уридиндифосфоглюкуронозилтрансферазы (УДФ-глюкуронозилтрансферазы). Этот конъюгированный билирубин выводится с желчью, где в конечном итоге будет выводиться с фекалиями и мочой.
У младенцев, особенно недоношенных, процессинг печени менее эффективен, что часто приводит к естественной физиологической желтухе.[12] При избытке продуктов распада HDFN эти незрелые механизмы процессинга перегружаются, что может привести к выраженной гипербилирубинемии. Накопление несвязанного билирубина может привести к неврологической дисфункции, поскольку несвязанный билирубин пересекает гематоэнцефалический барьер и откладывается в головном мозге развивающегося новорожденного.[13] Своевременное распознавание и лечение гипербилирубинемии и ГБПН имеют первостепенное значение для предотвращения долгосрочной неврологической дисфункции у этих детей.
Анамнез и физикальное исследование
Подробный анамнез может иметь важное значение для подозрения на гемолитическую болезнь плода и новорожденного. Особое внимание следует уделить выявлению любых событий, которые могли привести к фетоматеринскому кровотечению. К ним относятся предыдущие беременности с ГБПН или водянкой плода, выкидыши, внематочная беременность, прерывание беременности на ранних сроках, переливание крови у матери, забор ворсин хориона, амниоцентез или документирование кровотечения во время беременности [7].
В начале первого триместра всем беременным женщинам следует провести анализ крови. Люди с группой крови O естественным образом экспрессируют антитела к группам крови A и B; таким образом, их следует контролировать на предмет развития ГБПН, особенно в родах и сразу после родов. Антитела, экспрессируемые у матерей с группой крови O, обычно представляют собой иммуноглобулин G (IgG) и могут проникать через плаценту. И наоборот, у матерей с группой крови А есть антитела против группы крови В, которые представляют собой преимущественно иммуноглобулины М (IgM) и не проникают через плаценту.[8] Общепринятой практикой является проверка групп крови младенцев, рожденных от матерей с группой крови О при рождении, в то время как группы крови младенцев, матери которых имеют группу крови А, В или АВ, могут не проверяться (если резус-фактор положительный). .
Основными признаками гемолитической болезни новорожденных (ГБН) являются анемия и гипербилирубинемия, которые могут проявляться вялостью, желтухой, желтухой конъюнктивы, бледностью, гепатоспленомегалией, тахикардией или брадикардией, повышенной потребностью в кислороде и/или апноэ. [9] [13]
[9] [13]
Оценка
Гемолитическая болезнь плода и новорожденного следует учитывать при дифференциальной диагностике новорожденных с желтухой/гипербилирубинемией и, безусловно, в случае неонатальной анемии. Диагноз HDFN может быть поставлен путем определения наличия материнских антител к эритроцитам (агглютинация в непрямом тесте на антитела) и/или положительного прямого теста на антитела (DAT) в сыворотке младенца.[4] Если у беременной женщины выявлена аллоиммунизация, первым шагом в дальнейшем обследовании является определение антигенного статуса эритроцитов отца. В случае положительного результата следующим шагом будет определение группы крови плода, что обычно делается с помощью амниоцентеза.[7]
По данным Американской академии педиатрии (AAP), «если у матери не было пренатальной группы крови или она резус-отрицательна, прямой тест на антитела (или тест Кумбса), группа крови и резус-фактор (D) на (пуповинной) крови младенца настоятельно рекомендуется». возможно при беременности. Пораженные беременности можно контролировать путем мониторинга титров антител и скорости движения средней мозговой артерии плода, внутриутробных трансфузий и, возможно, досрочных родов, поскольку дети с тяжелой анемией могут плохо переносить срочные роды.
Пораженные беременности можно контролировать путем мониторинга титров антител и скорости движения средней мозговой артерии плода, внутриутробных трансфузий и, возможно, досрочных родов, поскольку дети с тяжелой анемией могут плохо переносить срочные роды.
Гемолитическая болезнь новорожденных лечится путем лечения гипербилирубинемии фототерапией и при необходимости обменными трансфузиями. Рутинный универсальный скрининг чрескожного билирубина (TcB) часто проводится в первые 24 часа жизни, но скрининг следует проводить, как только подозревается гипербилирубинемия. Повышенный TcB всегда следует подтверждать с помощью общего билирубина сыворотки (ТБ). Затем почасовая номограмма Бутани используется для стратификации риска по количеству билирубина в крови младенца.[13] Эта номограмма обеспечивает рекомендуемый порог для начала фототерапии по сравнению с ранними трансфузиями в зависимости от уровня риска для младенца.
Фототерапия была внедрена в 1970-х годах и стала основой лечения гипербилирубинемии у новорожденных. Фотоизомеризация вызывает превращение билирубина в водорастворимый изомер, который затем может выводиться почками и калом без необходимости переработки в печени. Основными факторами, определяющими эффективность фототерапии, являются длина волны используемого света, интенсивность этого света, общая доза света (время воздействия и площадь поверхности воздействия) и порог, при котором начинается фототерапия. AAP рекомендует использовать интенсивную фототерапию при HDFN. Оптимальный свет, используемый для фототерапии, имеет длину волны 460-490 нм. Свет должен быть на близком расстоянии (около 20 см над младенцем), и двойная фототерапия оказалась более эффективной, чем одиночная. Имеются ограниченные данные об эффективности непрерывной фототерапии по сравнению с прерывистой для младенцев с массой тела > 2000 г [1]. Во время фототерапии матерей следует поощрять кормить своих детей грудью через определенные промежутки времени, несмотря на то, что для этого им необходимо отключать их от фототерапии.
Фотоизомеризация вызывает превращение билирубина в водорастворимый изомер, который затем может выводиться почками и калом без необходимости переработки в печени. Основными факторами, определяющими эффективность фототерапии, являются длина волны используемого света, интенсивность этого света, общая доза света (время воздействия и площадь поверхности воздействия) и порог, при котором начинается фототерапия. AAP рекомендует использовать интенсивную фототерапию при HDFN. Оптимальный свет, используемый для фототерапии, имеет длину волны 460-490 нм. Свет должен быть на близком расстоянии (около 20 см над младенцем), и двойная фототерапия оказалась более эффективной, чем одиночная. Имеются ограниченные данные об эффективности непрерывной фототерапии по сравнению с прерывистой для младенцев с массой тела > 2000 г [1]. Во время фототерапии матерей следует поощрять кормить своих детей грудью через определенные промежутки времени, несмотря на то, что для этого им необходимо отключать их от фототерапии.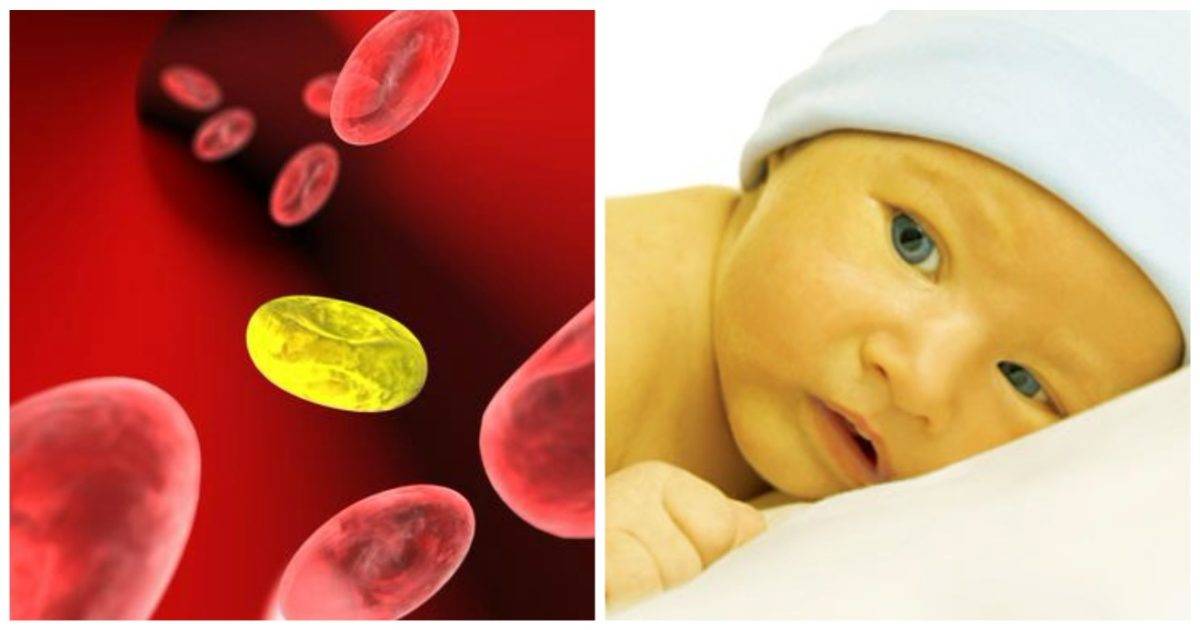
Обменное переливание может потребоваться для новорожденных с тяжелой анемией, которое включает замену эритроцитов новорожденных на антиген-отрицательные эритроциты, тем самым предотвращая дальнейший гемолиз. Аликвоты по 5 мл/кг удаляют и заменяют в течение нескольких минут для общего обмена эритроцитов на 25-50 мл/кг. Обменные переливания рекомендуются ААР, если уровни общего билирубина остаются выше порога переливания, несмотря на интенсивную фототерапию, или если присутствуют признаки билирубиновой энцефалопатии. Если рассматривается обменное переливание крови, следует измерить уровень альбумина. Альбумин 3,0 г/дл или менее считается независимым фактором риска гипербилирубинемии и снижает порог фототерапии. Без достаточного количества альбумина для связывания билирубина количество свободного неконъюгированного билирубина увеличивается, что увеличивает риск ядерной желтухи.[1]
Младенцам с анемией может потребоваться переливание крови с эритроцитарной массой, соответствующей системе ABO. Если считается, что необходима немедленная трансфузия, при родах должна быть доступна резус-отрицательная кровь O-типа, лейкодеплеция и облучение [1].
Если считается, что необходима немедленная трансфузия, при родах должна быть доступна резус-отрицательная кровь O-типа, лейкодеплеция и облучение [1].
Были рассмотрены и другие методы лечения, но они все еще остаются спорными. Внутривенный иммуноглобулин (ВВИГ) у младенцев может блокировать рецепторы Fc на макрофагах, тем самым уменьшая разрушение эритроцитов, покрытых антителами. AAP рекомендует ВВИГ, если общий билирубин в сыворотке продолжает расти, несмотря на интенсивную фототерапию, или находится в пределах 2-3 мг/дл от уровня обменного переливания. Введение ВВИГ матерям до родов не показало своей эффективности и в настоящее время не рекомендуется. Другие агенты, такие как альбумин, фенобарбитал, металлопорфирины, цинк, клофибрат и пребиотики, изучались в качестве возможных вариантов лечения гипербилирубинемии, но в настоящее время ни один из них не рекомендован [14]. В недавнем рандомизированном контролируемом исследовании с участием 70 младенцев с Rh-аллоиммунизацией было показано, что отсроченное пережатие пуповины уменьшает анемию без увеличения частоты побочных эффектов. Однако отсроченное пережатие пуповины не оказало существенного влияния на потребность в обменном переливании крови или продолжительность фототерапии.[15]
Однако отсроченное пережатие пуповины не оказало существенного влияния на потребность в обменном переливании крови или продолжительность фототерапии.[15]
Дифференциальный диагноз
Гемолитическая болезнь плода и новорожденного должна быть включена в дифференциальный диагноз младенцев с ранней, тяжелой или длительной желтухой и анемией. Другие причины желтухи и гипербилирубинемии у новорожденных включают физиологическую желтуху, недоношенность, желтуху грудного молока и грудного вскармливания, дефицит G6PD, талассемию, сепсис, родовую травму, синдром Жильбера и гипотиреоз [3]. Сбор анамнеза и физикальное, а также простое лабораторное обследование, как описано выше, могут помочь дифференцировать эти причины.
Планирование лечения
Американская ассоциация банков крови рекомендует повторный скрининг на антитела перед введением Rh-D иммунопрофилактики (Rh-D IgG) на 28 неделе беременности, в послеродовой период и при FMH[5]. В сетевом метаанализе, проведенном в Китае, наиболее эффективным протоколом для предотвращения материнской аллоиммунизации было введение Rh-D-иммунопрофилактики на 28 и 34 неделе беременности у резус-отрицательных женщин. [16]
[16]
Стандартная доза анти-RhD, вводимая во втором и третьем триместрах беременности и в послеродовом периоде, при необходимости, составляет 300 мкг. При необходимости в первом триместре рекомендуемая доза составляет 150 мкг. Одноразовая доза 300 мкг анти-RhD должна предотвратить изоиммунизацию, когда 15 мл или менее фетальных эритроцитов (или 30 мл цельной крови) попадает в кровоток матери. Тест на розетку — это качественный тест для оценки потенциальной FMH. В случае положительного результата за розеточным тестом следует провести тест Кляйхауэра-Бетке, чтобы количественно определить количество смешиваемой крови плода и матери, чтобы затем определить, нужны ли дополнительные дозы Rh-D-иммунопрофилактики.
Прогноз
Общий прогноз ГБПН благоприятный при своевременном выявлении и лечении. Хотя необратимая неврологическая дисфункция может быть результатом задержек в оказании помощи, в настоящее время это редкое явление благодаря достижениям в области мониторинга, а также профилактики ГБПН.
Осложнения
Острая билирубиновая энцефалопатия из-за накопления билирубина в мозгу младенца может проявляться гипотонией или плохим сосательным рефлексом, который затем прогрессирует до раздражительности и гипертонии с ретроколлисом и опистотонусом. Долгосрочные последствия хронической билирубиновой энцефалопатии могут привести к церебральному параличу, слуховой дисфункции, параличу взгляда вверх и стойкой интеллектуальной дисфункции.[13] Таким образом, раннее распознавание и лечение необходимы для предотвращения неблагоприятного прогрессирования ГБПН.
Предупреждение и обучение пациентов
Обучение пациентов в отношении рутинных лабораторных анализов и Rh-иммунопрофилактики у резус-отрицательных женщин необходимо для обеспечения регистрации возможных случаев FMH и надлежащего лечения беременных женщин. Кроме того, родители новорожденных могут быть проинформированы о признаках и симптомах, чтобы знать о гипербилирубинемии, чтобы помочь межпрофессиональной команде в раннем выявлении возможных случаев HDFN.
Улучшение результатов работы команды здравоохранения
Улучшение результатов межпрофессиональной бригады для пациентов с гемолитической болезнью плода и новорожденного требует тесного сотрудничества между акушерами-гинекологами и педиатрами, медсестрами, фармацевтами и персоналом банка крови. При ГБПН всегда необходимо учитывать двух пациентов — мать и плод/новорожденный. Когда ГБПН выявляется внутриутробно, родовспоможение должно быть хорошо осведомлено и заранее подготовлено для выявления признаков и симптомов ГБПН, поскольку этим детям может потребоваться своевременное переливание крови при рождении. Фармацевты и поставщики медицинских услуг должны определить, показана ли иммунопрофилактика резус-фактора D для предотвращения будущих случаев ГБПН на протяжении всей беременности. Благодаря развитию Rh-D-иммунопрофилактики и протоколов обследования новорожденных заболеваемость HDFN резко снизилась за последние 50 лет. Тем не менее, для обеспечения низкого уровня заболеваемости HDFN потребуется постоянное межпрофессиональное сотрудничество.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ree IMC, Smits-Wintjens VEHJ, van der Bom JG, van Klink JMM, Oepkes D, Lopriore E. Ведение новорожденных и исходы при аллоиммунном гемофилии литическая болезнь. Эксперт преподобный Гематол. 2017 июль; 10 (7): 607-616. [PubMed: 28503958]
- 2.
Basu S, Kaur R, Kaur G. Гемолитическая болезнь плода и новорожденного: современные тенденции и перспективы. Азиатский J Transfus Sci. 2011 янв;5(1):3-7. [Бесплатная статья PMC: PMC3082712] [PubMed: 21572705]
- 3.
де Хаас М., Тюрик Ф.Ф., Колевейн Дж.М., ван дер Шут С.Э. Гемолитическая болезнь плода и новорожденного. Вокс Санг. 2015 авг; 109 (2): 99-113. [PubMed: 25899660]
- 4.
Меткалф Р.А., Хан Дж., Эндрюс Дж., Мэйок Д., Биллимория З.
 , Пагано М.Б. Тяжелая гемолитическая болезнь АВО новорожденных, требующая обменного переливания крови. J Pediatr Hematol Oncol. 2019 ноябрь;41(8):632-634. [PubMed: 30044350]
, Пагано М.Б. Тяжелая гемолитическая болезнь АВО новорожденных, требующая обменного переливания крови. J Pediatr Hematol Oncol. 2019 ноябрь;41(8):632-634. [PubMed: 30044350]- 5.
Noronha SA. Приобретенная и врожденная гемолитическая анемия. Pediatr Rev. 2016 Jun;37(6):235-46. [В паблике: 27252179]
- 6.
Найман Ю.Л. О статье доктора Луи К. Даймонда 1932 года и последующем вкладе в эритробластоз плода. J Pediatr Hematol Oncol. 2001 ноябрь; 23 (8): 550-3. [PubMed: 11878786]
- 7.
Практический бюллетень ACOG № 192: Управление аллоиммунизацией во время беременности. Акушерство Гинекол. 2018 март; 131(3):e82-e90. [PubMed: 29470342]
- 8.
Мюррей Н.А., Робертс И.А. Гемолитическая болезнь новорожденных. Arch Dis Child Fetal Neonatal Ed. 2007 март;92(2):F83-8. [Бесплатная статья PMC: PMC2675453] [PubMed: 17337672]
- 9.
Делани М., Мэтьюз, округ Колумбия. Гемолитическая болезнь плода и новорожденного: ведение матери, плода и новорожденного.
 Гематология Программа Am Soc Hematol Educ. 2015;2015:146-51. [PubMed: 26637714]
Гематология Программа Am Soc Hematol Educ. 2015;2015:146-51. [PubMed: 26637714]- 10.
Практический бюллетень № 181: Профилактика Rh D Аллоиммунизация. Акушерство Гинекол. 2017 авг;130(2):e57-e70. [PubMed: 28742673]
- 11.
Moinuddin I, Fletcher C, Millward P. Распространенность и специфичность клинически значимых аллоантител к эритроцитам у беременных женщин — исследование, проведенное в больнице третичного уровня в Юго-восточном Мичигане. Дж. Кровь Мед. 2019;10:283-289. [Бесплатная статья PMC: PMC6708388] [PubMed: 31692490]
- 12.
Митра С., Ренни Дж. Желтуха новорожденных: этиология, диагностика и лечение. Br J Hosp Med (Лондон). 2017 02 декабря; 78 (12): 699-704. [PubMed: 29240507]
- 13.
Подкомитет Американской академии педиатрии по гипербилирубинемии. Лечение гипербилирубинемии у новорожденных в возрасте 35 и более недель гестации. Педиатрия. 2004 г., июль; 114 (1): 297–316.
 [В паблике: 15231951]
[В паблике: 15231951]- 14.
Li S, He Z, Mo C, Ji Y, Luo Y, Fang Q, Gao Y. Гипорегенеративная анемия при анти-М-ассоциированной гемолитической болезни плода. Переливание. 2021 июнь;61(6):1908-1915. [PubMed: 33938570]
- 15.
Саху Т., Тукрал А., Санкар М.Дж., Гупта С.К., Агарвал Р., Деорари А.К., Пол В.К. Отсроченное пережатие пуповины у Rh-аллоиммунизированных младенцев: рандомизированное контролируемое исследование. Eur J Педиатр. 2020 июнь; 179 (6): 881-889. [PubMed: 31974670]
- 16.
Xie X, Fu Q, Bao Z, Zhang Y, Zhou D. Клиническая ценность различных анти-D-иммуноглобулиновых стратегий для предотвращения резус-гемолитической болезни плода и новорожденного: сетевой метаанализ. ПЛОС Один. 2020;15(3):e0230073. [Бесплатная статья PMC: PMC7067404] [PubMed: 32163467]
Раскрытие информации: Виктория Холл заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.

Раскрытие информации: Indirapriya Darshini Avulakunta заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Гемолитические болезни новорожденных — StatPearls
Непрерывное обучение
Гемолитическая болезнь плода и новорожденного — это несоответствие эритроцитов между матерями и их плодами, которое может вызвать значительную заболеваемость и смертность. К счастью, фатальные последствия этого расстройства стали редкостью при соответствующем применении иммунопрофилактики. Однако, чтобы избежать фатальных последствий этого расстройства, жизненно важны своевременная диагностика и лечение. Это мероприятие рассматривает оценку, лечение и профилактику гемолитической болезни плода и новорожденного межпрофессиональной командой.
Цели:
Опишите этиологию и эпидемиологию гемолитической болезни плода и новорожденного.
Обзор патофизиологии гемолитической болезни плода и новорожденного.
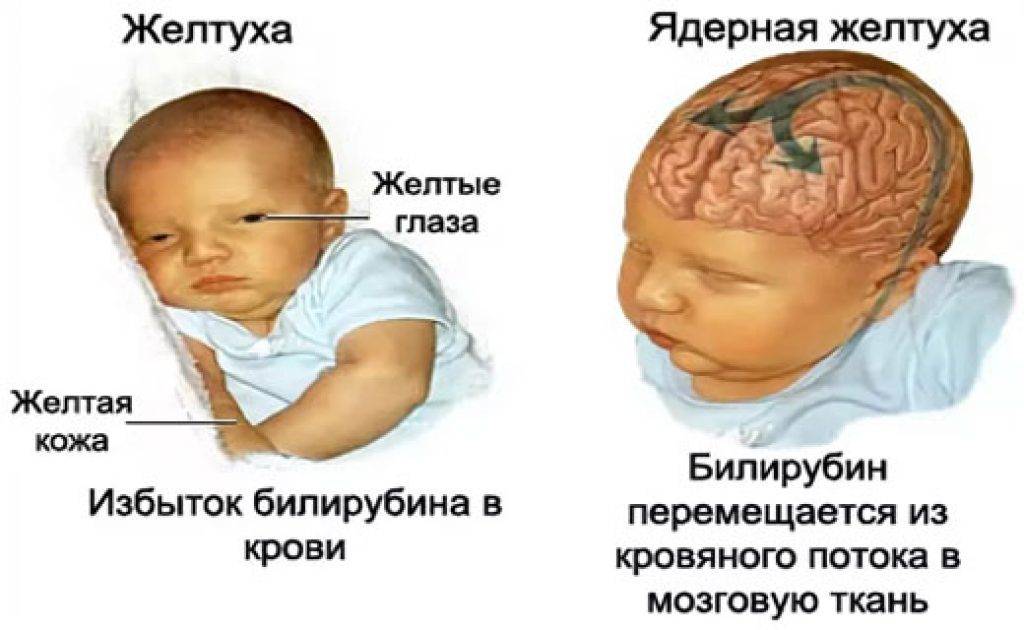
Схема лечения гемолитической болезни плода и новорожденного.
Обобщение межпрофессиональных командных стратегий по улучшению координации оказания медицинской помощи и коммуникации для улучшения лечения гемолитической болезни плода и новорожденного и улучшения исходов.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Гемолитическая болезнь плода и новорожденного (HDFN) представляет собой иммуноопосредованное заболевание эритроцитов (эритроцитов), при котором материнские антитела атакуют эритроциты плода или новорожденного.[1][2] HDFN может вызвать значительную заболеваемость и смертность, особенно в условиях ограниченных ресурсов здравоохранения. Эффекты HDFN варьируются от легкой анемии до водянки плода у плода и гипербилирубинемии и ядерной желтухи у новорожденных. Благодаря раннему выявлению, лечению и профилактике этого заболевания заболеваемость и распространенность ГБПН за последние 50 лет снизились в геометрической прогрессии. [1] 9[4] И наоборот, аллоиммунизация из-за фетоматеринского кровотечения (FMH) представляет собой приобретенный иммунно-опосредованный механизм, который обычно влияет на последующие беременности, а не на беременность, при которой происходит FMH.
[1] 9[4] И наоборот, аллоиммунизация из-за фетоматеринского кровотечения (FMH) представляет собой приобретенный иммунно-опосредованный механизм, который обычно влияет на последующие беременности, а не на беременность, при которой происходит FMH.
Эпидемиология
Гемолитическая болезнь плода и новорожденного впервые была описана доктором Луисом К. Даймондом в 1932, когда он написал об эритробластозе плода у новорожденных на основании мазков периферической крови.[6] Иммунопрофилактика резус-отрицательных (RhD) впервые была введена в 1968 году, благодаря чему заболеваемость ГБПН снизилась с 1% всех новорожденных во всем мире (с 50% смертностью) до 0,5% [1]. Заболеваемость HDFN снизилась еще больше до 0,1% при проведении дородовой иммунопрофилактики RhD [2]. Однако, несмотря на адекватную иммунопрофилактику RhD, по оценкам, от 1 до 3 из 1000 резус-отрицательных женщин все еще получают аллоиммунизацию. Таким образом, важно сохранять бдительность в отношении развития ГБПН.[1]
Резус-несовместимость зависит от расы, этнической принадлежности и факторов риска. Резус-отрицательная группа крови наиболее преобладает у белых рас (15%) по сравнению с афроамериканцами (от 5% до 8%) или азиатами и коренными американцами (от 1% до 2%). Среди белых женщин резус-отрицательная женщина имеет 85% шанс спаривания с резус-положительным мужчиной.[1] Эта часто встречающаяся резус-несовместимость увеличивает риск ГБПН при любом событии СМГ.
Резус-отрицательная группа крови наиболее преобладает у белых рас (15%) по сравнению с афроамериканцами (от 5% до 8%) или азиатами и коренными американцами (от 1% до 2%). Среди белых женщин резус-отрицательная женщина имеет 85% шанс спаривания с резус-положительным мужчиной.[1] Эта часто встречающаяся резус-несовместимость увеличивает риск ГБПН при любом событии СМГ.
Всего 0,1 мл крови плода, попадающей в кровоток матери, достаточно для аллоиммунизации.[7] Фактически, от 15 до 50 % беременных имеют достаточно фетально-материнских кровотечений, чтобы вызвать аллоиммунизацию, и только от 1 до 2 % всех резус-аллоиммунизаций вызваны дородовой FMH.[7] Таким образом, важно учитывать ГБПН на всех стадиях беременности, когда может возникнуть ЗМГ.
Патофизиология
Как уже упоминалось, существует два механизма, вызывающих гемолитическую болезнь плода и новорожденного. Во-первых, фето-материнская пара может иметь врожденную несовместимость по системе АВО, которая возникает в 15 – 25 % беременностей. [8] Только около 1% этих пар с высокими титрами IgG разовьют HDFN из-за несовместимости по системе ABO [8]. При несовместимости по системе ABO у матерей с группой крови O присутствуют естественные антигены против групп крови A или B. Если плод матери имеет группу крови A или B (или AB), материнские антитела анти-A и/или анти-B соответственно будут атаковать чужеродную группу крови плода. Антитела анти-А и анти-В представляют собой IgG, которые могут проникать через плаценту и воздействовать на развивающийся плод.[9]] По сравнению с FMH, несовместимость по системе ABO обычно вызывает менее тяжелую форму HDFN. Постулированные теории для этого включают в себя фетальные эритроциты экспрессируют меньше антигенов группы крови ABO, чем взрослые, и что антигены группы крови ABO экспрессируются многими тканями, что снижает вероятность того, что антитела специфически нацелены на антигены на фетальных эритроцитах.
[8] Только около 1% этих пар с высокими титрами IgG разовьют HDFN из-за несовместимости по системе ABO [8]. При несовместимости по системе ABO у матерей с группой крови O присутствуют естественные антигены против групп крови A или B. Если плод матери имеет группу крови A или B (или AB), материнские антитела анти-A и/или анти-B соответственно будут атаковать чужеродную группу крови плода. Антитела анти-А и анти-В представляют собой IgG, которые могут проникать через плаценту и воздействовать на развивающийся плод.[9]] По сравнению с FMH, несовместимость по системе ABO обычно вызывает менее тяжелую форму HDFN. Постулированные теории для этого включают в себя фетальные эритроциты экспрессируют меньше антигенов группы крови ABO, чем взрослые, и что антигены группы крови ABO экспрессируются многими тканями, что снижает вероятность того, что антитела специфически нацелены на антигены на фетальных эритроцитах.
Вторым механизмом, наиболее часто вызывающим ГБПН, является фетоматеринское кровотечение (ФМК), при котором материнские антитела вырабатываются после контакта с кровью плода. Когда эритроциты плода попадают в кровоток матери, материнские антитела могут вырабатываться к антигену, представленному на поверхности эритроцитов плода. Наиболее распространенным антигеном, участвующим в этом механизме, является антиген резуса D.[10] По оценкам, у 1,5–2,5% акушерских пациенток вырабатываются антитела к другим «второстепенным» антигенам. Хотя в большинстве этих случаев аллоиммунизация не вызывает значимой гемолитической болезни новорожденных, некоторые могут вызывать тяжелую анемию при низком пороге титра. Антитела против антигенов группы крови Келла, например, связаны с повышенным риском тяжелой анемии и/или гибели плода. Эти пациенты должны находиться под очень пристальным наблюдением на протяжении всей беременности.[3][7]
Когда эритроциты плода попадают в кровоток матери, материнские антитела могут вырабатываться к антигену, представленному на поверхности эритроцитов плода. Наиболее распространенным антигеном, участвующим в этом механизме, является антиген резуса D.[10] По оценкам, у 1,5–2,5% акушерских пациенток вырабатываются антитела к другим «второстепенным» антигенам. Хотя в большинстве этих случаев аллоиммунизация не вызывает значимой гемолитической болезни новорожденных, некоторые могут вызывать тяжелую анемию при низком пороге титра. Антитела против антигенов группы крови Келла, например, связаны с повышенным риском тяжелой анемии и/или гибели плода. Эти пациенты должны находиться под очень пристальным наблюдением на протяжении всей беременности.[3][7]
Антигены крови плода, чужеродные материнской крови, наследуются от отцовских генов. Например, у резус-отрицательной женщины может быть резус-положительный плод из-за того, что ее партнер является резус-положительным. Антитела, которые развиваются из-за FMH, подвергают последующие беременности риску HDFN, поскольку первые вырабатываемые антитела относятся к типу IgM, которые не могут проникать через плаценту. При последующих контактах с антигеном Rh-D материнские антитела быстро вырабатывают антитела IgG, которые проникают через плаценту.[11]
При последующих контактах с антигеном Rh-D материнские антитела быстро вырабатывают антитела IgG, которые проникают через плаценту.[11]
Когда эритроциты младенцев подвергаются атаке и разрушаются, у младенцев развивается гемолитическая анемия. Расщепление гема приводит к образованию билирубина, который выводится плацентой внутриутробно. При рождении печень начинает обрабатывать билирубин. Непрямой билирубин или неконъюгированный билирубин конъюгируют с прямым билирубином с помощью фермента уридиндифосфоглюкуронозилтрансферазы (УДФ-глюкуронозилтрансферазы). Этот конъюгированный билирубин выводится с желчью, где в конечном итоге будет выводиться с фекалиями и мочой.
У младенцев, особенно недоношенных, процессинг печени менее эффективен, что часто приводит к естественной физиологической желтухе.[12] При избытке продуктов распада HDFN эти незрелые механизмы процессинга перегружаются, что может привести к выраженной гипербилирубинемии. Накопление несвязанного билирубина может привести к неврологической дисфункции, поскольку несвязанный билирубин пересекает гематоэнцефалический барьер и откладывается в головном мозге развивающегося новорожденного. [13] Своевременное распознавание и лечение гипербилирубинемии и ГБПН имеют первостепенное значение для предотвращения долгосрочной неврологической дисфункции у этих детей.
[13] Своевременное распознавание и лечение гипербилирубинемии и ГБПН имеют первостепенное значение для предотвращения долгосрочной неврологической дисфункции у этих детей.
Анамнез и физикальное исследование
Подробный анамнез может иметь важное значение для подозрения на гемолитическую болезнь плода и новорожденного. Особое внимание следует уделить выявлению любых событий, которые могли привести к фетоматеринскому кровотечению. К ним относятся предыдущие беременности с ГБПН или водянкой плода, выкидыши, внематочная беременность, прерывание беременности на ранних сроках, переливание крови у матери, забор ворсин хориона, амниоцентез или документирование кровотечения во время беременности [7].
В начале первого триместра всем беременным женщинам следует провести анализ крови. Люди с группой крови O естественным образом экспрессируют антитела к группам крови A и B; таким образом, их следует контролировать на предмет развития ГБПН, особенно в родах и сразу после родов. Антитела, экспрессируемые у матерей с группой крови O, обычно представляют собой иммуноглобулин G (IgG) и могут проникать через плаценту. И наоборот, у матерей с группой крови А есть антитела против группы крови В, которые представляют собой преимущественно иммуноглобулины М (IgM) и не проникают через плаценту.[8] Общепринятой практикой является проверка групп крови младенцев, рожденных от матерей с группой крови О при рождении, в то время как группы крови младенцев, матери которых имеют группу крови А, В или АВ, могут не проверяться (если резус-фактор положительный). .
Антитела, экспрессируемые у матерей с группой крови O, обычно представляют собой иммуноглобулин G (IgG) и могут проникать через плаценту. И наоборот, у матерей с группой крови А есть антитела против группы крови В, которые представляют собой преимущественно иммуноглобулины М (IgM) и не проникают через плаценту.[8] Общепринятой практикой является проверка групп крови младенцев, рожденных от матерей с группой крови О при рождении, в то время как группы крови младенцев, матери которых имеют группу крови А, В или АВ, могут не проверяться (если резус-фактор положительный). .
Основными признаками гемолитической болезни новорожденных (ГБН) являются анемия и гипербилирубинемия, которые могут проявляться вялостью, желтухой, желтухой конъюнктивы, бледностью, гепатоспленомегалией, тахикардией или брадикардией, повышенной потребностью в кислороде и/или апноэ.[9] [13]
Оценка
Гемолитическая болезнь плода и новорожденного следует учитывать при дифференциальной диагностике новорожденных с желтухой/гипербилирубинемией и, безусловно, в случае неонатальной анемии. Диагноз HDFN может быть поставлен путем определения наличия материнских антител к эритроцитам (агглютинация в непрямом тесте на антитела) и/или положительного прямого теста на антитела (DAT) в сыворотке младенца.[4] Если у беременной женщины выявлена аллоиммунизация, первым шагом в дальнейшем обследовании является определение антигенного статуса эритроцитов отца. В случае положительного результата следующим шагом будет определение группы крови плода, что обычно делается с помощью амниоцентеза.[7]
Диагноз HDFN может быть поставлен путем определения наличия материнских антител к эритроцитам (агглютинация в непрямом тесте на антитела) и/или положительного прямого теста на антитела (DAT) в сыворотке младенца.[4] Если у беременной женщины выявлена аллоиммунизация, первым шагом в дальнейшем обследовании является определение антигенного статуса эритроцитов отца. В случае положительного результата следующим шагом будет определение группы крови плода, что обычно делается с помощью амниоцентеза.[7]
По данным Американской академии педиатрии (AAP), «если у матери не было пренатальной группы крови или она резус-отрицательна, прямой тест на антитела (или тест Кумбса), группа крови и резус-фактор (D) на (пуповинной) крови младенца настоятельно рекомендуется». возможно при беременности. Пораженные беременности можно контролировать путем мониторинга титров антител и скорости движения средней мозговой артерии плода, внутриутробных трансфузий и, возможно, досрочных родов, поскольку дети с тяжелой анемией могут плохо переносить срочные роды.
Гемолитическая болезнь новорожденных лечится путем лечения гипербилирубинемии фототерапией и при необходимости обменными трансфузиями. Рутинный универсальный скрининг чрескожного билирубина (TcB) часто проводится в первые 24 часа жизни, но скрининг следует проводить, как только подозревается гипербилирубинемия. Повышенный TcB всегда следует подтверждать с помощью общего билирубина сыворотки (ТБ). Затем почасовая номограмма Бутани используется для стратификации риска по количеству билирубина в крови младенца.[13] Эта номограмма обеспечивает рекомендуемый порог для начала фототерапии по сравнению с ранними трансфузиями в зависимости от уровня риска для младенца.
Фототерапия была внедрена в 1970-х годах и стала основой лечения гипербилирубинемии у новорожденных. Фотоизомеризация вызывает превращение билирубина в водорастворимый изомер, который затем может выводиться почками и калом без необходимости переработки в печени. Основными факторами, определяющими эффективность фототерапии, являются длина волны используемого света, интенсивность этого света, общая доза света (время воздействия и площадь поверхности воздействия) и порог, при котором начинается фототерапия. AAP рекомендует использовать интенсивную фототерапию при HDFN. Оптимальный свет, используемый для фототерапии, имеет длину волны 460-490 нм. Свет должен быть на близком расстоянии (около 20 см над младенцем), и двойная фототерапия оказалась более эффективной, чем одиночная. Имеются ограниченные данные об эффективности непрерывной фототерапии по сравнению с прерывистой для младенцев с массой тела > 2000 г [1]. Во время фототерапии матерей следует поощрять кормить своих детей грудью через определенные промежутки времени, несмотря на то, что для этого им необходимо отключать их от фототерапии.
AAP рекомендует использовать интенсивную фототерапию при HDFN. Оптимальный свет, используемый для фототерапии, имеет длину волны 460-490 нм. Свет должен быть на близком расстоянии (около 20 см над младенцем), и двойная фототерапия оказалась более эффективной, чем одиночная. Имеются ограниченные данные об эффективности непрерывной фототерапии по сравнению с прерывистой для младенцев с массой тела > 2000 г [1]. Во время фототерапии матерей следует поощрять кормить своих детей грудью через определенные промежутки времени, несмотря на то, что для этого им необходимо отключать их от фототерапии.
Обменное переливание может потребоваться для новорожденных с тяжелой анемией, которое включает замену эритроцитов новорожденных на антиген-отрицательные эритроциты, тем самым предотвращая дальнейший гемолиз. Аликвоты по 5 мл/кг удаляют и заменяют в течение нескольких минут для общего обмена эритроцитов на 25-50 мл/кг. Обменные переливания рекомендуются ААР, если уровни общего билирубина остаются выше порога переливания, несмотря на интенсивную фототерапию, или если присутствуют признаки билирубиновой энцефалопатии. Если рассматривается обменное переливание крови, следует измерить уровень альбумина. Альбумин 3,0 г/дл или менее считается независимым фактором риска гипербилирубинемии и снижает порог фототерапии. Без достаточного количества альбумина для связывания билирубина количество свободного неконъюгированного билирубина увеличивается, что увеличивает риск ядерной желтухи.[1]
Если рассматривается обменное переливание крови, следует измерить уровень альбумина. Альбумин 3,0 г/дл или менее считается независимым фактором риска гипербилирубинемии и снижает порог фототерапии. Без достаточного количества альбумина для связывания билирубина количество свободного неконъюгированного билирубина увеличивается, что увеличивает риск ядерной желтухи.[1]
Младенцам с анемией может потребоваться переливание крови с эритроцитарной массой, соответствующей системе ABO. Если считается, что необходима немедленная трансфузия, при родах должна быть доступна резус-отрицательная кровь O-типа, лейкодеплеция и облучение [1].
Были рассмотрены и другие методы лечения, но они все еще остаются спорными. Внутривенный иммуноглобулин (ВВИГ) у младенцев может блокировать рецепторы Fc на макрофагах, тем самым уменьшая разрушение эритроцитов, покрытых антителами. AAP рекомендует ВВИГ, если общий билирубин в сыворотке продолжает расти, несмотря на интенсивную фототерапию, или находится в пределах 2-3 мг/дл от уровня обменного переливания. Введение ВВИГ матерям до родов не показало своей эффективности и в настоящее время не рекомендуется. Другие агенты, такие как альбумин, фенобарбитал, металлопорфирины, цинк, клофибрат и пребиотики, изучались в качестве возможных вариантов лечения гипербилирубинемии, но в настоящее время ни один из них не рекомендован [14]. В недавнем рандомизированном контролируемом исследовании с участием 70 младенцев с Rh-аллоиммунизацией было показано, что отсроченное пережатие пуповины уменьшает анемию без увеличения частоты побочных эффектов. Однако отсроченное пережатие пуповины не оказало существенного влияния на потребность в обменном переливании крови или продолжительность фототерапии.[15]
Введение ВВИГ матерям до родов не показало своей эффективности и в настоящее время не рекомендуется. Другие агенты, такие как альбумин, фенобарбитал, металлопорфирины, цинк, клофибрат и пребиотики, изучались в качестве возможных вариантов лечения гипербилирубинемии, но в настоящее время ни один из них не рекомендован [14]. В недавнем рандомизированном контролируемом исследовании с участием 70 младенцев с Rh-аллоиммунизацией было показано, что отсроченное пережатие пуповины уменьшает анемию без увеличения частоты побочных эффектов. Однако отсроченное пережатие пуповины не оказало существенного влияния на потребность в обменном переливании крови или продолжительность фототерапии.[15]
Дифференциальный диагноз
Гемолитическая болезнь плода и новорожденного должна быть включена в дифференциальный диагноз младенцев с ранней, тяжелой или длительной желтухой и анемией. Другие причины желтухи и гипербилирубинемии у новорожденных включают физиологическую желтуху, недоношенность, желтуху грудного молока и грудного вскармливания, дефицит G6PD, талассемию, сепсис, родовую травму, синдром Жильбера и гипотиреоз [3]. Сбор анамнеза и физикальное, а также простое лабораторное обследование, как описано выше, могут помочь дифференцировать эти причины.
Сбор анамнеза и физикальное, а также простое лабораторное обследование, как описано выше, могут помочь дифференцировать эти причины.
Планирование лечения
Американская ассоциация банков крови рекомендует повторный скрининг на антитела перед введением Rh-D иммунопрофилактики (Rh-D IgG) на 28 неделе беременности, в послеродовой период и при FMH[5]. В сетевом метаанализе, проведенном в Китае, наиболее эффективным протоколом для предотвращения материнской аллоиммунизации было введение Rh-D-иммунопрофилактики на 28 и 34 неделе беременности у резус-отрицательных женщин.[16]
Стандартная доза анти-RhD, вводимая во втором и третьем триместрах беременности и в послеродовом периоде, при необходимости, составляет 300 мкг. При необходимости в первом триместре рекомендуемая доза составляет 150 мкг. Одноразовая доза 300 мкг анти-RhD должна предотвратить изоиммунизацию, когда 15 мл или менее фетальных эритроцитов (или 30 мл цельной крови) попадает в кровоток матери. Тест на розетку — это качественный тест для оценки потенциальной FMH. В случае положительного результата за розеточным тестом следует провести тест Кляйхауэра-Бетке, чтобы количественно определить количество смешиваемой крови плода и матери, чтобы затем определить, нужны ли дополнительные дозы Rh-D-иммунопрофилактики.
В случае положительного результата за розеточным тестом следует провести тест Кляйхауэра-Бетке, чтобы количественно определить количество смешиваемой крови плода и матери, чтобы затем определить, нужны ли дополнительные дозы Rh-D-иммунопрофилактики.
Прогноз
Общий прогноз ГБПН благоприятный при своевременном выявлении и лечении. Хотя необратимая неврологическая дисфункция может быть результатом задержек в оказании помощи, в настоящее время это редкое явление благодаря достижениям в области мониторинга, а также профилактики ГБПН.
Осложнения
Острая билирубиновая энцефалопатия из-за накопления билирубина в мозгу младенца может проявляться гипотонией или плохим сосательным рефлексом, который затем прогрессирует до раздражительности и гипертонии с ретроколлисом и опистотонусом. Долгосрочные последствия хронической билирубиновой энцефалопатии могут привести к церебральному параличу, слуховой дисфункции, параличу взгляда вверх и стойкой интеллектуальной дисфункции. [13] Таким образом, раннее распознавание и лечение необходимы для предотвращения неблагоприятного прогрессирования ГБПН.
[13] Таким образом, раннее распознавание и лечение необходимы для предотвращения неблагоприятного прогрессирования ГБПН.
Предупреждение и обучение пациентов
Обучение пациентов в отношении рутинных лабораторных анализов и Rh-иммунопрофилактики у резус-отрицательных женщин необходимо для обеспечения регистрации возможных случаев FMH и надлежащего лечения беременных женщин. Кроме того, родители новорожденных могут быть проинформированы о признаках и симптомах, чтобы знать о гипербилирубинемии, чтобы помочь межпрофессиональной команде в раннем выявлении возможных случаев HDFN.
Улучшение результатов работы команды здравоохранения
Улучшение результатов межпрофессиональной бригады для пациентов с гемолитической болезнью плода и новорожденного требует тесного сотрудничества между акушерами-гинекологами и педиатрами, медсестрами, фармацевтами и персоналом банка крови. При ГБПН всегда необходимо учитывать двух пациентов — мать и плод/новорожденный. Когда ГБПН выявляется внутриутробно, родовспоможение должно быть хорошо осведомлено и заранее подготовлено для выявления признаков и симптомов ГБПН, поскольку этим детям может потребоваться своевременное переливание крови при рождении. Фармацевты и поставщики медицинских услуг должны определить, показана ли иммунопрофилактика резус-фактора D для предотвращения будущих случаев ГБПН на протяжении всей беременности. Благодаря развитию Rh-D-иммунопрофилактики и протоколов обследования новорожденных заболеваемость HDFN резко снизилась за последние 50 лет. Тем не менее, для обеспечения низкого уровня заболеваемости HDFN потребуется постоянное межпрофессиональное сотрудничество.
Фармацевты и поставщики медицинских услуг должны определить, показана ли иммунопрофилактика резус-фактора D для предотвращения будущих случаев ГБПН на протяжении всей беременности. Благодаря развитию Rh-D-иммунопрофилактики и протоколов обследования новорожденных заболеваемость HDFN резко снизилась за последние 50 лет. Тем не менее, для обеспечения низкого уровня заболеваемости HDFN потребуется постоянное межпрофессиональное сотрудничество.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ree IMC, Smits-Wintjens VEHJ, van der Bom JG, van Klink JMM, Oepkes D, Lopriore E. Ведение новорожденных и исходы при аллоиммунном гемофилии литическая болезнь. Эксперт преподобный Гематол. 2017 июль; 10 (7): 607-616. [PubMed: 28503958]
- 2.
Basu S, Kaur R, Kaur G. Гемолитическая болезнь плода и новорожденного: современные тенденции и перспективы.
 Азиатский J Transfus Sci. 2011 янв;5(1):3-7. [Бесплатная статья PMC: PMC3082712] [PubMed: 21572705]
Азиатский J Transfus Sci. 2011 янв;5(1):3-7. [Бесплатная статья PMC: PMC3082712] [PubMed: 21572705]- 3.
де Хаас М., Тюрик Ф.Ф., Колевейн Дж.М., ван дер Шут С.Э. Гемолитическая болезнь плода и новорожденного. Вокс Санг. 2015 авг; 109 (2): 99-113. [PubMed: 25899660]
- 4.
Меткалф Р.А., Хан Дж., Эндрюс Дж., Мэйок Д., Биллимория З., Пагано М.Б. Тяжелая гемолитическая болезнь АВО новорожденных, требующая обменного переливания крови. J Pediatr Hematol Oncol. 2019 ноябрь;41(8):632-634. [PubMed: 30044350]
- 5.
Noronha SA. Приобретенная и врожденная гемолитическая анемия. Pediatr Rev. 2016 Jun;37(6):235-46. [В паблике: 27252179]
- 6.
Найман Ю.Л. О статье доктора Луи К. Даймонда 1932 года и последующем вкладе в эритробластоз плода. J Pediatr Hematol Oncol. 2001 ноябрь; 23 (8): 550-3. [PubMed: 11878786]
- 7.
Практический бюллетень ACOG № 192: Управление аллоиммунизацией во время беременности.
 Акушерство Гинекол. 2018 март; 131(3):e82-e90. [PubMed: 29470342]
Акушерство Гинекол. 2018 март; 131(3):e82-e90. [PubMed: 29470342]- 8.
Мюррей Н.А., Робертс И.А. Гемолитическая болезнь новорожденных. Arch Dis Child Fetal Neonatal Ed. 2007 март;92(2):F83-8. [Бесплатная статья PMC: PMC2675453] [PubMed: 17337672]
- 9.
Делани М., Мэтьюз, округ Колумбия. Гемолитическая болезнь плода и новорожденного: ведение матери, плода и новорожденного. Гематология Программа Am Soc Hematol Educ. 2015;2015:146-51. [PubMed: 26637714]
- 10.
Практический бюллетень № 181: Профилактика Rh D Аллоиммунизация. Акушерство Гинекол. 2017 авг;130(2):e57-e70. [PubMed: 28742673]
- 11.
Moinuddin I, Fletcher C, Millward P. Распространенность и специфичность клинически значимых аллоантител к эритроцитам у беременных женщин — исследование, проведенное в больнице третичного уровня в Юго-восточном Мичигане. Дж. Кровь Мед. 2019;10:283-289. [Бесплатная статья PMC: PMC6708388] [PubMed: 31692490]
- 12.

Митра С., Ренни Дж. Желтуха новорожденных: этиология, диагностика и лечение. Br J Hosp Med (Лондон). 2017 02 декабря; 78 (12): 699-704. [PubMed: 29240507]
- 13.
Подкомитет Американской академии педиатрии по гипербилирубинемии. Лечение гипербилирубинемии у новорожденных в возрасте 35 и более недель гестации. Педиатрия. 2004 г., июль; 114 (1): 297–316. [В паблике: 15231951]
- 14.
Li S, He Z, Mo C, Ji Y, Luo Y, Fang Q, Gao Y. Гипорегенеративная анемия при анти-М-ассоциированной гемолитической болезни плода. Переливание. 2021 июнь;61(6):1908-1915. [PubMed: 33938570]
- 15.
Саху Т., Тукрал А., Санкар М.Дж., Гупта С.К., Агарвал Р., Деорари А.К., Пол В.К. Отсроченное пережатие пуповины у Rh-аллоиммунизированных младенцев: рандомизированное контролируемое исследование. Eur J Педиатр. 2020 июнь; 179 (6): 881-889. [PubMed: 31974670]
- 16.
Xie X, Fu Q, Bao Z, Zhang Y, Zhou D.