Чем лечить цистит у детей 10 лет: Цистит у детей — причины, симптомы, методы диагностики и лечения цистита у детей в клинике для детей и подростков «СМ-Клиника»
Симптомы и лечение цистита у детей
Дата последнего обновления: 19.09.2022 г.
Содержание:
Описание заболевания и симптомы
Классификация заболевания
Причины цистита у детей
Диагностика цистита
Как лечить цистит у детей
Профилактика заболевания
Любой женщине знакомо это неприятное и мучительное заболевание. У детей симптомы цистита тоже появляются довольно часто. Хотя воспаление слизистой мочевого пузыря затрагивает не только женский пол, но преимущественно встречается у женщин и девочек. Однако у детей младшего возраста (до трех лет) количество случаев болезни примерно одинаковое вне зависимости от пола.
По данным статистики, девочки заболевают циститом в 3–5 раз чаще мальчиков. Этому есть объяснение: строение мочеполовой системы у девочек позволяет инфекции проникнуть в мочевой пузырь гораздо проще и быстрее, чем у мальчиков или мужчин.
Женская уретра широкая и короткая, и по ней без помех могут перемещаться микробы. Против девочек играет и близкое расположение анального отверстия и влагалища к отверстию уретры. Если добавить сюда частое инфицирование наружных половых органов, картина получится полной.
Против девочек играет и близкое расположение анального отверстия и влагалища к отверстию уретры. Если добавить сюда частое инфицирование наружных половых органов, картина получится полной.
Поэтому девочкам, а позже женщинам, важно своевременно проводить гигиенические процедуры и делать это с учетом физиологии. Научив дочь правильно подмываться, мама избавит ее от многих проблем в будущем.
По своей сути цистит — это воспаление слизистой мочевого пузыря, приводящее к неправильной работе последнего. Симптомы практически одинаковые у детей мужского и женского пола. Это частые позывы в туалет и мочеиспускание с болью или резью в нижней части живота, также встречается выделение крови с мочой.
Частые позывы к мочеиспусканию, как правило, не приводят к облегчению. Более того, остается чувство сильной наполненности мочевого пузыря. У детей часто возникает недержание мочи. Родителям следует знать о таком проявлении заболевания и не стыдить, а тем более не наказывать ребенка. Это симптом болезни, а не детская прихоть.
Это симптом болезни, а не детская прихоть.
У совсем маленьких детей можно заподозрить цистит, если ребенок становится беспокойным, а при мочеиспусканиях начинает плакать и кричать.
Температура при цистите, как правило, не повышается или повышается незначительно — до 37° C. Исключение бывает, если присоединяется воспаление почек: тогда температура достигает 38° C и более. Это повод немедленно обратиться к врачу! В целом при цистите общее состояние остается в норме.
Циститы подразделяются на первичные и вторичные. Первичные появляются без отягощения другими заболеваниями, вторичные — на фоне других инфекций или болезненных состояний, а также на фоне патологии развития органов. Как правило, у детей младшего возраста острый цистит возникает как вторичное заболевание.
По характеру протекания можно выделить острый цистит, возникший впервые, и хронический, который проявляется у ребенка уже не в первый раз. Хронические циститы могут давать о себе знать несколько раз в год.
По природе заболевания различают несколько видов:
По степени распространения цистит может быть диффузным и очаговым.
По морфологии выделяются такие типы цистита:
катаральный;
гнойный;
геморрагический;
язвенный;
гангренозный и др.
Цистит может быть неосложненным или сопровождаться иными инфекциями.
Есть несколько основных причин, способных привести к циститу:
Недостаток или избыток гигиены. И то и другое плохо: при недостаточной гигиене патогенные бактерии из кишечника и влагалища могут массово попадать в уретру и провоцировать воспаление. При избыточной гигиене вымывается вся полезная микрофлора, слизистые ребенка становятся беззащитными даже перед единичными бактериями, попадающими в мочеполовой тракт.
Переохлаждение ребенка и снижение иммунитета вследствие простудных заболеваний.
Аномалии развития мочевой системы и сопутствующие заболевания: спайки уретры, синехии, сахарный диабет и другие эндокринные заболевания, патология развития почек и т.
 д.
д.Цистит у детей иногда возникает как побочное действие некоторых лекарств.
Влияние внешних факторов, таких как радиация, химическое отравление и прочие.
Кроме того, цистит может наблюдаться при наличии новообразований, а также при нарушениях со стороны центральной нервной системы.
Выделяют несколько путей распространения инфекции:
Восходящая инфекция, когда патогенные бактерии перемещаются по органам мочеполовой системы вверх. Проводником для инфекции выступает уретра, в которую бактерии попадают из анального отверстия и влагалища. Это самый распространенный путь проникновения заболевания в мочевой пузырь.
Нисходящее инфицирование имеет место, например, когда патогенные микробы спускаются из почечных лоханок в мочевой пузырь.
Проникновение из других органов малого таза или из дальних очагов заражения. Этот путь возникновения цистита встречается намного реже и характерен для заболеваний, уже имеющихся в организме ребенка.
 Например, заболевание развивается как осложнение после перенесенной инфекции.
Например, заболевание развивается как осложнение после перенесенной инфекции.
Как правило, симптомы цистита очень характерные, по одним только жалобам можно заподозрить это заболевание. Однако в ряде случаев требуются дополнительные методы диагностики.
Для определения цистита прежде всего назначается анализ мочи. Признаками цистита у ребенка являются повышенный уровень лейкоцитов, избыточное количество плоского эпителия и наличие бактерий. Если в полость мочевого пузыря выделяется кровь, она также может присутствовать в анализе. Сама моча меняет цвет на темный, становится мутной, иногда с добавлением белковых хлопьев.
Кроме общего анализа мочи, назначается также посев на флору, чтобы определить, какими именно микроорганизмами вызвано заболевание.
Очень важно при диагностике отличить цистит от других похожих заболеваний. В частности, от вульвита и вульвовагинита у девочек и фимоза и баланита у мальчиков. Поможет в этом детальный осмотр наружных половых органов. Альтернативный вариант — взять анализ мочи с помощью катетера, чтобы исключить попадание в нее лейкоцитов из половых органов.
Поможет в этом детальный осмотр наружных половых органов. Альтернативный вариант — взять анализ мочи с помощью катетера, чтобы исключить попадание в нее лейкоцитов из половых органов.
По симптомам цистит имеет сходство с пиелонефритом, и выявить отличия бывает очень сложно. Единственный способ — наблюдение пациента в динамике, поскольку по мере развития пиелонефрита клиническая картина меняется.
Главная цель лечения детского цистита состоит в том, чтобы как можно раньше ликвидировать воспалительный процесс в мочевом пузыре, а также подавить размножение патогенных микробов и не дать им пойти дальше. Немаловажно также восстановить нормальную функцию мочевого пузыря и снять болевой синдром.
Как уже упоминалось, общее состояние у детей при этом заболевании остается удовлетворительным, однако во избежание лишнего стресса и ухудшения самочувствия лучше соблюдать постельный режим, особенно в активной стадии заболевания. По мере облегчения симптомов режим можно ослабить, перевести ребенка на полупостельный, а затем и домашний.
Важно! Значительно облегчает процесс выздоровления обильное питье, сохранение горизонтального положения тела и ограничение двигательной активности.
Большое значение имеет питание при цистите. Для скорейшего освобождения от неприятных ощущений следует отдать предпочтение молочно-растительной диете, исключив на время мясо. Острые и пряные блюда, а также фрукты и овощи с повышенным содержанием кислоты из рациона ребенка тоже убираются.
Не стоит забывать и про питьевой режим. Обильное теплое питье способствует промыванию почек и мочевого пузыря и нормализации их работы. В активную фазу заболевания пить нужно как можно больше.
Что касается лекарственной терапии от цистита для детей, врач наверняка назначит курс антибиотиков в форме суспензии. Волноваться не стоит: к услугам врачей хороший выбор антибактериальных средств последнего поколения. Курс применения таких препаратов при цистите обычно короткий — 5–7 дней.
К выбору препаратов для облегчения боли и лечения цистита нужно подойти очень внимательно, поскольку многие из них не подходят детям. Важно следовать принципу «не навреди». Также очень важно не допустить рецидивов этого крайне неприятного заболевания.
Поэтому лучше отдать предпочтение хорошо известному и положительно зарекомендовавшему себя растительному лекарственному препарату Канефрон® Н. Лекарство выпускается в двух формах: капли для приема внутрь (разрешены детям с 1 года) и таблетки (для детей с 6 лет).
Для лечения препарат рекомендуется использовать в составе комплексной терапии, поскольку он усиливает действие антибиотиков, а также обладает выраженным спазмолитическим действием и снимает воспаление. После ослабления остроты заболевания следует продолжить терапию в течение 2–4 недель.
Прогноз лечения благоприятный. Если родители своевременно обратились к врачу и лечение начато сразу же, а рекомендации врача строго соблюдаются, симптомы цистита у детей проходят за одну-две недели.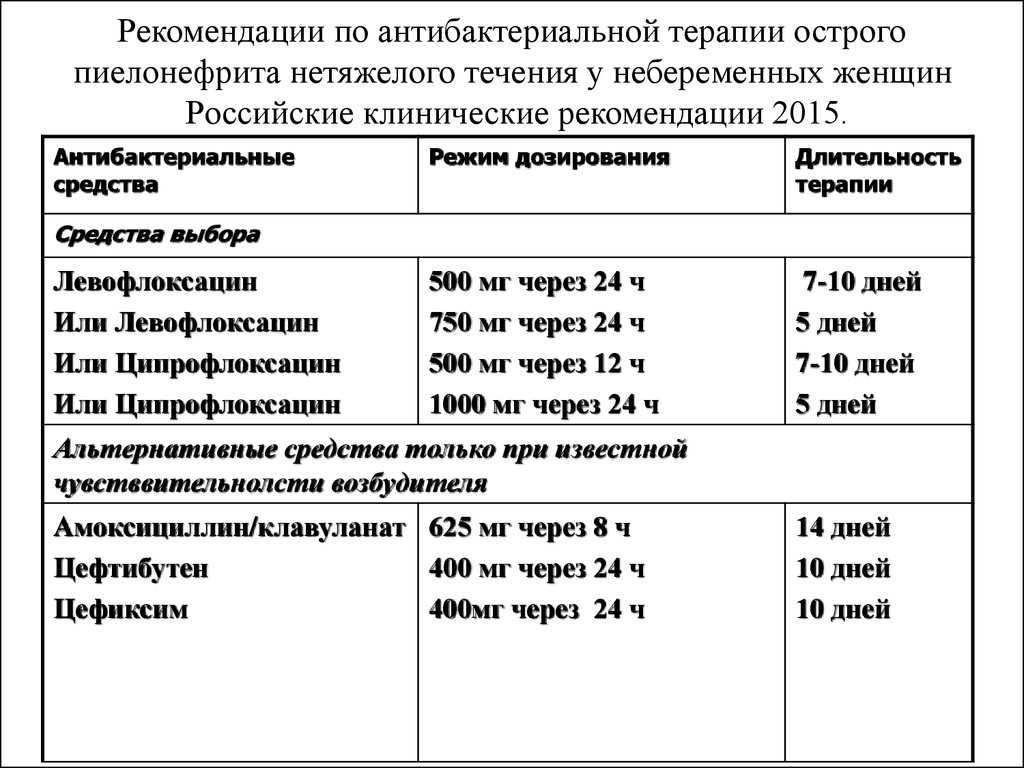
Вероятность повторного заболевания остается высокой, особенно при недолеченном цистите. Риск повышается и в случае, если не выявлена или неправильно определена основная причина заболевания.
Цистит может стать единственным неприятным воспоминанием, если придерживаться определенных правил и выполнять ряд мероприятий, направленных на защиту организма от этой напасти.
Рацион нужно составлять таким образом, чтобы он был сбалансированным, содержал все необходимые витамины и микроэлементы, а также включал минимум вредных для здоровья продуктов.
Питьевой режим не такой строгий, как при активной фазе болезни, но пить нужно достаточно. В объем получаемой жидкости входят супы и жидкие блюда. Если ребенок выпивает менее одного литра в день, увеличивается риск обострения цистита, а также других урологических проблем.
Одеваться следует по погоде: не переохлаждаться, но и не кутаться. Постепенно приучив ребенка к закаливанию, родители будут способствовать укреплению детского иммунитета. Не менее важна физическая активность. Длительные прогулки на воздухе, двигательная активность помогают циркуляции и обновлению крови и других жидкостей в организме.
Не менее важна физическая активность. Длительные прогулки на воздухе, двигательная активность помогают циркуляции и обновлению крови и других жидкостей в организме.
Необходимо своевременно опорожнять мочевой пузырь. Лучше лишний раз посетить туалет, даже если нет позывов. Это гораздо полезнее, чем терпеть, внезапно почувствовав потребность облегчиться в отсутствие туалета.
Инфекции, возникающие в организме, нужно всегда пролечивать. Недолеченная инфекция может стать входными воротами для цистита, который, перейдя в хроническую форму, будет досаждать еще много лет.
Если же заболевание перешло в хроническую форму или у ребенка сопутствующая патология мочевых путей, необходимо позаботиться о профилактике рецидива. Существует множество лекарственных средств, укрепляющих иммунитет и устраняющих патогенные бактерии, попавшие в мочевые пути ребенка.
Среди них важную роль занимают средства растительного происхождения, так как они обладают незначительным числом побочных эффектов, хорошо переносятся и могут назначаться для длительного применения. Это различные препараты клюквы, фиточаи и почечные сборы. При выборе фитопрепарата для профилактики лучше всего отдавать предпочтение проверенным и официально зарегистрированным лекарственным средствам.
Это различные препараты клюквы, фиточаи и почечные сборы. При выборе фитопрепарата для профилактики лучше всего отдавать предпочтение проверенным и официально зарегистрированным лекарственным средствам.
Лекарственный препарат на растительной основе Канефрон® Н прекрасно работает в качестве профилактического средства от рецидивов цистита у детей. Он способствует вымыванию патогенных бактерий, не накапливается в организме и может применяться курсами несколько раз в год, в том числе у маленьких детей и беременных женщин. Препарат отлично сочетается с другими видами терапии и даже усиливает действие уросептиков. Дозировка для дошкольников составляет 15 капель 3 раза в день, для детей с 7 лет — 25 капель либо 1 таблетка 3 раза в день.
Важно соблюдать правила личной гигиены, особенно девочкам. Водные процедуры нужно проводить регулярно. Половые органы следует подмывать движением спереди назад и ни в коем случае не менять направление.
Детям, у которых цистит перешел в хроническую форму, необходимо наблюдаться у врача и периодически сдавать анализ мочи, чтобы в случае рецидива выявить заболевание в начальной стадии.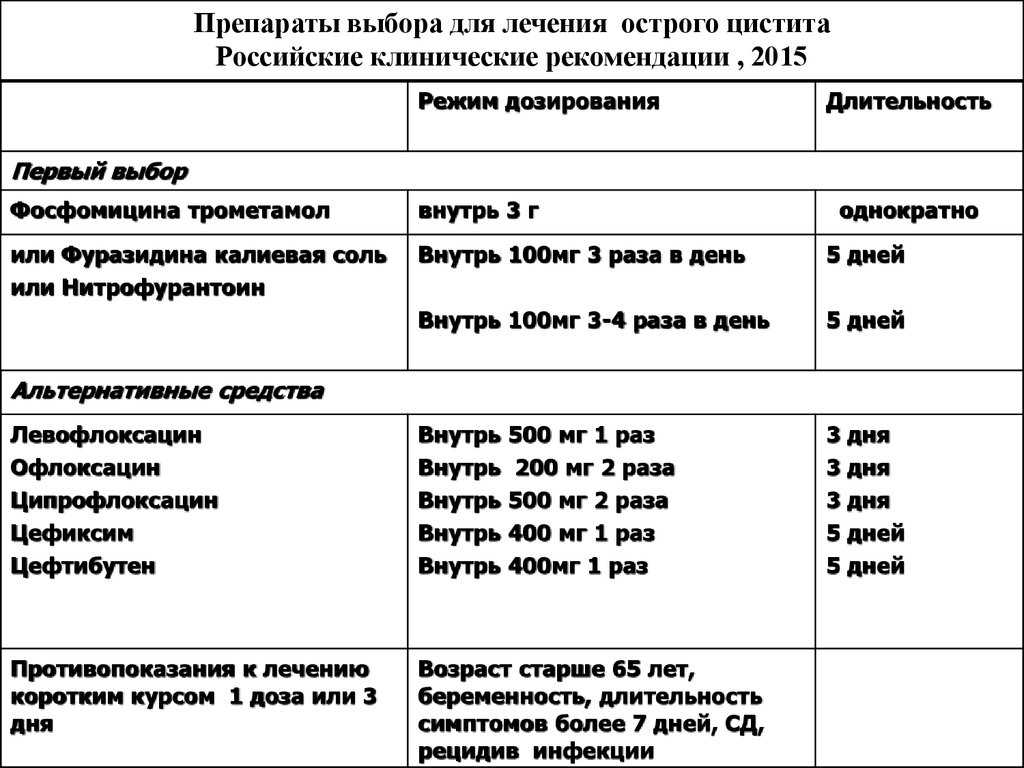 Легче предотвратить детский цистит, чем лечить рецидивы.
Легче предотвратить детский цистит, чем лечить рецидивы.
Цистит у детей — первые симптомы, причины возникновения, способы профилактика
Цистит — это воспалительное заболевание слизистой и подслизистого слоя мочевого пузыря.
Циститы встречаются у детей любого пола и возраста, но девочки дошкольного и младшего школьного возраста болеют им в пять-шесть раз чаще. Причина этого – особенности строения мочевыделительной системы (короткая уретра), поэтому инфекция легче может проникнуть в мочевой пузырь.
Причины
- Кишечная палочка, попавшая в мочевыводящие пути.
- Различные виды стафилококков, стрептококков, хламидий.
- Аномальное развитие органов – мочевыводящих путей, простаты, уретры.
- Глисты, острицы.
Симптомы
- Беспокойство малыша.
- Боли внизу живота.
- Помутнение мочи.
- Общее недомогание, слабость, вялость малыша.

- Плачь при мочеиспускании.
- Повышение температуры, иногда рвота, лихорадка.
У детей инфекция проходит быстро, если сразу же начинать ее лечить. В противном случае могут возникнуть серьезные последствия – снижение функции почек и даже сепсис.
Для диагностики цистита проводится анализ и посев мочи. Результаты бактериологического посева можно получить через 1-2 дня, но врач-уролог может назначить лечение на основании анализа мочи и осмотра.
Профилактика
- Соблюдать гигиену наружных половых органов.
- Исключить переохлаждение.
- Повышать иммунитет, сбалансировать поступление витаминов в организм.
- Своевременно обращаться за помощью к квалифицированному специалисту.
Подробнее о детской урологии в клинике «ЮгМед»
Оставляя свои персональные данные, Вы даете добровольное согласие на обработку своих персональных данных. Под персональными данными понимается любая информация, относящаяся к Вам, как субъекту персональных данных (ФИО, дата рождения, город проживания, адрес, контактный номер телефона, адрес электронной почты, род занятости и пр). Ваше согласие распространяется на осуществление Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» любых действий в отношении ваших персональных данных, которые могут понадобиться для сбора, систематизации, хранения, уточнения (обновление, изменение), обработки (например, отправки писем или совершения звонков) и т.п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
Под персональными данными понимается любая информация, относящаяся к Вам, как субъекту персональных данных (ФИО, дата рождения, город проживания, адрес, контактный номер телефона, адрес электронной почты, род занятости и пр). Ваше согласие распространяется на осуществление Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» любых действий в отношении ваших персональных данных, которые могут понадобиться для сбора, систематизации, хранения, уточнения (обновление, изменение), обработки (например, отправки писем или совершения звонков) и т.п. с учетом действующего законодательства. Согласие на обработку персональных данных даётся без ограничения срока, но может быть отозвано Вами (достаточно сообщить об этом в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед»). Пересылая в Общество с ограниченной ответственностью Научно-производственное объединение «Волгоградский центр профилактики болезней «ЮгМед» свои персональные данные, Вы подтверждаете, что с правами и обязанностями в соответствии с Федеральным законом «О персональных данных» ознакомлены.
Диагностика и лечение инфекций мочевыводящих путей у детей
БРЕТТ УАЙТ, MD
Острые инфекции мочевыводящих путей относительно часто встречаются у детей: 8% девочек и 2% мальчиков имеют по крайней мере один эпизод к семи годам жизни. Наиболее частым возбудителем является Escherichia coli , на долю которой приходится примерно 85 процентов инфекций мочевыводящих путей у детей. Дефекты почечной паренхимы обнаруживаются у 3-15% детей в течение одного-двух лет после первой диагностированной инфекции мочевыводящих путей. Клинические признаки и симптомы инфекции мочевыводящих путей зависят от возраста ребенка, но все лихорадящие дети в возрасте от 2 до 24 месяцев без очевидной причины инфекции должны быть обследованы на наличие инфекции мочевыводящих путей (за исключением обрезанных мальчиков старше 12 лет). месяцы). Обследование детей старшего возраста может зависеть от клинической картины и симптомов, указывающих на источник мочи (например, лейкоцитарная эстераза или нитрит, присутствующие при тестировании полосками; пиурия не менее 10 лейкоцитов в поле зрения с большим увеличением и бактериурия при микроскопии). Увеличены ставки Резистентность E. coli сделала амоксициллин менее приемлемым выбором для лечения, а исследования показали более высокие показатели излечения при применении триметоприма/сульфаметоксазола. Другие варианты лечения включают амоксициллин/клавуланат и цефалоспорины. Профилактическое назначение антибиотиков не снижает риск последующих инфекций мочевыводящих путей даже у детей с пузырно-мочеточниковым рефлюксом легкой и средней степени тяжести. Следует избегать запоров, чтобы предотвратить инфекции мочевыводящих путей. Ультразвуковое исследование, цистография и сканирование коры почек следует рассматривать у детей с инфекциями мочевыводящих путей.
месяцы). Обследование детей старшего возраста может зависеть от клинической картины и симптомов, указывающих на источник мочи (например, лейкоцитарная эстераза или нитрит, присутствующие при тестировании полосками; пиурия не менее 10 лейкоцитов в поле зрения с большим увеличением и бактериурия при микроскопии). Увеличены ставки Резистентность E. coli сделала амоксициллин менее приемлемым выбором для лечения, а исследования показали более высокие показатели излечения при применении триметоприма/сульфаметоксазола. Другие варианты лечения включают амоксициллин/клавуланат и цефалоспорины. Профилактическое назначение антибиотиков не снижает риск последующих инфекций мочевыводящих путей даже у детей с пузырно-мочеточниковым рефлюксом легкой и средней степени тяжести. Следует избегать запоров, чтобы предотвратить инфекции мочевыводящих путей. Ультразвуковое исследование, цистография и сканирование коры почек следует рассматривать у детей с инфекциями мочевыводящих путей.
Руководство по диагностике, лечению и последующему наблюдению за инфекциями мочевыводящих путей (ИМП) у детей продолжает развиваться. Хотя в настоящее время рекомендуется несколько менее агрессивный подход к оценке, для врачей первичного звена важно правильно диагностировать и лечить ИМП у детей. Некоторые основные этиологии, включая рубцевание почек и заболевания почек, могут привести к значительной заболеваемости в более позднем возрасте.
Хотя в настоящее время рекомендуется несколько менее агрессивный подход к оценке, для врачей первичного звена важно правильно диагностировать и лечить ИМП у детей. Некоторые основные этиологии, включая рубцевание почек и заболевания почек, могут привести к значительной заболеваемости в более позднем возрасте.
Острые ИМП относительно часто встречаются у детей. К семи годам у 8 процентов девочек и 2 процентов мальчиков будет хотя бы один эпизод. 1 В исследовании младенцев, поступающих в педиатрические отделения неотложной помощи, распространенность ИМП у младенцев в возрасте до 60 дней с температурой выше 100,4°F (38°C) составила 9 процентов. 2 Эталонный стандарт для диагностики ИМП представляет собой отдельный микроорганизм, выделенный из образца, полученного при следующих концентрациях: надлобковый аспирационный образец, более 1000 колониеобразующих единиц на мл; образец катетера, более 10 000 колониеобразующих единиц на мл; или чистый улов, средний образец, 100 000 колониеобразующих единиц на мл или больше. 3–5 Рекомендуется использовать более низкое количество колоний у пациентов с симптомами, 6 , хотя это не было включено в установленные руководства.
3–5 Рекомендуется использовать более низкое количество колоний у пациентов с симптомами, 6 , хотя это не было включено в установленные руководства.
Обычные уропатогены включают Escherichia coli (примерно 85 процентов UTI у детей), Klebsiella , Proteus , Enterobacter , Citrobacter , Staphyloccus saprophyticus 6666666666666666666666666666666666666666666. 6666666666. 66666666666666666666666 7 Систематический обзор показал, что дефекты почечной паренхимы выявляются у 3-15% детей в течение одного-двух лет после первой диагностированной ИМП. 8 Долгосрочные осложнения ИМП, связанные с рубцеванием почек, включают гипертонию, хроническую почечную недостаточность и токсикоз беременных. Данные долгосрочного наблюдения ограничены, хотя одно шведское исследование показало, что среди пациентов, перенесших рубцевание почек в результате пиелонефрита в детстве, у 23% развилась гипертония, а у 10% развилась терминальная стадия почечной недостаточности. 9 Однако более поздние исследования ставят под сомнение связь между пиелонефритом и терминальной стадией почечной недостаточности. 10 Исходные аномалии урогенитального тракта были зарегистрированы у 3,2% здоровых младенцев, прошедших скрининг. 11 Кроме того, обструктивные аномалии обнаруживаются у 4 %, а пузырно-мочеточниковый рефлюкс — у 8–40 % детей, обследованных на предмет первой ИМП. Дети младше двух лет могут подвергаться большему риску паренхиматозных дефектов, чем дети старшего возраста. 12
9 Однако более поздние исследования ставят под сомнение связь между пиелонефритом и терминальной стадией почечной недостаточности. 10 Исходные аномалии урогенитального тракта были зарегистрированы у 3,2% здоровых младенцев, прошедших скрининг. 11 Кроме того, обструктивные аномалии обнаруживаются у 4 %, а пузырно-мочеточниковый рефлюкс — у 8–40 % детей, обследованных на предмет первой ИМП. Дети младше двух лет могут подвергаться большему риску паренхиматозных дефектов, чем дети старшего возраста. 12
| Клинические рекомендации | Рейтинг доказательности | Ссылки |
|---|---|---|
| ИМП следует заподозрить у пациентов с наличием лейкоцитарной эстеразы и нитрита в тесте с тест-полосками или с гипербактериальной лейкоцитарной полиурией не менее 100 на микроскопию. | C | 13 , 16 |
У маленьких детей образцы мочи, собранные с помощью мешка, ненадежны при оценке ИМП. | C | 17 |
| Рекомендуемым начальным антибиотиком для большинства детей с ИМП является триметоприм/сульфаметоксазол (Бактрим, Септра). Альтернативные антибиотики включают амоксициллин/клавуланат (Аугментин) или цефалоспорины, такие как цефиксим (Супракс), цефподоксим, цефпрозил (Цефзил) или цефалексин (Кефлекс). | C | 10 |
| Двух-четырехдневный курс пероральных антибиотиков столь же эффективен, как и семи-14-дневный курс у детей с более низкой ИМП. Разовая доза или однодневный курс не рекомендуются. | A | 19–21 |
Детей с острым пиелонефритом можно эффективно лечить пероральными антибиотиками (например, амоксициллин/клавуланат, цефиксим, цефтибутен [Cedax]) в течение 10–14 дней или короткими курсами (два дня). до четырех дней) внутривенной терапии с последующей пероральной терапией. | A | 24 |
| Профилактическое назначение антибиотиков не снижает риск рецидива ИМП даже у детей с пузырно-мочеточниковым рефлюксом легкой и средней степени тяжести. | B | 25–27 |
| Рутинное обрезание у мальчиков не снижает риск ИМП настолько, чтобы оправдать риск хирургических осложнений. | Б | 32 |
Диагностика
ИСТОРИЯ И ФИЗИЧЕСКОЕ ОБСЛЕДОВАНИЕ
Клинические признаки и симптомы ИМП зависят от возраста ребенка. Новорожденные с ИМП могут проявляться желтухой, сепсисом, задержкой развития, рвотой или лихорадкой. У младенцев и детей младшего возраста типичные признаки и симптомы включают лихорадку, сильный запах мочи, гематурию, боль в животе или в боку и впервые возникшее недержание мочи. Дети школьного возраста могут иметь симптомы, сходные со взрослыми, включая дизурию, учащенное мочеиспускание или императивные позывы. Мальчики подвергаются повышенному риску ИМП, если им меньше шести месяцев или если они моложе 12 месяцев и не обрезаны. Девочки, как правило, подвержены повышенному риску ИМП, особенно в возрасте до одного года. 3 Результаты физикального обследования могут быть неспецифическими, но могут включать болезненность в надлобковой области или реберно-позвоночном углу.
Мальчики подвергаются повышенному риску ИМП, если им меньше шести месяцев или если они моложе 12 месяцев и не обрезаны. Девочки, как правило, подвержены повышенному риску ИМП, особенно в возрасте до одного года. 3 Результаты физикального обследования могут быть неспецифическими, но могут включать болезненность в надлобковой области или реберно-позвоночном углу.
ДИАГНОСТИЧЕСКИЕ ТЕСТЫ
Тест-полоски для ИМП включают лейкоцитарную эстеразу, нитриты, кровь и белок. Лейкоцитарная эстераза является наиболее чувствительным однократным тестом у детей с подозрением на ИМП. Тест на нитриты более специфичен, но менее чувствителен. Отрицательный результат на лейкоцитарную эстеразу значительно снижает вероятность ИМП, тогда как положительный результат на нитриты делает ее гораздо более вероятной; однако обратное неверно. Тест-полоски на кровь и белок имеют низкую чувствительность и специфичность при выявлении ИМП и могут вводить в заблуждение. Точность положительных результатов следующая (предполагается 10-процентная претестовая вероятность) 13 :
Нитрит: 53 -процентная чувствительность, 98 -процентная специфичность, 75 -процентная вероятность UTI
бактерии при микроскопии: 81 процентная чувствительность, 83 -процентная специфичность, 35 -процентная вероятность на UTI
Лейкоцитарная эстераза: 83% чувствительность, 78% специфичность, 30% вероятность ИМП
Лейкоцитарная эстераза или нитрит: чувствительность 93%, специфичность 72%, вероятность ИМП 27%
Кровь: чувствительность 47%, специфичность 78%, вероятность ИМП 19% , 76-процентная специфичность, 19-процентная вероятность ИМП
Улучшение функции мочеиспускания за счет своевременного мочеиспускания, процедур биологической обратной связи и антихолинергических препаратов у пациентов с нестабильным и маленьким мочевым пузырем. 16
Улучшение дисфункции мочеиспускания за счет своевременного опорожнения кишечника у пациентов с нечастым мочеиспусканием.
 16
16 Повышенное потребление жидкости.
Терапия тазового дна, особенно при рецидивирующей ИМП с детрузорно-сфинктерной диссинергией или дисфункцией мочеиспускания. 37 Улучшение опорожнения кишечника (запор, недержание кала). 16
Обрезание для снижения риска до 0,18%, 9 до 10 раз в первые 6 месяцев. 5 Рекомендация о рутинном обрезании противоречива и не подтверждается существующими доказательствами. 17 ,26 Он особенно эффективен у пациентов, предрасположенных к рецидивам ИМП без какого-либо документально подтвержденного источника, новорожденных с пренатальным гидронефрозом и ПМР, новорожденных с рефлюксом высокой степени или аномалиями мочеполовой системы, 5 ПМР у мужчин с односторонней агенезией или мультикистозной дисплазией почек, детей с высоким риском инфицирования ВИЧ 2 ,5 и детей, предрасположенных к рецидивирующим ИМП.
 26
26 Клюква рекомендуется для профилактики и лечения ИМП. Клюква имеет низкий переходный эффект в снижении рН мочи 7 и может быть полезным у пациентов старше 60 лет. По-видимому, он неэффективен для предотвращения или уменьшения ИМП. 6 Но метаанализа, подтверждающего благотворное влияние клюквы на детей, не проводилось, и это требует дополнительных исследований у детей.
9012 9012 9012 9012 902 9012 9012 9012 9012 9012 9012 9012 9012 9012 9012
 микроскопия: 73% чувствительность, 81% специфичность, 30% вероятность ИМП
микроскопия: 73% чувствительность, 81% специфичность, 30% вероятность ИМП Все лихорадящие дети в возрасте от 2 до 24 месяцев без очевидной причины инфекции должны быть обследованы на ИМП, за исключением обрезанных мальчиков старше 12 месяцев. 14 Детей старшего возраста следует обследовать, если клиническая картина указывает на источник мочи. Национальный институт здравоохранения и клинического мастерства в Соединенном Королевстве одобряет включение конкретных стратегий анализа мочи в зависимости от возраста ребенка 90 005 (рис. 1) . 15 В этой модели микроскопию и посев мочи следует проводить у детей в возрасте до трех лет вместо тестирования с помощью тест-полоски. Наличие пиурии не менее 10 лейкоцитов в поле зрения и бактериурии рекомендуются в качестве критериев диагностики ИМП при микроскопии. 16 У маленьких детей образцы мочи, собранные с помощью мешка, ненадежны по сравнению с образцами, собранными с помощью катетера. 17 Таким образом, у ребенка, который не может предоставить чистый образец, следует рассмотреть вопрос о катетеризации. Если посев мочи невозможен в течение четырех часов после сбора, образец следует хранить в холодильнике.
Наличие пиурии не менее 10 лейкоцитов в поле зрения и бактериурии рекомендуются в качестве критериев диагностики ИМП при микроскопии. 16 У маленьких детей образцы мочи, собранные с помощью мешка, ненадежны по сравнению с образцами, собранными с помощью катетера. 17 Таким образом, у ребенка, который не может предоставить чистый образец, следует рассмотреть вопрос о катетеризации. Если посев мочи невозможен в течение четырех часов после сбора, образец следует хранить в холодильнике.
Процедуры визуализации, получившие наивысшие оценки Американского колледжа радиологии Критериями приемлемости для дальнейшего обследования отдельных детей с ИМП являются УЗИ почек и мочевого пузыря, радионуклидная цистография или цистоуретрография мочеиспускания, а также сканирование коры почек. 18 Ультрасонография почек и мочевого пузыря эффективна для оценки анатомии, но ненадежна для выявления пузырно-мочеточникового рефлюкса. Радионуклидная цистография или цистоуретрография мочеиспускания эффективны для скрининга и оценки пузырно-мочеточникового рефлюкса, но требуют облучения и катетеризации.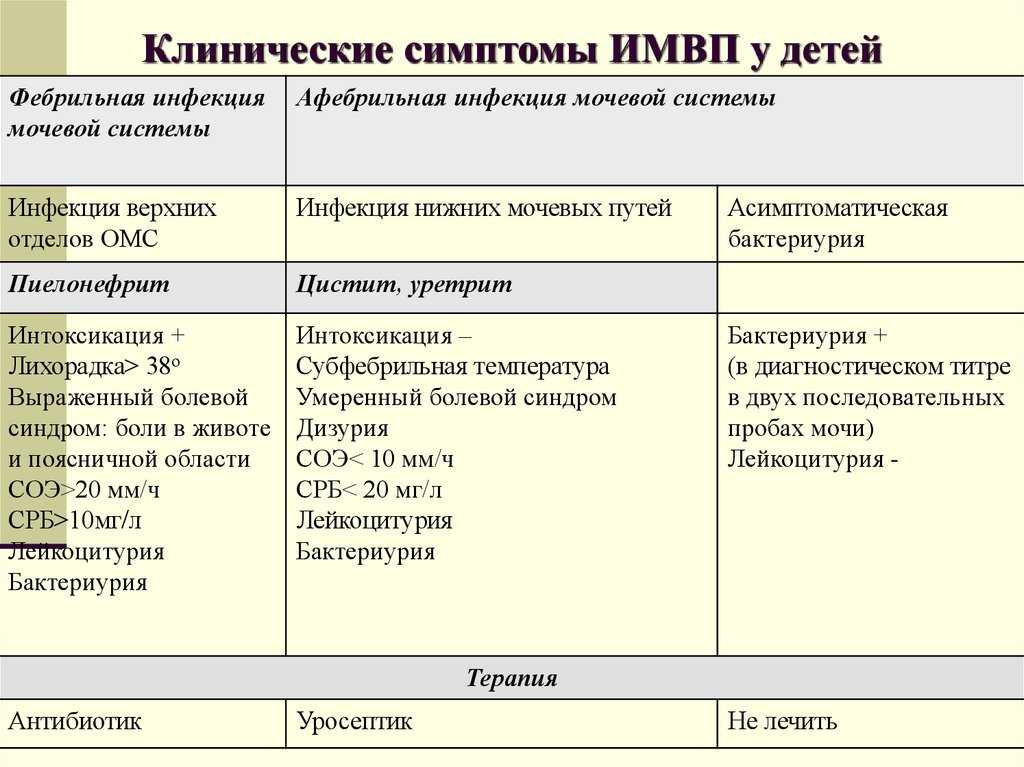 Хотя цистоуретрография мочеиспускания предлагается как девочкам, так и мальчикам, радионуклидная цистография предлагается только девочкам, потому что цистоуретрография мочеиспускания необходима для адекватной анатомической визуализации уретры и мочевого пузыря у мальчиков. Сканирование коры почек (также называемое сцинтиграфией или сканированием DMSA) использует технеций и эффективно для оценки почечных рубцов, но требует внутривенной инъекции радиоизотопа.
Хотя цистоуретрография мочеиспускания предлагается как девочкам, так и мальчикам, радионуклидная цистография предлагается только девочкам, потому что цистоуретрография мочеиспускания необходима для адекватной анатомической визуализации уретры и мочевого пузыря у мальчиков. Сканирование коры почек (также называемое сцинтиграфией или сканированием DMSA) использует технеций и эффективно для оценки почечных рубцов, но требует внутривенной инъекции радиоизотопа.
Исследования долгосрочных исходов для определения наилучшего начального визуализирующего исследования у детей с диагнозом ИМП не проводились. Руководящие принципы, основанные на обсервационных исследованиях и мнении экспертов, рекомендуют всем мальчикам, девочкам в возрасте до трех лет и девочкам в возрасте от трех до семи лет с температурой 101,3 °F (38,5 °C) или выше пройти цистографию и ультразвуковое исследование с первым разом. ИМП. 3 Дополнительной стратегией визуализации у детей с лихорадкой и ИМП, особенно у детей старше трех лет, является сначала выполнение ультразвукового исследования и сканирование коры почек.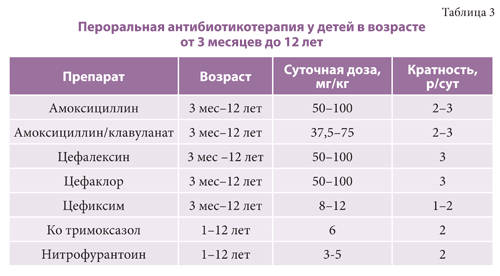 Эта стратегия позволяет избежать катетеризации мочевого пузыря с помощью цистографии и сводит к минимуму лучевую нагрузку, если результаты сканирования в норме. Однако, если пиелонефрит или рубцевание коры обнаруживаются при сканировании коры почки, показана цистография. 3
Эта стратегия позволяет избежать катетеризации мочевого пузыря с помощью цистографии и сводит к минимуму лучевую нагрузку, если результаты сканирования в норме. Однако, если пиелонефрит или рубцевание коры обнаруживаются при сканировании коры почки, показана цистография. 3
Наблюдение без визуализации следует рассматривать у девочек трех лет и старше с температурой менее 101,3°F и у всех девочек старше семи лет. 3 Семья должна принять решение о проведении визуализации при первой ИМП или отложить визуализацию до второй ИМП, если она произойдет. Рисунок 2. представляет собой алгоритм стратегий визуализации у детей с ИМП. 3
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ
Хотя лихорадка может быть единственным симптомом у детей в возрасте до 24 месяцев, результаты медицинского осмотра могут указать на альтернативный диагноз, включая средний отит, гастроэнтерит или инфекцию верхних дыхательных путей. Всегда следует учитывать скрытую бактериемию, хотя вероятность этого диагноза намного ниже, чем ИМП (менее 1% против 7%), у полностью иммунизированных детей, у которых при физикальном обследовании нет другого идентифицируемого потенциального источника лихорадки. 4 Мочевые конкременты, уретрит (включая инфекцию, передающуюся половым путем), дисфункцию выделения и сахарный диабет следует подозревать у вербальных детей с проблемами мочевыводящих путей.
4 Мочевые конкременты, уретрит (включая инфекцию, передающуюся половым путем), дисфункцию выделения и сахарный диабет следует подозревать у вербальных детей с проблемами мочевыводящих путей.
Лечение
Хотя амоксициллин традиционно использовался в качестве антибиотика первой линии при ИМП, возросшие показатели устойчивости к E. coli сделали его менее приемлемым выбором, а исследования показали более высокие показатели излечения при применении триметоприма/сульфаметоксазола (Бактрим, Септра). ). Другие варианты включают амоксициллин/клавуланат (Аугментин) или цефалоспорины, такие как цефиксим (Супракс), цефподоксим, цефпрозил (Цефзил) или цефалексин (Кефлекс). 10 В таблице 1 перечислены наиболее часто используемые антибиотики с информацией о дозировке и побочных эффектах. Врачи должны знать о местных образцах резистентности бактерий, которые могут повлиять на выбор антибиотиков.
| Антибиотик | Дозирование | Распространенные побочные эффекты |
|---|---|---|
| Amoxicillin/Clavulanate (AUPLINITININ) | Diarhea, тошнота/рвота, Rash | |
| CEFIXIME (SUPARS) | 8 мг на кг каждые 24 часа или деленные каждые 12 часов | COMONAL PAPE, Diarrhea, Flatulence, Rash | 70707070707063EF | 7070707070707063EF. на кг в день, разделяя каждые 12 часов | Боль в животе, диарея, тошнота, сыпь |
| Цефпрозил (Cefzil) | 30 мг на кг в день, разделяя каждые 12 часов | Боль в животе, диарея, повышенные результаты на функциональные пробы печени, тошнота |
| Цефалексин (Кефлекс) | 25–50 мг/кг в день, разделенные каждые 6–12 часов | Диарея, головная боль, тошнота/рвота, сыпь |
| 8–10 мг на кг в день, разделенные каждые 12 часов | Диарея, тошнота/рвота, фотосенсибилизация, сыпь |
В Кокрейновском обзоре, посвященном краткосрочному (от двух до четырех дней) и стандартному (от семи до 14 дней) пероральному приему антибиотиков у 652 детей с более низкой ИМП, не было обнаружено существенной разницы в положительных культурах мочи между видами терапии сразу после лечения (восемь исследований: относительный риск = 1,06;95% доверительный интервал, от 0,64 до 1,76) или через 15 месяцев после лечения (10 исследований: относительный риск = 0,95; 95% доверительный интервал, от 0,70 до 1,29). Также не было существенной разницы между короткой и стандартной терапией в отношении развития резистентных микроорганизмов в конце лечения. 19 Таким образом, двух-четырехдневный курс пероральных антибиотиков оказывается таким же эффективным, как и семи-14-дневный курс у детей с более низкими ИМП. 19 Однодозовый или однодневный курс может быть менее эффективным, чем более длительные курсы пероральных антибиотиков, и не рекомендуется. 20,21
Также не было существенной разницы между короткой и стандартной терапией в отношении развития резистентных микроорганизмов в конце лечения. 19 Таким образом, двух-четырехдневный курс пероральных антибиотиков оказывается таким же эффективным, как и семи-14-дневный курс у детей с более низкими ИМП. 19 Однодозовый или однодневный курс может быть менее эффективным, чем более длительные курсы пероральных антибиотиков, и не рекомендуется. 20,21
Если имеющиеся симптомы неспецифичны для ИМП или результаты анализа мочи с помощью тест-полоски неинформативны, лечение может быть отложено до получения результатов посева. Родители могут быть уверены, что антибиотики, начатые через 24 часа после начала лихорадки, не связаны с более высоким риском паренхиматозных дефектов, чем немедленные антибиотики у детей младше двух лет. 22 Однако отсрочка назначения антибиотиков на четыре дня и более может увеличить риск рубцевания почек. 8
Фторхинолоны обычно не используются у детей из-за потенциальных опасений по поводу длительного повреждения развивающихся суставов, хотя нет убедительных доказательств, подтверждающих возникновение этого явления. Фторхинолоны могут быть полезны, когда инфекция вызвана полирезистентными патогенами, для которых нет безопасной и эффективной альтернативы, парентеральная терапия невозможна, а других эффективных пероральных препаратов нет. Рекомендации Американской академии педиатрии рекомендуют ограничивать терапию фторхинолонами пациентам с ИМП, вызванными Pseudomonas aeruginosa или другие полирезистентные грамотрицательные бактерии. 23 Ципрофлоксацин (Cipro) одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для лечения осложненных ИМП и пиелонефрита, связанных с E. coli , у пациентов в возрасте от 1 до 17 лет. 23
Фторхинолоны могут быть полезны, когда инфекция вызвана полирезистентными патогенами, для которых нет безопасной и эффективной альтернативы, парентеральная терапия невозможна, а других эффективных пероральных препаратов нет. Рекомендации Американской академии педиатрии рекомендуют ограничивать терапию фторхинолонами пациентам с ИМП, вызванными Pseudomonas aeruginosa или другие полирезистентные грамотрицательные бактерии. 23 Ципрофлоксацин (Cipro) одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для лечения осложненных ИМП и пиелонефрита, связанных с E. coli , у пациентов в возрасте от 1 до 17 лет. 23
Кокрановский обзор показал, что детей с острым пиелонефритом можно эффективно лечить пероральными антибиотиками (например, амоксициллин/клавуланат, цефиксим, цефтибутен [Cedax]) в течение 10–14 дней или короткими курсами (два–четыре дня). ) внутривенной терапии с последующей пероральной терапией. Если используется внутривенная терапия, однократный ежедневный прием аминогликозидов безопасен и эффективен. Необходимы исследования для определения оптимальной продолжительности внутривенной терапии у детей с острым пиелонефритом, но обычно она составляет от 10 до 14 дней. 24 Госпитализация должна быть рассмотрена для любого ребенка, который не может переносить пероральный прием пищи, или если диагноз тяжелобольного ребенка неясен.
Если используется внутривенная терапия, однократный ежедневный прием аминогликозидов безопасен и эффективен. Необходимы исследования для определения оптимальной продолжительности внутривенной терапии у детей с острым пиелонефритом, но обычно она составляет от 10 до 14 дней. 24 Госпитализация должна быть рассмотрена для любого ребенка, который не может переносить пероральный прием пищи, или если диагноз тяжелобольного ребенка неясен.
Последующая оценка для подтверждения надлежащего клинического ответа должна проводиться через 48–72 часа после начала антимикробной терапии у всех детей с ИМП. Результаты посева и чувствительности могут указывать на необходимость смены антибиотика. Если ожидаемого клинического улучшения не происходит, рассмотрите возможность дальнейшего обследования (например, лабораторные исследования, визуализация, консультации с узкими специалистами). Направление к узкому специалисту показано при обнаружении пузырно-мочеточникового рефлюкса, рубцевания почек, анатомических аномалий или камней в почках, или если рассматриваются инвазивные процедуры визуализации.
Профилактика
В обсервационном исследовании относительно здоровых детей с первой ИМП профилактика антибиотиками не была связана со снижением риска рецидива ИМП и повышением риска резистентных к лечению возбудителей. 25 Рандомизированное контролируемое исследование детей в возрасте от двух месяцев до семи лет показало, что профилактический прием антибиотиков в течение 12 месяцев после фебрильной ИМП не снижает риск последующей ИМП даже у детей с пузырно-мочеточниковым рефлюксом легкой и средней степени тяжести. 26 Другое рандомизированное контролируемое исследование детей и подростков с пиелонефритом показало, что профилактика антибиотиками не предотвращает повторные ИМП у пациентов без документально подтвержденного пузырно-мочеточникового рефлюкса или с пузырно-мочеточниковым рефлюксом легкой и средней степени тяжести. 27 Однако антибиотикопрофилактика может быть более эффективной у детей с более тяжелым пузырно-мочеточниковым рефлюксом. 28 В самом последнем Кокрановском обзоре по этому вопросу сделан вывод о том, что необходимы крупные, должным образом рандомизированные, двойные слепые исследования для определения эффективности длительного применения антибиотиков для профилактики ИМП у восприимчивых детей. 1 Кроме того, постоянная профилактика антибиотиками у детей младше двух с половиной лет с пузырно-мочеточниковым рефлюксом может не снизить риск пиелонефрита или повреждения почек. 29
28 В самом последнем Кокрановском обзоре по этому вопросу сделан вывод о том, что необходимы крупные, должным образом рандомизированные, двойные слепые исследования для определения эффективности длительного применения антибиотиков для профилактики ИМП у восприимчивых детей. 1 Кроме того, постоянная профилактика антибиотиками у детей младше двух с половиной лет с пузырно-мочеточниковым рефлюксом может не снизить риск пиелонефрита или повреждения почек. 29
Запор следует лечить у младенцев и детей, перенесших ИМП, чтобы предотвратить последующие инфекции. 30 Имеются некоторые доказательства того, что клюквенный сок уменьшает выраженность симптоматических ИМП в течение 12 месяцев, особенно у женщин с рецидивирующими ИМП. 31 Эффективность клюквенного сока у детей менее определенна, а высокий показатель отсева в исследованиях указывает на то, что клюквенный сок может быть неприемлем для долгосрочной профилактики. Систематический обзор пришел к выводу, что обычное обрезание у мальчиков не снижает риск ИМП в достаточной степени, чтобы оправдать риск хирургических осложнений. 32
32
Лечение и профилактика инфекций мочевыводящих путей у детей
Int J Prev Med. январь-март 2011 г.; 2(1): 4–9.
1 и 2
Информация об авторе Примечания к статье Информация об авторских правах и лицензии Отказ от ответственности
Инфекция мочевыводящих путей (ИМП) является наиболее распространенной серьезной бактериальной инфекцией в раннем возрасте. Надлежащая диагностика и лечение предотвращают такие осложнения, как артериальная гипертензия, протеинурия и терминальная стадия почечной недостаточности. Был проведен компьютеризированный поиск в MEDLINE, Embase и других базах данных, чтобы найти последние результаты лечения и профилактики ИМП у детей. Оценивались рандомизированные контрольные испытания, систематические обзоры и оригинальные статьи. Поисковыми запросами были «ИМП, лечение, профилактика, профилактика и дети». В наше поисковое исследование были включены все дети с осложненной или простой ИМП от периода новорожденности до позднего детства, и были рассмотрены медицинские аспекты лечения. В последнее время подходы к лечению изменились за счет упрощения введения препаратов. Пероральное лечение рекомендуется, особенно у младенцев и детей старшего возраста, вместо строгого внутривенного лечения и госпитализации пациента. Кроме того, профилактическое лечение становится проще и ограничивается отдельными случаями. В этой статье мы рассмотрим последнюю информацию и подходы в этой области.
В наше поисковое исследование были включены все дети с осложненной или простой ИМП от периода новорожденности до позднего детства, и были рассмотрены медицинские аспекты лечения. В последнее время подходы к лечению изменились за счет упрощения введения препаратов. Пероральное лечение рекомендуется, особенно у младенцев и детей старшего возраста, вместо строгого внутривенного лечения и госпитализации пациента. Кроме того, профилактическое лечение становится проще и ограничивается отдельными случаями. В этой статье мы рассмотрим последнюю информацию и подходы в этой области.
Ключевые слова: Инфекции мочевыводящих путей, лечение, профилактика, профилактика, дети менингит, пневмония и скрытая бактериемия. 1 – 3 Включает 10% всех лихорадящих детей, 13,6% лихорадящих детей и 7% лихорадящих новорожденных. 4 – 6 ИМП встречается у 17–20% беременных и приводит к преждевременному излитию плодных оболочек, хориоамниониту, преждевременным родам и послеродовой инфекции у матери и новорожденного. 7 Большинство пациентов обращаются в течение первого года жизни. Может быть вовлечено до 1% доношенных новорожденных и 4-25% недоношенных. 8 Заболевание чаще встречается в неонатальном периоде и в раннем младенчестве у мальчиков, впоследствии снижается. Около 8 % девочек (3 % в препубертатном возрасте) и 2 % мальчиков (1 % в препубертатном возрасте) испытывают по крайней мере один эпизод ИМП до 7 лет. 5 ,9 Встречается у 0,1-0,4% девочек раннего возраста и увеличивается до 1,4% в течение 1-5 лет и 0,7-2,3% в школьном возрасте. В группу риска входят около 0,2% обрезанных и 0,7% необрезанных мальчиков, который достигает 0,1-0,2 в 1-5 лет и 0,04-0,2 в школьном возрасте. 10 ИМП может привести к транзиторной почечной недостаточности у 40% и необратимому повреждению почек у 5% пациентов. 11 Встречается в 15-33% трансплантаций почки, приводя к острой дисфункции трансплантата и хронической нефропатии аллотрансплантата, что влияет на долгосрочную почечную выживаемость.
7 Большинство пациентов обращаются в течение первого года жизни. Может быть вовлечено до 1% доношенных новорожденных и 4-25% недоношенных. 8 Заболевание чаще встречается в неонатальном периоде и в раннем младенчестве у мальчиков, впоследствии снижается. Около 8 % девочек (3 % в препубертатном возрасте) и 2 % мальчиков (1 % в препубертатном возрасте) испытывают по крайней мере один эпизод ИМП до 7 лет. 5 ,9 Встречается у 0,1-0,4% девочек раннего возраста и увеличивается до 1,4% в течение 1-5 лет и 0,7-2,3% в школьном возрасте. В группу риска входят около 0,2% обрезанных и 0,7% необрезанных мальчиков, который достигает 0,1-0,2 в 1-5 лет и 0,04-0,2 в школьном возрасте. 10 ИМП может привести к транзиторной почечной недостаточности у 40% и необратимому повреждению почек у 5% пациентов. 11 Встречается в 15-33% трансплантаций почки, приводя к острой дисфункции трансплантата и хронической нефропатии аллотрансплантата, что влияет на долгосрочную почечную выживаемость. 12 Может проявляться бессимптомной бактериурией и осложненными или неосложненными инфекциями верхних и нижних отделов мочевыделительной системы. 13 Идеальное лечение приводит к облегчению симптомов, предотвращает прогрессирующее повреждение почек и уросепсис с немедленной эрадикацией бактерий. 14 На протяжении многих лет методы лечения вызывали споры. Эмпирический антибиотик должен иметь первичную экскрецию с мочой, чтобы достичь высокого уровня в моче. 13 Выбор антибиотика зависит от выявления доминирующих уропатогенов (в зависимости от возраста), тяжести симптомов, последующего наблюдения за пациентом, чувствительности к противомикробным препаратам, резистентности сообщества, фармакокинетики, токсичности препарата и экономической эффективности. 15 – 17
12 Может проявляться бессимптомной бактериурией и осложненными или неосложненными инфекциями верхних и нижних отделов мочевыделительной системы. 13 Идеальное лечение приводит к облегчению симптомов, предотвращает прогрессирующее повреждение почек и уросепсис с немедленной эрадикацией бактерий. 14 На протяжении многих лет методы лечения вызывали споры. Эмпирический антибиотик должен иметь первичную экскрецию с мочой, чтобы достичь высокого уровня в моче. 13 Выбор антибиотика зависит от выявления доминирующих уропатогенов (в зависимости от возраста), тяжести симптомов, последующего наблюдения за пациентом, чувствительности к противомикробным препаратам, резистентности сообщества, фармакокинетики, токсичности препарата и экономической эффективности. 15 – 17
Острый пиелонефрит на 2/3 состоит из фебрильных ИМП в раннем детском возрасте. 1 Должны быть госпитализированы следующие пациенты: новорожденные в возрасте до 1 месяца для исключения септицемии и менингита, неадекватной абсорбции лекарств, незрелой иммунной системы и повышенной диссеминации инфекции, 15 неблагоприятных общих состояний, таких как интоксикация, септицемия, вялость, малокровие давление, тяжелая дегидратация, низкая комплаентность, трудное последующее наблюдение, острое заболевание, иммунодефицит и осложненная ИМП, непереносимость или несоблюдение режима лечения и тяжелая осложненная ИМП. 15 – 17
15 – 17
Пероральное и амбулаторное лечение было безопасным и эффективным, как и внутривенная терапия при остром пиелонефрите. 6 Бактериемия встречается у 6,1–22,7% детей в возрасте до 2 месяцев и у 9,3% детей в возрасте до 6 месяцев. После 6 мес жизни это не характерно. 18 Внутривенное (в/в) лечение рекомендуется многими авторами пациентам менее 1 месяца (менее 3 месяцев другими авторами) в течение 7-10 дней или 3-7 дней до клинического улучшения с последующим пероральным приемом антибиотиков до 14 дней. Пероральное лечение может быть рассмотрено у детей в возрасте 1–3 месяцев без бактериемии или менингита, при тщательном наблюдении и хорошем общем состоянии. 15 В другом исследовании было сообщено о безопасности амбулаторного внутривенного введения. 10 Не было выявлено существенных различий в продолжительности лихорадки, персистенции инфекции, рецидивирующих ИМП и поражении почечной паренхимы между полным пероральным (10-14 дней), полным внутривенным (7-14 дней) и коротким внутривенным (2- 4 дня) лечения с последующим пероральным лечением (7-11 дней) у детей старше 2 месяцев без септицемии или менингита, что соответствует потреблению жидкости. 19 Детям в возрасте от 2 месяцев до 2 лет Американская академия педиатрии (ААП) рекомендовала пройти курс лечения продолжительностью от 7 до 14 дней, но у детей старшего возраста этот вопрос является спорным. 20
19 Детям в возрасте от 2 месяцев до 2 лет Американская академия педиатрии (ААП) рекомендовала пройти курс лечения продолжительностью от 7 до 14 дней, но у детей старшего возраста этот вопрос является спорным. 20
Начальное лечение часто эмпирическое. Он должен обладать хорошей проникающей способностью через паренхиму, низкой токсичностью и хорошей переносимостью. Некоторыми из хорошо известных препаратов являются ампициллин и гентамицин против энтерококков, стрептококков группы В и грамотрицательных бактерий, 15 и третье (цефтазидим или цефтриаксон старше 1 месяца) или четвертое (цефепим) поколения цефалоспоринов, которые используются особенно при резистентных уропатогенах с менее нефротоксичность. 17 Несколько исследований показали, что парентеральное введение гентамицина или цефтриаксона один раз в день в дневном стационаре является безопасным, эффективным и экономически выгодным при ИМП. 15 Однократная суточная доза гентамицина безопасна с аналогичным или большим терапевтическим эффектом, аналогичной или меньшей нефротоксичностью и ототоксичностью по сравнению с приемом 3 раза в день. 3 ,19 Антибиотики широкого спектра действия, такие как амоксициллин/клавулановая кислота, цефалоспорины второго (цефуроксим, цефпрозил) и третьего (цефиксим, цефподоксим, цефтибутен, цефдинир) поколений и триметоприм-сульфаметоксазол рекомендуются для перорального лечения. 2 ,21 Нитрофурантоин имеет высокую концентрацию в моче и низкую концентрацию в сыворотке и не рекомендуется при остром пиелонефрите. 10 Одно исследование показало, что пероральный прием цефтибутена в течение 14 дней оказывает сходное с цефтриаксоном/цефтибутеном действие на образование рубцов на почках. 18 Систематический обзор не выявил существенных различий между коротким курсом и стандартным лечением в развитии устойчивых микроорганизмов. 21
3 ,19 Антибиотики широкого спектра действия, такие как амоксициллин/клавулановая кислота, цефалоспорины второго (цефуроксим, цефпрозил) и третьего (цефиксим, цефподоксим, цефтибутен, цефдинир) поколений и триметоприм-сульфаметоксазол рекомендуются для перорального лечения. 2 ,21 Нитрофурантоин имеет высокую концентрацию в моче и низкую концентрацию в сыворотке и не рекомендуется при остром пиелонефрите. 10 Одно исследование показало, что пероральный прием цефтибутена в течение 14 дней оказывает сходное с цефтриаксоном/цефтибутеном действие на образование рубцов на почках. 18 Систематический обзор не выявил существенных различий между коротким курсом и стандартным лечением в развитии устойчивых микроорганизмов. 21
Краткосрочное (3-5 дней) пероральное лечение эффективно и приемлемо для детей старше 2 лет в стабильном состоянии с нормальным состоянием мочевыводящих путей. 14 ,22 Он так же эффективен, как 7-14-дневный курс лечения нижних мочевых путей. 23 При остром цистите режим однократной дозы имеет меньшую эффективность и высокую частоту рецидивов (20%). 15 Эмпирическое лечение является основным методом лечения неосложненного цистита. Варианты включают антибиотики широкого спектра действия, такие как сульфаниламиды, триметоприм-сульфаметоксазол, нитрофурантоин, амоксициллина клавуланат, цефалоспорины и триметоприм. 14 Из-за резистентности микробов амоксициллин и цефалоспорины первого поколения не рассматриваются в эмпирической терапии. 2 Сообщалось, что краткосрочные фторхинолоны безопасны и хорошо переносятся в качестве терапии второй линии при осложненных ИМП. У здоровых детей с самокупирующимся геморрагическим циститом рекомендуется консервативное лечение противовоспалительными препаратами и адекватная гидратация. Рибавирин показан иммунодефицитным пациентам с геморрагической аденовирусной инфекцией. Цидофовир предлагается при полиоме и тяжелой аденовирусной инфекции с ограниченными показаниями.
23 При остром цистите режим однократной дозы имеет меньшую эффективность и высокую частоту рецидивов (20%). 15 Эмпирическое лечение является основным методом лечения неосложненного цистита. Варианты включают антибиотики широкого спектра действия, такие как сульфаниламиды, триметоприм-сульфаметоксазол, нитрофурантоин, амоксициллина клавуланат, цефалоспорины и триметоприм. 14 Из-за резистентности микробов амоксициллин и цефалоспорины первого поколения не рассматриваются в эмпирической терапии. 2 Сообщалось, что краткосрочные фторхинолоны безопасны и хорошо переносятся в качестве терапии второй линии при осложненных ИМП. У здоровых детей с самокупирующимся геморрагическим циститом рекомендуется консервативное лечение противовоспалительными препаратами и адекватная гидратация. Рибавирин показан иммунодефицитным пациентам с геморрагической аденовирусной инфекцией. Цидофовир предлагается при полиоме и тяжелой аденовирусной инфекции с ограниченными показаниями. 10 ,14 Руководство ВОЗ рекомендует пероральный котримоксазол или соответствующие альтернативы, такие как ампициллин, амоксициллин и цефалексин, у пациентов с ИМП в течение 5 дней. Внутривенное лечение ампициллином и гентамицином или цефалоспоринами рекомендуется у резистентных пациентов с подозрением на острый пиелонефрит и у детей младше 2 месяцев с последующим амбулаторным лечением у стабильных пациентов. 4
10 ,14 Руководство ВОЗ рекомендует пероральный котримоксазол или соответствующие альтернативы, такие как ампициллин, амоксициллин и цефалексин, у пациентов с ИМП в течение 5 дней. Внутривенное лечение ампициллином и гентамицином или цефалоспоринами рекомендуется у резистентных пациентов с подозрением на острый пиелонефрит и у детей младше 2 месяцев с последующим амбулаторным лечением у стабильных пациентов. 4
Бессимптомная бактериурия (ББУ) рассматривается скорее как отдельное состояние, чем как предвестник симптоматической инфекции. 20 Посев мочи становится отрицательным у 40-50% детей в возрасте 2-5 лет. 2 Он не будет прогрессировать до симптоматической инфекции, рубцевания почек и нарушения роста или функции почек. Антимикробное лечение приводит к эрадикации нормальной флоры, тканевой инвазии и пиелонефрита с различными видами бактерий и обычно не рекомендуется. 16 ,20 Пациентам без урологических отклонений рекомендуется периодическое наблюдение без антимикробной терапии, 17 снижение роста или функции почек, рубцевание почек и симптоматическая ИМП. 16 Лечение показано при иммунодефиците, перед урологическими операциями, при повреждении слизистой оболочки, биопсии слизистой оболочки во время цистоскопии, 22 при беременности и у пациентов с симптомами.
16 Лечение показано при иммунодефиците, перед урологическими операциями, при повреждении слизистой оболочки, биопсии слизистой оболочки во время цистоскопии, 22 при беременности и у пациентов с симптомами.
Антибиотикопрофилактика (ежедневное лечение в течение не менее 2 месяцев) была введена Гельмгольцем в 1941 для профилактики рецидивов ИМП (2 и более инфекций в течение 6 мес) и поражения почек. Рецидив ИМП может возникать у 30–50% пациентов 25 , особенно в первые 2–6 мес. В настоящее время ранняя диагностика и лечение анафилактического пурпурного нефрита (АПН) считаются единственным эффективным подходом к уменьшению рубцевания почек. Пиковый эффект приходится на первые 6 месяцев лечения, 25 , когда риск рецидива ИМП наиболее высок. Предрасполагающие факторы включают пузырно-мочеточниковый рефлюкс (особенно высокой степени), генетику (уротелиальные рецепторы), аномалии мочеполовой системы, женский пол, фекальную и перинеальную колонизацию, иммунодефицитные состояния, секреторный статус, дефицит IL8, опосредованного нейтрофилами и хемокинового рецептора (CXCR1), нестабильность мочевого пузыря, ИМП в анамнезе, редкое мочеиспускание, дисфункция мочеиспускания, гиперкальциурия, недостаточное потребление жидкости, неадекватная гигиена половых органов, больные диабетом, запоры, энкопрез, аномалии почек, молодой возраст (менее 6 месяцев при первой ИМП) и белая раса. Хирургические причины бактериальной персистенции включают инфекционный камень, инфицированные нефункциональные почечные сегменты, инфицированные культи мочеточников после нефрэктомии, пузырно-кишечные или уретроректальные свищи, пузырно-влагалищные свищи, инфицированные некротические сосочки при папиллярном некрозе, одностороннюю медуллярную губчатую почку, инфицированную кисту мочевого пузыря, инфицированный дивертикул уретры или периуретральные железы. . 9 ,26
Хирургические причины бактериальной персистенции включают инфекционный камень, инфицированные нефункциональные почечные сегменты, инфицированные культи мочеточников после нефрэктомии, пузырно-кишечные или уретроректальные свищи, пузырно-влагалищные свищи, инфицированные некротические сосочки при папиллярном некрозе, одностороннюю медуллярную губчатую почку, инфицированную кисту мочевого пузыря, инфицированный дивертикул уретры или периуретральные железы. . 9 ,26
Профилактика должна продолжаться до снижения частоты возникновения факторов риска, таких как мужчины старше 1 года с мониторируемым пузырно-мочеточниковым рефлюксом (ПМР), мужчины с ПМР низкой степени, дети старше 7-8 лет с ПМР низкой степени) или отсутствием риска рубцевания почки (пожилой возраст). 16 ,25 Профилактика показана в условиях высокого риска развития почечного рубцевания или уросепсиса (расширенная ПМР, тяжелая обструкция, рецидивирующая симптоматическая ИМП, особенно при нестабильности мочевого пузыря или дисфункции мочеиспускания и у девочек с частыми ИМП для облегчения симптомов, инфекционных камней , вплоть до реконструкции почечной аномалии, предрасположенной к ИМП, симптоматической ВУР, пациентов с риском рецидивирующего пиелонефрита (более одного эпизода пиелонефрита), симптоматического рефлюкса, 24 высокий риск рецидива ИМП и рубцевания почки, дети до 8 лет с ПМР и рецидивирующей симптоматической ИМП, ПМР при нейрогенном мочевом пузыре, дети до 18 месяцев с нерефлюксным острым пиелонефритом, 16 до завершения процедур визуализации и учреждения стратегии лечения, 6 пациентов, восприимчивых к рецидивирующей ИМП без какого-либо документированного источника, 5 иммунодефицита, 17 и до разрешения обструкции. 26 Рецидивирующий цистит является сомнительным показанием. 27 Купание в ванне с пеной, уборка (задом наперед) и плавание не считаются убедительными доказательствами. 2 ,28
26 Рецидивирующий цистит является сомнительным показанием. 27 Купание в ванне с пеной, уборка (задом наперед) и плавание не считаются убедительными доказательствами. 2 ,28
Идеальное лечение зависит от местной чувствительности к противомикробным препаратам. 17 Он должен иметь низкий уровень в сыворотке и высокий уровень в моче, широкий спектр активности, а также наименьшее влияние на фекальную флору, минимальные побочные эффекты и минимальную бактериальную резистентность. 24 ,26 Ампициллин, амоксициллин и цефалексин являются подходящими профилактическими препаратами для детей младше 3 месяцев. Нитрофурантоин, триметоприм, котримоксазол и цефалексин являются подходящими препаратами для детей старше 4 месяцев. 16 Профилактическое действие цефиксима больше, чем у NFT, а у последнего больше, чем у TMP, с большим количеством побочных эффектов. Отмена NFT более вероятна, чем котримоксазол, из-за желудочно-кишечных осложнений. 11 Повышение устойчивости к противомикробным препаратам ампициллину и амоксициллину сделало их менее эффективными, и их не рекомендуется применять в течение первых 2 месяцев. 29 Положительный эффект профилактики кажется небольшим 25 и больше не является общепризнанным. 24 Профилактический прием антибиотиков не очень эффективен для предотвращения рецидивирующей ИМП, рецидивирующего ОПН или нового рубца на почке и может привести к появлению резистентных микроорганизмов при рецидивирующей ИМП. 30 Эффект профилактики при ПМР сомнительный. 31 Легкая или умеренная степень ПМР не увеличивает частоту ОПН или почечного рубца. 30 ,32 Осложнения профилактики при рефлюксе низкой степени выше, чем ее преимущества 23 , а профилактика не рекомендуется при рефлюксе низкой степени в шведских рекомендациях и некоторых других источниках. 27 ,31 В связи с неопределенностью положительного эффекта долгосрочной профилактики и низкой эффективностью в некоторых исследованиях, 26 ,27 рекомендуется провести дополнительные исследования с контрольной группой для оценки этого лечения.
11 Повышение устойчивости к противомикробным препаратам ампициллину и амоксициллину сделало их менее эффективными, и их не рекомендуется применять в течение первых 2 месяцев. 29 Положительный эффект профилактики кажется небольшим 25 и больше не является общепризнанным. 24 Профилактический прием антибиотиков не очень эффективен для предотвращения рецидивирующей ИМП, рецидивирующего ОПН или нового рубца на почке и может привести к появлению резистентных микроорганизмов при рецидивирующей ИМП. 30 Эффект профилактики при ПМР сомнительный. 31 Легкая или умеренная степень ПМР не увеличивает частоту ОПН или почечного рубца. 30 ,32 Осложнения профилактики при рефлюксе низкой степени выше, чем ее преимущества 23 , а профилактика не рекомендуется при рефлюксе низкой степени в шведских рекомендациях и некоторых других источниках. 27 ,31 В связи с неопределенностью положительного эффекта долгосрочной профилактики и низкой эффективностью в некоторых исследованиях, 26 ,27 рекомендуется провести дополнительные исследования с контрольной группой для оценки этого лечения. 1 ,33 Осложнения длительной антибиотикопрофилактики возникают у 8-10% больных, особенно в течение первых 6 мес, включая тошноту, рвоту, кожные реакции, гепатотоксичность и гематологические осложнения, с отрицательным эффектом в виде образования кишечно- и ротоглоточной резистентных микроорганизмов 25 ,30 и повышенный риск симптоматической инфекции мочевыводящих путей резистентными микроорганизмами, 27 даже у пациентов с чистой периодической катетеризацией 31 и повышенной устойчивостью к цефалоспоринам 3 rd поколения. 26 Conway сообщил о 7-кратном увеличении частоты рецидивов ИМП с резистентными микроорганизмами при антимикробной профилактике. 1
1 ,33 Осложнения длительной антибиотикопрофилактики возникают у 8-10% больных, особенно в течение первых 6 мес, включая тошноту, рвоту, кожные реакции, гепатотоксичность и гематологические осложнения, с отрицательным эффектом в виде образования кишечно- и ротоглоточной резистентных микроорганизмов 25 ,30 и повышенный риск симптоматической инфекции мочевыводящих путей резистентными микроорганизмами, 27 даже у пациентов с чистой периодической катетеризацией 31 и повышенной устойчивостью к цефалоспоринам 3 rd поколения. 26 Conway сообщил о 7-кратном увеличении частоты рецидивов ИМП с резистентными микроорганизмами при антимикробной профилактике. 1
Осложнения у детей возникают реже, чем у взрослых, из-за более низкой дозировки и, как правило, отсутствия лекарственного взаимодействия у детей. 26 Angocin Anti-Infekt N, растительный лекарственный препарат, обладает эффективностью и безопасностью при профилактическом лечении хронически рецидивирующих ИМП. 34 Катетеризация мочевого пузыря является важным фактором при внутрибольничных инфекциях. Продолжительность катетеризации важна при ятрогенной инфекции. Катетеризация увеличивала вероятность ИМП на 5-10% каждый день после первых 48 часов. Таким образом, гигиена рук, стерильная катетеризация, закрытый стерильный катетер и сокращение времени катетеризации рекомендуются для предотвращения внутрибольничной ИМП. Катетеризация рекомендуется в необходимых случаях. 35 ,36
34 Катетеризация мочевого пузыря является важным фактором при внутрибольничных инфекциях. Продолжительность катетеризации важна при ятрогенной инфекции. Катетеризация увеличивала вероятность ИМП на 5-10% каждый день после первых 48 часов. Таким образом, гигиена рук, стерильная катетеризация, закрытый стерильный катетер и сокращение времени катетеризации рекомендуются для предотвращения внутрибольничной ИМП. Катетеризация рекомендуется в необходимых случаях. 35 ,36
Существует множество немедикаментозных рекомендаций по профилактике рецидивирующих ИМП. Вот некоторые из них:
Считается, что витамин С повышает рН мочи, но доказательств недостаточно. Повышенное образование камней из оксалата кальция уменьшило его клиническое использование. 7 Витамин А, хрен (armoracia rusticana radix), пробиотики, клюква и настурция (tropaeoli majoris herba) дают благоприятные, но неубедительные результаты у взрослых. Повторные инфекции все еще возможны. 25 Недостаточно данных о профилактическом эффекте пробиотиков при рецидивирующих ИМП, особенно у детей 7 ,16 , что предполагает их ограниченное значение. Рандомизированное исследование, проведенное в 2007 г., продемонстрировало незначительное различие между пробиотиками и котримоксазолом в профилактике ИМП. 25 Сообщалось, что вакцинация инактивированными уропатогенами, уроваксом, в течение 3 недель подряд и бустерная доза через 6 месяцев является эффективным методом и снижает вероятность инфекции и повышает уровень секреторного IgA в моче. 26 Грудное молоко содержит защитные факторы, такие как секреторный IgA, лактоферрин, антиадгезивные олигосахариды, гликопротеины и цитокины, которые защищают от ИМП в первые 7 месяцев жизни. 14 Клинических испытаний метенамина гиппурата у детей не проводилось. Это может быть полезно при нормальном почечном тракте без серьезных нарушений. 25
Рандомизированное исследование, проведенное в 2007 г., продемонстрировало незначительное различие между пробиотиками и котримоксазолом в профилактике ИМП. 25 Сообщалось, что вакцинация инактивированными уропатогенами, уроваксом, в течение 3 недель подряд и бустерная доза через 6 месяцев является эффективным методом и снижает вероятность инфекции и повышает уровень секреторного IgA в моче. 26 Грудное молоко содержит защитные факторы, такие как секреторный IgA, лактоферрин, антиадгезивные олигосахариды, гликопротеины и цитокины, которые защищают от ИМП в первые 7 месяцев жизни. 14 Клинических испытаний метенамина гиппурата у детей не проводилось. Это может быть полезно при нормальном почечном тракте без серьезных нарушений. 25
Лечение ИМП было терапевтической проблемой в детской нефрологии. В зависимости от лекарственной устойчивости и изменений в сознании были предложены новые лекарства и протоколы лечения. Тяжесть и продолжительность лечения снизились, и были введены более простые методы с меньшими ограничениями.
Заявление о конфликте интересов: Все авторы заявляют
что у них нет конфликта интересов.
Источник финансирования: Нет
1. Керен Р. Визуализация и стратегии лечения детей после первой инфекции мочевыводящих путей. Curr Opin Педиатр. 2007;19(6):705–10. [PubMed] [Google Scholar]
2. Wald ER. Учебник детских инфекционных болезней. В: Фейгин Р.Д., Черри Д.Д., Деммлер Г.Дж., Каплан С.Л., редакторы. Цистит и пиелонефрит. 5-е изд. Филадельфия: компания Saunders; 2004. стр. 541–53. [Академия Google]
3. Шахид М., Кук Р. Является ли однократная суточная доза гентамицина безопасной и эффективной при лечении ИМП у младенцев и детей? Арч Дис Чайлд. 2007;92(9):823–4. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Wolff O, Maclennan C. Фактические данные, лежащие в основе рекомендаций ВОЗ: стационарная помощь детям: какая эмпирическая антибиотикотерапия является подходящей при неосложненных инфекциях мочевыводящих путей у детей в развивающихся странах. ? J Trop Педиатр. 2007;53(3):150–2. [PubMed] [Академия Google]
? J Trop Педиатр. 2007;53(3):150–2. [PubMed] [Академия Google]
5. Бауэр Р., Коган Б.А. Новые разработки в диагностике и лечении ИМП у детей. Урол Клин Норт Ам. 2008;35(1):47–58. [PubMed] [Google Scholar]
6. Alper BS, Curry SH. Инфекции мочевыводящих путей у детей. Ам семейный врач. 2005;72(12):2483–8. [PubMed] [Google Scholar]
7. Masson P, Matheson S, Webster AC, Craig JC. Мета-анализ профилактики и лечения инфекций мочевыводящих путей. Заразить Dis Clin North Am. 2009;23(2):355–85. [PubMed] [Академия Google]
8. Састре Дж. Б., Апарисио А. Р., Котальо Г. Д., Коломер Б. Ф., Эрнандес М. С. Инфекции мочевыводящих путей у новорожденных: клинические и рентгенологические исследования. Педиатр Нефрол. 2007;22(10):1735–41. [PubMed] [Google Scholar]
9. Ma JF, Shortliffe LM. Инфекции мочевыводящих путей у детей: этиология и эпидемиология. Урол Клин Норт Ам. 2004;31(3):517–51x. [PubMed] [Google Scholar]
10. Clark CJ, Kennedy WA, Shortliffe LD. Инфекции мочевыводящих путей у детей: когда следует беспокоиться. Урол Клин Норт Ам. 2010;37(2):229–41. [PubMed] [Google Scholar]
Урол Клин Норт Ам. 2010;37(2):229–41. [PubMed] [Google Scholar]
11. Williams GJ, Lee A, Craig JC. Антибиотики длительного действия для профилактики рецидивирующих инфекций мочевыводящих путей у детей. Cochrane Database Syst Rev. 2001;(4):CD001534. [PubMed] [Google Scholar]
12. John U, Kemper MJ. Инфекции мочевыводящих путей у детей после трансплантации почки. Педиатр Нефрол. 2009;24(6):1129–36. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Николь Л.Е. Инфекции мочевыводящих путей: традиционная фармакологическая терапия. Am J Med. 2002; 113 (Приложение 1A): 35S–44S. [PubMed] [Академия Google]
14. Малхотра С.М., Кеннеди, Вашингтон. Инфекции мочевыводящих путей у детей: лечение. Урол Клин Норт Ам. 2004;31(3):527–34, х. [PubMed] [Google Scholar]
15. Янтауш Б., Хер К.К. Клиническая детская нефрология. В: Хер К.К., Шнапер Х.В., Маккер С.П., Маккер С.П., редакторы. Инфекция мочевыводящих путей. 2-е изд. Лондон: Информа Здравоохранение; 2006. стр. 553–73. [Google Scholar]
стр. 553–73. [Google Scholar]
16. Shah G, Upadhyay J. Противоречия в диагностике и лечении инфекций мочевыводящих путей у детей. Педиатрические препараты. 2005;7(6):339–46. [PubMed] [Google Scholar]
17. Chang SL, Shortliffe LD. Детские инфекции мочевыводящих путей. Педиатр Клин Норт Ам. 2006;53(3):379–400, vi. [PubMed] [Google Scholar]
18. Neuhaus TJ, Berger C, Buechner K, Parvex P, Bischoff G, Goetschel P, et al. Рандомизированное исследование пероральных и последовательных внутривенных/пероральных цефалоспоринов у детей с пиелонефритом. Eur J Педиатр. 2008;167(9):1037–47. [PubMed] [Google Scholar]
19. Ходсон Э.М., Уиллис Н.С., Крейг Дж.К. Антибиотики при остром пиелонефрите у детей. Кокрановская база данных систематических обзоров. 2007; (4) CD003772. [PubMed] [Академия Google]
20. Зорк Дж.Дж., Кидду Д.А., Шоу К.Н. Диагностика и лечение инфекций мочевыводящих путей у детей. Clin Microbiol Rev. 2005;18(2):417–22. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Michael M, Hodson EM, Craig JC, Martin S, Moyer VA. Короткая по сравнению со стандартной продолжительностью лечения антибиотиками инфекций мочевыводящих путей: систематический обзор рандомизированных контролируемых исследований. Арч Дис Чайлд. 2002;87(2):118–23. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Michael M, Hodson EM, Craig JC, Martin S, Moyer VA. Короткая по сравнению со стандартной продолжительностью лечения антибиотиками инфекций мочевыводящих путей: систематический обзор рандомизированных контролируемых исследований. Арч Дис Чайлд. 2002;87(2):118–23. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Drekonja DM, Johnson JR. Инфекции мочевыводящих путей. Прим Уход. 2008;35(2):345–67, vii. [PubMed] [Академия Google]
23. Hellerstein S. Острая инфекция мочевыводящих путей — оценка и лечение. Curr Opin Педиатр. 2006;18(2):134–8. [PubMed] [Google Scholar]
24. Битц Р. Можем ли мы продолжить антибактериальную профилактику инфекций мочевыводящих путей? Педиатр Нефрол. 2006;21(1):5–13. [PubMed] [Google Scholar]
25. Williams G, Craig JC. Профилактика рецидивирующих инфекций мочевыводящих путей у детей. Curr Opin Infect Dis. 2009;22(1):72–6. [PubMed] [Google Scholar]
26. Сонг С.Х., Ким К.С. Антибиотикопрофилактика в детской урологии. Индиан Дж. Урол. 2008;24(2):145–9.. [Статья бесплатно PMC] [PubMed] [Google Scholar]
Урол. 2008;24(2):145–9.. [Статья бесплатно PMC] [PubMed] [Google Scholar]
27. Le Saux N, Pham B, Moher D. Оценка преимуществ противомикробной профилактики для предотвращения инфекций мочевыводящих путей у детей: систематический обзор. CMAJ. 2000;163(5):523–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Modgil G, Baverstock A. Следует ли избегать ванн с пеной у детей с инфекциями мочевыводящих путей? Арч Дис Чайлд. 2006;91(10):863–5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Mattoo TK. Медикаментозное лечение пузырно-мочеточникового рефлюкса – опрос в статье. Не забывайте о плацебо. Педиатр Нефрол. 2007;22(8):1113–20. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Conway PH, Cnaan A, Zaoutis T, Henry BV, Grundmeier RW, Keren R. Рецидивирующие инфекции мочевыводящих путей у детей: факторы риска и связь с профилактическим применением противомикробных препаратов. ДЖАМА. 2007;298(2):179–86. [PubMed] [Google Scholar]
31. Faust WC, Pohl HG. Роль профилактики пузырно-мочеточникового рефлюкса. Курр Опин Урол. 2007;17(4):252–6. [PubMed] [Google Scholar]
Faust WC, Pohl HG. Роль профилактики пузырно-мочеточникового рефлюкса. Курр Опин Урол. 2007;17(4):252–6. [PubMed] [Google Scholar]
32. Smith EA. Пиелонефрит, рубцевание почек и рефлюксная нефропатия: взгляд детского уролога. Педиатр Радиол. 2008; 38 (Приложение 1): S76–S82. [PubMed] [Академия Google]
33. Williams G, Lee A, Craig J. Антибиотики для профилактики инфекций мочевыводящих путей у детей: систематический обзор рандомизированных контролируемых исследований. J Педиатр. 2001;138(6):868–74. [PubMed] [Google Scholar]
34. Albrecht U, Goos KH, Schneider B. Рандомизированное двойное слепое плацебо-контролируемое исследование растительного лекарственного средства, содержащего Tropaeoli majoris her-ba (Nasturtium) и Armoraciae rusticanae radix ( Хрен) для профилактического лечения больных с хронически рецидивирующими инфекциями нижних мочевыводящих путей. Curr Med Res Opin. 2007;23(10):2415–22. [PubMed] [Академия Google]
35. Ksycki MF, Namias N. Внутрибольничная инфекция мочевыводящих путей.

 9007. 9007. 9007. 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007. 9007. 9007. 9007.
9007. 9007. 9007. 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007 9007. 9007. 9007. 9007.