У новорожденного белок в крови: Биохимический анализ крови — что показывает, какая норма
Анализ белка в пуповинной крови поможет прогнозировать смерть и развитие ДЦП у новорожденных
Отсутствие белка гаптоглобина у недоношенных детей
может указывать необходимость усиления мониторинга или других
профилактических вмешательств, — пишет eurekalert.org.
Исследователи из Университета Иллинойса в Чикаго обнаружили, что
некоторые недоношенные дети, рожденные без гаптоглобина — белка в
клетках крови, имеют более высокие риски кровоизлияния в мозг,
церебрального паралича и смерти. Результаты показывают, что
отсутствие белка может служить потенциальным биомаркером,
указывать на необходимость усиления мониторинга или других
профилактических вмешательств.
Исследование, опубликованное в журнале Lancet EClinicalMedicine,
представляло собой трансляционный анализ данных и образцов
пуповинной крови новорожденных, хранящихся в Национальных
институтах здравоохранения из предыдущего клинического испытания.
Доктор Университета Иллинойса Каталин Бухимски и д-р Ирина
Бухимски провели исследование и проанализировали образцы
пуповинной крови у 921 новорожденного, чтобы выяснить, был ли
гаптоглобин связан с развитием внутриутробного воспаления,
которое приводит к 30 процентам всех преждевременных родов.
Рассчитав отношения шансов — статистические данные, указывающие
на силу или слабость связей, они обнаружили, что недоношенные
дети, которые подвергались воспалению и которым не хватало
гаптоглобина, с большей вероятностью умерли до 1 года, либо у них
развился церебральный паралич, в отличие от недоношенных детей,
которые не подвергались воспалению и имели белок. Вероятность
внутрижелудочкового кровоизлияния, известного как кровотечение в
головном мозге, также была выше в группе с недостатком белка.
Эти результаты сохранялись даже при оценке потенциально смешанных
факторов, таких как масса тела при рождении, гестационный
возраст, пол плода или некоторые виды лечения, такие как сульфат
магния, применяемый для нейропротекции.
«Наше исследование предоставляет убедительные доказательства
того, что отсутствие гаптоглобина у недоношенных детей,
подвергшихся воспалению, является показателем повышенного риска
таких осложнений, как кровотечение в мозг, церебральный паралич и
даже смерть, — сказал доктор Каталин Бухимски, — профессор
акушерства и гинекологии в медицинском колледже Университета
Иллинойса и автор статьи.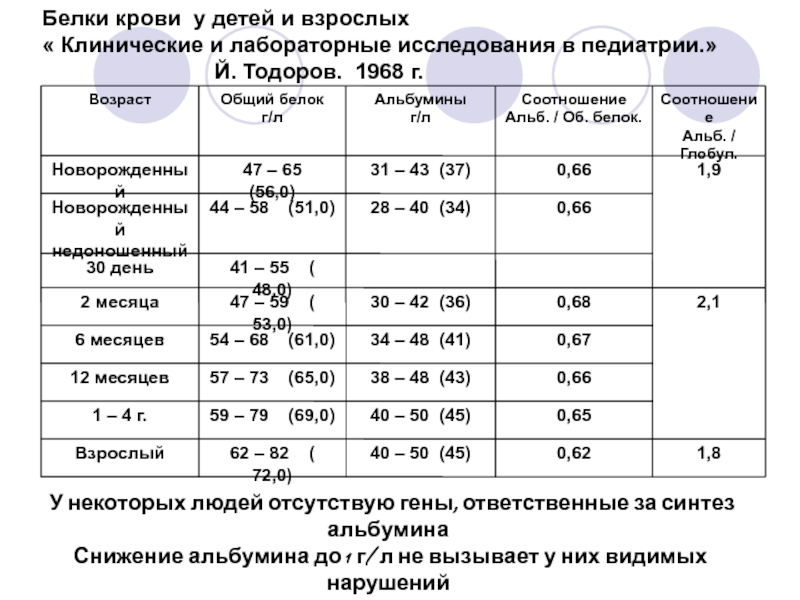 — Это подчеркивает потенциальную
— Это подчеркивает потенциальную
защитную роль гаптоглобина против краткосрочных и долгосрочных
неблагоприятных неонатальных исходов и предполагает, что белок
может быть ценным маркером неврологического повреждения и
необходимости клинических вмешательств».
Каталин Бухимски и Ирина Бухимски провели многочисленные
исследования гаптоглобина у недоношенных детей, но это первое
исследование, включающее большую репрезентативную выборку
участников.
По мнению Ирины Бухимски, необходим индивидуальный подход к теме
преждевременных родов в каждом конкретном случае. «Это
исследование также особенно увлекательно, потому что гаптоглобин
является известным белком. Исследователи видели его сотни раз, но
все время не под таким углом».
Для своих исследований Каталин Бухимски и Ирина Бухимски
разработали новый метод тестирования гаптоглобина на очень низких
уровнях, поскольку белок не достигает уровня взрослого до тех
пор, пока детям не исполнится около года.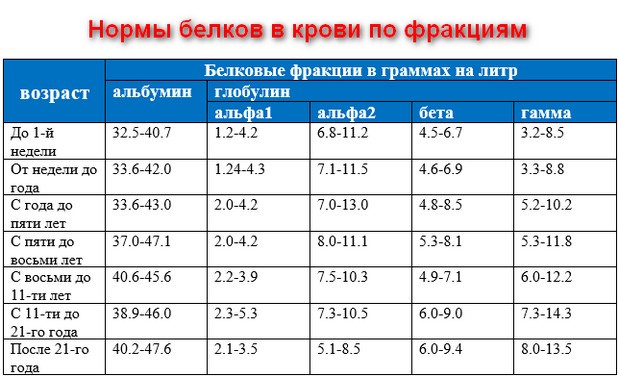
«Вывод этого исследования заключается в том, что простой анализ
пуповинной крови после родов может помочь врачам разработать
индивидуальный план ухода за некоторыми новорожденными из группы
риска», — сказал Каталин Бухимски.
[Фото: parents.ru]
Высокочувствительный С-реактивный белок (кардио), (СРБ высокочувствительный, high sensitivity CRP, hs-CRP)
Исследуемый материал
Сыворотка крови
Метод определения
Иммунотурбидиметрический, высокочувствительный (нижний предел обнаружения — 0,1 мг/л)
Синонимы: С-реактивный белок ультрачувствительный; СРБ кардио; High-sensitivity C-reactive protein (hs-CRP), quantitative; Cardio CRP; High-sensitivity CRP; Ultra-sensitive CRP.
Краткая характеристика определяемого вещества Высокочувствительный С-реактивный белок
С-реактивный белок – один из наиболее чувствительных маркеров острой фазы воспаления. Уровень СРБ значительно повышается при инфекциях, воспалительных процессах и любом повреждении тканей. Традиционное использование теста СРБ нацелено на выявление инфекций и выраженного воспаления в организме (см. тест № 43). В таком стандартном варианте исследования используют диагностический порог СРБ <5 мг/л или <10 мг/л, превышение которого указывает на наличие значимого воспаления или инфекции, или повреждения тканей разного происхождения.
Традиционное использование теста СРБ нацелено на выявление инфекций и выраженного воспаления в организме (см. тест № 43). В таком стандартном варианте исследования используют диагностический порог СРБ <5 мг/л или <10 мг/л, превышение которого указывает на наличие значимого воспаления или инфекции, или повреждения тканей разного происхождения.
Установлено, что концентрация СРБ в небольшой степени повышается также при эндогенном сосудистом вялотекущем воспалении низкого уровня активности, сопровождающем процесс развития атеросклероза сосудов. Для выявления такого персистирующего воспаления низкой степени, связываемого с повышением кардиорисков, необходимы высокочувствительные методы определения СРБ, позволяющие достаточно точно различать концентрации СРБ даже в обычно считающемся нормальным диапазоне 0,5-5,0 (10,0) мг/л.
Определение концентрации С-реактивного белка с целью оценки риска сердечно-сосудистых заболеваний следует проводить в отсутствие острых или недавних воспалительных заболеваний (включая инфекции и травмы). По данным проведенных исследований, у лиц с уровнем высокочувствительного СРБ, приближающемся к верхнему пределу стандартного диапазона нормы, потенциальный риск развития в будущем сердечно-сосудистых заболеваний ориентировочно от 1,5 до 4 раз выше, чем у лиц с значениями СРБ <1,0 мг/л.
По данным проведенных исследований, у лиц с уровнем высокочувствительного СРБ, приближающемся к верхнему пределу стандартного диапазона нормы, потенциальный риск развития в будущем сердечно-сосудистых заболеваний ориентировочно от 1,5 до 4 раз выше, чем у лиц с значениями СРБ <1,0 мг/л.
Для индивидуального определения потенциального сердечно-сосудистого риска применяют различные алгоритмы, из которых в настоящее время рекомендована и широко используется шкала SCORE. Она основана на учете возраста, пола, величины систолического артериального давления, уровня общего холестерина (с уточнением по уровню холестерина антиатерогенных липопротеидов высокой плотности – ЛПВП), факта курения.
Определение потенциальных сердечно-сосудистых рисков с использованием подобных систем оценки рекомендуется применять взрослым лицам старше 40 лет, за исключением тех, кого автоматически относят к группе высокого и очень высокого сердечно-сосудистого риска (пациенты с сердечно-сосудистыми заболеваниями, сахарным диабетом, хронической болезнью почек или очень высокими уровнями отдельных факторов риска). Такая оценка позволяет вовремя применить профилактические меры. Однако и инфаркт, и инсульт иногда неожиданно развиваются и у людей с умеренным или низким по указанным базовым факторам расчетным риском. Поэтому лицам, отнесенным в группу умеренного сердечно-сосудистого риска, для более точных оценок целесообразно определять дополнительные биомаркеры, в том числе маркер воспаления (высокочувствительный СРБ), маркер поражения клеток миокарда (сердечный тропонин I).
Такая оценка позволяет вовремя применить профилактические меры. Однако и инфаркт, и инсульт иногда неожиданно развиваются и у людей с умеренным или низким по указанным базовым факторам расчетным риском. Поэтому лицам, отнесенным в группу умеренного сердечно-сосудистого риска, для более точных оценок целесообразно определять дополнительные биомаркеры, в том числе маркер воспаления (высокочувствительный СРБ), маркер поражения клеток миокарда (сердечный тропонин I).
С какой целью проводят исследование крови на Высокочувствительный С-реактивный белок
Данное исследование является вариантом оценки уровня С-реактивного белка, предназначенным для дополнительного уточнения сердечно-сосудистых рисков у пациентов, отнесенных в группу умеренного риска по базовым факторам.
Что может повлиять на результат исследования крови на Высокочувствительный С-реактивный белок
Прогностическая значимость высокочувствительного исследования СРБ в оценке сердечно-сосудистых рисков ограничена тем, что его уровень в крови подвержен влиянию большого числа факторов. При выявлении признаков повышенного кардиориска в тесте высокочувствительного СРБ, его исследование целесообразно через некоторое время повторить, чтобы убедиться в том, что полученный результат не случаен.
При выявлении признаков повышенного кардиориска в тесте высокочувствительного СРБ, его исследование целесообразно через некоторое время повторить, чтобы убедиться в том, что полученный результат не случаен.
Следует понимать, что СРБ высокочувствительным (тест № 1643) и СРБ стандартным (тест № 43) тестами определяется один и тот же белок. При значениях СРБ выше 10 мг/л следует исключить наличие инфекционного процесса. Лицам с хроническими воспалительными заболеваниями (например, ревматоидным артритом) нецелесообразно применять высокочувствительный СРБ, поскольку уровень С-реактивного белка при этом заболевании всегда высокий, и использование высокочувствительного формата теста не имеет значения.
Влияние лекарственных препаратов: нестероидные противовоспалительные лекарственные препараты (аспирин, ибупрофен и пр.), статины снижают уровень С-реактивного белка (поскольку снижают активность воспаления).
Литература
- Бойцов С. А. и др. Кардиоваскулярная профилактика 2017.
 Российские национальные рекомендации //Российский кардиологический журнал. – 2018. – №. 6.
Российские национальные рекомендации //Российский кардиологический журнал. – 2018. – №. 6. - Rusnak J. et al. Biomarkers in stable coronary artery disease //Current pharmaceutical biotechnology. – 2017. – Т. 18. – №. 6. – С. 456-471.
- Denegri A., Boriani G. High sensitivity C-reactive protein (hsCRP) and its implications in cardiovascular outcomes //Current Pharmaceutical Design. – 2020.
Исследование Хопкинса показывает, что повышенный уровень белка может помочь предсказать травму головного мозга у новорожденных
Результаты также проливают свет на ценность охлаждения всего тела для предотвращения повреждения головного мозга
Дата выпуска: 13 октября 2011 г.
Исследователи из Университета Джона Хопкинса обнаружили, что повышенный уровень в крови белка, специфичного для клеток центральной нервной системы, который жизненно важен для структуры мозга, может помочь врачам выявить новорожденных с травмами головного мозга из-за недостатка кислорода.
Измерения белка также могут отслеживать, насколько хорошо работает терапия охлаждением тела, предназначенная для предотвращения необратимого повреждения головного мозга. Подробный отчет о находке команды Хопкинса опубликован в текущем Американском журнале акушерства и гинекологии.
В ходе годичного исследования изучались уровни глиального фибриллярного кислого белка (GFAP) у 23 новорожденных, родившихся между 36 и 41 неделей беременности, у которых был диагностирован клинический дефицит кислорода в головном мозге (гипоксически-ишемическая энцефалопатия, или ГИЭ), и сравнивали их с таковыми в дети, рожденные в один и тот же период беременности без черепно-мозговых травм».
ГИЭ может вызвать смерть в период новорожденности или привести к задержке развития, умственной отсталости или церебральному параличу. В США заболеваемость ГИЭ составляет от 1 до 8 случаев на 1000 рождений.
«GFAP, циркулирующий белок, специфичный для головного мозга, уже измеряется у взрослых пациентов после инсульта, остановки сердца или черепно-мозговой травмы, чтобы дать прогноз выживания или повреждения головного мозга», — говорит Эрнест М. Грэм, доктор медицинских наук, доцент гинекологии и акушерства, а также экспертом в области медицины матери и плода в Университете Джонса Хопкинса. «Теперь мы знаем, что этот биомаркер может служить надежным предиктором заболевания, развития травмы и исхода у новорожденных», — добавляет он.
Грэм, доктор медицинских наук, доцент гинекологии и акушерства, а также экспертом в области медицины матери и плода в Университете Джонса Хопкинса. «Теперь мы знаем, что этот биомаркер может служить надежным предиктором заболевания, развития травмы и исхода у новорожденных», — добавляет он.
В рамках исследования исследователи получили белок GFAP из пуповинной крови во время рождения, из крови новорожденных, взятых при поступлении в отделение интенсивной терапии новорожденных (NICU), и из ежедневных образцов крови в течение семидневного периода. Уровни GFAP были значительно выше у детей с черепно-мозговой травмой из-за недостатка кислорода в течение первой недели жизни.
«Акушеры и неонатологи сталкиваются со сложной задачей быстрой идентификации ГИЭ у новорожденных, потому что современные маркеры для идентификации были неточными», — говорит Грэм. «Тесты GFAP могут удовлетворить эту потребность».
Младенцы в исследовании, у которых были аномальные МРТ головного мозга и которых лечили охлаждением всего тела, имели самые высокие уровни GFAP. Лечение снижает температуру тела до 92,3 градусов по Фаренгейту, начиная с шести часов после рождения и продолжая в течение трех дней.
Лечение снижает температуру тела до 92,3 градусов по Фаренгейту, начиная с шести часов после рождения и продолжая в течение трех дней.
«Несмотря на то, что охлаждающая терапия снижает риск смерти и неврологических нарушений у новорожденных, она далека от идеальной терапии, и ее эффективность варьируется от ребенка к ребенку», — говорит соавтор Аллен Эверетт, доктор медицинских наук, детский кардиолог из Детской больницы Джона Хопкинса. Центр. «На самом деле мы не знаем наверняка, действительно ли за 72 часа охлаждения мозг восстанавливается. Биомаркеры, такие как GFAP, могут устранить эту неопределенность, сообщая врачам, как реагирует мозг, позволяя им соответствующим образом адаптировать лечение».
По словам Грэма, у половины детей с черепно-мозговой травмой в этом исследовании был повышен уровень GFAP после завершения 72-часового периода охлаждения. «Увеличение после охлаждения может быть результатом продолжающейся травмы головного мозга или может быть свидетельством травмы от согревания. У нас нет суррогатных маркеров терапевтического успеха. Вполне возможно, что белки мозга, такие как GFAP, восполнят этот пробел».
У нас нет суррогатных маркеров терапевтического успеха. Вполне возможно, что белки мозга, такие как GFAP, восполнят этот пробел».
По данным Graham, легкое охлаждение сразу после ГИЭ сохраняет энергетический метаболизм головного мозга, уменьшает цитотоксический отек и улучшает гистологический и функциональный результат.
«Хотя предварительные выводы исследователей могут проложить путь к более широкому изучению образцов крови и более длительному и более глубокому охлаждению, чтобы увидеть, насколько хорошо этот биомаркер может помочь оценить эффективность лечения. Необходимы дальнейшие исследования, чтобы узнать, как повышенные уровни GFAP связаны с неврологической инвалидностью, что оценивается по долгосрочному наблюдению и степени повреждения головного мозга на МРТ», — говорит Грэм.
Аллен Эверетт
http://www.hopkinschildrens.org/staffDetail.aspx?id=2030&terms=allen+everett
Информация о скрининге новорожденных на дефицит трифункционального белка | Первый тест ребенка | Скрининг новорожденных
Последующее обследование
Врач вашего ребенка может спросить вас, проявляются ли у вашего ребенка какие-либо признаки СФП (см.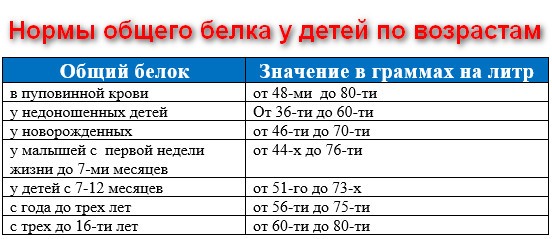 Ранние признаки ниже). Если у вашего ребенка есть определенные признаки, врач вашего ребенка может предложить начать немедленное лечение.
Ранние признаки ниже). Если у вашего ребенка есть определенные признаки, врач вашего ребенка может предложить начать немедленное лечение.
Если результат скрининга новорожденного вашего ребенка на дефицит трифункционального белка (TFP) выходит за пределы нормы, лечащий врач вашего ребенка или сотрудники программы скрининга штата свяжутся с вами, чтобы организовать дополнительное обследование вашего ребенка. Важно помнить, что результат скрининга, выходящий за пределы диапазона, не обязательно означает, что у вашего ребенка есть заболевание. Результат может выйти за пределы допустимого диапазона, поскольку первоначальный образец крови был слишком мал или тест был проведен слишком рано. Тем не менее, поскольку у некоторых детей действительно есть это заболевание, очень важно, чтобы вы пришли на повторный прием для проведения подтверждающего теста. Поскольку вредное воздействие невылеченного TFP может проявляться вскоре после рождения, последующее обследование должно быть завершено как можно скорее, чтобы определить, есть ли у вашего ребенка заболевание.
Последующее тестирование будет включать проверку образцов мочи и крови вашего ребенка на наличие вредных уровней кислот и токсинов. Определенные кислоты и токсины накапливаются в организме, когда у ребенка есть состояние окисления жирных кислот, поэтому измерение уровня этих веществ в организме вашего ребенка может помочь врачам определить, есть ли у вашего ребенка заболевание. Специфическая картина ацилкарнитинов в крови и органических кислот в моче может указывать на то, что у вашего ребенка TFP. Поскольку TFP имеет многие из тех же признаков, что и другое состояние окисления жирных кислот, называемое LCHAD, врач вашего ребенка может назначить дальнейшее тестирование, чтобы увидеть, есть ли у вашего ребенка какое-либо состояние. Иногда последующее тестирование может также включать тестирование очень небольшого образца кожи.
О дефиците трифункционального белка
Ранние признаки
В зависимости от возраста возникновения различают три различные формы дефицита трифункционального белка (TFP): ранний, детский и легкий. Если у вашего ребенка ранний TFP, вы начнете видеть признаки в период между рождением и возрастом 2, тогда как у людей с TFP в детстве признаки проявляются после младенчества. Легкий TFP встречается очень редко. Если у вашего ребенка легкая форма TFP, у него могут начать проявляться признаки в любое время в возрасте от 2 лет до совершеннолетия.
Если у вашего ребенка ранний TFP, вы начнете видеть признаки в период между рождением и возрастом 2, тогда как у людей с TFP в детстве признаки проявляются после младенчества. Легкий TFP встречается очень редко. Если у вашего ребенка легкая форма TFP, у него могут начать проявляться признаки в любое время в возрасте от 2 лет до совершеннолетия.
Признаки ранней СФП включают:
- Плохой аппетит
- Сон дольше или чаще
- Усталость
- Слабый мышечный тонус (так называемый гипотония)
- Лихорадка
- Рвота
- Диарея
- Низкий уровень сахара в крови (так называемый гипогликемия) )
- Раздражительность
- Изменения в поведении
- Отсутствие рефлексов или реакции на боль
- Задержка развития
Многие из этих признаков могут проявляться, когда ваш ребенок ест продукты, которые его организм не может расщепить. Они могут быть вызваны длительными периодами времени без еды, болезнями и инфекциями.
Если у вашего ребенка проявляются какие-либо из этих признаков, обязательно немедленно обратитесь к педиатру.
Если вас интересует информация о признаках детского возраста или легкой формы TFP, посетите веб-сайт STAR-G.
Лечение
Ваш ребенок должен будет соблюдать ограниченную диету, чтобы избежать определенных продуктов с высоким содержанием жиров, которые организм вашего ребенка не может расщепить. Диетолог или нутрициолог может помочь вам спланировать диету, которая сохранит здоровье вашего ребенка и обеспечит его питательными веществами, необходимыми для здорового роста.
Ваш ребенок также должен есть часто, чтобы избежать многих признаков, упомянутых в разделе «Ранние признаки».
Пищевые добавки и лекарства
Врач вашего ребенка может порекомендовать пищевые добавки для вашего ребенка. Масло со средними цепочками триглицеридов (MCT) — это добавка, которая дает энергию вашему ребенку, поскольку оно содержит жирные кислоты, которые могут переваривать люди с дефицитом трифункционального белка (TFP). Поговорите с врачом вашего ребенка, прежде чем начинать это лечение.
Поговорите с врачом вашего ребенка, прежде чем начинать это лечение.
Некоторые дети с TFP также принимают рецептурные добавки L-карнитина. L-карнитин — это вещество, которое вырабатывается организмом естественным образом, но организм вашего ребенка может не вырабатывать его в достаточном количестве. Прием L-карнитина может помочь вашему ребенку с TFP расщеплять жиры и удалять вредные вещества из организма. Врач вашего ребенка должен будет выписать вам рецепт на эти добавки.
Изменение образа жизни
Вам необходимо оградить своего ребенка от очень высоких и низких температур. Экстремальные температуры могут способствовать разрушению мышц.
Ожидаемые результаты
Если у вашего ребенка в детстве или умеренная недостаточность трифункционального белка (TFP), он может вести здоровый образ жизни с помощью лечения. У некоторых детей все еще могут быть эпизоды гипогликемии (низкий уровень сахара в крови) даже при лечении.
Младенцам с ранней TFP может помочь лечение. Тем не менее, большинство детей рискуют умереть молодыми от проблем с сердцем и дыханием, даже при лечении.
Тем не менее, большинство детей рискуют умереть молодыми от проблем с сердцем и дыханием, даже при лечении.
Если TFP не лечить, эпизоды гипогликемии могут привести к коме или даже смерти.
Причины
Когда мы едим пищу, ферменты помогают ее расщеплению. Некоторые ферменты помогают расщеплять жиры на строительные блоки, называемые жирными кислотами. Другие ферменты расщепляют эти жирные кислоты.
Жирные кислоты построены в виде цепочек, и эти цепи бывают разной длины. Они классифицируются как короткие, средние, длинные или очень длинные. Различные ферменты предназначены для расщепления жирных кислот разной длины. Ферментный комплекс (несколько связанных друг с другом ферментов), называемый трифункциональным белком, помогает расщеплять «длинные» цепи жирных кислот. Если у вас есть вопрос о том, что делает «длинную» жирную кислоту, перейдите по этой ссылке.
Если у вашего ребенка дефицит трифункционального белка (TFP), его организм либо не вырабатывает достаточно, либо вырабатывает нерабочие ферменты трифункционального белка. Это вредно для организма, потому что сердце и мышцы вашего ребенка нуждаются в жирных кислотах для получения энергии. Организму вашего ребенка также необходимо расщеплять жирные кислоты, когда не хватает сахара, например, между приемами пищи.
Это вредно для организма, потому что сердце и мышцы вашего ребенка нуждаются в жирных кислотах для получения энергии. Организму вашего ребенка также необходимо расщеплять жирные кислоты, когда не хватает сахара, например, между приемами пищи.
TFP является аутосомно-рецессивным генетическим заболеванием. Это означает, что ребенок должен унаследовать две копии неработающего гена TFP, по одной от каждого родителя, чтобы иметь заболевание. Каждый из родителей ребенка с аутосомно-рецессивным заболеванием является носителем одной копии неработающего гена, но обычно у них не проявляются признаки и симптомы заболевания. Хотя рождение ребенка с TFP встречается редко, когда оба родителя являются носителями, у них может быть более одного ребенка с этим заболеванием. Узнайте больше об аутосомно-рецессивном наследовании.
Поддержка дефицита трифункционального белка
Support Services
Группы поддержки могут помочь связать людей, у которых есть ребенок или другой член семьи, страдающий дефицитом трифункционального белка (TFP), с поддерживающим сообществом людей, которые имеют опыт и знания в жизни с этим заболеванием. Эти организации предлагают ресурсы для пострадавших лиц и их семей, а также поставщиков медицинских услуг.
Эти организации предлагают ресурсы для пострадавших лиц и их семей, а также поставщиков медицинских услуг.
- Группа поддержки семьи FOD
Accessing Care
Вместе с лечащим врачом определите дальнейшие шаги по уходу за ребенком. Врач вашего ребенка может помочь вам координировать лечение с врачом, который специализируется на обмене веществ, диетологом, который может помочь спланировать специализированную диету вашего ребенка, и другими медицинскими ресурсами в вашем районе. В зависимости от признаков и симптомов дефицита трифункционального белка (TFP) у вашего ребенка врач вашего ребенка может работать с другими врачами, специализирующимися на лечении сердца, легких или мышц, чтобы заботиться о вашем ребенке. Некоторые дети с TFP имеют задержки в развитии. Если вы считаете, что ваш ребенок не соответствует основным этапам своего развития, спросите своего лечащего врача о следующих шагах для получения доступа к оценке развития и уходу.
Поскольку TFP является генетическим заболеванием, вы можете поговорить со специалистом-генетиком. Генетический консультант или генетик может помочь вам понять причины состояния, обсудить генетическое тестирование на TFP и понять, что этот диагноз означает для других членов семьи и будущих беременностей. Поговорите с врачом вашего ребенка о получении направления. Поисковая система Clinic Services, предлагаемая Американским колледжем медицинской генетики и геномики (ACMG), и инструмент «Найти консультанта-генетика» на веб-сайте Национального общества консультантов-генетиков (NSGC) — это два полезных ресурса, которыми вы или поставщик медицинских услуг вашего ребенка можете воспользоваться. выявить местных специалистов.
Генетический консультант или генетик может помочь вам понять причины состояния, обсудить генетическое тестирование на TFP и понять, что этот диагноз означает для других членов семьи и будущих беременностей. Поговорите с врачом вашего ребенка о получении направления. Поисковая система Clinic Services, предлагаемая Американским колледжем медицинской генетики и геномики (ACMG), и инструмент «Найти консультанта-генетика» на веб-сайте Национального общества консультантов-генетиков (NSGC) — это два полезных ресурса, которыми вы или поставщик медицинских услуг вашего ребенка можете воспользоваться. выявить местных специалистов.
Семейный опыт
Опыт каждой семьи с заболеванием уникален, но есть некоторые аспекты диагностики, опыта и лечения дефицита трифункционального белка (TFP), которые аналогичны другим состояниям окисления жирных кислот. Возможно, вам будет полезно прочитать истории семей, пострадавших от других условий окисления жирных кислот. Фонд «Спасите младенцев с помощью скрининга» публикует истории семей, у которых есть ребенок с состоянием окисления жирных кислот.
