Митохондриальная недостаточность у детей: Митохондриальная патология у детей | #01/16
Проявления митохондриальной дисфункции у детей с дисплазией соединительной ткани и хроническим гастродуоденитом | Иванова
1. Брин И.Л., Неудахин Е.В., Дунайкин М.Л. Карнитин в педиатрии: исследования и клиническая практика. М.: Медпрактика-М, 2015; 112. [Brin I.L., Neudahin E.V., Dunajkin M.L. Carnitine in Pediatrics: research and clinical practice. Moscow: Medpraktika-M, 2015; 112 (in Russ.)]
2. Ивянский С.А., Балыкова Л.А., Щекина Н.В., Аритки- на А.А., Варлашина К.А., Широкова А.А. и др. Нарушения соединительной ткани у детей и подростков, занимающихся спортом. Consilium Medicum. Педиатрия 2016; 4: 94–101. [Ivyanskiy S.A., Balykova L.A., SHCHekina N.V., Aritkina A.A., Varlashina K.A., SHirokova A.A. et al. Disorders of connective tissue in children and adolescents involved in sports. Consilium Medicum. Pediatriya 2016; 4: 94–101 (in Russ.)]
3. Николаева Е.А. Митохондриальные болезни у детей: клинические проявления, возможности диагностики и лечения. Учебное пособие. М., 2017; 88. [Nikolaeva E.A. Mitochondrial diseases in children: clinical manifestations, diagnostics and treatment. Tutorial. Moscow, 2017; 88 (in Russ.)]
М., 2017; 88. [Nikolaeva E.A. Mitochondrial diseases in children: clinical manifestations, diagnostics and treatment. Tutorial. Moscow, 2017; 88 (in Russ.)]
4. Кадурина Т.И., Гнусаев С.Ф., Аббакумова Л.Н., Алимова И.Л., Антонова Н.С., Апенченко Ю.С. и др. Наследственные и многофакторные нарушения соединительной ткани у детей: алгоритмы диагностики, тактика ведения. Проект Российских рекомендаций. Педиатрия. Журнал им. Г.Н. Сперанского 2014; 93(5): Приложение: 1–40. [Kadurina T.I., Gnusaev S.F., Abbakumova L.N., Alimova I.L., Antonova N.S., Apenchenko Yu.S. et al. Inherited and multifactorial disorders of connective tissue in children: diagnostic algorithms and management. The project of the Russian recommendations. Pediatriya. Zhurnal im. G.N. Speranskogo ( Pediatria. Journal named after G.N. Speransky) 2014: 93(5): Suppl: 1–40 (in Russ.)]
5. Полиорганные нарушения при дисплазиях соединительной ткани у детей. Алгоритмы диагностики. Тактика ведения. Российские рекомендации. Часть 2. Вопросы детской диетологии 2017; 15(3): 47–70. [Multiorgan disorders in connective tissue dysplasia in children. Algorithms of diagnostics. Tactics of reference. Russian recommendations. Part 2. Voprosy detskoi dietologii 2017; 15 (3): 47–70 (in Russ.)]
Вопросы детской диетологии 2017; 15(3): 47–70. [Multiorgan disorders in connective tissue dysplasia in children. Algorithms of diagnostics. Tactics of reference. Russian recommendations. Part 2. Voprosy detskoi dietologii 2017; 15 (3): 47–70 (in Russ.)]
6. Кадурина Т.И., Горбунова В.Н. Дисплазия соединительной ткани: Руководство для врачей. СПб: Элби-СПб 2009; 704. [Kadurina T.I., Gorbunova V.N. Connective tissue dysplasia: a Guide for physicians. SPb.: EHlbi-SPb, 2009; 704 (in Russ.)]
7. Чемоданов В.В., Краснова Е.Е. Особенности течения заболеваний у детей с дисплазией соединительной ткани. Иваново: ГОУ ВПО ИвГМА Росздрава, 2009; 140. [Chemodanov V.V., Krasnova E.E. Peculiarities of disease in children with connective tissue dysplasia. Ivanovo: GOU VPO IvGMA Roszdrava, 2009; 140 (in Russ.)]
8. Арсентьев В.Г., Арзуманова Т.И., Асеев М.В., Баранов В.С., Калядин С.Б., Никифорова И.Д., Шабалов Н.П. Полиорганные нарушения при ДСТ у детей и подростков. Педиатрия 2009; 88(1): 135–138. [Arsent’ev V.G., Arzumanova T.I., Aseev M.V., Baranov V.S., Kalyadin S.B., Nikiforova I.D., Shabalov N.P. Multiple organ disorders in connective tissue dysplasia in children and adolescents. Pediatriya 2009; 88(1): 135–138 (in Russ.)]
[Arsent’ev V.G., Arzumanova T.I., Aseev M.V., Baranov V.S., Kalyadin S.B., Nikiforova I.D., Shabalov N.P. Multiple organ disorders in connective tissue dysplasia in children and adolescents. Pediatriya 2009; 88(1): 135–138 (in Russ.)]
9. Апенченко Ю.С., Басалаева Н.В., Капустина Л.В., Иванова И.И. Клинические и биохимические признаки дисплазии соединительной ткани у детей с гастроэзофагеальной рефлюксной болезнью. Вестник Ивановской медицинской академии 2014; 19(3): 17–19. [Apenchenko Yu.S., Basalaeva N.V., Kapustina L.V., Ivanova I.I. Clinical and biochemical signs of connective tissue dysplasia in children with gastroesophageal reflux disease. Vestnik Ivanovskoi meditsinskoi akademii 2014; 19(3): 17–19 (in Russ.)]
10. Иванова И.И., Гнусаев С.Ф., Апенченко Ю.С., Капустина Л.В., Герасимов Н.А., Солдатова И.А. Особенности проявлений заболеваний пищеварительного тракта у детей с дисплазией соединительной ткани. Вопросы современной педиатрии 2012; 11(5): 50–55. [Ivanova I.I., Gnusaev S. F., Apenchenko Yu.S., Kapustina L.V., Gerasimov N.A., Soldatova I.A. Features of diseases of the digestive tract in children with connective tissue dysplasia. Voprosy sovremennoi pediatrii 2012; 11(5): 50–55 (in Russ.)]
F., Apenchenko Yu.S., Kapustina L.V., Gerasimov N.A., Soldatova I.A. Features of diseases of the digestive tract in children with connective tissue dysplasia. Voprosy sovremennoi pediatrii 2012; 11(5): 50–55 (in Russ.)]
11. Смирнова Е.В., Лобанов Ю.Ф., Скударнов Е.В. Особенности течения эрозивного гастродуоденита у детей с дисплазией соединительной ткани. Вопросы современной педиатрии 2006; 5(4): 122–129. [Smirnova E.V., Lobanov Yu.F., Skudarnov E.V. Peculiarities of erosive gastroduodenitis in children with connective tissue dysplasia. Voprosy sovremennoi pediatrii 2006; 5(4): 122–129 (in Russ.)]
12. Демин В.Ф., Ключников С.О., Ключникова М.А. Значение соединительнотканных дисплазий в патологии детского возраста. Вопросы современной педиатрии 2005; 4(1): 50–56. [Demin V.F., Klyuchnikov S.O., Klyuchnikova M.A. The value of connective tissue dysplasia in childhood pathology. Voprosy sovremennoi pediatrii 2005; 4(1): 50–56 (in Russ.)]
13. Трутнева Л.А., Чемоданов В.В. Особенности гастродуоденальных заболеваний у детей с недифференцированной дисплазией соединительной ткани. Педиатрия. Журнал им. Г.Н. Сперанского 2010; 89(2): 12–17. [Trutneva L.A., Chemodanov V.V. Peculiarities of gastroduodenal diseases in children with undifferentiated dysplasia of connective tissue. Pediatriya. Zhurnal im. G.N. Speranskogo ( Pediatria. Journal named after G.N. Speransky) 2010; 89(2): 12–17 (in Russ.)]
Педиатрия. Журнал им. Г.Н. Сперанского 2010; 89(2): 12–17. [Trutneva L.A., Chemodanov V.V. Peculiarities of gastroduodenal diseases in children with undifferentiated dysplasia of connective tissue. Pediatriya. Zhurnal im. G.N. Speranskogo ( Pediatria. Journal named after G.N. Speransky) 2010; 89(2): 12–17 (in Russ.)]
14. Рахматуллина З.А., Выхристюк О.Ф., Русакова В.Д. Дис- плазии соединительной ткани и полиорганная патология у детей. Мед помощь 2008; 5: 29–31. [Rahmatullina Z.A., Vyhristyuk O.F., Rusakova V.D. Connective tissue dysplasia and multiple organ pathology in children. Med pomoshch’ 2008; 5: 29–31 (in Russ.)]
15. Сухоруков В.С. Очерки митохондриальной патологии. М.: Медпрактика-М, 2011; 288. [Suhorukov V.S. Study of mitochondrial pathology. Moscow: Medpraktika-M, 2011; 288 (in Russ.)]
16. Баедилова М.Т., Суменко В.В., Сухоруков В.С., Лебедькова С.Е., Трусова О.Ю. Эффективность энерготропной терапии при нарушении клеточного энергообмена у детей с пролапсом митрального клапана Российский вестник перинатологии и педиатрии 2017; 62(1): 74–80. [Baedilova M.T., Sumenko V.V., Suhorukov V.S., Lebed’kova S.E., Trusova O.Yu. The effectiveness of energotropic therapy in violation of cellular energy exchange in children with mitral valve prolapse. Rossiyskiy Vestnik Perinatologii i Pediatrii ( Russian Bulletin of Perinatology and Pediatrics) 2017; 62(1): 74–80 (in Russ.)] DOI: 10.21508/1027-4065-2017-62-1-74-80
[Baedilova M.T., Sumenko V.V., Suhorukov V.S., Lebed’kova S.E., Trusova O.Yu. The effectiveness of energotropic therapy in violation of cellular energy exchange in children with mitral valve prolapse. Rossiyskiy Vestnik Perinatologii i Pediatrii ( Russian Bulletin of Perinatology and Pediatrics) 2017; 62(1): 74–80 (in Russ.)] DOI: 10.21508/1027-4065-2017-62-1-74-80
17. Думова С.В., Чугунова О.Л. Внутриклеточные энергетические нарушения у недоношенных детей с задержкой внутриутробного развития и их коррекция. Практика педиатра 2013; 1: 68–69. [Dumova S.V., Chugunova O.L. Intracellular energy disorders in premature infants with intrauterine growth retardation and their correction. Praktika pediatra (Current Pediatrics) 2013; 1: 68–69 (in Russ.)]
18. Неудахин Е.В. Целесообразность использования препаратов карнитина при лечении хронических расстройств питания у детей. Практика педиатра 2015; 2: 48–52. [Neudahin E.V. The feasibility of using preparations of carnitine in the treatment of chronic eating disorders in children. Praktika pediatra ( Current Pediatrics) 2015; 2: 48–52 (in Russ.)]
Praktika pediatra ( Current Pediatrics) 2015; 2: 48–52 (in Russ.)]
19. Иванова И.И., Гнусаев С.Ф., Коваль Н.Ю., Герасимов Н.А., Солдатова И.А. Метаболические аспекты недифференцированной дисплазии соединительной ткани у детей. Российский вестник перинатологии и педиатрии 2012; 57(4): 103–111. [Ivanova I.I., Gnusaev S.F., Koval’ N.Yu., Gerasimov N.A., Soldatova I.A. Metabolic aspects of undifferentiated connective tissue dysplasia in children. Rossiyskiy Vestnik Perinatologii i Pediatrii ( Russian Bulletin of Perinatology and Pediatrics) 2012; 57(4): 103–111 (in Russ.)]
20. Parich S., Goldstein A., Koenig M.K., Scaglia F., Enns G.M., Saneto R. et al. Diagnosis and management of mitochondrial disease: a consensus statement from the Mitochondrial Medicine Society. J Genet Med 2015; 17(9): 689–701. DOI: 10.1038/gim.2014.177
21. Иванова И.И., Гнусаев С.Ф., Ильина А.А. Клинические проявления нарушений клеточного энергообмена при соматических заболеваниях у детей. Российский вестник перинатологии и педиатрии 2018; 63(2): 27–33. DOI: 10.21508/1027-4065-2018-63-2-27-33 [Ivanova I.I., Gnusaev S.F., Il’ina A.A. Clinical manifestations of cellular energy exchange disorders in somatic diseases in children. Rossiyskiy Vestnik Perinatologii i Pediatrii (Russian Bulletin of Perinatology and Pediatrics) 2018; 63(2): 27–33 (in Russ.)]
DOI: 10.21508/1027-4065-2018-63-2-27-33 [Ivanova I.I., Gnusaev S.F., Il’ina A.A. Clinical manifestations of cellular energy exchange disorders in somatic diseases in children. Rossiyskiy Vestnik Perinatologii i Pediatrii (Russian Bulletin of Perinatology and Pediatrics) 2018; 63(2): 27–33 (in Russ.)]
22. Каламбет Е.И., Османов И.М., Сухоруков В.С., Шабельникова Е.И., Хавкин А.И. Нарушения клеточного энергообмена и их коррекция при заболеваниях органов пищеварения у детей. Вопросы практической педиатрии 2012; 2: 69–72. [Kalambet E.I., Osmanov I.M., Suhorukov V.S., Shabel’nikova E.I., Khavkin А.I. Violation of cellular energy metabolism and their correction in diseases of the digestive system in children. Voprosy prakticheskoi pediatrii 2012; 2: 69–72 (in Russ.)]
23. Зиганшина А.А., Сухоруков В.С., Булатов В.П. Митохондриальная дисфункция у детей с рефлюкс-эзофагитом. Российский вестник перинатологии и педиатрии 2017; 62(2): 88–92. DOI: 10.21508/1027-4065-2017-62-2-88-93 [Ziganshina A. A., Suhorukov V.S., Bulatov V.P. Mitochondrial dysfunction in children with reflux esophagitis. Rossiyskiy Vestnik Perinatologii i Pediatrii (Russian Bulletin of Perinatology and Pediatrics) 2017; 62(2): 88–92 (in Russ.)]
A., Suhorukov V.S., Bulatov V.P. Mitochondrial dysfunction in children with reflux esophagitis. Rossiyskiy Vestnik Perinatologii i Pediatrii (Russian Bulletin of Perinatology and Pediatrics) 2017; 62(2): 88–92 (in Russ.)]
24. Ключников С.О., Ильяшенко Д.А., Ключникова М.С. Обоснование применения L-карнитина и коэнзима Q10 у подростков. Вопросы современной педиатрии 2008; 7(4): 102–104. [Klyuchnikov S.O., Il’yashenko D.А., Klyuchnikovа M.S. The rationale for the use of L-carnitine and coenzyme Q10 in adolescents. Voprosy Sovremennoi Pediatrii (Current Pediatrics) 2008; 7(4): 102–104 (in Russ.)]
25. Кадурина Т.И., Аббакумова Л.Н. Оценка степени тяжести недифференцированной дисплазии соединительной ткани у детей. Медицинский вестник Северного Кавказа 2008; 2: 15–21. [Kadurina T.I., Abbakumova L.N. Assessment of severity of undifferentiated connective tissue dysplasia in children. Meditsinskii vestnik Severnogo Kavkaza 2008; 2: 15–21 (in Russ.)]
26. Иванова И.И., Гнусаев С. Ф., Сухоруков В.С. Опыт применения препарата L-карнитина у детей с ХГД и ДСТ. Вопросы практической педиатрии 2018; 13(6): 72–78. DOI: 10.20953/1817-7646-2018-6-72-78 [Ivanova I.I., Gnusaev S.F., Suhorukov V.S. Experience with L-carnitine in children with chronic gastroduodenitis and connective tissue dysplasia. Voprosy prakticheskoi pediatrii 2018; 13(6): 72–78 (in Russ.)]
Ф., Сухоруков В.С. Опыт применения препарата L-карнитина у детей с ХГД и ДСТ. Вопросы практической педиатрии 2018; 13(6): 72–78. DOI: 10.20953/1817-7646-2018-6-72-78 [Ivanova I.I., Gnusaev S.F., Suhorukov V.S. Experience with L-carnitine in children with chronic gastroduodenitis and connective tissue dysplasia. Voprosy prakticheskoi pediatrii 2018; 13(6): 72–78 (in Russ.)]
Актуальные вопросы лечения митохондриальных нарушений uMEDp
Среди ярких событий современной медицинской науки одно из значимых мест занимает появление области, которую все чаще называют «митохондриальной медициной». Она интересна со многих точек зрения. Во-первых, как и полагается новому систематическому объединению, она знаменует собой выделение новых патологических процессов и нозологических форм. Во-вторых, ее безусловное прикладное значение определяется наличием специфической, так называемой энерготропной, терапии.
Первичные и вторичные митохондриальные нарушения
Ключевая область этого раздела медицины – наследственные синдромы, в основе которых лежат мутации генов, ответственных за митохондриальные белки (синдромы Кернса – Сейра, MELAS (mitochondrial encephalomyopathy, lactic acidosis, and stroke-like episodes), MERRF (myoclonic epilepsy with ragged red fibers), Пирсона, Барта и др. ). Однако класс состояний, характеризующихся митохондриальной недостаточностью, отнюдь не ограничивается этими «первичными» митохондриальными заболеваниями. Огромное количество болезней включает в себя нарушения клеточного энергообмена в качестве «вторичных» звеньев патогенеза: синдром хронической усталости, мигрени, кардиомиопатии, гликогенозы, заболевания соединительной ткани, диабет, рахит, тубулопатии, панцитопения, гипопаратиреоз, печеночная недостаточность и др. Особое значение для практической медицины имеет изучение указанных нарушений в связи с разработкой в этой области эффективных методов терапевтической коррекции.
). Однако класс состояний, характеризующихся митохондриальной недостаточностью, отнюдь не ограничивается этими «первичными» митохондриальными заболеваниями. Огромное количество болезней включает в себя нарушения клеточного энергообмена в качестве «вторичных» звеньев патогенеза: синдром хронической усталости, мигрени, кардиомиопатии, гликогенозы, заболевания соединительной ткани, диабет, рахит, тубулопатии, панцитопения, гипопаратиреоз, печеночная недостаточность и др. Особое значение для практической медицины имеет изучение указанных нарушений в связи с разработкой в этой области эффективных методов терапевтической коррекции.
К настоящему времени наиболее изучены дефекты, связанные с дефицитом различных комплексов дыхательной цепи и некоторых ферментов матрикса. Появляются клинические описания дефекта и других ферментов, например, наружной митохондриальной мембраны [1], так что до полного представления о тонких механизмах митохондриальной дисфункции еще далеко, и часто речь идет о недостаточности митохондриальной функции в целом. Ткани и органы зависят от митохондриальной активности в различной степени [2–5]. В их ряду на первом месте стоят нервные элементы, затем сердечная и скелетная мышечная ткани, почки, эндокринные железы и печень. Увеличение количества митохондрий и их структурные нарушения широко определяются в эндотелиальных клетках, гладких миоцитах и перицитах различных сосудов [6].
Ткани и органы зависят от митохондриальной активности в различной степени [2–5]. В их ряду на первом месте стоят нервные элементы, затем сердечная и скелетная мышечная ткани, почки, эндокринные железы и печень. Увеличение количества митохондрий и их структурные нарушения широко определяются в эндотелиальных клетках, гладких миоцитах и перицитах различных сосудов [6].
К болезням, причиной которых являются мутации митохондриальных генов, относятся синдромы Кернса – Сейра (нарушения со стороны глаз, атаксия, мышечная слабость, нарушения сердечной проводимости и другие симптомы), Пирсона (вялость, нарушения со стороны крови, кишечника, поджелудочной железы), MELAS (энцефаломиопатия, лактат-ацидоз, инсультоподобные эпизоды), оптическая нейропатия Лебера и многие другие. Причем описание таких синдромов продолжается и сейчас – так, в XXI веке уже опубликованы описания нескольких новых заболеваний.
Поскольку все митохондрии достаются новому организму только от цитоплазмы яйцеклетки, многие митохондриальные заболевания являются или спорадическими, или наследуются с нарушением законов Менделя – «внеядерное» или «цитоплазматическое» наследование по материнской линии. Распространенность этих болезней плохо изучена, но ясно, что они относятся к сравнительно редким наследственным заболеваниям. Отсюда и малый интерес широкого круга медиков к митохондриальной патологии.
Распространенность этих болезней плохо изучена, но ясно, что они относятся к сравнительно редким наследственным заболеваниям. Отсюда и малый интерес широкого круга медиков к митохондриальной патологии.
Однако эти заболевания, хотя и создали ядро «митохондриальной медицины», отнюдь не составляют всего ее спектра. В последние годы внимание медиков начал все больше приковывать следующий факт: несмотря на наличие в митохондриях собственной ДНК, кодируются ею всего около 2% белков, используемых в митохондриях. Иными словами, 98% наследственной информации о митохондриальных белках заложено в ядре, а значит, количество наследственных митохондриальных нарушений, связанных с ядерными мутациями, должно быть несоизмеримо больше тех, о которых упоминалось выше. А известно их на сегодняшний день не так много (среди них различные формы младенческих миопатий, болезни Альперса, Лея, Барта, Менкеса, синдромы недостаточности карнитина, некоторых ферментов цикла Кребса и дыхательной цепи), что понятно – маленькую митохондриальную ДНК гораздо легче изучать, чем гигантский ядерный геном.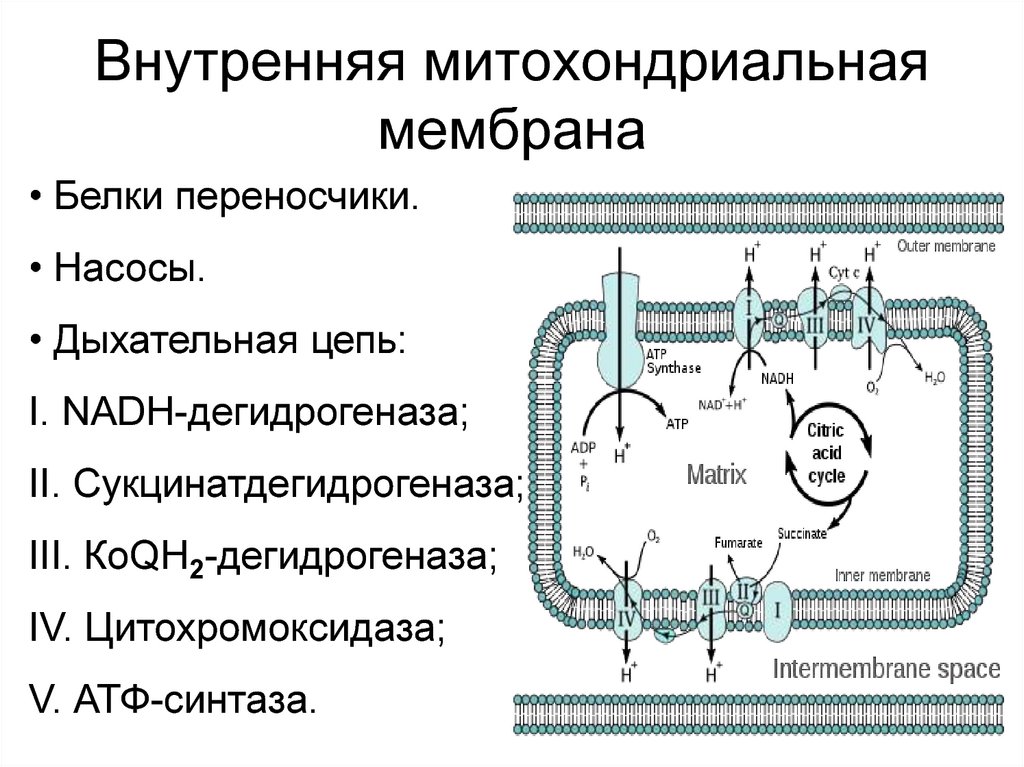 Таким образом, значительное число таких состояний сейчас можно предсказать только гипотетически.
Таким образом, значительное число таких состояний сейчас можно предсказать только гипотетически.
Интенсивное изучение признаков болезней клеточной энергетики приводит к еще более важному выводу: распространенность состояний, связанных с митохондриальной недостаточностью, не ограничивается наследственными синдромами, вызываемыми мутациями генов, непосредственно ответственных за митохондриальные белки. Умеренные нарушения клеточной энергетики могут не проявляться в виде самостоятельного заболевания, однако сказываются на характере течения других болезней. Широчайший круг других заболеваний включает в себя те или иные нарушения клеточной энергетики как вторичные звенья патогенеза.
Проведенные недавно в нашем институте исследования группы из 100 детей, поступивших в генетическую клинику с недифференцированными нарушениями физического и нервно-психического развития, показали, что у 49 из них отмечены нарушения клеточного энергообмена. Кроме того, нами выявлено влияние митохондриальной недостаточности на характер послеожогового рубцевания у детей, течение тонзиллитов, некоторых кардиологических, наследственных соединительнотканных, урологических и других заболеваний. Изучение этих патологических состояний и распространение информации о важности анализа энергетических дисфункций тем более актуально, что в настоящее время существуют действенные методы коррекции митохондриальной недостаточности, которые помогают в лечении перечисленных выше, не всегда истинно «митохондриальных» заболеваний.
Изучение этих патологических состояний и распространение информации о важности анализа энергетических дисфункций тем более актуально, что в настоящее время существуют действенные методы коррекции митохондриальной недостаточности, которые помогают в лечении перечисленных выше, не всегда истинно «митохондриальных» заболеваний.
Многие факторы окружающей среды и лекарственные препараты, вероятно, представляют собой существенную причину патологических изменений митохондрий. К этим факторам относится действие алкилирующих агентов (например, нитрозамины из окружающей среды), гидроксильных радикалов, высоких доз ультрафиолетового и ионизирующего излучений, лекарственных препаратов (бриостатин, азидотимидин), других химических агентов (аллоксан, цианиды, моноокись углерода и др.). Причиной митохондриального повреждения может быть и недостаточность некоторых микроэлементов, например селена. Во многих случаях чувствительность митохондриальной ДНК к действию повреждающих факторов окружающей среды в несколько раз выше по сравнению с чувствительностью ядерного генома. В целом область патогенетически целесообразного использования препаратов, воздействующих на митохондрии, включает в себя:
В целом область патогенетически целесообразного использования препаратов, воздействующих на митохондрии, включает в себя:
Лечение:
- митохондриальных болезней;
- «вторичных» (эндогенных и экзогенных) митохондриальных нарушений при других заболеваниях и состояниях.
Профилактика:
- возможных осложнений различных заболеваний у пациентов с энергодефицитным диатезом;
- преждевременных патологических нарушений, связанных с пожилым возрастом.
- Реабилитационные мероприятия при различных хронических заболеваниях.
Кроме того, целесообразно применение энерготропных препаратов в качестве стимуляторов адаптационных процессов при заболеваниях, не несущих митохондриальной дисфункции в качестве патогенетической составляющей. Эта область наименее изучена, однако, по нашим данным, повышенная митохондриальная пролиферация может обладать важным адаптационным потенциалом, компенсирующим функциональный дефект при некоторых заболеваниях (например, при врожденных структурных миопатиях).
Общая характеристика энерготропных препаратов
Потенциальные возможности лечения митохондриальных болезней распределяются по трем основным направлениям [7]:
- Применение фармакологических препаратов и биологически активных добавок.
- Модификация макронутриентной поддержки, диетотерапия.
- Использование реабилитационных методов лечебной физкультуры.
Терапевтические подходы к лечению митохондриальных болезней подразделяются на семь категорий [8]:
- паллиативная терапия;
- удаление вредных метаболитов;
- применение искусственных акцепторов электронов;
- применение метаболитов и кофакторов;
- применение поглотителей кислородных радикалов;
- генная терапия;
- генетическое консультирование.
Большая группа лекарственных препаратов, которые принято называть метаболическими, пользуется чрезвычайной популярностью у широкого круга врачей. Можно без преувеличения сказать, что лекарства и нелекарственные средства, в разных количествах и соотношениях содержащие аминокислоты и пептиды, витамины и витаминоподобные вещества, коферменты и микроэлементы, применяются во всех областях медицины и по любому поводу. Такая популярность, очевидно, может объясняться как их эффективностью при лечении разнообразных патологических состояний, так и относительной безвредностью. Это сочетание факторов приводит к тому, что врачу легче назначить тот или иной препарат «на всякий случай», чем разбираться в целесообразности такого назначения. В результате из-за бездумного применения, из-за отсутствия методологической базы страдает эффективность лечения, что, в свою очередь, часто порождает сомнение в его принципиальной результативности. Все это диктует необходимость создания рациональной концепции применения лекарственных средств, относимых к метаболическим [9].
Можно без преувеличения сказать, что лекарства и нелекарственные средства, в разных количествах и соотношениях содержащие аминокислоты и пептиды, витамины и витаминоподобные вещества, коферменты и микроэлементы, применяются во всех областях медицины и по любому поводу. Такая популярность, очевидно, может объясняться как их эффективностью при лечении разнообразных патологических состояний, так и относительной безвредностью. Это сочетание факторов приводит к тому, что врачу легче назначить тот или иной препарат «на всякий случай», чем разбираться в целесообразности такого назначения. В результате из-за бездумного применения, из-за отсутствия методологической базы страдает эффективность лечения, что, в свою очередь, часто порождает сомнение в его принципиальной результативности. Все это диктует необходимость создания рациональной концепции применения лекарственных средств, относимых к метаболическим [9].
Важная группа таких препаратов представлена так называемыми энерготропными средствами, то есть средствами, усиливающими интенсивность обмена энергии на клеточном уровне. Наибольшее значение в контексте настоящей статьи имеют препараты (в таблице представлены некоторые из них), воздействующие на процессы, происходящие в универсальных клеточных органеллах – митохондриях. Митохондрии выполняют много функций, однако их основная задача – образование молекул аденозинтрифосфата (АТФ) в биохимических циклах клеточного дыхания. Накопленная энергия в последующем используется в других участках клетки.
Наибольшее значение в контексте настоящей статьи имеют препараты (в таблице представлены некоторые из них), воздействующие на процессы, происходящие в универсальных клеточных органеллах – митохондриях. Митохондрии выполняют много функций, однако их основная задача – образование молекул аденозинтрифосфата (АТФ) в биохимических циклах клеточного дыхания. Накопленная энергия в последующем используется в других участках клетки.
Нарушения функций митохондрий относятся к важнейшим (часто ранним) этапам повреждения клеток. Эти нарушения ведут к недостаточности энергообеспечения клеток, к нарушению многих других важных обменных процессов, к дальнейшему развитию клеточного повреждения, вплоть до гибели клетки. Для клинициста оценка степени митохондриальной дисфункции имеет существенное значение как для формирования представлений о сути и степени происходящих на тканевом уровне процессов, так и для разработки плана терапевтической коррекции патологического состояния. Степень выраженности патологического процесса в том или ином органе связана со степенью зависимости его тканевых элементов от эффективности аэробного окисления.
Несмотря на то что в основе митохондриальных заболеваний могут быть сотни первичных биохимических дефектов, основные изученные звенья патогенеза, на которых и основаны современные подходы к коррекции митохондриальной недостаточности, связаны с нарушением реакций окисления пирувата до ацетил-КоА с помощью пируватдегидрогеназного комплекса; окисления ацетил-КоА до углекислого газа и образования восстановленных носителей электронов NADH и FADh3; реокисления восстановленного коэнзима Q ферментами электронно-транспортной цепи внутренней митохондриальной мембраны; транспорта свободных жирных кислот через мембрану митохондрии в виде эфиров карнитина; окислительного дезаминирования аминокислот с последующим поступлением их углеродного скелета в цикл Кребса; перекисного окисления и образования свободных радикалов.
Оценка достоверной эффективности энерготропных препаратов при митохондриальных болезнях сложна по многим причинам [7]. Вариабельность комплексных фенотипов затрудняет сравнение даже двух отдельно взятых больных с одним и тем же заболеванием. Поражение различных органов усложняет сравнительную оценку эффективности результата в целом. Большой проблемой является отсутствие четких критериев оценки динамики заболевания, наиболее выраженные признаки которого – это такие спорадические события, как инсультоподобные эпизоды или судороги.
Поражение различных органов усложняет сравнительную оценку эффективности результата в целом. Большой проблемой является отсутствие четких критериев оценки динамики заболевания, наиболее выраженные признаки которого – это такие спорадические события, как инсультоподобные эпизоды или судороги.
Все это во многом объясняет тот факт, что, проанализировав в огромной работе 1335 источников о лечении митохондриальных болезней, Джералд Пфеффер (G. Pfeffer) и соавт. [7] смогли отобрать только 12 исследований, строго соответствующих критериям рандомизированного клинического исследования, причем в большинстве случаев они касались воздействия на нервно-мышечные проявления митохондриальных заболеваний с возможностью долговременной оценки таких признаков, как мышечная сила.
Проблема выбора дозы энерготропных препаратов
Сложность проблемы определяется, в частности, двумя факторами: во-первых, бытующим требовательным ожиданием заместительного эффекта при терапии митохондриальных болезней, а во-вторых, недоверием многих клинических биохимиков и фармакологов к возможности легкого введения тех или иных органических молекул внутрь митохондрии.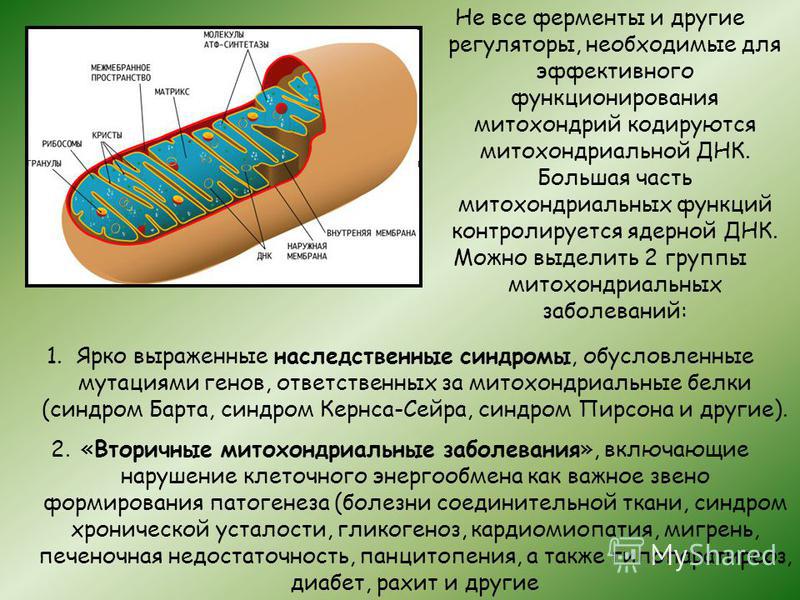 Исходя исключительно из подобных теоретических соображений, ставятся, например, под сомнение как обоснованность применения янтарной кислоты, одного из ключевых метаболитов митохондрий, так и достоверность наблюдаемых позитивных эффектов этого препарата. Однако недавними исследованиями М.Н. Кондрашовой и сотрудников ее школы показано, что терапевтический эффект янтарной кислоты основан не на заместительном принципе, а на сигнальном. Таким образом, чтобы получить эффект, совершенно не нужно заполнять все митохондрии во всех клетках организма янтарной кислотой путем искусственного введения в больших количествах, достаточно назначить микродозы (5–10 мг/кг/сут). В нашей работе, используя новые диагностические приемы с применением транскутанного мониторирования рО2 и рСО2, мы выявили наличие подобного эффекта у L-карнитина. Вполне вероятно, что подобный же принцип может быть применен и к другим лекарственным веществам, используемым в терапии полисистемных нарушений цитоэнергетики.
Исходя исключительно из подобных теоретических соображений, ставятся, например, под сомнение как обоснованность применения янтарной кислоты, одного из ключевых метаболитов митохондрий, так и достоверность наблюдаемых позитивных эффектов этого препарата. Однако недавними исследованиями М.Н. Кондрашовой и сотрудников ее школы показано, что терапевтический эффект янтарной кислоты основан не на заместительном принципе, а на сигнальном. Таким образом, чтобы получить эффект, совершенно не нужно заполнять все митохондрии во всех клетках организма янтарной кислотой путем искусственного введения в больших количествах, достаточно назначить микродозы (5–10 мг/кг/сут). В нашей работе, используя новые диагностические приемы с применением транскутанного мониторирования рО2 и рСО2, мы выявили наличие подобного эффекта у L-карнитина. Вполне вероятно, что подобный же принцип может быть применен и к другим лекарственным веществам, используемым в терапии полисистемных нарушений цитоэнергетики.
Кроме того, в настоящий момент недоверие к возможности введения тех или иных молекул в митохондрию значительно поколеблено благодаря открытию большого и сложного комплекса транспортных систем, обслуживающих эти органеллы [10]. Нельзя не упомянуть о работах, показывающих эффективность применения энерготропных препаратов в достаточно высоких дозах. Так, в работе Р. Боулса [11] описана эффективность применения больших доз коэнзима Q10 (10 мг/кг/сут, но не более 200 мг в сутки) и L-карнитина (100 мг/кг/сут, но не более 2 г в сутки) в лечении синдрома циклической рвоты и других состояний, предположительно связанных с митохондриальными дисфункциями, – мигренозной головной боли, миалгии и синдрома множественных локальных болей.
Нельзя не упомянуть о работах, показывающих эффективность применения энерготропных препаратов в достаточно высоких дозах. Так, в работе Р. Боулса [11] описана эффективность применения больших доз коэнзима Q10 (10 мг/кг/сут, но не более 200 мг в сутки) и L-карнитина (100 мг/кг/сут, но не более 2 г в сутки) в лечении синдрома циклической рвоты и других состояний, предположительно связанных с митохондриальными дисфункциями, – мигренозной головной боли, миалгии и синдрома множественных локальных болей.
В настоящее время нет единого понимания, какая длительность курса может быть оптимальной при энерготропной терапии. Естественно, во многих случаях (например, при лечении хронических заболеваний) необходимо достаточно длительное лечение, особенно если принимать во внимание вероятность заместительного механизма действия. Однако, исходя из практического опыта многих клиницистов и с учетом рекомендаций патофизиологов, длительное постоянное применение энерготропных препаратов (во всяком случае некоторых) не нужно. Целесообразнее применять схемы с периодическими назначением (1–3 месяца) и отменой (примерно на такой же или несколько больший период). Таким образом, совершенно актуально использование как высокодозовых и длительных, так и низкодозовых кратковременных схем применения энерготропных препаратов. Поскольку выявление сигнальных и заместительных составляющих эффекта для большинства энерготропных препаратов – дело будущего, выбор схемы применения до сих пор зависит от искусства врача.
Целесообразнее применять схемы с периодическими назначением (1–3 месяца) и отменой (примерно на такой же или несколько больший период). Таким образом, совершенно актуально использование как высокодозовых и длительных, так и низкодозовых кратковременных схем применения энерготропных препаратов. Поскольку выявление сигнальных и заместительных составляющих эффекта для большинства энерготропных препаратов – дело будущего, выбор схемы применения до сих пор зависит от искусства врача.
Коэнзим Q10
Коэнзим Q (коэнзим Q10, убихинон, витамин Q10) – небольшая жирорастворимая молекула, непосредственно участвующая в транспорте электронов по дыхательной цепи митохондрий. Она свободно диффундирует в мембранном бислое и помимо электронов передает ферментному комплексу III также и протоны, которые захватывает из водной среды. Убихинону свойственны витаминоподобные функции. Будучи введенным в организм, он оказывает значительный антиоксидантный эффект, повышает продукцию АТФ и стабилизирует состояние кальциевых каналов.
Коэнзим Q – один из наиболее распространенных и эффективных энерготропных препаратов [12, 13]. В суточных дозах 300–1500 мг он эффективен при дефиците убихинона, дефектах второго и третьего ферментных комплексов дыхательной цепи, клинически выражающихся в синдроме MILS (maternally inherited Leigh syndrome), синдромах MERRF, MELAS и Кернса – Сейра. Его высокая клиническая эффективность в лечении атаксии Фридрейха и других нейродегенеративных заболеваний показана в нескольких работах [14].
Эффект высоких доз коэнзима Q10 (600 мг 2 раза в день перорально в течение двух месяцев) у больных с синдромом MELAS, прогрессирующей наружной офтальмоплегией и некоторыми другими формами митохондриальных болезней был изучен в двойном слепом плацебоконтролируемом исследовании [7, 15]. Было показано, что на фоне увеличения концентраций коэнзима Q10 в крови снижался уровень лактата при кратковременной, но не при долгосрочной нагрузке. Достоверных изменений других биохимических показателей отмечено не было.
Так же как и для многих других энерготропных препаратов, примеры эффективного применения коэнзима Q10 часто можно обнаружить в работах, посвященных терапии состояний, связанных с различными вторичными проявлениями тканевой гипоксии. Так, Д.М. Ароновым и соавт. [16] было проведено рандомизированное проспективное исследование коэнзима Q10 (препарат Кудевита®) в лечении пациентов с ишемической болезнью сердца с сердечной недостаточностью II–III функционального класса. Пациенты основной группы принимали препарат в дозе 150 мг/сут: по 2 капсулы (60 мг) утром и 3 капсулы (90 мг) вечером. Одновременно пациенты основной и контрольной групп получали стандартную терапию, показанную при данном заболевании. В процессе исследования не назначали препараты, влияющие на метаболизм миокарда, кардиопротекторы и антиоксиданты (триметазидин, мельдоний, оксиметилэтилпиридина сукцинат, инозин, аденозинтрифосфат, кокарбоксилаза, витаминные и иные метаболические средства). Длительность наблюдения составила 3 месяца.
В результате было показано, что лечение больных хронической сердечной недостаточностью на фоне ишемической болезни сердца и перенесенного инфаркта миокарда, находящихся на поликлиническом наблюдении, оказало за относительно небольшой отрезок времени существенное влияние на состояние сердечно-сосудистой системы. При этом препарат способствовал снижению диастолического артериального давления, достоверному улучшению физической работоспособности, сократительной функции сердца и гемодинамики по данным ультразвукового исследования (УЗИ), улучшению картины электрокардиограммы (ЭКГ), указывающей на положительные сдвиги в метаболизме миокарда, липидного профиля плазмы крови. Клинически отмечалось уменьшение количества и выраженности приступов боли в груди; уменьшалась частота приема нитроглицерина.
Препараты, содержащие коэнзим Q10, хорошо знакомы врачам разных специальностей, но до недавнего времени они не могли широко применяться в лечебной практике, так как были представлены в России в виде БАД. Кудевита® в настоящее время является единственным зарегистрированным в России безрецептурным лекарственным препаратом с активным действующим веществом убидекаренон (коэнзим Q10) и, несомненно, поможет более успешно лечить различные заболевания у детей.
Кудевита® в настоящее время является единственным зарегистрированным в России безрецептурным лекарственным препаратом с активным действующим веществом убидекаренон (коэнзим Q10) и, несомненно, поможет более успешно лечить различные заболевания у детей.
L-карнитин
Карнитин – низкомолекулярное соединение, производное аминомасляной кислоты. В тканях млекопитающих присутствует только L-стереоизомер (левокарнитин), именно он биологически эффективен. Карнитин принимает непосредственное участие в катаболизме липидов, обеспечивая перенос длинноцепочечных жирных кислот в виде сложных эфиров (ацилкарнитинов) из цитоплазмы через наружную и внутреннюю митохондриальные мембраны в матрикс митохондрий. Внутри митохондрий транспортированные жирные кислоты подвергаются бета-окислению с образованием ацетил-КоА, который служит субстратом для цикла трикарбоновых кислот Кребса и последующего синтеза АТФ в организме. Наряду с этим окисление жирных кислот – главный путь кетогенеза, а кетоновые тела являются дополнительным энергетическим источником для периферических тканей и головного мозга.
Влияние карнитина на жировой обмен осуществляется также его участием в цитоплазматическом синтезе жирных кислот путем обратного переноса необходимых для этого ацетильных групп митохондриального ацетил-КоА через митохондриальную мембрану в цитоплазму. Помимо перечисленного, карнитин регулирует отношение «ацил-КоА/свободный КоА» в митохондриях. Связывая ацильный радикал, он высвобождает КоА и тем самым активирует интенсивность энергетического метаболизма в тканях. Исключительное значение карнитина становится очевидным в условиях высокого расходования энергетических ресурсов – при заболеваниях, усиленных физических или эмоциональных нагрузках, а также при недостаточном питании. После истощения запасов углеводов липиды становятся главным источником синтеза АТФ в организме.
Другая важная функция карнитина заключается в его способности образовывать соединения с различными органическими кислотами, являющимися промежуточными продуктами окислительных процессов. Данные вещества, накапливаясь в митохондриях и цитоплазме клеток, оказывают мембранотоксическое действие и ингибируют активность ряда ферментов. Выведение этих токсичных органических соединений из организма происходит через почки в виде ацилкарнитинов.
Выведение этих токсичных органических соединений из организма происходит через почки в виде ацилкарнитинов.
Левокарнитин высокоэффективен при лечении как первичных форм дефицита карнитина, так и широкого круга заболеваний, связанных со вторичным снижением его содержания в организме. Кроме того, занимая уникальное положение относительно митохондрии и стимулируя приток в нее энергосубстратов, карнитин является универсальным стимулятором тканевого энергообмена, что актуально не только в отношении компенсации энергодефицита, но и в отношении компенсаторной адаптации практически к любым структурно-функциональным дефектам. Данные об эффективности применения препаратов L-карнитина у больных митохондриальными заболеваниями достаточно многочисленны [13, 17], хотя чаще описывают их применение в комплексе с другими энерготропными средствами (см. ниже).
Отдельно следует упомянуть о важности применения L-карнитина при формах его наследственной недостаточности. В качестве примера упомянем работу Е. А. Николаевой и соавт. [18], в которой была показана эффективность применения препарата Элькар® в дозе 800 мг/сут с двухлетнего возраста у больного с первичным системным дефицитом карнитина. Динамическое наблюдение в течение 2 лет показало выраженное улучшение самочувствия и состояния мальчика на фоне терапии Элькаром. Ребенок и его родители не предъявляли жалоб, связанных с лечением препаратом, физическое развитие в возрасте 4 лет было средним (вырос на 19 см), мышечный тонус физиологическим. В результате лечения отмечены положительные изменения со стороны сердца, улучшились биохимические показатели крови.
А. Николаевой и соавт. [18], в которой была показана эффективность применения препарата Элькар® в дозе 800 мг/сут с двухлетнего возраста у больного с первичным системным дефицитом карнитина. Динамическое наблюдение в течение 2 лет показало выраженное улучшение самочувствия и состояния мальчика на фоне терапии Элькаром. Ребенок и его родители не предъявляли жалоб, связанных с лечением препаратом, физическое развитие в возрасте 4 лет было средним (вырос на 19 см), мышечный тонус физиологическим. В результате лечения отмечены положительные изменения со стороны сердца, улучшились биохимические показатели крови.
Креатин
Моногидрат креатина представляет собой дополнительный источник энергии. В отличие от нестабильных форм – чистого креатина и фосфата креатина, – моногидрат креатина прекрасно всасывается и с успехом применяется в спортивной медицине. Отмечена его эффективность в лечении различных митохондриальных болезней: синдромов Лея, Кернса – Сейра, MELAS и др. [14, 19–21]. Однако существуют и противоположные данные, не подтверждающие его эффективность при митохондриальных болезнях [12].
Однако существуют и противоположные данные, не подтверждающие его эффективность при митохондриальных болезнях [12].
В рандомизированном плацебоконтролируемом исследовании [7, 22, 23] эффективности моногидрата креатина, применяемого в течение трех недель (4–10 г в сутки) у больных синдромом MELAS и митохондриальной миопатией, отмечено достоверное увеличение мышечной силы и снижение уровня лактата после нагрузки. В двойных слепых плацебоконтролируемых исследованиях у больных с прогрессирующей наружной офтальмоплегией и митохондриальной миопатией [24] (20 г в сутки в течение месяца) и у больных с хронической прогрессирующей наружной офтальмоплегией и с синдромом Кернса – Сейра [25] (150 мг/кг в течение 6 недель) клиническая эффективность моногидрата креатина не выявлена.
Дихлорацетат
Дихлорацетат – активатор пируватдегидрогеназы – уже значительное время активно изучается в качестве возможного средства исправления митохондриальных функций [12]. В ряде работ показана его эффективность при лечении синдрома MELAS [26, 27], дефицита пируватдегидрогеназного комплекса [28], а также при исправлении митохондриальных функций в опухолевых клетках, ведущем к позитивному эффекту при лечении рака. Некоторые исследователи столь высоко оценивают его лечебный потенциал, что назначают этот препарат несмотря на то, что применение дихлорацетата (в частности в суточных дозах 25 мг/кг) может вызывать развитие периферических полиневропатий [29].
Некоторые исследователи столь высоко оценивают его лечебный потенциал, что назначают этот препарат несмотря на то, что применение дихлорацетата (в частности в суточных дозах 25 мг/кг) может вызывать развитие периферических полиневропатий [29].
В двойном слепом плацебоконтролируемом исследовании эффективности дихлорацетата у больных с различными митохондриальными заболеваниями [7, 30] (50 мг/кг в сутки в течение недели двумя курсами с интервалом три месяца) было отмечено значительное снижение концентраций лактата, пирувата и аланина в крови (в покое и после нагрузки), а в мозге – значительное снижение соотношения «лактат/креатин» и повышение соотношений «холин/креатин» и «ацетиласпартат/креатин». В других подобных работах [28, 31, 32] была также отмечена нормализация уровня лактата (а в первых двух из этих работ – и пирувата) после приема дихлорацетата.
Янтарная кислота
Сукцинат – один из эффективных медиаторов транспорта электронов, успешно использующийся при острых нарушениях тканевого дыхания. В отношении хронических расстройств целесообразность его применения спорна, однако в научной литературе приводятся описания эффективности сукцината при недостаточности I дыхательного комплекса [33] и при синдроме MELAS (длительная монотерапия суточной дозой 6 г) [34].
В отношении хронических расстройств целесообразность его применения спорна, однако в научной литературе приводятся описания эффективности сукцината при недостаточности I дыхательного комплекса [33] и при синдроме MELAS (длительная монотерапия суточной дозой 6 г) [34].
Фолиевая кислота
Фолиевая кислота – водорастворимый витамин (В9), необходимый в первую очередь при активной репликации ДНК, то есть делении клеток. Однако описан выраженный положительный эффект этого витамина в суточной дозе 1–2,5 мг/кг при синдроме Кернса – Сейра [33].
L-аргинин
L-аргинин – незаменимая для детей аминокислота, снабжающая азотом систему NO-синтаз. В настоящее время растет число указаний [12] на эффективность применения L-аргинина при синдроме MELAS, в частности, в отношении терапии инсультоподобных эпизодов и сердечно-сосудистых нарушений. Так, например, с использованием позитронно-эмиссионной томографии показано, что применение L-аргинина эффективно при лечении кардиомиопатии при синдроме MELAS [35].
Другие вещества
Наряду с вышеперечисленными, к веществам, несомненно позитивно влияющим на клеточный энергообмен, относят витамин Е (альфа-токоферол), витамин С (аскорбиновая кислота), липоевую кислоту, глутатион, рибофлавин, тиамин и др. Однако в литературе, посвященной митохондриальным болезням, пока не находится четких доказательств их эффективности (по крайней мере, в моноварианте), хотя эти вещества часто используются в комплексных схемах энерготропной терапии.
В настоящее время в различных, в первую очередь экспериментальных, работах активно исследуются новые вещества, представляющие собой потенциально перспективные препараты для лечения митохондриальных заболеваний – антиоксиданты в соединении с трифенилфосфониевым катионом (митохинон, MitoVitE, MitoTEMPOL, MitoPBN, смесь Скулачева), тролокс, SS-пептиды (Szeto-Schiller peptides) [14, 36, 37], ресвератрол [38], препараты, влияющие на сборку дыхательных комплексов [39], оптимизирующие обмен кальция [40], активаторы митохондриального биогенеза [41] и др.
Комплексная энерготропная терапия
Спектр потенциальных патологических нарушений клеточного энергообмена чрезвычайно велик (повреждения различных звеньев цикла Кребса, дыхательной цепи, бета-окисления и др.). Хотя перечень энерготропных препаратов также достаточно широк, далеко не всегда имеется возможность выявить конкретное точечное повреждение митохондрий и точно подобрать подходящий лекарственный препарат. В связи с этим наиболее эффективными в широкой клинической практике могут быть комплексы энерготропных препаратов, обладающих способностью воздействовать сразу на несколько ключевых этапов клеточного энергообмена. При этом на первое место по значимости выдвигаются такие препараты, как L-карнитин, коэнзим Q10, цитохром С и их комплексы с другими вышеперечисленными лекарственными средствами [42–44]. Схемы лекарственной коррекции цитоэнергетической недостаточности у детей активно разрабатываются в настоящее время в Московском НИИ педиатрии и детской хирургии и в Российском национальном исследовательском медицинском университете им. Н.И. Пирогова.
Н.И. Пирогова.
Так, данные Е.А. Николаевой свидетельствуют о том, что при митохондриальных энцефаломиопатиях комплексная энерготропная терапия позволяет добиться существенного клинического эффекта во всех сферах проявления патологического процесса. Результатом лечения является нарастание массы тела, уменьшение выраженности сердечно-сосудистых нарушений, снижение частоты приступов рвоты, судорог, уменьшение выраженности проявлений энцефалопатии и миопатии, снижение утомляемости. Некоторые примеры свидетельствуют о том, что эффективность правильно подобранной энерготропной терапии даже при тяжелых «первичных» митохондриальных синдромах может быть поразительной. В качестве одного из примеров можно привести историю болезни ребенка с синдромом Барта – одним из таких синдромов, клиническая картина которого характеризуется задержкой роста и психомоторного развития, миопатией, кардиомиопатией, нарушениями со стороны крови. Многолетнее лечение комплексом препаратов, включавшим в себя коэнзим Q10, цитохром С, L-карнитин (Элькар) и некоторые другие, привело к тому, что в подростковом возрасте главной проблемой этого мальчика с тяжелым наследственным заболеванием стали попытки избежать постановки на воинский учет.
В двойном слепом плацебоконтролируемом исследовании [7, 14, 45] у больных с такими митохондриальными заболеваниями, как синдром Кернса – Сейра, синдром MELAS, хроническая наружная офтальмоплегия, оптическая нейропатия Лебера, митохондриальная нейрогастроинтестинальная энцефаломиопатия, а также с митохондриальными заболеваниями с редкими точковыми мутациями была проведена оценка двухмесячного комплексного применения креатина, коэнзима Q10 и липоевой кислоты. В этой работе выявлено статистически достоверное снижение уровней лактата в плазме крови и 8-изопростана – в моче. У больных с синдромом MELAS отмечено также нарастание массы тела (не за счет жировой ткани). Есть указания [46] на то, что в лечении митохондриальных болезней (как психических, так и соматических нарушений) могут быть эффективны комплексы, содержащие коэнзим Q10 (200–400 мг/сут) и рибофлавин (100–400 мг/сут), в некоторых случаях с добавлением витамина С (1000 мг/сут), витамина Е (400 МЕ/сут), карнитина (2000 мг/сут), креатина (5000 мг/сут) и магнезии (250–500 мг/сут).
При заболеваниях, включающих в свой симптомокомплекс «вторичную» митохондриальную недостаточность, также можно добиться улучшения качества жизни больных. Приведем весьма «эффектный» пример: у низкорослых детей c различными неэндокринными наследственными заболеваниями на фоне лечения энерготропными препаратами – L-карнитином (Элькар), коэнзимом Q10 и другими – удается достичь значительной стимуляции роста – до 6–7 см в год. При некоторых заболеваниях благодаря энерготропной терапии впервые была продемонстрирована возможность относительного успеха в лечении (например, при лечении синдрома Ретта и туберозного склероза отмечено улучшение когнитивных и эмоциональных функций). Существенный позитивный эффект применения энерготропных препаратов наблюдался и в ряде других отделений нашего института: урологическом (при комплексном лечении гидронефроза и гиперактивного мочевого пузыря), ожоговом центре (при реабилитации детей после ожогов), кардиологии (при лечении кардиомиопатий, миокардиодистрофии и нарушений сердечного ритма), пульмонологии (при лечении ряда хронических заболеваний легких) и др.
Применение средств метаболической коррекции позволило оказать существенное влияние на состояние здоровья детей дошкольного возраста с различными вариантами нарушения речевого развития (общее недоразвитие речи, дислалия, задержка психоречевого развития), у детей с соединительнотканной дисплазией и в группе так называемых часто болеющих детей. Эти работы выполнялись нами совместно со специалистами Российского государственного медицинского университета им. Н.И. Пирогова (группа С.О. Ключникова). В лечении этих групп детей были применены комплексы, включающие коэнзим Q10, L-карнитин (Элькар), ряд других энерготропных препаратов. Указанное лечение дети получали, как правило, длительно, в течение 2–3 месяцев, после чего они проходили повторное обследование, позволившее выявить существенную положительную динамику в состоянии здоровья. Отмечались минимизация предъявляемых жалоб, улучшение сна и аппетита, исчезновение или снижение выраженности ряда клинических признаков заболеваний, нормализация лабораторных показателей; возрастала выносливость в отношении физических и интеллектуальных нагрузок.
Заключение
Все вышесказанное свидетельствует о необходимости научно-прикладных разработок, направленных на создание современных принципов энерготропного лечения (по отработке состава энерготропных комплексов, тщательному подбору доз активных веществ, определению оптимальных схем назначения, в том числе с учетом хронобиологических ритмов). Приведенные выше примеры свидетельствуют о необходимости именно комплексного использования таких средств. Однако при каждой нозологической форме должны разрабатываться свои специализированные комплексы, включающие патогенетически наиболее значимые компоненты клеточного энергообмена (например, коэнзим Q10, L-карнитин, цитохром С, янтарная кислота и др.).
Кудевита® – безрецептурный лекарственный препарат коэнзима Q10
Учитывая высокую потребность в безопасных и высокоэффективных препаратах при лечении различных заболеваний у детей, компания ПИК-ФАРМА, производитель известных лекарственных препаратов Элькар® и Пантогам®, в апреле 2012 г. выпустила новый лекарственный препарат на основе коэнзима Q10 – Кудевита® (МНН: убидекаренон) капсулы 30 мг № 60.
выпустила новый лекарственный препарат на основе коэнзима Q10 – Кудевита® (МНН: убидекаренон) капсулы 30 мг № 60.
Лекарственный препарат Кудевита® рекомендуется для профилактики и устранения недостаточности коэнзима Q10, улучшения адаптации к повышенным физическим нагрузкам; для профилактики и в составе комплексной терапии сердечно-сосудистых заболеваний.
В составе комплексной терапии Кудевита® назначается детям старше 12 лет в дозировке 30–90 мг (1–3 капсулы) в сутки после еды, с целью профилактики – по 30 мг (1 капсула) в сутки.
Препарат имеется в наличии в аптеках, отпускается без рецепта.
У низкорослых детей c различными неэндокринными наследственными заболеваниями на фоне лечения энерготропными препаратами – L-карнитином (Элькар), коэнзимом Q10 и другими – удается достичь значительной стимуляции роста – до 6–7 см в год.
Митохондриальная энцефаломиопатия, обусловленная недостаточностью пируватдегидрогеназного комплекса
Сотрудниками Российского национального исследовательского медицинского университета им. Н.И. Пирогова и Казанского государственного медицинского университета проведен анализ полиморфизма клинических проявлений прогрессирующей митохондриальной энцефаломиопатии, обусловленной патогенными вариантами ядерного Х-сцепленного гена PDHA1 (кодирует альфа-субъединицу пируватдегидрогеназы).
Н.И. Пирогова и Казанского государственного медицинского университета проведен анализ полиморфизма клинических проявлений прогрессирующей митохондриальной энцефаломиопатии, обусловленной патогенными вариантами ядерного Х-сцепленного гена PDHA1 (кодирует альфа-субъединицу пируватдегидрогеназы).
Митохондриальные заболевания — обширная гетерогенная группа наследственных болезней. Тяжесть течения, инвалидизация и высокая смертность пациентов определяют необходимость поиска средств ранней диагностики и лечения. Несмотря на достижения медицинской генетики за последние годы и интенсивное внедрение результатов исследований в практику, диагностика митохондриальных заболеваний представляет для педиатров значительные трудности. В частности, клинические проявления этих заболеваний чрезвычайно разнообразны и включают большое число симптомокомплексов или клинических фенотипов, многие из которых характеризуются неспецифической симптоматикой, обусловленной вовлечением ЦНС и мышечной системы (энцефаломиопатия). Одной из причин митохондриальной патологии являются дефекты мультиферментного пируватдегидрогеназного комплекса (ПДК), распространенность которых в детской популяции остается неуточненной.
Одной из причин митохондриальной патологии являются дефекты мультиферментного пируватдегидрогеназного комплекса (ПДК), распространенность которых в детской популяции остается неуточненной.
ПДК функционирует в митохондриальном матриксе и играет центральную роль в процессах клеточной биоэнергетики — обеспечивает окислительное декарбоксилирование пирувата, что ведет к образованию ацетил-КоА — важного субстрата для цикла Кребса. Таким путем осуществляется интеграция продуктов гликолиза в энергетический метаболизм клетки. ПДК состоит из трех ферментов (E1, E2 и E3), коферментов (тиаминдифосфат, липоевая кислота и другие) и регуляторных белков. Комплекс функционирует под контролем по крайней мере 6 генов ядерной ДНК. Фермент E1 (пируватдегидрогеназа) — тетрамер, включающий по две альфа- и бета-субъединицы. Альфа-субъединицы пируватдегидрогеназы представляют собой центральную структуру ПДК. Кодирует альфа-субъединицы ген PDHA1, расположенный на коротком плече хромосомы Х, в регионе Xp22. 12. Изменения этого гена являются самой частой (около 60% случаев) причиной снижения активности ПДК. К настоящему времени известно не менее 100 патогенных вариантов гена PDHA1, наследуемых доминантно, сцепленно с хромосомой Х, с неполной пенетрантностью у женщин. У лиц мужского пола, как правило, регистрируют миссенс-мутации, возникшие de novo, у женщин чаще встречаются изменения в гене со сдвигом рамки считывания. Недостаточность ПДК ведет к нарушению утилизации углеводов как основных субстратов энергетического обмена, накоплению пирувата и лактата, уменьшению активности цикла Кребса. Указанные процессы приводят к снижению интенсивности продукции редуцирующих эквивалентов (NADH, FADh3), нарушению функционирования митохондриальной электронно-транспортной цепи и окислительного фосфорилирования.
12. Изменения этого гена являются самой частой (около 60% случаев) причиной снижения активности ПДК. К настоящему времени известно не менее 100 патогенных вариантов гена PDHA1, наследуемых доминантно, сцепленно с хромосомой Х, с неполной пенетрантностью у женщин. У лиц мужского пола, как правило, регистрируют миссенс-мутации, возникшие de novo, у женщин чаще встречаются изменения в гене со сдвигом рамки считывания. Недостаточность ПДК ведет к нарушению утилизации углеводов как основных субстратов энергетического обмена, накоплению пирувата и лактата, уменьшению активности цикла Кребса. Указанные процессы приводят к снижению интенсивности продукции редуцирующих эквивалентов (NADH, FADh3), нарушению функционирования митохондриальной электронно-транспортной цепи и окислительного фосфорилирования.
Первые сообщения о пациентах с дефицитом ПДК появились 50 лет назад. Клиническая картина варьирует по степени тяжести и возрасту манифестации болезни от тяжелого, летального неонатального/младенческого лактатацидоза до поздно манифестирующей интермиттирующей атаксии. Клинические проявления включают в себя нарушение психомоторного развития, мышечную гипотонию, вялость/летаргию, судороги, дистонические кризы, атаксию, микроцефалию, лицевой дизморфизм. Отмечено сходство фациального фенотипа с лицами детей при фетальном алкогольном синдроме. Реже наблюдаются мышечный гипертонус, спастичность, периферическая нейропатия, полирадикулонейропатия по типу синдрома Guillain–Barré, нистагм, страбизм, птоз век, хореоатетоз. В ряде случаев заболевание имеет пренатальные проявления: нарушение течения беременности у матерей (преэклампсия, олигогидрамнион, гестационный сахарный диабет), синдром задержки внутриутробного развития плода, вентрикуломегалия по данным пренатальной ультрасонографии. При биохимическом исследовании крови у большинства пациентов регистрируют лактат- и пируват-ацидоз, может быть повышена концентрация аланина в крови. У большей части больных на МРТ головного мозга выявляют структурные нарушения — кортикальную атрофию, вентрикуломегалию, изменение сигнала в области базальных ганглиев (Ли-подобный синдром), агенезию/гипоплазию мозолистого тела.
Клинические проявления включают в себя нарушение психомоторного развития, мышечную гипотонию, вялость/летаргию, судороги, дистонические кризы, атаксию, микроцефалию, лицевой дизморфизм. Отмечено сходство фациального фенотипа с лицами детей при фетальном алкогольном синдроме. Реже наблюдаются мышечный гипертонус, спастичность, периферическая нейропатия, полирадикулонейропатия по типу синдрома Guillain–Barré, нистагм, страбизм, птоз век, хореоатетоз. В ряде случаев заболевание имеет пренатальные проявления: нарушение течения беременности у матерей (преэклампсия, олигогидрамнион, гестационный сахарный диабет), синдром задержки внутриутробного развития плода, вентрикуломегалия по данным пренатальной ультрасонографии. При биохимическом исследовании крови у большинства пациентов регистрируют лактат- и пируват-ацидоз, может быть повышена концентрация аланина в крови. У большей части больных на МРТ головного мозга выявляют структурные нарушения — кортикальную атрофию, вентрикуломегалию, изменение сигнала в области базальных ганглиев (Ли-подобный синдром), агенезию/гипоплазию мозолистого тела.
Важность установления митохондриальной энцефаломиопатии, вызванной дефицитом ПДК, обусловлена возможностью проведения специализированной терапии. В частности, в ряде случаев отмечен положительный эффект применения высоких доз тиамина и кетогенной диеты. Вместе с тем диагностика заболевания может вызывать значительные трудности, в т. ч. и по причине отсутствия описания таких больных в российских медицинских журналах. В связи с этим был изучен полиморфизм клинических проявлений прогрессирующей митохондриальной энцефаломиопатии, обусловленной мутацией ядерного гена PDHA1. Представленное описание клинических наблюдений нацелено на повышение осведомленности врачей в вопросах диагностики митохондриальной энцефаломиопатии, вызванной дефицитом ПДК, у детей с признаками поражения нервной системы.
О пациентах. При поступлении детей под наше наблюдение родители предъявляли жалобы на задержку психомоторного и речевого развития. Возраст детей и основные клинические данные при обследовании в отделении представлены.
Начальные признаки заболевания в виде задержки развития и мышечной гипотонии у 3 детей были выявлены с рождения (у одного из этих пациентов наблюдали респираторный дистресс-синдром), у 2 детей — в первом полугодии жизни. У 3 мальчиков болезнь дебютировала позже, в возрасте 1,5–3 лет, после перенесенной респираторной вирусной инфекции; обращали на себя внимание нарушение походки, транзиторная дистония и приступы вялости. У 2 детей в числе первых признаков болезни отмечали птоз век, появившийся в возрасте 6 и 18 мес. По данным генеалогического анализа (7 родословных): в 5 родословных больной ребенок единственный; в одной родословной больны 2 сибса, а в другой у пробанда есть клинически здоровая сестра в возрасте 7 лет (генетически не обследована). У 5 из 7 матерей при клиническом осмотре не обнаружено признаков болезни, в т. ч. у матери двух больных сибсов, являющейся носителем патогенного варианта с.662A>G гена PDHA1. У двух женщин отмечены атаксия, нарушение походки, смазанность речи; одна из них — носитель патогенного варианта гена PDHA1, вторая генетически не обследована. Изучение данных перинатального анамнеза показало, что во всех случаях беременность у матерей протекала неблагоприятно — с выраженным токсикозом (7), инфекциями (4), угрозой невынашивания (4), хронической фетоплацентарной недостаточностью (1). В 4 случаях роды произошли на 35–36-й нед беременности, из них в 3 случаях путем экстренного кесарева сечения. Четверо детей родились на сроке 40 нед, из них у 2 зарегистрирована задержка внутриутробного развития по гипопластическому типу.
Изучение данных перинатального анамнеза показало, что во всех случаях беременность у матерей протекала неблагоприятно — с выраженным токсикозом (7), инфекциями (4), угрозой невынашивания (4), хронической фетоплацентарной недостаточностью (1). В 4 случаях роды произошли на 35–36-й нед беременности, из них в 3 случаях путем экстренного кесарева сечения. Четверо детей родились на сроке 40 нед, из них у 2 зарегистрирована задержка внутриутробного развития по гипопластическому типу.
Физикальная диагностика. Согласно результатам обследования в отделении, основу клинического симптомокомплекса составляли задержка психомоторного развития (у всех детей), атаксия (у 5), миопатические проявления (у 7). Дистонические атаки наблюдали у 2 сибсов, деформации скелета — у 4 детей, лицевой дизморфизм — у 1 ребенка.
Результаты МРТ головного мозга. Данные МРТ головного мозга были получены для всех детей: в 1 случае исследование было выполнено в медицинском учреждении по месту жительства за 2 мес до госпитализации, у остальных больных — в стационаре. Выявлены характерные для дефицита ПДК нарушения: очаги изменения МР-сигнала в базальных ядрах — у 6 детей, вентрикуломегалия — у 2.
Выявлены характерные для дефицита ПДК нарушения: очаги изменения МР-сигнала в базальных ядрах — у 6 детей, вентрикуломегалия — у 2.
Лабораторные исследования. Метаболический ацидоз был обнаружен у 6 пациентов и отсутствовал у 2 больных старшего возраста. У всех детей имела место гиперлактатацидемия от 3,0 до 11,8 ммоль/л. В 3 случаях отмечено умеренное повышение активности лактатдегидрогеназы в крови до 451–546 Ед/л. Данные о содержании аланина в крови были известны для 2 больных: у одного концентрация была нормальной, у второго — умеренно повышенной до 1095 мкмоль/л (норма 85–950 мкмоль/л). Органические кислоты в моче были определены у 4 детей. У всех 4 выявлена кетонурия с высокой экскрецией 2-гидроксиизомасляной и 3-гидроксимасляной кислот; повышенная экскреция лактата и пирувата — только у 1 из них. У всех детей диагноз митохондриальной энцефаломиопатии, обусловленной недостаточностью ПДК, был подтвержден результатами секвенирования и выявлением патогенного/вероятно патогенного варианта (согласно рекомендациям) гена PDHA1: миссенс-мутаций —у 6 детей (в т. ч. у сибсов), инсерции c дупликациями, включающими 6 и 16 пар оснований, — у 2.
ч. у сибсов), инсерции c дупликациями, включающими 6 и 16 пар оснований, — у 2.
Терапия. Для облегчения состояния пациентов была использована диетотерапия. В суточном рационе ограничивали содержание углеводов (до 8–10% физиологической нормы), в рацион включали богатые липидами продукты (сливки, сливочное и оливковое масло, жирные сорта рыбы, говядину, свинину, мясные бульоны, орехи, авокадо). Рекомендованное для проведения в амбулаторных условиях медикаментозное лечение предполагало назначение тиамина в дозе до 300 мг/сут, а так-же курсы левокарнитина (50 мг/кг/сут на протяжении 3 мес), коэнзима Q10 (60–90 мг/сут на протяжении 6 мес), цитофлавина (5–10 мл внутривенно № 5–10 2–3 раза в год).
Динамика и исходы.Длительное (более 1,5 лет) наблюдение за 4 детьми (в остальных случаях исходы болезни неизвестны) показало умеренную положительную динамику в виде стабилизации состояния, отсутствия метаболических кризов, снижения частоты эпизодов дистонии. Из них у 2 детей старшего возраста отмечена низкая приверженность диетическим рекомендациям.
Из них у 2 детей старшего возраста отмечена низкая приверженность диетическим рекомендациям.
Анализ клинических данных показал, что ранним предиктором степени тяжести митохондриальной энцефаломиопатии, по-видимому, может быть возраст возникновения первых признаков. Так, в случае дебюта болезни в первые 3 мес жизни выявлялась более тяжелая степень нарушения психоречевого и моторного развития. У этих детей наблюдали симптоматическую эпилепсию (у 1 ребенка), бульбарные симптомы — поперхивание, гиперсаливация, гипомимия (у 2). У больных с более поздней манифестацией заболевания состояние здоровья было расценено как среднетяжелое; отмечены умеренное отставание в психоречевом развитии или легкая интеллектуальная недостаточность (у 2 больных), у 2 больных сибсов интеллект находился в пределах нормы. Тяжесть состояния определялась главным образом наличием атаксии (у 3 детей), дистонических атак (у 2). 1 ребенок страдал сенсоневральной тугоухостью. Значимых различий в биохимических показателях у детей с разными по степени тяжести формами заболевания не обнаружено. Вместе с тем криз метаболической декомпенсации наблюдали у ребенка № 4 с тяжелой формой митохондриальной энцефаломиопатии. Также следует отметить, что выраженность изменений по данным МРТ головного мозга не коррелировала со степенью тяжести болезни у детей с разными сроками дебюта митохондриальной энцефаломиопатии: в подгруппах, отмеченных выше, были дети как с вентрикуломегалией, так и с поражением базальных ганглиев.
Вместе с тем криз метаболической декомпенсации наблюдали у ребенка № 4 с тяжелой формой митохондриальной энцефаломиопатии. Также следует отметить, что выраженность изменений по данным МРТ головного мозга не коррелировала со степенью тяжести болезни у детей с разными сроками дебюта митохондриальной энцефаломиопатии: в подгруппах, отмеченных выше, были дети как с вентрикуломегалией, так и с поражением базальных ганглиев.
Обращает на себя внимание нарушение течения внутриутробного периода развития всех детей, что очевидно указывает на пренатальное влияние дефицита пируватдегидрогеназы. Не исключено, что имеет место негативный фетальный эффект на организм женщины в случае наличия болезни у внутриутробного ребенка. Подобный неблагоприятный эффект характерен, например, для дефицита трифункционального белка (заболевание из группы нарушений митохондриального в-окисления жирных кислот).
Заключение. Дефицит ПДК — тяжелое орфанное заболевание, связанное с нарушением митохондриального биоэнергетического обмена. Постановка диагноза имеет значение для определения тактики лечения, облегчающего состояние детей. В то же время очевидно, что высокоэффективное лечение данного заболевания пока не разработано. Это обстоятельство обусловливает особую значимость медико-генетического консультирования и оказания медико-генетической помощи членам семьи в виде оценки риска рождения больного ребенка и проведения пренатальной диагностики в случае планирования беременности высокого генетического риска.
Постановка диагноза имеет значение для определения тактики лечения, облегчающего состояние детей. В то же время очевидно, что высокоэффективное лечение данного заболевания пока не разработано. Это обстоятельство обусловливает особую значимость медико-генетического консультирования и оказания медико-генетической помощи членам семьи в виде оценки риска рождения больного ребенка и проведения пренатальной диагностики в случае планирования беременности высокого генетического риска.
Источник: Митохондриальная энцефаломиопатия, обусловленная недостаточностью пируватдегидрогеназного комплекса.
Николаева Е.А., Волгина С.Я., Халиуллина Ч.Д., Боченков С.В., Данцева М.А.
Вопросы современной педиатрии 2021 том 20, № 1
Метки: клинический опыт, научные исследования
04.03.2021
Пирсона синдром — причины, признаки и симптомы, диагностика и лечение
Суть болезни
Синдром Пирсона — тяжелое врожденное заболевание, при котором наблюдаются серьезные нарушения кроветворения (прежде всего выработки эритроцитов) и функции поджелудочной железы. Кроме того, нередко у больных встречаются печеночная и почечная недостаточность, а также нарушения работы желез внутренней секреции.
Кроме того, нередко у больных встречаются печеночная и почечная недостаточность, а также нарушения работы желез внутренней секреции.
Синдром Пирсона относится к группе митохондриальных заболеваний. Это означает, что его появление связано с «поломкой» в ДНК — но не в тех молекулах ДНК, которые содержатся в хромосомах в ядре клетки и являются основными носителями наследственной информации, а в тех небольших молекулах ДНК, которые содержатся в митохондриях — особых структурах, являющихся «энергетическими фабриками» клеток.
Частота встречаемости
Синдром Пирсона — очень редкое заболевание. В России диагностированы лишь единичные случаи. В мире на данный момент описано менее 100 случаев синдрома Пирсона.
Синдром Пирсона относится к генетически обусловленным болезням. Однако наследование митохондриальных заболеваний отличается от наследования заболеваний, вызванных «обычными» хромосомными дефектами. Митохондриальная ДНК передается детям только от матери; при этом для проявления болезни необходимо, чтобы число доставшихся ребенку дефектных молекул митохондриальной ДНК было достаточно велико – а это число зависит от множества случайных факторов. Поэтому при синдроме Пирсона генетическое консультирование затруднено. В одной и той же семье могут родиться и клинически здоровые, и больные дети.
Поэтому при синдроме Пирсона генетическое консультирование затруднено. В одной и той же семье могут родиться и клинически здоровые, и больные дети.
Признаки и симптомы
Многие проявления синдрома Пирсона связаны с неспособностью костного мозга больных производить нормальные клетки крови. Так, характерной чертой болезни является сидеробластная анемия. Это значит, что в предшественниках эритроцитов нарушено использование железа для синтеза гемоглобина, и возникают сидеробласты — клетки, где под микроскопом видны гранулы «неиспользованного» железа, расположенные обычно в виде кольца вокруг ядра клетки.
Анемия у таких больных не поддается терапии препаратами железа и витаминами, поэтому бывают необходимы переливания донорских эритроцитов. Нередко наблюдается также низкий уровень тромбоцитов (проявляющийся повышенной склонностью к кровотечениям и образованию синяков) и лейкоцитов (низкая сопротивляемость инфекциям).
Вторая важная черта синдрома Пирсона — недостаточная выработка ферментов поджелудочной железы. В результате пища плохо усваивается, возникает хронический понос. Довольно часто наблюдаются также печеночная недостаточность, проблемы с почками, иногда — нарушения выработки гормонов.
В результате пища плохо усваивается, возникает хронический понос. Довольно часто наблюдаются также печеночная недостаточность, проблемы с почками, иногда — нарушения выработки гормонов.
Первые проявления болезни возникают в раннем возрасте, иногда даже с самого рождения. Дети медленно растут и недостаточно набирают вес, плохо развиваются, страдают от постоянного поноса, у них увеличена печень. Время от времени у них случаются метаболические кризы с эпизодами рвоты, сонливости и т.п. Периодически наблюдаются также тяжелые симптомы, связанные с ацидозом, то есть слишком высокой кислотностью крови; при этом страдают многие системы организма, включая желудочно-кишечный тракт, центральную нервную систему, сердце, мышцы, органы дыхания.
Диагностика
При диагностике синдрома Пирсона принимают во внимание как клинические проявления, так и результаты лабораторных исследований. При исследованиях обнаруживается анемия с присутствием значительного количества кольцевых сидеробластов и определенные изменения в клетках костного мозга. Для изучения состояния поджелудочной железы могут использоваться измерения концентрации ее ферментов в сыворотке крови и другие анализы. Измеряется уровень молочной кислоты в сыворотке крови, так как при синдроме Пирсона ее обмен нарушен. Применяются и другие методы исследования.
Для изучения состояния поджелудочной железы могут использоваться измерения концентрации ее ферментов в сыворотке крови и другие анализы. Измеряется уровень молочной кислоты в сыворотке крови, так как при синдроме Пирсона ее обмен нарушен. Применяются и другие методы исследования.
Разумеется, прямую информацию о наличии синдрома Пирсона можно было бы получить путем генетического анализа митохондриальной ДНК. К сожалению, не всегда этот анализ дает надежные результаты, так как митохондриальная ДНК существует в различных вариантах (это называется гетероплазмией) не только в пределах организма, но даже внутри одной клетки.
Лечение
Специфического лечения синдрома Пирсона не существует. Однако в ряде случаев можно облегчить состояние пациентов и продлить им жизнь.
Из-за анемии больным нужны переливания компонентов крови. Недостаточность поджелудочной железы требует приема панкреатических ферментов. Поскольку у больных нарушен обмен веществ, им бывает необходима инфузионная терапия для коррекции водно-электролитного баланса. Кроме того, так как при синдроме Пирсона обычно наблюдается повышенная кислотность крови, больные получают терапию бикарбонатом натрия или дихлорацетатом. Для купирования инфекционных осложнений используются антибиотики.
Кроме того, так как при синдроме Пирсона обычно наблюдается повышенная кислотность крови, больные получают терапию бикарбонатом натрия или дихлорацетатом. Для купирования инфекционных осложнений используются антибиотики.
Трансплантация костного мозга теоретически может привести к нормализации показателей крови. Но, к сожалению, она не снимает прочие проблемы, возникающие при синдроме Пирсона. Кроме того, при нарушениях, развившихся в результате синдрома Пирсона, сама по себе процедура трансплантации сопряжена с повышенным риском и почти никогда не применяется.
Прогноз
Большинство больных синдромом Пирсона умирает в первые 2-3 года жизни, несмотря на поддерживающее лечение. Однако немногочисленные пациенты проживают более долгую жизнь, причем иногда анемия прекращается сама собой. У таких больных могут развиться признаки синдрома Кернса-Сейра — особой разновидности митохондриальных болезней, которая характеризуется мышечными и другими нарушениями.
Главная — Журнал нефрология и диализ
Главная — Журнал нефрология и диализ
В последнем номере:
Аниконова Л.
 И., Воробьева О.А., Бакулина Н.В., 
И., Воробьева О.А., Бакулина Н.В., 
ATTR-амилоидоз — системное заболевание с вовлечением почекЛитун А.В., Симонова Ж.Г., Колмакова Е.В., 
Профилирование натрия и ультрафильтрации у больных на программном гемодиализе: Фокус на качество жизниВасильева И.А., 
Факторы, ассоциированные с качеством жизни на додиализных стадиях хронической болезни почек. Обзор литературыЧеботарева Н.
 В., Лысенко Л.В., 
В., Лысенко Л.В., 
Поражение почек, ассоциированное с нестероидными противовоспалительными препаратамиЗахарова Е.В., Кривушкин С.А., Виноградова О.В. и соавт., 
Фибриллярный гломерулонефрит — трудности и возможности диагностикиКозловская Н.Л., Стариков Д.В., Бондаренко Т.В. и соавт., 
Вторичная тромботическая микроангиопатия или вторичный ГУС: виноваты наркотики или злокачественная артериальная гипертония? Клиническое наблюдение и обзор литературыЯнковой А.
 Г., Зулькарнаев А.Б., 
Г., Зулькарнаев А.Б., 
Травма центральных сосудов, приведшая к профузному кровотечению, после имплантации туннельных диализных катетеров у больных, находящихся на лечении гемодиализомГордеева О.М., Карпина Н.Л., 
Выявление факторов риска развития туберкулеза органов дыхания среди больных хронической болезнью почек в терминальной стадииМанченко О.В., Белавина Н.И., Жданова А.В. и соавт., 
Минерально-костные нарушения и внекостная кальцификация у пациента на программном гемодиализеХудякова А.
 Д., Каширина А.П., Карасева А.А. и соавт., 
Д., Каширина А.П., Карасева А.А. и соавт., 
Почечная дисфункция и гиперурикемия у пациентов, перенесших новую коронавирусную инфекциюАлидади Али, Фатиде Тахере Мохаммади, 
Интраназальный вазопрессин (DDAVP) и частота внутридиализной гипотензии при терминальной стадии почечной недостаточности
Наиболее читаемые статьи
Руководство по клинической практике перии послеоперационного ухода за артериовенозными фистулами и сосудистыми протезами для гемодиализа у взрослых пациентов. Краткий обзор рекомендаций Европейской наилучшей клинической практики в нефрологи (ERBP)
Клинические Практические Рекомендации KDIGO 2012 по Диагностике и Лечению Хронической Болезни Почек
Заместительная терапия больных с хронической почечной недостаточностью в Российской Федерации в 1998-2011 гг.
 (Отчет по данным Российского регистра заместительной почечной терапии. Часть первая)
(Отчет по данным Российского регистра заместительной почечной терапии. Часть первая)
Бикбов Б.Т., Томилина Н.А.
Откуда у девочки Аланы три родителя
- Шарлотт Притчард
- Би-би-си
Подпишитесь на нашу рассылку ”Контекст”: она поможет вам разобраться в событиях.
Алана Сааринен любит играть в гольф и на фортепиано, слушать музыку и общаться с друзьями. В этом отношении она мало отличается от других подростков. Но кое в чем Алана отличается от большинства людей: каждая клетка ее тела содержит ДНК трех человек. Таких людей в мире совсем немного.
«Многие говорят, что черты лица у меня от мамы, глаза от папы. .. Я унаследовала от них некоторые признаки, и характер тоже», — говорит Алана.
.. Я унаследовала от них некоторые признаки, и характер тоже», — говорит Алана.
«Но у меня есть ДНК от еще одной женщины. Ее я третьим родителем не считаю, у меня просто митохондрии от нее», — замечает девочка.
Митохондрии часто называют энергетическими станциями клетки. Они вырабатывают энергию, необходимую для деятельности каждой клетки, и тем самым поддерживают функционирование организма. Но еще в них содержится небольшое количество ДНК.
В мире живет всего лишь от 30 до 50 человек, рожденных из яйцеклеток, в которые были пересажены митохондрии, а вместе с ними и ДНК, от третьего лица. Алана – одна из них. Она была зачата в США в рамках эксперимента по лечению бесплодия. Метод, применявшийся в ходе этого эксперимента, впоследствии был запрещен.
Но, возможно, в скором времени людей с тремя биологическими родителями, как у Аланы, станет больше, поскольку в Великобритании рассматривается идея легализации нового, похожего метода, предусматривающего использование донорских митохондрий для лечения опасных генетических заболеваний.
Новый метод называется митохондриальной заменой. Если парламент одобрит его применение, Великобритания станет единственной страной в мире, допускающей рождение детей с тремя родителями.
Цитоплазматический перенос
Подпись к фото,
Шарон Сааринен (на фото слева) не нарадуется на свою дочь
Пропустить Подкаст и продолжить чтение.
Подкаст
Что это было?
Мы быстро, просто и понятно объясняем, что случилось, почему это важно и что будет дальше.
эпизоды
Конец истории Подкаст
Метод лечения бесплодия, благодаря которому Алана появилась на свет, называется цитоплазматическим переносом. Ее мать, Шарон Сааринен, 10 лет пыталась зачать. Перепробовала все существовавшие тогда методы искусственного оплодотворения, — но все безуспешно.
«Я чувствовала себе никчемной. Я испытывала чувство вины перед мужем за то, что не могла дать ему ребенка. Когда хочешь родить биологического ребенка, но не можешь, возникает чувство отчаяния. Невозможно заснуть, это с тобой постоянно, занимает все твои мысли», — вспоминает женщина.
Я испытывала чувство вины перед мужем за то, что не могла дать ему ребенка. Когда хочешь родить биологического ребенка, но не можешь, возникает чувство отчаяния. Невозможно заснуть, это с тобой постоянно, занимает все твои мысли», — вспоминает женщина.
В конце 1990-х годов клинический эмбриолог доктор Жак Коэн и его команда из Института Сент-Барнабус в Нью-Джерси (США) предложили технологию цитоплазматического переноса.
«Мы чувствовали, что есть шанс, что какой-то элемент, какая-то структура в цитоплазме клетки функционирует не оптимально. И одним из главных кандидатов […] были структуры митохондрий», — рассказывает Коэн.
Коэн пересадил содержавшую митохондрии цитоплазму из клеток женщины-донора в яйцеклетку Шарон Сааринен. После этого он оплодотворил ее яйцеклетку спермой ее мужа. В оплодотворенную яйцеклетку попали и донорские митохондрии, а с ними и ДНК.
В клинике Коэна методом цитоплазматического переноса было зачато 17 младенцев, несущих в себе, таким образом, ДНК трех человек.
Опасность аномалий
Применение этого метода вызывало определенные опасения. Всего забеременело 12 женщин, но у одной из них беременность закончилась выкидышем на раннем сроке.
Коэн и его коллеги полагают, что выкидыш был обусловлен отсутствием X-хромосомы и что в принципе один случай из 12 – это ожидаемый процент.
«Там еще было зачатие близнецов, и один из них родился совершенно нормальным, а у второго отсутствовала X-хромосома. То есть две [аномалии] на всю эту небольшую группу зародышей, зачатых в результате применения этой процедуры. Но и это нас беспокоило, и мы должным образом отразили этот факт в литературе и сообщили комитету по этике, надзирающему за нашей деятельностью», — говорит ученый.
Все прочие дети на момент рождения представлялись здоровыми, но через год-два у одного из них выявились «ранние признаки комплексных нарушений развития, включавших в себя широкий спектр когнитивных расстройств, в том числе аутизм», отметил Коэн.
По его словам, трудно сказать, были ли эти отклонения от нормы случайностью или же закономерным следствием цитоплазматического переноса.
Метод переняли другие клиники, и, по оценке Коэна, таким путем в мире родилось от 30 до 50 детей с ДНК трех человек.
Однако в 2002 году американское Управление по безопасности пищевых продуктов и лекарственных средств потребовало прекратить применение метода цитоплазматического переноса, до тех пор пока не будет доказана его этичность и безопасность. Все клиники выполнили требование надзорного органа.
«Была реакция ученых, специалистов по этике, общественности. В основном реакция была позитивная, но была и критика. По-моему это нормально. Каждый раз, когда в медицине проводится эксперимент, возникает реакция: а каковы риски?» – объясняет Коэн.
Основной момент, на который указывали критики, заключался в том, что эксперимент воздействовал и на структуру уже оплодотворенной клетки, тогда как прежние методы затрагивали лишь структуру сперматозоидов и яйцеклеток. Алана может передать свой необычный генетический код своим детям, а те, в свою очередь, следующим поколениям. Последствия этого пока не изучены.
Алана может передать свой необычный генетический код своим детям, а те, в свою очередь, следующим поколениям. Последствия этого пока не изучены.
Новый метод
Из-за недостаточности финансирования не было возможности отследить дальнейшую судьбу детей, родившихся на свет, как Алана, в результате цитоплазматического переноса, говорит Коэн. Однако недавно Институт Сент-Барнабус все же нашел необходимые средства.
Митохондрии наследуются только от матери, поэтому только девочки могут передать свой необычный генетический код.
Шарон Сааринен говорит, что ее дочь – совершенно типичный подросток и пышет здоровьем.
«Она всегда была здоровой. Никогда не болела ничем серьезнее простуды или гриппа. Вообще никаких проблем со здоровьем», — замечает Сааринен.
Здоровье детей, родившихся путем цитоплазматического переноса, вызывает пристальное внимание потому, что митохондриальная замена, которую предлагают легализовать в Великобритании, предназначена для совсем другой цели, нежели лечение бесплодия.
Этот метод рассчитан на женщин с болезнями, вызванными дефектами митохондриальной ДНК. Митохондриальная замена призвана пересадить им здоровую ДНК, чтобы они не могли передать наследственные заболевания потомству.
Потенциально возможно два метода митохондриальной замены:
- Берутся яйцеклетки матери с дефектными митохондриями и донора со здоровыми. Из обеих клеток удаляется ядро, содержащее основную массу генетического материала. Ядро донорской клетки уничтожается. Затем материнское ядро пересаживается в здоровую донорскую яйцеклетку, и та, в свою очередь, оплодотворяется спермой отца.
- Отцовской спермой оплодотворяются обе яйцеклетки – и материнская, и донорская, так что получается два эмбриона. После этого из обеих оплодотворенных яйцеклеток извлекается формирующееся ядро. Ядро, производное от донорской клетки, уничтожается, а на его место пересаживается материнское ядро.
Митохондриальные болезни
«Митохондриальные заболевания обычно поражают ткани и органы, поглощающие большое количество энергии», — говорит профессор Даг Турнбулл из Университета Ньюкасла. Он уже не один десяток лет лечит людей с такими генетическими отклонениями и участвовал в создании технологий лечения от этих болезней, – а они, по его словам, причиняют людям много страданий.
Он уже не один десяток лет лечит людей с такими генетическими отклонениями и участвовал в создании технологий лечения от этих болезней, – а они, по его словам, причиняют людям много страданий.
«Заболевания затрагивают сердце, мозг, иногда скелетные мышцы. У людей появляются серьезнейшие пороки сердца, приводящие, в конечном счете, к его остановке, крайняя слабость, при которой люди не могут жить без дыхательных аппаратов или передвигаться без инвалидной коляски. Если болезнь поражает мозг, то отмечается эпилепсия, инсульты, а позже острые формы приобретенного слабоумия», — говорит профессор.
По его оценке, митохондриальными болезнями в Великобритании страдает один человек из 3-5 тысяч. «Мы лечим симптомы. Мы можем улучшить качество и продолжительность жизни таких пациентов, но излечить их мы не можем», — добавляет Турнбулл.
При этом по его словам, в митохондрии содержится всего 13 «важных генов». Для сравнения, в ядре клетки – 23 тыс. генов, определяющих важнейшие физические и психические свойства человека.
«Мы не пытаемся искусственно сделать человека сильнее, или чтобы у него были белокурые волосы. Мы лишь пытаемся предотвратить серьезную болезнь, и это единственное обоснование», — говорит Турнбулл.
Автор фото, Charlotte Pritchard
Шарон Бернарди живет в Сазерленде на севере Англии. Стены ее гостиной увешаны фотографиями ее детей. Все они умерли.
«Мои дети похоронены на трех разных кладбищах, — говорит она. – На это не рассчитываешь, когда пытаешься завести семью. У меня остались чудные фото и воспоминания, но больше ничего».
Почти все дети Бернарди умерли спустя считанные часы после рождения. Врачи не знали, в чем причина. Поэтому Бернарди не оставляла попытки завести здорового ребенка.
Четвертый ее ребенок, Эдвард, сразу не умер. Напротив, он благополучно, как казалось, дожил до четырех с половиной лет. Тут-то ему и поставили диагноз – синдром Лея. Это редкая митохондриальная болезнь. С годами ему становилось все хуже.
«С 20 лет Эдварду стало труднее передвигаться. У него появились новые симптомы – спазмы. Он кричал… по четыре, пять, шесть часов подряд. У него сводило мускулы, руки, лицо. Это было похоже на дистонические спазмы – они очень болезненные. Он по восемь часов кричал от боли. Лицо корчилось, руки немели и не слушались. Смотреть на это было тяжело», — рассказывает Бернарди.
Три года назад, прожив всего 21 год, Эдвард скончался.
«Чтобы Эдвард умер не напрасно»
Автор фото, BBC World Service
«Вся моя жизнь была посвящена Эдварду. Даже сейчас, когда я засыпаю, я иногда вдруг просыпаюсь от мысли: «Что-то тихо». И только потом вспоминаю, «Брось, Эдварда больше нет», — говорит Шарон Бернарди.
«Я бы без колебаний согласилась на [митохондриальную замену]. Надеюсь, что этот новый вариант кому-то поможет. И что к нему отнесутся серьезно и разрешат», — говорит она.
«Я не хочу, чтобы получилось так, что мой сын умер ни за что. Я хочу, чтобы его смерть сыграла положительную роль. Он лишился жизни в 21 год. Мы хотим, чтобы такого больше не было. Люди должны понять, что эта болезнь калечит всю жизнь. Мы хотим, чтобы она не передавалась по наследству, и тем самым избавить от нее будущие семьи», — подчеркивает Бернарди.
Я хочу, чтобы его смерть сыграла положительную роль. Он лишился жизни в 21 год. Мы хотим, чтобы такого больше не было. Люди должны понять, что эта болезнь калечит всю жизнь. Мы хотим, чтобы она не передавалась по наследству, и тем самым избавить от нее будущие семьи», — подчеркивает Бернарди.
Однако не все настроены столь однозначно. Некоторые считают, что это первый шаг на скользком пути к созданию генетически модифицированных людей.
Фиона Брюс, лидер британской межфракционной парламентской группы за жизнь, говорит, что в случае одобрения новый метод позволит изменять гены на уровне оплодотворенной клетки, а это «определяется в Хартии ЕС об основных правах как по сути евгеника».
«Мы разрешим эту технологию, а для чего она будет использоваться в будущем, — кто знает? Мы открываем ящик Пандоры», — указывает политик.
Решение относительно нового метода предстоит принять британскому Управлению по оплодотворению человека и эмбриологии. Оно заказало три независимых анализа для изучения его безопасности. Исследования пришли к выводу, что митохондриальную замену «нет оснований считать небезопасной».
Оно заказало три независимых анализа для изучения его безопасности. Исследования пришли к выводу, что митохондриальную замену «нет оснований считать небезопасной».
Это значит, что «после некоторых дополнительных экспериментов будет разумно ввести этот метод в клиническую практику при наличии всех необходимых обстоятельств», говорит Питер Брод, почетный профессор акушерства и гинекологии в лондонском Кингс-Колледже. Он участвовал во всех трех группах, анализировавших безопасность митохондриальной замены.
Элемент риска
«В любом переходе от научных исследований к клинической практике есть элемент риска – на него приходится идти», — отмечает Брод.
Он указывает, что когда внедряли экстракорпоральное оплодотворение (ЭКО), высказывались все те же самые опасения. Великобритания уже десятки лет находится на переднем крае вспомогательных репродуктивных технологий, именно здесь еще в 1978 году родилась первая девочка, «зачатая в пробирке», — Луиз Браун.
«И тогда тоже в газетах писали, что мы «играем в бога» и создаем «генетически модифицированных людей», — вспоминает Брод.
«В истории вспомогательных репродуктивных технологий мне известно очень мало случаев, когда новые методы приходилось запрещать из-за опасности. Напротив, насколько я знаю, все идет как по маслу», — указывает он.
Митохондриальная замена, по словам ученого, подвергнется такому же тщательному анализу, как и другие, теперь уже широко применяемые методы, в том числе ЭКО.
«Изначально все техники внедрялись сразу после экспериментов на мышах, кроликах и других лабораторных животных. А здесь все испытывалось на приматах, обезьянах-макаках, и все это было в высшей степени полезно и обнадеживающе. Вот поэтому мы и пришли к выводу, что нет оснований считать митохондриальную замену небезопасной», — отмечает Брод.
Эксперименты на макаках проводились в штате Орегон в США. Родившиеся в ходе эксперимента обезьяны прожили уже пять лет и вроде бы вполне здоровы.
Брод отмечает, что само по себе присутствие ДНК третьего лица в организме не несет в себе ничего нового.
«Представьте себе пересадку костного мозга, допустим, вам не повезло заболеть лейкемией, ваш костный мозг убили облучением вместе с раковой опухолью, а на его место пересадили донорский – например от меня. По сути с этого времени в вашем организме будет содержаться моя ДНК. Но это не будет означать, что вы мой родственник. Вы будете мне благодарны, а ведь у вас в теле появится ДНК третьего лица», — указывает Брод.
Голос скептиков
Критики указывают на то, что в случае митохондриальной замены эта чужеродная ДНК будет передаваться будущим поколениям.
Доктор Тед Морроу из Университета Сассекса и его коллеги проводили эксперименты по митохондриальной замене на животных и в ряде публикаций указывали на определенные риски.
«У мышей, — говорит он, — отмечались изменения в когнитивных способностях – способностях учиться и задействовать мозг. У мух-пестрокрылок изменялась фертильность самцов, менялись процессы старения, в разных экспериментах затрагивался широкий спектр признаков».
У мух-пестрокрылок изменялась фертильность самцов, менялись процессы старения, в разных экспериментах затрагивался широкий спектр признаков».
Выводы Морроу обсуждались в исследованиях, заказанных Управлением по оплодотворению человека и эмбриологии, но их посчитали не относящимися к людям, поскольку эксперименты проводились на животных, подвергавшихся инбридингу.
Однако Морроу настаивает на актуальности своих исследований и считает, что от них не следовало так легко отмахиваться.
Его данные подхватили противники митохондриальной замены, такие как Фиона Брюс, потребовавшая провести специальные дебаты по этому вопросу в палате общин. «Сам по себе этот метод может привести к тому, что ребенок унаследует неизученные медицинские осложнения», — указывает она.
Морроу находит странным то, что в прессе его изображали союзником групп, выступающих против репродуктивной медицины в целом и абортов в частности. «Я ученый, и я не с теми, кто «за жизнь». Я просто считаю, что здесь и правда есть опасения по поводу безопасности», — говорит он.
Я просто считаю, что здесь и правда есть опасения по поводу безопасности», — говорит он.
«Я все сделала правильно»
Подпись к фото,
Алана Сааринен не придает большого значения донору митохондрий в своей жизни
Алана и Шарон Сааринен с интересом следят за британскими дебатами из США.
«Я бы хотела встретиться с ней, с женщиной-донором, чтобы сказать, как я ей благодарна за то, что она для нас сделала. Как отблагодарить человека, который дал тебе жизнь? Это же невозможно», — говорит Шарон.
Алана соглашается с матерью, но осторожно: «Да, я думаю, что было бы хорошо сказать ей спасибо. Но я не хотела бы завязывать с ней какие-то отношения или связи. ДНК от нее у меня совсем немного».
Шарон, однако, не унимается: «Я знаю, что у моей дочери митохондрии другого человека, но посмотрите, какой из нее замечательный человек вырос, и здоровая! А что она передаст гены своим детям, меня нисколько не беспокоит. Я знаю, что все сделала правильно. Каждый день у меня перед глазами живое доказательство того, что все кончилось хорошо».
Я знаю, что все сделала правильно. Каждый день у меня перед глазами живое доказательство того, что все кончилось хорошо».
Митохондриальная болезнь | Бостонская детская больница
Как диагностируются митохондриальные нарушения?
Поскольку симптомы очень разнообразны и поражают несколько органов тела, диагностика митохондриального заболевания может быть сложной задачей. Иногда другие заболевания, не связанные с митохондриями, ошибочно диагностируются как митохондриальные заболевания. Верно и обратное: иногда у людей, у которых действительно есть митохондриальное заболевание, диагностируют что-то другое.
Многие симптомы митохондриального заболевания, такие как задержка развития, низкорослость, плохая выносливость, задержка развития, судороги, плохой мышечный тонус, рвота, сильный запор или диарея, имеют множество других причин. Из-за этого обычно не один симптом, а комбинация двух, трех или более различных симптомов заставляет клиницистов подозревать митохондриальное заболевание.
Генетическое тестирование — самый надежный способ диагностики и классификации митохондриального заболевания. Мы можем порекомендовать генетическое тестирование вашего ребенка (а иногда и родителей) при наличии любого из следующих симптомов:
- задержка развития с поражением других органов
- дардиомиопатия (заболевание сердечной мышцы) или необъяснимая блокада сердца, или нарушение электрических сигналов в сердце
- высокий уровень лактата в крови или спинномозговой жидкости при наличии других симптомов
- определенные аномальные результаты при визуализации головного мозга
- офтальмоплегия (нарушение движения глаз) или птоз (опущение верхнего века)
- потеря слуха
- тяжелые нарушения моторики желудочно-кишечного тракта (слабые или утраченные мышечные сокращения в кишечнике) или кишечная псевдонепроходимость (кишечная непроходимость, вызванная неспособностью кишечника протолкнуть пищу)
- значительная регрессия развития на фоне болезни
Генетическое тестирование часто начинается с анализа митохондриальной ДНК и, если результаты отрицательные, с проверки ядерной ДНК на наличие генов, которые, как известно, участвуют в митохондриальных заболеваниях. Если эти тесты окажутся отрицательными, может потребоваться полный анализ ядерной ДНК ребенка путем секвенирования всего экзома (это похоже на секвенирование всего генома, но анализируются только гены, кодирующие белки).
Если эти тесты окажутся отрицательными, может потребоваться полный анализ ядерной ДНК ребенка путем секвенирования всего экзома (это похоже на секвенирование всего генома, но анализируются только гены, кодирующие белки).
Тип и глубина генетического тестирования, которые мы рекомендуем, будут зависеть от симптомов у ребенка и от того, насколько сильно мы подозреваем митохондриальное заболевание. К сожалению, на момент написания этой статьи обширное генетическое тестирование не всегда покрывается страховкой. Если вы или ваш ребенок нуждаетесь в тестировании, мы будем сотрудничать с вашими страховыми компаниями, чтобы помочь с процессом утверждения.
Дополнительные негенетические тесты также помогают в диагностике митохондриальных заболеваний. К ним относятся:
- биохимические исследования мочи, крови и спинномозговой жидкости
- биопсия мышц для исследования митохондрий и определения уровня ферментов
- магнитно-резонансная томография (МРТ) головного и спинного мозга
Если подозревается или выявлено митохондриальное заболевание, мы можем направить вашего ребенка на дальнейшее обследование и консультацию у специалистов. Тестирование зависит от симптомов и может включать:
Тестирование зависит от симптомов и может включать:
- эхокардиограмму
- электрокардиограмма (ЭКГ)
- осмотр глаз
- проверки слуха
Управление состоянием вашего ребенка
Хотя митохондриальные расстройства неизлечимы, дети часто чувствуют себя лучше, когда симптомы обнаруживаются и лечатся на ранней стадии. Ваш ребенок будет находиться под пристальным наблюдением и обследоваться на различные состояния, связанные с митохондриальными заболеваниями, такие как проблемы с сердцем, зрением и слухом. Симптомы часто можно облегчить, поддерживая хорошее общее состояние здоровья, уделяя особое внимание питанию и избегая инфекций и обезвоживания.
Упражнения — один из немногих проверенных методов улучшения функционирования митохондрий, которые могут помочь сохранить силу и выносливость вашего ребенка. Режимы упражнений должны контролироваться, их интенсивность должна нарастать очень постепенно, и их следует приостанавливать во время болезни.
Какие существуют варианты лечения митохондриальных заболеваний?
В настоящее время витамины и добавки являются основой лечения митохондриальных заболеваний. Считается, что они помогают митохондриям вырабатывать энергию и уменьшают накопление токсичных соединений внутри клеток. Эти добавки и кофакторы иногда дают вместе в «коктейлях». В настоящее время наиболее хорошо протестированные соединения включают коэнзим Q10 и креатин, но мы также используем множество других добавок.
Схемы лечения конкретных митохондриальных заболеваний могут включать соединения, дефицит которых обусловлен заболеванием, такие как аргинин (при MELAS) и фолиновая кислота (при синдроме Кернса-Сейра). В Boston Children’s мы тестируем дихлорацетат (DCA), который противостоит высоким уровням молочной кислоты, обнаруживаемым при некоторых митохондриальных заболеваниях. При определенных заболеваниях мы можем назначить специальную диету.
Поддерживающая терапия
Поскольку дети с митохондриальными заболеваниями, как правило, очень чувствительны к стрессам, вызванным легкими заболеваниями, такими как простуда и лихорадка, ваш врач иногда назначает дополнительную поддерживающую терапию, когда ребенок болен. Они могут включать витамины, кофакторы, лекарства для противодействия биохимическому дисбалансу, которые могут возникнуть, напитки, содержащие электролиты, а иногда и внутривенную (IV) гидратацию и внутривенные антибиотики. В некоторых случаях вашему ребенку может потребоваться наблюдение в больнице.
Они могут включать витамины, кофакторы, лекарства для противодействия биохимическому дисбалансу, которые могут возникнуть, напитки, содержащие электролиты, а иногда и внутривенную (IV) гидратацию и внутривенные антибиотики. В некоторых случаях вашему ребенку может потребоваться наблюдение в больнице.
Известно также, что дети с митохондриальными заболеваниями чувствительны к различным лекарствам, а также анестетикам, используемым при хирургических процедурах.
Митохондриальные заболевания у детей — PubMed
Обзор
. 2020 июнь; 287 (6): 609-633.
doi: 10.1111/joim.13054.
Epub 2020 7 апр.
С Рахман
1
Принадлежности
принадлежность
- 1 Группа митохондриальных исследований, Институт детского здоровья на Грейт-Ормонд-стрит Калифорнийского университета в Лондоне, Лондон, Великобритания.

PMID:
32176382
DOI:
10.1111/joim.13054
Бесплатная статья
Обзор
С Рахман.
J Интерн Мед.
2020 июнь
Бесплатная статья
. 2020 июнь; 287 (6): 609-633.
doi: 10.1111/joim.13054.
Epub 2020 7 апр.
Автор
С Рахман
1
принадлежность
- 1 Группа митохондриальных исследований, Институт детского здоровья на Грейт-Ормонд-стрит Калифорнийского университета в Лондоне, Лондон, Великобритания.

PMID:
32176382
DOI:
10.1111/joim.13054
Абстрактный
Митохондриальное заболевание, проявляющееся в детском возрасте, характеризуется клинической, биохимической и генетической сложностью. Некоторые дети страдают каноническими синдромами, но у большинства наблюдаются неклассические мультисистемные проявления болезни, вовлекающие практически любой орган в организме. Каждый ребенок имеет уникальное сочетание клинических признаков и траектории заболевания, что приводит к огромным проблемам в диагностике и лечении этих гетерогенных расстройств. В этом обзоре обсуждаются классические митохондриальные синдромы, наиболее часто проявляющиеся в детском возрасте, а затем представлена органная перспектива, включая системы, менее часто связанные с митохондриальными заболеваниями, такие как аномалии кожи и волос и иммунная дисфункция. Затем представлен подход к диагностике, включающий клиническую оценку и биохимические, нейровизуализационные и генетические исследования, с акцентом на проблему фенокопий. Обсуждается влияние секвенирования следующего поколения, а также важность функциональной проверки новых генетических вариантов, никогда ранее не связанных с митохондриальными заболеваниями. Обзор завершается кратким обсуждением доступных в настоящее время и новых методов лечения. Область митохондриальной медицины добилась огромных успехов за последние 30 лет: около 400 различных генов в двух геномах теперь связаны с первичными митохондриальными заболеваниями. Тем не менее, многие важные вопросы остаются без ответа, в том числе причины тканевой специфичности и вариабельности клинических проявлений у людей с одинаковыми генными дефектами, а также отсутствие терапии, модифицирующей заболевание, и биомаркеров для мониторинга прогрессирования заболевания и/или ответа на лечение.
Затем представлен подход к диагностике, включающий клиническую оценку и биохимические, нейровизуализационные и генетические исследования, с акцентом на проблему фенокопий. Обсуждается влияние секвенирования следующего поколения, а также важность функциональной проверки новых генетических вариантов, никогда ранее не связанных с митохондриальными заболеваниями. Обзор завершается кратким обсуждением доступных в настоящее время и новых методов лечения. Область митохондриальной медицины добилась огромных успехов за последние 30 лет: около 400 различных генов в двух геномах теперь связаны с первичными митохондриальными заболеваниями. Тем не менее, многие важные вопросы остаются без ответа, в том числе причины тканевой специфичности и вариабельности клинических проявлений у людей с одинаковыми генными дефектами, а также отсутствие терапии, модифицирующей заболевание, и биомаркеров для мониторинга прогрессирования заболевания и/или ответа на лечение.
Ключевые слова:
диагностический подход; дифференциальный диагноз; митохондриальная генетика; секвенирование нового поколения; фенокопии; феноменика.
© 2020 Ассоциация по изданию журнала внутренней медицины.
Похожие статьи
Распознавание, исследование и лечение митохондриальных заболеваний.
Дэвисон Дж. Э., Рахман С.
Дэвисон Дж. Э. и соавт.
Арч Дис Чайлд. 2017 ноябрь;102(11):1082-1090. doi: 10.1136/archdischild-2016-311370. Epub 2017 24 июня.
Арч Дис Чайлд. 2017.PMID: 28647693
Обзор.
Нарушения функции митохондрий.
Дебре Ф.Г., Ламберт М., Митчелл Г.А.
Дебре Ф.Г. и соавт.
Curr Opin Педиатр. 2008 авг; 20 (4): 471-82. doi: 10.1097/MOP.0b013e328306ebb6.
Curr Opin Педиатр. 2008.PMID: 18622207
Обзор.
Диагностический подход у младенцев и детей с митохондриальными заболеваниями.

Чи КС.
Чи КС.
Педиатр Неонатол. 2015 фев;56(1):7-18. doi: 10.1016/j.pedneo.2014.03.009. Epub 2014 20 августа.
Педиатр Неонатол. 2015.PMID: 25151629
Обзор.
Генетика и патология митохондриальных болезней.
Alston CL, Rocha MC, Lax NZ, Turnbull DM, Taylor RW.
Алстон С.Л. и соавт.
Джей Патол. 2017 Январь; 241(2):236-250. doi: 10.1002/path.4809. Epub 2016 2 ноября.
Джей Патол. 2017.PMID: 27659608
Бесплатная статья ЧВК.Обзор.
[Митохондриальные заболевания у детей, включая синдром Лея — биохимические и молекулярные предпосылки].
Проницка Е, Пекутовска-Абрамчук Д, Проницки М.
Проницка Э. и др.
Постэпи Биохим. 2008;54(2):161-8.
Постэпи Биохим. 2008.
PMID: 18807927
Обзор.
польский.
Посмотреть все похожие статьи
Цитируется
Последние достижения в области митохондриальных заболеваний: от молекулярного понимания до терапевтических перспектив.
Альдоссари А.М., Тауфик Э.А., Аломари М.Н., Алсудир С.А., Альфахад А.Дж., Альшехри А.А., Альмугем Ф.А., Мохаммед Р.Ю., Альзайди М.М.
Альдоссари А.М. и соавт.
Saudi Pharm J. 30 августа 2022 г. (8): 1065-1078. doi: 10.1016/j.jsps.2022.05.011. Epub 2022 28 мая.
Саудовская Фарм Дж. 2022.PMID: 36164575
Бесплатная статья ЧВК.Обзор.
Первичные и вторичные митохондриальные заболевания: этиология и терапевтические стратегии.
Валенти Д., Вакка Р.А.

Валенти Д. и др.
Дж. Клин Мед. 2022 июль 20;11(14):4209. doi: 10.3390/jcm11144209.
Дж. Клин Мед. 2022.PMID: 35887983
Бесплатная статья ЧВК.Митохондрии при нейродегенерации.
Чу КТ.
Чу КТ.
Curr Opin Physiol. 2022 апр;26:100532. doi: 10.1016/j.cophys.2022.100532. Epub 2022 1 апр.
Curr Opin Physiol. 2022.PMID: 35814636
Артериоэктатическая спинальная ангиопатия у детей: клиническое, визуализирующее, лабораторное, гистологическое и генетическое описание новой сосудистой патологии ЦНС.
Абруццо Т., ван ден Берг Р., Вадивелу С., Хеттс С.В., Дишоп М., Корнехо П., Нараянан В., Рэмси К.Е., Купвуд С., Медичи-ван ден Херик Э.Г., Розендаль С.Д., Лоутон М., Бернес С.
Абруццо Т. и др.
AJNR Am J Нейрорадиол. 2022 июль; 43 (7): 1060-1067. doi: 10.3174/ajnr.A7551. Epub 2022 30 июня.
2022 июль; 43 (7): 1060-1067. doi: 10.3174/ajnr.A7551. Epub 2022 30 июня.
AJNR Am J Нейрорадиол. 2022.PMID: 35772802
Использование секвенирования нового поколения для выявления митохондриальных заболеваний.
Махмуд С., Бисвас С., Афрос С., Мита М.А., Хасан М.Р., Шиму М.С.С., Пол Г.К., Чанг С., Салех М.А., Альшехри С., Гонейм М.М., Алрувайли М., Ким Б.
Махмуд С. и др.
Curr выпускает Mol Biol. 2022 27 февраля; 44 (3): 1127-1148. дои: 10.3390/cimb44030074.
Curr выпускает Mol Biol. 2022.PMID: 35723297
Бесплатная статья ЧВК.Обзор.
Просмотреть все статьи «Цитируется по»
использованная литература
Рахман Дж., Рахман С. Митохондриальная медицина в эпоху омики. Ланцет 2018; 391: 2560-74.

Торберн Др. Митохондриальные расстройства: распространенность, мифы и достижения. Дж Наследовать Метаб Дис 2004; 27: 349-62.
Парих С., Караа А., Гольдштейн А. и др. Диагностика «возможного» митохондриального заболевания: экзистенциальный кризис. J Med Genet 2019; 56: 123-30.
Альперс Б. Диффузная прогрессирующая дегенерация серого вещества головного мозга. Архив Neurol Psychiat 1931; 25: 469-505.
Ли Д. Подострая некротизирующая энцефаломиелопатия у младенца. J Neurol Neurosurg Psychiat 1951; 14: 216-221.
Типы публикаций
термины MeSH
Грантовая поддержка
- DH_/Министерство здравоохранения/Соединенное Королевство
Митохондриальная болезнь | KidsHealth NZ
Митохондриальные заболевания
Понятно, что диагноз митохондриального заболевания может быть разрушительным. Будет много вопросов и эмоций. Эта страница предназначена для предоставления информации и поддержки новозеландцам, пострадавшим от «мито», а также их семьям и друзьям.
Будет много вопросов и эмоций. Эта страница предназначена для предоставления информации и поддержки новозеландцам, пострадавшим от «мито», а также их семьям и друзьям.
Ключевые моменты, которые следует помнить о митохондриальных заболеваниях
- У всех нас есть митохондрии – они находятся в каждой клетке нашего тела
- митохондрии — это крошечные части наших клеток, которые отвечают за выработку энергии и известны как «электростанция» или батарея клетки. энергия
Диагноз митохондриального заболевания?
Диагноз митохондриального заболевания, по понятным причинам, может быть разрушительным. Будет много вопросов и эмоций. Эта страница предназначена для предоставления информации и поддержки новозеландцам, пострадавшим от мито, а также их семьям и друзьям.
Что такое митохондрии?
В каждой клетке нашего тела есть митохондрии. Это крошечные части наших клеток, которые отвечают за выработку энергии — «электростанция» или батарея клетки. Через ряд сложных химических реакций они превращают глюкозу и кислород в энергетическое химическое вещество, называемое АТФ. Этот химический процесс называется окислительным фосфорилированием. Они также производят энергию из жира (окисление жирных кислот). Когда митохондрии не работают должным образом, в клетке происходит сбой питания, и пораженный орган начинает отключаться. Этот сбой питания называется митохондриальной болезнью.
Через ряд сложных химических реакций они превращают глюкозу и кислород в энергетическое химическое вещество, называемое АТФ. Этот химический процесс называется окислительным фосфорилированием. Они также производят энергию из жира (окисление жирных кислот). Когда митохондрии не работают должным образом, в клетке происходит сбой питания, и пораженный орган начинает отключаться. Этот сбой питания называется митохондриальной болезнью.
Что такое митохондриальная болезнь?
Митохондриальная болезнь или митохондриальная болезнь возникает, когда наши митохондрии не работают должным образом. Митохондриальная дисфункция может привести к повреждению клеток и отказу органов. Повреждение может быть вызвано, когда организм находится в состоянии сильного стресса, например, во время болезни. Мито может быть дегенеративным заболеванием, которое обычно поражает части нашего тела, требующие наибольшего количества энергии, такие как мозг, сердце, почки и мышцы, но может быть затронута любая система органов в любом возрасте. В настоящее время не существует лекарства от митохондриальной болезни.
В настоящее время не существует лекарства от митохондриальной болезни.
Каковы признаки и симптомы митохондриального заболевания?
Тяжесть симптомов Мито различается от человека к человеку, даже в пределах одной семьи. Путь у всех разный. Многие люди будут иметь полиорганное заболевание. У младенцев часто вовлекается головной мозг. Некоторыми симптомами могут быть:
- нормальное развитие с последующей потерей навыков
- плохой рост, трудности при кормлении
- инсультоподобные события, поражающие определенные части мозга
- судороги
- нарушение координации, тремор или задержка моторных вех
- мышечная слабость (гипотония или миопатия)
- неспособность к обучению у детей или ранняя деменция у взрослых
- снижение движения глаз (офтальмоплегия), потеря зрения или опущение век (птоз) )
- неврологическая глухота
- утолщение сердца или нарушение сердечного ритма
- заболевание печени или почек или недостаточность
Взрослые могут иметь ранний диабет и множественные выкидыши.
Человек с Мито может выглядеть «нормально», но из-за своего состояния сталкивается с большими проблемами и потенциальными проблемами со здоровьем.
Почему возникают митохондриальные заболевания?
Все белки в нашем организме сделаны из нашей ДНК — нашего генетического материала, который делает нас людьми. У нас есть 2 типа ДНК:
- Наша ядерная ДНК (яДНК), которую мы наследуем от обоих родителей. В нашей нДНК более 20 000 генов. Более 1000 участвуют в обеспечении функционирования митохондрий.
- Митохондриальная ДНК (мтДНК), которая унаследована от нашей матери, поскольку только яйцеклетка содержит мтДНК. Это кольцо ДНК есть в каждой митохондрии. Он содержит 37 генов.
Митохондриальное заболевание может быть вызвано одним из следующих:
- нарушением (мутацией) яДНК, которая унаследована от обоих родителей (аутосомно-рецессивное наследование)
- мутацией в мтДНК, которая может быть унаследована от матери наследственность)
- мутация в мтДНК или яДНК, которая, по-видимому, впервые возникает у больного (de novo)
- мутация яДНК, передающаяся от одного больного родителя (аутосомно-доминантная или сцепленная с Х-хромосомой)
Как диагностируется митохондриальное заболевание?
Не существует простого теста для диагностики митохондриального заболевания. Постановка диагноза часто требует сложения кусочков головоломки. Многие симптомы Мито похожи на симптомы других болезней. Симптомы могут быть неустойчивыми, сначала малозаметными, что еще больше усложняет путь к постановке диагноза. Клинические и рентгенологические признаки, кровь, моча и другие биохимические анализы могут убедительно свидетельствовать о митохондриальном заболевании. Для подтверждения Мито обычно требуется тестирование ДНК и, в меньшей степени, биопсия мышц. Иногда конкретный генетический диагноз поставить невозможно, поэтому диагноз «подозрение на митохондриальное заболевание» ставится на основании всех клинических и биохимических признаков. Наше понимание генетической основы Мито постоянно растет. Конкретный генетический диагноз может помочь семьям лучше понять состояние, узнать, чего ожидать в будущем, и помочь им принять решение о будущих беременностях.
Постановка диагноза часто требует сложения кусочков головоломки. Многие симптомы Мито похожи на симптомы других болезней. Симптомы могут быть неустойчивыми, сначала малозаметными, что еще больше усложняет путь к постановке диагноза. Клинические и рентгенологические признаки, кровь, моча и другие биохимические анализы могут убедительно свидетельствовать о митохондриальном заболевании. Для подтверждения Мито обычно требуется тестирование ДНК и, в меньшей степени, биопсия мышц. Иногда конкретный генетический диагноз поставить невозможно, поэтому диагноз «подозрение на митохондриальное заболевание» ставится на основании всех клинических и биохимических признаков. Наше понимание генетической основы Мито постоянно растет. Конкретный генетический диагноз может помочь семьям лучше понять состояние, узнать, чего ожидать в будущем, и помочь им принять решение о будущих беременностях.
Существует ли какое-либо лечение митохондриальной болезни?
Жизнь с митохондриальным заболеванием может быть очень сложной и сложной физически, психологически и эмоционально для больного человека, его друзей и семьи. В настоящее время нет доказанных с медицинской точки зрения методов лечения Мито. Однако есть некоторые клинические испытания, и ведутся многообещающие исследования для некоторых заболеваний. Некоторые люди могут очень хорошо реагировать на определенные витамины или определенные методы лечения в зависимости от генетического диагноза. Для большинства «лечение» — это поддерживающая терапия, сосредоточенная на точной и своевременной диагностике, лечении симптомов, поддержании хорошего питания, предотвращении болезней, где это возможно, и отказе от некоторых лекарств, которые могут повредить митохондрии. Некоторые врачи рекомендуют «митохондриальный витаминный коктейль» для поддержки митохондрий. Однако нет никаких доказательств того, что это полезно для большинства митохондриальных заболеваний.
В настоящее время нет доказанных с медицинской точки зрения методов лечения Мито. Однако есть некоторые клинические испытания, и ведутся многообещающие исследования для некоторых заболеваний. Некоторые люди могут очень хорошо реагировать на определенные витамины или определенные методы лечения в зависимости от генетического диагноза. Для большинства «лечение» — это поддерживающая терапия, сосредоточенная на точной и своевременной диагностике, лечении симптомов, поддержании хорошего питания, предотвращении болезней, где это возможно, и отказе от некоторых лекарств, которые могут повредить митохондрии. Некоторые врачи рекомендуют «митохондриальный витаминный коктейль» для поддержки митохондрий. Однако нет никаких доказательств того, что это полезно для большинства митохондриальных заболеваний.
Кто помогает лечить митохондриальные заболевания в Новой Зеландии?
Пациентам с митохондриальными заболеваниями иногда может потребоваться группа людей, чтобы справиться с их симптомами и проблемами. В эту группу могут входить члены семьи, невролог, офтальмолог, участковые медсестры, врачи общей практики, психологи, социальные работники, физиотерапевты, логопеды, диетологи или специалисты по паллиативной помощи. Иногда Национальная метаболическая служба Новой Зеландии лечит пациентов с митохондриальными заболеваниями. Специалисты по метаболизму (дети и взрослые) — доктор Каллум Уилсон, доктор Брайони Райдер и доктор Эмма Гламузина из Детской больницы Starship. Они и их команда могут помочь в координации с местными специалистами и другими членами команды. Они работают в международной сети специалистов и исследователей митохондриальных заболеваний.
В эту группу могут входить члены семьи, невролог, офтальмолог, участковые медсестры, врачи общей практики, психологи, социальные работники, физиотерапевты, логопеды, диетологи или специалисты по паллиативной помощи. Иногда Национальная метаболическая служба Новой Зеландии лечит пациентов с митохондриальными заболеваниями. Специалисты по метаболизму (дети и взрослые) — доктор Каллум Уилсон, доктор Брайони Райдер и доктор Эмма Гламузина из Детской больницы Starship. Они и их команда могут помочь в координации с местными специалистами и другими членами команды. Они работают в международной сети специалистов и исследователей митохондриальных заболеваний.
Не теряйте надежды — не дайте погаснуть электричеству!
Благодарности
Внешние ссылки и загрузки
Теги
Все условия
Последнее рассмотрение этой страницы 05 ноября 2019 .
Митохондриальные заболевания | Детское здоровье Райли
Найти доктора
Запросить встречу
- На этой странице:
- Лечение
- Ключевые моменты, которые следует помнить
- Службы поддержки и ресурсы
- Места
- Отделения, лечащие это заболевание
Вернуться к началу страницы
Митохондрии
маленькие,
энергопродуцирующие структуры в клетках. Митохондрии иногда называют
Митохондрии иногда называют
электростанции клеток, потому что они производят большую часть энергии, необходимой вашему телу
функционировать. Митохондриальное расстройство возникает при повреждении
митохондрии, что истощает энергию клеток.
Митохондриальные расстройства различаются по тяжести и возрасту начала у разных людей. Они могут проявиться в любой момент жизни, хотя, как правило, первые симптомы проявляются в детстве. Если у вашего ребенка митохондриальное заболевание, скорее всего, будут затронуты мозг, мышцы и желудочно-кишечный тракт (ЖКТ), поскольку каждая из этих частей тела требует большого количества энергии для нормального функционирования, хотя может быть затронута практически любая система органов. Митохондриальные заболевания могут наследоваться по-разному, но точную картину в данной семье определить сложно.
Некоторые симптомы митохондриальных нарушений включают:
- Вздутие живота
- Слепота
- Кардиомиопатия
- Глухота
- Деменция
- Задержка развития
- Проблемы с кормлением
- Частые инфекции
- Нарушения сердечного ритма
- Повышенная утомляемость
- Низкий мышечный тонус
- Мигрень
- Мышечная слабость
- Тошнота
- Изъятия
- Тяжелый запор
- Ночное апноэ
- Симптомы, подобные инсульту
- Проблемы с движением глаз
- Рвота
Пациенты обычно не испытывают всех этих симптомов. Наиболее распространенными симптомами являются усталость, низкий мышечный тонус, задержка развития и проблемы с ЖКТ.
Наиболее распространенными симптомами являются усталость, низкий мышечный тонус, задержка развития и проблемы с ЖКТ.
Диагностика митохондриальных заболеваний
Следующие обследования и тесты могут быть использованы для определения наличия у вашего ребенка митохондриального расстройства:
- Медицинский осмотр
- Анализы крови для определения повышенного уровня молочной кислоты или других биохимических отклонений
- Тестирование специфических митохондриальных и/или ядерных генов
- Магнитно-резонансная томография (МРТ) головного мозга
- Электрокардиограмма и эхокардиограмма
- Проверка зрения
- Неврологическое обследование
- Проверка слуха
Лечение
Лечение
Лекарства от митохондриальных заболеваний не существует. Однако лечение может
помогают уменьшить симптомы и замедлить долгосрочное ухудшение здоровья. вашего ребенка
вашего ребенка
врач может порекомендовать избегать некоторых видов лекарств, которые могут увеличить
симптомы, такие как седативные препараты. Кроме того, такие добавки, как карнитин и/или
коэнзим Q часто назначают, чтобы помочь контролировать
симптомы, вызванные митохондриальным расстройством. Врачи надеются на улучшение состояния пациента
качество жизни, управляя симптомами с помощью этих методов лечения.
Ключевые моменты, которые следует помнить
Ключевые моменты, которые следует помнить
- Митохондриальное заболевание возникает при повреждении митохондрий, которое истощает энергию клеток и, следовательно, истощает энергию организма.
- Большинство митохондриальных заболеваний поражают головной мозг, мышцы и желудочно-кишечный тракт, но могут поражаться и другие органы.
- Лекарства от митохондриальных заболеваний не существует. Однако лечение некоторыми лекарствами может помочь улучшить симптомы.

Службы поддержки и ресурсы
Службы поддержки и ресурсы
Посетите следующие веб-сайты, чтобы узнать больше о диагностике и лечении митохондриальных нарушений.
Райли из IU Health предлагает широкий спектр вспомогательных услуг, чтобы сделать жизнь лучше для семей, выбравших нас для ухода за своими детьми.
Узнайте больше об услугах поддержки Riley
Справочник по генетике
Этот онлайн-ресурс Национальной медицинской библиотеки США предоставляет дополнительную информацию о митохондриальных заболеваниях.
Объединенный фонд митохондриальных заболеваний
Объединенный фонд митохондриальных заболеваний предлагает поддержку и информацию, а также продвигает исследования по лечению митохондриальных заболеваний.
Места
Места
Местоположения
В дополнение к нашей основной больнице в Академическом медицинском центре в Индианаполисе, штат Индиана, у нас есть удобные места, чтобы лучше обслуживать наши сообщества по всему штату.
Сортировать по
3 объекта
предлагает Митохондриальные расстройства уход , введя свой город или почтовый индекс ниже.
Посмотреть все объекты →
Отделения, лечащие это заболевание
Отделения, занимающиеся этим заболеванием
Психологическое функционирование детей с подозрением на митохондриальное заболевание: необходимость наблюдения | Orphanet Journal of Rare Diseases
- Исследования
- Открытый доступ
- Опубликовано:
- Ким Ф. Э. ван де Лоо
Orcid: orcid.org/0000-0002-9030-8302 1 , - Хосе А. Э. Куристы 2 ,
- Saskia Koene 3,4 ,
- Inge-Lot Klein 2 ,
- Inge-Lot Klein 2 ,
- Inge-Lot Klein 2 ,
- . Янссен 5 ,
- Ян А. М. Смейтинк 6 и
- …
- Кристиан М. Верхаак 1
Orphanet Journal of Rare Diseases
том 15 , Номер статьи: 76 (2020)
Процитировать эту статью
1702 доступа
6 цитирований
Детали показателей
Abstract
История вопроса
Митохондриальные заболевания (МЗ) обычно представляют собой серьезные и прогрессирующие наследственные метаболические заболевания. Существует высокая коморбидность тревоги и депрессии, а также ограничения в повседневном функционировании. Сложность и длительность диагностического процесса и отсутствие знаний о прогнозе приводит к неопределенности. В этом исследовании мы исследовали психологическое благополучие детей с подозрением на МД и их родителей.
Существует высокая коморбидность тревоги и депрессии, а также ограничения в повседневном функционировании. Сложность и длительность диагностического процесса и отсутствие знаний о прогнозе приводит к неопределенности. В этом исследовании мы исследовали психологическое благополучие детей с подозрением на МД и их родителей.
Методы
Всего 122 ребенка с подозрением на БМ и их родители получили анкеты в рамках стандартного клинического обследования.
Результаты
Доверенный отчет родителей выявил более низкое качество жизни (КЖ) по сравнению с нормой и даже больше физических проблем по сравнению с хронически больными пациентами. Они также сообщали о большем количестве поведенческих проблем в целом и большем количестве проблем интернализации по сравнению с нормами. Наиболее частыми соматическими жалобами были утомляемость и боль. Родители не сообщали о повышенном уровне стресса в отношении воспитания детей и получали достаточную социальную поддержку. В конце диагностического процесса у 5,7% детей был установлен генетически подтвержденный диагноз МД, у 26% были обнаружены неубедительные отклонения в биоптатах мышц, у 54% не было поставлено никакого диагноза, а остальным были поставлены другие диагнозы. Поразительно, что у детей без диагноза качество жизни и поведенческие проблемы были такими же, как и у детей с диагнозом, и даже больше проблем с интернализацией.
В конце диагностического процесса у 5,7% детей был установлен генетически подтвержденный диагноз МД, у 26% были обнаружены неубедительные отклонения в биоптатах мышц, у 54% не было поставлено никакого диагноза, а остальным были поставлены другие диагнозы. Поразительно, что у детей без диагноза качество жизни и поведенческие проблемы были такими же, как и у детей с диагнозом, и даже больше проблем с интернализацией.
Выводы
Это исследование подчеркивает психологические проблемы детей с подозрением на БМ. Важно понимать, что так же, как и дети с подтвержденным диагнозом, дети без диагноза уязвимы, так как объяснение их жалоб до сих пор отсутствует.
Исходная информация
Митохондриальные заболевания (МЗ) — это редкие наследственные метаболические заболевания, которые могут проявляться любыми симптомами, в любом возрасте и при любом типе наследования [1]. Как правило, это тяжелые и прогрессирующие заболевания с непредсказуемым течением. Общая заболеваемость составляет примерно 1:5000 живорожденных [2, 3]. Митохондрии играют важную роль в производстве энергии в клетке. Органы с наибольшей потребностью в энергии, такие как мозг и мышцы, чаще всего поражаются [4]. Существует большое разнообразие генетического и биохимического участия, а также фенотипической экспрессии [5]. МД может быть вызвана мутацией в митохондриальной ДНК (мтДНК) или ядерной ДНК (яДНК). Диагноз МД ставится в несколько этапов; клиническая картина (жалобы, признаки и симптомы, наследование), клиническая биохимия, метаболические исследования, патологическая оценка, биохимическое и генетическое тестирование [6]. На сегодняшний день лекарства не существует.
Общая заболеваемость составляет примерно 1:5000 живорожденных [2, 3]. Митохондрии играют важную роль в производстве энергии в клетке. Органы с наибольшей потребностью в энергии, такие как мозг и мышцы, чаще всего поражаются [4]. Существует большое разнообразие генетического и биохимического участия, а также фенотипической экспрессии [5]. МД может быть вызвана мутацией в митохондриальной ДНК (мтДНК) или ядерной ДНК (яДНК). Диагноз МД ставится в несколько этапов; клиническая картина (жалобы, признаки и симптомы, наследование), клиническая биохимия, метаболические исследования, патологическая оценка, биохимическое и генетическое тестирование [6]. На сегодняшний день лекарства не существует.
Последствия наличия БМ очень важны для ребенка и его/ее родителей. Наиболее тягостными жалобами у детей являются быстрая утомляемость, нарушения поведения и речи, эпилепсия и мышечная слабость, высокая степень ограничений в повседневной деятельности [1]. Кроме того, тревога и депрессия распространены у детей с МД [7, 8], с еще более высокой коморбидностью по сравнению с детьми с другими видами врожденных нарушений обмена веществ и по сравнению с пациентами с синдромом Сотоса [8]. Серьезные ограничения, с которыми сталкиваются дети, и большая вариабельность клинических проявлений также оказывают сильное влияние на благополучие опекуна [9].]. Родители часто испытывают стресс и беспокойство [10, 11]. Родительский стресс выше, когда больше госпитализаций и более широкое использование специальных служб, а также когда вовлечено больше органов [11].
Серьезные ограничения, с которыми сталкиваются дети, и большая вариабельность клинических проявлений также оказывают сильное влияние на благополучие опекуна [9].]. Родители часто испытывают стресс и беспокойство [10, 11]. Родительский стресс выше, когда больше госпитализаций и более широкое использование специальных служб, а также когда вовлечено больше органов [11].
Кажется очевидным, что психологическое воздействие МД велико. Меньше известно о психологическом функционировании детей и их родителей, находящихся в диагностическом процессе. Диагностический процесс сложен и может занять годы между появлением первых симптомов и подтвержденным диагнозом [12]. Это длительное время, а также отсутствие знаний о диагностике приводит к неуверенности и стрессу [12]. Насколько нам известно, у детей и их родителей не проводилось исследований, посвященных психологическому благополучию в процессе диагностики. Основной целью настоящего исследования является изучение психологического благополучия детей с подозрением на БМ и их родителей.
Методы
Участники
Все родители детей (< 18 лет) с подозрением на МД, которым была проведена биопсия мышц в Центре митохондриальной медицины Радбауд (RCMM), Детская больница Амалии Радбудума в Неймегене (Нидерланды) в период с января 2010 г. и апрель 2019 года. Показания к биопсии мышц были определены на основании международных рекомендаций на момент оценки.
Процедура
Перед биопсией мышц родители получили анкеты в рамках стандартной программы медицинского обслуживания. Эта программа была начата в январе 2010 г., а включение закончилось в апреле 2019 г.. Родители должны были свободно владеть голландским языком, чтобы понимать анкеты. После заполнения анкет также были исследованы результаты окончательного диагноза (на основе исследований биопсии мышц, мтДНК и/или секвенирования всего экзома).
Материалы
Демографические факторы и характеристики заболеваний
Демографические характеристики и характеристики заболеваний, такие как продолжительность жалоб на здоровье и привлеченные специалисты, оценивались с помощью анкеты из 20 пунктов, заполняемой одним из родителей каждого ребенка.
Критерии исхода для детей
Качество жизни (КЖ) оценивали с помощью педиатрического опросника качества жизни (PedsQL) [13]. Был использован родительский прокси-отчет (дети в возрасте от 5 до 18 лет). Более высокий балл указывает на лучшее качество жизни, связанное со здоровьем [13].
Поведенческие проблемы ребенка оценивались с помощью Контрольного списка поведения ребенка (CBCL) (опросник, сообщаемый родителями) [14, 15]. CBCL предоставляет баллы по глобальным, внутренним и внешним поведенческим проблемам. CBCL делится на две возрастные категории: от 1,5 до 5 лет и от 6 до 18 лет. Имеющиеся нормы обеспечивают Т-показатели, стандартизированные по возрасту и полу ( М = 50; SD = 10). Суммарные, внутренние и внешние Т-баллы ≥60 и Т-баллы по синдромной шкале ≥65 представляют пограничный уровень, тогда как Т-баллы по шкале ≥64 и Т-баллы по синдромной шкале ≥70 представляют клинический диапазон в общей популяции [14, 15] .
Показатели исхода для родителей
Стресс у родителей оценивали с помощью Индекса стресса родителей (PSI), сокращенная версия (Nijmeegse Ouderlijke Stress Index NOSIK) [16]. Этот опросник оценивает стресс, который испытывают родители при воспитании ребенка в возрасте от 1 до 13 лет. Баллы были классифицированы как нормальные (у матерей < 74; у отцов < 64), субклинические (у матерей 74–89 баллов).; оценка отцов 64–78) и клинические уровни родительского стресса (оценка матерей > 89; оценка отцов > 78).
Этот опросник оценивает стресс, который испытывают родители при воспитании ребенка в возрасте от 1 до 13 лет. Баллы были классифицированы как нормальные (у матерей < 74; у отцов < 64), субклинические (у матерей 74–89 баллов).; оценка отцов 64–78) и клинические уровни родительского стресса (оценка матерей > 89; оценка отцов > 78).
Воспринимаемая родителями социальная поддержка оценивалась с помощью Опросника социальной уверенности (ISR) [17]. ISR оценивает сеть социальной поддержки родителей детей в возрасте от 0 до 18 лет. Общий балл использовался в качестве меры опытной социальной поддержки. Баллы выше 10 расценивались как нормальный/достаточный уровень социальной поддержки, 7–9 – низкий уровень, 6 и ниже – недостаточный уровень социальной поддержки [18].
Статистический анализ
Все статистические анализы проводились с использованием Статистического пакета для социальных наук (SPSS) для Windows версии 25.0 (IBM Corp., Армонк, Нью-Йорк). Нормальное распределение непрерывных данных оценивали с помощью критерия нормальности Шапиро-Уилка.
Показатели родительского отчета PedsQL сравнивались с использованием t-критерия одной выборки с нормальными показателями выборки здоровой популяции и выборки общего хронического состояния здоровья, определенных в Varni et al. (2006) как « состояние физического или психического здоровья, которое длилось или, как ожидается, продлится не менее 6 месяцев и мешает активности ребенка» [19].
Отчет родительского доверенного лица о поведенческих проблемах (CBCL) был оценен с различными возрастными версиями. Поскольку субшкалы обеих версий используют схожие концепции, мы использовали суммарный балл каждой концепции для расчетов, когда это было возможно. Был рассчитан процент поведенческих проблем выше клинического порога. Суммарные, интериоризированные и экстернализирующие проблемы сравнивались с нормами [14, 15]. Оценка депрессии в соматической популяции затруднена, поскольку жизненно важные аспекты депрессии также проявляются в виде симптомов соматических состояний (например, снижение активности). После оценки депрессии у взрослого населения [20] мы исключили из оценки депрессии пункты, относящиеся к жизненно важным функциям. Мы использовали как исходную шкалу (CBCL втянуто/депрессивно), так и скорректированную подшкалу (CBCL втянуто/депрессивно 9).0669 прил. ), в котором соматические элементы заменяются средним баллом остальных элементов подшкалы. Конкретные пункты соматических жалоб, которые также могли быть основными симптомами БМ, исследовались с использованием процентного отношения баллов по пунктам > 2. Критерии хи-квадрат, линейная ассоциация, использовались для изучения различий между детьми с диагнозом или без него в балльные пункты (0,1,2) соматических жалоб. В качестве индикатора возможных неудовлетворенных потребностей мы исследовали, сколько детей с поведенческими проблемами (общая клиническая оценка, шкала интернализации или экстернализации) получали поддержку от профильного специалиста, психолога или педагога по коррекции поведения.
После оценки депрессии у взрослого населения [20] мы исключили из оценки депрессии пункты, относящиеся к жизненно важным функциям. Мы использовали как исходную шкалу (CBCL втянуто/депрессивно), так и скорректированную подшкалу (CBCL втянуто/депрессивно 9).0669 прил. ), в котором соматические элементы заменяются средним баллом остальных элементов подшкалы. Конкретные пункты соматических жалоб, которые также могли быть основными симптомами БМ, исследовались с использованием процентного отношения баллов по пунктам > 2. Критерии хи-квадрат, линейная ассоциация, использовались для изучения различий между детьми с диагнозом или без него в балльные пункты (0,1,2) соматических жалоб. В качестве индикатора возможных неудовлетворенных потребностей мы исследовали, сколько детей с поведенческими проблемами (общая клиническая оценка, шкала интернализации или экстернализации) получали поддержку от профильного специалиста, психолога или педагога по коррекции поведения.
Различия между детьми с (МД, неопределенными аномалиями или другими диагнозами) и без диагноза исследовали с помощью t-критерия независимых выборок или, в случае ненормального распределения, U-критерия Манна-Уитни. Для анализа использовались представляющие интерес переменные (отчет матерей по общей шкале PedsQL, общий показатель CBCL, интернализация, экстернализация, тревога/депрессия, замкнутость/депрессия (прил.) , соматические жалобы, а также PSI и ISR отцов и матерей).
Для анализа использовались представляющие интерес переменные (отчет матерей по общей шкале PedsQL, общий показатель CBCL, интернализация, экстернализация, тревога/депрессия, замкнутость/депрессия (прил.) , соматические жалобы, а также PSI и ISR отцов и матерей).
Результаты
Демографические характеристики и характеристики заболеваний
Всего участвовало 122 ребенка и их родителей (таблица 1). Большинство детей предъявляли жалобы на здоровье более 3-х лет. Почти у 75% детей были задействованы один или несколько специалистов. Чаще всего привлекались физиотерапевты (55%), затем логопед и диетолог (оба по 28%). К психологу или коррекционному педагогу привлекались соответственно 17 и 11% всех детей.
Таблица 1 Демографические переменные и характеристики, связанные с болезнью/здоровьем
Полная таблица
Результаты биопсии мышц и дальнейшей диагностики (генетики) показывают, что 54,9% всех детей не получили никакого диагноза, и только 5,7% получили диагноз МД. У 26,2% детей в момент биопсии мышц и генетического анализа были обнаружены неубедительные отклонения. Остальным 12,3% были поставлены другие генетические диагнозы, и у одного пациента окончательный диагноз на сегодняшний день отсутствует.
У 26,2% детей в момент биопсии мышц и генетического анализа были обнаружены неубедительные отклонения. Остальным 12,3% были поставлены другие генетические диагнозы, и у одного пациента окончательный диагноз на сегодняшний день отсутствует.
Исходы для детей
Качество жизни
Прокси-отчет родителей выявил более низкое качество жизни в целом и по всем субшкалам по сравнению с населением в целом (таблица 2). По сравнению с другими пациентами с хроническим заболеванием, отцы и матери также сообщали о большем количестве проблем с физическим функционированием у своих детей, а матери также о более низком качестве жизни в целом. Напротив, отцы сообщили о лучшем социальном функционировании своих детей по сравнению с другими пациентами с хроническими заболеваниями.
Таблица 2 Качество жизни детей по словам их родителей (PedsQL)
Полноразмерная таблица
Поведение ребенка
Средние баллы, стандартные отклонения, а также процентные баллы в клиническом диапазоне CBCL описаны в Таблице 3. И матери, и отцы сообщали о более высоких баллах по общей шкале (Mothers X 2 [1]=12,67, p = .000, отцы X 2 [1]=8,65, p = .003) и другие проблемы интернализации (Матери X 2 [1,72]=138 p = .000, отцы X 2 [1]=57,32, p = .000) в клиническом диапазоне по сравнению с нормой.
И матери, и отцы сообщали о более высоких баллах по общей шкале (Mothers X 2 [1]=12,67, p = .000, отцы X 2 [1]=8,65, p = .003) и другие проблемы интернализации (Матери X 2 [1,72]=138 p = .000, отцы X 2 [1]=57,32, p = .000) в клиническом диапазоне по сравнению с нормой.
Таблица 3 Поведенческие проблемы ребенка по словам их родителей (CBCL)
Полная таблица
В общей сложности 12,3% детей демонстрируют замкнутое/депрессивное поведение по словам их матерей и 13,3% по словам их отцов. При поправке на неоднозначные пункты, которые одновременно нагружают замкнутость/депрессию, а также симптомы болезни, поведение ребенка было оценено как замкнутость/депрессия у 7,0% (сообщение матерей) и 4,8% (сообщение отцов) детей. Баллы по скорректированной шкале замкнутости/депрессии были значительно ниже, что указывает на меньшее беспокойство, после поправки на соматические элементы у обеих матерей (t(113) = − 9. 57, p = .000) и отчет отцов (t(82) = − 7,11, p = .000).
57, p = .000) и отчет отцов (t(82) = − 7,11, p = .000).
Наиболее частыми соматическими жалобами были усталость (матери сообщают: 51,9%, отцы сообщают: 40,7%) и боль (матери сообщают: 34,2%, отцы сообщают: 27,7%).
Всего у 52 из 113 детей были обнаружены поведенческие проблемы по одной из шкал (общие, интернализирующие или экстернализирующие), из которых 9 (17%) получали помощь психолога или коррекционного педагога.
Показатели результатов для родителей
Родительский стресс
По сравнению с клинической популяцией и отцы, и матери сообщали о меньшем родительском стрессе. Матери также сообщали о меньшем родительском стрессе по сравнению с немедицинским населением. Не было существенной разницы между отцами и матерями в отношении родительского стресса (t(67) = − 0,46, p = 0,649). В общей сложности 5,9% матерей испытывали родительский стресс в клинических пределах и 11,1% отцов (таблица 4).
Таблица 4 Показатели результатов для родителей: родительский стресс (PSI) и социальная поддержка (ISR)
Полноразмерный стол
Социальная поддержка
И матери, и отцы получали большую социальную поддержку по сравнению с нормой [17] и большую социальную поддержку по сравнению с пациентами с ревматоидным артритом [18] (таблица 4). Всего 98,2% матерей и 97,8% отцов получали достаточную социальную поддержку.
Всего 98,2% матерей и 97,8% отцов получали достаточную социальную поддержку.
Сравнение детей с диагнозом психологического функционирования и без него
Не было различий между детьми с любым диагнозом и без диагноза в КЖ (отчет матерей: t(81) = −0,806, p = .422) или в целом или внешних поведенческих проблемах (см. Таблицу 3). Что касается внутренних поведенческих проблем, матери сообщали о большем количестве проблем у своих детей без диагноза (средний Т-балл = 61,35) по сравнению с детьми с диагнозом (средний Т-балл = 56,36). Различий между детьми с диагнозом и без него по количеству соматических жалоб, за исключением головной боли, не было. Матери детей без диагноза сообщают о большем количестве жалоб на головную боль у своего ребенка по сравнению с детьми с диагнозом.
Не было существенных различий между группами с диагнозом родительского стресса или без него (матери t(82) = −0,626, p = 0,533, отцы t(69) = 0,246, p = . 806) и социальной поддержки (матери t(108) = −0,447, p = 0,665, отцы t(86) = 1,134, p = 0,260).
Обсуждение
Насколько нам известно, это первое исследование, посвященное психологическому благополучию детей, находящихся в процессе диагностики подозреваемого БМ, и их родителей. В целом, результаты показали существенные проблемы в психологическом функционировании ребенка, в то время как родители не сообщают о повышенном уровне родительского стресса или отсутствии социальной поддержки.
Родительский прокси-отчет выявил более низкое КЖ по всем направлениям по сравнению с нормой, что согласуется с исследованиями взрослых пациентов с доказанным МД [21, 22]. У детей также было больше проблем с физическим функционированием по сравнению с детьми с другими общими хроническими заболеваниями, что указывает на серьезные нарушения.
Что касается поведенческих проблем, по сравнению с нормой, родители сообщали о большем количестве проблем в целом и о большем количестве проблем интернализации конкретно у их ребенка, что согласуется с другими литературными данными о детях с хроническими заболеваниями [23]. Хотя как общая шкала CBCL, так и шкала интернализации включают соматические элементы, метаанализ [23] показал, что повышенные уровни обеих шкал остаются после учета смешанных аспектов элементов, связанных с соматическим состоянием. Удивительно, но дети без диагноза демонстрировали больше проблем интернализации по сравнению с детьми с диагнозом, что указывает на высокую потребность в помощи у этих детей. Основываясь на результатах этого исследования, мы не можем объяснить эти выводы. Механизмы, лежащие в основе поведенческих проблем, могут различаться в этих группах и должны быть изучены в будущих исследованиях.
Хотя как общая шкала CBCL, так и шкала интернализации включают соматические элементы, метаанализ [23] показал, что повышенные уровни обеих шкал остаются после учета смешанных аспектов элементов, связанных с соматическим состоянием. Удивительно, но дети без диагноза демонстрировали больше проблем интернализации по сравнению с детьми с диагнозом, что указывает на высокую потребность в помощи у этих детей. Основываясь на результатах этого исследования, мы не можем объяснить эти выводы. Механизмы, лежащие в основе поведенческих проблем, могут различаться в этих группах и должны быть изучены в будущих исследованиях.
Как упоминалось ранее, тревога и депрессия часто встречаются у детей с МД [7, 8], что предполагает возможную связь с нарушением энергетического метаболизма центральной нервной системы [7]. Это исследование также показало высокий процент тревожного/депрессивного поведения и замкнутого/депрессивного поведения. После коррекции возможных соматических симптомов процент жалоб на замкнутость/депрессию значительно снизился. Кроме того, мы не обнаружили никаких различий между детьми с диагнозом или без него. Объяснение может заключаться в том, что жалобы на замкнутость/депрессию могут быть не только присущи болезни, но также могут быть связаны с другими факторами, например, присущими длительному анамнезу специфических соматических жалоб.
Кроме того, мы не обнаружили никаких различий между детьми с диагнозом или без него. Объяснение может заключаться в том, что жалобы на замкнутость/депрессию могут быть не только присущи болезни, но также могут быть связаны с другими факторами, например, присущими длительному анамнезу специфических соматических жалоб.
Известно, что подшкалу соматических жалоб CBCL трудно интерпретировать у детей с хроническим заболеванием, поскольку элементы могут пересекаться со специфическими симптомами заболевания [23, 24]. На уровне пунктов результаты выявили удивительно высокий процент усталости и боли у детей с подозрением на БМ, которые также являются основными симптомами заболевания. Различий по этим пунктам между детьми с диагнозом и детьми без диагноза не было. Удивительно, но дети без диагноза чаще предъявляли жалобы на головную боль, что свидетельствует об изнурительных соматических проблемах в этой группе.
Вопреки тому, что ожидалось [10, 11], большинство родителей не сообщали о родительском стрессе, а матери сообщали о еще меньшем родительском стрессе по сравнению с населением в целом. Хотя не было обнаружено никакой разницы между родителями детей с диагнозом или без него, в этом исследовании изучался родительский стресс до постановки диагноза, а не после него. Диагноз МД приносит, например. больше госпитализаций и более широкое использование специальных медицинских услуг, что коррелирует с более высоким родительским стрессом [12]. Важно отметить, что измерения и, следовательно, концепции родительского стресса различались между исследованиями. Другим объяснением может быть то, что родители в нашем исследовании получали достаточную социальную поддержку со стороны своего окружения, что рассматривается как здоровое копинг-поведение, связанное с меньшим родительским стрессом [11]. Наконец, нахождение на этапе диагностики также может повлиять на количество сообщений о проблемах. Возможно, благополучие ребенка является сутью вопроса во время оценки, и родители интерпретируют поведение своего ребенка в свете возможного заболевания и, следовательно, не столько как «стрессовое», а скорее в свете сострадания и сочувствия.
Хотя не было обнаружено никакой разницы между родителями детей с диагнозом или без него, в этом исследовании изучался родительский стресс до постановки диагноза, а не после него. Диагноз МД приносит, например. больше госпитализаций и более широкое использование специальных медицинских услуг, что коррелирует с более высоким родительским стрессом [12]. Важно отметить, что измерения и, следовательно, концепции родительского стресса различались между исследованиями. Другим объяснением может быть то, что родители в нашем исследовании получали достаточную социальную поддержку со стороны своего окружения, что рассматривается как здоровое копинг-поведение, связанное с меньшим родительским стрессом [11]. Наконец, нахождение на этапе диагностики также может повлиять на количество сообщений о проблемах. Возможно, благополучие ребенка является сутью вопроса во время оценки, и родители интерпретируют поведение своего ребенка в свете возможного заболевания и, следовательно, не столько как «стрессовое», а скорее в свете сострадания и сочувствия. Было бы интересно отслеживать родительский стресс после диагностического процесса, особенно при отсутствии диагноза, чтобы исследовать влияние возможного заболевания на восприятие родительского стресса.
Было бы интересно отслеживать родительский стресс после диагностического процесса, особенно при отсутствии диагноза, чтобы исследовать влияние возможного заболевания на восприятие родительского стресса.
В этой когорте пациентов с подозрением на БМ 7 из 122 детей получили генетически подтвержденный диагноз, в то время как у 26% детей были обнаружены неубедительные аномалии в биопсии мышц без еще подтвержденной генетической мутации. При интерпретации этих результатов важно помнить, что это исследование началось в 2011 году, и с тех пор доступные генетические знания и инструменты диагностики митохондриальных заболеваний заметно улучшились. Несмотря на это, все еще существует несколько ограничений в диагностических шагах, необходимых для постановки диагноза, среди которых недостаточное понимание роли всего генома в митохондриальной функции [25]. Мы ожидаем, что у некоторых детей с наблюдаемыми неубедительными отклонениями в биопсии мышц будущие исследования выявят патогенные мутации. Однако для других они могут быть не обнаружены, например, из-за негенетические внешние факторы, препятствующие правильному функционированию митохондрий, такие как неиспользование мышц.
Однако для других они могут быть не обнаружены, например, из-за негенетические внешние факторы, препятствующие правильному функционированию митохондрий, такие как неиспользование мышц.
В конце диагностического процесса, не ограничиваясь только митохондриальным заболеванием, более половины пациентов не получили никакого диагноза, объясняющего их изнурительные жалобы. Учитывая тот факт, что мы обнаружили, что у этих детей такое же количество психологических проблем и физических жалоб, как и у детей с диагнозом, и даже больше беспокойства, связанного с проблемами интернализации и головной болью, эти дети особенно уязвимы. В Нидерландах эти пациенты автоматически не имеют такого же доступа к медицинской помощи, как пациенты с подтвержденным диагнозом, поскольку они не вписываются в стандартную программу лечения. Мы настоятельно рекомендуем этим детям пройти скрининг на наличие психологических проблем и обеспечить доступ к необходимой им помощи.
Наличие ребенка с серьезными необъяснимыми жалобами ставит родителей детей с редким заболеванием в серьезную неуверенность. Неопределенность в отношении состояния здоровья особенно характерна для неоднозначных, сложных и непредсказуемых ситуаций [26], что применимо к жалобам детей в данном исследовании. Отсутствие диагноза оставляет пациентов и родителей с еще большей неуверенностью. Исследования влияния редких заболеваний на детей и их родителей подчеркивают влияние длительного диагностического процесса и задержки диагностики [27, 28]. Этот длительный период может серьезно сказаться на здоровье детей и их семей. Не только из-за того, что возможные потребности в медицинской помощи остаются неудовлетворенными, но и из-за влияния неопределенности в отношении здоровья ребенка и поиска диагностики и адекватной помощи, это является серьезным бременем. Поставщики медицинских услуг могли бы направлять родителей по возможным дополнительным диагностическим траекториям, поддерживая их в преодолении неопределенности и сосредоточив внимание на аспектах своей жизни, которые они могут контролировать. В этом документе подчеркивается важность того, чтобы эти дети и их родители были в центре нашего внимания.
Неопределенность в отношении состояния здоровья особенно характерна для неоднозначных, сложных и непредсказуемых ситуаций [26], что применимо к жалобам детей в данном исследовании. Отсутствие диагноза оставляет пациентов и родителей с еще большей неуверенностью. Исследования влияния редких заболеваний на детей и их родителей подчеркивают влияние длительного диагностического процесса и задержки диагностики [27, 28]. Этот длительный период может серьезно сказаться на здоровье детей и их семей. Не только из-за того, что возможные потребности в медицинской помощи остаются неудовлетворенными, но и из-за влияния неопределенности в отношении здоровья ребенка и поиска диагностики и адекватной помощи, это является серьезным бременем. Поставщики медицинских услуг могли бы направлять родителей по возможным дополнительным диагностическим траекториям, поддерживая их в преодолении неопределенности и сосредоточив внимание на аспектах своей жизни, которые они могут контролировать. В этом документе подчеркивается важность того, чтобы эти дети и их родители были в центре нашего внимания.
При исследовании удовлетворенных потребностей всех включенных детей, с диагнозом или без него, только 17% детей с поведенческими проблемами получили помощь специалиста по детскому поведению, а 73% детей, нуждающихся в помощи, были исключены. Включив в диагностические процедуры оценку психологического здоровья, желательно с помощью стандартных опросников, и психолога, адекватная помощь может быть оказана на ранней стадии.
При интерпретации вышеупомянутых результатов важно учитывать сильные стороны и ограничения. Сильной стороной является относительно большой размер выборки. Во-вторых, при скрининге в начале диагностического процесса, до постановки диагноза, на воспринимаемые жалобы не влияло знание того, есть ли у них заболевание или нет. Ограничением является большой временной отрезок данного исследования, поскольку диагностические критерии и возможности были усовершенствованы. Кроме того, из-за возрастных ограничений различных анкет не все пациенты и родители заполняли одинаковые анкеты. Наконец, поскольку все пациенты заполнили анкеты в рамках стандартного лечения, нет информации, например, о. была доступна утомляемость у детей в возрасте <6 лет, которая является основной жалобой на MD у детей [1].
Наконец, поскольку все пациенты заполнили анкеты в рамках стандартного лечения, нет информации, например, о. была доступна утомляемость у детей в возрасте <6 лет, которая является основной жалобой на MD у детей [1].
Выводы
Это исследование подчеркивает психологические проблемы детей с подозрением на БМ. Важно знать об этих проблемах на ранней стадии и оказывать адекватную помощь независимо от окончательного диагноза. Особенно уязвимы дети без подтвержденного диагноза, поскольку они остаются в неопределенности и не вписываются в стандартную программу специального ухода.
Доступность данных и материалов
Набор данных, использованный в ходе настоящего исследования, можно получить у соответствующего автора по обоснованному запросу.
Сокращения
- CBCL:
Контрольный список поведения ребенка
- ISR:
Инвентарь социального обеспечения
- МД:
Митохондриальные болезни
- мтДНК:
Митохондриальная ДНК
- нДНК:
Ядерная ДНК
- НОСИК:
Индекс стресса Nijmeegse Ouderlijke
- PedsQL:
Педиатрическая инвентаризация качества жизни
- Качество жизни:
Качество жизни
- RCMM:
Радбаудский центр митохондриальной медицины
- SPSS:
Статистический пакет для социальных наук
Ссылки
- «>
Парих С., Гольдштейн А., Караа А., Кениг М.К., Ансельм И., Брунел-Гиттон С. и др. Стандарты ухода за пациентами при первичном митохондриальном заболевании: консенсусное заявление общества митохондриальной медицины. Генет Мед. 2017; 19:1–18.
Шефер А.М., Тейлор Р.В., Тернбулл Д.М., Чиннери П.Ф. Эпидемиология митохондриальных расстройств — прошлое, настоящее и будущее. Биохим Биофиз Акта. 1659;2004:115–20.
Google ученый
Купман В.Дж., Виллемс П.Х., Смейтинк Дж.А. Моногенные митохондриальные нарушения.
 N Engl J Med. 2012; 366:1132–41.
N Engl J Med. 2012; 366:1132–41.КАС
СтатьяGoogle ученый
Смейтинк Дж.А., Зевиани М., Тернбулл Д.М., Джейкобс Х.Т. Митохондриальная медицина: метаболический взгляд на патологию нарушений окислительного фосфорилирования. Клеточный метаб. 2006;3:9–13.
КАС
СтатьяGoogle ученый
Парих С., Гольдштейн А., Кениг М.К., Скалья Ф., Эннс Г.М., Сането Р. и др. Диагностика и лечение митохондриальных заболеваний: консенсусное заявление общества митохондриальной медицины. Генет Мед. 2015; 17: 689–701.
КАС
СтатьяGoogle ученый
Koene S, Kozicz TL, Rodenburg RJ, Verhaak CM, de Vries MC, Wortmann S, et al. Большая депрессия у детей-подростков с последовательным диагнозом митохондриального расстройства. J Аффективное расстройство. 2009 г.
 ;114:327–32.
;114:327–32.КАС
СтатьяGoogle ученый
Morava E, Gardeitchik T, Kozicz T, de Boer L, Koene S, de Vries MC, et al. Депрессивное поведение у детей с диагнозом митохондриальное расстройство. Митохондрия. 2010; 10: 528–33.
КАС
СтатьяGoogle ученый
Софу К. Митохондриальная болезнь: проблема для лиц, осуществляющих уход, семьи и общества. J Чайлд Нейрол. 2013;28:663–7.
Артикул
Google ученый
Чтение CY. Требования биохимических генетических нарушений: обследование матерей детей с митохондриальной болезнью или фенилкетонурией. J Педиатр Нурс. 2003; 18:181–186.
Артикул
Google ученый
Сенгер Б.А., Уорд Л.Д., Барбоза-Лейкер С., Биндлер Р.С. Стресс и совладание родителей, ухаживающих за ребенком с митохондриальным заболеванием.
 Appl Nurs Res. 2016;29: 195–201.
Appl Nurs Res. 2016;29: 195–201.Артикул
Google ученый
Сенгер Б.А., Уорд Л.Д., Барбоза-Лейкер С., Биндлер Р.С. Опыт родителей по уходу за ребенком с митохондриальным заболеванием. J Педиатр Нурс. 2016;31:32–41.
Артикул
Google ученый
Варни Дж.В., Сейд М., Куртин П.С. PedsQL 4.0: надежность и валидность базовых шкал Педиатрического опросника качества жизни версии 4.0 для здоровых и пациентов. Мед уход. 2001;39: 800–12.
КАС
СтатьяGoogle ученый
Achenbach TM, Rescorla LA. Руководство для дошкольных форм и профилей ASEBA. Берлингтон: Исследовательский центр для детей, молодежи и семей Университета Вермонта; 2000.
Google ученый
Achenbach TM, Rescorla LA.
 Пособие по формам и профилям школьного возраста ASEBA. Берлингтон: Исследовательский центр для детей, молодежи и семей Университета Вермонта; 2001.
Пособие по формам и профилям школьного возраста ASEBA. Берлингтон: Исследовательский центр для детей, молодежи и семей Университета Вермонта; 2001.Google ученый
De Brock AJLL, Vermulst AA, Gerris JRM, Abidin RR. NOSI, индекс стресса Nijmeegse ouderlijke. Lisse: Swets & Zeitlinger; 1992.
Google ученый
Van Dam-Baggen R, Kraaimaat F. De inventarisatieliijst sociale betrokkenheid (ISB): Een zelfbeoordelingslijst om sociale steun te meten. Гедрагстерапия. 1992; 25: 27–46.
Google ученый
Huiskes CJAE, Kraaimaat FW, Bijlsma JWJ. IRGL, привлеченный van reuma op gezondheid en leefwijze. Zelfbeoordelingslijst. St Radboud, Неймеген: Afdeling Medische Psychologie, Universitair Medisch Centrum; 2004.
Google ученый
«>Бек А.Т., Гут Д., Стир Р.А., Болл Р. Скрининг больших депрессивных расстройств у стационарных больных с помощью перечня депрессии Бека для первичной медико-санитарной помощи. Behav Res Ther. 1997; 35: 785–91.
КАС
СтатьяGoogle ученый
Custers JAE, de Laat P, Koene S, Smeitink J, Janssen MCH, Verhaak C. Страх перед прогрессированием заболевания у носителей мутации m.3243A > G. Orphanet J Rare Dis. 2018;13:203.
Артикул
Google ученый
Verhaak C, de Laat P, Koene S, Tibosch M, Rodenburg R, de Groot I, et al. Качество жизни, утомляемость и психическое здоровье у пациентов с мутацией m.
 3243A > G и ее связь с генетическими особенностями и манифестацией заболевания. Orphanet J Rare Dis. 2016;11:25.
3243A > G и ее связь с генетическими особенностями и манифестацией заболевания. Orphanet J Rare Dis. 2016;11:25.Артикул
Google ученый
Pinquart M, Shen Y. Поведенческие проблемы у детей и подростков с хроническими соматическими заболеваниями: метаанализ. J Pediatr Psychol. 2011;36:1003–16.
Артикул
Google ученый
Perrin EC, Stein RE, Drotar D. Меры предосторожности при использовании контрольного списка поведения детей: наблюдения, основанные на исследованиях детей с хроническими заболеваниями. J Pediatr Psychol. 1991; 16: 411–21.
КАС
СтатьяGoogle ученый
Парих С., Караа А., Гольдштейн А., Бертини Э.С., Чиннери П.Ф., Христодулу Дж. и др. Диагностика «возможного» митохондриального заболевания: экзистенциальный кризис. J Med Genet.
 2019;56:123–30.
2019;56:123–30.КАС
СтатьяGoogle ученый
Мишель М.Х. Теории неопределенности в болезни. В: Smith MJ, Liehr PR, редакторы. Теория среднего диапазона для сестринского дела. 3-е изд. Нью-Йорк: Springer Publishing Company, LLC; 2014. с. 53–86.
Google ученый
Андерсон М., Эллиотт Э.Дж., Зурински Ю.А. Австралийские семьи, живущие с редкими заболеваниями: опыт диагностики, использования медицинских услуг и потребности в психосоциальной поддержке. Orphanet J редкий дис. 2013;8:22.
Артикул
Google ученый
Zurynski Y, Deverell M, Dalkeuth T, Johnson S, Christodoulou J, Leonard H. Австралийские дети, живущие с редкими заболеваниями: опыт диагностики и предполагаемые последствия задержек диагностики. Orphanet J редкий дис. 2017;12:86.
Артикул
Google ученый
Koene S, Wortmann SB, de Vries MC, Jonckheere AI, Morava E, de Groot IJ, et al. Разработка показателей исходов для педиатрических митохондриальных расстройств: какие жалобы и ограничения наиболее обременительны для пациентов и их родителей? Митохондрия. 2013;13:15–24.
КАС
Статья
Google ученый
Varni JW, Burwinkle TM, Seid M. PedsQL 4.0 как показатель здоровья школьников: осуществимость, надежность и достоверность. Качество жизни Res. 2006; 15: 203–15.
Артикул
Google ученый
Ссылки на скачивание
Благодарности
Авторы благодарят Лиду Набуурс, Моник Хенсельманс, Лауру Вербек, Марион Херманс-Петерс, Лоннеке де Бур и Маайке де Врис за их вклад в уход за пациентами и сбор данных.
Финансирование
Внешнее финансирование отсутствует.
Информация об авторе
Авторы и организации
Институт наук о здоровье Радбуда, отделение медицинской психологии, Центр митохондриальной медицины Радбуда, Детская больница Амалия, Медицинский центр Университета Радбауд, Герт Грутеплейн Зюйд 10, П.О. Вставка 9101, 6500HB, Неймеген, Нидерланды
Ким Ф. Э. ван де Лу и Кристианна М. Верхаак
Институт медицинских наук Радбуда, кафедра медицинской психологии, Центр митохондриальной медицины Радбуда, Медицинский центр Университета Радбуда, Неймеген, Нидерланды
José A. E. Custers & Inge-Lot Klein
Отделение педиатрии, Центр митохондриальной медицины Радбауд, Медицинский центр Университета Радбауд, Неймеген, Нидерланды
Saskia Koene
Кафедра клинической генетики, Медицинский центр Лейденского университета, Неймеген, Нидерланды
Saskia Koene
Институт молекулярных наук о жизни Радбуда, кафедра внутренней медицины, Университет Радбауда, Митохондриальный центр Медицинский центр, Неймеген, Нидерланды
Mirian C.
 H. Janssen
H. JanssenИнститут молекулярных наук о жизни Радбуда, кафедра педиатрии, Центр митохондриальной медицины Радбуда, Медицинский центр Университета Радбуда, Неймеген, Нидерланды
Ян А. М. Смейтинк
Авторы
- Ким Ф. Э. ван де Лоо
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - José A. E. Custers
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Saskia Koene
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - Inge-Lot Klein
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Mirian CH Janssen
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Ян А.
 М. Смейтинк
М. СмейтинкПросмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия - Christianne M. Verhaak
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Contributions
KvdL участвовал в разработке концепции и дизайна, сборе данных, анализе и интерпретации, а также в подготовке статьи. JC участвовал в разработке концепции и дизайна исследования, анализа и интерпретации, а также критически рассмотрел рукопись. SK, IK, MJ и JS участвовали в разработке концепции и дизайна исследования, интерпретации результатов и критически рецензировали рукопись. CV участвовал в разработке концепции и дизайна исследования, сборе данных, анализе и интерпретации, а также критически рецензировал рукопись. Все авторы прочитали и одобрили окончательный вариант рукописи.
Автор, ответственный за переписку
Переписка с
Ким Ф. Э. ван де Лу.
Э. ван де Лу.
Декларация этики
Утверждение этики и согласие на участие
Настоящее исследование не подпадает под действие Закона о медицинских исследованиях с участием человека (ВМО). Исследование было рассмотрено комитетом по этике на основе Голландского кодекса поведения в области медицинских исследований, Голландского кодекса поведения для ответственного использования, Закона Нидерландов о защите персональных данных и Закона о соглашении о лечении. Комитет по этике вынес положительное заключение об исследовании.
Пациенты получали анкеты как стандартное лечение, лечение как обычно. Никаких дополнительных анкет для целей настоящего исследования не предоставлялось. Никакого вмешательства не последовало.
Согласие на публикацию
Неприменимо.
Конкурирующие интересы
Это исследование не спонсировалось промышленностью. KvdL, JC, SK, IK, MJ и CV не сообщают о раскрытии информации. Профессор Ян Смейтинк является генеральным директором-основателем Khondrion BV.
Дополнительная информация
Примечание издателя
Springer Nature сохраняет нейтралитет в отношении юрисдикционных претензий в опубликованных картах и институциональной принадлежности.
Права и разрешения
Открытый доступ Эта статья находится под лицензией Creative Commons Attribution 4.0 International License, которая разрешает использование, совместное использование, адаптацию, распространение и воспроизведение на любом носителе или в любом формате, при условии, что вы укажете соответствующую ссылку на оригинальный автор(ы) и источник, предоставьте ссылку на лицензию Creative Commons и укажите, были ли внесены изменения. Изображения или другие сторонние материалы в этой статье включены в лицензию Creative Commons на статью, если иное не указано в кредитной строке материала. Если материал не включен в лицензию Creative Commons статьи, а ваше предполагаемое использование не разрешено законом или выходит за рамки разрешенного использования, вам необходимо получить разрешение непосредственно от правообладателя. Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Чтобы просмотреть копию этой лицензии, посетите http://creativecommons.org/licenses/by/4.0/. Отказ Creative Commons от права на общественное достояние (http://creativecommons.org/publicdomain/zero/1.0/) применяется к данным, представленным в этой статье, если иное не указано в кредитной линии данных.
Перепечатки и разрешения
Об этой статье
повседневные мероприятия для детей с митохондриальным расстройством: ретроспективная обзор диаграммы
на этой странице
AbstractIntroductionmethodSresultsDiscusionConclusionConflicts offectAckNowledgmentsCopyRightReLIGUSCIONCONCONCONCONCONFLICTS 9005.
050505050505050505050505050505050505050505050505050505.comertcopyrichuscusionConclusionConconconConsConflicts. Участие в повседневной деятельности важно для здоровья и благополучия детей. У детей с митохондриальными нарушениями нарушена выработка энергии, что приводит к ограничению активности. Неизвестно, какую деятельность выполняют эти дети и отличается ли характер деятельности низкофункциональных детей от среднефункциональных детей. Таким образом, в этом пилотном исследовании изучалась деятельность, зарегистрированная в историях болезни гетерогенной группы детей с генетически подтвержденными митохондриальными нарушениями. Методы . Ретроспективный качественный направленный контент-анализ, проведенный медицинскими работниками, показал действия (в рамках их профессиональных обязанностей по обоснованию) в медицинских картах пациентов с детьми с митохондриальными расстройствами. Результаты . Семнадцать историй болезни пациентов, содержащие записи о способностях и выполняемых действиях, содержали обзор повседневной деятельности, охватывающей следующие категории: уход за собой, домашние дела, терапия, школа, работа на компьютере, хобби, игры, спорт и мобильность/транспорт. Категории активности детей с низким уровнем функционирования не отличались от детей со средним уровнем функционирования, хотя описания конкретных видов деятельности различались между группами. Заключение . Это экспериментальное исследование показывает, что виды деятельности, которые выполняют дети с митохондриальными нарушениями, не обязательно связаны с нарушениями у ребенка.
Таким образом, в этом пилотном исследовании изучалась деятельность, зарегистрированная в историях болезни гетерогенной группы детей с генетически подтвержденными митохондриальными нарушениями. Методы . Ретроспективный качественный направленный контент-анализ, проведенный медицинскими работниками, показал действия (в рамках их профессиональных обязанностей по обоснованию) в медицинских картах пациентов с детьми с митохондриальными расстройствами. Результаты . Семнадцать историй болезни пациентов, содержащие записи о способностях и выполняемых действиях, содержали обзор повседневной деятельности, охватывающей следующие категории: уход за собой, домашние дела, терапия, школа, работа на компьютере, хобби, игры, спорт и мобильность/транспорт. Категории активности детей с низким уровнем функционирования не отличались от детей со средним уровнем функционирования, хотя описания конкретных видов деятельности различались между группами. Заключение . Это экспериментальное исследование показывает, что виды деятельности, которые выполняют дети с митохондриальными нарушениями, не обязательно связаны с нарушениями у ребенка. Однако, по-видимому, существуют различия в уровнях независимости, использовании вспомогательных устройств и затратах на электроэнергию. Будущие исследования должны быть посвящены точке зрения ребенка и значению деятельности.
Однако, по-видимому, существуют различия в уровнях независимости, использовании вспомогательных устройств и затратах на электроэнергию. Будущие исследования должны быть посвящены точке зрения ребенка и значению деятельности.
1. Введение
Выполнение повседневных дел рассматривается как важный фактор благополучия человека и важная детерминанта здоровья [1–3]. Если дети не могут заниматься повседневными делами, они не имеют возможности исследовать окружающую среду и в меньшей степени способны расти как уникальные личности [4]. Хотя дети с ограниченными возможностями могут заниматься теми же видами деятельности и иметь те же желания, что и их здоровые развивающиеся сверстники [5, 6], они могут испытывать ограничения в деятельности, что приводит к ограничению их участия в повседневной жизни.
Митохондриальные нарушения, распространенность которых составляет 23 случая на 100 000, являются одними из наиболее частых наследственных нарушений метаболизма [7]. Митохондриальные нарушения могут быть вызваны мутацией генов, кодируемых ядерной ДНК (яДНК) или митохондриальной ДНК (мтДНК) [8]. Мутации были идентифицированы в более чем 230 различных генах [8, 9], и число идентифицированных генов, связанных с митохондриальными нарушениями, постоянно увеличивается [10]. Эта генетическая гетерогенность также отражается в клинических фенотипах, связанных с митохондриальными нарушениями, с большим спектром симптомов и нарушений [11–13]. Ранее было установлено, что дети (когда в данной статье мы говорим о детях, имеем в виду детей и подростков в возрасте от 0 до 18 лет) с митохондриальными нарушениями менее физически активны и меньше занимаются активной деятельностью по сравнению со здоровыми сверстниками [14]. . Дети с митохондриальным расстройством испытывают эти ограничения в выполнении повседневной деятельности из-за двигательных и когнитивных нарушений, включая мышечную слабость, проблемы с равновесием, проблемы с концентрацией внимания и умственную отсталость [13]. Эти нарушения имеют последствия для повседневной жизнедеятельности и участия. Степень предполагаемых ограничений в деятельности и участии детей с митохондриальными нарушениями варьируется от нулевой до чрезвычайно высокой [13].
Мутации были идентифицированы в более чем 230 различных генах [8, 9], и число идентифицированных генов, связанных с митохондриальными нарушениями, постоянно увеличивается [10]. Эта генетическая гетерогенность также отражается в клинических фенотипах, связанных с митохондриальными нарушениями, с большим спектром симптомов и нарушений [11–13]. Ранее было установлено, что дети (когда в данной статье мы говорим о детях, имеем в виду детей и подростков в возрасте от 0 до 18 лет) с митохондриальными нарушениями менее физически активны и меньше занимаются активной деятельностью по сравнению со здоровыми сверстниками [14]. . Дети с митохондриальным расстройством испытывают эти ограничения в выполнении повседневной деятельности из-за двигательных и когнитивных нарушений, включая мышечную слабость, проблемы с равновесием, проблемы с концентрацией внимания и умственную отсталость [13]. Эти нарушения имеют последствия для повседневной жизнедеятельности и участия. Степень предполагаемых ограничений в деятельности и участии детей с митохондриальными нарушениями варьируется от нулевой до чрезвычайно высокой [13]. В то время как некоторые дети остаются в общеобразовательной школе и достигают нормальных результатов, другие практически не взаимодействуют с окружающей средой [15].
В то время как некоторые дети остаются в общеобразовательной школе и достигают нормальных результатов, другие практически не взаимодействуют с окружающей средой [15].
Хотя в литературе утверждается, что дети с митохондриальным расстройством испытывают ограничения в деятельности, четкого представления об их повседневной деятельности нет. Обычно ожидается, что характер деятельности различается в зависимости от глобального функционирования ребенка. Знание этих возможных различий и сходств важно для выбора или разработки оценок для этой группы населения, для оценки результатов лечения при участии, а также для адаптации оценок и лечения к конкретным пожеланиям ребенка и родителей. Поскольку медицинские работники принимают клинические решения на основе информации о способностях и деятельности ребенка, мы ожидаем, что информация о деятельности ребенка будет отражена в историях болезни. Таким образом, это пилотное исследование направлено на изучение того, какие повседневные действия детей с генетически подтвержденными митохондриальными нарушениями указываются в медицинских картах пациентов, и на понимание профиля деятельности, в которой участвуют эти дети.
2. Методы
Был проведен ретроспективный обзор карт [16, 17]. Направленный контент-анализ [18] был использован для изучения того, какие повседневные действия были зарегистрированы в медицинских картах пациентов, и для изучения того, различались ли они среди функциональных профилей детей.
2.1. Участники
Участниками этого исследования были дети (0–18 лет) с генетически подтвержденным митохондриальным заболеванием, которые периодически оценивались в так называемом «MitoRoute», междисциплинарной, медицинской и смежной программе скрининга в области здравоохранения в Центре Радбуда. Митохондриальная медицина (RCMM), Медицинский центр Университета Радбауд (Radboudumc), Неймеген. Во время MitoRoute детей оценивала команда, состоящая из нескольких врачей разных специальностей и смежных медицинских работников, включая физиотерапевта, трудотерапевта, логопеда, диетолога, социального работника и психолога. Цель этой программы скрининга состояла в том, чтобы составить подробный обзор последствий расстройства для ребенка по различным параметрам Международной классификации функционирования, инвалидности и здоровья детей и молодежи (МКФ-ДП) [19]. ], чтобы предотвратить и выявить возможные осложнения и сформулировать рекомендации по лечению. В это исследование были включены истории болезни всех детей с генетически подтвержденным митохондриальным заболеванием, которые проходили скрининг с мая 2015 года по май 2016 года в Радбудуме.
], чтобы предотвратить и выявить возможные осложнения и сформулировать рекомендации по лечению. В это исследование были включены истории болезни всех детей с генетически подтвержденным митохондриальным заболеванием, которые проходили скрининг с мая 2015 года по май 2016 года в Радбудуме.
2.2. Сбор данных
Качественные данные о деятельности детей с митохондриальными нарушениями были извлечены из клинических записей (смежных) медицинских работников (MitoRoute) в электронных картах пациентов. Записи о пациентах содержали непреднамеренную письменную информацию, относящуюся к оценке и беседам, проведенным (смежными) медицинскими работниками, поскольку их не просили собирать данные, относящиеся к этому исследованию.
2.3. Стратификация
Поскольку двигательные функции, когнитивные способности и коммуникативные способности влияют на участие в деятельности [20, 21], эти характеристики были использованы для построения профилей функциональных возможностей детей. Для обеспечения качества стратификации на профили велся журнал, в котором документировались мыслительные процессы и отслеживалось принятие решений. Проверка участников с медицинскими работниками использовалась для проверки профилей. Функциональные возможности были стратифицированы следующим образом: Когнитивное развитие (на основе теста на возрастную норму, используемого для каждого ребенка): 1 = крайне низкие когнитивные функции, 2 = низкие когнитивные функции, 3 = средние когнитивные функции и 4 = хорошие когнитивные функции; Ходьба (Шкала Хоффера [22], с нормальным уровнем ходьбы, добавленным Schoenmakers et al. [23]): 1 = непередвижение, 2 = нефункциональное передвижение, 3 = домашнее передвижение, 4 = общественное передвижение и 5 = нормальное передвижение ; и Речевые способности (оценка дизартрии Радбауда [24]): 1 = устное общение невозможно, 2 = общение с известным человеком, 3 = частые повторения (частые повторения, чтобы гарантировать, что они будут поняты), 4 = случайные повторения, 5 = эффективные несмотря на небольшие проблемы, и 6 = эффективное общение.
Для обеспечения качества стратификации на профили велся журнал, в котором документировались мыслительные процессы и отслеживалось принятие решений. Проверка участников с медицинскими работниками использовалась для проверки профилей. Функциональные возможности были стратифицированы следующим образом: Когнитивное развитие (на основе теста на возрастную норму, используемого для каждого ребенка): 1 = крайне низкие когнитивные функции, 2 = низкие когнитивные функции, 3 = средние когнитивные функции и 4 = хорошие когнитивные функции; Ходьба (Шкала Хоффера [22], с нормальным уровнем ходьбы, добавленным Schoenmakers et al. [23]): 1 = непередвижение, 2 = нефункциональное передвижение, 3 = домашнее передвижение, 4 = общественное передвижение и 5 = нормальное передвижение ; и Речевые способности (оценка дизартрии Радбауда [24]): 1 = устное общение невозможно, 2 = общение с известным человеком, 3 = частые повторения (частые повторения, чтобы гарантировать, что они будут поняты), 4 = случайные повторения, 5 = эффективные несмотря на небольшие проблемы, и 6 = эффективное общение.
Другие собираемые характеристики пациентов включали пол, возраст, развитие крупной моторики (на основе тестов, ориентированных на норму), работоспособность в повседневной деятельности (на основе педиатрической оценки инвалидности (PEDI) [25]) и утомляемость (измеренная с помощью Pediatric Quality многомерной шкалы усталости Life Inventory (PedsQL-MFS) [26]). Эти характеристики не использовались при определении профилей, но использовались в качестве описательных результатов, связанных с каждым профилем.
2.4. Профили, основанные на функциональных возможностях
Три профиля могут быть определены на основе функциональных возможностей детей:
Глобально низкий уровень функционирования : дети с чрезвычайно низким или низким уровнем когнитивного развития и ограниченными двигательными функциями, которые приводят к нефункциональному передвижению на открытом воздухе и нефункциональное общение.
Низкие когнитивные функции с передвижением от умеренного до нормального : дети с крайне низким или низким уровнем когнитивного развития и некоторыми ограничениями двигательных функций, но способные к функциональному передвижению. Речевые способности по этому профилю различаются у детей.
Речевые способности по этому профилю различаются у детей.
Общее умеренное функционирование : дети со средним уровнем когнитивного развития и некоторыми ограничениями двигательных функций, но способные к функциональному передвижению. Речевых способностей достаточно, чтобы сделать себя понятным.
2.5. Анализ данных
В этом предварительном исследовании был использован метод направленного контент-анализа [18] фрагментов текста, извлеченных из карт пациентов [27–29]. Фрагменты текста были сосредоточены на информации, сообщаемой медицинскими работниками об опыте детей и родителей в их повседневных жизненных ситуациях. Прежде чем приступить к анализу историй болезни, были проведены два предварительных этапа:
(1) Определить ключевое понятие «деятельность» как начальную категорию кодирования (2) Операционализировать понятие «деятельность», используя теорию
На этапе 2 анализа данных термин «активность» был определен на основании МКФ-ТП [19] и литературы по трудотерапии [30–32] как деятельность, которая представляет собой осмысленное целенаправленное выполнение задач и/или действий. отдельными людьми, такими как игра на гитаре, одевание, еда и езда на велосипеде.
отдельными людьми, такими как игра на гитаре, одевание, еда и езда на велосипеде.
Для анализа истории болезни одним из исследователей были выполнены следующие шаги:
(1) Прочитайте текст и выделите весь текст, который кажется представляющим деятельность (2) Кодируйте выделенный текст кодами, соответствующими понятию деятельности (3) Разделите коды на группы действий (4) Организуйте категории (различные группы действий) на три области профессиональной деятельности Рида и Сандерсона [33]: личное обслуживание, производительность и отдых
Процедура анализа и результаты шагов 4 и 6 были рецензированы четвертым автором (TS).
2.6. Этические соображения
Данные, использованные в этом исследовании, были получены во время медицинского обслуживания, на использование которого ребенок и родители дали разрешение анонимно для исследования (номер одобрения совета по этике 2013-287). Данные были деидентифицированы перед анализом. Исследование проводилось в соответствии с этическими принципами Хельсинкской декларации [34].
3. Результаты
Были включены истории болезни семнадцати детей (пять девочек и двенадцать мальчиков). Возраст детей варьировался от 4 до 18 лет. У восьми детей была мутация в ядерной ДНК и у девяти детей в митохондриальной ДНК. Пять детей продемонстрировали общий профиль низкого функционирования, пять детей продемонстрировали низкий профиль когнитивных функций с умеренной или нормальной походкой, а семеро детей продемонстрировали общий профиль умеренного функционирования. Клинические и генетические характеристики детей представлены в таблице 1. Более клинически значимые приоритеты препятствовали планированию оценки усталости в двух случаях. Поэтому на графике их не было.
Как упоминалось ранее, деятельность была организована по трем направлениям профессиональной деятельности Рида и Сандерсона: личное обслуживание, продуктивность и отдых [33]. Действия по личному обслуживанию позволяют человеку поддерживать индивидуальные потребности жизнеобеспечения, например, одеваться или принимать душ. Производственная деятельность помогает обществу облегчить каждому человеку удовлетворение индивидуальных потребностей за счет использования коллективных ресурсов, например, ходить на работу или выполнять домашнюю работу. Досуг позволяет человеку выразить потребность в творчестве, например, в рисовании или плавании [33]. Результатом шага 5 анализа были категории деятельности: уход за собой, работа по дому, терапия, школа, работа на компьютере, хобби, игра, спорт и мобильность/транспорт. Некоторые категории деятельности могут быть отнесены к двум сферам профессиональной деятельности, поскольку значение или ценность деятельности не были отмечены. Например, мобильность/транспортная деятельность может выполняться как личное обслуживание, но также и как отдых. Результаты, включая любое двойное размещение, представлены на рисунке 1.9.0005
Производственная деятельность помогает обществу облегчить каждому человеку удовлетворение индивидуальных потребностей за счет использования коллективных ресурсов, например, ходить на работу или выполнять домашнюю работу. Досуг позволяет человеку выразить потребность в творчестве, например, в рисовании или плавании [33]. Результатом шага 5 анализа были категории деятельности: уход за собой, работа по дому, терапия, школа, работа на компьютере, хобби, игра, спорт и мобильность/транспорт. Некоторые категории деятельности могут быть отнесены к двум сферам профессиональной деятельности, поскольку значение или ценность деятельности не были отмечены. Например, мобильность/транспортная деятельность может выполняться как личное обслуживание, но также и как отдых. Результаты, включая любое двойное размещение, представлены на рисунке 1.9.0005
3.1. Индивидуальное обслуживание
Область личного обслуживания включает в себя все действия, которые дети выполняют, чтобы заботиться о себе и организовывать свою жизнь. Он включает следующие категории: уход за собой, работа по дому и мобильность/транспорт. По трем профилям (смежные) медицинские работники сообщили обо всех трех различных категориях личного обслуживания. Записи пациентов показали сходство по профилям в действиях по уходу за собой, таких как принятие душа, прием пищи, отдых и одевание. В категории деятельности, связанной с мобильностью/транспортом, чаще всего сообщалось о езде на велосипеде и автобусе. Несмотря на то, что в этой категории и в категории «Домашние дела», деятельность показала больше различий между профилями. Занятия варьировались от мытья посуды до стрижки газона.
Он включает следующие категории: уход за собой, работа по дому и мобильность/транспорт. По трем профилям (смежные) медицинские работники сообщили обо всех трех различных категориях личного обслуживания. Записи пациентов показали сходство по профилям в действиях по уходу за собой, таких как принятие душа, прием пищи, отдых и одевание. В категории деятельности, связанной с мобильностью/транспортом, чаще всего сообщалось о езде на велосипеде и автобусе. Несмотря на то, что в этой категории и в категории «Домашние дела», деятельность показала больше различий между профилями. Занятия варьировались от мытья посуды до стрижки газона.
Примечания в историях болезни указывают на разницу в поддержке или помощи, которую дети получали при выполнении задания. Например, активное питание было упомянуто как « она может есть самостоятельно », « с намазыванием масла и нарезкой ему помогают » и « он использует приспособление для еды, которое позволяет ему самостоятельно перемещать столовые приборы к себе». рот ». В нескольких видах деятельности упоминалось получение помощи или использование вспомогательных устройств или приспособлений. Например, процесс одевания и принятия душа упоминался как «с помощью» или как «самостоятельный». Иногда никаких заметок о поддержке или помощи не писалось.
рот ». В нескольких видах деятельности упоминалось получение помощи или использование вспомогательных устройств или приспособлений. Например, процесс одевания и принятия душа упоминался как «с помощью» или как «самостоятельный». Иногда никаких заметок о поддержке или помощи не писалось.
3.2. Продуктивность
В области производительности представлены все действия, которые дети выполняют, чтобы учиться и работать. Он включал следующие категории: школьные мероприятия и терапевтические мероприятия. Тем не менее, терапевтические мероприятия также можно рассматривать как личное обслуживание. По трем профилям (союзные) медицинские работники задокументировали заметки, которые соответствуют обеим категориям продуктивности. Все дети с глобальным низкофункциональным профилем посещали специальное образование, некоторые с подготовкой к будущей работе: « Он получает среднее специальное образование, одновременно проходя двухдневную производственную практику в центре занятости людей с ограниченными интеллектуальными возможностями ». Трое детей с низким когнитивным уровнем и средним или нормальным профилем ходьбы посещали специальное образование, а двое детей посещали обычное образование. Двое детей с глобальным профилем умеренного функционирования посещали специальное образование, а пятеро посещали обычное образование. Иногда делались небольшие переделки: « Она учится в обычной школе, но когда слишком устает, остается дома до обеда . Эта цитата также иллюстрирует, что уровень энергии используется в качестве решающего фактора при выполнении или отказе от деятельности. Заметки об уровне энергии как решающем факторе присутствовали во всех областях профессиональной деятельности. Хотя тип образования варьировался от специального до обычного образования, спектр деятельности не отличался среди трех профилей. Большинство детей посещали занятия, которые включали письмо, правописание и счет, а также физическую и/или трудотерапию.
Трое детей с низким когнитивным уровнем и средним или нормальным профилем ходьбы посещали специальное образование, а двое детей посещали обычное образование. Двое детей с глобальным профилем умеренного функционирования посещали специальное образование, а пятеро посещали обычное образование. Иногда делались небольшие переделки: « Она учится в обычной школе, но когда слишком устает, остается дома до обеда . Эта цитата также иллюстрирует, что уровень энергии используется в качестве решающего фактора при выполнении или отказе от деятельности. Заметки об уровне энергии как решающем факторе присутствовали во всех областях профессиональной деятельности. Хотя тип образования варьировался от специального до обычного образования, спектр деятельности не отличался среди трех профилей. Большинство детей посещали занятия, которые включали письмо, правописание и счет, а также физическую и/или трудотерапию.
3.3. Досуг
В зоне досуга представлены все виды деятельности, которыми дети занимаются, играя или занимаясь в свободное время. Он включал следующие категории: компьютеры, хобби, игры и спорт. В каждом из трех профилей (союзные) медицинские работники отметили все четыре различные категории досуга. О физически пассивной деятельности сообщалось больше в глобальном низкофункциональном профиле, чем в двух других профилях. Например, было упомянуто, что: « После школы он устал и использует свой ноутбук или планшет для игр, использует Facebook или смотрит фильмы ». В профилях детей с лучшей походкой было больше регулярных занятий физической культурой, например, « После выполнения домашнего задания он обычно выходит на улицу и прыгает на батуте или играет в футбол ». Анализ показал, что дети выполняли индивидуальные виды досуга, например, катались на лошадях, прыгали на батуте, смотрели футбол или ходили на изучение Библии. Некоторые виды деятельности были более популярны, включая плавание, гимнастику, просмотр телевизора или кино.
Он включал следующие категории: компьютеры, хобби, игры и спорт. В каждом из трех профилей (союзные) медицинские работники отметили все четыре различные категории досуга. О физически пассивной деятельности сообщалось больше в глобальном низкофункциональном профиле, чем в двух других профилях. Например, было упомянуто, что: « После школы он устал и использует свой ноутбук или планшет для игр, использует Facebook или смотрит фильмы ». В профилях детей с лучшей походкой было больше регулярных занятий физической культурой, например, « После выполнения домашнего задания он обычно выходит на улицу и прыгает на батуте или играет в футбол ». Анализ показал, что дети выполняли индивидуальные виды досуга, например, катались на лошадях, прыгали на батуте, смотрели футбол или ходили на изучение Библии. Некоторые виды деятельности были более популярны, включая плавание, гимнастику, просмотр телевизора или кино.
4. Обсуждение
В этом исследовании представлен первый обзор категорий активности детей с митохондриальными нарушениями. Три области профессиональной деятельности: личное обслуживание, производительность и досуг [33] включали, как сообщают смежные медицинские работники в записях пациентов, девять категорий деятельности: уход за собой, работа по дому, терапия, школа, работа на компьютере, хобби, игра, спорт, и мобильность/транспорт. Вопреки нашим ожиданиям, мы обнаружили, что все категории активности присутствуют в каждом глобально функционирующем профиле. Это соответствует руководящим принципам реабилитации детей в Нидерландах, которые предусматривают, что дети с ограниченными возможностями являются полноправными участниками повседневной жизни [35].
Три области профессиональной деятельности: личное обслуживание, производительность и досуг [33] включали, как сообщают смежные медицинские работники в записях пациентов, девять категорий деятельности: уход за собой, работа по дому, терапия, школа, работа на компьютере, хобби, игра, спорт, и мобильность/транспорт. Вопреки нашим ожиданиям, мы обнаружили, что все категории активности присутствуют в каждом глобально функционирующем профиле. Это соответствует руководящим принципам реабилитации детей в Нидерландах, которые предусматривают, что дети с ограниченными возможностями являются полноправными участниками повседневной жизни [35].
Действия, выполняемые детьми с митохондриальными нарушениями, как определено в этом исследовании, напоминают действия типично развивающихся детей, указанные в PACS Pediatric Activity Card Sort: PACS [36], за одним исключением: «терапевтическая деятельность». PACS была разработана на основе типичных детских занятий, актуальных для всех, а не только для типично развивающихся детей. Это означает, что этот инструмент может быть использован в качестве критерия исхода для детей с митохондриальными нарушениями. Хотя в текущем исследовании активность детей с митохондриальными нарушениями не сравнивалась со здоровыми сверстниками, результаты, по-видимому, повторяют выводы Shields et al. [6] и Кинг и др. [37], которые обнаружили, что в участии детей с ограниченными интеллектуальными возможностями и их типично развивающихся сверстников больше сходства, чем различий. Текущие результаты и существующая литература подчеркивают тот факт, что тип деятельности, которой занимается ребенок, не обязательно связан с инвалидностью ребенка, но характер деятельности отличается.
Это означает, что этот инструмент может быть использован в качестве критерия исхода для детей с митохондриальными нарушениями. Хотя в текущем исследовании активность детей с митохондриальными нарушениями не сравнивалась со здоровыми сверстниками, результаты, по-видимому, повторяют выводы Shields et al. [6] и Кинг и др. [37], которые обнаружили, что в участии детей с ограниченными интеллектуальными возможностями и их типично развивающихся сверстников больше сходства, чем различий. Текущие результаты и существующая литература подчеркивают тот факт, что тип деятельности, которой занимается ребенок, не обязательно связан с инвалидностью ребенка, но характер деятельности отличается.
В рамках мероприятий и между ними мы обнаружили различия в объеме оказываемой поддержки или помощи, а также в оборудовании, используемом детьми для обеспечения успешного участия. Например, сообщалось, что езда на велосипеде выполнялась по-разному, например, на обычном велосипеде, велосипеде для ходьбы или велосипеде для дуэтов, а также под руководством или самостоятельно. Кроме того, прием пищи представлял собой деятельность, о которой сообщалось, что она выполняется самостоятельно, с помощью или с помощью приспособления для еды. Можно предположить, что регулярное использование PEDI [25] могло повлиять на примечания в файлах пациентов в качестве вспомогательных устройств или поддержки, измеряемой этой оценкой. Однако только эрготерапевт использовал PEDI, другие (смежные) медицинские работники этого не делали, но они также сообщали об объеме помощи или вспомогательных устройств. В дополнение к заметкам о независимости были также заметки об уровне энергии как решающем факторе в выполнении или избегании деятельности. Это неудивительно, учитывая, что в профессиональной литературе, посвященной уходу за детьми с митохондриальными нарушениями, часто упоминается утомляемость [13]. Хотя дизайн исследования не позволял сравнивать объем помощи или адаптацию к уровням энергии при исполнительской деятельности, есть признаки того, что существуют различия в уровнях независимости, вспомогательных устройств и затратах энергии у детей.
Кроме того, прием пищи представлял собой деятельность, о которой сообщалось, что она выполняется самостоятельно, с помощью или с помощью приспособления для еды. Можно предположить, что регулярное использование PEDI [25] могло повлиять на примечания в файлах пациентов в качестве вспомогательных устройств или поддержки, измеряемой этой оценкой. Однако только эрготерапевт использовал PEDI, другие (смежные) медицинские работники этого не делали, но они также сообщали об объеме помощи или вспомогательных устройств. В дополнение к заметкам о независимости были также заметки об уровне энергии как решающем факторе в выполнении или избегании деятельности. Это неудивительно, учитывая, что в профессиональной литературе, посвященной уходу за детьми с митохондриальными нарушениями, часто упоминается утомляемость [13]. Хотя дизайн исследования не позволял сравнивать объем помощи или адаптацию к уровням энергии при исполнительской деятельности, есть признаки того, что существуют различия в уровнях независимости, вспомогательных устройств и затратах энергии у детей. Когда дети имеют ограниченные способности или более зависимы, на родителей ложится более высокая нагрузка по содействию участию и автономии [38, 39].]. Это говорит о том, что будущие исследования должны быть сосредоточены на различиях в уровнях независимости и вспомогательных устройств в зависимости от затрат на энергию и нагрузки на лиц, осуществляющих уход.
Когда дети имеют ограниченные способности или более зависимы, на родителей ложится более высокая нагрузка по содействию участию и автономии [38, 39].]. Это говорит о том, что будущие исследования должны быть сосредоточены на различиях в уровнях независимости и вспомогательных устройств в зависимости от затрат на энергию и нагрузки на лиц, осуществляющих уход.
Мы нашли четкие категории деятельности, которые представляют различные виды деятельности и могут быть организованы в часто используемые области профессиональной деятельности [33], как описано в литературе. Категории деятельности также согласуются с (под)доменами МКФ-ДП [19]. Мы организовали мероприятия по категориям на основе типичной цели занятий для детей, которые лучше всего соответствуют трем областям профессиональной деятельности Рида и Сандерсона [33]. Было замечено, что некоторые категории деятельности могут быть связаны с большим количеством областей профессиональной деятельности, чем другие. Например, компьютерная деятельность используется для обучения или работы (производительность), а также для отдыха. Это подтверждает идею о том, что смысл деятельности можно рассматривать с разных точек зрения, он может различаться для каждого ребенка и что категории деятельности не связаны исключительно с определенной областью профессиональной деятельности [40]. Чтобы подтвердить, к каким категориям деятельности относится деятельность, нам необходимо получить представление о точках зрения детей на индивидуальное значение, которое каждое действие имеет для них. Таким образом, категоризация деятельности самих детей подходит для использования в будущих исследованиях.
Это подтверждает идею о том, что смысл деятельности можно рассматривать с разных точек зрения, он может различаться для каждого ребенка и что категории деятельности не связаны исключительно с определенной областью профессиональной деятельности [40]. Чтобы подтвердить, к каким категориям деятельности относится деятельность, нам необходимо получить представление о точках зрения детей на индивидуальное значение, которое каждое действие имеет для них. Таким образом, категоризация деятельности самих детей подходит для использования в будущих исследованиях.
Использование карт пациентов привело к некоторым ограничениям в интерпретации результатов. Поскольку письменная информация была предоставлена без подсказки, не каждый (смежный) медицинский работник сообщил одну и ту же информацию. Еще одним последствием использования историй болезни пациентов является то, что не всегда было ясно, связаны ли действия, которые выполнялись во время терапии, с действиями, которые дети выполняли и воспринимали как значимые в повседневной жизненной ситуации. Например, « Ребенок нашел карандаши и сразу начал раскрашивать 9».0584». Эта запись о тестовой ситуации в одной из историй болезни может означать, что ребенок любит раскрашивать, но это спорно. Исходы тестовых ситуаций нельзя рассматривать как репрезентативные для повседневной жизни ребенка [41]. В этом исследовании мы сосредоточились на результативности деятельности, которая описывает то, что человек фактически делает в повседневной жизни, выражая вовлеченность человека в жизненную ситуацию [42]. Опрос самих детей позволит получить информацию об их самооценке деятельности и опыте в повседневной жизни.
Например, « Ребенок нашел карандаши и сразу начал раскрашивать 9».0584». Эта запись о тестовой ситуации в одной из историй болезни может означать, что ребенок любит раскрашивать, но это спорно. Исходы тестовых ситуаций нельзя рассматривать как репрезентативные для повседневной жизни ребенка [41]. В этом исследовании мы сосредоточились на результативности деятельности, которая описывает то, что человек фактически делает в повседневной жизни, выражая вовлеченность человека в жизненную ситуацию [42]. Опрос самих детей позволит получить информацию об их самооценке деятельности и опыте в повседневной жизни.
Другим ограничением исследования является небольшой размер выборки и разделение выборки на три глобально функционирующих профиля. Тем не менее, размер выборки в целом подходит для поискового исследования с учетом низкой распространенности заболевания. В каждом профиле участников было еще меньше; однако это было необходимо, чтобы учесть разницу в уровнях функционирования детей. Прогнозирование профиля активности на основе уровня нарушений в этой популяции затруднено, учитывая непредсказуемый характер состояния. Тем не менее, наше исследование показало большое разнообразие функциональных возможностей, что указывает на то, что мы охватили широкий спектр нарушений и ограничений, наблюдаемых в этой популяции [43]. Разделение на профили функциональных возможностей расширило представление о категориях активности всей исследуемой популяции и каждого профиля в отдельности. И наоборот, ошибка отбора могла иметь место, потому что были включены только отчеты о детях в пределах определенного MitoRoute. Педиатры направляют всех детей с митохондриальными нарушениями на обследование в MitoRoute по разным причинам (например, новый диагноз, двухгодичный скрининг или ухудшение клинического состояния). Хотя не все родители и/или дети с митохондриальным расстройством соглашаются участвовать в MitoRoute, неизвестно, приведет ли это к предвзятости отбора и каким образом. Несмотря на это, мы считаем, что результаты могут дать обзор категорий активности, возможно, для всех детей с митохондриальными нарушениями.
Прогнозирование профиля активности на основе уровня нарушений в этой популяции затруднено, учитывая непредсказуемый характер состояния. Тем не менее, наше исследование показало большое разнообразие функциональных возможностей, что указывает на то, что мы охватили широкий спектр нарушений и ограничений, наблюдаемых в этой популяции [43]. Разделение на профили функциональных возможностей расширило представление о категориях активности всей исследуемой популяции и каждого профиля в отдельности. И наоборот, ошибка отбора могла иметь место, потому что были включены только отчеты о детях в пределах определенного MitoRoute. Педиатры направляют всех детей с митохондриальными нарушениями на обследование в MitoRoute по разным причинам (например, новый диагноз, двухгодичный скрининг или ухудшение клинического состояния). Хотя не все родители и/или дети с митохондриальным расстройством соглашаются участвовать в MitoRoute, неизвестно, приведет ли это к предвзятости отбора и каким образом. Несмотря на это, мы считаем, что результаты могут дать обзор категорий активности, возможно, для всех детей с митохондриальными нарушениями. Будущие исследования должны включать репрезентативную по всем характеристикам выборку детей с митохондриальными нарушениями.
Будущие исследования должны включать репрезентативную по всем характеристикам выборку детей с митохондриальными нарушениями.
Клинические последствия большого разнообразия активности, обнаруженной в этом исследовании, могут заключаться в том, что медицинские работники должны учитывать все девять категорий активности при оценке и лечении. Кроме того, клиницисты должны проконсультироваться с детьми о значении, которое они придают деятельности, чтобы решить, к какой категории деятельности она принадлежит. Кроме того, оценки и вмешательства должны быть достаточно адаптированы, чтобы охватить разнообразие выполняемых действий, как видно из глобальных профилей функциональных возможностей детей и индивидуальных предпочтений в выполнении действий.
5. Выводы
Этот экспериментальный ретроспективный обзор карт дает представление о повседневной деятельности детей с митохондриальными нарушениями, о которой сообщают специалисты. Было определено девять категорий деятельности, которые представляют обычные детские занятия. Мы обнаружили, что, хотя дети различались по способностям и ограничениям, все категории активности присутствовали в каждом профиле глобального функционирования. Есть признаки того, что дети выполняют деятельность по-разному с точки зрения уровня независимости, использования вспомогательных устройств и затрат энергии. Это исследование закладывает основу для качественного изучения активности детей с митохондриальными нарушениями и того, поддерживают ли их практику специалисты из смежных областей здравоохранения. Кроме того, он поддерживает потребность в индивидуальном и основанном на силе уходе, что делает упор на учет точки зрения детей в уходе.
Мы обнаружили, что, хотя дети различались по способностям и ограничениям, все категории активности присутствовали в каждом профиле глобального функционирования. Есть признаки того, что дети выполняют деятельность по-разному с точки зрения уровня независимости, использования вспомогательных устройств и затрат энергии. Это исследование закладывает основу для качественного изучения активности детей с митохондриальными нарушениями и того, поддерживают ли их практику специалисты из смежных областей здравоохранения. Кроме того, он поддерживает потребность в индивидуальном и основанном на силе уходе, что делает упор на учет точки зрения детей в уходе.
Конфликт интересов
Авторы сообщают об отсутствии конфликта интересов.
Благодарности
Авторы выражают благодарность специалистам MitoRoute в Радбудуме, Неймеген, Нидерланды, а именно: (i) Ким ван де Лоо, магистр наук, и д-р Хосе Кластерс, психологи; (ii) Марджо ван Гервен, логопед; (iii) д-р Аньо Янссен, детский физиотерапевт; и (iv) Ивонн Винхуизен, магистр наук, и Анита ван дер Молен, эрготерапевты. Авторы использовали свои данные, чтобы разделить детей на три профиля: общее низкое функционирование, низкое когнитивное функционирование с передвижением от умеренного до нормального и общее умеренное функционирование. За возможность изучить все записи пациентов авторы хотели бы поблагодарить профессора доктора Дж. А. М. Смейтинка, руководителя Радбаудского центра митохондриальной медицины. Авторы также благодарят его за критический обзор рукописи и предложенные улучшения.
Авторы использовали свои данные, чтобы разделить детей на три профиля: общее низкое функционирование, низкое когнитивное функционирование с передвижением от умеренного до нормального и общее умеренное функционирование. За возможность изучить все записи пациентов авторы хотели бы поблагодарить профессора доктора Дж. А. М. Смейтинка, руководителя Радбаудского центра митохондриальной медицины. Авторы также благодарят его за критический обзор рукописи и предложенные улучшения.
Ссылки
М. Асбьернслетт и Х. Хеммингссон, «Участие в школе для подростков с ограниченными физическими возможностями», Скандинавский журнал профессиональной терапии , том. 15, нет. 3, стр. 153–161, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
R.M. Bendixen and C.M. Kreider, «Обзор исследований трудотерапии в практике детей и молодежи», The American Journal of Occupational Therapy , том.
 65, нет. 3, стр. 351–359, 2011.
65, нет. 3, стр. 351–359, 2011.Посмотреть по адресу:
Сайт издателя | Google Scholar
М. Лоу, К. Миссиуна, Н. Поллок и Д. Стюарт, «Основы практики трудотерапии с детьми», в Трудотерапия для детей , Дж. Кейс-Смит, изд., стр. 53–87, Elsevier Mosby, Сент-Луис, Миссури, США, 2005.
Посмотреть по адресу:
Google Scholar
Г. Кинг, М. Лоум, С. Кинг, П. Розенбаум, М. К. Кертой и Н. Л. Янг, «Концептуальная модель факторов, влияющих на участие детей с ограниченными возможностями в отдыхе и досуге», Физиотерапия и трудотерапия в педиатрии , том. 23, нет. 1, стр. 63–90, 2003 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
T. Heah, T. Case, B. McGuire и M. Law, «Успешное участие: жизненный опыт среди детей с ограниченными возможностями», Canadian Journal of Occupational Therapy , vol.
 74, нет. 1, стр. 38–47, 2007 г.
74, нет. 1, стр. 38–47, 2007 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
Н. Шилдс, М. Кинг, М. Корбетт и К. Иммс, «Сходно ли участие детей с ограниченными интеллектуальными возможностями во внешкольных мероприятиях по сравнению с их типично развивающимися сверстниками? Систематический обзор», Развивающая нейрореабилитация , том. 17, нет. 1, стр. 64–71, 2014 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Г. С. Горман, А. М. Шефер, Ю. Нг и др., «Распространенность мутаций ядерной и митохондриальной ДНК, связанных с митохондриальными заболеваниями у взрослых», Annals of Neurology , vol. 77, нет. 5, стр. 753–759, 2015.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Купман В.
 Дж., Виллемс П. Х. и Смейтинк Дж. А., «Моногенные митохондриальные расстройства», стр. 9.0649 Медицинский журнал Новой Англии , том. 366, нет. 12, стр. 1132–1141, 2012.
Дж., Виллемс П. Х. и Смейтинк Дж. А., «Моногенные митохондриальные расстройства», стр. 9.0649 Медицинский журнал Новой Англии , том. 366, нет. 12, стр. 1132–1141, 2012.Посмотреть по адресу:
Сайт издателя | Google Scholar
A. Rötig, «Генетика недостаточности митохондриальной дыхательной цепи», Revue Neurologique , vol. 170, нет. 5, стр. 309–322, 2014.
Посмотреть по адресу:
Сайт издателя | Google Scholar
J. B. WJ Koopman, C. W. Fung, S. Koene, R. J. Rodenburg, P. H. Willems и J. A. Smeitink, «Митохондриальные нарушения у детей: на пути к разработке стратегий лечения низкомолекулярными препаратами», EMBO Молекулярная медицина , том. 8, нет. 4, стр. 311–327, 2016 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
А.
 Дасслер и П. Дж. Аллен, «Митохондриальные заболевания у детей и подростков», Pediatric Nursing , vol. 40, с. 150, 2014.
Дасслер и П. Дж. Аллен, «Митохондриальные заболевания у детей и подростков», Pediatric Nursing , vol. 40, с. 150, 2014.Посмотреть по адресу:
Google Scholar
Кислер Дж. Э., Уиттакер Р. Г. и Макфарланд Р. Митохондриальные заболевания у детей: клинический подход к исследованию и лечению, стр. 9.0649 Медицина развития и детская неврология , том. 52, нет. 5, стр. 422–433, 2010.
Посмотреть по адресу:
Сайт издателя | Google Scholar
S. Koene, S.B. Wortmann, M.C. de Vries et al., «Разработка показателей исходов для педиатрических митохондриальных расстройств: какие жалобы и ограничения наиболее обременительны для пациентов и их родителей?» Митохондрия , об. 13, нет. 1, стр. 15–24, 2013 г.
Посмотреть по адресу:
Сайт издателя | Академия Google
Мартенс А.
 М., Гортер Х., Вассинк Р. Г. и Ритман Х. Физическая активность детей с митохондриальным заболеванием по сравнению со здоровыми детьми, Pediatric Physical Therapy , vol. 26, нет. 1, стр. 19–26, 2014 г.
М., Гортер Х., Вассинк Р. Г. и Ритман Х. Физическая активность детей с митохондриальным заболеванием по сравнению со здоровыми детьми, Pediatric Physical Therapy , vol. 26, нет. 1, стр. 19–26, 2014 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
S. Koene, M. Jansen, C.M. Verhaak, R.L.A. De Vrueh, IJM De Groot и J.A.M. Smeitink, «На пути к гармонизации показателей результатов у детей с митохондриальными нарушениями», Медицина развития и детская неврология , том. 55, нет. 8, стр. 698–706, 2013 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Д. Р. Хесс, «Ретроспективные исследования и обзоры диаграмм», Respiratory Care , vol. 49, нет. 10, стр. 1171–1174, 2004.
Просмотр по адресу:
Google Scholar
М.
 Вассар и М. Хольцманн, «Ретроспективный обзор диаграммы: важные методологические соображения», Journal of Educational Evaluation for Health Professions , том. 10, с. 12, 2013.
Вассар и М. Хольцманн, «Ретроспективный обзор диаграммы: важные методологические соображения», Journal of Educational Evaluation for Health Professions , том. 10, с. 12, 2013.Посмотреть по адресу:
Сайт издателя | Google Scholar
H. F. Hsieh and S. E. Shannon, «Три подхода к качественному анализу контента», Qualitative Health Research , vol. 15, нет. 9, стр. 1277–1288, 2005.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Всемирная организация здравоохранения, Международная классификация функционирования, инвалидности и здоровья: версия для детей и молодежи: ICF-CY. , Всемирная организация здравоохранения, 2007 г.
М. КВН Браун и Д. Л. Йергин-Аллсопп, «Ограничения активности среди молодых людей с нарушениями развития: последующее популяционное исследование», Research in Developmental Disability , vol.
 . 30, нет. 1, стр. 179–191, 2009 г.
. 30, нет. 1, стр. 179–191, 2009 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
О. В. М. К. Булт, М. Дж. Йонгманс, Э. Линдеман и М. Кетелаар, «Что влияет на участие в досуговой деятельности детей и молодежи с ограниченными физическими возможностями? Систематический обзор», Исследования нарушений развития , vol. 32, нет. 5, стр. 1521–1529, 2011.
Посмотреть по адресу:
Сайт издателя | Google Scholar
E. MM Hoffer, R. Feiwell, J. Perry и C. B. Perry, «Функциональное передвижение у пациентов с миеломенингоцеле», The Journal of Bone & Joint Surgery , vol. 55, нет. 1, стр. 137–148, 1973.
Посмотреть по адресу:
Сайт издателя | Google Scholar
M. A. Schoenmakers, V. A. Gulmans, R.
 H. Gooskens, P. J. Helders, «Расщепление позвоночника на крестцовом уровне: более чем незначительные нарушения походки», Клиническая реабилитация , том. 18, нет. 2, стр. 178–185, 2004 г.
H. Gooskens, P. J. Helders, «Расщепление позвоночника на крестцовом уровне: более чем незначительные нарушения походки», Клиническая реабилитация , том. 18, нет. 2, стр. 178–185, 2004 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
S. Knuijt, JG Kalf, BMG Van Engelen, BJM De Swart и ACH Geurts, «Оценка дизартрии Радбуда: развитие и клиническая оценка», Folia Phoniatrica et Logopaedica , vol. 69, нет. 4, стр. 143–153, 2017 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Дж. Вассенберг-Северийнен и Дж. Кастерс, Handleiding PEDI-NL , Pearson, 2005.
J. W. Varni, Масштабирование и оценка педиатрического опросника качества жизни™ (PedsQL™) , Mapi Research Trust, Lyon, 14 edition, 9 012 14 edition, 2014.
Х. Прист, П. Робертс и Л.
 Вудс, «Обзор трех различных подходов к интерпретации качественных данных. Часть 1: теоретические вопросы», Nurse Researcher , vol. 10, нет. 1, стр. 30–42, 2002 г.
Вудс, «Обзор трех различных подходов к интерпретации качественных данных. Часть 1: теоретические вопросы», Nurse Researcher , vol. 10, нет. 1, стр. 30–42, 2002 г.Посмотреть по адресу:
Сайт издателя | Академия Google
С. Эло и Х. Кингэс, «Процесс анализа качественного содержания», Journal of Advanced Nursing , vol. 62, нет. 1, стр. 107–115, 2008 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
М. Стэнли, «Качественное описание», в Методологии качественных исследований для профессиональной науки и терапии , С. Наяр и М. Стэнли, ред., Routledge, 2015.
Посмотреть по адресу:
Google Ученый
R. Hagedorn, Foundations for Practice in Occupational Therapy , Elsevier Health Sciences, 2001.

M. le Granse and M. J. Hartingsveldt, Grondslagen van de Ergotherapie , Reed Business, 2012.
A. A. Wilcock, An Occupational Perspective of Health , Slack Incorporated, 2006.
K.L. Reed and S.N. Sanderson, Concepts of Occupational Therapy , Lippincott Williams & Wilkins, 1999.
Всемирная медицинская ассоциация, «Хельсинкская декларация Всемирной медицинской ассоциации. Этические принципы медицинских исследований с участием людей», Bulletin World Health Organization , vol. 79, pp. 373-374, 2001.
View at:
Google Scholar
A. H. M. Mulders, M. J. Meihuizen-de Regt, and J. M. H. de Moor, “Kinderrevalidatie: een plaatsbepaling,” in Kinderrevalidatie , M. J. Meihuizen-de Regt, JMH Moor и AHM Mulders, Eds., стр. 1–48, Koninklijke Van Gorcum BV, Assen, 2009 г..
Посмотреть по адресу:
Google Scholar
А.
 Мандич, Х. Полатайко, Л. Миллер и К. Баум, The Pediatric Activity Card Sort (PACS) , Канадская ассоциация трудотерапии, Оттава, 2004 г.
Мандич, Х. Полатайко, Л. Миллер и К. Баум, The Pediatric Activity Card Sort (PACS) , Канадская ассоциация трудотерапии, Оттава, 2004 г.М. Кинг, Н. Шилдс, К. Иммс, М. Блэк и К. Ардерн, «Участие детей с умственной отсталостью по сравнению с обычно развивающимися детьми», Research in Developmental Disabilities , vol. 34, нет. 5, стр. 1854–1862, 2013.
Посмотреть по адресу:
Сайт издателя | Google Scholar
B. Piškur, AJ Beurskens, MJ Jongmans et al., «Действия, проблемы и потребности родителей при обеспечении участия детей с ограниченными физическими возможностями: предварительный обзор», BMC Pedias , vol. 12, нет. 1, с. 177, 2012.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Б. Пишкур, М. К. А. Дж. Берскенс, М. Дж. Йонгманс, Б. М. Каспари и Р.
 Дж. Смитс, «Ежедневные действия, проблемы и потребности голландских родителей при поддержке участия их ребенка с физическими недостатками дома, в школе и в сообществе: качественное дневниковое исследование» BMC Pediatrics , vol. 17, нет. 1, с. 12, 2017.
Дж. Смитс, «Ежедневные действия, проблемы и потребности голландских родителей при поддержке участия их ребенка с физическими недостатками дома, в школе и в сообществе: качественное дневниковое исследование» BMC Pediatrics , vol. 17, нет. 1, с. 12, 2017.Посмотреть по адресу:
Сайт издателя | Google Scholar
Д. Перссон, Л. Эрландссон, М. Эклунд и С. Иварссон, «Ценные измерения, значение и сложность человеческой деятельности — предварительная структура для анализа», Scandinavian Journal of Occupational Therapy , об. 8, нет. 1, стр. 7–18, 2001 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
К. Моррис, «Измерение участия в детской инвалидности: как подход, основанный на возможностях, улучшает наше понимание?» Медицина развития и детская неврология , том. 51, нет. 2, стр.
 92–94, 2009 г.
92–94, 2009 г.Посмотреть по адресу:
Сайт издателя | Google Scholar
M. E. Michielsen, M. de Niet, G. M. Ribbers, H. J. Stam и J. B. Bussmann, «Доказательства логарифмической зависимости между двигательной способностью и фактической производительностью в повседневной жизни паретичной руки после инсульта», Journal of Реабилитационная медицина , вып. 41, нет. 5, стр. 327–331, 2009.
Просмотр:
Сайт издателя | Google Scholar
С. Коэн и Дж. Смейтинк, «Митохондриальная медицина: вступление в эру лечения», Journal of Internal Medicine , vol. 265, нет. 2, стр. 193–209, 2009 г.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Copyright
Copyright © 2018 Marieke Lindenschot et al.
