Миотонический синдром у грудничка что это: Миотонический синдром у детей — причины, симптомы, диагностика и лечение
Миотонический синдром — лечение, симптомы, причины, диагностика
Миотония это не заболевание, а симптом группы мышечных нарушений, для которых характерно нарушение способности мышцы к релаксации после сокращения. У большинства людей миотоническая атака имеет временный характер и проявляется выраженной скованностью, которая возникает после выполнения определенного вида движений. Невозможность сжатых мышц расслабиться и трудности при вставании из сидячего положения являются наиболее частыми проявлениями миотонической атаки.
Длительность миотонической атаки может быть продолжительностью от секунд до минут и по интенсивности колебаться от небольшого дискомфорта до выраженного нарушения двигательных возможностей. Как правило, миотоническая атака возникает после интенсивной физической нагрузки или после длительного периода отдыха, но иногда возникает как реакция на низкие температуры или даже резкий звук.
При миотонии идет вовлечение только скелетной мускулатуры, выполняющей произвольные движения. Таким образом, миотоническая атака может возникнуть только при выполнении осознанных движений, но не поражает мышцу сердца или мышечные структуры пищеварительного тракта. В зависимости от типа и серьезности миотония может возникнуть в ногах, лице, руках, в плечах, стопе, в мышцах век глаз и даже способности говорить четко.
Таким образом, миотоническая атака может возникнуть только при выполнении осознанных движений, но не поражает мышцу сердца или мышечные структуры пищеварительного тракта. В зависимости от типа и серьезности миотония может возникнуть в ногах, лице, руках, в плечах, стопе, в мышцах век глаз и даже способности говорить четко.
Как правило, миотонические синдромы являются генетически детерминированными и могут быть у любого человека. Миотонические нарушения могут быть как у женщин, так и мужчин и в любом возрасте могут быть симптомы миотонических атак. В зависимости от выраженности миотонических симптомов первые признаки этих нарушений могут появиться в подростковом возрасте или у взрослых. Наследование миотонических синдромов происходит двумя путями аутосомально-доминантным генетическим паттерном или аутосомально-рецессивным генетическим паттерном.
Аутосомально доминантное наследование
Нарушения, связанные с аутосомально-доминантным наследованием обычно проявляется в каждом поколении без исключений. Аутосомальный означает то, что генетическая ошибка может располагаться на любой хромосоме, в каждой клетке организма, за исключением половых хромосом. Доминантный означает, что достаточно одного родителя носителя дефектного гена для передачи заболевания по наследству. И так как нарушения могут передаваться любым родителем, то любой ребенок от родителя с генетическим дефектом имеет 50% шанс наследовать это нарушение. Выраженность нарушения и возраст дебюта могут варьировать в зависимости от конкретного индивидуума.
Аутосомальный означает то, что генетическая ошибка может располагаться на любой хромосоме, в каждой клетке организма, за исключением половых хромосом. Доминантный означает, что достаточно одного родителя носителя дефектного гена для передачи заболевания по наследству. И так как нарушения могут передаваться любым родителем, то любой ребенок от родителя с генетическим дефектом имеет 50% шанс наследовать это нарушение. Выраженность нарушения и возраст дебюта могут варьировать в зависимости от конкретного индивидуума.
Аутосомально-рецессивное наследование
При аутосомально-рецессивном наследовании заболевание появляется в одном поколении и обычно без наличия семейного анамнеза этого состояния. Оба родителя могут быть носителями этого гена. Носитель дефектного гена может не отмечать какой-либо симптоматики. Рецессивность означает то, что для проявления этого гена и заболевания необходимо, чтобы у обоих родителей был дефектный ген. Дети обоего пола могут наследовать дефектный ген по этому типу наследования. При каждой беременности у 25 % детей есть вероятность наследования дефектного гена от обоих родителей. Если ребенок наследует дефектный ген от одного родителя, то он будет носителем дефектного гена, но, скорее всего, проявляться это симптомами не будет. В 50% случаев ребенок будет носителем гена. В то же время вероятность того, что ребенок не наследует дефектный ген и не будет носителем и не будет иметь клиническую манифестацию, составляет 25%.
При каждой беременности у 25 % детей есть вероятность наследования дефектного гена от обоих родителей. Если ребенок наследует дефектный ген от одного родителя, то он будет носителем дефектного гена, но, скорее всего, проявляться это симптомами не будет. В 50% случаев ребенок будет носителем гена. В то же время вероятность того, что ребенок не наследует дефектный ген и не будет носителем и не будет иметь клиническую манифестацию, составляет 25%.
Виды миотоний
Миотония конгенита
Миотония конгенита наиболее часто встречающаяся непрогрессирующая форма миотонического синдрома и вызвана мутацией гена, отвечающего за натриевые ионные каналы мышц. Эта форма миотонии не оказывает влияние на продолжительность жизни и имеет незначительное влияние на структуру тела или рост опорно-двигательного аппарата. Существует две формы миотонии конгенита в зависимости от типа наследования.
Частой и довольно тяжелым типом миотонии конгенита является генерализованная миотония Бейкера, и наследование этого заболевания происходит по аутосомально-рецессивному типу. Дебют этой формы миотонии бывает в детстве или раннем подростковом возрасте, но иногда при тяжелом течение дебют может быть и в раннем детском возрасте. Симптоматика может нарастать прогрессивно, в течение нескольких лет после постановки диагноза или постепенно нарастать до достижения пациентом двадцатилетнего возраста.
Дебют этой формы миотонии бывает в детстве или раннем подростковом возрасте, но иногда при тяжелом течение дебют может быть и в раннем детском возрасте. Симптоматика может нарастать прогрессивно, в течение нескольких лет после постановки диагноза или постепенно нарастать до достижения пациентом двадцатилетнего возраста.
Аутосомально — доминантная форма наследования называют болезнью Томсена. Заболевание названо в честь датского врача Асмуса Юлиуса Томсена у которого было это заболевание и который проследил наличие этого заболевания в своей семье. Симптомы миотонии Томсена, как правило, значительно мягче, чем при миотонии Бейкера и хотя дебют заболевания бывает раньше, и первые признаки становятся заметными в раннем детстве и иногда при рождении. В редких случаях симптомы могут быть незначительными, в течение многих лет после постановки диагноза.
Основным симптомом обеих заболеваний является генерализованная миотония, вызванная произвольными движениями. Как правило, такая симптоматика провоцируется значительной физической нагрузкой или наоборот длительным периодом отдыха и мышечной релаксации. Миотония более выражена в ногах, что вызывает затруднения при ходьбе и иногда даже падения. Также миотонией бывают охвачены мышцы плечевого пояса и головы, что может вызвать затруднения при хватании предметов, жевании или мигании. В редких случаях при миотонии Бейкера может быть обездвиживающая слабость, появляющаяся после миотонической атаки.
Миотония более выражена в ногах, что вызывает затруднения при ходьбе и иногда даже падения. Также миотонией бывают охвачены мышцы плечевого пояса и головы, что может вызвать затруднения при хватании предметов, жевании или мигании. В редких случаях при миотонии Бейкера может быть обездвиживающая слабость, появляющаяся после миотонической атаки.
После миотонической атаки при обоих типах миотонии снять скованность можно с помощью повторных движений в скованных мышцах. Как правило, скованность увеличивается после нескольких первых сокращений заинтересованных мышц, а затем после пяти сокращений миотоническая скованность исчезает, что позволяет восстановить нормальную работу мышц на определенный промежуток времени. Это эффект называется эффектом разминки (разогрева) и позволяет людям с миотонией заниматься тяжелыми физическими нагрузками и силовыми видами спорта.
И хотя миотония конгенита не оказывает значительного влияния формирование опорно-двигательного аппарата, в то же время миотония влияет на размер определенных мышц. Обе миотонии Бейкера и Томсена могут вызывать необычное увеличение размеров скелетных мышц, особенно в области ног ягодиц, но также и в области рук плеч и мышц спины. Такое увеличение может считаться мышечной гипертрофией и иногда такие пациенты выглядят как настоящие атлеты. При миотонии Бейкера гипертрофия мышц более выражена, чем при миотонии Томсена.
Обе миотонии Бейкера и Томсена могут вызывать необычное увеличение размеров скелетных мышц, особенно в области ног ягодиц, но также и в области рук плеч и мышц спины. Такое увеличение может считаться мышечной гипертрофией и иногда такие пациенты выглядят как настоящие атлеты. При миотонии Бейкера гипертрофия мышц более выражена, чем при миотонии Томсена.
Парамиотония конгенита
Эта миотония является редкой патологией, связанной нарушением натриевых каналов и передающаяся по аутосомно-доминантному типу. Этот тип миотонии не сокращает продолжительность жизни, и интенсивность миотонии сохраняется стабильной в течение жизни. Дебют заболевания возникает в период между рождением и ранним детским возрастом. Характерным симптомом парамиотонии конгенита является генерализованная миотоническая скованность, которая в большей степени поражает руки и лицо, а также области шеи и руки. Так же, как и при других непрогрессирующих миотониях, парамиотония конгенита провоцируется интенсивными произвольными нагрузками, а в некоторых случаях провоцируются низкой температурой. Во многих случаях, миотонические атаки индуцированные холодом и связанную с ними мышечную скованность можно снять теплом.
Во многих случаях, миотонические атаки индуцированные холодом и связанную с ними мышечную скованность можно снять теплом.
Атаки миотонической скованности часто сопровождаются обездвиживающей слабостью в заинтересованных зонах. Слабость может быть более длительной, чем эпизод миотонической скованности, ослабляя мышцы на период от нескольких минут до нескольких часов. Но слабость не характерна для парамиотонии конгенита. Кроме того, в отличие от других непрогрессирующих форм миотонии, для парамиотонии не характерно наличие эффекта разминки, при котором происходит снижение скованности после нескольких сокращений мышц. Наоборот, миотоническая скованность обычно увеличивается после продолжающейся активности мышц, что еще больше снижает двигательную активность. Этот феномен обычно называют парадоксальной миотонией.
Синдром Шварц Джемпела
Синдром Шварц — Джемпела является наиболее тяжелой формой непрогрессирующей миотонии. Это очень редкий тип миотонии передается по аутосомально-рецессивному типу. Дебют заболевания возникает или сразу после рождения или через небольшое время после рождения. Характер и интенсивность симптоматики могут иметь индивидуальные особенности. Одним из главных симптомов является миотоническая скованность, наиболее выраженная в лице и бедрах. При этой миотонии имеется тенденция к падениям нарушениям речи и лицевым изменениям. Как и при миотонии конгенита дополнительные сокращения мышц вызывают эффект разминки и снижают скованность. Но эффект разминки имеет незначительную степень, а некоторых случаях отсутствует. Для синдрома Шварца-Джемпела характерны различные скелетные деформации. Эти деформации к проблема роста организма и, как правило, это проявляется уменьшением роста, а также аномалиям лица, что придает лицу маскообразную форму. Другие симптомы включают гипертрофированные бедра, атрофированные плечевой пояс и длительные мышечные подергивания, а иногда и нарушения интеллектуальной сферы.
Дебют заболевания возникает или сразу после рождения или через небольшое время после рождения. Характер и интенсивность симптоматики могут иметь индивидуальные особенности. Одним из главных симптомов является миотоническая скованность, наиболее выраженная в лице и бедрах. При этой миотонии имеется тенденция к падениям нарушениям речи и лицевым изменениям. Как и при миотонии конгенита дополнительные сокращения мышц вызывают эффект разминки и снижают скованность. Но эффект разминки имеет незначительную степень, а некоторых случаях отсутствует. Для синдрома Шварца-Джемпела характерны различные скелетные деформации. Эти деформации к проблема роста организма и, как правило, это проявляется уменьшением роста, а также аномалиям лица, что придает лицу маскообразную форму. Другие симптомы включают гипертрофированные бедра, атрофированные плечевой пояс и длительные мышечные подергивания, а иногда и нарушения интеллектуальной сферы.
Причина синдрома Шварца-Джемпела не известна. Не исключается, что этот вид миотонии является разновидностью мышечных нарушений, а также возможно иметь связь с нарушениями в нервной системе или является сочетанием нарушениям в мышцах и нервах.
Диагностика
Даже на основании физикального обследования врач может провести определенные диагностические тесты, такие как миотоническая реакция на нагрузку, воздействие холодом или другие стимуляции. Но очень важно диффенцировать эти миотонии с прогрессирующими заболеваниями, такими как миотонические дистрофии. И для дифференциального диагноза необходимы специальные методы исследования. Эти исследования включают проведение ЭМГ, который позволяет определить электрическую активность мышечных ткани; лабораторные исследования (анализы крови и анализ ДНК) биопсию мышц, которая бывает иногда необходима для окончательного диагноза мышечного заболевания.
Лечение
В настоящее время не существует методов лечения, позволяющих избавиться полностью от какого либо миотонического синдрома. Лечение носит симптоматический характер. Если миотонические атаки становятся интенсивными, возникает необходимость применения медикаментов, позволяющих снизить симптоматику. Наиболее известным препаратом является мексилитен, а также такие препараты как гуанин, прокаинамид, тегретол, фенитоин. Но все эти препараты имеют массу побочных эффектов и поэтому их длительное употребление не желательно. Наиболее оптимально, когда пациент знает провоцирующие миотонические атаки факторы и старается по возможности избегать провоцирующих ситуаций, а после атак дает возможность мышцам восстановиться с помощью отдыха.
Наиболее известным препаратом является мексилитен, а также такие препараты как гуанин, прокаинамид, тегретол, фенитоин. Но все эти препараты имеют массу побочных эффектов и поэтому их длительное употребление не желательно. Наиболее оптимально, когда пациент знает провоцирующие миотонические атаки факторы и старается по возможности избегать провоцирующих ситуаций, а после атак дает возможность мышцам восстановиться с помощью отдыха.
Миотонический синдром у взрослых — что это, как лечить миотонический болевой синдром у женщин, диагностика и лечение миотонии в Москве
Миотонический синдром — это комплекс нервно-мышечных нарушений, при котором у человека нарушается способность мышцы расслабляться после сокращения. Для миотонического синдрома характерен преимущественно наследственный характер – это геномная патология аутосомно-рецессивного или аутосомно-доминантного типа наследования. Характерными симптомами миотонии являются: мышечная гипотония и слабость, впоследствии – спазмы, боли и напряженность.
Диагностика и лечение миотонического синдрома проводится в центре реабилитации Юсуповской больницы – ведущем медицинском центре Москвы, оснащенном новейшим медицинским оборудованием, позволяющим нашим высококвалифицированным специалистам точно и в короткие сроки обнаружить патологию и подобрать наиболее эффективную индивидуальную схему лечения.
Формы заболевания
При отсутствии лечения даже умеренный миотонический синдром может привести к нарушению осанки, нарушению работы суставов, нарушению деятельности желудочно-кишечного тракта, желчевыводящих путей, хроническим запорам (вследствие поражения мышц передней брюшной стенки).
Ослабление мышечного тонуса может сопровождаться недержанием мочи, развитием близорукости, искривлением позвоночника, остеохондрозом. У больных с миотоническим синдромом отмечается появление интенсивных головных болей, вследствие чего нарушается психика и снижается трудоспособность.
Миотония может быть врожденной — иметь генетический характер. В этом случае появление геномной патологии связано с поражением того или иного отдела головного мозга. Миотонический синдром может наблюдаться у людей любого возраста и пола. Продолжительность миотонической атаки составляет несколько секунд или минут. Различна и интенсивность атаки – у одних больных могут возникать дискомфортные ощущения, у других — болезненные дисфункциональные нарушения. Развитие миотонической атаки может быть обусловлено физическим перенапряжением, длительным отдыхом, холодовым воздействием, резкими и громкими звуками.
В этом случае появление геномной патологии связано с поражением того или иного отдела головного мозга. Миотонический синдром может наблюдаться у людей любого возраста и пола. Продолжительность миотонической атаки составляет несколько секунд или минут. Различна и интенсивность атаки – у одних больных могут возникать дискомфортные ощущения, у других — болезненные дисфункциональные нарушения. Развитие миотонической атаки может быть обусловлено физическим перенапряжением, длительным отдыхом, холодовым воздействием, резкими и громкими звуками.
Существует и приобретенная форма миотонии. Она возникает при травмах, полученных в процессе родов, метаболических нарушениях, после перенесенного рахита. Грудные дети не могут разжать пальцы рук, пытаясь захватить предмет, у них отмечается слабая выраженность сосательного рефлекса. У детей постарше возникают трудности с подъемом тела после падений, подвижными играми.
Для выбора грамотного метода лечения миотонического синдрома специалисты Юсуповской больницы проводят предварительное комплексное обследование больных, позволяющее выявить причину, которая спровоцировала развитие данной патологии.
Как проявляется у женщин и мужчин?
Клиническая картина миотонии зависит от того, где локализован очаг поражения. У больных с нарушением активности мышц рук, ног, лица, плеч, шеи, отмечаются сложности с ходьбой, удержанием осанки, речевой функцией, управлением мимикой, приемом пищи.
К общим симптомам миотонического синдрома относят:
- мышечную слабость;
- апатию;
- быструю утомляемость;
- энурез;
- нарушение функции желудочно-кишечного тракта: кишечные колики и хронические запоры;
- цефалгию невыясненной этиологии;
- сгорбленность, сутулость;
- потеря устойчивости; нарушение равновесия;
- миопию;
- нарушения речи;
- снижение интеллекта;
- неуверенную походку при резком спуске и крутом подъеме.
Чаще всего болезнь впервые проявляется в детском возрасте. Больным малышам сложнее, чем здоровым детям, держать голову, они позже начинают ходить, разговаривать. Ребенок с миотоническим синдромом не в состоянии нормально контролировать свои движения.
Ребенок с миотоническим синдромом не в состоянии нормально контролировать свои движения.
У них отмечается нарушение стула, развитие хронических запоров, дисфункции желчевыводящих протоков и мочевого пузыря.
Миотонический синдром у взрослых может проявляться гипертрофией перенапряженных мышц, увеличением их объема. Больные с миотоническим синдромом часто выглядят как бодибилдеры.
При поражении мышц лица и шеи (шейный миотонический синдром) наблюдается изменение внешнего вида больного, изменение тембра голоса, нарушение глотательных и дыхательных процессов – развивается одышка и дисфагия.
Как обнаружить у взрослых?
Для того, чтобы выявить миотонический болевой синдром, специалисты Юсуповской больницы используют мультидисциплинарный подход с привлечением неврологов, ортопедов, терапевтов, офтальмологов.
В первую очередь врач собирает наследственный анамнез пациента: выясняет сведения о наличии миотонического синдрома у членов семьи больного. Затем с помощью перкуссионного молоточка простукивает мышцы для выявления дефекта.
Затем с помощью перкуссионного молоточка простукивает мышцы для выявления дефекта.
Для того, чтобы выявить миотоническую реакцию на внешние раздражители (нагрузки, резкие звуки, холод) специалисты Юсуповской больницы проводят специфический тест.
Исследовать биоэлектрические потенциалы, возникающие в скелетных мышцах при возбуждении мышечных волокон, позволяет электромиография.
Для определения параклинических и биохимических показателей проводится анализ крови.
Дополнительно назначается проведение молекулярно-генетического исследования, биопсии и гистологического исследования мышечных волокон.
Как вылечить?
Метод лечения миотонического синдрома напрямую зависит от причины, спровоцировавшей его возникновение.
Больным с приобретенным миотоническим синдромом назначается проведение комплексной терапии, направленной на устранение этиопатогенетических факторов и последствий их воздействия.
Врожденный миотонический синдром считается неизлечимым заболеванием. Для облегчения состояния больных необходимо проведение общетерапевтических мероприятий.
Для облегчения состояния больных необходимо проведение общетерапевтических мероприятий.
Всем больным назначается симптоматическая терапия, позволяющая нормализовать мышечный тонус, стабилизировать метаболизм в организме, способствующая быстрому восстановлению мышц после сокращения и перенапряжения. Чаще всего рекомендуется прием сосудистых, ноотропных, метаболических и нейропротекторных средств:
- актовегина – для активации обмена веществ в тканях, улучшения трофики и клеточного метаболизма, стимуляции процесса регенерации;
- пантогама – ноотропного препарата для запуска метаболических процессов в клетках мозга и устранения последствий психомоторного возбуждения;
- фенитоина – миорелаксанта, оказывающего противоконвульсивное действие;
- элькара – для повышения активности головного мозга, нормализации обменных процессов;
- кортексина – мощного антиоксиданта и антигипоксанта, используемого для улучшения функций головного мозга и повышения устойчивости организма к внешним раздражителям;
- верошпирона, гипотиазида – диуретиков, снижающих уровень калия в крови;
- церебролизина – для стимуляции мозговой деятельности благодаря функциональной нейромодуляции и нейротрофической активности.

Тяжелые случаи требуют применения иммуносупрессивной терапии – внутривенного введения иммуноглобулина, преднизолона, циклофосфамида.
Кроме медикаментозной терапии в клинике реабилитации Юсуповской больницы проводятся лечебные мероприятия, непосредственно воздействующие на мышцы и направленные на их тренировку и укрепление: массаж, лечебная физкультура, закаливание. Ежедневное выполнение гимнастики и сеансов массажа способствует восстановлению мышечной активности, нормализации тонуса мышц, устранению неприятных симптомов миотонического синдрома.
Для лечения миотонического синдрома в клинике реабилитации Юсуповской больницы пациентам назначается проведение физиотерапевтических процедур: озокеритовых аппликаций, электрофоретического воздействия, иглорефлексотерапии, электростимуляции.
Для улучшения самочувствия больных в Юсуповской больнице организовано диетическое питание с низким содержанием солей калия.
В целях профилактики возникновения миотонических атак пациентам рекомендуется по возможности стараться исключить провоцирующие факторы патологии: физическое перенапряжение, конфликтные ситуации, психоэмоциональные всплески, переохлаждение, долгое пребывание в одной и той же позе.
Записаться на прием к специалисту центра реабилитации Юсуповской больницы, получить подробную информацию о методах лечения миотонического синдрома и их стоимости можно по телефону или онлайн на сайте Юсуповской больницы.
лечение и симптомы, прогнозы и упражнения
Пожаловаться
Обновлено
Содержание:
Возникновение расстройства
Классификация
Клинические проявления
Негативные последствия
Диагностические мероприятия
Подходы к терапии
Видео
Миотонический синдром у детей — это совокупность расстройств тонуса мышц, характеризующаяся нарушениями сокращения мышечных волокон после расслабления. Симптоматика возникает на фоне различных приобретенных и врожденных заболеваний. Для назначения эффективного лечения врач должен выявить основную причину. Прогноз при патологии благоприятный.
Миотонический синдром у детей: симптомы и лечение
Возникновение расстройства
Причины появления нарушений мышечного тонуса не всегда удается выявить. У некоторых детей миотонический синдром развивается на фоне генетической предрасположенности. В этих случаях в генах имеются мутации, влияющие на работу мышечных волокон. Врожденные формы патологии встречаются в семьях, где ранее были схожие двигательные расстройства у детей.
У некоторых детей миотонический синдром развивается на фоне генетической предрасположенности. В этих случаях в генах имеются мутации, влияющие на работу мышечных волокон. Врожденные формы патологии встречаются в семьях, где ранее были схожие двигательные расстройства у детей.
Помимо наследственной предрасположенности, большое значение имеют следующие факторы:
- родовые травмы с поражением структур центральной нервной системы;
- тяжелое течение рахита или отсутствие его своевременной терапии;
- нарушения обмена веществ и болезни эндокринных органов;
- наличие сопутствующих нервно-мышечных патологий;
- тяжелая перинатальная энцефалопатия.
На фоне указанных состояний возникают очаги поражения головного мозга органического и функционального характера. Если факторы не устранить, то заболевание будет прогрессировать на фоне проводимого лечения.
Классификация
Врачи выделяют несколько видов миотонического синдрома. Каждый из типов нарушения имеет свои особенности возникновения и требует специфической терапии. В медицине говорят про следующие разновидности патологии:
Каждый из типов нарушения имеет свои особенности возникновения и требует специфической терапии. В медицине говорят про следующие разновидности патологии:
- дистрофическая миотония, характеризующаяся сопутствующим поражением эндокринной и вегетативной нервной системы, а также нарушениями зрения;
- врожденная парамиотония — редкий вид заболевания, сопровождающийся парезами и параличами;
- миотония Томсона, имеющая наследственный характер и проявляющаяся симптомами в возрасте от 6 до 12 лет;
- миотония Беккера — встречается чаще всего. Признаки болезни развиваются после 4 лет;
- синдром Шварца-Джампела сопровождается аномалиями скелета и тяжелой умственной отсталостью.
Конкретный вид синдрома у ребенка определяет лечащий врач на основании проведенного клинического обследования.
Клинические проявления
Миотонический синдром у детей проявляется спазмами различных групп скелетных мышц. Он возникает как в покое, так и на фоне физической нагрузки. Симптомы приводят к тому, что ребенок долгое время учится ходить и испытывает дискомфорт при любых движениях.
Он возникает как в покое, так и на фоне физической нагрузки. Симптомы приводят к тому, что ребенок долгое время учится ходить и испытывает дискомфорт при любых движениях.
Основные клинические проявления следующие:
- гипотрофия и атрофические изменения в мышцах лица и шеи;
- спастические сокращения мимической и жевательной мускулатуры;
- спазмы мышц возникают при физической активности;
- в связи со спазмами мышц ребенок часто падает и ошибается при совершении любых действий;
- у грудных детей спазмы возникают в процессе сосания;
- нарушения мышечного тонуса и движений приводят к деформации суставных сочленений;
- во время кашля развивается недержание мочи;
- в период между мышечными спазмами отмечается общая гипотония и слабость;
- нарушения глотания и дизартрия у ребенка;
- потеря и плохой набор массы тела;
- головные боли диффузного характера, возникающие без причины;
- быстрая утомляемость при физической работе;
- отставание от сверстников в физическом развитии.

Симптомы заболевания снижают качество жизни ребенка и нарушают его социальную адаптацию. В отсутствии терапии проявления прогрессируют, приводя к инвалидности.
Негативные последствия
Миотонический синдром возникает на фоне состояний, характеризующихся поражением различных внутренних органов и их систем. В связи с этим патология в отсутствии лечения приводит к осложнениям различной степени тяжести. К ним относятся:
- близорукость, имеющая тенденцию к прогрессированию;
- сколиоз и другие нарушения осанки;
- дизартрия с первых лет жизни;
- патология сердечно-сосудистой и дыхательной системы;
- энурез;
- задержка психомоторного развития
Профилактика развития осложнений — раннее обращение за медицинской помощью. Самолечение при патологии недопустимо.
Диагностические мероприятия
Разновидности миотонии выявляются с помощью электромиографии и других методов
Обследование ребенка проводят педиатр и врач-генетик. Для проведения дифференциальной диагностики между разновидностями синдрома и другими болезнями, приводящими к нарушению мышечного тонуса, необходимо комплексное использование лабораторных и инструментальных методов.
Для проведения дифференциальной диагностики между разновидностями синдрома и другими болезнями, приводящими к нарушению мышечного тонуса, необходимо комплексное использование лабораторных и инструментальных методов.
Для оценки состояния мышц и наличия их повреждений в крови определяется уровень молочной кислоты. Также в биохимическое исследование входит креатинин, печеночные ферменты и воспалительные белки (С-реактивный белок и фибриноген). Электромиография позволяет оценить функциональную способность мышц и их реакцию на возбуждающие стимулы.
Всех больных осматривает врач-невролог. Для оценки состояния головного мозга проводится электроэнцефалография, компьютерная или магнитно-резонансная томография. ЭЭГ позволяет оценить функциональную активность отдельных участков ЦНС, а КТ или МРТ — их структурную целостность.
В сложных диагностических случаях проводится биопсия мышц. Врач изучает морфологию и молекулярные изменения в мышечных волокнах, выставляя окончательный диагноз.
Подходы к терапии
Лечение основывается на комплексном подходе. Терапия подбирается только лечащим врачом после обследования ребенка. Самолечение и применение народных средств недопустимы, так как могут стать причиной прогрессирования симптоматики.
Лекарственные средства при миотоническом синдроме позволяет устранить клинические проявления болезни. Используются медикаменты со следующим действием на организм:
- устраняющие спазм мускулатуры;
- повышающие энергетический ресурс клеток;
- антиоксиданты и ноотропы;
- мембраностабилизирующие лекарства.
Помимо медикаментозной терапии обязательно проводится детский массаж. Для этого следует обратиться к квалифицированному специалисту. Неправильный массаж снижает эффективность комплексного лечения. В месяц проводится 10-12 массажных процедур.
Для нормализации мышечного тонуса и физического развития ребенка ему показана лечебная физкультура. ЛФК проводится в лечебном учреждении и дома. Используются простые упражнения: подъемы ног вверх лежа, разведение и махи руками, приседания и пр. Перечень заданий и их интенсивность зависит от возраста ребенка.
ЛФК проводится в лечебном учреждении и дома. Используются простые упражнения: подъемы ног вверх лежа, разведение и махи руками, приседания и пр. Перечень заданий и их интенсивность зависит от возраста ребенка.
При наличии дизартрии проводятся занятия с логопедом и психологом. Специалисты облегчают социальную адаптацию ребенка и способствуют улучшению обучения в детском саду и школе.
Миотонический синдром — проявление ряда неврологических и обменных заболеваний. Выявление его причины является важной частью обследования. Прогноз при раннем обращении за медицинской помощью и комплексной терапии благоприятный. Мышечный тонус ребенка постепенно нормализуется и симптоматика болезни проходит бесследно. В тяжелых случаях и при отсутствии лечения ребенок становится инвалидом и нуждается в помощи близких людей. Инвалидность развивается на фоне прогрессирующих нарушений тонуса мышц и сопутствующих изменений в костной системе.
Видео
Читайте далее: водянка головного мозга у новорожденных
* Представленная информация не может быть использована для самостоятельной постановки диагноза, определения лечения и не заменяет обращение к врачу!
РубрикаЗдоровье новорожденного
Можно ли купать ребенка при температуре: показания и противопоказания?
Причины, признаки и методы лечения вентрикуломегалии у плода
Самый дорогой подарок – бирочка, на которой написан рост, вес, дата и время рождения вашего ребенка
Комментарии
Узнавай и участвуй
Клубы на Бэби.ру — это кладезь полезной информации
Как не провести осень на больничном?Покупать ли лекарства на маркетплейсах?Как выбрать продукты для ребенка?Первая аптечка для малышаГалерея пятен вашего малыша
Если ребенок не говорит.
 .. — Голос
.. — Голос
Задержка речевого развития встречается у современных детей довольно часто. Но хватает и других неврологических проблем
Если ребенок не говорит…
Как быть, если малыш в два с половиной года произносит только слоги, упорно не желая складывать их в слова? Как заставить ребенка собираться в школу или детский сад быстрее, вернуть его из мира грез и фантазий? Эти и другие вопросы родители адресовали специалисту, врачу-неврологу Ольге Шаровой.
Моему ребенку 2,5 года, он почти не говорит. Произносит только отдельные слоги, но не слова. Нам ставят миотонический синдром. Необходимо ли обратиться к специалисту? Анна
Задержка речевого развития у ребенка в этом возрасте — повод для родителей насторожиться и показаться специалисту. Миотонический синдром сейчас встречается у детей достаточно часто. Его причина — повреждение шейного отдела позвоночника, где находится ретикулярная формация, отвечающая за тонус мышц. Необходимо делать массаж, электрофорез, причем направленный именно на шейно-воротниковую зону. Такие детки, как правило, выглядят разболтанными вследствие переразгибания, рекурвации в суставах. И в этом случае в первую очередь помогут занятия лечебной физкультурой, когда ребенок может сам «собрать» себя. Поставьте дома шведскую стенку, купите мяч с рожками, чтобы ребенок мог на нем прыгать. Для формирования мышечных каркасов подойдут плавание и гимнастика, упражнения на растяжку, пилатес, йога. Минимизируйте статические нагрузки, следите за тем, чтобы ребенок не сидел длительное время. Это чревато сколиозом и другими нарушениями опорно-двигательной системы.
Такие детки, как правило, выглядят разболтанными вследствие переразгибания, рекурвации в суставах. И в этом случае в первую очередь помогут занятия лечебной физкультурой, когда ребенок может сам «собрать» себя. Поставьте дома шведскую стенку, купите мяч с рожками, чтобы ребенок мог на нем прыгать. Для формирования мышечных каркасов подойдут плавание и гимнастика, упражнения на растяжку, пилатес, йога. Минимизируйте статические нагрузки, следите за тем, чтобы ребенок не сидел длительное время. Это чревато сколиозом и другими нарушениями опорно-двигательной системы.
Ребенку два года. Он всегда спит в одной позе — на спине, сильно запрокидывая голову назад. Это должно меня насторожить или ему просто так удобно? Ирина
Возможно, выбирая эту позу, ребенок тем самым улучшает гемооттоки, сам находит такое положение, в котором ему комфортно. Однако запрокидывание головы — это также один из признаков внутричерепной гипертензии, она может сопровождаться метеозависимостью. Нужно понимать, что внутричерепная гипертензия не появляется из ниоткуда, ее симптомы должны проявиться в более раннем возрасте, до года. Они выражаются в срыгивании, немотивированном плаче, перекресте ножек. Ребенок встает на цыпочки, не ступая на всю стопу. Также вы можете заметить это по глазам малыша. Существует такое понятие, как «синдром заходящего солнца», при котором сверху видна белая полоска оболочки глаза (склеры).
Они выражаются в срыгивании, немотивированном плаче, перекресте ножек. Ребенок встает на цыпочки, не ступая на всю стопу. Также вы можете заметить это по глазам малыша. Существует такое понятие, как «синдром заходящего солнца», при котором сверху видна белая полоска оболочки глаза (склеры).
У меня очень медлительный ребенок. Сборы в детский сад занимают у нас очень много времени. Сын может начать одеваться и замечтается о чем-то своем. В таком состоянии может находиться достаточно долго. Как помочь стать ему организованнее и собраннее? Елена
Такое поведение ребенка — это проявление синдрома нарушенного внимания в чистом виде. Его характеризуют медлительность, частые отвлечения на посторонние предметы, рассеянность. Какие можно дать советы? Портфель в школу собирайте с вечера, чтобы не тратить на это время утром. Подарите ребенку блокнот-ежедневник, в который он может записывать важную информацию, что ему необходимо сделать в течение дня. Учите ребенка выполнять самые ответственные и важные задания в первую очередь. Не нагружайте его множеством задач — не больше двух, остальные он все равно забудет. Поощряйте настольные книги, чередуйте режим труда и отдыха, обязательно проводите физкульт-минутки. Рекомендовано дообследование на гипотиреоз.
Не нагружайте его множеством задач — не больше двух, остальные он все равно забудет. Поощряйте настольные книги, чередуйте режим труда и отдыха, обязательно проводите физкульт-минутки. Рекомендовано дообследование на гипотиреоз.
Есть такая проблема у многих первоклассников, когда они не усваивают материал того или иного предмета. Я как учитель пытаюсь объяснить родителям, что во избежание проблем в дальнейшем ребенку необходимо показаться специалисту. Наталкиваюсь на полное непонимание и обиду. Взрослые твердят, что ребенок нормальный и никакого лечения ему не требуется. Как донести до родителей информацию о недальновидности такого подхода? Валентина Васильевна
Прежде всего родителям необходимо объяснить, что без лечения проблемы у ребенка будут накапливаться как снежный ком. Во-первых, у таких детей не будет никакой мотивации для учебы, а значит, и шанса после окончания школы получить высшее образование. Во-вторых, чтобы не быть голословным, необходимо наглядно продемонстрировать родителям, что у их ребенка есть проблемы. Как это сделать? Например, проведите с детьми тест Тулуз-Пьерона. Если у ребенка есть проблемы с восприятием материала, это непременно отразится на результатах теста. В-третьих, подскажите родителям несложные задания, которые они могут давать своим детям. Элементарный пример. Дайте ребенку газету или журнал и попросите на одной страничке или в одной статье вычеркнуть все буквы «а». Получилось? Усложните задание: пусть он на другой странице вычеркивает буквы «а» и обводит в кружок все буквы «о».
Как это сделать? Например, проведите с детьми тест Тулуз-Пьерона. Если у ребенка есть проблемы с восприятием материала, это непременно отразится на результатах теста. В-третьих, подскажите родителям несложные задания, которые они могут давать своим детям. Элементарный пример. Дайте ребенку газету или журнал и попросите на одной страничке или в одной статье вычеркнуть все буквы «а». Получилось? Усложните задание: пусть он на другой странице вычеркивает буквы «а» и обводит в кружок все буквы «о».
Сыну 3 года. Иногда, забегавшись, а бывает и ночью, он писается. Нужно ли бить тревогу, что у него энурез? Виктория
Ребенку младше 5 лет диагноз «энурез» не ставится. Если ребенок старше этого возраста мочится два раза в неделю, не пробуждается ночью, чтобы сходить в туалет, то да — можно говорить о признаках энуреза. Энурезы бывают разные — ночные, дневные, сочетанные формы. Они характеризуются тем, что мочевой пузырь опорожняется автономно. Происходит это вследствие того, что при его наполнении сигнал не дошел до коры головного мозга. Значит, где-то этот сигнал блокируется и необходимо искать уровень, где это происходит. В зависимости от результата поиска будет подбираться разное лечение.
Значит, где-то этот сигнал блокируется и необходимо искать уровень, где это происходит. В зависимости от результата поиска будет подбираться разное лечение.
У меня дочь школьного возраста. В последнее время часто жалуется на боли в шее. Это опасно? Ольга
При нарушении работы шейного отдела позвоночника может возникать онемение рук, плече-лопаточные периартриты. Что необходимо сделать, чтобы избежать этого? Я за немедикаментозное лечение: иглотерапию, физиопроцедуры, массаж. Ребенку не нужно носить тяжестей. Следует активно заниматься плаванием, скандинавской ходьбой, йогой, выполнять упражнения на растяжку. Также я бы рекомендовала сделать рентгеновский снимок и при необходимости получить консультацию специалиста.
Миотонический синдром у детей особенности, миопатическая болезнь у взрослых
Миотонический синдром – это цепь различных нарушений внутри мышц, во время которых страдает функция мышечного волокна сокращаться после процесса расслабления. По какой причине развивается миотонический синдром у маленьких детей и как преодолеть это заболевание?
- Особенности развития миотонического синдрома и характер заболевания у детей
- Главная симптоматика болезни
- Развитие миотонических атак у ребёнка
- Последствия после болезни
- Определение наличия болезни в организме
- Особенности лечения организма ребёнка
- Главные методы лечения миотонии
- Миотонический синдром возможные причины появления и прогрессирования
- Общая клиническая картина
Миотонический синдром – это не одна болезнь. Как можно понять из названия, под этой болезнью кроется целая совокупность различных симптомов, которые связаны с дисфункцией в работе отдельных групп мышц. Данная болезнь может происходить во время разных врождённых, а также приобретённых заболеваний, быть лишь главным признаком либо оставаться одним симптомом из общего заболевания.
Как можно понять из названия, под этой болезнью кроется целая совокупность различных симптомов, которые связаны с дисфункцией в работе отдельных групп мышц. Данная болезнь может происходить во время разных врождённых, а также приобретённых заболеваний, быть лишь главным признаком либо оставаться одним симптомом из общего заболевания.
Миотония у детей чаще всего развивается по причинам:
- Генетическая предрасположенность организма малыша.
- Родовые травмы.
- Рахит и различные болезни, которые связаны с нарушением правильного синтеза веществ в организме.
- Нарушение правильного внутриутробного развития нервной системы (мозжечка, а также подкорковых ядер).
Миотония у малышей и детей после первого года жизни чаще всего имеет врождённую форму. Узнать точную причину развития этой болезни удаётся в очень редких случаях. Использование лекарственных средств на ранних сроках вынашивания ребёнка, перенесения тяжёлых инфекций, проживание в области с плохой экологией и жизненным фоном – все эти факторы могут отрицательно повлиять на процесс формирования и роста плода и может приводить к развитию миотонической болезни.
Миотония – это болезнь, от которой больше всего страдают лишь скелетные мышцы. Именно данные мышечные волокна отвечают у человека за произвольные передвижения частей тела (туловища, конечностей и головы). Гладкой мускулатуре человека внутренних органов, которая сокращается самостоятельно без воздействия со стороны человека, такая опасность не грозит.
Главная симптоматика болезни
Миотония у малыша может возникать совершенно в любом возрасте. Если существует врождённая патология, то первые симптомы болезни дают понять о себе скоро после появления малыша на свет. У малыша проявляется выраженная гипотония мышц. Малыш позже всех своих сверстников начинает самостоятельно удерживать голову, переворачиваться на другую сторону, вставать на ноги.
Отставание в развитии физического состояния ребёнка может оставаться совершенно незаметным для окружающих, и тогда родители малыша попросту не смогут распознать эту болезни и симптоматику. В будущем даже небольшая миотония способна негативно сказаться на ребёнке и вызвать негативные последствия и различные болезни.
В будущем даже небольшая миотония способна негативно сказаться на ребёнке и вызвать негативные последствия и различные болезни.
Так, регулярное посещение врача педиатра на первом году жизни младенца помогут заранее выявить патологию в организме и начать лечение.
У ребёнка более старшего возраста миотоническое заболевание возникает со следующими симптомами:
- Общая мышечная слабость в организме.
- Регулярная потеря равновесия и координации движения во время передвижения.
- Быстрая утомляемость во время бега либо подъёма по лестнице.
Миотония у малыша чаще всего возникает по причине поражения нижней конечности. Первые острые симптомы родители замечают во время прогулки, при подъёме по лестнице, пробежке либо игре. Ещё недавно полностью здоровый ребёнок начинает часто останавливаться, делать передышки, проситься на руки либо в коляску, теряет своё равновесие и падает. Если такая проблема проявляется и не связана с утомлением либо наличием инфицирования у ребёнка, то следует пристально обратить внимание на такой симптом и обратиться за помощью к лечащему специалисту.
Детям, которые обладают синдромом миотонии, тяжело совершать движения, которые требуют особой ловкости и сосредоточенности. Ходьба по борту, прыжки на определённой ноге, замирание на одном месте в процессе игры – всё это плохо получается у малыша. Деятельность, которая требует от малыша напряжения мелких мышц кисти, также приносит ребёнку большое количество трудностей.
Основной симптом наличия миотонии – это выраженный спазм мышц у ребёнка в процессе лёгкого удара по ним. Волокна в мышцах в это время медленно сокращаются, что чаще всего происходит совместно с болезненными ощущениями внутри руки. Процесс расслабления также происходит очень долго. После полного расслабления можно почувствовать напряжение в мышечном валике малыша.
Развитие миотонических атак у ребёнка
Миотоническая атака – это одно из типичных проявлений этой патологии. Родители могут увидеть, как малыш во время попыток встать либо убежать сначала замирает на некоторое время, а потом падает на землю. После ребёнка совершает определённое усилие — и продолжает начатое действие. С течением времени миотонические атаки могут возникать всё чаще и чаще.
После ребёнка совершает определённое усилие — и продолжает начатое действие. С течением времени миотонические атаки могут возникать всё чаще и чаще.
Подобное явление в миотоническом синдроме связано с особенностями изменения в функционировании мышц малыша. Мышечные волокна, которые не могут быстро сокращаться и полноценно расслабляться, не могут нормально реагировать на запросы и попытки ребёнка совершать какое – либо передвижение. При попытке совершить какое-либо передвижение ребёнок теряет своё равновесие и попросту падает. Через некоторое время мышца ребёнка приходят в норму и он может свободно продолжать свои действия. Чем больше движений будет совершать малыш в это время, тем быстрее будут проходить миотанические атаки.
Последствия после болезни
Миотонический синдром у детей в редких случаях проходит, не оставляя после себя никаких последствий. Даже лёгкая форма синдрома способна развить у малыша разные проблемы с организмом:
- Нарушение осанки и искривление позвоночника.

- Запоры.
- Энурёз.
- Боли в голове.
- Быстрый процесс утомляемости, а также выраженная слабость.
- Расстройства, связанные с речевой функцией.
- Наличие близорукости.
Все представленные выше осложнения обладают единичной причиной – снижение функционирования волокон в мышцах. Мышцы, которые теряют свою способность нормально расслабляться и качественно сокращаться, не могут полностью сохранить свои функции. Слабость в спинных мышцах может привести к развитию неправильной осанки у ребёнка, брюшного пресса – к запорам и другим патологиям с пищеварительной системой ребёнка. С течением времени у ребёнка происходит накапливание большого букета разных проблем со здоровьем, и справиться с симптомами мионии становится всё сложнее и сложнее.
Определение наличия болезни в организме
Поставить предварительный диагноз может сам невролог уже после полного осмотра малыша. Затягивать с обращением к лечащему специалисту за помощью не рекомендуется. Чем быстрее врач сможет определить причину развития болезни, тем проще будет устранить последствия и осложнения заболевания.
Чем быстрее врач сможет определить причину развития болезни, тем проще будет устранить последствия и осложнения заболевания.
Для того чтобы поставить точный диагноз делается электромиография. Данный метод основан главным образом на измерении электрической активности в мышцах, их способности совершать сокращение и расслабление. Если это необходимо, то невролог способен отправить маленького пациента на осмотр у других специалистов (офтальмолог, а также гастроэнтеролог).
Особенности лечения организма ребёнка
Эффективное лечение для нарушенных мышц ещё до сих пор не найдено. Миотинический синдром развивается с человеком на протяжении всей его жизни. Всё, что может предложить лечащий специалист – это снизить возможность проявления и развития данного осложнения, а также улучшить качество жизни малыша.
Главные методы лечения миотонии
- Лечебная гимнастика.
Двигательная активность – это очень важная часть для достижения особого успеха в методе лечения ребёнка от миотонического заболевания. Заниматься с малышом стоит с самого раннего возраста. С младенцем можно проделывать простые движения конечностей – велосипед. Разминка для мышц ребёнка должна стать ежедневным занятием – только в это время может произойти должный эффект в организме ребёнка и произойти положительный результат.
Заниматься с малышом стоит с самого раннего возраста. С младенцем можно проделывать простые движения конечностей – велосипед. Разминка для мышц ребёнка должна стать ежедневным занятием – только в это время может произойти должный эффект в организме ребёнка и произойти положительный результат.
Создайте из зарядки весёлую игру — именно тогда ребёнок начнётся с увлечением поддерживать оздоровительное занятие и всегда будет принимать в нём активное участие.
Обучение малыша навыкам продвижению требует от родителей большого количества терпения и понимания. Если ребёнок не встанет на ноги, то нужно будет каждый раз приподнимать его самостоятельно, при этом показывая, как и в какое место стоит ставить ноги для дальнейшей опоры. Ребёнок, который обладает синдромом миотонии, на протяжении долгого времени будет передвигаться, держась за руку родителей. Гиподинамия для такого ребёнка очень опасна. Чем больше малыш начнёт двигаться в повседневной жизни, тем легче ему будет побороть данное заболевание, а также уйти от возможных осложнений в организме.
Все дети с миотонией должны всегда ходить в бассейн. Плавание – это наилучший способ для того чтобы повысить крепость мышц, а также улучшить тонус всего организма. Грудничка можно учить плаванию в простой ванне, применяя при этом надувной круг либо другие специализированные предметы. Малышам в более старшем возрасте нужно выделить уже большее пространство. В летнее время стоит как можно больше выбираться с ребёнком на пляж и давать ему плавать в воде столько, сколько ему нужно.
- Применение массажа.
Сеансы терапии массажа нужно проводить совместно с профессиональным мастером, который может грамотно работать с детьми и уже имел до этого определённый опыт. Чаще всего сеанс простого массажа происходит в течение 10 дней, после которых лечащий врач оценивает качество и эффект после совершённой процедуры лечения. Если возникает особая необходимость, то можно повторять курс терапии через каждый 3–6 месяца. Будет хорошо, если родитель научится совершать простой массаж самостоятельно.
- Физиолечение ребёнка.
Физиотерапия применяется во время развития миотонического синдрома ещё с самого раннего возраста. Электрофорез и различные другие процедуры происходят в самой поликлинике. Длительность и регулярность терапии лечения будет установлена лечащим врачом.
- Лечение при помощи медикаментов.
Использование во время синдрома миотонии лекарственных средств не во всех случая является правильным действием. В большинстве случаев справиться с таким заболеванием способен массаж либо специальная гимнастика. Терапия медикаментами используется лишь в серьёзных случаях, когда болезнь требует особого лечения. Вопрос об использовании тех либо иных препаратов решается индивидуально после консультации с лечащим специалистом.
Миотонический синдром возможные причины появления и прогрессирования
Миотонический синдром у ребёнка, при условии того, что он обладает врождённое формой, является заболеванием наследственного характера. На сегодняшний день медицина ещё не смогла с точностью назвать фактор, влияющий на развитие данного заболеваний но в качестве провоцирующего фактора в большинстве ситуаций специалисты выделяют поражение в подкорковых ядрах, патологические процессы внутри мозжечка и различные нарушения, которые связаны с вегетативными нервными центрами в организме ребёнка.
На сегодняшний день медицина ещё не смогла с точностью назвать фактор, влияющий на развитие данного заболеваний но в качестве провоцирующего фактора в большинстве ситуаций специалисты выделяют поражение в подкорковых ядрах, патологические процессы внутри мозжечка и различные нарушения, которые связаны с вегетативными нервными центрами в организме ребёнка.
В то время, когда миотонический синдром не является следствием генетического заболевания, то в качестве причины болезни можно выделить такие заболевания, как рахит, нарушение в обменен веществ, различные нарушения внутриутробного характера, а также травмы , развивающиеся в процессе родов. Следует отметить, что часто происходят такие ситуации, когда диагноз болезни не распознаётся: состояние тонуса мышц ребёнка может быть ошибочно охарактеризовано.
Общая клиническая картина
Миотонический синдром у ребёнка характеризуется свободным процессом затруднения двигательных действий. Если в нормальной ситуации мышцы после своего сокращения сразу же начинают расслабляться, то в этом случае, всё происходит наоборот, происходит тоническое напряжение. После того, как происходит несколько сокращений подряд, мышца начинает со временем расслабляться. Дальнейшее её функционирование происходит намного проще. В общем, симптоматика у малыша начинается с поражения нижних конечностей, поэтому специалисты говорят родителям обращать пристальное внимание на то, как ребёнок спускается, а также поднимается по лестнице.
После того, как происходит несколько сокращений подряд, мышца начинает со временем расслабляться. Дальнейшее её функционирование происходит намного проще. В общем, симптоматика у малыша начинается с поражения нижних конечностей, поэтому специалисты говорят родителям обращать пристальное внимание на то, как ребёнок спускается, а также поднимается по лестнице.
Миотонический синдром у детей лечение. Миотонический синдром у детей
Содержание
- Особенности развития миотонического синдрома и характер заболевания у детей
- Главная симптоматика болезни
- Развитие миотонических атак у ребёнка
- Последствия после болезни
- Определение наличия болезни в организме
- Особенности лечения организма ребёнка
- Главные методы лечения миотонии
- Миотонический синдром возможные причины появления и прогрессирования
- Миотонический синдром причины
- Диагностика
- МРТ (магнитно-резонансная томография)
- Чек-ап (комплексное обследование организма)
- Компьютерная электроэнцефалография
- Компьютерная топография позвоночника Diers
- Дуплексное сканирование
- УЗИ (ультразвуковое исследование)
- КТ (компьютерная томография)
- Лечение
- Медикаментозное лечение
- Массаж
- Электрофорез
- Гимнастика
- Симптомы
- Диагностика миотонии у ребёнка
- Основные проявления
- Видео: лекция о врожденном миотоническом синдроме
- Рекомендации родителям
- Лечебные мероприятия
- Осложнения
- Последствия
- Медикаментозное воздействие
- Как выявить отклонение у детей?
- К какому врачу обратиться
- Лалаян Тигран Владимирович
- Понеделко Татьяна Сергеевна
- Мальцев Сергей Игоревич
- Троицкая Татьяна Евгеньевна
- Астахова Елена Вячеславовна
- Александров Антон Валерьевич
- Гаджимурадов Абдула Гаджимурадович
- Смирнов Егор Николаевич
- Телеев Марат Султанбекович
- Бодань Станислав Михайлович
- Булацкий Сергей Олегович
- Всему виной гены!
- Проявление недуга у взрослых
- Другие причины
- Миотоническая атака
Особенности развития миотонического синдрома и характер заболевания у детей
Миотонический синдром – это не одна болезнь. Как можно понять из названия, под этой болезнью кроется целая совокупность различных симптомов, которые связаны с дисфункцией в работе отдельных групп мышц. Данная болезнь может происходить во время разных врождённых, а также приобретённых заболеваний, быть лишь главным признаком либо оставаться одним симптомом из общего заболевания.
Как можно понять из названия, под этой болезнью кроется целая совокупность различных симптомов, которые связаны с дисфункцией в работе отдельных групп мышц. Данная болезнь может происходить во время разных врождённых, а также приобретённых заболеваний, быть лишь главным признаком либо оставаться одним симптомом из общего заболевания.
Миотония у детей чаще всего развивается по причинам:
- Генетическая предрасположенность организма малыша.
- Родовые травмы.
- Рахит и различные болезни, которые связаны с нарушением правильного синтеза веществ в организме.
- Нарушение правильного внутриутробного развития нервной системы (мозжечка, а также подкорковых ядер).
Миотония у малышей и детей после первого года жизни чаще всего имеет врождённую форму. Узнать точную причину развития этой болезни удаётся в очень редких случаях. Использование лекарственных средств на ранних сроках вынашивания ребёнка, перенесения тяжёлых инфекций, проживание в области с плохой экологией и жизненным фоном – все эти факторы могут отрицательно повлиять на процесс формирования и роста плода и может приводить к развитию миотонической болезни.
Миотония – это болезнь, от которой больше всего страдают лишь скелетные мышцы. Именно данные мышечные волокна отвечают у человека за произвольные передвижения частей тела (туловища, конечностей и головы). Гладкой мускулатуре человека внутренних органов, которая сокращается самостоятельно без воздействия со стороны человека, такая опасность не грозит.
Главная симптоматика болезни
Миотония у малыша может возникать совершенно в любом возрасте. Если существует врождённаяпатология, то первые симптомы болезни дают понять о себе скоро после появления малыша на свет. У малыша проявляется выраженная гипотония мышц. Малыш позже всех своих сверстников начинает самостоятельно удерживать голову, переворачиваться на другую сторону, вставать на ноги.
Отставание в развитии физического состояния ребёнка может оставаться совершенно незаметным для окружающих, и тогда родители малыша попросту не смогут распознать эту болезни и симптоматику. В будущем даже небольшая миотония способна негативно сказаться на ребёнке и вызвать негативные последствия и различные болезни.
В будущем даже небольшая миотония способна негативно сказаться на ребёнке и вызвать негативные последствия и различные болезни.
Так, регулярное посещение врача педиатра на первом году жизни младенца помогут заранее выявить патологию в организме и начать лечение.
У ребёнка более старшего возраста миотоническое заболевание возникает со следующими симптомами:
- Общая мышечная слабость в организме.
- Регулярная потеря равновесия и координации движения во время передвижения.
- Быстрая утомляемость во время бега либо подъёма по лестнице.
Миотония у малыша чаще всего возникает по причине поражения нижней конечности. Первые острые симптомы родители замечают во время прогулки, при подъёме по лестнице, пробежке либо игре. Ещё недавно полностью здоровый ребёнок начинает часто останавливаться, делать передышки, проситься на руки либо в коляску, теряет своё равновесие и падает. Если такая проблема проявляется и не связана с утомлением либо наличием инфицирования у ребёнка, то следует пристально обратить внимание на такой симптом и обратиться за помощью к лечащему специалисту.
Детям, которые обладают синдромом миотонии, тяжело совершать движения, которые требуют особой ловкости и сосредоточенности. Ходьба по борту, прыжки на определённой ноге, замирание на одном месте в процессе игры – всё это плохо получается у малыша. Деятельность, которая требует от малыша напряжения мелких мышц кисти, также приносит ребёнку большое количество трудностей.
Основной симптом наличия миотонии – это выраженный спазм мышц у ребёнка в процессе лёгкого удара по ним. Волокна в мышцах в это время медленно сокращаются, что чаще всего происходит совместно с болезненными ощущениями внутри руки. Процесс расслабления также происходит очень долго. После полного расслабления можно почувствовать напряжение в мышечном валике малыша.
Развитие миотонических атак у ребёнка
Миотоническая атака – это одно из типичных проявлений этой патологии. Родители могут увидеть, как малыш во время попыток встать либо убежать сначала замирает на некоторое время, а потом падает на землю. После ребёнка совершает определённое усилие — и продолжает начатое действие. С течением времени миотонические атаки могут возникать всё чаще и чаще.
После ребёнка совершает определённое усилие — и продолжает начатое действие. С течением времени миотонические атаки могут возникать всё чаще и чаще.
Подобное явление в миотоническом синдроме связано с особенностями изменения в функционировании мышц малыша. Мышечные волокна, которые не могут быстро сокращаться и полноценно расслабляться, не могут нормально реагировать на запросы и попытки ребёнка совершать какое – либо передвижение. При попытке совершить какое-либо передвижение ребёнок теряет своё равновесие и попросту падает. Через некоторое время мышца ребёнка приходят в норму и он может свободно продолжать свои действия. Чем больше движений будет совершать малыш в это время, тем быстрее будут проходить миотанические атаки.
Последствия после болезни
Миотонический синдром у детей в редких случаях проходит, не оставляя после себя никаких последствий. Даже лёгкая форма синдрома способна развить у малыша разные проблемы с организмом:
- Нарушение осанки и искривление позвоночника.
- Запоры.
- Энурёз.
- Боли в голове.
- Быстрый процесс утомляемости, а также выраженная слабость.
- Расстройства, связанные с речевой функцией.
- Наличие близорукости.
Все представленные выше осложнения обладают единичной причиной – снижение функционирования волокон в мышцах. Мышцы, которые теряют свою способность нормально расслабляться и качественно сокращаться, не могут полностью сохранить свои функции. Слабость в спинных мышцах может привести к развитию неправильной осанки у ребёнка, брюшного пресса – к запорам и другим патологиям с пищеварительной системой ребёнка. С течением времени у ребёнка происходит накапливание большого букета разных проблем со здоровьем, и справиться с симптомами мионии становится всё сложнее и сложнее.
Определение наличия болезни в организме
Поставить предварительный диагноз может сам невролог уже после полного осмотра малыша. Затягивать с обращением к лечащему специалисту за помощью не рекомендуется. Чем быстрее врач сможет определить причину развития болезни, тем проще будет устранить последствия и осложнения заболевания.
Чем быстрее врач сможет определить причину развития болезни, тем проще будет устранить последствия и осложнения заболевания.
Для того чтобы поставить точный диагноз делается электромиография. Данный метод основан главным образом на измерении электрической активности в мышцах, их способности совершать сокращение и расслабление. Если это необходимо, то невролог способен отправить маленького пациента на осмотр у других специалистов (офтальмолог, а также гастроэнтеролог).
Особенности лечения организма ребёнка
Эффективное лечение для нарушенных мышц ещё до сих пор не найдено. Миотинический синдром развивается с человеком на протяжении всей его жизни. Всё, что может предложить лечащий специалист – это снизить возможность проявления и развития данного осложнения, а также улучшить качество жизни малыша.
Главные методы лечения миотонии
- Лечебная гимнастика.
Двигательная активность – это очень важная часть для достижения особого успеха в методе лечения ребёнка от миотонического заболевания. Заниматься с малышом стоит с самого раннего возраста. С младенцем можно проделывать простые движения конечностей – велосипед. Разминка для мышц ребёнка должна стать ежедневным занятием – только в это время может произойти должный эффект в организме ребёнка и произойти положительный результат.
Заниматься с малышом стоит с самого раннего возраста. С младенцем можно проделывать простые движения конечностей – велосипед. Разминка для мышц ребёнка должна стать ежедневным занятием – только в это время может произойти должный эффект в организме ребёнка и произойти положительный результат.
Создайте из зарядки весёлую игру — именно тогда ребёнок начнётся с увлечением поддерживать оздоровительное занятие и всегда будет принимать в нём активное участие.
Обучение малыша навыкам продвижению требует от родителей большого количества терпения и понимания. Если ребёнок не встанет на ноги, то нужно будет каждый раз приподнимать его самостоятельно, при этом показывая, как и в какое место стоит ставить ноги для дальнейшей опоры. Ребёнок, который обладает синдромом миотонии, на протяжении долгого времени будет передвигаться, держась за руку родителей. Гиподинамия для такого ребёнка очень опасна. Чем больше малыш начнёт двигаться в повседневной жизни, тем легче ему будет побороть данное заболевание, а также уйти от возможных осложнений в организме.
Все дети с миотонией должны всегда ходить в бассейн. Плавание – это наилучший способ для того чтобы повысить крепость мышц, а также улучшить тонус всего организма. Грудничка можно учить плаванию в простой ванне, применяя при этом надувной круг либо другие специализированные предметы. Малышам в более старшем возрасте нужно выделить уже большее пространство. В летнее время стоит как можно больше выбираться с ребёнком на пляж и давать ему плавать в воде столько, сколько ему нужно.
- Применение массажа.
Сеансы терапии массажа нужно проводить совместно с профессиональным мастером, который может грамотно работать с детьми и уже имел до этого определённый опыт. Чаще всего сеанс простого массажа происходит в течение 10 дней, после которых лечащий врач оценивает качество и эффект после совершённой процедуры лечения. Если возникает особая необходимость, то можно повторять курс терапии через каждый 3–6 месяца. Будет хорошо, если родитель научится совершать простой массаж самостоятельно.
Будет хорошо, если родитель научится совершать простой массаж самостоятельно.
- Физиолечение ребёнка.
Физиотерапия применяется во время развития миотонического синдрома ещё с самого раннего возраста. Электрофорез и различные другие процедуры происходят в самой поликлинике. Длительность и регулярность терапии лечения будет установлена лечащим врачом.
- Лечение при помощи медикаментов.
Использование во время синдрома миотонии лекарственных средств не во всех случая является правильным действием. В большинстве случаев справиться с таким заболеванием способен массаж либо специальная гимнастика. Терапия медикаментами используется лишь в серьёзных случаях, когда болезнь требует особого лечения. Вопрос об использовании тех либо иных препаратов решается индивидуально после консультации с лечащим специалистом.
Миотонический синдром возможные причины появления и прогрессирования
Миотонический синдром у ребёнка, при условии того, что он обладает врождённое формой, является заболеванием наследственного характера. На сегодняшний день медицина ещё не смогла с точностью назвать фактор, влияющий на развитие данного заболеваний но в качестве провоцирующего фактора в большинстве ситуаций специалисты выделяют поражение в подкорковых ядрах, патологические процессы внутри мозжечка и различные нарушения, которые связаны с вегетативными нервными центрами в организме ребёнка.
На сегодняшний день медицина ещё не смогла с точностью назвать фактор, влияющий на развитие данного заболеваний но в качестве провоцирующего фактора в большинстве ситуаций специалисты выделяют поражение в подкорковых ядрах, патологические процессы внутри мозжечка и различные нарушения, которые связаны с вегетативными нервными центрами в организме ребёнка.
В то время, когда миотонический синдромне является следствием генетического заболевания, то в качестве причины болезни можно выделить такие заболевания, как рахит, нарушение в обменен веществ, различные нарушения внутриутробного характера, а также травмы , развивающиеся в процессе родов. Следует отметить, что часто происходят такие ситуации, когда диагноз болезни не распознаётся: состояние тонуса мышц ребёнка может быть ошибочно охарактеризовано.
Миотонический синдром причины
Миотонический синдром может быть врождённым заболеванием и проявиться уже в первые месяцы жизни человека. К основным причинам его возникновения врачи относят поражения ядер подкорки головного мозга, патологию мозжечка и сбои в работе вегетативных нервных центров. Если же проявления синдрома на обусловлены генными причинами, можно сделать вывод что его появление обусловлено детскими патологиями, такими, как рахит, сбои течения процесса обмена веществ, травмы, полученные при родах, нарушения внутриутробного развития плода. Необходимо отметить, что встречаются случаи, когда первоначальный диагноз не подтверждается, при этом может иметь место неправильная интерпретация тонуса мышц.
К основным причинам его возникновения врачи относят поражения ядер подкорки головного мозга, патологию мозжечка и сбои в работе вегетативных нервных центров. Если же проявления синдрома на обусловлены генными причинами, можно сделать вывод что его появление обусловлено детскими патологиями, такими, как рахит, сбои течения процесса обмена веществ, травмы, полученные при родах, нарушения внутриутробного развития плода. Необходимо отметить, что встречаются случаи, когда первоначальный диагноз не подтверждается, при этом может иметь место неправильная интерпретация тонуса мышц.
Диагностика
С подозрениями на миотонический синдром необходимо обращаться к неврологу. Если болезнь проявляется в детском возрасте изначально потребуется консультация педиатра, который перенаправит к детскому неврологу. Для диагностики миотонического синдрома врач проводит внешний неврологический осмотр, изучает историю болезни, расспрашивает о возможной патологической наследственности. Специалист попросит сжать и разжать кулак. Замедленное разжимание, которое проходит после нескольких попыток, подтверждает диагноз миотонии.
Замедленное разжимание, которое проходит после нескольких попыток, подтверждает диагноз миотонии.
С помощью лабораторных анализов выявляют антитела к кальциевым каналам. Подтверждением миотонического синдрома служат данные игольчатой электромиографии, биопсии мышц, биохимического анализа крови, генетического анализа. Необходимо исключить заболевания с подобными проявлениями: синдром ригидного человека, миопатию, функциональные нарушения щитовидной железы.
В сети клиник ЦМРТ диагностику причин миотонического синдрома проводят с помощью следующих исследований:
МРТ (магнитно-резонансная томография)
Чек-ап (комплексное обследование организма)
Компьютерная электроэнцефалография
Компьютерная топография позвоночника Diers
Дуплексное сканирование
УЗИ (ультразвуковое исследование)
КТ (компьютерная томография)
Лечение
На сегодняшний день нет действенной терапевтической методики, которая позволяет устранить в полной мере какой-либо миотонический синдром. Терапия будет иметь симптоматический характер. Когда миотонические атаки станут интенсивнее, появится необходимость использования медикаментозных средств, которые позволят уменьшить симптомы.
Терапия будет иметь симптоматический характер. Когда миотонические атаки станут интенсивнее, появится необходимость использования медикаментозных средств, которые позволят уменьшить симптомы.
Кроме того, симптоматическое лечение заболевания в обязательном порядке предполагает такие методы:
- Мануальный массаж.
- Лечебные гимнастические упражнения (с 5-летнего возраста).
- Иглорефлексотерапия.
- Физиотерапевтические процедуры (электрофорез).
- Вспомогательная работа с психологами и логопедом.
Терапия миотонии будет зависеть от фактора, который спровоцировал возникновение патологического процесса. Когда болезнь приобретенная, специалиста назначат комплексное лечение, которое устраняет этиопатогенетические причины и последствия их влияния. Врожденная форма патология является неизлечимой, которая останется в течение всей жизни. Общетерапевтические меры могут в существенной степени облегчить самочувствие пациента, потому станут обязательными к выполнению.
Медикаментозное лечение
Часть специалистов полагает, что бороться с миотонией с помощью медикаментозных средств бездейственно, а положительные изменения возможны лишь при постоянной физической нагрузке. Устанавливает уровень нагрузки лишь специалист. Однако, чтобы устранить мышечное спазмирование, в определенных ситуациях назначают лекарственное средство «Фенитоин». Является мышечным релаксантом, который обладает антисудорожным эффектом. Дневную дозировку препарата рассчитывают с учетом массы тела и возрастных показателей больного. Во взрослом возрасте она не превышает 500 мг, в детском – не более 300 мг в день.
Кроме того, при миотонии назначаются такие медикаменты:
- Актовегин. Активизирует обменные процессы в тканях, улучшает трофику и клеточный метаболизм, стимулирует регенерацию.

- Пантогам. Ноотропное лекарственное средство, которое используется чтобы запустить клеточный метаболизм в мозге и устранить последствия психомоторного возбуждения.
- Элькар. Принимается, чтобы повысить активность в головном мозге, привести в норму процессы обмена.
- Кортексин. Мощный антиоксидант и антигипоксант, который используется в целях улучшения функционирования головного мозга и невосприимчивости организма к раздражителям извне.
- Верошпирон, Гипотиазид. Диуретические препараты, которые снижают содержание калия в кровотоке, в основном увеличивается после приступа.
- Церебролизин. Принимают, чтобы стимулировать деятельность мозга.
В сложных ситуациях необходимо проводить иммуносупрессивное лечение – внутривенно вводится Иммуноглобулин, Преднизолон, Циклофосфамид.
Массаж
Существенно облегчить самочувствие возможно после проведения массажа, как дополнительного терапевтического метода. Под воздействием массажа становится лучше функциональное состояние в мышцах и нервных окончаниях, снижается рефлекторная возбудимость и улучшается мышечное сокращение, устраняется напряжение.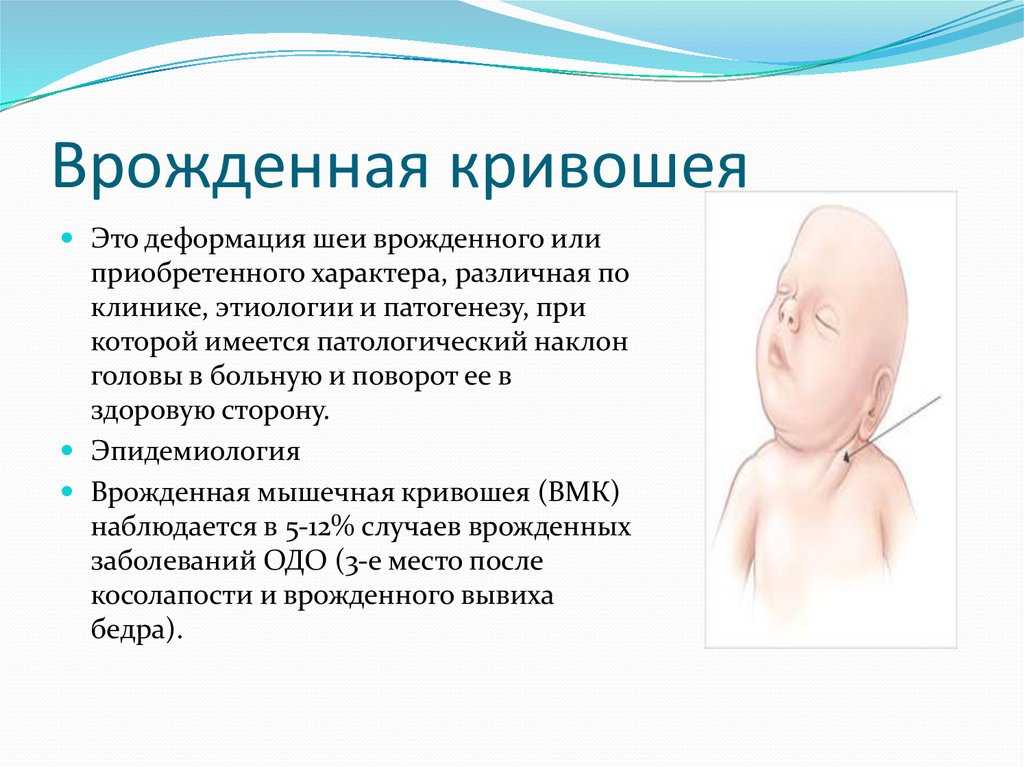 Процедура проводится на спине и в пояснично-крестцовом отделе, основной акцент делается на месте выхода спинальных нервных окончаний по паравертебральным линиям. Массаж отличается умеренной интенсивностью и состоит из поглаживаний и растираний.
Процедура проводится на спине и в пояснично-крестцовом отделе, основной акцент делается на месте выхода спинальных нервных окончаний по паравертебральным линиям. Массаж отличается умеренной интенсивностью и состоит из поглаживаний и растираний.
Вся процедура продолжается не больше 40 минут каждый день. На массаж спины и в пояснично-крестцовом отделе отводят четверть часа, на 1 руку – до 5 минут, на ногу – до 8 минут. Длительность терапии – приблизительно 15 сеансов. Курсы повторяются постоянно по прошествии 1-1,5 месяцев в течение продолжительного периода времени. Когда вовлекаются в массаж мимическая и жевательная мускулатура, требуется провести массаж спереди и сзади шейного отдела и лицевой части. В данных областях проводится лишь поглаживание и растирание.
Давления рук специалиста в процессе осуществления массажа на лице и шейном отделе небольшое, а движения рук — плавные, мягкие, эластичные и медленные.
Электрофорез
В качестве дополнительной терапевтической методики при наличии миотонии больным могут быть назначены физиопроцедуры:
- озокеритовые аппликации,
- электрофоретическое воздействие,
- иглорефлексотерапия,
- электростимуляция.

Электрофорез дает существенное облегчение пациентам, которые страдают от рассматриваемого патологического процесса. Методика полностью безболезненна и предусматривает местное введение медикаментозных средств с помощью тока постоянной частоты.
Гимнастика
Лечебные гимнастические упражнения во время миотонического синдрома, которые назначаются в определенном дозировании, рассматривают как способ активирования организма. Гимнастика дает антипарабиотический эффект, усиливается адаптационно-трофическое воздействие и повышается качество движений. Помимо лечебных упражнений, которые считаются наиболее действенными, также рекомендуется трудотерапия и прогулки пешком.
Комплекс гимнастических занятий во время патологических болезней данного типа основывается на мышечном гипертонусе и имеющейся быстрой утомляемости. Непосредственно потому гимнастика во время миотонического синдрома должна отличаться простотой и отсутствием напряжения.
Эффективно проводить тренинг с палкой, добавляя элементы коррекции и перебрасывания, прокатывания мяча. Махи и расслабляющие движения обладают прямым практическим значением. Дыхательная гимнастика помогает предотвратить физическую усталость и в целях дозирования общих нагрузок. Подобный тренинг выполняется с определенной ритмичностью, однако в размеренном темпе, повышая количество движений поэтапно. Гимнастику оптимально осущестлвять в обособленном помещении, создав специальную атмосферу.
Махи и расслабляющие движения обладают прямым практическим значением. Дыхательная гимнастика помогает предотвратить физическую усталость и в целях дозирования общих нагрузок. Подобный тренинг выполняется с определенной ритмичностью, однако в размеренном темпе, повышая количество движений поэтапно. Гимнастику оптимально осущестлвять в обособленном помещении, создав специальную атмосферу.
Изначальные положения – вертикально либо сидя (чередуются). Процесс продолжается до трети часа. Как и лечебные упражнения для ребенка, предполагают временные интервалы для отдыха. Гимнастический тренинг рекомендовано осуществлять в утреннее время, по прошествии 1-2 часов по окончании трапезы. Повторяется каждый комплекс трижды в сутки.
В соответствии с медицинскими исследованиями, лечебные гимнастические упражнения в значительной степени увеличивают подвижность в мышцах, на определенное время облегчает пациентам двигательную активность, увеличивают динамические и статические мышечные показатели.
Симптомы
В основе патологии, лежит увеличение отдельных мышц, но одновременно с этим, можно увидеть истощение мышечного волокна. Первый дебют патологии приходится на возрастную группу 8 – 14 лет, и первыми признаками будут миотонические спазмы – мышцы после напряжения плохо и медленно расслабляются.
Эти спазмы могут локализоваться в различных мышечных группах, но чаще в конечностях, жевательной мускулатуре и др. Для диагностирования патологии достаточно провести определённый тест – ребёнка просят сжать кулак и после резко распрямить кисть. Дети с патологией не могут сделать это быстро.
Внешний вид ребёнка при этом довольно своеобразный, из-за разрастания различный мышц, фигура малыша серьёзно изменяется и становится похожа на атлетическую. При осмотре у доктора, определяется уплотнённые мышцы, они становятся твёрдыми, но при исследовании мышечной силы, отмечается их уменьшение. Для патологии характерно медленное течение, при этом трудоспособность ребёнка сохраняется.
Миотонии – собирательный термин, который объединяет в себе несколько видов заболевания. При некоторых врождённых формах, в патологический процесс могут вовлекаться и некоторые системы органов:
- нервная – нарушение проводимости импульсов, нарушение интеллекта и памяти;
- эндокринная система – у девочек может нарушаться регулирование менструального цикла, у мальчиков – импотенция;
- сердечно-сосудистая система – аритмия и др.
При некоторых формах миотонии, может формироваться «холодовая реакция». При выходе на холод, формируется парез или спазм мышц.
Диагностика миотонии у ребёнка
Диагностированием патологии занимается сразу несколько специалистов – педиатр, невролог, эндокринолог, ортопед и даже генетики. Постановка диагноза начинается с опроса, важно выявить не только то время, когда появились симптомы. А были ли подобные проявления у ближайших кровных родственников. Как и при многих наследственных патологиях, в процесс диагностирования включаются и сами родители – ДНК анализ.
В последующей, доктор переходит к осмотру, пальпации и перкуссии. Эти исследования позволяют выявить тонус мышц, оценить их развитие и силу. Анализ этих данных уже позволит заподозрить диагноз, но все же, он ещё требует подтверждения. В обязательном порядке назначаются и лабораторные методы исследования – анализ крови.
Окончательно подтвердить диагноз позволяет электромиография (ЭМГ). Этот вид исследования позволяет выявить миотоническую реакцию.
Основные проявления
Миотония у ребенка может проявиться в любом возрасте. При врожденной патологии первые признаки заболевания дают о себе знать вскоре после рождения. У новорожденного обращает на себя внимание выраженная гипотония мышц. Малыш позже своих сверстников начинает держать голову, переворачиваться, вставать на ножки. Отставание в физическом развитии может быть совсем незаметным, и тогда родители просто не обращают внимания на подобный симптом. В дальнейшем даже умеренная миотония может привести к неблагоприятным последствиям и различным проблемам со здоровьем.
Совет
Плановые визиты к врачу на первом году жизни помогут вовремя выявить миотонию.
У ребенка старше года миотонический синдром проявляется следующими симптомами:
- общая мышечная слабость;
- быстрая утомляемость при беге, подъеме по лестнице;
- частая потеря равновесия при ходьбе.
Миотония у ребенка обычно начинается с поражения нижних конечностей. Первые тревожные симптомы родители могут заметить на прогулках, при подъеме по лестнице или во время игры. Еще недавно полный сил малыш постоянно останавливается, просится на ручки, теряет равновесие. Если такая ситуация не связана с общим переутомлением или болезнью ребенка, следует обратить внимание на подобный симптом и обследоваться у врача.
Детям с миотонией очень тяжело даются движения, требующие ловкости и сосредоточенности. Ходьба по бортику, прыжки на одной ноге, замирание на месте во время игры – все это получается у ребенка не слишком хорошо. Работа, требующая напряжения мелких мышц кистей, также дается малышу с большим трудом.
Типичный симптом миотонии – выраженный спазм мышц при легком ударе по ним. Мышечные волока при этом медленно сокращаются, что нередко сопровождается весьма болезненными ощущениями. Расслабление также происходит достаточно медленно. После расслабления под кожей можно ощутить напряженные мышечные валики.
Видео: лекция о врожденном миотоническом синдроме
Рекомендации родителям
Врожденные болезни нервной системы требуют постоянного поддерживающего лечения. Для того чтобы уменьшить симптоматику проявления недуга, врачи рекомендуют заниматься плаванием. Маленькому ребенку достаточно пространства будет и в домашней ванне, а в старшем возрасте можно посещать бассейн.
В поликлинике в обязательном порядке ребенку назначают физиотерапевтические процедуры. Отказываться от них не желательно, потому как электрофорез действительно приносит облегчение деткам, страдающим от миотонии. Метод абсолютно безболезненный и предполагает местное введение лекарств посредством постоянного тока.
Необходима консультация врача-генетика и при планировании беременности. В зоне риска находятся мужчины и женщины, в чьем роду уже встречались хромосомные отклонения. Настоятельно рекомендуется таким парам проходить генетическую диагностику во время самой беременности. Для этого применяется анализ околоплодных вод (амниоцентез) на 14-18 неделе, биопсия хориона на 10-12 неделе, кордоцентез (проводится после 18 недель). Стоит отметить, что риск рождения ребенка с таким отклонение значительно повышается, если женщине более 35 лет. С помощью генетического исследования крови врачи могут определить предрасположенность будущего малыша к серьезным недугам.
Лечебные мероприятия
Лечение миотонического синдрома зависит от его причин. Если недуг приобретенный, врачи назначают комплексную терапию, устраняющую этиопатогенетические факторы и последствия их воздействия. Врожденный синдром — неизлечимое заболевание, которое остается с ребенком на всю жизнь.
Общетерапевтические мероприятия способны существенно облегчить состояние больных, поэтому являются обязательно необходимыми.
Всем больным проводят симптоматическую терапию, направленную на нормализацию мышечного тонуса, их быстрое восстановление после перенапряжения или сокращения, стабилизацию метаболизма в организме. Обычно назначают ноотропные, сосудистые, нейропротекторные и метаболические средства:
- «Актовегин» активизирует обмен веществ в тканях, улучшает трофику и метаболизм на клеточном уровне, стимулирует процесс регенерации.
- «Пантогам» – ноотропный препарат, запускающий метаболические процессы в клетках мозга и устраняющий последствия психомоторного возбуждения.
- «Фенитоин» – миорелаксант с противоконвульсивным действием.
- «Элькар» повышает активность мозга и нормализует обменные процессы.
- Диуретики «Верошпирон» и «Гипотиазид» применяют для снижения калия в крови.
- «Церебролизин» стимулирует мозговую деятельность, проявляя функциональную нейромодуляцию и нейротрофическую активность.

- «Кортексин» – мощный антиоксидант и антигипоксант, улучшающий функции головного мозга и повышающий устойчивость организма к внешним раздражителям.
- В тяжелых случаях проводится иммуносупрессивная терапия – внутривенное введение иммуноглобулина человека, «Преднизолона», «Циклофосфамида».
- Кроме медикаментозного лечения необходимо непосредственное воздействие на мышцы с целью их тренировки и укрепления. Для этого проводят несколько курсов массажа, занятия ЛФК, закаливание. Ежедневная гимнастика и сеансы массажа помогут восстановить мышечную активность, нормализовать тонус мышц, устранить неприятные симптомы синдрома.
- Для улучшения самочувствия необходимо придерживаться диетического питания с ограничением солей калия.
- Взрослым пациентам полезно плавание в бассейне, а малышам – в домашней ванне.
- Физиотерапевтические процедуры, эффективные при миотонии — озокеритовае аппликации, электрофоретическое воздействие, иглорефлексотерапия, электростимуляция.

- Коррекционные занятия с больными детьми в специализированном медицинском центре.
- Занятия с логопедом, психологом, дефектологом.
Специалисты рекомендуют своим пациентам избегать воздействия провоцирующих факторов: конфликтных ситуаций, психоэмоциональных всплесков, физического перенапряжения, долгого пребывания в одной и той же позе, переохлаждения.
Если родители приложат определенные усилия и начнут лечить детей с раннего детства, они вырастут и будут жить полноценной жизнью. Сразу после того, как родится малыш, ему следует организовать правильный уход: кормить грудью, часто и подолгу гулять с ним на свежем воздухе, делать массаж, выполнять зарядку по утрам. Эти профилактические мероприятия помогут избежать дальнейшего прогрессирования мышечной слабости.
Если не предавать особого значения симптомам патологии, можно нанести непоправимый вред здоровью малыша. Он начнет позже сверстников держать головку, сидеть и ходить, в дальнейшем возникнут проблемы с речью. К тяжелым осложнениям синдрома относятся: постоянная мигрень, энурез, снижение остроты зрения, искривление позвоночника.
К тяжелым осложнениям синдрома относятся: постоянная мигрень, энурез, снижение остроты зрения, искривление позвоночника.
Медико-генетическое консультирование показано всем лицам, планирующим беременность и находящимся в группе риска. Это касается семейных пар, у которых в роду имелись хромосомные аномалии. Женщинам во время беременности показана пренатальная диагностика генетических расстройств, которая включает неинвазивные и инвазивные методики. Для этого проводят УЗИ плода, скрининг биохимических сывороточных маркеров, амниоцентез, плацентоцентез, биопсию ворсин хориона, кордоцентез.
Миотонический синдром не так страшен, как о нем думают обеспокоенные молодые мамочки. Своевременная и корректная диагностика, а также адекватное лечение позволяют таким малышам вырасти здоровыми и счастливыми.
Осложнения
Важно, как можно раньше обнаружить миотонический синдром у детей, и начать лечение. Запущенные нервно-мышечные расстройства негативно отражаются на развитии ребенка: начинает поздно держать голову, спину, в дальнейшем нарушается осанка. Кроме того, если тоническое напряжение затрагивает мышцы лица, то наблюдается задержка речевого развития — отсутствие фразовой, связной речи.
Кроме того, если тоническое напряжение затрагивает мышцы лица, то наблюдается задержка речевого развития — отсутствие фразовой, связной речи.
К другим последствиям миотонического синдрома при отказе от лечения относят:
- постоянные головные боли;
- хроническое недержание мочи;
- остеохондроз;
- искривление осанки;
- близорукость.
Последствия
Миотонический синдром у детей редко проходит бесследно. Даже легкая форма патологии приводит к различным проблемам со здоровьем:
- нарушение осанки;
- речевые расстройства;
- близорукость;
- запоры;
- энурез;
- головные боли;
- быстрая утомляемость и выраженная слабость.
Все эти осложнения имеют единственную причину – снижение работоспособности мышечных волокон. Мышцы, потерявшие способность правильно сокращаться и расслабляться, не могут в полной мере выполнять свои функции. Слабость мышц спины приводит к неправильной осанке, брюшного пресса – к запорам и другим проблемам с пищеварением. Со временем у ребенка накапливается целый букет различных заболеваний, и справляться с симптомами миотонии становится все сложнее.
Со временем у ребенка накапливается целый букет различных заболеваний, и справляться с симптомами миотонии становится все сложнее.
Медикаментозное воздействие
Некоторые специалисты придерживаются мнения, что лечить миотонический синдром лекарственными препаратами абсолютно не эффективно, и положительный результат возможет только при постоянных физических занятиях. Определять нагрузку должен только специалист. Но для того чтобы снять спазм мышц в некоторых случаях назначают препарат «Фенитоин». Это мышечный релаксант, обладающий противосудорожным действием. Суточная доза средства рассчитывается в зависимости от веса и возраста пациента. У взрослых она не может превышать 500 мг, у детей – 300 мг в сутки.
При миотоническом синдроме также могут быть назначены следующие препараты:
- «Актовегин» – способствует повышению энергетического ресурса клеток, улучшает процессы метаболизма. Препарат можно применять как для внутривенного введения (инъекции), так и в форме таблеток.

- «Пантогам» – эффективное ноотропное средство, активизирующее метаболизм в клетках и имеющее противосудорожное действие. Справляется с психомоторной возбудимостью, неврозами. Хорошо зарекомендовал себя в лечении умственной отсталости у детей.
- «Элькар» – капли, повышающие мозговую активность и нормализующие процессы метаболизма. В списке показаний к назначению присутствует хроническая мышечная слабость, наследственные патологии мышечной дистрофии.
В обязательном порядке больным с миотоническим синдромом назначают диуретики. Они снижают уровень калия в плазме крови, который обычно повышается после очередного приступа.
Как выявить отклонение у детей?
Распознать отклонения могут родители у новорожденного малыша. Миотонический синдром у грудничка проявляется даже при сосательных движениях. Такие детки начинают намного позже держать голову, переворачиваться со спины на живот, ползать и ходить. Мышечная слабость приводит к развитию неправильной осанки, сколиозу, возникновению проблем с желудочно-кишечным трактом (запоры, колики).
Миотонический синдром у детей проявляется и тем, что не позволяет вовремя делать первые шаги. Малыши часто падают, теряют равновесие, не могут быстро бегать и ходить по лестнице из-за мышечного спазма. Играть в подвижные активные игры им также не под силу – дети быстро устают.
Слабость лицевых мышц влияет на способность нормально разговаривать. Уже в раннем возрасте проявляются признаки близорукости, так как синдром поражает и глазные мышцы. Симптоматика недуга у каждого ребенка проявляется в разной степени. Следует учитывать, что первые проявления могут возникнуть только в подростковом возрасте. Определить синдром можно попытаться самостоятельно. Для этого по икроножной мышце необходимо легонько постучать, и если произойдет спазм (иногда даже болезненный), значит, понадобиться консультация врача-невролога.
К какому врачу обратиться
Диагностикой и лечением миотонического синдрома занимается невролог.
Лалаян Тигран Владимирович
Невролог • Мануальный терапевт
Стаж 22 года
Понеделко Татьяна Сергеевна
Невролог • Иглорефлексотерапевт
Стаж 13 лет
Мальцев Сергей Игоревич
Массажист • Кинетрак
Стаж 14 лет
Троицкая Татьяна Евгеньевна
Физиотерапевт
Стаж 33 года
Астахова Елена Вячеславовна
Невролог
Стаж 14 лет
Александров Антон Валерьевич
Ортопед
Стаж 11 лет
Гаджимурадов Абдула Гаджимурадович
Ортопед • Стромально-васкулярная фракция
Стаж 5 лет
Смирнов Егор Николаевич
Ортопед • Стромально-васкулярная фракция
Стаж 6 лет
Телеев Марат Султанбекович
Ортопед • Стромально-васкулярная фракция
Стаж 5 лет
Бодань Станислав Михайлович
Ортопед • Стромально-васкулярная фракция
Стаж 23 года
Булацкий Сергей Олегович
Ортопед • Стромально-васкулярная фракция
Стаж 11 лет
Всему виной гены!
В настоящее время установить истинную причину миотонического синдрома ученым не удалось. Врожденный недуг (классическая форма) передается по аутосомно-доминантному типу, хондродистрофическая миотония – по аутосомно-рецессивному. Это значит, что в первом случае измененный ген начинает доминировать и подавлять нормальную копию, тем самым вызывая развитие генетических отклонений. Вероятность того, что ребенок родится с врожденным недугом (у больного родителя) – 50%. Не стоит отчаиваться, ведь каждый малыш имеет шанс появиться на свет абсолютно здоровым, если ему передастся здоровая копия гена. Врожденный миотонический синдром у детей может проявляться в разной степени, но встречается он в каждом поколении.
Врожденный недуг (классическая форма) передается по аутосомно-доминантному типу, хондродистрофическая миотония – по аутосомно-рецессивному. Это значит, что в первом случае измененный ген начинает доминировать и подавлять нормальную копию, тем самым вызывая развитие генетических отклонений. Вероятность того, что ребенок родится с врожденным недугом (у больного родителя) – 50%. Не стоит отчаиваться, ведь каждый малыш имеет шанс появиться на свет абсолютно здоровым, если ему передастся здоровая копия гена. Врожденный миотонический синдром у детей может проявляться в разной степени, но встречается он в каждом поколении.
По аутосомно-рецессивному типу наследуется синдром Шварца-Джампела (хондродистрофическая миотония). Для того чтобы недуг себя проявил, необходимо получить от каждого из родителей по одной измененной копии гена. Если же ребенок унаследует только одну «неправильную» копию, а вторую – здоровую, он будет являться только носителем.
Проявление недуга у взрослых
В юношеском и зрелом возрасте могут проявиться признаки дистрофического типа миотонического синдрома (болезнь Штейнера). Довольно часто это сопровождается сопутствующими патологиями сердца, нарушением менструального цикла у женской половины пациентов и импотенцией у мужчин. Помимо неврологических отклонений, наблюдается значительное снижение уровня интеллекта.
Довольно часто это сопровождается сопутствующими патологиями сердца, нарушением менструального цикла у женской половины пациентов и импотенцией у мужчин. Помимо неврологических отклонений, наблюдается значительное снижение уровня интеллекта.
Миотонический синдром у взрослых лиц проявляется весьма своеобразно. Мужчины (более подвержены синдрому) с гипертрофией мышц выглядят спортивно и подтянуто, но на самом деле такие мышцы не обладают силой. Миотонические спазмы приводят к изменению голоса, трудностям при глотании и дыхании (поражение дыхательных мышц). Первые спазмы мышц обычно поражают ноги. При этом больной может абсолютно нормально ходить по ровной поверхности, но если ему понадобится подняться по ступенькам, то есть задействовать другую группу мышц, преодолеть первый подъем будет довольно сложно.
У пациента с миотоническим синдромом можно наблюдать феномен приседания. Ему не удастся присесть так, чтобы задняя поверхность бедер соприкасалась с голенью и при этом полностью опираться на стопу. Больной не в состоянии удержать равновесие в таком положении и просто упадет. Обычное для здорового человека полное приседание он выполняет с широко расставленными ногами и опирается на носки (полностью присесть при этом все равно не получается).
Больной не в состоянии удержать равновесие в таком положении и просто упадет. Обычное для здорового человека полное приседание он выполняет с широко расставленными ногами и опирается на носки (полностью присесть при этом все равно не получается).
Другие причины
Неврологический миотонический синдром в большинстве случаев является наследственным недугом, но вызвать его могут и не «генные» причины, среди которых:
- Родовые травмы.
- Перинатальная энцефалопатия.
- Нарушение обмена веществ.
- Малая двигательная активность в детском возрасте.
- Перенесенный в младенчестве рахит.
- Нервно-мышечные заболевания.
- Гиподинамия (снижение активности) в период беременности.
Синдром, который развился вследствие возникновения этих причин, считается приобретенным и хорошо поддается лечению, в отличие от генетического типа недуга.
Миотоническая атака
Миотоническая атака – одно из типичных проявлений патологии. Родители могут заметить, как ребенок при попытке встать или пробежаться замирает и тут же падает. Далее ребенок делает определенное усилие – и продолжает начатое движение. Со временем миотонические атаки могут повторяться все чаще и чаще.
Далее ребенок делает определенное усилие – и продолжает начатое движение. Со временем миотонические атаки могут повторяться все чаще и чаще.
Подобное проявление миотонического синдрома связано с особенностями работы измененных мышц. Мышечные волокна, не способные быстро сокращаться и расслабляться, не могут отвечать на запросы тела ребенка. При попытке сделать несколько движений малыш теряет равновесие и падает. Через несколько секунд мышцы разрабатываются, и ребенок продолжает движение. Чем больше будет двигаться ребенок в этот момент, тем быстрее закончится миотоническая атака.
Источники
- https://mama.guru/detskie-zabolevaniya-i-medikamenty/miotonicheskiy-sindrom-u-detey-lechenie.html
- http://krampf.ru/o-spazmakh/99-miotonicheskij-sindrom
- https://cmrt.ru/zabolevaniya/nervnoy-sistemy/miotonicheskiy-sindrom/
- https://bolivspinenet.ru/miotonicheskij-sindrom/
- https://DetStrana.ru/service/disease/children/miotoniya/
- http://TheRebenok.
 ru/zdorove/miotonicheskij-sindrom-u-rebenka.html
ru/zdorove/miotonicheskij-sindrom-u-rebenka.html - https://sindrom.info/miotonicheskij/
- https://www.syl.ru/article/210101/new_miotonicheskiy-sindrom-simptomyi-i-lechenie
голоса
Рейтинг статьи
Педиатрическая миотоническая дистрофия
Наша приверженность обеспечению вашей безопасности
Мы никогда не считали само собой разумеющимся святое доверие, которое вы возлагаете на нас, чтобы заботиться о своем ребенке, и сегодня мы более чем когда-либо благодарны за эту привилегию. Чтобы узнать обо всех способах, которыми мы работаем, чтобы обезопасить вас, вашу семью и членов нашей команды, посетите нашу страницу обновлений COVID-19.
Узнайте больше о наших обязательствах по обеспечению вашей безопасности
Узнайте больше о наших обязательствах по обеспечению вашей безопасности
Компания Children’s Health имеет большой опыт лечения миотонической дистрофии. Вашего ребенка будет лечить команда, состоящая из широкого круга специалистов, видевших много детей с этим редким заболеванием.
Что такое детская миотоническая дистрофия?
Миотоническая дистрофия — редкое заболевание, которое может вызывать слабость в мышцах и других частях тела. Часто вызывает слабость в лице, шее, руках и ногах. Миотоническая дистрофия поражает различные системы организма и со временем может медленно прогрессировать.
У детей с этим заболеванием обычно наблюдается миотония. Это трудности с расслаблением мышц после того, как они были сокращены, например, трудности с раскрытием сжатого кулака. Дети также могут испытывать трудности с некоторыми видами движений, такими как подъем по лестнице. В тяжелых случаях это состояние может:
- Влиять на мозг и вызывать задержку развития ребенка
- Вызывают проблемы с сердцем и дыханием
- Вызывают проблемы с пищеварительной системой
Какие существуют виды детской миотонической дистрофии?
Различные типы этого состояния проявляются в разном возрасте, но симптомы схожи.
Врожденная миотоническая дистрофия
Дети с этой формой миотонической дистрофии рождаются с этим заболеванием. При рождении они слабые и могут проявлять другие симптомы миотонической дистрофии. Младенцам может понадобиться дыхательная трубка или трубка для кормления, а их мозг может быть поврежден из-за нехватки кислорода. Это самая распространенная форма среди детей.
Детская и ювенильная миотоническая дистрофия
Эта форма миотонической дистрофии проявляется в детском или подростковом возрасте. Он может быть легким или тяжелым. Легкая миотоническая дистрофия может вызывать слабость некоторых мышц. Более тяжелая форма будет иметь более сильный эффект и может затронуть больше частей тела.
Каковы признаки и симптомы детской миотонической дистрофии?
Признаки и симптомы миотонической дистрофии могут включать:
- Мышечная слабость, в том числе в области лица
- Боль в мышцах, судороги и усталость
- Искривление позвоночника (сколиоз)
- Трудности с обучением
- Трудности с речью
- Болезнь щитовидной железы или диабет
- Затрудненное дыхание или прием пищи у младенцев
- Воздействие на глаза, сердце, легкие и пищеварительную систему
Как диагностируется детская миотоническая дистрофия?
Врачи могут использовать следующие шаги для диагностики миотонической дистрофии у ребенка:
- Сбор семейного анамнеза
- Проверить, может ли ребенок сжать и разжать кулак
- Проведение медицинского осмотра
- Генетическое тестирование для подтверждения диагноза
Что вызывает миотоническую дистрофию у детей?
Это состояние вызвано изменением (мутацией) в генах. Он может передаваться от родителей к детям.
Он может передаваться от родителей к детям.
Некоторые родители могут иметь легкие симптомы, но не знать, что у них миотоническая дистрофия. Если у родителя есть легкие симптомы, такие как слабость мышц рук или трудности с расслаблением рук, им также следует подумать о том, чтобы пройти обследование.
Как лечится детская миотоническая дистрофия?
В Children’s Health℠ мы следим за детьми с этим заболеванием, чтобы убедиться, что они получают всю необходимую помощь. Мы сосредоточены на предотвращении усугубления таких проблем, как затрудненное дыхание.
Мы разрабатываем программу ухода, адаптированную для каждого ребенка, и продолжаем оказывать поддержку по мере его взросления. Вашего ребенка может лечить группа медицинских работников, в которую входят:
- Эрготерапевты и физиотерапевты, которые помогают поддерживать подвижность суставов и мышц
- Кардиолог, который проверит сердце вашего ребенка
- Пульмонолог, который поможет сохранить легкие вашего ребенка крепкими
- Генетические консультанты, которые могут определить ген, вызывающий миотоническую дистрофию
- Специалисты по физической медицине и реабилитации
- Диетолог для работы с семьей по диете
- Гастроэнтеролог, который будет работать с вами, чтобы пищеварительная система вашего ребенка работала как можно лучше.

Детская миотоническая дистрофия Врачи и поставщики услуг
В Children’s Health команда по уходу за вашим ребенком может включать специалистов, которые могут помочь с его лечением.
Часто задаваемые вопросы
Есть ли лекарство от миотонической дистрофии?
Лекарства пока нет, но мы работаем над организацией испытаний различных видов лекарств, которые можно использовать для лечения этого заболевания.
Какой последующий уход потребуется моему ребенку с миотонической дистрофией?
Ваш ребенок должен проходить регулярные осмотры сердца, легких, уровня сахара в крови и здоровья костей.
Ресурсы
- Фонд миотонической дистрофии
- Ассоциация мышечной дистрофии
- Национальная организация редких заболеваний
Признаки и симптомы врожденного СД1 — Миотоническая дистрофия (СД) — Заболевания
Перейти к основному содержанию
Врожденный СД1
Оценки заболеваемости врожденным СД сильно различаются, варьируя от 2 до 28 на 100 000 живорождений в различных исследованиях. 23 , 24 При появлении симптомов СД при рождении развиваются опасные для жизни осложнения. Однако, как только этот критический период пройден, в раннем детстве, вероятно, наступит улучшение. Позже, когда ребенок приближается к подростковому возрасту, вполне вероятно, что появятся симптомы СД1, дебютирующего во взрослом возрасте.
23 , 24 При появлении симптомов СД при рождении развиваются опасные для жизни осложнения. Однако, как только этот критический период пройден, в раннем детстве, вероятно, наступит улучшение. Позже, когда ребенок приближается к подростковому возрасту, вполне вероятно, что появятся симптомы СД1, дебютирующего во взрослом возрасте.
Врожденный СД наблюдался только при СД1. Чтобы узнать больше, см. «Энергия, самоотверженность, надежда в помощь родителям детей с врожденным СД1», часть серии Quest «В центре внимания: миотоническая дистрофия».
Когда ребенок рождается с врожденным СД1, у матери обычно развивается СД1 во взрослом возрасте, даже если ее симптомы могут быть настолько легкими, что она не знала, что у нее заболевание. Матери с СД также могут перейти во взрослую форму. Ребенок может унаследовать болезнь от отца, но почти всегда это форма с началом во взрослом возрасте. Эти необычные особенности не наблюдаются при других генетических нарушениях. 25 , 26 Подробнее см. в разделе Причины/Наследование.
25 , 26 Подробнее см. в разделе Причины/Наследование.
Поражение органов дыхания является распространенным явлением и является основной причиной смерти в неонатальном периоде. Механическая вентиляция требуется от 70% до 80% и более пациентов. 27 , 24 Также распространены трудности с кормлением, многим детям требуется назогастральный или желудочный зонд для кормления. И сосание, и глотание связаны со слабостью мышц лица и области горла.
Общая смертность составляет приблизительно 15-20% процентов и приближается к 40% у тяжело пораженных младенцев. 27
Когнитивные нарушения при врожденном СД
Новорожденные с врожденным СД часто имеют серьезные когнитивные нарушения, хотя это не всегда так. Умственная отсталость присутствует у 50-60% выживших детей. 27 Это состояние, по-видимому, связано с аномальным развитием частей мозга, предположительно вызванным генетическими аномалиями.
Некоторые эксперты предположили, что очень высокая частота осложнений при родах у матерей с СД также может быть фактором, способствующим когнитивным проблемам, наблюдаемым у этих детей.
Преодоление врожденной дерматомиозита
Когнитивные трудности не улучшаются, но в целом они также не ухудшаются, и дети могут учиться, если им предоставлены правильные инструменты, инструкции и окружающая среда. См. Медицинское управление. Однако, несмотря на ранние успехи в детстве, у детей с врожденным СД, скорее всего, разовьется взрослая форма СД, когда они достигнут подросткового или взрослого возраста.
Нарушения речи, слуха и зрения
Мышцы, участвующие в разговоре, часто поражаются при врожденном СД. Слух также может быть нарушен. Мышцы глаз поражены и не всегда выровнены, состояние, называемое косоглазием.
Катаракта, часто встречающаяся при СД у взрослых, не характерна для врожденного СД в раннем детстве. Однако у детей с врожденным СД они, вероятно, разовьются позже. 2
2
Слабые мышцы
У детей с врожденным СД1 очень слабые мышцы и отсутствие мышечного тонуса (гипотония), а не миотония. Они кажутся вялыми, им трудно дышать, они плохо сосут и глотают.
В прошлом многие младенцы с врожденным СД не выживали. Сегодня, при особом уходе в отделениях реанимации новорожденных, такие дети имеют гораздо больше шансов на выживание, хотя в детстве они все равно столкнутся с многочисленными проблемами.
Дети с врожденным СД1 часто рождаются с косолапостью, искривлением стоп и голеней. Проблема может быть связана с аномальным развитием мышц голеней и стоп во время внутриутробного развития.
Младенцы с СД1 вначале не имеют миотонии, но развиваются в более позднем возрасте. 27
Ссылки
- Turner, C. & Hilton-Jones, D. Миотоническая дистрофия: диагностика, лечение и новые методы лечения. Текущее мнение по неврологии (2014). doi:10.1097/WCO.0000000000000128
- Day, J.
 W. и др. Миотоническая дистрофия 2 типа: молекулярный, диагностический и клинический спектр. Неврология (2003). дои: 10.1212/01.WNL.0000054481.84978.F9
W. и др. Миотоническая дистрофия 2 типа: молекулярный, диагностический и клинический спектр. Неврология (2003). дои: 10.1212/01.WNL.0000054481.84978.F9 - Мачука-Цили, Л., Брук, Д. и Хилтон-Джонс, Д. Клинические и молекулярные аспекты миотонических дистрофий: обзор. Мышцы и нервы (2005). doi:10.1002/mus.20301
- Васкес, Дж. А. и др. Гипоталамо-гипофизарно-тестикулярная функция у 70 больных миотонической дистрофией. Дж. Эндокринол. расследование Выключенный. Дж. Итал. соц. Эндокринол. (1990). дои: 10.1007/BF03350681
- Ørngreen, M.C., Arlien-Søborg, P., Duno, M., Hertz, J.M. & Vissing, J. Эндокринная функция у 97 пациентов с миотонической дистрофией типа 1. J. Neurol. (2012). doi:10.1007/s00415-011-6277-5
- Перик, С. и др. Гипогонадизм и эректильная дисфункция при миотонической дистрофии 1 типа. Acta Myol. (2013).
- Меола Г. и Моксли Р. Т. Миотоническая дистрофия 2 типа и связанные с ней миотонические расстройства.
 Журнал неврологии (2004). дои: 10.1007/s00415-004-0590-1
Журнал неврологии (2004). дои: 10.1007/s00415-004-0590-1 - Wiles, C.M. и др. Падения и спотыкания при миотонической дистрофии. Дж. Нейрол. Нейрохирург. Психиатрия (2006). doi:10.1136/jnnp.2005.066258
- Рикер, К. и др. Проксимальная миотоническая миопатия: новое доминирующее заболевание с миотонией, мышечной слабостью и катарактой. Неврология (1994). дои:дои:10. 1212/ВНЛ.44.8.1448
- Udd, B., Krahe, R., Wallgren-Pettersson, C., Falck, B. & Kalimo, H. Проксимальная миотоническая дистрофия. Семья с аутосомно-доминантной мышечной дистрофией, катарактой, потерей слуха и гипогонадизмом: гетерогенность проксимальной миотонической дистрофии. синдромы? Нервно-мышечная. Беспорядок. (1997). дои: 10.1016/S0960-8966(97)00041-2
- Heatwole, C. и др. Сообщаемое пациентами влияние симптомов миотонической дистрофии 2 типа (PRISM-2). Неврология (2015). doi:10.1212/WNL.0000000000002225
- Суокас, К.
 И., Хаанпаа, М., Каутиайнен, Х., Удд, Б. и Хиетахарью, А. Дж. Боль у пациентов с миотонической дистрофией типа 2: почтовый опрос в Финляндии. Мышцы и нервы (2012 г.). дои: 10.1002/муз.22249
И., Хаанпаа, М., Каутиайнен, Х., Удд, Б. и Хиетахарью, А. Дж. Боль у пациентов с миотонической дистрофией типа 2: почтовый опрос в Финляндии. Мышцы и нервы (2012 г.). дои: 10.1002/муз.22249 - George A., Schneider-Gold C., Zier S., Reiners K. & Sommer C. Скелетно-мышечные боли у пациентов с миотонической дистрофией 2 типа. Арх. Нейрол. (2004 г.). doi:10.1001/archneur.61.12.1938
- Гадалла, С. М. и др. Онкологический риск у больных миотонической мышечной дистрофией. ДЖАМА — Дж. Ам. Мед. доц. (2011). дои: 10.1001/jama.2011.1796
- Меола, Г. и др. Исполнительная дисфункция и избегающая черта личности при миотонической дистрофии 1 типа (СД-1) и проксимальной миотонической миопатии (ПРОММ/СД-2). Нервно-мышечная. Беспорядок. (2003 г.). doi:10.1016/S0960-8966(03)00137-8
- Удд, Б. и Крахе, Р. Миотонические дистрофии: молекулярные, клинические и терапевтические проблемы. The Lancet Neurology (2012).
 дои: 10.1016/S1474-4422(12)70204-1
дои: 10.1016/S1474-4422(12)70204-1 - Экстрем, А. Б., Хакенас-Плате, Луиза, Тулиниус, М. и Венц, Э. Когнитивные и адаптивные навыки при миотонической дистрофии типа 1: исследование 55 человек с врожденными и детскими формами. Дев. Мед. Детский Нейрол. (2009 г.). doi:10.1111/j.1469-8749.2009.03300.x
- Дуньоль, М. и др. Психиатрический и когнитивный фенотип детской миотонической дистрофии 1 типа. Dev. Мед. Детский Нейрол. (2012). doi:10.1111/j.1469-8749.2012.04379.x
- Ангерд, Н. и др. Новое окно нейрокогнитивной дисфункции при детской форме миотонической дистрофии 1 типа (СД1). Нервно-мышечная. Беспорядок. (2011). doi:10.1016/j.nmd.2011.04.009
- Echenne, B. и др. Миотоническая дистрофия I типа в детском возрасте. Долгосрочная эволюция у пациентов, переживших неонатальный период. Евро. Дж. Педиатр. Нейрол. (2008 г.). doi:10.1016/j.ejpn.2007.07.014
- Бхакта Д., Лоу М.
 Р. и Грох В. Дж. Распространенность структурных аномалий сердца у пациентов с миотонической дистрофией I типа. Am. Харт Дж. (2004). doi:10.1016/j.ahj.2003.08.008
Р. и Грох В. Дж. Распространенность структурных аномалий сердца у пациентов с миотонической дистрофией I типа. Am. Харт Дж. (2004). doi:10.1016/j.ahj.2003.08.008 - Bassez, G. и др. Тяжелые нарушения сердечного ритма у пациентов молодого возраста с миотонической дистрофией 1 типа. Неврология (2004). doi:10.1212/01.WNL.0000144343.
.CF
- Весстрем Г., Бенш Дж. и Шоллин Дж. Врожденная миотоническая дистрофия. Заболеваемость, клинические аспекты и ранний прогноз. Acta Педиатр. Сканд. (1986).
- Кэмпбелл, К., Левин, С., Сиу, В.М., Венанс, С. и Джейкоб, П. Врожденная миотоническая дистрофия: канадское популяционное эпиднадзорное исследование. Ж. Педиатр. (2013). doi:10.1016/j.jpeds.2012.12.070
- Harley, HG и др. Размер нестабильной повторяющейся последовательности CTG по отношению к фенотипу и родительской передаче при миотонической дистрофии. утра. Дж. Хам. Жене. (1993).
- Уилан, Д.
 Т., Карсон, Н. и Зесман, С. Передача отцовской формы врожденной формы миотонической дистрофии типа 1: новый случай и обзор литературы. 902:04 утра. Дж. Мед. Жене. (2002 г.). doi:10.1002/ajmg.10141
Т., Карсон, Н. и Зесман, С. Передача отцовской формы врожденной формы миотонической дистрофии типа 1: новый случай и обзор литературы. 902:04 утра. Дж. Мед. Жене. (2002 г.). doi:10.1002/ajmg.10141 - Даррас, Б. Т. и Вольпе, Дж. Дж. Вовлечение мышц и ограниченные расстройства. в Неврология новорожденных Вольпе (2017). дои: 10.1016/B978-0-323-42876-7.00033-8
Найдите свой MDA
Care Center
Врожденная и детская миотоническая дистрофия: текущие аспекты болезни и будущие направления
1. Bushby K, Finkel R, Birnkrant DJ, Case LE, Clemens PR, Cripe L, Kaul A, Kinnett K, McDonald C, Pandya S, et al. . Диагностика и лечение мышечной дистрофии Дюшенна, часть 1: диагностика, фармакологическое и психосоциальное лечение. Ланцет Нейрол. 2010;9: 77–93. [PubMed] [Google Scholar]
2. Bushby K, Finkel R, Birnkrant DJ, Case LE, Clemens PR, Cripe L, Kaul A, Kinnett K, McDonald C, Pandya S, et al. Диагностика и лечение мышечной дистрофии Дюшенна, часть 2: осуществление междисциплинарной помощи. Ланцет Нейрол. 2010;9:177–189. [PubMed] [Google Scholar]
Ланцет Нейрол. 2010;9:177–189. [PubMed] [Google Scholar]
3. Wang CH, Finkel RS, Bertini ES, Schroth M, Simonds A, Wong B, Aloysius A, Morrison L, Main M, Crawford TO, et al. Заявление о консенсусе в отношении стандарта медицинской помощи при спинальной мышечной атрофии. J Чайлд Нейрол. 2007; 22:1027–1049.. [PubMed] [Google Scholar]
4. Кэмпбелл С., Левин С., Сиу В.М., Венанс С., Джейкоб П. Врожденная миотоническая дистрофия: Канадское популяционное исследование. J Педиатр. 2013;163:120–5.e1-120-5.e3. [PubMed] [Google Scholar]
5. Echenne B, Bassez G. Врожденная и инфантильная миотоническая дистрофия. Handb Clin Neurol. 2013; 113:1387–1393. [PubMed] [Google Scholar]
6. Hageman AT, Gabreëls FJ, Liem KD, Renkawek K, Boon JM. Врожденная миотоническая дистрофия; отчет о тринадцати случаях и обзор литературы. J Neurol Sci. 1993;115:95–101. [PubMed] [Google Scholar]
7. Меола Г., Кардани Р. Миотонические дистрофии: обновленная информация о клинических аспектах, генетике, патологии и молекулярных патомеханизмах. Биохим Биофиз Акта. 2015; 1852: 594–606. [PubMed] [Google Scholar]
Биохим Биофиз Акта. 2015; 1852: 594–606. [PubMed] [Google Scholar]
8. Echenne B, Rideau A, Roubertie A, Sébire G, Rivier F, Lemieux B. Миотоническая дистрофия I типа в детском возрасте Долгосрочная эволюция у пациентов, переживших неонатальный период. Eur J Paediatr Neurol. 2008;12:210–223. [PubMed] [Академия Google]
9. Wallgren-Pettersson C, Bushby K, Mellies U, Simonds A. 117-й семинар ENMC: вентиляционная поддержка при врожденных нервно-мышечных нарушениях — врожденные миопатии, врожденные мышечные дистрофии, врожденная миотоническая дистрофия и SMA (II) 4-6 апреля 2003 г., Наарден, Нидерланды. Нервно-мышечное расстройство. 2004; 14:56–69. [PubMed] [Google Scholar]
10. Mathieu J, Allard P, Potvin L, Prévost C, Bégin P. 10-летнее исследование смертности в когорте пациентов с миотонической дистрофией. Неврология. 1999;52:1658–1662. [PubMed] [Google Scholar]
11. Kroksmark AK, Ekström AB, Björck E, Tulinius M. Миотоническая дистрофия: поражение мышц в зависимости от типа заболевания и размера расширенной последовательности CTG-повторов. Dev Med Child Neurol. 2005; 47: 478–485. [PubMed] [Google Scholar]
Dev Med Child Neurol. 2005; 47: 478–485. [PubMed] [Google Scholar]
12. Harper PS. Миотоническая дистрофия. 3-е изд. Лондон: WB Сондерс; 2001. [Google Scholar]
13. Шара У., Шосер Б.Г. Миотонические дистрофии 1 и 2 типа: краткое изложение современных аспектов. Семин Педиатр Нейрол. 2006; 13:71–79. [PubMed] [Google Scholar]
14. Pace-Schott EF, Hobson JA. Нейробиология сна: генетика, клеточная физиология и подкорковые сети. Нат Рев Нейроски. 2002; 3: 591–605. [PubMed] [Google Scholar]
15. Hobson JA, Pace-Schott EF. Когнитивная нейронаука сна: нейронные системы, сознание и обучение. Нат Рев Нейроски. 2002; 3: 679–693. [PubMed] [Google Scholar]
16. Laberge L, Gagnon C, Dauvilliers Y. Дневная сонливость и миотоническая дистрофия. Curr Neurol Neurosci Rep. 2013; 13:340. [PubMed] [Академия Google]
17. Quera Salva MA, Blumen M, Jacquette A, Durand MC, Andre S, De Villiers M, Eymard B, Lofaso F, Heron D. Нарушения сна при детской миотонической дистрофии типа 1. Нервно-мышечное расстройство. 2006; 16: 564–570. [PubMed] [Google Scholar]
Нервно-мышечное расстройство. 2006; 16: 564–570. [PubMed] [Google Scholar]
18. Ono S, Kanda F, Takahashi K, Fukuoka Y, Jinnai K, Kurisaki H, Mitake S, Inagaki T, Nagao K. Потеря нейронов в медуллярной ретикулярной формации при миотонической дистрофии: a клинико-патологическое исследование. Неврология. 1996; 46: 228–231. [PubMed] [Академия Google]
19. Оно С., Курисаки Х., Сакума А., Нагао К. Миотоническая дистрофия с альвеолярной гиповентиляцией и гиперсомнией: клинико-патологическое исследование. J Neurol Sci. 1995; 128: 225–231. [PubMed] [Google Scholar]
20. Кулебрас А., Подольский С., Леопольд Н.А. Отсутствие связанных со сном повышений гормона роста при миотонической дистрофии. Неврология. 1977; 27: 165–167. [PubMed] [Google Scholar]
21. Йоханссон А., Карлстрем К., Арен Б., Седерквист К., Крилборг Э., Форсберг Х., Олссон Т. Аномальная регуляция цитокинов и адренокортикальных гормонов при миотонической дистрофии. J Clin Endocrinol Metab. 2000;85:3169–3176. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
22. Minnerop M, Weber B, Schoene-Bake JC, Roeske S, Mirbach S, Anspach C, Schneider-Gold C, Betz RC, Helmstaedter C, Tittgemeyer M, et al. Мозг при миотонической дистрофии 1 и 2: свидетельство преимущественного поражения белого вещества. Мозг. 2011; 134:3530–3546. [PMC free article] [PubMed] [Google Scholar]
23. Yu H, Laberge L, Jaussent I, Bayard S, Scholtz S, Raoul M, Pages M, Dauvilliers Y. Дневная сонливость и характеристики быстрого сна при миотонической дистрофии: исследование случай-контроль. Спать. 2011; 34:165–170. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Cirignotta F, Mondini S, Zucconi M, Barrot-Cortes E, Sturani C, Schiavina M, Coccagna G, Lugaresi E. Связанное со сном нарушение дыхания при миотонической дистрофии. Дж Нейрол. 1987; 235:80–85. [PubMed] [Google Scholar]
25. Laberge L, Bégin P, Dauvilliers Y, Beaudry M, Laforte M, Jean S, Mathieu J. Полисомнографическое исследование дневной сонливости при миотонической дистрофии типа 1. J Neurol Neurosurg Psychiatry. 2009; 80: 642–646. [PubMed] [Google Scholar]
J Neurol Neurosurg Psychiatry. 2009; 80: 642–646. [PubMed] [Google Scholar]
26. Уолтерс А.С., Рай Д.Б. Обзор связи синдрома беспокойных ног и периодических движений конечностей во сне с гипертонией, сердечными заболеваниями и инсультом. Спать. 2009 г.;32:589–597. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Douniol M, Jacquette A, Cohen D, Bodeau N, Rachidi L, Angeard N, Cuisset JM, Vallée L, Eymard B, Plaza M, et al. Психиатрический и когнитивный фенотип детской миотонической дистрофии 1 типа. Dev Med Child Neurol. 2012;54:905–911. [PubMed] [Google Scholar]
28. Анжеард Н., Гарджуло М., Жакетт А., Радвани Х., Эймар Б., Херон Д. Когнитивный профиль при детской миотонической дистрофии 1 типа: есть ли глобальные нарушения? Нервно-мышечное расстройство. 2007; 17: 451–458. [PubMed] [Академия Google]
29. Angeard N, Jacquette A, Gargiulo M, Radvanyi H, Moutier S, Eymard B, Héron D. Новое окно в нейрокогнитивную дисфункцию при детской форме миотонической дистрофии 1 типа (DM1) Нервно-мышечное расстройство. 2011; 21: 468–476. [PubMed] [Google Scholar]
2011; 21: 468–476. [PubMed] [Google Scholar]
30. Рубинштейн Дж. С., Рубинштейн Д. С., Гудберн С., Холланд А. Дж. Апатия и гиперсомния являются общими признаками миотонической дистрофии. J Neurol Нейрохирург Психиатрия. 1998; 64: 510–515. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Экстрем А.Б., Хакенас-Плате Л., Самуэльссон Л., Тулиниус М., Венц Э. Состояния аутистического спектра при миотонической дистрофии 1 типа: исследование 57 человек с врожденными и детские формы. Am J Med Genet B Neuropsychiatr Genet. 2008;147Б:918–926. [PubMed] [Google Scholar]
32. Kuo HC, Hsiao KM, Chen CJ, Hsieh YC, Huang CC. Изменения магнитно-резонансной томографии головного мозга в семье с врожденной и классической миотонической дистрофией. Мозг Дев. 2005; 27: 291–296. [PubMed] [Google Scholar]
33. Тернер С., Хилтон-Джонс Д. Миотоническая дистрофия: диагностика, лечение и новые методы лечения. Карр Опин Нейрол. 2014; 27: 599–606. [PubMed] [Google Scholar]
34. Veyckemans F, Scholtes JL. Миотонические дистрофии 1 и 2 типа: анестезиологическая помощь. Педиатр Анест. 2013;23:794–803. [PubMed] [Google Scholar]
Veyckemans F, Scholtes JL. Миотонические дистрофии 1 и 2 типа: анестезиологическая помощь. Педиатр Анест. 2013;23:794–803. [PubMed] [Google Scholar]
35. Андерсон В.Б., Маккензи Дж.А., Сетон С., Фитцджеральд Д.А., Вебстер Р.И., Норт К.Н., Джоффе Д.А., Янг Х.К. Понюхайте носовое давление на вдохе и нарушение дыхания во сне при нервно-мышечных расстройствах у детей. Нервно-мышечное расстройство. 2012; 22: 528–533. [PubMed] [Google Scholar]
36. Керр Т.П., Робб С.А., Клейден Г.С. Поражение нижних отделов желудочно-кишечного тракта при врожденной миотонической дистрофии. Eur J Педиатр. 2002; 161: 468–469. [PubMed] [Google Scholar]
37. Рирдон В., Ньюкомб Р., Фентон И., Сиберт Дж., Харпер П.С. Естественная история врожденной миотонической дистрофии: смертность и отдаленные клинические аспекты. Арч Дис Чайлд. 1993;68:177–181. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Rönnblom A, Andersson S, Hellström PM, Danielsson A. Опорожнение желудка при миотонической дистрофии. Евро Джей Клин Инвест. 2002; 32: 570–574. [PubMed] [Google Scholar]
Евро Джей Клин Инвест. 2002; 32: 570–574. [PubMed] [Google Scholar]
39. Rönnblom A, Forsberg H, Danielsson A. Желудочно-кишечные симптомы при миотонической дистрофии. Scand J Гастроэнтерол. 1996; 31: 654–657. [PubMed] [Google Scholar]
40. Bellini M, Biagi S, Stasi C, Costa F, Mumolo MG, Ricchiuti A, Marchi S. Желудочно-кишечные проявления при миотонической мышечной дистрофии. Мир J Гастроэнтерол. 2006; 12:1821–1828. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Rönnblom A, Andersson S, Danielsson A. Механизмы диареи при миотонической дистрофии. Eur J Гастроэнтерол Гепатол. 1998; 10: 607–610. [PubMed] [Google Scholar]
42. Тарнопольский М.А., Пирс Э., Маттелиано А., Джеймс С., Армстронг Д. Синдром избыточного бактериального роста при миотонической мышечной дистрофии потенциально излечим. Мышечный нерв. 2010;42:853–855. [PubMed] [Google Scholar]
43. Rönnblom A, Hellström PM, Holst JJ, Theodorsson E, Danielsson A. Миоэлектрическая активность желудка и секреция гормонов кишечника при миотонической дистрофии. Eur J Гастроэнтерол Гепатол. 2001; 13: 825–831. [PubMed] [Академия Google]
Eur J Гастроэнтерол Гепатол. 2001; 13: 825–831. [PubMed] [Академия Google]
44. Rönnblom A, Danielsson A, el-Salhy M. Эндокринные клетки кишечника при миотонической дистрофии: иммуноцитохимическое и компьютерное аналитическое исследование изображений. J Интерн Мед. 1999; 245:91–97. [PubMed] [Google Scholar]
45. Экстрем А.Б., Тулиниус М., Шёстрём А., Аринг Э. Зрительные функции при врожденной и детской миотонической дистрофии 1 типа. Офтальмология. 2010; 117:976–982. [PubMed] [Google Scholar]
46. О’Брайен Т.А., Харпер П.С. Течение, прогноз и осложнения миотонической дистрофии детского возраста. Dev Med Child Neurol. 1984;26:62–67. [PubMed] [Google Scholar]
47. Farrar MA, Vucic S, Johnston HM, du Sart D, Kiernan MC. Патофизиологическое понимание, полученное из естественного течения и двигательной функции спинальной мышечной атрофии. J Педиатр. 2013; 162:155–159. [PubMed] [Google Scholar]
48. Moxley RT. Каналопатии, поражающие скелетные мышцы: миотонические расстройства, включая миотоническую дистрофию и периодический паралич. В: Джонс Х., Де Виво Д., Даррас Б., редакторы. нервно-мышечная. Беспорядок. Младенчество, Детство, Подросток. Клин. Подход. проиллюстрировано Баттервортом-Хайнеманном; 2003. стр. 783–812. [Академия Google]
В: Джонс Х., Де Виво Д., Даррас Б., редакторы. нервно-мышечная. Беспорядок. Младенчество, Детство, Подросток. Клин. Подход. проиллюстрировано Баттервортом-Хайнеманном; 2003. стр. 783–812. [Академия Google]
49. Воет Н.Б., ван дер Коой Э.Л., Рифаген И.И., Линдеман Э., ван Энгелен Б.Г., Герц А.С. Силовые тренировки и аэробные упражнения при мышечных заболеваниях. Кокрановская система базы данных, ред. 2013;7:CD003907. [PubMed] [Google Scholar]
50. Трип Дж., Дрост Г., ван Энгелен Б.Г., Фабер К.Г. Медикаментозное лечение миотонии. Cochrane Database Syst Rev. 2006;(1):CD004762. [Бесплатная статья PMC] [PubMed] [Google Scholar]
51. Logigian EL, Martens WB, Moxley RT, McDermott MP, Dilek N, Wiegner AW, Pearson AT, Barbieri CA, Annis CL, Thornton CA, et al. Мексилетин является эффективным антимиотоническим средством при миотонической дистрофии 1 типа. Неврология. 2010;74:1441–1448. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52. Engvall M. О состоянии полости рта у детей и взрослых с миотонической дистрофией. Swed Dent J Suppl. 2010;(203):1–51. [PubMed] [Google Scholar]
Swed Dent J Suppl. 2010;(203):1–51. [PubMed] [Google Scholar]
53. Sansone VA, Gagnon C. 207-й семинар ENMC по хронической дыхательной недостаточности при миотонических дистрофиях: лечение и последствия для исследований, 27–29 июня 2014 г., Наарден, Нидерланды. Нервно-мышечное расстройство. 2015; 25: 432–442. [PubMed] [Google Scholar]
54. Лазарус А., Варин Дж., Жовер Г., Алонсо С., Дюбок Д. Связь между сердечными аритмиями и апноэ во сне у пациентов с миотонической дистрофией I типа с постоянной кардиостимуляцией. Нервно-мышечное расстройство. 2007;17:392–399. [PubMed] [Google Scholar]
55. Мачука-Цили Л., Брук Д., Хилтон-Джонс Д. Клинические и молекулярные аспекты миотонических дистрофий: обзор. Мышечный нерв. 2005; 32:1–18. [PubMed] [Google Scholar]
56. Cobo AM, Poza JJ, Martorell L, López de Munain A, Emparanza JI, Baiget M. Вклад молекулярного анализа в оценку риска врожденной миотонической дистрофии. J Med Genet. 1995; 32: 105–108. [Бесплатная статья PMC] [PubMed] [Google Scholar]
57. Redman JB, Fenwick RG, Fu YH, Pizzuti A, Caskey CT. Взаимосвязь между длиной родительского тринуклеотидного повтора GCT и тяжестью миотонической дистрофии у потомства. ДЖАМА. 1993;269:1960–1965. [PubMed] [Google Scholar]
Redman JB, Fenwick RG, Fu YH, Pizzuti A, Caskey CT. Взаимосвязь между длиной родительского тринуклеотидного повтора GCT и тяжестью миотонической дистрофии у потомства. ДЖАМА. 1993;269:1960–1965. [PubMed] [Google Scholar]
58. Martorell L, Cobo AM, Baiget M, Naudó M, Poza JJ, Parra J. Пренатальная диагностика миотонической дистрофии типа 1. Тринадцать лет опыта: значение для репродуктивного консультирования в семьях с DM1. Пренат Диагн. 2007; 27: 68–72. [PubMed] [Google Scholar]
59. Magee AC, Hughes AE, Kidd A, Lopez De Munain A, Cobo AM, Kelly K, Dean J, Nevin NC. Репродуктивное консультирование женщин с миотонической дистрофией. J Med Genet. 2002;39:E15. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Кох М.С., Гримм Т., Харли Х.Г., Харпер П.С. Генетические риски для детей женщин с миотонической дистрофией. Am J Hum Genet. 1991; 48: 1084–1091. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Phillips MF, Steer HM, Soldan JR, Wiles CM, Harper PS.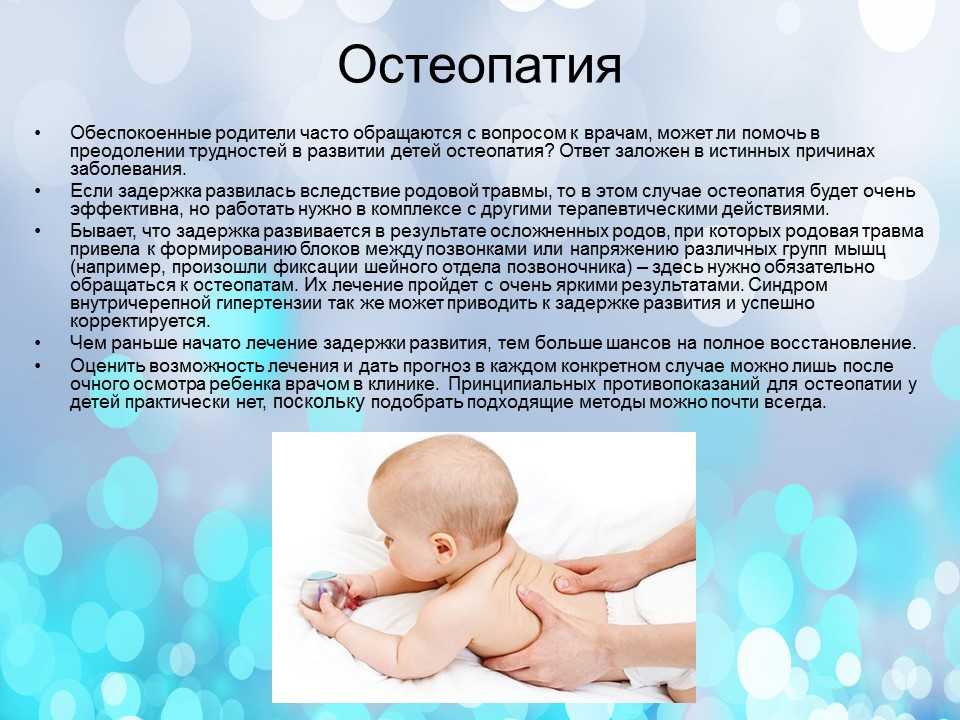 Дневная сонливость при миотонической дистрофии. Дж Нейрол. 1999; 246: 275–282. [PubMed] [Google Scholar]
Дневная сонливость при миотонической дистрофии. Дж Нейрол. 1999; 246: 275–282. [PubMed] [Google Scholar]
62. Dauvilliers YA, Laberge L. Миотоническая дистрофия 1 типа, дневная сонливость и нарушение регуляции быстрого сна. Sleep Med Rev. 2012; 16:539–545. [PubMed] [Google Scholar]
63. Аннан Д., Мур Д.Х., Барнс П.Р., Миллер Р.Г. Психостимуляторы при гиперсомнии (чрезмерной дневной сонливости) при миотонической дистрофии. Cochrane Database Syst Rev. 2006:(13): CD003218. [Бесплатная статья PMC] [PubMed] [Google Scholar]
64. Кумар Р. Утвержденное и исследовательское использование модафинила: обзор, основанный на фактических данных. Наркотики. 2008; 68: 1803–1839. [PubMed] [Google Scholar]
65. Hilton-Jones D, Bowler M, Lochmueller H, Longman C, Petty R, Roberts M, Rogers M, Turner C, Wilcox D. Модафинил при чрезмерной дневной сонливости при миотонической дистрофии 1 типа. — точка зрения пациентов. Нервно-мышечное расстройство. 2012;22:597–603. [PubMed] [Google Scholar]
66. Morgenthaler TI, Kapur VK, Brown T, Swick TJ, Alessi C, Aurora RN, Boehlecke B, Chesson AL, Friedman L, Maganti R, et al. Практические параметры лечения нарколепсии и других гиперсомний центрального генеза. Спать. 2007; 30:1705–1711. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Morgenthaler TI, Kapur VK, Brown T, Swick TJ, Alessi C, Aurora RN, Boehlecke B, Chesson AL, Friedman L, Maganti R, et al. Практические параметры лечения нарколепсии и других гиперсомний центрального генеза. Спать. 2007; 30:1705–1711. [Бесплатная статья PMC] [PubMed] [Google Scholar]
67. Brook JD, McCurrach ME, Harley HG, Buckler AJ, Church D, Aburatani H, Hunter K, Stanton VP, Thirion JP, Hudson T. Молекулярные основы миотоники дистрофия: расширение тринуклеотидного (CTG) повтора на 3′-конце транскрипта, кодирующего члена семейства протеинкиназ. Клетка. 1992;69:385. [PubMed] [Google Scholar]
68. Махадеван М., Цильфидис С., Сабурин Л., Шутлер Г., Амемия С., Янсен Г., Невилл С., Наранг М., Барсело Дж., О’Хой К. Мутация миотонической дистрофии: нестабильная КТГ повтор в 3′-нетранслируемой области гена. Наука. 1992; 255:1253–1255. [PubMed] [Google Scholar]
69. Tsilfidis C, MacKenzie AE, Mettler G, Barceló J, Korneluk RG. Корреляция между длиной тринуклеотидного повтора CTG и частотой тяжелой врожденной миотонической дистрофии. Нат Жене. 1992;1:192–195. [PubMed] [Google Scholar]
Нат Жене. 1992;1:192–195. [PubMed] [Google Scholar]
70. Brunner HG, Brüggenwirth HT, Nillesen W, Jansen G, Hamel BC, Hoppe RL, de Die CE, Höweler CJ, van Oost BA, Wieringa B. Влияние пола передающего родителя а также размера родительского аллеля на экспансию КТГ при миотонической дистрофии (СД) Am J Hum Genet. 1993;53:1016–1023. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Лаведан С., Хофманн-Радвани Х., Шелбурн П., Рабес Дж. П., Дюрос С., Савой Д., Дехаупас И., Люс С., Джонсон К., Джуньен С. Миотоническая дистрофия : зависящая от размера и пола динамика мейотической нестабильности КТГ и соматического мозаицизма. Am J Hum Genet. 1993;52:875–883. [Бесплатная статья PMC] [PubMed] [Google Scholar]
72. Ashizawa T, Anvret M, Baiget M, Barceló JM, Brunner H, Cobo AM, Dallapiccola B, Fenwick RG, Grandell U, Harley H. Характеристики межпоколенческих сокращений повтора КТГ при миотонической дистрофии. Am J Hum Genet. 1994; 54: 414–423. [Бесплатная статья PMC] [PubMed] [Google Scholar]
73. Santoro M, Masciullo M, Pietrobono R, Conte G, Modoni A, Bianchi ML, Rizzo V, Pomponi MG, Tasca G, Neri G, et al. Молекулярные, клинические и мышечные исследования миотонической дистрофии 1 типа (DM1), связанной с новым вариантом расширения CCG. Дж Нейрол. 2013; 260:1245–1257. [PubMed] [Академия Google]
Santoro M, Masciullo M, Pietrobono R, Conte G, Modoni A, Bianchi ML, Rizzo V, Pomponi MG, Tasca G, Neri G, et al. Молекулярные, клинические и мышечные исследования миотонической дистрофии 1 типа (DM1), связанной с новым вариантом расширения CCG. Дж Нейрол. 2013; 260:1245–1257. [PubMed] [Академия Google]
74. Тимченко Л.Т., Тимченко Н.А., Каски С.Т., Робертс Р. Новые белки со специфичностью связывания повторов CTG ДНК и повторов CUG РНК: значение для миотонической дистрофии. Хум Мол Жене. 1996; 5: 115–121. [PubMed] [Google Scholar]
75. Paul S, Dansithong W, Kim D, Rossi J, Webster NJ, Comai L, Reddy S. Взаимодействие мышечной слепоты, белков CUG-BP1 и hnRNP H в DM1-ассоциированном аберрантном сплайсинге IR . EMBO J. 2006; 25: 4271–4283. [Бесплатная статья PMC] [PubMed] [Google Scholar]
76. Манкоди А., Тенг-Умнуай П., Крым М., Хендерсон Д., Суонсон М., Торнтон К.А. Рибонуклеарные включения в скелетных мышцах при миотонической дистрофии 1 и 2 типа. Ann Neurol. 2003; 54: 760–768. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
77. Холт И., Жакемин В., Фардаи М., Сьюри К.А., Батлер-Браун Г.С., Ферлинг Д., Брук Д.Д., Моррис Г.Э. Мышечно-слепоподобные белки: сходства и различия в мышцах в норме и при миотонической дистрофии. Ам Джей Патол. 2009; 174: 216–227. [Бесплатная статья PMC] [PubMed] [Google Scholar]
78. Чаризанис К., Ли К.И., Батра Р., Гудвин М., Чжан С., Юань Ю., Шиуэ Л., Клайн М., Скотти М.М., Ся Г. и соавт. Мышечно-слепоподобный 2-опосредованный альтернативный сплайсинг в развивающемся мозге и дисрегуляция при миотонической дистрофии. Нейрон. 2012;75:437–450. [Бесплатная статья PMC] [PubMed] [Google Scholar]
79. Куюмку-Мартинес Н.М., Ван Г.С., Купер Т.А. Повышенные устойчивые уровни CUGBP1 при миотонической дистрофии 1 обусловлены PKC-опосредованным гиперфосфорилированием. Мол Ячейка. 2007; 28:68–78. [Бесплатная статья PMC] [PubMed] [Google Scholar]
80. Филипс А.В., Тимченко Л.Т., Купер Т.А. Нарушение сплайсинга, регулируемого CUG-связывающим белком, при миотонической дистрофии. Наука. 1998; 280:737–741. [PubMed] [Google Scholar]
Наука. 1998; 280:737–741. [PubMed] [Google Scholar]
81. Савкур Р.С., Филипс А.В., Купер Т.А. Аберрантная регуляция альтернативного сплайсинга рецепторов инсулина связана с резистентностью к инсулину при миотонической дистрофии. Нат Жене. 2001; 29:40–47. [PubMed] [Google Scholar]
82. Huichalaf C, Sakai K, Jin B, Jones K, Wang GL, Schoser B, Schneider-Gold C, Sarkar P, Pereira-Smith OM, Timchenko N, et al. Экспансия повторов РНК CUG вызывает стресс и ингибирование трансляции в клетках миотонической дистрофии 1 (DM1). FASEB J. 2010; 24: 3706–3719.. [Бесплатная статья PMC] [PubMed] [Google Scholar]
83. Charlet-B N, Savkur RS, Singh G, Philips AV, Grice EA, Cooper TA. Потеря специфического для мышц хлоридного канала при миотонической дистрофии 1 типа из-за неправильной регуляции альтернативного сплайсинга. Мол Ячейка. 2002; 10:45–53. [PubMed] [Google Scholar]
84. Gambardella S, Rinaldi F, Lepore SM, Viola A, Loro E, Angelini C, Vergani L, Novelli G, Botta A. Сверхэкспрессия микроРНК-206 в скелетных мышцах при миотонической дистрофии больные 1 типа. J Transl Med. 2010;8:48. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Сверхэкспрессия микроРНК-206 в скелетных мышцах при миотонической дистрофии больные 1 типа. J Transl Med. 2010;8:48. [Бесплатная статья PMC] [PubMed] [Google Scholar]
85. Lee JE, Lee JY, Wilusz J, Tian B, Wilusz CJ. Систематический анализ цис-элементов в нестабильных мРНК показывает, что CUGBP1 является ключевым регулятором распада мРНК в мышечных клетках. ПЛОС Один. 2010;5:e11201. [Бесплатная статья PMC] [PubMed] [Google Scholar]
86. Zu T, Gibbens B, Doty NS, Gomes-Pereira M, Huguet A, Stone MD, Margolis J, Peterson M, Markowski TW, Ingram MA и др. . Трансляция, не инициируемая ATG, направляется микросателлитными расширениями. Proc Natl Acad Sci USA. 2011; 108: 260–265. [Бесплатная статья PMC] [PubMed] [Google Scholar]
87. Кумар А., Кумар В., Сингх С.К., Мутусвами С., Агарвал С. Несбалансированное соотношение оксидантов и антиоксидантов при миотонической дистрофии 1 типа. Свободнорадикальные рез. 2014; 48: 503–510. [PubMed] [Google Scholar]
88. Wheeler TM, Lueck JD, Swanson MS, Dirksen RT, Thornton CA. Коррекция сплайсинга ClC-1 устраняет хлоридную каналопатию и миотонию в мышиных моделях миотонической дистрофии. Джей Клин Инвест. 2007; 117:3952–3957. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Коррекция сплайсинга ClC-1 устраняет хлоридную каналопатию и миотонию в мышиных моделях миотонической дистрофии. Джей Клин Инвест. 2007; 117:3952–3957. [Бесплатная статья PMC] [PubMed] [Google Scholar]
89. Wheeler TM, Leger AJ, Pandey SK, MacLeod AR, Nakamori M, Cheng SH, Wentworth BM, Bennett CF, Thornton CA. Ориентация на ядерную РНК для коррекции миотонической дистрофии in vivo. Природа. 2012; 488:111–115. [Бесплатная статья PMC] [PubMed] [Google Scholar]
90. Wheeler TM, Sobczak K, Lueck JD, Osborne RJ, Lin X, Dirksen RT, Thornton CA. Изменение доминирования РНК замещением белка, секвестрированного на триплетных повторах РНК. Наука. 2009; 325:336–339. [PMC free article] [PubMed] [Google Scholar]
91. Furling D, Doucet G, Langlois MA, Timchenko L, Belanger E, Cossette L, Puymirat J. Вирусный вектор, продуцирующий антисмысловую РНК, восстанавливает функции миотонической дистрофии миобластов. Джин Тер. 2003; 10: 795–802. [PubMed] [Академия Google]
92. Mulders SA, van den Broek WJ, Wheeler TM, Croes HJ, van Kuik-Romeijn P, de Kimpe SJ, Furling D, Platenburg GJ, Gourdon G, Thornton CA, et al. Опосредованное триплетными повторами олигонуклеотидное обращение токсичности РНК при миотонической дистрофии. Proc Natl Acad Sci USA. 2009;106:13915–13920. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Mulders SA, van den Broek WJ, Wheeler TM, Croes HJ, van Kuik-Romeijn P, de Kimpe SJ, Furling D, Platenburg GJ, Gourdon G, Thornton CA, et al. Опосредованное триплетными повторами олигонуклеотидное обращение токсичности РНК при миотонической дистрофии. Proc Natl Acad Sci USA. 2009;106:13915–13920. [Бесплатная статья PMC] [PubMed] [Google Scholar]
93. Krol J, Fiszer A, Mykowska A, Sobczak K, de Mezer M, Krzyzosiak WJ. Рибонуклеаза дайсер расщепляет шпильки триплетных повторов на более короткие повторы, которые заглушают определенные мишени. Мол Ячейка. 2007; 25: 575–586. [PubMed] [Академия Google]
94. Zhang W, Wang Y, Dong S, Choudhury R, Jin Y, Wang Z. Лечение миотонической дистрофии 1 типа с помощью конструирования сайт-специфических РНК-эндонуклеаз, нацеленных на повторы (CUG)(n). Мол Тер. 2014;22:312–320. [Бесплатная статья PMC] [PubMed] [Google Scholar]
95. Wheeler TM. Миотоническая дистрофия: терапевтические стратегии на будущее. Нейротерапия. 2008; 5: 592–600. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
96. Lin X, Miller JW, Mankodi A, Kanadia RN, Yuan Y, Moxley RT, Swanson MS, Thornton CA. Нарушение MBNL1-зависимых постнатальных переходов сплайсинга при миотонической дистрофии. Хум Мол Жене. 2006; 15: 2087–209.7. [PubMed] [Google Scholar]
97. Warf MB, Nakamori M, Matthys CM, Thornton CA, Berglund JA. Пентамидин устраняет дефекты сплайсинга, связанные с миотонической дистрофией. Proc Natl Acad Sci USA. 2009;106:18551–18556. [Бесплатная статья PMC] [PubMed] [Google Scholar]
98. Griggs RC, Pandya S, Florence JM, Brooke MH, Kingston W, Miller JP, Chutkow J, Herr BE, Moxley RT. Рандомизированное контролируемое исследование тестостерона при миотонической дистрофии. Неврология. 1989; 39: 219–222. [PubMed] [Академия Google]
99. Walter MC, Reilich P, Lochmüller H, Kohnen R, Schlotter B, Hautmann H, Dunkl E, Pongratz D, Müller-Felber W. Моногидрат креатина при миотонической дистрофии: двойное слепое плацебо-контролируемое клиническое исследование. Дж Нейрол. 2002; 249:1717–1722. [PubMed] [Google Scholar]
Дж Нейрол. 2002; 249:1717–1722. [PubMed] [Google Scholar]
100. Schneider-Gold C, Beck M, Wessig C, George A, Kele H, Reiners K, Toyka KV. Моногидрат креатина при DM2/PROMM: двойное слепое плацебо-контролируемое клиническое исследование. Проксимальная миотоническая миопатия. Неврология. 2003; 60: 500–502. [PubMed] [Академия Google]
101. Сугино М., Осава Н., Ито Т., Исида С., Ямасаки Х., Кимура Ф., Шинода К. Пилотное исследование дегидроэпиандростерона сульфата при миотонической дистрофии. Неврология. 1998; 51: 586–589. [PubMed] [Google Scholar]
102. Heatwole CR, Eichinger KJ, Friedman DI, Hilbert JE, Jackson CE, Logigian EL, Martens WB, McDermott MP, Pandya SK, Quinn C, et al. Открытое исследование рекомбинантного человеческого инсулиноподобного фактора роста 1/рекомбинантного человеческого инсулиноподобного фактора роста, связывающего белок 3, при миотонической дистрофии 1 типа. Arch Neurol. 2011;68:37–44. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Миотоническая мышечная дистрофия — Детская больница Сиэтла
Что такое миотоническая мышечная дистрофия?
Мышечная дистрофия (МД) — это генетическое заболевание, которое со временем медленно ослабляет мышцы вашего ребенка. Существует несколько форм МД, которые могут поражать разные наборы мышц и вызывать большую или меньшую слабость.
Существует несколько форм МД, которые могут поражать разные наборы мышц и вызывать большую или меньшую слабость.
Миотоническая мышечная дистрофия (ММД) вызывает слабость, сокращение мышц и медленное расслабление некоторых мышц после их сокращения (миотония). Это может также повлиять на многие другие части тела вашего ребенка, такие как сердце, мозг, гормоны и зрение.
MMD широко варьируется от человека к человеку, даже в одной семье.
- У некоторых людей симптомы отсутствуют или симптомы настолько легкие, что человек не знает, что у них есть заболевание. Они могут узнать, что у них MMD, только если они пройдут генетическое тестирование после того, как родственнику будет поставлен диагноз.
- У других людей симптомы легче заметить. Они ухудшаются со временем, обычно медленно. MMD может изменить способности вашего ребенка и привести к целому ряду проблем со здоровьем, от легких до серьезных.
- Самая тяжелая форма ММД, которая начинается при рождении или вскоре после него (врожденная ММД), может быть опасной для жизни.
 Новорожденным с симптомами, которые могут быть вызваны MMD, обычно требуется неонатальная интенсивная терапия.
Новорожденным с симптомами, которые могут быть вызваны MMD, обычно требуется неонатальная интенсивная терапия.
MMD возникает из-за проблемы в гене DMPK на хромосоме 19 или в гене CNBP (также известном как ZNF9) на хромосоме 3.
Некоторые строительные блоки ДНК в этих генах повторяются намного чаще, чем обычно. Это препятствует тому, чтобы клетки в мышцах и других тканях вашего ребенка работали должным образом.
Если у ребенка ММД, это означает, что ему передался аномальный ген от одного из родителей. Часто у родителей были легкие симптомы или они отсутствовали, и они не знали, что являются носителями гена.
Если проблема в гене DMPK, то каждый раз, когда ген передается новому поколению, повторяющийся участок строительных блоков расширяется — иногда резко. (Это называется ожиданием.) Это может привести к более серьезным симптомам, которые начинаются в более раннем возрасте.
Родитель с MMD имеет 50% шанс передать ген каждому своему ребенку.

Существует 2 основных типа MMD, в зависимости от того, какой ген является аномальным:
- MMD1, также называемый типом 1: DMPK является аномальным. Симптомы могут начаться в любом возрасте. Обычно они начинаются у подростков или молодых людей.
- MMD2, также называемый типом 2: CNBP (ZNF9) ненормальный. Этот тип начинается позже, обычно между 30 и 60 годами.
Врачи часто группируют детей с ММД1 по возрасту, когда появились симптомы.
- Врожденный MMD: Начавшийся при рождении или незадолго до него.
- Начало в детстве MMD: Начало после младенчества, но до подросткового возраста. Этот тип иногда называют ММД с ювенильным началом.
- Начало во взрослом возрасте MMD: Начало в подростковом или взрослом возрасте. Этот тип иногда называют классическим ММД.
Миотоническую мышечную дистрофию также называют:
- Миотоническая дистрофия
- Миотоническая дистрофия, или СД (СД1 для типа 1 и СД2 для типа 2)
Каждый ребенок с ММД уникален.
 Врачам трудно предсказать, как MMD повлияет на вашего ребенка. Как правило, чем старше ваш ребенок, когда появляются симптомы, тем мягче последствия и тем медленнее прогрессирует заболевание.
Врачам трудно предсказать, как MMD повлияет на вашего ребенка. Как правило, чем старше ваш ребенок, когда появляются симптомы, тем мягче последствия и тем медленнее прогрессирует заболевание.MMD не всегда вызывает серьезную инвалидность, но может. Обычно у детей с более серьезной инвалидностью симптомы появляются в раннем детстве.
Это заболевание пока неизлечимо, но лечение симптомов, а также предотвращение или лечение осложнений может значительно улучшить качество жизни вашего ребенка. Вместе вы и лечащая команда вашего ребенка можете ставить цели и принимать решения по уходу, чтобы помочь вашему ребенку учиться и расти в полной мере.
Миотоническая мышечная дистрофия в детской больнице Сиэтла
Детская нервно-мышечная программа Сиэтла предлагает наиболее комплексную помощь детям с мышечной дистрофией на северо-западе Тихоокеанского региона.
- Ассоциация мышечной дистрофии присвоила нам статус Центра лечения MDA.

- Наша преданная команда — врачи, практикующие медсестры, терапевты, диетологи, генетические консультанты и социальные работники — обладают знаниями и опытом в диагностике и лечении ММД. Многие медицинские работники в сообществе не так хорошо знакомы с MMD, потому что они редко видят детей, у которых он есть.
- Seattle Children’s объединяет педиатрических специалистов из реабилитационной медицины, неврологии, легочной медицины и медицины сна, а также Центра сердца, чтобы оценить уникальные потребности вашего ребенка.
- Ассоциация мышечной дистрофии присвоила нам статус Центра лечения MDA.
- Мы разрабатываем и обеспечиваем уход, чтобы помочь вашему ребенку и семье справиться с MMD и обеспечить вашему ребенку наилучшее возможное функционирование и качество жизни сейчас и по мере его роста.
- Seattle Children’s предоставляет полный спектр услуг, от лекарств, физиотерапии и средств передвижения до искусственной вентиляции легких, ухода за сердцем и ортопедической хирургии.
- В нейромышечной программе ваш ребенок может видеть всю свою команду в 1 комнате в течение одного дня, что облегчит процесс для вас и вашего ребенка.

- Чтобы убедиться, что ваш ребенок прошел полное обследование и получил полноценный, скоординированный уход, мы привлечем экспертов со всех уголков Seattle Children’s.
- В зависимости от потребностей вашего ребенка в вашу команду могут входить специалисты из ортопедии, ортопедии, речевых и языковых служб, клиники нейроразвития и других специальностей и программ.
- В нейромышечной программе ваш ребенок может видеть всю свою команду в 1 комнате в течение одного дня, что облегчит процесс для вас и вашего ребенка.
Симптомы миотонической мышечной дистрофии
Симптомы MMD могут проявиться в любом возрасте и варьироваться от легких до серьезных. У вашего ребенка могут быть некоторые симптомы MMD, а не другие, и у него могут появиться новые симптомы в более позднем возрасте.
У детей с симптомами ММД при рождении или вскоре после него могут быть:
- Серьезные проблемы с дыханием из-за слабости дыхательных мышц
- Серьезная мышечная слабость и отсутствие мышечного тонуса, из-за чего они могут казаться вялыми
- Затрудненное сосание и глотание
- Косолапость или зажатые лодыжки
- Нарушение когнитивного развития
- Проблемы со слухом, зрением и речью
- Задержка развития
Дыхание и движения мышц улучшаются в первые пару лет.
 Большинство детей учатся сидеть, стоять и ходить. Для достижения этих вех может потребоваться больше времени, чем в среднем.
Большинство детей учатся сидеть, стоять и ходить. Для достижения этих вех может потребоваться больше времени, чем в среднем.По достижении подросткового возраста у детей с врожденной ММД начинают проявляться симптомы ММД у взрослых.
Если симптомы появляются в детстве, но после младенчества, первыми симптомами обычно являются:
- Умственная отсталость, например, трудности с планированием наперед, принятием решений, обработкой визуальной или пространственной информации или концентрацией внимания
- Неспособность к обучению
Ваш ребенок может также:
- Ограничивать или избегать взаимодействия с людьми или вести себя по-другому с людьми, опасаясь осуждения (избегающая личность)
- Кажется, что ему не хватает эмоций или интереса (апатичная личность), что может быть вызвано проблемами с организацией и обработкой информации и принятием решений, а не безразличием
Со временем у вашего ребенка начнутся проблемы с мышцами и другие симптомы ММД, начинающейся во взрослом возрасте.

Если симптомы появляются в подростковом или юношеском возрасте, первое, что вы можете заметить, это слабость скелетных мышц, которая постепенно ухудшается.
При MMD1 слабость обычно начинается в:
- На лице и шее, что может вызвать слабую улыбку, опущение век и затрудненное глотание
- Пальцы, кисти и предплечья, которые могут стать причиной слабого захвата
- Ступни и голени, что может привести к свисанию стопы
Со временем слабость может распространиться на другие группы мышц, например, на мышцы бедер и дыхательные мышцы.
Другие симптомы или последствия для здоровья MMD1 у взрослых могут включать:
- Миотония
- Сокращение мышц (атрофия)
- Проблемы с мышцами пищеварительной системы, которые могут привести к удушью, попаданию пищи или жидкости в дыхательные пути (аспирация), камням в желчном пузыре, запорам, диарее или боли
- Недостаточно хорошо дышит, особенно во сне
- Аритмия и кардиомиопатия
- Катаракта
- Когнитивные нарушения или трудности в обучении
- Избегающая личность или апатичная личность
- Необычайная сонливость в течение дня (что может быть связано со слабостью, затрудненным дыханием, влиянием MMD на мозг или другими факторами)
- Гормональные проблемы, такие как гипотиреоз, резистентность к инсулину, диабет или, у мужчин, гипогонадизм, ведущий к бесплодию
Некоторые из этих эффектов, такие как кардиомиопатия и катаракта, вряд ли повлияют на вашего ребенка в течение многих лет, если вообще повлияют на него.

ММД может поражать мышцы матки, поэтому девочки и женщины с ММД нуждаются в особом уходе, если они забеременеют.
Диагностика миотонической мышечной дистрофии
Врач вашего ребенка, скорее всего, назначит визит в клинику по телефону:
- Запросит вас о симптомах, развитии, истории болезни и семейной истории вашего ребенка
- Осмотрите своего ребенка и найдите признаки мышечной слабости и истощения, миотонии и других признаков мышечной дистрофии
Вашему ребенку могут потребоваться анализы, в том числе:
- Анализ крови для проверки уровня фермента (креатинкиназы в сыворотке), который повышается при повреждении мышц
- Генетический тест для поиска изменений в одном из генов, вызывающих MMD
- Электромиограмма (ЭМГ) для измерения электрических сигналов в мышцах
- Биопсия мышц, чтобы проверить, выглядят ли мышечные клетки вашего ребенка нормальными
Seattle Children’s также предлагает генетическое консультирование и тестирование для родителей и других членов семьи детей с мышечной дистрофией.
Чтобы понять, как MMD влияет на вашего ребенка, ваша команда Seattle Children’s может предложить другие тесты и обследования, например:
- Тесты моторики и силы
- Электрокардиограмма
- Тесты функции легких
- Анализы крови для выявления проблем со щитовидной железой или резистентности к инсулину
- Исследования сна
- Проверка зрения
- Оценка глотания
- Когнитивные тесты
Лечение миотонической мышечной дистрофии
В детском саду Seattle Children’s ваш ребенок получает полный уход от команды нашей нервно-мышечной программы и, при необходимости, от других наших программ. Мы предлагаем ряд процедур, которые помогут вашему ребенку стать сильнее, подвижнее, комфортнее и здоровее.
Не каждый ребенок с ММД нуждается во всех видах лечения. План лечения вашего ребенка будет разработан специально для него и будет меняться со временем по мере изменения его потребностей.
Хотя лекарства от MMD не существует, лечение может оказать большое влияние на качество жизни вашего ребенка, уменьшая или купируя последствия болезни.
В команду нейромышечной программы входят эксперты из реабилитационной медицины, эндокринологии, неврологии, пульмонологии и медицины сна и Центра сердца, а также диетолог, генетический консультант и социальный работник.
В зависимости от потребностей вашего ребенка мы привлекаем специалистов из других клиник и программ в районе Seattle Children’s, например:
- Гастроэнтерология при проблемах с пищеварением
- Нейроразвитие для проверки способности к обучению или проблем с обучением
- Речевые и языковые услуги, если у вашего ребенка проблемы с глотанием или общением
- Ортопедия, если операция на мышцах, сухожилиях или костях поможет вашему ребенку
- Офтальмология для оценки и лечения заболеваний глаз
Новорожденных с врожденным ММД лечат в нашем отделении интенсивной терапии новорожденных (ОИТН) уровня IV врачи, разбирающиеся в этой форме заболевания.
Общие методы лечения для поддержания способности вашего ребенка двигаться и делать то, что он хочет, включают:
- Физиотерапия для поддержания мышечного тонуса и улучшения диапазона движений
- Трудотерапия, чтобы помочь ребенку с такими действиями, как одевание и использование компьютерной клавиатуры
- Упражнения и растяжка для поддержания силы и выносливости вашего ребенка, улучшения напряженных мышц и суставов (контрактуры) и контроля боли
- Шины или скобы для рук или ног вашего ребенка, чтобы обеспечить поддержку, чтобы ваш ребенок мог делать больше самостоятельно
- Лекарственное средство для облегчения миотонии или боли в скелетных мышцах
- Устройства, которые помогают вашему ребенку передвигаться, например, ходунки или инвалидное кресло, или помогают ему выполнять повседневные задачи, например, специальный стул для сидения в душе
- Операция по устранению контрактур (скованность мышц и суставов) или помощь ребенку в ходьбе
Если диафрагма и другие дыхательные мышцы вашего ребенка слабы, мы оценим, насколько хорошо работают его легкие, уделяя особое внимание профилактике и лечению респираторных инфекций.

Инфекции могут стать серьезными, если из-за слабости дыхательных мышц вашему ребенку будет трудно откашливать мокроту. Устройство, называемое аппаратом от кашля, может помочь вашему ребенку сделать более глубокий вдох, а затем очистить дыхательные пути. Респираторный терапевт настраивает аппарат и учит вас, как им пользоваться.
Некоторым детям, рожденным с врожденным ММД, может потребоваться аппарат для помощи при дыхании сначала в отделении интенсивной терапии, пока они не смогут нормально дышать самостоятельно. Это может означать постоянное положительное давление в дыхательных путях (CPAP), двухуровневое положительное давление в дыхательных путях (Bi-PAP) или вентилятор.
Некоторым людям с MMD требуется CPAP или Bi-PAP, чтобы облегчить дыхание во время сна.
Ежегодно ваш ребенок будет проходить обследование для выявления проблем с электрическими сигналами, которые контролируют его частоту сердечных сокращений и ритм (дефекты сердечной проводимости).
 Программа детской аритмии в Сиэтле обеспечивает всестороннюю оценку и лечение, включая лекарства, имплантацию кардиостимулятора и имплантацию дефибриллятора.
Программа детской аритмии в Сиэтле обеспечивает всестороннюю оценку и лечение, включая лекарства, имплантацию кардиостимулятора и имплантацию дефибриллятора.Нейропсихолог может оценить поведение и когнитивные функции вашего ребенка, включая мышление, память, внимание и обучение, и порекомендовать лечение или услуги, которые могут понадобиться вашему ребенку, например:
- Стратегии специального образования
- Консультации
Дети с когнитивными нарушениями могут учиться с помощью преподавания и инструментов, соответствующих их способностям и потребностям.
Лекарства могут помочь в лечении ряда других эффектов MMD, в том числе:
- Инсулинорезистентность
- Гипотиреоз
- Гипогонадизм у мужчин
- Запор
Врач-диетолог будет работать с вами и вашим ребенком, чтобы:
- Убедитесь, что ваш ребенок получает необходимое количество калорий, чтобы иметь энергию, поддерживать силы и быть настолько здоровым и активным, насколько это возможно
- Профилактика или лечение запоров, диареи или камней в желчном пузыре
Детям, рожденным с врожденным ММД, может потребоваться назогастральный зонд, гастростомическая трубка, внутривенное (в/в) питание или специальная бутылочка для получения всех необходимых им питательных веществ.
Социальный работник занимается поддержкой вашего ребенка и семьи и помогает справиться с трудностями, социальными отношениями, поведением и эмоциями. Вместе с врачами, медсестрами и терапевтами вашего ребенка социальный работник соединит вас с полезными ресурсами в Seattle Children’s и в обществе.
Свяжитесь с нами
Обратитесь в Нейромышечную программу по телефону 206-987-2114, чтобы получить направление, второе мнение или дополнительную информацию.
Миотоническая мышечная дистрофия (неонатальная) | МедЛинк Неврология
PMID 11768387

PMID 298
PMID 7436809
ИДПМ 8116611
PMID 28484315
PMID 28257691
 Педиатр 1972; 81:83-6.
Педиатр 1972; 81:83-6.PMID 5034872
PMID 29
0
PMID 4814710
PMID 1310900
PMID 24613228
 , Левин С., Сиу В.М., Венанс С., Джейкоб П. Врожденная миотоническая дистрофия: канадское популяционное исследование. J Pediatr 2013;163(1):120-5.e1-3.
, Левин С., Сиу В.М., Венанс С., Джейкоб П. Врожденная миотоническая дистрофия: канадское популяционное исследование. J Pediatr 2013;163(1):120-5.e1-3.PMID 23415617
PMID 15060232
PMID 25504326
PMID 12601109
 Rev Neurol (Париж) 2016;172(10):572-80.
Rev Neurol (Париж) 2016;172(10):572-80.PMID 27665240
PMID 34655747
PMID 18541397
PMID 18337099

PMID 14223223
PMID 19543792
PMID 4735462
PMID 23622362
ПМИД 17892958
 Am J Med Genet B Neuropsychiatr Genet 2008;147B:918-26.
Am J Med Genet B Neuropsychiatr Genet 2008;147B:918-26.PMID 18228241
PMID 17587294
PMID 31701525
PMID 4150367
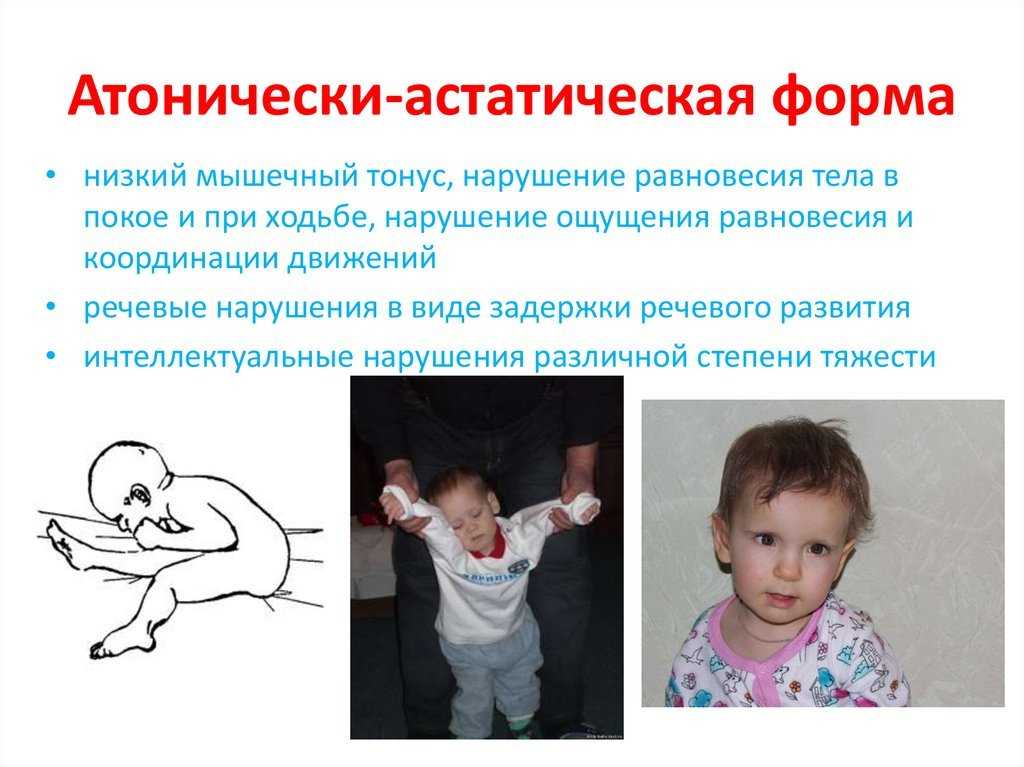 Наука 1992;255:1256-8.
Наука 1992;255:1256-8.PMID 1546326
PMID 27671786
PMID 17449544
PMID 28473756
PMID 1101835
 , Люббе Э., Розеро С. и др. Мексилетин при миотонической дистрофии 1 типа: рандомизированное двойное слепое плацебо-контролируемое исследование. Неврология 2021;96(2):e228-40.
, Люббе Э., Розеро С. и др. Мексилетин при миотонической дистрофии 1 типа: рандомизированное двойное слепое плацебо-контролируемое исследование. Неврология 2021;96(2):e228-40.PMID 33046619
PMID 29871899
PMID 26566479
PMID 32942085
 Neurol Clin Pract 2019;9(5):443-54.
Neurol Clin Pract 2019;9(5):443-54.PMID 31750030
PMID 27306634
PMID 32203199
PMID 34029782
PMID 4795420
 К., Чо Ч.Х., Ян Э.М., Сонг Э.С., Чой Ю.Ю. Транзиторная полная атриовентрикулярная блокада у недоношенного новорожденного с врожденной миотонической дистрофией: клинический случай. J Korean Med Sci 2014; 29:879-83.
К., Чо Ч.Х., Ян Э.М., Сонг Э.С., Чой Ю.Ю. Транзиторная полная атриовентрикулярная блокада у недоношенного новорожденного с врожденной миотонической дистрофией: клинический случай. J Korean Med Sci 2014; 29:879-83.PMID 24932094
PMID 26122101
PMID 28673557
PMID 15862193
 , Доган С., Де Антонио М. и др. Крупное многоцентровое исследование детской миотонической дистрофии 1 типа для доказательного лечения. Неврология 2019;92(8):e852-65.
, Доган С., Де Антонио М. и др. Крупное многоцентровое исследование детской миотонической дистрофии 1 типа для доказательного лечения. Неврология 2019;92(8):e852-65.PMID 30659139
PMID 31326502
PMID 30706460
PMID 32971903
 Наука 1992;255:1253-5.
Наука 1992;255:1253-5.PMID 1546325
PMID 33171139
PMID 17154336
PMID 26217220

PMID 24882752
PMID 34432028
PMID 25052313
PMID
21
PMID 26747623
 , Монктон Д.Г., Ле Н., Туладхар А.М., Раафорст Дж., ван Энгелен БГМ. Визуализация головного мозга при миотонической дистрофии 1 типа: систематический обзор. Неврология 2017;89(9):960-9.
, Монктон Д.Г., Ле Н., Туладхар А.М., Раафорст Дж., ван Энгелен БГМ. Визуализация головного мозга при миотонической дистрофии 1 типа: систематический обзор. Неврология 2017;89(9):960-9.PMID 28768849
PMID 33798646
PMID 35008780
PMID 25605794
 Мол Тер Нуклеиновые Кислоты 2017;9:337-48.
Мол Тер Нуклеиновые Кислоты 2017;9:337-48.PMID 29246312
PMID 5950778
PMID 33341951
PMID 8464127
PMID 32693949
 , Мацумура К., Кагеяма М. и др. Влияние недоношенности и длины повтора КТГ на исходы при врожденной миотонической дистрофии. Примечания BMC Res 2020; 13 (1): 4-9.
, Мацумура К., Кагеяма М. и др. Влияние недоношенности и длины повтора КТГ на исходы при врожденной миотонической дистрофии. Примечания BMC Res 2020; 13 (1): 4-9.PMID 32703309
PMID 1641160
PMID 779728
PMID 132914
PMID 29327796
 , Кусумото Т., Тагава М. и др. Два инфантильных случая врожденной миотонической дистрофии с желчнокаменной болезнью/холестазом. Pediatr Int 2005;47:586-8.
, Кусумото Т., Тагава М. и др. Два инфантильных случая врожденной миотонической дистрофии с желчнокаменной болезнью/холестазом. Pediatr Int 2005;47:586-8.PMID 161
PMID 808120
PMID
18
PMID 10722967

PMID 28698297
PMID 28376341
PMID 20179953
PMID 13780165
PMID 23384336

PMID 15036328
PMID 34830473
PMID 6028243
PMID 3564952
PMID 287
 Curr Opin Genet Dev 2017; 44:30-7.
Curr Opin Genet Dev 2017; 44:30-7.PMID 28213156
PMID 11807903
Согласованные рекомендации по лечению врожденной и детской миотонической дистрофии типа 1
Октябрь 2019 г.; 9 (5) ReviewOpen Access
Николас Э. Джонсон, Эудженио Сапата Алдана, Натали Ангерд, Тетсуо Ашизава, Кира Н. Берггрен, Кьяра Марини-Беттоло, Тина Дуонг, Анне-Берит Экстрем, Валерия Сансоне, Куиксия Тиан, Лия Хеллерштейн , Craig Campbell
Впервые опубликовано 24 апреля 2019 г., DOI: https://doi.org/10.1212/CPJ.0000000000000646
Полный PDF
Разрешения
Загрузки
2378
- Статья
- Цифры и данные
- Информация и раскрытие информации
Abstract
Цель обзора Миотоническая дистрофия 1 типа представляет собой мультисистемное заболевание, вызванное некодирующим триплетным повтором. Возраст начала варьирует на протяжении всей жизни, но в наиболее тяжелой форме симптомы появляются при рождении (врожденная миотоническая дистрофия) или в детском возрасте (миотоническая дистрофия с началом в детском возрасте). Эти дети имеют ряд нарушений, которые сокращают продолжительность жизни и вызывают значительную заболеваемость. В настоящее время нет согласованных рекомендаций по уходу за такими детьми.
Возраст начала варьирует на протяжении всей жизни, но в наиболее тяжелой форме симптомы появляются при рождении (врожденная миотоническая дистрофия) или в детском возрасте (миотоническая дистрофия с началом в детском возрасте). Эти дети имеют ряд нарушений, которые сокращают продолжительность жизни и вызывают значительную заболеваемость. В настоящее время нет согласованных рекомендаций по уходу за такими детьми.
Недавние находки Фонд миотонической дистрофии нанял 11 международных клиницистов, имеющих опыт лечения врожденной миотонической дистрофии и миотонической дистрофии с дебютом в детском возрасте, для разработки согласованных рекомендаций по лечению. Эксперты использовали двухэтапную методику с использованием элементов однотекстовой процедуры и методики номинальных групп. Завершение этого процесса привело к разработке клинических рекомендаций по уходу за этой популяцией.
Резюме Дети с миотонической дистрофией часто нуждаются в наблюдении и вмешательстве для увеличения продолжительности и качества жизни. Полученные рекомендации призваны стандартизировать и улучшить уход за детьми с миотонической дистрофией.
Полученные рекомендации призваны стандартизировать и улучшить уход за детьми с миотонической дистрофией.
Миотоническая дистрофия типа 1 (DM1) представляет собой аутосомно-доминантное заболевание, вызванное экспансией токсического повтора CTG в 3’UTR гена DMPK . 1,–,3 У взрослых с СД1 симптомы характеризуются прогрессирующей слабостью дистальных мышц, миотонией, ранней катарактой, сердечными и желудочно-кишечными проблемами и дисфункцией ЦНС. 4,5 Полиорганное поражение часто бывает более выраженным и с более ранним началом у лиц с дебютом симптомов в детстве. Возраст начала СД1 вариабелен, и повторная экспансия между поколениями (известная как ожидание) может привести к появлению симптомов в детстве. Когда симптомы появляются при рождении, это известно как врожденная миотоническая дистрофия (CDM). Появление симптомов после периода новорожденности и до 18 лет обычно называют детской миотонической дистрофией (ХДМ). Однако альтернативные определения обозначают дополнительные точки среза в зависимости от возраста начала заболевания. 6,7 Хотя точная глобальная распространенность неизвестна, дети с CDM, вероятно, составляют 10–30% от общей популяции с СД1. 4,8
6,7 Хотя точная глобальная распространенность неизвестна, дети с CDM, вероятно, составляют 10–30% от общей популяции с СД1. 4,8
Эти заболевания вызывают значительную заболеваемость и смертность. Детям с CDM часто требуется интенсивное вмешательство при рождении из-за гипотонии, дыхательной недостаточности и трудностей с кормлением. 4,9 У детей с ЦДМ, находящихся на ИВЛ дольше 3 мес, на первом году жизни отмечается 30% смертность. 10 У детей как с CDM, так и с ChDM в детстве могут быть симптомы, связанные с синдромом дефицита внимания и гиперактивностью или расстройством аутистического спектра (иногда называемым расстройством социальной коммуникации). 11,12 У них также наблюдается значительная задержка моторики 13 и могут быть трудноизлечимые симптомы раздраженного кишечника, включая недержание мочи. Предыдущие исследования показывают, что 88% людей с врожденной или детской миотонической дистрофией не имеют работы в возрасте старше 18 лет. 14
14
Мультисистемный характер, заболеваемость и смертность, связанные с врожденной и детской миотонической дистрофией, требуют разработки рекомендаций по уходу для стандартизации ухода. Эти рекомендации, основанные на консенсусе, также заложат основу для инновационных клинических инициатив там, где существуют пробелы, а также для дальнейших исследований по улучшению аспектов лечения. Эти рекомендации по уходу могут также лучше подготовить педиатрическое сообщество с СД1 к будущим клиническим испытаниям, потому что различия в клинической помощи могут иметь значительное влияние на результаты детей, участвующих в географически разбросанных клинических исследованиях.
Методы
Набор участников
Фонд миотонической дистрофии нанял клиницистов из США, Канады и Европы, имеющих опыт лечения детей с СД1, для разработки согласованных рекомендаций.
Консенсусный подход
Как было описано ранее, Фонд миотонической дистрофии разработал двухэтапную методологию достижения консенсуса с использованием компонентов единой текстовой процедуры и метода номинальной группы. 15 Этот подход был выбран из-за нехватки литературы по многим клиническим аспектам и обширного опыта клиницистов в этой области.
15 Этот подход был выбран из-за нехватки литературы по многим клиническим аспектам и обширного опыта клиницистов в этой области.
Трое авторов (N.E.J., C.C. и E.Z.) создали первоначальный проект документа, опираясь на существующую литературу и клиническую практику, которые послужили исходным текстом для разработки рекомендаций.
После создания единого текста заинтересованные стороны были привлечены к уточнению рекомендаций на основе подхода, основанного на консенсусе. Первоначально эксперты были назначены для конкретных областей рекомендаций, где они уточняли рекомендации. Затем фасилитатор (LH) проводит серию встреч для рассмотрения, пересмотра и окончательной доработки рекомендаций со всей группой авторов.
Результатом этих усилий стали окончательные рекомендации по уходу, основанные на консенсусе, а также краткое справочное руководство. Рекомендации по уходу разделены на 2 основных раздела: «Общие соображения по уходу» и «Системный подход к лечению». Поскольку существуют различия между СД1 с детским началом и врожденным СД1, рекомендации, относящиеся к СД1, разделены по всему документу. Краткое справочное руководство представлено в виде приложения, а полный документ доступен в Интернете (приложение e-1, links.lww.com/CPJ/A89).). Оба имеют блок-схемы и другую инфографику для простоты использования.
Поскольку существуют различия между СД1 с детским началом и врожденным СД1, рекомендации, относящиеся к СД1, разделены по всему документу. Краткое справочное руководство представлено в виде приложения, а полный документ доступен в Интернете (приложение e-1, links.lww.com/CPJ/A89).). Оба имеют блок-схемы и другую инфографику для простоты использования.
Общие рекомендации по уходу
Диагностика и классификация
Диагноз СД 1 следует заподозрить у любого ребенка с семейным анамнезом СД 1 и/или наличием одного или нескольких из следующих признаков:
◦ птоз век и/или орально-моторная слабость
◦ Дистальная слабость, преимущественно сгибателей пальцев и запястья, без контрактур или слабость сгибателей шеи
◦ Миотония или «жесткость» мышц
◦ Аутистические особенности или трудности в социальной связи
◦ Расстройство дефицита внимания, беспокойство и другие проблемы с поведенческими.

◦ Нарушения обучаемости (например, дислексия, дискалькулия)
◦ Чрезмерная дневная сонливость (EDS)
◦ Желудочно-кишечные расстройства: запор или диарея
◦ Сколиоз
◦ Арритмия
◦ Длительное выздоровление или остановка дыхания после анестезии
° Ноноона.
Классификация врожденного и детского СД1 представлена в таблице 1 Краткого справочного руководства. Обратите внимание, что диагноз может быть поставлен ретроспективно после анализа появления симптомов. Ткань плода с длинными повторами CTG не следует называть CDM, потому что этот диагноз зарезервирован для новорожденных. В этих случаях мы бы предложили использовать фетальный DM1 как более подходящий.
Генетическое консультирование рекомендуется для пациентов с клиническими признаками, указывающими на СД1, или для членов семьи из группы риска, чтобы они могли принять обоснованное решение о том, следует ли приступать к генетическому тестированию.
 Считается, что у людей с 37–49 повторами CTG очень маловероятно развитие обнаруживаемых симптомов СД1. Однако такие «премутации» могут распространяться на диапазон заболеваний в последующих поколениях, особенно если они передаются женщинами. Выявленным таким образом лицам следует предложить генетическое консультирование (см. Генетическое консультирование) для обсуждения риска передачи СД1.
Считается, что у людей с 37–49 повторами CTG очень маловероятно развитие обнаруживаемых симптомов СД1. Однако такие «премутации» могут распространяться на диапазон заболеваний в последующих поколениях, особенно если они передаются женщинами. Выявленным таким образом лицам следует предложить генетическое консультирование (см. Генетическое консультирование) для обсуждения риска передачи СД1.
Генетическое консультирование
Направление к генетическому консультированию (см. nsgc.org) рекомендуется для всех пациентов с врожденным и детским СД1 и их родителей, а также для оценки родителей для диагностики СД1.
Генетическое консультирование в пораженных семьях должно предоставлять информацию о:
◦ Типе наследования заболевания (аутосомно-доминантное наследование)
◦ Широкая вариабельность в масштабах и тяжести симптомов СД1, даже в пределах одной семья
◦ Возможность изменения масштабов и тяжести симптомов с течением времени
◦ Вероятность того, что мутация будет распространяться и заболевание станет более тяжелым по мере передачи из поколения в поколение (ожидание)
◦ Особое внимание к возможности рождения ребенка с тяжелым заболеванием у матери с минимальным заболеванием
◦ Варианты планирования семьи
Не используйте повторные номера КТГ, если они доступны, для генетической консультации или прогноза; их необходимо обсудить с консультантом-генетиком.
 В частности, размер повтора может быть показателем тяжести, но он не дает никакой информации о прогнозе.
В частности, размер повтора может быть показателем тяжести, но он не дает никакой информации о прогнозе.
Фокус на CDM
Неонатальный уход
Акушер-акушер — с высоким риском должен оказывать дородовую акушерскую помощь матерям, о которых известно или предполагается, что они вынашивают ребенка с СД1.
Врач-педиатр или специалист по неонатологии должен присутствовать при родах, если известно, что у матери СД1 или если известно или подозревается наличие СД1 у ребенка.
Фокус на CDM
Детям с CDM часто требуется лечение в отделении интенсивной терапии новорожденных, где есть возможность заниматься поддержкой дыхания и кормления. Этой команде требуется ряд неонатальных специалистов и специалистов-консультантов, которые могут справиться с генетическими, респираторными, желудочно-кишечными, ортопедическими, нервно-мышечными, нейрохирургическими и сердечными проблемами. См.
 рис. 1 в Кратком справочном руководстве по неонатальной помощи.
рис. 1 в Кратком справочном руководстве по неонатальной помощи.
Консультирование и ведение в конце жизни
Рекомендовать введение паллиативной помощи во время постановки диагноза и через регулярные промежутки времени после этого. При наличии официальной педиатрической бригады паллиативной помощи следует проконсультироваться с ними.
Распознавание и решение проблемы опекуна, независимо от того, есть ли у опекуна DM1, предложение временного ухода или эквивалентных мер для пациента для улучшения поддержки семьи. Обратитесь к обычному горю со стороны пациента и его семьи и при необходимости предложите психологическую помощь.
Составьте план оказания неотложной медицинской помощи и заблаговременно распорядитесь вместе с семьей.
Фокус на CDM
Ввести понятие о том, что естественное течение болезни включает прогрессивное улучшение силы в течение первого десятилетия жизни; однако осложнения CDM могут быть критическими и иметь высокий риск смертности, особенно в первый год жизни.

Сообщите семьям или лицам, осуществляющим уход, о том, что инвазивная и неинвазивная вентиляция легких (НИВЛ) и питание через гастростому являются приемлемыми элементами ухода за пациентами с CDM.
Хирургия и анестезия
Проинформируйте всех лиц, осуществляющих уход, о том, что любой, кто вводит анестетик, должен знать о диагнозе СД1.
По возможности совмещайте процедуры под одной седацией.
Организуйте визит перед анестезией для всех детей, планирующих провести глубокую седацию для диагностического теста, процедуры или операции. Если возможно, пригласите на этот визит пульмонолога, специализирующегося на нервно-мышечных заболеваниях.
Даже если у пациента СД 1 легкой степени тяжести, мониторинг в течение более длительного периода времени, чем обычно, после анестезии или хирургического вмешательства позволит выявить серьезные нежелательные явления в условиях стационара.
Поставщикам медицинских услуг рекомендуется ознакомиться с документом Фонда миотонической дистрофии «Практические предложения по анестезиологическому лечению пациента с миотонической дистрофией» (myotonic.
 org/sites/default/files/MDF_LongForm_AnesGuidelines_01C.pdf) на предмет рисков анестезии и рекомендаций перед любыми операциями или процедуры, требующие анестезии и Краткое справочное руководство по анестезии (myotonic.org/sites/default/files/MDF Anesthesia Guidelines FNL 2016 2 2. pdf). Эти документы должны быть рассмотрены до принятия решения о лечении.
org/sites/default/files/MDF_LongForm_AnesGuidelines_01C.pdf) на предмет рисков анестезии и рекомендаций перед любыми операциями или процедуры, требующие анестезии и Краткое справочное руководство по анестезии (myotonic.org/sites/default/files/MDF Anesthesia Guidelines FNL 2016 2 2. pdf). Эти документы должны быть рассмотрены до принятия решения о лечении.
Фокус на МДК
Системный подход к ведению
Респираторная система
Признаки респираторных нарушений у детей с миотонической дистрофией включают неэффективный кашель, рецидивирующие легочные инфекции, ортопноэ, одышку, плохой сон, утренние головные боли , усталость и храп.
См. рис. 2 в Кратком справочном руководстве, где представлена блок-схема вариантов тестирования и лечения при врожденной миотонической дистрофии и миотонической дистрофии с дебютом в детском возрасте.
Фокус на CDM
У детей с CDM, которые остаются на более длительной трахеостомической вентиляции, часто наблюдается улучшение силы дыхания с течением времени, и после тщательного рассмотрения с многопрофильной командой, включая невролога, следует рассмотреть вопрос о деканюляции трахеостомы.
 ; респираторология; ухо, нос и горло; и семья. Учет контроля проходимости дыхательных путей, частота респираторных инфекций, способность переносить лицевую или назальную маску для НИВЛ, а также соблюдение и сотрудничество с поддерживающей легочной терапией, такой как помощь при кашле, задержка дыхания и т. д. Перед деканюляцией следует провести тестирование на гиповентиляцию во сне.
; респираторология; ухо, нос и горло; и семья. Учет контроля проходимости дыхательных путей, частота респираторных инфекций, способность переносить лицевую или назальную маску для НИВЛ, а также соблюдение и сотрудничество с поддерживающей легочной терапией, такой как помощь при кашле, задержка дыхания и т. д. Перед деканюляцией следует провести тестирование на гиповентиляцию во сне.
Сердечно-сосудистые заболевания
Информировать членов семьи о рисках аритмий и сердечной дисфункции и о важности неотложной медицинской помощи при появлении симптомов (например, учащенного сердцебиения, предобморочного состояния, обморока, одышки, боли в груди, необъяснимой усталости).
◦ ЭКГ в 12 отведениях должна выполняться при установлении диагноза СД1, и, если все в норме и пациент остается бессимптомным, ЭКГ следует выполнять ежегодно и требует дополнительного обследования, если у пациента есть симптомы.
◦ Если ЭКГ нормальная, а клинические подозрения высоки, 24-часовое холтеровское мониторирование может рассматриваться как исследование второй линии.

◦ Поскольку некоторые лекарства, такие как мексилетин и психостимуляторы, являются антиаритмическими, рекомендуется снимать ЭКГ перед применением, снова в течение 3 месяцев после начала терапии, а затем с последовательными интервалами.
◦ Рассмотрите возможность проведения стационарного кардиомониторинга для выявления аритмий при госпитализации на более длительный срок, чем обычно, после хирургических процедур или при госпитализации в связи с тяжелым заболеванием или инфекцией
Для молодых пациентов с СД1 могут быть рассмотрены серийные нагрузочные тесты и ЭКГ с усреднением сигнала.
Оценка и лечение с помощью Американской ассоциации кардиологов (AHA) ([Американский колледж кардиологов]/AHA)/ESC (Европейское общество кардиологов) Руководство по ведению пациентов с желудочковыми аритмиями и профилактике внезапной сердечной смерти (см. ncbi.nlm.nih.gov/pubmed/16949478) — раздел по вопросам педиатрии 13.
 4. Слабость скелетных мышц, ортопедические осложнения и реабилитация0003
4. Слабость скелетных мышц, ортопедические осложнения и реабилитация0003◦ Валовая задержка двигателя
◦ Валовая и тонкая моторная слабость
◦ Дизартрия и потенциальная расширенная и альтернативная связь
◦ Задержка. для сколиоза и, при необходимости, рассмотреть вопрос о корсетировании или направлении к хирургу-ортопеду.
Детей следует поощрять к участию в логопедических занятиях, нацеленных на речь, язык и общение, с самого раннего возраста.
Акцент на CDM
Новорожденным с CDM часто трудно вскармливаться и следует рассмотреть альтернативное питание. Примерно через год активной работы с логопедом или эрготерапевтом большинство детей обычно могут переходить на оральное питание.
У детей с CDM наблюдается прогрессивное улучшение проксимальной силы как минимум до подросткового возраста. Поэтому детей следует поощрять к физической активности.

Профилактика контрактур суставов является ключом к лечению и должна тщательно контролироваться при раннем начале растяжения. Лечение эквиноварусной косолапости и других контрактур суставов должно включать в себя начальную растяжку и соответствующую фиксацию голеностопного сустава (при эквиноварусной косолапости). Можно рассмотреть возможность серийного литья.
Миотония скелетных мышц
Замедленная релаксация после захвата или перкуссии, затруднения, связанные с повседневной деятельностью, прогрессирующее нарушение речи или выраженные симптомы раздраженного кишечника являются признаками, часто связанными с миотонией.
Мексилетин (Мекситил) является вариантом лечения миотонии, если она проявляется и беспокоит пациента. Мексилетин может быть одобрен для использования не во всех странах. В этих случаях можно рассмотреть возможность применения других антагонистов натриевых каналов.
◦ Поскольку мексилетин является антиаритмическим средством, рекомендуется проводить ЭКГ перед применением, повторно в течение 3 месяцев после начала терапии, а затем с последовательными интервалами.

◦ Проинструктируйте пациента, чтобы он избегал диспепсии и преходящих «головокружений», связанных с лечением мексилетином, принимая его с пищей для увеличения абсорбции и снижения пикового уровня в крови.
Лечение глаз и слуха
Необходимо проводить базовую аудиометрию, особенно в школьном возрасте.
Офтальмологическое обследование следует проводить при постановке диагноза и не реже одного раза в год для оценки дальнозоркости, стигматизма, косоглазия и остроты зрения, чтобы предотвратить развитие нарушений зрения.
Птоз век; если птоз становится тяжелым и мешает зрению, может быть оправдано вмешательство, такое как «костыли» для век, которые можно вставить в очки. Попробуйте костыли в качестве средства от птоза, прежде чем рассматривать операцию на веках из-за риска анестезии. Можно рассмотреть офтальмологические лубриканты для лечения сухости глаз.
Лечение желудочно-кишечного тракта и мочеполовой системы
Наличие желудочно-кишечных симптомов, таких как боль в животе, запор, недержание кала или диарея, может быть частой проблемой.
 Симптомы могут имитировать синдром раздраженного кишечника (СРК). 15 Добавка клетчатки (более 8 г в день) является терапией первой линии.
Симптомы могут имитировать синдром раздраженного кишечника (СРК). 15 Добавка клетчатки (более 8 г в день) является терапией первой линии.Мягкие слабительные (см. ниже) при запорах. Масла следует избегать, так как они могут привести к диарее. Если пациент не отвечает на приведенные ниже рекомендации первой или второй линии, следует рассмотреть вопрос о направлении к гастроэнтерологу для проведения анальной манометрии:
◦ Рекомендации по терапии первой линии: полиэтиленгликоль (Миралакс), сенна (Ex-Lax, Senokot), докузат (Colace) или лактулоза (Cholac)
◦ Рекомендации по терапии второй линии: бисакодил (Dulcolax , Correctol), lubiprostone (Amitiza) или linaclotide (Linzess)
◦ Метоклопрамид (Reglan) можно использовать для уменьшения симптомов гастропареза, псевдообструкции и желудочного рефлюкса. Медицинские работники должны знать о риске острых дистонических реакций при приеме этого лекарства. Длительное применение не рекомендуется, поскольку этот препарат может вызвать позднюю дискинезию.

◦ Холестирамин и лоперамид являются другими вариантами лечения при преимущественно диарее и антихолинергических препаратах, таких как гиосциамина сульфат, при наличии СРК. Поскольку антихолинергические препараты могут оказывать антиаритмическое действие, о лечении см. раздел «Кардиотерапия».
◦ Мексилетин может рассматриваться при рефрактерной диарее или запоре, поскольку препарат может быть антиаритмическим, см. раздел «Кардиотерапия», посвященный лечению.
Если при дыхательном тесте обнаруживается избыточный рост бактерий, лечение антибиотиками может уменьшить диарею.
Фокус на CDM
Как упоминалось в разделе неонатальной помощи, детям с CDM может потребоваться временная трубка для кормления. Если дисфагия сохраняется, следует рассмотреть возможность энтерального питания. Обратитесь к логопеду. Детей следует периодически переоценивать для улучшения дисфагии.
Детям с CDM часто помогает терапия дисфагии.
 При агрессивной терапии дисфагии дети с CDM часто могут питаться перорально в течение первого года жизни.
При агрессивной терапии дисфагии дети с CDM часто могут питаться перорально в течение первого года жизни.
Управление развитием нервной системы
Рекомендации
Каждому ребенку с СД 1 следует проводить нейропсихологическое тестирование для выявления сильных и слабых сторон когнитивных функций. Это может включать следующее:
◦ Психометрическая оценка общих интеллектуальных способностей и адаптивных функций
◦ Оценка исполнительных функций
◦ Оценка социального познания
◦Assessment of visuomotor integration and visuospatial ability
◦ Assessment of receptive and expressive language abilities
◦ Assessment of EDS
◦ Assessment of learning disabilities (specific tests for dyscalculia, dyslexia, and dyspraxia )
Обследования следует проводить при врожденной форме в дошкольном возрасте и повторять, в зависимости от уровня функционирования, 2–3 раза до наступления совершеннолетия.
 При СД1 детского возраста нейропсихологическое тестирование рекомендуется проводить при постановке диагноза и повторять в дошкольном или школьном возрасте, а также в студенческие годы.
При СД1 детского возраста нейропсихологическое тестирование рекомендуется проводить при постановке диагноза и повторять в дошкольном или школьном возрасте, а также в студенческие годы.Пациентов с психическими или поведенческими проблемами следует направлять к специалисту по психическому здоровью для оценки расстройств аутистического спектра, дефицита внимания с гиперактивностью или без нее, алекситмии и других поведенческих проблем.
Психостимуляторы могут быть полезны, если дефицит внимания связан с ухудшением уровня усталости или СЭД (см. чрезмерная дневная сонливость). Поскольку психостимуляторы могут быть проаритмическими, см. раздел «Кардиотерапия», посвященный управлению стимуляторами:
◦ Антидепрессанты, усиливающие серотонин, при наличии чрезмерной тревожности или других излечимых психических симптомов
◦ Специальные программы когнитивной реабилитации для повышения социально-эмоциональных способностей (визуальный контакт, совместное внимание, эмоциональная регуляция) или эффективности исполнительных функций (тормозной контроль , внимания, рабочей памяти и когнитивной гибкости) с использованием специального программного обеспечения (например, Cogmed®)
Необходимо рассмотреть языковую коррекцию и терапию чтения из-за наличия когнитивного дефицита даже у детей с нормальным интеллектом.
 Дефицит внимания, утомляемость и дисфункция зрительно-пространственного построения могут привести к специфическим расстройствам обучения с нарушением чтения и правописания, а также математики.
Дефицит внимания, утомляемость и дисфункция зрительно-пространственного построения могут привести к специфическим расстройствам обучения с нарушением чтения и правописания, а также математики.
Психосоциальное сопровождение
Медицинские работники несут ответственность за координацию услуг специализированного ухода и поддержки для детей с СД1. Необходимо быть настороже в отношении психологических и социальных дисфункций и следить за домашними и образовательными обстоятельствами. Связь между агентствами необходима для обеспечения последовательного подхода между агентствами здравоохранения, образования и социального обеспечения.
Дети с СД1 должны иметь доступ к соответствующим психологическим и терапевтическим услугам в раннем возрасте, чтобы гарантировать, что они максимально реализуют свой потенциал и изучают стратегии выживания в дальнейшей жизни. Модификация деятельности, включая стратегии социальной активности, послужит основой для роста уверенности и уважения каждого ребенка.

Семейный уход и поддержка необходимы на протяжении всего детства, а при необходимости поддержка и социальная помощь. Школы должны быть обеспечены специальной информацией об уходе и ведении ребенка с СД1. Консультация по социальной работе или направление к специалисту по медицинскому обслуживанию также могут быть полезны для пациентов. Целостный подход имеет решающее значение, поскольку пострадавшему родителю также может потребоваться дополнительная помощь.
Семьи должны иметь доступ к пособиям по инвалидности, адекватному жилью и адаптации во время прогрессирования заболевания.
Чрезмерная дневная сонливость
Члены семьи и педагоги должны быть осведомлены о EDS, который приходит с DM1.
Детей следует обследовать на наличие признаков СЭД, включая продолжительный сон или засыпание в школе.
Возможное апноэ во сне следует оценивать с помощью ночной оксиметрии или полисомнограммы.

Вентиляция с положительным давлением может быть рассмотрена, если сонливость пациента с СД1 связана с ночной или дневной гиповентиляцией или апноэ во сне. Пациентов следует направлять к пульмонологам, имеющим опыт лечения нервно-мышечных заболеваний, для рассмотрения вопроса о вспомогательной вентиляции легких.
Стимулирующая терапия психостимуляторами, такими как модафинил (Provigil), метилфенидат или другие стимуляторы, может быть рассмотрена при подозрении на центральную гиперсомнию. Часто трудности с бодрствованием в школе являются провоцирующим фактором. Особую осторожность следует соблюдать у детей с ранее выявленной сердечной аритмией (см. раздел «Кардиотерапия» по применению стимуляторов).
Эндокринная система и обмен веществ
Пациенты мужского пола с СД1 должны пройти детальное физикальное обследование для выявления атрофии гонад или крипторхизма.
Пациентам следует измерять уровень HbA1c, тиреотропного гормона и свободного T4 исходно и каждые 3 года или при наличии клинического подозрения.

Подростки должны проходить скрининг как взрослые пациенты:
◦ Недостаточность гонад и осложнения со стороны репродуктивной системы: Запрос на аменорею или дисменорею у пациенток женского пола и эректильную дисфункцию у пациентов мужского пола
липиды, глюкоза плазмы, ферменты печени, уровни билирубина и гамма-глутамилтранспептидаза должны быть измерены на исходном уровне.
Выводы
Рекомендации по лечению врожденной миотонической дистрофии и миотонической дистрофии с дебютом в детском возрасте были созданы на основе консенсуса клиницистов, имеющих опыт ведения таких больных. Учитывая отсутствие тщательных исследований во многих из этих областей, эти рекомендации были созданы на основе консенсуса. Они предназначены для стандартизации ухода за детьми с полисистемным заболеванием, которое приводит к значительной заболеваемости и смертности.
Финансирование исследования
Фонд миотонической дистрофии.
Раскрытие информации
Н. Джонсон входит в состав научных консультативных советов Cytokinetics, AveXis, AMO Pharma и Biogen Idec; получил финансирование на поездку и / или гонорары выступающих от Strongbridge; работает консультантом для AMO Pharma, AveXis и Vertex Pharma; и получает исследовательскую поддержку от Ionis Pharmaceuticals, Biogen Idec, Valerion Therapeutics, Cytokinetics, Acceleron, AveXis, AMO Pharma, NIH/NINDS, FDA, Ассоциации мышечной дистрофии и Фонда миотонической дистрофии. Э.З. Алдана и Н. Ангерд не сообщают о раскрытии информации. Т. Ашизава входит в состав научных консультативных советов Фонда миотонической дистрофии, Национального института здравоохранения и Национального фонда атаксии; получил финансирование на поездку от Biohaven, PacBio и NIH; получает исследовательскую поддержку от Фонда миотонической дистрофии, Национального фонда атаксии, Biohaven Pharmaceuticals, Biogen и NIH/NINDS; и является профессором Медицинского колледжа Вейла Корнелла, адъюнкт-профессором Медицинского колледжа Бэйлора, приглашенным преподавателем Центрального Южного Университета, Китай. К.Н. Берггрен входит в научный консультативный совет Biogen и получает финансирование на поездки и / или гонорары спикеров от HDSA и FSH Society. К. Марини-Беттоло входил в состав научных консультативных советов компаний Avexis и Biogen. Т. Дуонг, А.-Б. Экстрем, В. Сансоне, К. Тиан и Л. Хеллерштейн не сообщают о раскрытии информации. К. Кэмпбелл входит в состав научных консультативных советов компаний Catabasis и PTC Therapeutics и получает исследовательскую поддержку от компаний Valerion Pharmaceuticals, PTC Therapeutics, Pfizer, Ionis, Eli Lilly, Prosensa, Child Health Foundation и Jesse’s Journey Foundation. Полная форма раскрытия информации, предоставленная авторами, доступна с полным текстом этой статьи на Neurology.org/cp.
К.Н. Берггрен входит в научный консультативный совет Biogen и получает финансирование на поездки и / или гонорары спикеров от HDSA и FSH Society. К. Марини-Беттоло входил в состав научных консультативных советов компаний Avexis и Biogen. Т. Дуонг, А.-Б. Экстрем, В. Сансоне, К. Тиан и Л. Хеллерштейн не сообщают о раскрытии информации. К. Кэмпбелл входит в состав научных консультативных советов компаний Catabasis и PTC Therapeutics и получает исследовательскую поддержку от компаний Valerion Pharmaceuticals, PTC Therapeutics, Pfizer, Ionis, Eli Lilly, Prosensa, Child Health Foundation и Jesse’s Journey Foundation. Полная форма раскрытия информации, предоставленная авторами, доступна с полным текстом этой статьи на Neurology.org/cp.
Приложение Авторы
Сноски
Информация о финансировании и раскрытие информации представлены в конце статьи. Полная форма раскрытия информации, предоставленная авторами, доступна с полным текстом этой статьи на Neurology.org/cp.

Плата за обработку статьи финансировалась Фондом миотонической дистрофии.
- Поступила 21 декабря 2018 г.
- Принята 04 марта 2019 г.
Это статья с открытым доступом, распространяемая в соответствии с лицензией Creative Commons Attribution-NonCommercial-NoDerivatives License 4.0 (CC BY-NC-ND), которая разрешает загрузку и совместное использование работы при условии правильного цитирования. Работа не может быть каким-либо образом изменена или использована в коммерческих целях без разрешения журнала.
Ссылки
- 1.↵
- Fu YH,
- Pizzuti A,
- Fenwick RG Jr., et al
. Нестабильный триплетный повтор в гене, связанном с миотонической мышечной дистрофией. Наука 1992;255:1256–1258.

- 2.↵
- Brook JD,
- McCurrach ME,
- Harley HG и др.
. Молекулярная основа миотонической дистрофии: экспансия тринуклеотидного (CTG) повтора на 3’-конце транскрипта, кодирующего члена семейства протеинкиназ. Сотовый 1992; 68: 799–808.
- 3.↵
- Махадеван М.,
- Цильфидис С.,
- Сабурин Л. и др.
. Мутация миотонической дистрофии: нестабильный повтор CTG в 3′-нетранслируемой области гена. Наука 1992;255:1253–1255.
- 4.↵
- Harper PS
. Миотоническая дистрофия, 3-е изд. Лондон: WB Сондерс; 2001.
- 5.↵
- Bugiardini E,
- Meola G
; Группа ДМ-ЦНС. Консенсус в отношении вовлечения головного мозга в миотоническую дистрофию.
 Нервно-мышечное расстройство 2014; 24:445–452.
Нервно-мышечное расстройство 2014; 24:445–452. - 6.↵
- Koch MC,
- Grimm T,
- Harley HG,
- Harper PS
. Генетические риски для детей женщин с миотонической дистрофией. Am J Hum Genet 1991; 48:1084–1091.
- 7.↵
- Gagnon C,
- Heatwole C,
- Hébert LJ, et al
. Отчет о третьей оценке результатов лечения миотонической дистрофии типа 1 (OMMYD-3), международный семинар Париж, Франция, 8 июня 2015 г. J Neuromuscul Dis 2018;5:523–537.
- 8.↵
- Johnson NE,
- Hung M,
- Nasser E, и др.
. Влияние беременности на миотоническую дистрофию: исследование на основе регистра. J Neuromuscul Dis 2015;2:447–452.
- 9.↵
- Кэмпбелл С.
 ,
, - Левин С.,
- Сиу В.М. и др.
. Врожденная миотоническая дистрофия: канадское популяционное эпиднадзорное исследование. J Pediatr 2013;163:120–123.
- Кэмпбелл С.
- 10.↵
- Кэмпбелл С,
- Шерлок Р,
- Джейкоб П,
- Блейни М
. Врожденная миотоническая дистрофия: длительность вспомогательной вентиляции и исход. Педиатрия 2004;113:811–816.
- 11.↵
- Анжард Н.,
- Гарджуло М.,
- Жакет А. и др.
. Когнитивный профиль при детской миотонической дистрофии 1 типа: есть ли глобальные нарушения? Нервно-мышечное расстройство 2007;17:451–458.
- 12.↵
- Экстром AB,
- Hakenas-Plate L,
- Tulinius M,
- Wentz E
.


