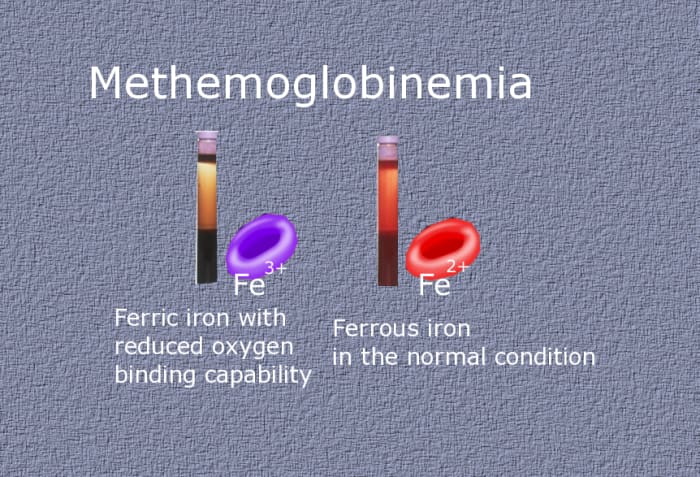
Метгемоглобинемия это: Метгемоглобин в крови
причины, симптомы, диагностика и лечение
Метгемоглобинемия – состояние, характеризующееся повышенным содержанием метгемоглобина (окисленного гемоглобина) в крови и тканевой гипоксией. Развитие метгемоглобинемии сопровождается акроцианозом, слабостью, головными болями, головокружением, сердцебиением, одышкой при нагрузке. Характерным признаком метгемоглобинемии служит коричнево-шоколадный цвет крови. Для подтверждения диагноза проводится оценка симптоматики, лабораторные исследования и тесты. При тяжелой степени метгемоглобинемии показана кислородотерапия, введение аскорбиновой кислоты, раствора метиленового синего, в ряде случаев — обменная гемотрансфузия.
Общие сведения
Метгемоглобинемия – увеличение уровня гемоглобина, содержащего окисленное железо (метгемоглобин – MtHb), в эритроцитах крови. Метгемоглобин относится к так называемым дисгемоглобинам — дериватам гемоглобина, не способным транспортировать кислород. В обычных условиях в крови присутствует небольшое количество метгемоглобина — не более 1% от общего содержания Hb. При метгемоглобинемии эндогенные механизмы оказываются не способными регулировать концентрацию дисгемоглобина, в результате чего страдает кислородно-транспортная функция эритроцитов. В гематологии метгемоглобинемии подразделяются на наследственные и приобретенные. Первые из них распространены среди коренного населения Аляски, Гренландии, Якутии; частота развития приобретенных метгемоглобинемий неизвестна.
При метгемоглобинемии эндогенные механизмы оказываются не способными регулировать концентрацию дисгемоглобина, в результате чего страдает кислородно-транспортная функция эритроцитов. В гематологии метгемоглобинемии подразделяются на наследственные и приобретенные. Первые из них распространены среди коренного населения Аляски, Гренландии, Якутии; частота развития приобретенных метгемоглобинемий неизвестна.
Метгемоглобинемия
Причины метгемоглобинемии
В процессе метаболических превращений в крови здоровых людей в очень небольших количествах образуются дисгемоглобины: карбоксигемоглобин, сульфгемоглобин, метгемоглобин (0,1-1 %). Вместе с тем, в эритроцитах содержится ряд факторов, которые поддерживают долю фракции метгемоглобина на уровне, не превышающем 1,0-1,5% от общего Hb. В частности, в реакции восстановления метгемоглобина в гемоглобин участвует фермент метгемоглобин-редуктаза. В отличие от оксигемоглобина (НbО2), содержащего восстановленное железо (Fe++), в метгемоглобине содержится окисленное железо (Fe+++), не способное переносить кислород. Поэтому при метгемоглобинемии, прежде всего, страдает кислородно-транспортная функция крови, следствием которой служит тканевая гипоксия.
Поэтому при метгемоглобинемии, прежде всего, страдает кислородно-транспортная функция крови, следствием которой служит тканевая гипоксия.
Наследственные формы метгемоглобинемии представлены либо ферментопатиями (врожденной низкой активностью или отсутствием фермента метгемоглобин-редуктазы), либо М-гемоглобинопатиями (синтезом аномальных белков, содержащих окисленное железо).
В структуре приобретенных (вторичных) метгемоглобинемий выделяют токсические экзогенные и токсические эндогенные формы. Метгемоглобинемии экзогенного происхождения могут быть связаны с передозировкой лекарственных средств (сульфаниламидов, нитритов, викасола, противомалярийных препаратов, лидокаина, новокаина и др.) или отравлением химическими агентами (анилиновыми красителями, нитратом серебра, тринитротолуолом, хлорбензолом, питьевой водой и пищевыми продуктами с высоким содержанием нитратов и др.).
Повышенный уровень MtHb в крови наблюдается у недоношенных и доношенных новорожденных, что связано с низкой активностью фермента метгемоглобин-редуктазы и окислительным стрессом в родах.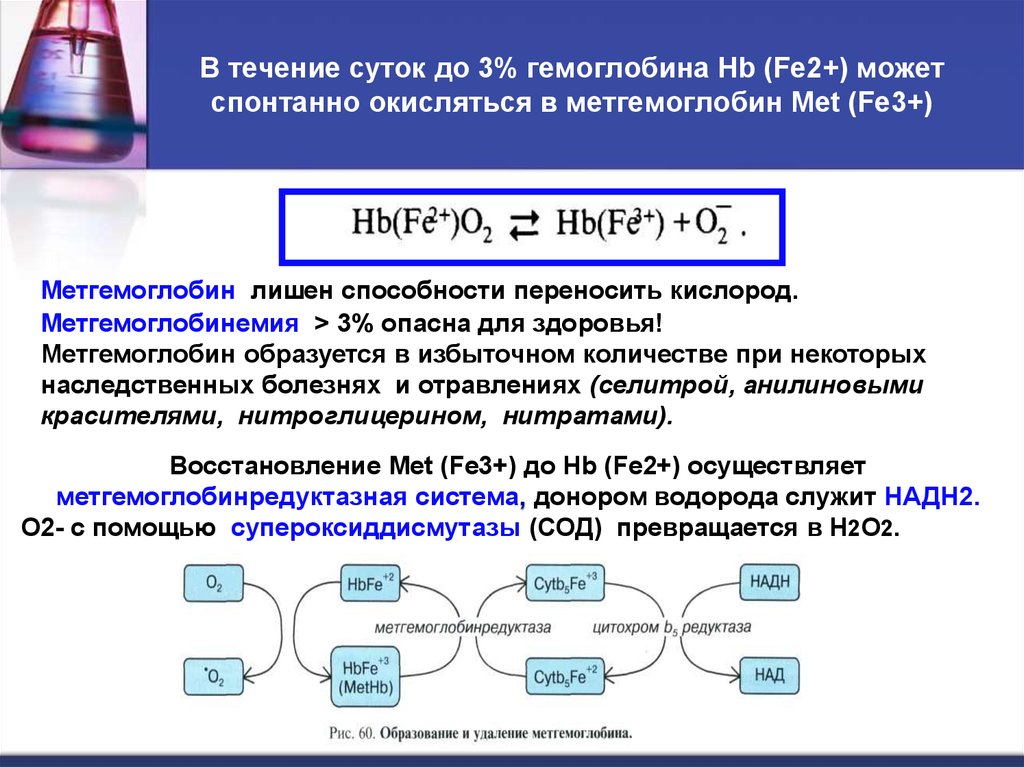 Однако даже при тяжелой гипоксии и желтухе новорожденных подъем MtHb не столь выражен и клинически значим, чтобы послужить причиной метгемоглобинемии. Однако при диарее, бактериальных и вирусных энтероколитах, в условиях метаболического ацидоза у детей первого года жизни может легко развиться приобретенная эндогенная метгемоглобинемия.
Однако даже при тяжелой гипоксии и желтухе новорожденных подъем MtHb не столь выражен и клинически значим, чтобы послужить причиной метгемоглобинемии. Однако при диарее, бактериальных и вирусных энтероколитах, в условиях метаболического ацидоза у детей первого года жизни может легко развиться приобретенная эндогенная метгемоглобинемия.
О смешанной форме патологии говорят в том случае, если метгемоглобинемия развивается под воздействием экзогенных факторов у здоровых лиц, являющихся гетерозиготными носителями генов наследственной формы заболевания.
Симптомы метгемоглобинемии
Признаки наследственной метгемоглобинемии становятся заметны в период новорожденности. На коже и видимых слизистых ребенка (в области губ, носогубного треугольника, мочек ушей, ногтевого ложа) заметен цианоз. Кроме наследственной метгемоглобинемии, у детей часто выявляются другие врожденные аномалии — изменения конфигурации черепа, недоразвитие верхних конечностей, атрезия влагалища, талассемия и пр. Нередко дети отстают в психомоторном развитии.
Нередко дети отстают в психомоторном развитии.
В зависимости от уровня фракции MtHb, выраженность проявлений врожденной и приобретенной метгемоглобинемии может значительно варьировать.
При концентрации MtHb в крови:
- <3% клинические проявления отсутствуют
- 3-15% — кожные покровы приобретают сероватый оттенок
- 15-30% — развивается цианоз, кровь становится шоколадно-коричневого цвета
- 30-50% — появляется слабость, головная боль, тахикардия, одышка при физической нагрузке, головокружение, возникают обмороки
- 50-70% — возникает аритмия, учащенное дыхание, судороги; развивается метаболический ацидоз; отмечаются признаки угнетения ЦНС, возможна кома
- >70% — выраженная гипоксия, летальный исход.
Для любых форм метгемоглобинемии характерна грифельно-серая окраска кожных покровов, однако отсутствуют характерные для сердечно-легочных заболеваний изменения ногтевых фаланг по типу «барабанных палочек». Акроцианоз усиливается при охлаждении, употреблении в пищу нитратосодержащих продуктов, при токсикозах беременности у женщин, а также приеме метгемоглобинобразующих медикаментов.
Акроцианоз усиливается при охлаждении, употреблении в пищу нитратосодержащих продуктов, при токсикозах беременности у женщин, а также приеме метгемоглобинобразующих медикаментов.
Сероватый цвет кожных покровов при метгемоглобинемии
Диагностика метгемоглобинемии
Важным диагностическим признаком метгемоглобинемии служит темно-коричный цвет крови, которая, будучи помещенной в пробирку или на фильтровальную бумагу, не изменяет свой цвет на красный. При положительной пробе проводится спектроскопия, определение концентрации MtHb, активности НАД-зависимой метгемоглобинредуктазы, электрофорез гемоглобина.
В общем анализе крови может присутствовать компенсаторный эритроцитоз, увеличение Hb, ретикулоцитоз, уменьшение СОЭ. При исследовании биохимических показателей крови определяется незначительная билирубинемия, обусловленная увеличением непрямой фракции пигмента. Для хронической метгемоглобинемии типично появление в эритроцитах телец Гейнца-Эрлиха.
У больных с энзимопенической или токсической метгемоглобинемией показательна терапевтическая проба с внутривенным введением метиленового синего – после инъекции цианоз быстро исчезает, а кожа и видимые слизистые приобретают розовую окраску.
При анализе причин метгемоглобинемии важно выяснить, имел ли больной контакт с токсическими веществами, принимал ли метгемоглобинобразующие лекарственные препараты. При подозрении на врожденную метгемоглобинемию изучается родословная, проводится консультация генетика, определяется тип наследования патологии крови. Наследственные метгемоглобинемии требуют дифференциации с врожденными пороками сердца синего типа, аномалиями развития легких и другими состояниями, сопровождающимися гипоксией.
Шоколадно-коричневый цвет крови в пробирках 1 и 2 при метгемоглобинемии
Лечение и профилактика метгемоглобинемии
Больные с отсутствием клинических проявлений не нуждаются в специальной терапии. При значительной концентрации MtHb в крови и развернутой симптоматике метгемоглобинемии назначается медикаментозная терапия, способствующая превращению метгемоглобина в гемоглобин. Такими восстанавливающими свойствами обладают аскорбиновая кислота и метиленовый синий. Аскорбиновая кислота назначается внутрь сначала в больших, а по мере нормализации состояния — в поддерживающих дозах. Раствор метиленовой сини вводится внутривенно. При выраженном цианозе проводится кислородная терапия. Тяжелая форма метгемоглобинемии является показанием к обменному переливанию крови.
При значительной концентрации MtHb в крови и развернутой симптоматике метгемоглобинемии назначается медикаментозная терапия, способствующая превращению метгемоглобина в гемоглобин. Такими восстанавливающими свойствами обладают аскорбиновая кислота и метиленовый синий. Аскорбиновая кислота назначается внутрь сначала в больших, а по мере нормализации состояния — в поддерживающих дозах. Раствор метиленовой сини вводится внутривенно. При выраженном цианозе проводится кислородная терапия. Тяжелая форма метгемоглобинемии является показанием к обменному переливанию крови.
Течение наследственной и лекарственной метгемоглобинемии, как правило, доброкачественное. Неблагоприятный исход возможен при тяжелых формах токсической метгемоглобинемии с высоким содержанием MtHb в эритроцитах. Пациентам с подобной патологией следует избегать контакта с метгемоглобинобразующими веществами, переохлаждений и других провоцирующих факторов. Профилактика врожденной метгемоглобинемии заключается в проведении медико-генетической консультации для выявления гетерозиготных носителей среди будущих родителей.
причины, симптомы, диагностика и лечение
Метгемоглобинемия – состояние, характеризующееся повышенным содержанием метгемоглобина (окисленного гемоглобина) в крови и тканевой гипоксией. Развитие метгемоглобинемии сопровождается акроцианозом, слабостью, головными болями, головокружением, сердцебиением, одышкой при нагрузке. Характерным признаком метгемоглобинемии служит коричнево-шоколадный цвет крови. Для подтверждения диагноза проводится оценка симптоматики, лабораторные исследования и тесты. При тяжелой степени метгемоглобинемии показана кислородотерапия, введение аскорбиновой кислоты, раствора метиленового синего, в ряде случаев — обменная гемотрансфузия.
Общие сведения
Метгемоглобинемия – увеличение уровня гемоглобина, содержащего окисленное железо (метгемоглобин – MtHb), в эритроцитах крови. Метгемоглобин относится к так называемым дисгемоглобинам — дериватам гемоглобина, не способным транспортировать кислород. В обычных условиях в крови присутствует небольшое количество метгемоглобина — не более 1% от общего содержания Hb. При метгемоглобинемии эндогенные механизмы оказываются не способными регулировать концентрацию дисгемоглобина, в результате чего страдает кислородно-транспортная функция эритроцитов. В гематологии метгемоглобинемии подразделяются на наследственные и приобретенные. Первые из них распространены среди коренного населения Аляски, Гренландии, Якутии; частота развития приобретенных метгемоглобинемий неизвестна.
При метгемоглобинемии эндогенные механизмы оказываются не способными регулировать концентрацию дисгемоглобина, в результате чего страдает кислородно-транспортная функция эритроцитов. В гематологии метгемоглобинемии подразделяются на наследственные и приобретенные. Первые из них распространены среди коренного населения Аляски, Гренландии, Якутии; частота развития приобретенных метгемоглобинемий неизвестна.
Метгемоглобинемия
Причины метгемоглобинемии
В процессе метаболических превращений в крови здоровых людей в очень небольших количествах образуются дисгемоглобины: карбоксигемоглобин, сульфгемоглобин, метгемоглобин (0,1-1 %). Вместе с тем, в эритроцитах содержится ряд факторов, которые поддерживают долю фракции метгемоглобина на уровне, не превышающем 1,0-1,5% от общего Hb. В частности, в реакции восстановления метгемоглобина в гемоглобин участвует фермент метгемоглобин-редуктаза. В отличие от оксигемоглобина (НbО2), содержащего восстановленное железо (Fe++), в метгемоглобине содержится окисленное железо (Fe+++), не способное переносить кислород.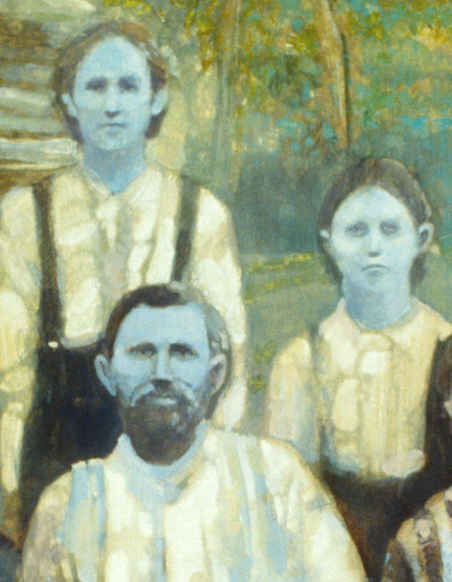 Поэтому при метгемоглобинемии, прежде всего, страдает кислородно-транспортная функция крови, следствием которой служит тканевая гипоксия.
Поэтому при метгемоглобинемии, прежде всего, страдает кислородно-транспортная функция крови, следствием которой служит тканевая гипоксия.
Наследственные формы метгемоглобинемии представлены либо ферментопатиями (врожденной низкой активностью или отсутствием фермента метгемоглобин-редуктазы), либо М-гемоглобинопатиями (синтезом аномальных белков, содержащих окисленное железо).
В структуре приобретенных (вторичных) метгемоглобинемий выделяют токсические экзогенные и токсические эндогенные формы. Метгемоглобинемии экзогенного происхождения могут быть связаны с передозировкой лекарственных средств (сульфаниламидов, нитритов, викасола, противомалярийных препаратов, лидокаина, новокаина и др.) или отравлением химическими агентами (анилиновыми красителями, нитратом серебра, тринитротолуолом, хлорбензолом, питьевой водой и пищевыми продуктами с высоким содержанием нитратов и др.).
Повышенный уровень MtHb в крови наблюдается у недоношенных и доношенных новорожденных, что связано с низкой активностью фермента метгемоглобин-редуктазы и окислительным стрессом в родах. Однако даже при тяжелой гипоксии и желтухе новорожденных подъем MtHb не столь выражен и клинически значим, чтобы послужить причиной метгемоглобинемии. Однако при диарее, бактериальных и вирусных энтероколитах, в условиях метаболического ацидоза у детей первого года жизни может легко развиться приобретенная эндогенная метгемоглобинемия.
Однако даже при тяжелой гипоксии и желтухе новорожденных подъем MtHb не столь выражен и клинически значим, чтобы послужить причиной метгемоглобинемии. Однако при диарее, бактериальных и вирусных энтероколитах, в условиях метаболического ацидоза у детей первого года жизни может легко развиться приобретенная эндогенная метгемоглобинемия.
О смешанной форме патологии говорят в том случае, если метгемоглобинемия развивается под воздействием экзогенных факторов у здоровых лиц, являющихся гетерозиготными носителями генов наследственной формы заболевания.
Симптомы метгемоглобинемии
Признаки наследственной метгемоглобинемии становятся заметны в период новорожденности. На коже и видимых слизистых ребенка (в области губ, носогубного треугольника, мочек ушей, ногтевого ложа) заметен цианоз. Кроме наследственной метгемоглобинемии, у детей часто выявляются другие врожденные аномалии — изменения конфигурации черепа, недоразвитие верхних конечностей, атрезия влагалища, талассемия и пр. Нередко дети отстают в психомоторном развитии.
Нередко дети отстают в психомоторном развитии.
В зависимости от уровня фракции MtHb, выраженность проявлений врожденной и приобретенной метгемоглобинемии может значительно варьировать.
При концентрации MtHb в крови:
- <3% клинические проявления отсутствуют
- 3-15% — кожные покровы приобретают сероватый оттенок
- 15-30% — развивается цианоз, кровь становится шоколадно-коричневого цвета
- 30-50% — появляется слабость, головная боль, тахикардия, одышка при физической нагрузке, головокружение, возникают обмороки
- 50-70% — возникает аритмия, учащенное дыхание, судороги; развивается метаболический ацидоз; отмечаются признаки угнетения ЦНС, возможна кома
- >70% — выраженная гипоксия, летальный исход.
Для любых форм метгемоглобинемии характерна грифельно-серая окраска кожных покровов, однако отсутствуют характерные для сердечно-легочных заболеваний изменения ногтевых фаланг по типу «барабанных палочек».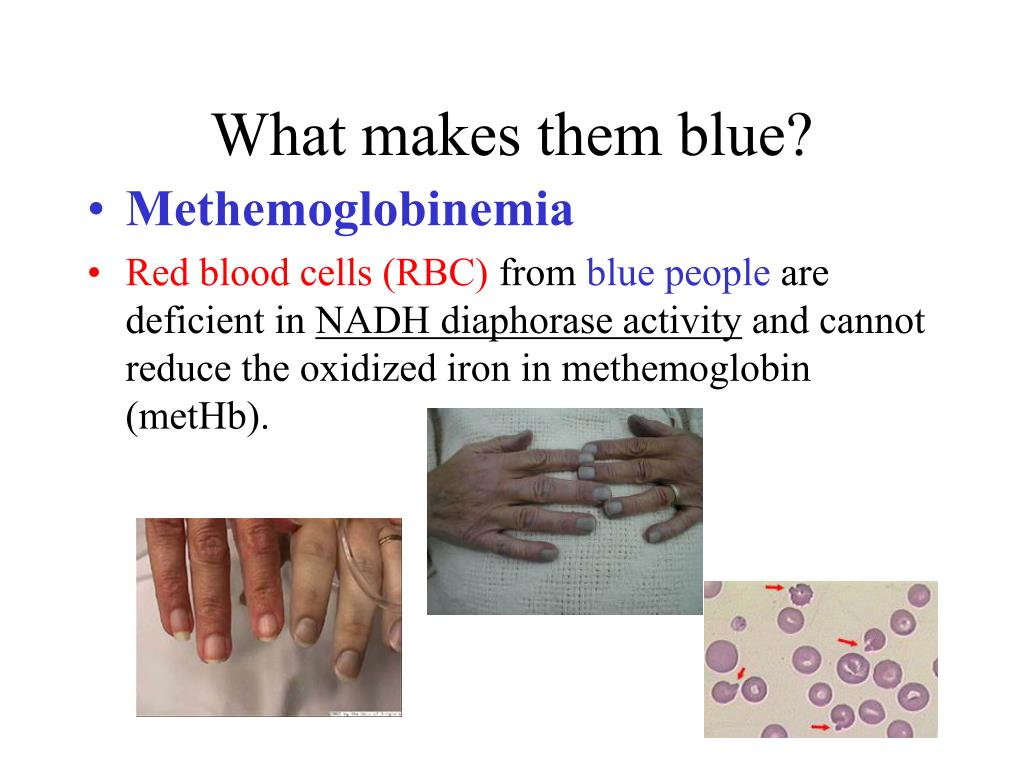 Акроцианоз усиливается при охлаждении, употреблении в пищу нитратосодержащих продуктов, при токсикозах беременности у женщин, а также приеме метгемоглобинобразующих медикаментов.
Акроцианоз усиливается при охлаждении, употреблении в пищу нитратосодержащих продуктов, при токсикозах беременности у женщин, а также приеме метгемоглобинобразующих медикаментов.
Сероватый цвет кожных покровов при метгемоглобинемии
Диагностика метгемоглобинемии
Важным диагностическим признаком метгемоглобинемии служит темно-коричный цвет крови, которая, будучи помещенной в пробирку или на фильтровальную бумагу, не изменяет свой цвет на красный. При положительной пробе проводится спектроскопия, определение концентрации MtHb, активности НАД-зависимой метгемоглобинредуктазы, электрофорез гемоглобина.
В общем анализе крови может присутствовать компенсаторный эритроцитоз, увеличение Hb, ретикулоцитоз, уменьшение СОЭ. При исследовании биохимических показателей крови определяется незначительная билирубинемия, обусловленная увеличением непрямой фракции пигмента. Для хронической метгемоглобинемии типично появление в эритроцитах телец Гейнца-Эрлиха.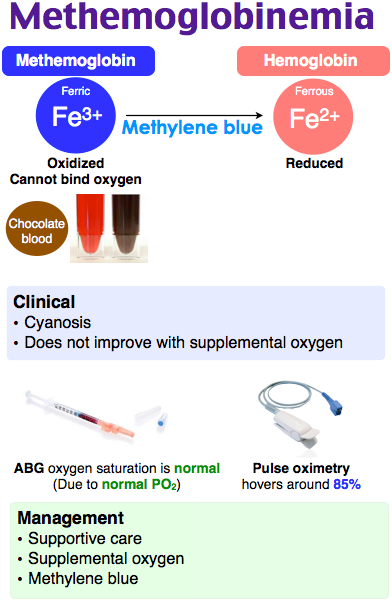
У больных с энзимопенической или токсической метгемоглобинемией показательна терапевтическая проба с внутривенным введением метиленового синего – после инъекции цианоз быстро исчезает, а кожа и видимые слизистые приобретают розовую окраску.
При анализе причин метгемоглобинемии важно выяснить, имел ли больной контакт с токсическими веществами, принимал ли метгемоглобинобразующие лекарственные препараты. При подозрении на врожденную метгемоглобинемию изучается родословная, проводится консультация генетика, определяется тип наследования патологии крови. Наследственные метгемоглобинемии требуют дифференциации с врожденными пороками сердца синего типа, аномалиями развития легких и другими состояниями, сопровождающимися гипоксией.
Шоколадно-коричневый цвет крови в пробирках 1 и 2 при метгемоглобинемии
Лечение и профилактика метгемоглобинемии
Больные с отсутствием клинических проявлений не нуждаются в специальной терапии. При значительной концентрации MtHb в крови и развернутой симптоматике метгемоглобинемии назначается медикаментозная терапия, способствующая превращению метгемоглобина в гемоглобин. Такими восстанавливающими свойствами обладают аскорбиновая кислота и метиленовый синий. Аскорбиновая кислота назначается внутрь сначала в больших, а по мере нормализации состояния — в поддерживающих дозах. Раствор метиленовой сини вводится внутривенно. При выраженном цианозе проводится кислородная терапия. Тяжелая форма метгемоглобинемии является показанием к обменному переливанию крови.
При значительной концентрации MtHb в крови и развернутой симптоматике метгемоглобинемии назначается медикаментозная терапия, способствующая превращению метгемоглобина в гемоглобин. Такими восстанавливающими свойствами обладают аскорбиновая кислота и метиленовый синий. Аскорбиновая кислота назначается внутрь сначала в больших, а по мере нормализации состояния — в поддерживающих дозах. Раствор метиленовой сини вводится внутривенно. При выраженном цианозе проводится кислородная терапия. Тяжелая форма метгемоглобинемии является показанием к обменному переливанию крови.
Течение наследственной и лекарственной метгемоглобинемии, как правило, доброкачественное. Неблагоприятный исход возможен при тяжелых формах токсической метгемоглобинемии с высоким содержанием MtHb в эритроцитах. Пациентам с подобной патологией следует избегать контакта с метгемоглобинобразующими веществами, переохлаждений и других провоцирующих факторов. Профилактика врожденной метгемоглобинемии заключается в проведении медико-генетической консультации для выявления гетерозиготных носителей среди будущих родителей.
Метгемоглобинемия — StatPearls — NCBI Bookshelf
Continuing Education Activity
Метгемоглобинемия — это состояние с опасным для жизни состоянием, при котором происходит снижение способности циркулирующего гемоглобина переносить кислород из-за превращения некоторых или всех четырех форм железа из состояние восстановленного железа (Fe2+) в состояние окисленного железа (Fe3+). Трехвалентное железо не способно связывать и транспортировать кислород. Повышение уровня метгемоглобина приводит к функциональной анемии. В этом упражнении рассматривается причина, патофизиология и проявление метгемоглобинемии, а также подчеркивается роль межпрофессиональной команды в ее лечении.
Цели:
Рассмотрите причины метгемоглобинемии.
Опишите внешний вид
метгемоглобинемия.Объясните управление
метгемоглобинемия.Объясните важность улучшения координации помощи между членами межпрофессиональной бригады для улучшения результатов лечения пациентов с метгемоглобинемией.

Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Метгемоглобинемия представляет собой потенциально опасное для жизни состояние, при котором происходит снижение способности циркулирующего гемоглобина переносить кислород из-за превращения некоторых или всех четырех соединений железа из восстановленного двухвалентного [Fe2+] состояния в окисленное трехвалентное [Fe3+] состояние. Трехвалентное железо не способно связывать и транспортировать кислород. Повышение уровня метгемоглобина приводит к функциональной анемии.
Этиология
Метгемоглобинемия может быть результатом врожденных или приобретенных процессов. Врожденные формы метгемоглобинемии возникают из-за аутосомно-рецессивных дефектов фермента цитохром b5 редуктазы (CYB5R) или из-за аутосомно-доминантных мутаций в генах, которые кодируют белки глобина, известные под общим названием гемоглобины M. [1] Описано множество вариантов гемоглобина М (Бостон, Форт-Рипли, Гайд-Парк, Ивате, Канкаки, Осака, Саскатун) [2].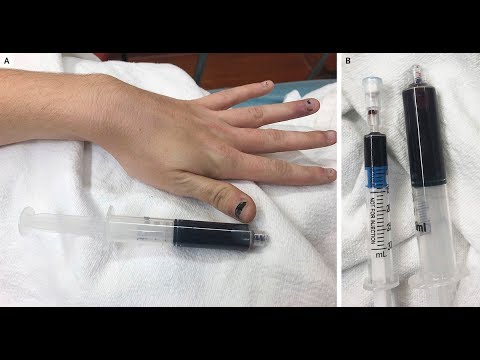 Врожденная метгемоглобинемия I типа представляет собой состояние, при котором дефект CYB5R выражен только на эритроцитах. Врожденная метгемоглобинемия типа II возникает, когда все клетки экспрессируют дефект.[3] Болезнь гемоглобина М представляет собой совокупность возможных мутаций, которые обычно возникают в альфа- или бета-цепях гемоглобина рядом с железом гема. Мутация приводит к более легкому окислению железа до трехвалентного состояния [Fe3+].[5] Приобретенная метгемоглобинемия, встречающаяся значительно чаще, возникает в результате воздействия веществ, прямо или косвенно вызывающих окисление гемоглобина. Это воздействие приводит к выработке метгемоглобина , который превышает способность организма преобразовывать железо в гемоглобине обратно в его двухвалентное состояние. Приобретенная метгемоглобинемия может быть связана с воздействием окислителей прямого действия (например, бензокаина и прилокаина), непрямого окисления (например, нитратов) или метаболической активации (например, анилина и дапсона) [6].
Врожденная метгемоглобинемия I типа представляет собой состояние, при котором дефект CYB5R выражен только на эритроцитах. Врожденная метгемоглобинемия типа II возникает, когда все клетки экспрессируют дефект.[3] Болезнь гемоглобина М представляет собой совокупность возможных мутаций, которые обычно возникают в альфа- или бета-цепях гемоглобина рядом с железом гема. Мутация приводит к более легкому окислению железа до трехвалентного состояния [Fe3+].[5] Приобретенная метгемоглобинемия, встречающаяся значительно чаще, возникает в результате воздействия веществ, прямо или косвенно вызывающих окисление гемоглобина. Это воздействие приводит к выработке метгемоглобина , который превышает способность организма преобразовывать железо в гемоглобине обратно в его двухвалентное состояние. Приобретенная метгемоглобинемия может быть связана с воздействием окислителей прямого действия (например, бензокаина и прилокаина), непрямого окисления (например, нитратов) или метаболической активации (например, анилина и дапсона) [6]. Классические примеры включают воздействие бензокаина на пациентов в кабинете эндоскопии и воздействие нитритов из колодезной воды на детей.
Классические примеры включают воздействие бензокаина на пациентов в кабинете эндоскопии и воздействие нитритов из колодезной воды на детей.
Эпидемиология
Врожденная метгемоглобинемия из-за дефицита цитохром b5 редуктазы встречается очень редко, но фактическая заболеваемость неизвестна. Повышенная частота заболевания обнаружена у сибирских якутов, атабасков, эскимосов и навахо.[7] Приобретенная метгемоглобинемия встречается значительно чаще, чем врожденная форма; хотя это тоже редкое явление. В большинстве случаев это происходит из-за непреднамеренного воздействия химического вещества или использования местных или местных анестетиков. Одноцентровый обзор почти 30 000 чреспищеводных эхокардиограмм показал, что частота метгемоглобинемии составляет 0,067% [8]. Систематический обзор случаев метгемоглобинемии, связанной с местными анестетиками, показал, что бензокаин был агентом в двух третях случаев.] Эта более высокая связь с продуктами, содержащими бензокаин, привела к тому, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США выпустило несколько рекомендаций относительно использования пероральных продуктов, содержащих бензокаин.
Патофизиология
Метгемоглобин формируется, когда гемоглобин окисляется, чтобы содержать железо в трехвалентном [Fe3+], а не в нормальном двухвалентном [Fe2+]. Любой из четырех видов железа в молекуле гемоглобина, которые находятся в трехвалентной форме, не способен связывать кислород. Присутствие железа в трехвалентном состоянии [Fe3+] приводит к аллостерическим изменениям в молекуле, что сдвигает кривую диссоциации кислорода влево. Этот сдвиг приводит к увеличению сродства двухвалентного железа к кислороду и, таким образом, к нарушению выделения кислорода в ткани.[11] Конечным результатом этих изменений является снижение доставки кислорода, что приводит к гипоксии тканей.
При болезни гемоглобина М мутация в гене, кодирующем один из белков глобина, обычно приводит к замене аминокислоты на тирозин. Эта мутация позволяет стабилизировать железо в трехвалентном состоянии [Fe3+]. Пациенты с болезнью гемоглобина М обычно имеют уровень метгемоглобина между 15-30% и остаются бессимптомными [1].
В нормальных условиях небольшое количество железа окисляется до трехвалентного состояния [Fe3+] во время обычной доставки кислорода к тканям. Поддержание уровня метгемоглобина обычно ниже 1% благодаря действию фермента цитохром-b5 редуктазы. Цитохром-b5 редуктаза использует НАДН, образующийся во время гликолиза, для восстановления метгемоглобина до функционального гемоглобина.[12]
Альтернативный путь снижения уровня метгемоглобина – это действие никотинамидадениндинуклеотидфосфатгидрометгемоглобинредуктазы (NADPH-MetHb). НАДФН-MetHb редуктаза использует НАДФН, который образуется под действием глюкозо-6-фосфатдегидрогеназы (Г6ФД) в гексозомонофосфатном шунте, из-за его восстановительной способности.[1] В нормальных физиологических условиях NADPH-MetHb редуктаза очень мало способствует восстановлению метгемоглобина, но при окислительном стрессе функция этого альтернативного пути восстановления может быть усилена присутствием экзогенных доноров электронов, таких как метиленовый синий. Эта связь с G6PD часто приводит к путанице в том, что дефицит G6PD сам по себе является фактором риска метгемоглобинемии.
Эта связь с G6PD часто приводит к путанице в том, что дефицит G6PD сам по себе является фактором риска метгемоглобинемии.
Токсикокинетика
Метгемоглобинемия, вторичная по отношению к токсическим воздействиям, возникает, когда способность цитохром-b5 редуктазы восстанавливать трехвалентный гемоглобин или метгемоглобин подавляется индуцированным окислительным стрессом. В результате повышается концентрация метгемоглобина, что приводит к метгемоглобинемии.
Анамнез и физикальное исследование
Метгемоглобинемию следует рассматривать при наличии одышки или цианоза и гипоксемии, которые устойчивы к дополнительному кислороду, особенно при воздействии известного окислительного агента. Однако проявления могут варьироваться по степени тяжести от минимально симптоматических до тяжелых. Клиническая картина метгемоглобинемии основана на заболевании спектра, которое связано с цианозом, бледностью, утомляемостью, слабостью, головной болью, угнетением центральной нервной системы, метаболическим ацидозом, судорогами, аритмиями, комой и смертью. Степень тяжести симптомов является многофакторной и зависит от процентного содержания метгемоглобина у пациента, скорости накопления метгемоглобина, способности человека естественным образом очищать его и основного состояния здоровья пациента. Продолжительность и степень воздействия окислителя также могут играть роль.
Степень тяжести симптомов является многофакторной и зависит от процентного содержания метгемоглобина у пациента, скорости накопления метгемоглобина, способности человека естественным образом очищать его и основного состояния здоровья пациента. Продолжительность и степень воздействия окислителя также могут играть роль.
Метгемоглобин выражается в виде концентрации или процента, и это далее описывается при оценке. Процент метгемоглобина рассчитывается путем деления концентрации метгемоглобина на концентрацию общего гемоглобина. Процент метгемоглобина, вероятно, является лучшим показателем тяжести заболевания, чем общая концентрация, поскольку важную роль играют основные заболевания. Например, концентрация метгемоглобина 1,5 г/дл может составлять 10 % у здорового в других отношениях пациента с исходным уровнем гемоглобина 15 мг/дл, в то время как наличие такой же концентрации метгемоглобина в 1,5 г/дл у больного анемией пациент с исходным уровнем гемоглобина 8 г/дл будет представлять процент 18,75%. Первый пациент останется с концентрацией функционального гемоглобина 13,5 г/дл и потенциально останется бессимптомным, в то время как второй пациент с концентрацией функционального гемоглобина 6,5 г/дл может иметь серьезные симптомы с метгемоглобином менее 20%. Это может быть дополнительно усугублено снижением способности «функционального гемоглобина» высвобождать кислород в присутствии метгемоглобина. Анемия, застойная сердечная недостаточность, хроническая обструктивная болезнь легких и практически любая патология , которая ухудшает способность доставки кислорода, могут ухудшить симптомы метгемоглобинемии.
Первый пациент останется с концентрацией функционального гемоглобина 13,5 г/дл и потенциально останется бессимптомным, в то время как второй пациент с концентрацией функционального гемоглобина 6,5 г/дл может иметь серьезные симптомы с метгемоглобином менее 20%. Это может быть дополнительно усугублено снижением способности «функционального гемоглобина» высвобождать кислород в присутствии метгемоглобина. Анемия, застойная сердечная недостаточность, хроническая обструктивная болезнь легких и практически любая патология , которая ухудшает способность доставки кислорода, могут ухудшить симптомы метгемоглобинемии.
У здорового в остальном человека цианоз может быть клинически очевиден при содержании метгемоглобина всего 10%.[11] Классический вид «шоколадно-коричневой крови» может присутствовать всего в 15%. Когда процент метгемоглобинемии приближается к 20 %, пациент может испытывать тревогу, головокружение и головные боли. При уровне метгемоглобина 30-50% могут быть тахипноэ, спутанность сознания и потеря сознания. При приближении 50 % у пациента возникает риск судорог, аритмии, метаболического ацидоза и комы. Уровни выше 70 % часто смертельны.[13]
При приближении 50 % у пациента возникает риск судорог, аритмии, метаболического ацидоза и комы. Уровни выше 70 % часто смертельны.[13]
См. Таблицу 1: Симптомы, основанные на уровне метгемоглобина
Оценка
Метгемоглобинемия — это клинический диагноз, основанный на анамнезе и проявляющихся симптомах, включая гипоксемию, устойчивую к дополнительному кислороду, и вероятное наличие крови шоколадного цвета. Диагноз подтверждается газовым составом артериальной или венозной крови с кооксиметрией, которая определяет гемоглобин для определения концентрации и процентного содержания метгемоглобина.[10] Измерения SpO2 нельзя использовать для прямого расчета тяжести метгемоглобинемии.
«Рефрактерная гипоксемия» является важным диагностическим признаком. Как правило, это очевидно при пульсовой оксиметрии при измерении насыщения кислородом (SpO2) на основе определения длины волны, но не при расчете на основе анализа газов крови с использованием парциального давления кислорода в крови (SaO2). Традиционная двухволновая пульсоксиметрия неточна при метгемоглобинемии, поскольку эти пульсоксиметры измеряют поглощение света на двух длинах волн — 660 и 940 нм. Отношение этого поглощения позволяет различать оксигемоглобин и дезоксигемоглобин с выраженным процентным содержанием или SpO2, указывающим измеренное количество гемоглобина, насыщенного кислородом. Метгемоглобин имеет высокое поглощение на обеих этих длинах волн, что приводит к интерференции, которая приводит к неточным показаниям SpO2. Когда уровень метгемоглобина приближается к 30-35%, коэффициент поглощения становится равным 1,0. Соотношение абсорбции (A660/A940) 1,0 читается как SpO2 85%.[14] Существует непропорциональная обратная зависимость между концентрацией метгемоглобина и SpO2, и, несмотря на то, что SpO2 постоянно снижается, обычно это ложно повышенный показатель истинного насыщения кислородом, который варьируется в зависимости от конкретного устройства.
Традиционная двухволновая пульсоксиметрия неточна при метгемоглобинемии, поскольку эти пульсоксиметры измеряют поглощение света на двух длинах волн — 660 и 940 нм. Отношение этого поглощения позволяет различать оксигемоглобин и дезоксигемоглобин с выраженным процентным содержанием или SpO2, указывающим измеренное количество гемоглобина, насыщенного кислородом. Метгемоглобин имеет высокое поглощение на обеих этих длинах волн, что приводит к интерференции, которая приводит к неточным показаниям SpO2. Когда уровень метгемоглобина приближается к 30-35%, коэффициент поглощения становится равным 1,0. Соотношение абсорбции (A660/A940) 1,0 читается как SpO2 85%.[14] Существует непропорциональная обратная зависимость между концентрацией метгемоглобина и SpO2, и, несмотря на то, что SpO2 постоянно снижается, обычно это ложно повышенный показатель истинного насыщения кислородом, который варьируется в зависимости от конкретного устройства.
В то время как измерения SpO2 неточны и занижены из-за интерференции длин волн, часто до 75-90% даже с дополнительным кислородом, расчеты SaO2 ложно нормальны из-за предположения, что весь гемоглобин представляет собой либо оксигемоглобин, либо дезоксигемоглобин. [10] Разница между пониженным измерением SpO2 и ложно нормальным расчетом SaO2 известна как «разрыв насыщения». Этот дополнительный диагностический признак должен указывать на наличие гемоглобинопатии, но он неспецифичен и не может быть использован для подтверждения диагноза метгемоглобинемии. Разрыв сатурации более 5% возникает в случаях повышенных аномальных форм гемоглобина, таких как карбоксигемоглобин, метгемоглобин и сульфгемоглобин.[15]
[10] Разница между пониженным измерением SpO2 и ложно нормальным расчетом SaO2 известна как «разрыв насыщения». Этот дополнительный диагностический признак должен указывать на наличие гемоглобинопатии, но он неспецифичен и не может быть использован для подтверждения диагноза метгемоглобинемии. Разрыв сатурации более 5% возникает в случаях повышенных аномальных форм гемоглобина, таких как карбоксигемоглобин, метгемоглобин и сульфгемоглобин.[15]
Лечение/управление
Лечение метгемоглобинемии включает удаление провоцирующего агента и рассмотрение вопроса о лечении антидотом, метиленовым синим (тетраметилтионин хлорид). Кислород с высокой скоростью, подаваемый маской без ребризера, увеличивает доставку кислорода к тканям и усиливает естественную деградацию метгемоглобина.
Метиленовый синий обычно действует быстро и эффективно благодаря его взаимодействию с вышеупомянутым вторичным путем восстановления метгемоглобина, где НАДФН-MetHb редуктаза восстанавливает метиленовый синий до лейкометиленового синего с использованием НАДФН из Г6ФД-зависимого гексозомонофосфатного шунта. Затем лейкометиленовый синий действует как донор электронов, восстанавливая метгемоглобин до гемоглобина. В случаях приобретенной метгемоглобинемии лечение метиленовым синим следует проводить, когда уровень метгемоглобина превышает 20-30% или при более низких уровнях, если у пациента есть симптомы. Решение о лечении следует принимать на основании клинических проявлений, а не откладывать до подтверждения лабораторными данными. Доза метиленового синего составляет 1-2 мг/кг (0,1-0,2 мл/кг 1% раствора) внутривенно в течение 5 минут.[12] Дозу можно повторить через 30-60 минут, если значительные симптомы или уровни остаются выше порога лечения.
Затем лейкометиленовый синий действует как донор электронов, восстанавливая метгемоглобин до гемоглобина. В случаях приобретенной метгемоглобинемии лечение метиленовым синим следует проводить, когда уровень метгемоглобина превышает 20-30% или при более низких уровнях, если у пациента есть симптомы. Решение о лечении следует принимать на основании клинических проявлений, а не откладывать до подтверждения лабораторными данными. Доза метиленового синего составляет 1-2 мг/кг (0,1-0,2 мл/кг 1% раствора) внутривенно в течение 5 минут.[12] Дозу можно повторить через 30-60 минут, если значительные симптомы или уровни остаются выше порога лечения.
Практикующие врачи должны знать о побочных эффектах метиленового синего. Доброкачественные побочные эффекты включают окрашивание мочи в зеленый или синий цвет, о чем следует предупредить пациентов. Значительные побочные эффекты основаны на метиленовом синем, который сам по себе является окислителем и ингибитором моноаминоксидазы А (МАО-А). В качестве окислителя метиленовый синий может вызвать метгемоглобинемию или гемолиз в высоких дозах или при неэффективном уменьшении.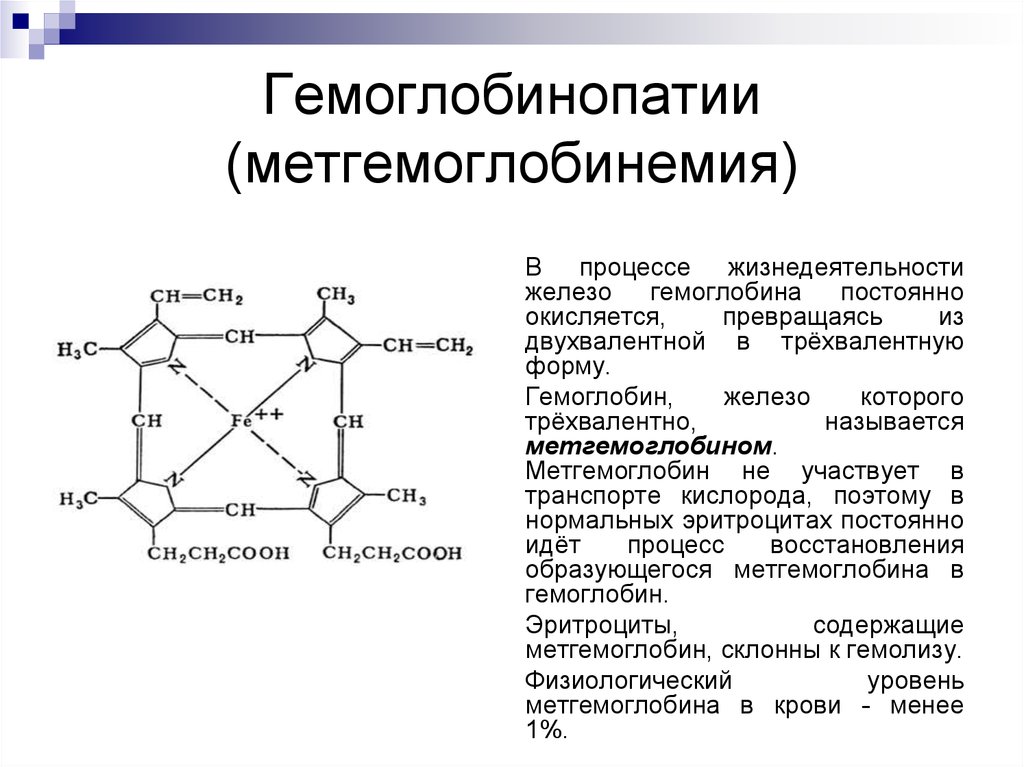 Введение метиленового синего пациенту, принимающему серотонинергические средства, может предрасполагать к развитию серотонинового синдрома.[16] Следует также соблюдать осторожность при лечении новорожденных, поскольку они также очень чувствительны к окислителям. Кроме того, метиленовый синий является препаратом категории X для беременных Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), что указывает на то, что исследования показали конкретные доказательства риска для человеческого плода.
Введение метиленового синего пациенту, принимающему серотонинергические средства, может предрасполагать к развитию серотонинового синдрома.[16] Следует также соблюдать осторожность при лечении новорожденных, поскольку они также очень чувствительны к окислителям. Кроме того, метиленовый синий является препаратом категории X для беременных Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), что указывает на то, что исследования показали конкретные доказательства риска для человеческого плода.
Хотя введение метиленового синего вызывает споры при дефиците G6PD из-за сниженного уровня NADPH, оно не противопоказано и должно вводиться осторожно и разумно. У многих пациентов с дефицитом G6PD может быть некоторый уровень G6PD, который все еще может вызвать адекватный ответ, и поэтому от лечения не следует отказываться. Дозы метиленового синего, вызывающие гемолиз у пациентов с дефицитом G6PD, превышают 5 мг/кг, что более чем в два раза превышает рекомендуемую дозу. [17]
[17]
Если введение метиленового синего неэффективно после второй дозы, в качестве причин невосприимчивости к лечению следует рассматривать основные состояния, включая, помимо прочего, дефицит G6PD и NADPH-MetHb редуктазы. Однако сама по себе метгемоглобинемия не является показанием для скрининга этих болезненных процессов.
Если лечение метиленовым синим неэффективно или не рекомендуется, дополнительные варианты могут включать аскорбиновую кислоту, обменное переливание крови, гипербарическую оксигенотерапию.[18][19]] Высокие дозы аскорбиновой кислоты (витамина С) до 10 г/дозу внутривенно можно рассматривать для лечения метгемоглобина. Однако, как правило, это неэффективно и не считается стандартом лечения. Введение высоких доз аскорбиновой кислоты связано с повышенной экскрецией оксалата с мочой. При наличии почечной недостаточности высокие дозы аскорбиновой кислоты могут предрасполагать к почечной недостаточности из-за гипероксалурии.[20]
Дифференциальная диагностика
Дифференциальная диагностика цианоза также включает: 9
Застойная сердечная недостаточность
Цианотический врожденный порок сердца оз
Полицитемия
Сульфгемоглобинемия
Дифференциальный диагноз синюшности Изменение цвета кожи также включает:
Энтеропатический акродерматит
Амиодарон-индуцированная пигментация кожи
Аргирия
Прогноз
Большинство пациентов с метгемоглобинемией хорошо реагируют на лечение и могут быть выписаны после короткого периода наблюдения. Любой человек с сохраняющимися симптомами после первоначального лечения или обострением основного заболевания должен быть рассмотрен для госпитализации.
Любой человек с сохраняющимися симптомами после первоначального лечения или обострением основного заболевания должен быть рассмотрен для госпитализации.
Консультации
Все случаи метгемоглобинемии следует лечить в консультации с врачом-токсикологом.
Жемчуг и другие предметы
Диагноз метгемоглобинемии клинический и подтверждается анализом газов артериальной крови с кооксиметрией не следует откладывать получение результатов кооксиметрии.
Метиленовый синий является ИМАО и при введении пациенту, принимающему любой другой серотонинергический препарат, может вызвать серотониновый синдром.
Метиленовый синий следует использовать с осторожностью и осторожностью у младенцев и пациентов с дефицитом G6PD, но он не противопоказан.
Улучшение результатов медицинской бригады
Все случаи следует лечить в консультации с медицинским токсикологом. Интенсивная терапия может быть необходима в тех случаях, когда оправдано длительное лечение или наблюдение, или если в результате повышенного уровня метгемоглобина были серьезные неблагоприятные исходы. В случае приобретенной метгемоглобинемии пациенты должны получить информацию о том, как воздействие возбудителя привело к развитию метгемоглобинемии. Пациент должен быть проинструктирован, чтобы избежать воздействия в будущем.
В случае приобретенной метгемоглобинемии пациенты должны получить информацию о том, как воздействие возбудителя привело к развитию метгемоглобинемии. Пациент должен быть проинструктирован, чтобы избежать воздействия в будущем.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Таблица 1: Симптомы в зависимости от уровня метгемоглобина. Предоставлено R. Gentry Wilkerson, MD
Ссылки
- 1.
Карри С. Метгемоглобинемия. Энн Эмерг Мед. 1982 апр; 11 (4): 214-21. [PubMed: 7073040]
- 2.
Хеймонд С., Кариаппа Р., Эби К.С., Скотт М.Г. Лабораторная оценка оксигенации при метгемоглобинемии. Клин Хим. 2005 г., февраль; 51(2):434-44. [В паблике: 15514101]
- 3.
Кедар П.С., Гупта В., Варанг П., Чиддарвар А., Мадкаикар М. Новая мутация (R192C) в гене CYB5R3, вызывающая дефицит NADH-цитохром b5 редуктазы у восьми индийских пациентов, связанный с аутосомно-рецессивным врожденным типом метгемоглобинемии- Я.
 Гематология. 2018 сен; 23 (8): 567-573. [PubMed: 29482478]
Гематология. 2018 сен; 23 (8): 567-573. [PubMed: 29482478]- 4.
Percy MJ, Lappin TR. Рецессивная врожденная метгемоглобинемия: дефицит цитохрома b(5) редуктазы. Бр Дж Гематол. 2008 май; 141 (3): 298-308. [PubMed: 18318771]
- 5.
Spears F, Banerjee A. Вариант гемоглобина M и врожденная метгемоглобинемия: метиленовый синий не будет эффективен в присутствии гемоглобина M. Can J Anaesth. 2008 г., июнь; 55 (6): 391-2. [PubMed: 18566207]
- 6.
Брэдберри С.М. Профессиональная метгемоглобинемия. Механизмы производства, особенности, диагностика и лечение, включая использование метиленового синего. Toxicol Rev. 2003;22(1):13-27. [В паблике: 14579544]
- 7.
Бурцева Т.Е., Аммосова Т.Н., Протопопова Н.Н., Яковлева С.Ю., Слободчикова М.П. Энзимопеническая врожденная метгемоглобинемия у детей Республики Саха (Якутия). J Pediatr Hematol Oncol. 2017 Январь; 39 (1): 42-45. [PubMed: 27879543]
- 8.

Кейн Г.К., Хён С.М., Беренбек Т.Р., Малва С.Л. Бензокаин-индуцированная метгемоглобинемия, основанная на опыте клиники Майо по 28 478 чреспищеводным эхокардиограммам: частота, исходы и предрасполагающие факторы. Arch Intern Med. 2007 Окт 08;167(18):1977-82. [PubMed: 17923598]
- 9.
Guay J. Метгемоглобинемия, связанная с местными анестетиками: краткое изложение 242 эпизодов. Анест Анальг. 2009 март; 108(3):837-45. [PubMed: 19224791]
- 10.
Nappe TM, Pacelli AM, Katz K. Атипичный случай метгемоглобинемии из-за самостоятельного введения бензокаина. Представитель Emerg Med. 2015;2015:670979. [Бесплатная статья PMC: PMC4383305] [PubMed: 25874137]
- 11.
Райт Р.О., Левандер В.Дж., Вульф А.Д. Метгемоглобинемия: этиология, фармакология и клиническое лечение. Энн Эмерг Мед. 1999 ноября; 34 (5): 646-56. [PubMed: 10533013]
- 12.
Скольд А., Коско Д.Л., Кляйн Р. Метгемоглобинемия: патогенез, диагностика и лечение.
 South Med J. 2011, ноябрь; 104 (11): 757-61. [PubMed: 22024786]
South Med J. 2011, ноябрь; 104 (11): 757-61. [PubMed: 22024786]- 13.
Вилкерсон Р.Г. Получение блюза на рок-концерте: случай тяжелой метгемоглобинемии. Emerg Med Australas. 2010 окт; 22 (5): 466-9. [PubMed: 21040486]
- 14.
Чан ЭД, Чан ММ, Чан ММ. Пульсоксиметрия: понимание ее основных принципов облегчает понимание ее ограничений. Респир Мед. 2013 июнь;107(6):789-99. [PubMed: 234
]
- 15.
Ахтар Дж., Джонстон Б.Д., Крензелок Э.П. Имейте в виду разрыв. J Emerg Med. 2007 авг; 33 (2): 131-2. [PubMed: 17692762]
- 16.
Рамзи Р.Р., Данфорд С., Гиллман П.К. Метиленовый синий и токсичность серотонина: ингибирование моноаминоксидазы А (МАО А) подтверждает теоретический прогноз. Бр Дж. Фармакол. 2007 ноябрь; 152 (6): 946-51. [Бесплатная статья PMC: PMC2078225] [PubMed: 17721552]
- 17.
KELLERMEYER RW, TARLOV AR, BREWER GJ, CARSON PE, ALVING AS. Гемолитическое действие лечебных препаратов.
 Клинические аспекты гемолиза примахинового типа. ДЖАМА. 1962 мая 05; 180:388-94. [PubMed: 14454972]
Клинические аспекты гемолиза примахинового типа. ДЖАМА. 1962 мая 05; 180:388-94. [PubMed: 14454972]- 18.
Грауман Неандер Н., Лонер К.А., Ротоли Дж.М. Неотложное лечение метгемоглобинемии у беременных. J Emerg Med. 2018 май; 54(5):685-689. [PubMed: 29627348]
- 19.
Чо И, Пак С.В., Хан С.К., Ким Х.Б., Ём С.Р. Случай метгемоглобинемии, успешно вылеченной монотерапией гипербарической оксигенацией. J Emerg Med. 2017 ноябрь;53(5):685-687. [PubMed: 28838565]
- 20.
Lee KW, Park SY. Высокие дозы витамина С для лечения метгемоглобинемии. Am J Emerg Med. 2014 авг; 32 (8): 936. [PubMed: 24972962]
Метгемоглобинемия: Медицинская энциклопедия MedlinePlus
Метгемоглобинемия (MetHb) — это заболевание крови, при котором вырабатывается аномальное количество метгемоглобина. Гемоглобин — это белок красных кровяных телец (эритроцитов), который переносит и распределяет кислород в организме. Метгемоглобин представляет собой форму гемоглобина.
При метгемоглобинемии гемоглобин может переносить кислород, но не способен эффективно отдавать его тканям организма.
Заболевание MetHb может быть:
- Передаваемым из поколения в поколение (наследственным или врожденным)
- Вызванным воздействием определенных лекарств, химических веществ или пищевых продуктов (приобретенным)
Существуют две формы наследственного MetHb. Первую форму передают оба родителя. Родители обычно сами не болеют этим заболеванием. Они несут ген, вызывающий заболевание. Это происходит, когда есть проблема с ферментом, называемым цитохром b5 редуктазой.
Существует два типа наследственного MetHb:
- Тип 1 (также называемый дефицитом редуктазы эритроцитов) возникает, когда в эритроцитах отсутствует фермент.
- Тип 2 (также называемый генерализованным дефицитом редуктазы) возникает, когда фермент не работает в организме.
Вторая форма наследственного MetHb называется болезнью гемоглобина М. Это вызвано дефектами в самом белке гемоглобина. Только один родитель должен передать аномальный ген, чтобы ребенок унаследовал болезнь.
Это вызвано дефектами в самом белке гемоглобина. Только один родитель должен передать аномальный ген, чтобы ребенок унаследовал болезнь.
Приобретенный MetHb встречается чаще, чем наследственные формы. Это происходит у некоторых людей после воздействия определенных химических веществ и лекарств, в том числе:
- Анестетики, такие как бензокаин
- Нитробензол
- Некоторые антибиотики (включая дапсон и хлорохин)
- Нитриты (используются в качестве добавок для предотвращения порчи мяса)
Симптомы MetHb типа 1 включают:
- Синеватая окраска кожи (так называемый цианоз)
Симптомы MetHb типа 2 включают:
- Отставание в развитии
- Неспособность процветать
- Интеллектуальная недееспособность
- Судороги
Симптомы болезни гемоглобина М включают:
- Голубоватый оттенок кожи
Симптомы приобретенного MetHb включают:
- Синеватая окраска кожи
- Головная боль
- Головокружение
- Измененное психическое состояние
- Усталость
- Одышка
- Недостаток энергии
У ребенка с этим заболеванием при рождении или вскоре после него будет синеватый цвет кожи (цианоз). Медицинский работник проведет анализы крови для диагностики состояния. Анализы могут включать:
Медицинский работник проведет анализы крови для диагностики состояния. Анализы могут включать:
- Проверка уровня кислорода в крови (пульсоксиметрия)
- Анализ крови для проверки уровня газов в крови (анализ газов артериальной крови)
Люди с болезнью гемоглобина М не имеют симптомов. Таким образом, они могут не нуждаться в лечении.
Лекарство под названием метиленовый синий используется для лечения тяжелого MetHb. Метиленовый синий может быть небезопасен для людей, которые имеют или могут быть подвержены риску заболевания крови, называемого дефицитом G6PD. Они не должны принимать это лекарство. Если у вас или у вашего ребенка дефицит G6PD, всегда сообщайте об этом своему врачу перед началом лечения.
Аскорбиновую кислоту также можно использовать для снижения уровня метгемоглобина.
Альтернативные методы лечения включают гипербарическую оксигенацию, переливание эритроцитарной массы и обменные переливания.
В большинстве случаев легкого приобретенного MetHb лечение не требуется. Но вам следует избегать лекарств или химических веществ, вызвавших проблему. В тяжелых случаях может потребоваться переливание крови.
Но вам следует избегать лекарств или химических веществ, вызвавших проблему. В тяжелых случаях может потребоваться переливание крови.
Люди с MetHb типа 1 и заболеванием гемоглобина M часто чувствуют себя хорошо. MetHb типа 2 более серьезен. Это часто приводит к смерти в течение первых нескольких лет жизни.
Люди с приобретенным MetHb часто чувствуют себя очень хорошо, когда выявляют и избегают лекарств, продуктов питания или химических веществ, вызвавших проблему.
Осложнения MetHb включают:
- Шок
- Судороги
- Смерть
Позвоните своему врачу, если вы: 4
Позвоните 911 или местному немедленно позвоните по номеру экстренной помощи, если у вас сильная одышка.
Генетическое консультирование рекомендуется парам с семейным анамнезом MetHb, которые рассматривают возможность завести детей.
Дети в возрасте 6 месяцев и младше более склонны к развитию метгемоглобинемии. Поэтому следует избегать домашних пюре для детского питания, приготовленных из овощей с высоким содержанием натуральных нитратов, таких как морковь, свекла или шпинат.
Болезнь гемоглобина М; дефицит редуктазы эритроцитов; Генерализованная недостаточность редуктазы; MetHb
- Клетки крови
Бенц Э.Дж., Эберт Б.Л. Варианты гемоглобина, связанные с гемолитической анемией, измененным сродством к кислороду и метгемоглобинемиями. В: Хоффман Р., Бенц Э.Дж., Зильберштейн Л.Е., ред. Гематология: основные принципы и практика . 7-е изд. Филадельфия, Пенсильвания: Elsevier; 2018: глава 43.
Letterio J, Pateva I, Petrosiute A, Ahuja S. Гематологические и онкологические проблемы у плода и новорожденного. В: Мартин Р.Дж., Фанарофф А.А., Уолш М.К., ред. Неонатальная и перинатальная медицина Фанарова и Мартина . 11-е изд. Филадельфия, Пенсильвания: Elsevier; 2020: глава 79.
Означает РТ. Подход к анемиям. В: Goldman L, Schafer AI, ред. Медицина Голдман-Сесил . 26-е изд. Филадельфия, Пенсильвания: Elsevier; 2020: глава 149.
Обновлено: Тоддом Герстеном, доктором медицины, гематология/онкология, Флоридский онкологический институт специалистов и исследований, Веллингтон, Флорида.