Чем отличается гистология от биопсии: Биопсия и гистологическое исследование — виды эндоскопии, цены в отделении клиники в Санкт-Петербурге
Биопсия или гистологическое исследование
Биопсия или гистологическое исследование — это анализ, позволяющий определить природу новообразования, то есть злокачественный или доброкачественный характер имеет опухоль. Суть биопсии заключается в удалении небольшого участка , либо всей опухоли для подробного лабораторного исследования. К сожалению, ни маммография, ни УЗИ не способны определить, злокачественно ли новообразование. Такие возможности доступны только биопсии. Чаще всего данная процедура не требует нахождения в стационаре; она может быть проведена в кабинете маммолога в день обращения. Для проведения биопсии может применяться анестезия, в том случае, если необходимо оперативное вмешательство.
С помощью биопсии можно обнаружить и доброкачественные образования, например, кисты или папилломы. Также она помогает обнаружить опухоли, которые называются жировым некрозом (омертвевшие жировые клетки молочной железы, что очень часто встречается после перенесенной травмы).
Чаще всего перед биопсией пациент проходит ряд исследований, направленных на то, чтобы выяснить объемы распространения опухоли. К таким исследованиям относятся маммография и УЗИ.С помощью данных методов специалист делает вывод о местонахождении опухоли, ее и ее глубине. Если опухоль расположена очень глубоко, биопсия проводится под контролем УЗИ или рентгена.
Аспирационная биопсия
Одним из неоперативных методов является аспирационная биопсия, которая предполагает взятие образца беспокоящего участка молочной железы с помощью иглы или шприца. Данный метод имеет ряд преимуществ. Например, пациент подвергается меньшему нервному воздействию, кроме того кожа не повреждается, поэтому на коже молочной железы не остается ни рубцов, ни шрамов. Это важно не только с эстетической, но и медицинской точки зрения. При последующих маммографических исследованиях рубец не будет мешать качественной расшифровке результатов. Кроме того такой вид биопсии предполагает минимальный риск осложнений. Однако, у неоперативных способов диагностики есть существенный минус – не всегда с их помощью можно поставить верный и окончательный диагноз. Именно поэтому, в большинстве случаев оперативное вмешательство необходимо.
Однако, у неоперативных способов диагностики есть существенный минус – не всегда с их помощью можно поставить верный и окончательный диагноз. Именно поэтому, в большинстве случаев оперативное вмешательство необходимо.
Виды биопсии:
- Тонкоигольная аспирационная биопсия — применяется для проведения биопсии тех опухолей молочной железы, которые доступны при пальпации. Процедура выполняется в положении сидя. Врач делает на кожном покрове обозначение, то есть отмечает то место, откуда будет взят образец.Оно обрабатывается специальным веществом, содержащим антисептик. Затем в железу вводится длинная тонкая игла. После того как шприц проникает внутрь ткани, врач несколько раз оттягивает поршень шприца, что позволяет забору небольшого количества ткани. Если необходимо забрать пункцию кисту, в шприц собирается содержащаяся в ней жидкость. Боль, наносимая пациенту кистой, утихает после того, как из нее откачивают всю жидкость.
- Стереотаксическая тонкоигольная биопсия — суть данного метода заключается в том, что из нескольких участков опухоли берется необходимое количество образцов.
 Бывают ситуации, когда новообразование невозможно обнаружить с помощью пальпации или оно расположено слишком глубоко. В таких случаях места для проведения биопсии врач находит с помощью маммографии или УЗИ, которые способны предоставить объемную картину.
Бывают ситуации, когда новообразование невозможно обнаружить с помощью пальпации или оно расположено слишком глубоко. В таких случаях места для проведения биопсии врач находит с помощью маммографии или УЗИ, которые способны предоставить объемную картину. - Толстоигольная биопсия — благодаря ей врач может получить более обширный участок молочной железы, так как проводится данный вид диагностики с помощью толстой иглы, имеющей режущее устройство.Главным преимуществом этой разновидности биопсии является тот факт, что взятому образцу можно поставить более точный размер, что становится возможным из-за его существенных размеров.
- Инцизионная биопсия — ее проведение требует иссечения небольшого участка новообразования, что делает ее похожей на оперативное вмешательство. Проводится она под местной анестезией, чаще всего в ситуациях, когда нельзя полностью полагаться на данные аспирационной биопсии. Несмотря на то, что оба исследования могут дать неверные результаты, у них есть неоспоримый плюс – быстрота.

- Эксцизионная биопсия — ее можно отнести к разряду небольших операций, во время которых врач иссекает либо всю опухоль, либо ее часть. Данное обследование нельзя считать лечебным, потому что в случае злокачественной природы образования должно проводиться удаление лимфатических узлов, а также может возникнуть надобность более обширного вмешательства. Полное удаление опухоли показано в случаях. Когда ее размеры не превышают 2.5 см. В остальных ситуациях производится частичное иссечение.
Подводя итог, еще раз напомним, что главное предназначение биопсии — выяснить, какова природа опухоли. Если у пациента имеются симптомы, указывающие на ее наличие в организме. Диагноз может быть поставлен только после проведения биопсии. Проведение биопсии возможно либо путем хирургического вмешательства, либо с помощью неоперативных методов (тонкой игла). Они оказывают меньшее стрессовое влияние на организм пациента , а также имеют меньший риск возникновения осложнений. Однако, вероятность получения неправильных результатов при проведении биопсии нехирургическими методами достаточно велика. В 80 % случаев биопсия определяет доброкачественные процессы.
Однако, вероятность получения неправильных результатов при проведении биопсии нехирургическими методами достаточно велика. В 80 % случаев биопсия определяет доброкачественные процессы.
Гистология (морфология) — исследование образцов, полученных в результате биопсии пищевода, желудка и кишечника
Гистология — это исследование тканей под микроскопом, которое позволяет получить информацию о состоянии клеток и структуре исследуемого образца. Материал для исследования получают с помощью биопсии или других инвазивных методов.
Небольшие кусочки ткани слизистой пищевода, желудка или кишечника, для гистологии врач-эндоскопист берет с помощью специальных биопсийных щипцов, встроенных в эндоскоп, во время эндоскопического обследования желудочно-кишечного тракта. Биопсия проводится с подозрительных участков слизистой оболочки (язвы, эрозии, атрофия, гиперплазия, полипы). Эта процедура практически не вызывает болезненных ощущений и ненамного увеличивает время обследования.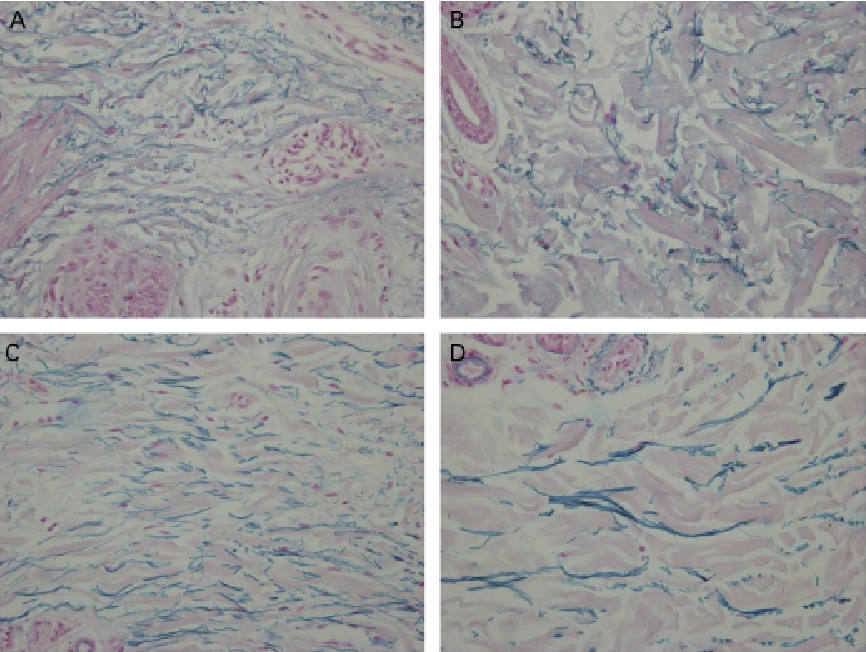
Правильно приготовленный материал для исследования и точно выполненная биопсия является залогом достоверности гистологического исследования. Необходимое эндоскопическое обследование с биопсией можно пройти в нашем центре, а также получить заключение врача-патоморфолога.
Пациент в результате обследования получит
Заключение врача-патоморфолога о результатах микроскопического исследования тканей слизистой оболочки пищевода, желудка или кишечника, в котором содержится информация о наличии или отсутствии патологического изменения клеток и/или воспалительного процесса, а также клеточном составе исследуемых образцов. В заключении может присутствовать предварительный или заключительный диагноз, а также микроскопическое описание тканей и клеток в образцах полученных с помощью биопсии, которое поможет вашему лечащему врачу подтвердить или опровергнуть предварительный диагноз и назначить подходящее лечение и дополнительное обследование при необходимости.
Справочная информация
Гистологическое исследование тканей пищевода, желудка или кишечника может понадобиться для уточнения диагностики заболеваний этих органов, выявления предраковых состояний (метаплазия, дисплазия) и установления характера новообразований (доброкачественные или злокачественные).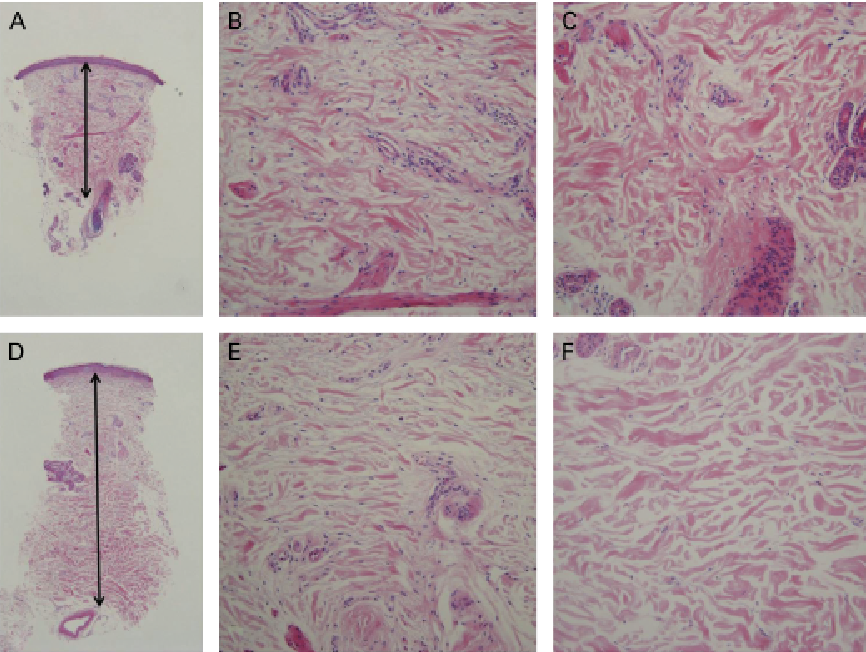 Обычно эндоскопическое обследование в сочетании с гистологией позволяет поставить окончательный диагноз, но иногда могут понадобиться дополнительные обследования.
Обычно эндоскопическое обследование в сочетании с гистологией позволяет поставить окончательный диагноз, но иногда могут понадобиться дополнительные обследования.
Когда нужна гистология при заболеваниях желудочно-кишечного тракта?
Патоморфологические исследования
Патоморфологические исследования – это метод диагностики, основанный на изучении строения и изменений, происходящих в тканях, при помощи микроскопа.
В онкологии данный метод имеет чрезвычайно важное значение, так как позволяет не только подтвердить наличие опухоли, но и уточнить ее конкретный вариант, а в ряде случаев, при использовании дополнительных окрасок, и индивидуальные характеристики конкретной опухоли, что влияет на выбор лечения.
Микроскопически исследуются небольшие фрагменты ткани, полученные при биопсии, удаленные во время операции органы и все тканевые образцы, которые самопроизвольно отделились от тела.
Исследование операционного материала помимо гистологической характеристики опухоли позволяет оценить качество и полноту операции, края резекции, уточнить локальную стадию, что влияет на прогноз заболевания и тактику ведения пациента.
Гистологические препараты могут длительно храниться, это не требует специальных условий. При необходимости и желании они в любой момент могут быть пересмотрены, гистологические материалы служат юридическим документом.
В НМИЦ онкологии выполняются следующие виды патоморфологических исследований:
Гистологическое исследование с последующим патоморфологическим заключением новообразований любой локализации:
- конуса шейки матки
- мультифокальной биопсии предстательной железы
- операционного материала
и тд
Иммуногистохимические исследования с широкой панелью маркеров при заболеваниях любой локализации:
- гемато-лимфоидной ткани
- опухолях мягких тканей
- раке молочной железы
и т.д.
Кроме того выполняются FISH-исследования, например амплификации HER2.
Осуществляется подбор материала для молекулярно-генетического исследования.
Существует возможность сканирования гистологических препаратов с изготовлением их полноценной цифровой копии.
Консультация врачом готовых гистологических препаратов может быть выполнена срочно в том числе в течение 1 дня, при возможности, что будет оценено при сдаче материала.
Консультация препаратов образований костей и суставов производится мультидисциплинарной группой врачей с обязательным клинико-рентгено-морфологическим сопоставлением.
На пересмотр необходимо сдавать не только стекла, но и снимки (до вмешательств и операций). Кроме того, обязательно требуются снимки (до биопсии или операции) при консультации препаратов образований головного мозга.
Для сокращения сроков и повышения качества диагностического заключения необходимо по возможности предоставлять все имеющиеся данные обследований.
Биопсия шейки матки (под наркозом) – Цена, порядок взятия анализа, расшифровка результатов – Клиника ЦКБ РАН в Москве
Биопсия шейки матки – один из наиболее эффективных методов диагностики состояния тканей шейки. Основная цель процедуры – диагностика патологий женских половых органов в случаях, когда другие методы не дают нужной информации. С помощью биопсии диагностируется в том числе рак шейки матки. В основе исследования – взятие биопсии на анализ и последующее исследование всех слоев материала в лаборатории. Основным преимуществом метода является возможность ранней диагностики опасных заболеваний и проведение их успешного лечения.
Основная цель процедуры – диагностика патологий женских половых органов в случаях, когда другие методы не дают нужной информации. С помощью биопсии диагностируется в том числе рак шейки матки. В основе исследования – взятие биопсии на анализ и последующее исследование всех слоев материала в лаборатории. Основным преимуществом метода является возможность ранней диагностики опасных заболеваний и проведение их успешного лечения.
Оптимальным временем для взятия образца считается несколько дней после окончания менструации. Таким образом минимизируется риск воспаления и дается максимум времени для полного восстановления тканей до следующего цикла.
Когда назначается биопсия
Есть несколько показаний для проведения анализа:
- Уточнение диагноза, поставленного ранее.
- Неэффективность кольпоскопии и пап-анализа.
- Любые тревожные подозрения, возникшие на осмотре у гинеколога.
- Неудовлетворительные результаты мазка на цитологию.
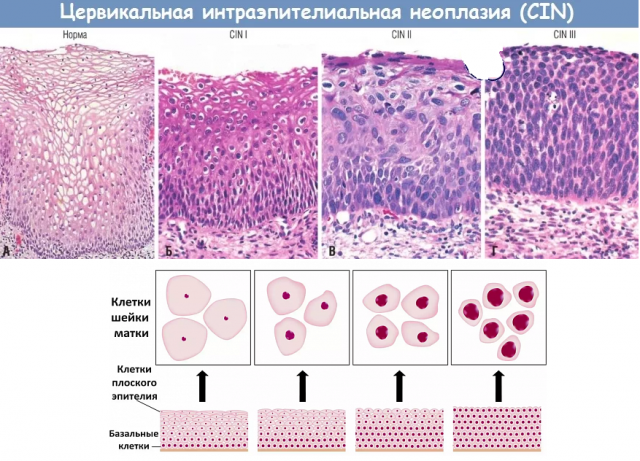
- Кисты, полипы, лейкоплакия, эрозия.
- Мозаика, пунктуация, сосуды нетипичного характера.
- Йод-негативные участки, измененный эпителий шейки.
- Подозрение на развитие раковой опухоли, бугристая поверхность.
Противопоказания
Биопсия не проводится в следующих случаях:
- При воспалительных и инфекционных заболеваниях половых органов.
- При нарушении свертываемости крови.
- При менструальных выделениях.
- При беременности (биопсия может проводиться при наличии особых условий.
Особенной осторожности требует анализ на ранних и поздних сроках беременности, так как риск прерывания сильно возрастает в эти периоды. Оптимально проведение биопсии после родов (через несколько недель).
Виды анализа
Для получения тканей на анализ используются разные методики. Часть из них не только позволяют произвести забор материала, но и ускорить процесс лечения. Выбор метода в каждом случае индивидуален и зависит от особенностей клинической картины. Наиболее часто используются следующие методы биопсии:
Выбор метода в каждом случае индивидуален и зависит от особенностей клинической картины. Наиболее часто используются следующие методы биопсии:
- Прицельная. Осуществляется во время кольпоскопии, позволяет взять небольшой фрагмент подозрительной ткани. Забор материала проводится иглой, без обезболивания, амбулаторно. Ощущения пациентки сводятся к небольшому покалыванию и ощущению давления.
- Электрохирургическая или петлевая. На анализ берется конусовидный или другой участок ткани, отслаиваемый петлевидным инструментом при помощи тока. Электричество помогает отделять ткани легко, требуется местная анестезия. Процедура также проводится амбулаторно. За счет некоторого количество обгоревших участков ткани результаты могут быть изменены. Заживление после такого вмешательства достаточно долгое, есть кровянистые выделения. Пациенткам, планирующим беременность, метод не рекомендуется, так как может образоваться рубец и снизиться эластичность.
- Холодно-ножевая или клиновидная.
 Проводится скальпелем, при помощи которого вырезается кусочек треугольной формы. Процедура может также носить лечебных характер, так как часть пораженных тканей удаляется. Требуется общая или спинальная анестезия, биопсия этого типа проводится в стационаре с выпиской в тот же день или на следующий в зависимости от реакции организма.
Проводится скальпелем, при помощи которого вырезается кусочек треугольной формы. Процедура может также носить лечебных характер, так как часть пораженных тканей удаляется. Требуется общая или спинальная анестезия, биопсия этого типа проводится в стационаре с выпиской в тот же день или на следующий в зависимости от реакции организма. - Конхотомная. Очень похожа на пункционную, но проводимую конхотомом. Инструмент схож с ножницами. Проводится амбулаторно под местной анестезией.
- Циркулярная или круговая. При взятии материала используется радиоволновой нож или скальпель. Участок, который отделяется, достаточно объемный. Захватывается часть цервикального канала. Помимо диагностики метод позволяет избавиться от некоторой части патологических тканей, то есть его можно также считать лечебным. Это биопсия под наркозом, требует общей или спинальной анестезии, некоторого времени пребывания в больничной палате. Восстановление занимает несколько недель, в течение всего периода может наблюдаться выделение крови и боль.

- Лазерная. Проводится под общим наркозом лазерным ножом, пациентка находится в стационаре. Негативные последствия возникают редко, реабилитация не нужна.
- Радиоволновая. Проводится с применением радиоволнового ножа «Сургитрон». Сильных повреждений ткани нет, могут быть небольшие кровянистые выделения, которые быстро пройдут. Рубцы не образуются, другие осложнения происходят крайне редко, метод идеально подходит те, кто планирует беременность в будущем.
- Кюретаж, или эндоцервикальный метод. Предполагает выскабливание цервикального канала. Проводится с использованием внутривенной анестезии.
В какое время проводится
Оптимальным считается период между пятым и седьмым днем цикла. Менструальные выделения к этому времени прекращаются, риск инфекции минимальный и есть время для заживления дол наступления следующей менструации.
Необходимые анализы
Область, которая остается незащищенной после взятия материала на анализ, может подвергнуться инфицированию. Для минимизации срока заживления и снижения вероятности осложнений исследование проводится после оценки основных параметров. Это данные:
Для минимизации срока заживления и снижения вероятности осложнений исследование проводится после оценки основных параметров. Это данные:
- Коагулограммы.
- Развернутого анализа крови.
- Цитологического исследования мазка.
- Анализа на ЗППП, гепатит, ВИЧ.
Подготовительные мероприятия
Для точности результата и максимальной безопасности нужна предварительная подготовка. Она включает:
- Половой покой минимум за двое суток до процедуры.
- Отказ от спринцеваний, использования тампонов, введения лекарственных средств во влагалище.
- Пробу на лекарственные препараты, чтобы избежать нежелательной реакции на анестезию.
- Беседу с анестезиологом.
- Душ, удаление лобковых волос.
- Ограничение приема пищи перед процедурой за 8-12 часов.
Ход проведения анализа
Ход процедуры зависит от выбранного типа. Она может быть амбулаторной или проводиться в условиях стационара.
Она может быть амбулаторной или проводиться в условиях стационара.
Без госпитализации
Процедура не предполагает госпитализации и наркоза:
- Женщина помещается на гинекологическое кресло в классической позиции (как при обычном осмотре).
- Вводится зеркало.
- Нужная область обрабатывается антисептиком, проводится местное обезболивание.
- Берется материал.
- Пациентка может уйти домой сразу или через несколько часов после процедуры.
Время проведения – не более получаса.
Биопсия в стационаре
Стационарного пребывания требует анализ, проводимый под общим или эпидуральным наркозом. Реабилитация после такого вмешательства длится до десяти суток. Кровянистые выделения разной интенсивности наблюдаются в течение нескольких дней. Пациентке необходимо придерживаться некоторых правил:
- Не поднимать тяжести, избегать интенсивных физических усилий.
- Половые контакты должны быть ограничены.
- Не пользоваться тампонами, вагинальными кремами и свечами, если это не предусмотрено врачом.
- Отказаться от ванны, сауны, посещения бассейна.
В каких случаях нужно обратиться к врачу
В ряде случаев биопсия может сопровождаться осложнениями. Среди тревожных сигналов:
- Выделение алой крови, сгустков, сильные кровотечения.
- Выделения, похожие на менструации, продолжающиеся более десяти дней.
- Изменение температуры тела.
- Боли в нижней части живота.
- Выделения, которые не прекращаются четырнадцать и более дней.
- Выделения, которые имеют желтый оттенок и неприятный запах.
Эти симптомы указывают на неправильное заживление, присоединение инфекции и другие серьезные нарушения.
Возможные риски
Осложнения после биопсии возникают редко, при грамотном подходе она переносится пациентками хорошо. После проведения анализа циркулярным, коническим и петлевым методом могут возникать рубцы. Это в свою очередь провоцирует проблемы в дальнейшем для зачатия и родов. Поэтому пациенткам детородного возраста проводятся щадящие процедуры взятия тканей.
Что показывает исследование
Результаты биопсии формируются по тому же принципу, что и пап-тест. Ее точность выше, результат достовернее. Точно расшифровать результат может только врач, который знаком с клинической картиной. Основные заболевания, которые выявляет анализ:
- Опухоли и рак шейки.
- Кондиломы.
- Лейкоплакия.
- Воспаление цервикального канала.
- Дисплазия.
Большинство выявляемых заболеваний поддаются лечению и успешно устраняются при своевременном обращении. Речь не идет о запущенной онкологии.
Какой специалист назначает биопсию шейки матки
На анализ направляет гинеколог или онколог. Как правило, поводом для проведения исследования служит подозрение на рак, полипы, наличие эрозии, плохие показатели пап-теста и кольпоскопии. Метод инвазивный, однако потенциальный дискомфорт полностью оправдывается его высочайшей эффективностью. Цена исследования и способ забора материала определяется в зависимости от выбранной процедуры.
Пройти биопсию в современной клинике предлагает ЦКБ РАН в Москве. Изучить отзывы пациентов и другую полезную информацию можно на сайте. Запись на прием по телефону или онлайн через форму обратной связи.
Стоимость биопсии шейки матки
|
Название услуги |
Стоимость, руб |
|
|
2500 |
Пункционная биопсия различных органов и тканей
Пункционная биопсия – это метод исследования, при котором проводится прижизненный забор клеток или фрагментов тканей с диагностической целью, в том числе с применением диагностической аппаратуры для навигации (УЗД, КТ, МРТ, рентген), с дальнейшим исследованием клеток или фрагмента ткани (цитология и гистология). Биопсия является обязательным методом подтверждения диагноза, особенно при подозрении на наличие онкологических заболеваний.
Тонкоигольная пункционная аспирационная биопсия (ТАПБ, получаемый материал – клетки, с последующим цитологическим исследованием) проводится с использованием обычного инъекционного шприца без анестезии или, при желании пациента, под местной анестезией.
CORE биопсия (КОР, сердцевинная, режущая биопсия, получаемый материал – фрагмент ткани, с последующим гистологическим исследованием) проводится с использованием специальной иглы и автоматического биопсийного пистолета под местной анестезией или, при желании пациента, под внутривенным наркозом.
Аспирационно-режущая биопсия – с помощью специальной иглы одномоментно проводится забор клеток и мелких фрагментов ткани органа. Отличается меньшей сохранностью ткани при заборе, однако позволяет получить материал за один прокол, что менее травматично(больше подходит для щитовидной железы).
Биопсии в нашем учреждении проводятся специалистами, имеющими специализацию в лучевой диагностике, хирургии, урологии и гинекологии, с использованием современного оборудования и расходных материалов.
Для проведения ТАПБ используется система для ручной биопсии фирмы SteryLab, позволяющая быстро, точно и безболезненно получать материал из очагов размерами от 5 мм.
Для проведения CORE биопсий используется автоматическая биопсийная система фирмы Bard, позволяющая эффективно и быстро получать материал из органов и тканей.
Для ЭХО-навигации используются УЗ-сканеры фирм Aloka (A6), ESaote (MyLab30) и Toshiba (Aplio 400).
Записаться на биопсию и уточнить стоимость можно по телефону +7(495) 594-4444. Стоимость также указана в прайс-листе, размещённом на сайте нашего учреждения
Для проведения биопсий внутренних органов необходима госпитализация на срок до 24 часов.
О готовности результатов цитологического и гистологического исследований вам сообщат по телефону.
Выдача результатов биопсий проводится ежедневно с 08:00 до 20:00, кроме субботы и воскресенья.
В стационаре выдаётся выписка с результатами проведенной цитологической или гистологической диагностики.
В нашей клинике проводятся
Пункция щитовидной железы под эхо-навигацией
ТАПБ щитовидной железы (тонкоигольная аспирационная пункционная биопсия под ЭХО-навигацией) является информативным методом, позволяющим оценить изменения в органе, ранее обнаруженные при проведении аппаратной диагностики (УЗИ).
Результаты цитологического исследования позволяют оценить характер процесса (доброкачественный или злокачественный), что определяет дальнейшую тактику лечения: наблюдение в динамике, медикаментозное лечение, операция.
Перед проведением пункции необходимо получить консультацию эндокринолога или хирурга.
Уровень гормонов щитовидной железы в крови, после проведения ТАПБ, может повышаться на срок до 2 недель, поэтому кровь на гормоны необходимо сдать до проведения биопсии.
CORE или аспирационно-режущая биопсия, в сравнении с ТАПБ, даёт более точные результаты, проводится под местной анестезией или, при желании пациента, под внутривенным наркозом, с забором столбика ткани и дальнейшим гистологическим и/или цитологическим исследованием.Специальная подготовка не требуется.
Пункция молочной железы
Приоритетной задачей при наблюдении за состоянием молочных желез у женщин является исключение наличия патологических объёмных образований (опухолей).
При обнаружении образования, независимо от его размера, необходимо удостовериться в отсутствии злокачественного процесса, для чего и проводится биопсия.
Рекомендуется проведение ТАПБ (тонкоигольной аспирационной биопсии) при самостоятельном обнаружении пациентом уплотнений в молочных железах, после проведения УЗИ, маммографии, желательно с предварительной консультацией хирурга, маммолога.
CORE или аспирационно режущая биопсия, в сравнении с ТАПБ даёт более точные результаты, проводится под местной анестезией или, при желании пациента, под внутривенном наркозом, с забором столбика ткани и дальнейшим гистологическим и/или цитологическим исследованием.
Специальная подготовка не требуется.
Пункция лимфоузлов
Пункционная биопсия лимфоузлов, образований мягких тканей (тонкоигольная аспирационная или CORE биопсия) проводятся при обнаружении пациентом подозрительных уплотнений под кожей. Желательна предварительная консультация хирурга, онколога.
Специальная подготовка не требуется.
Пункция предстательной железы
Биопсия предстательной железы (трансректальная мультифокальная CORE биопсия под ЭХО-навигацией) обеспечивает гистологическую верификацию и позволяет, наряду с такими методами как УЗД и МРТ, оценить характер изменений в органе, исключить злокачественное поражение.
Процедура проводится в условиях стационара, через прямую кишку, под местной анестезией или, при желании пациента, под наркозом, после получения консультации уролога.
Подготовка к процедуре проводится в стационаре.
Пункция образования яичка
ТАПБ образования яичка (тонкоигольная аспирационная биопсия под ЭХО-навигацией) обеспечивает цитологическую верификацию, позволяет, наряду с такими методами как УЗД и МРТ, оценить характер изменений в органе, исключить злокачественное поражение.
CORE биопсия, в сравнении с ТАПБ, даёт более точные результаты, однако травматична для органа, проводится строго по назначению уролога или хирурга, под внутривенном наркозом, с забором столбика ткани и дальнейшим гистологическим исследованием.
Подготовка к процедуре проводится в стационаре.
Пункция почки под эхо-навигацией
Пункционная биопсия почки, образования почки под ЭХО-навигацией применяется для оценки ткани и выявленного образования почки, исключения злокачественного поражения. Обеспечивает гистологическую верификацию патологического очага и позволяет, наряду с такими методами как УЗД, КТ и МРТ, оценить степень поражения, что обеспечивает выбор адекватного метода лечения.
Процедура проводится в условиях стационара, под местной анестезией или, при желании пациента, под наркозом, обязательно после получения консультации уролога.
Подготовка к процедуре проводится в стационаре.
Трансвагинальная гарпунная биопсия под эхо-навигацией
CORE Биопсия образования яичника, малого таза (трансвагинальная CORE биопсия под ЭХО-навигацией) обеспечивает гистологическую верификацию, позволяет, наряду с такими методами как УЗД и МРТ, оценить характер изменений в органе, исключить злокачественное поражение.
Процедура проводится в условиях стационара, преимущественно через влагалище, только под наркозом, строго после получения консультации гинеколога.
Подготовка к процедуре проводится в стационаре.
Гарпунная биопсия печени, поджелудочной железы под эхо-навигацией
CORE биопсия печени, поджелудочной железы, образований печени и поджелудочной железы под ЭХО-навигацией обеспечивает гистологическую верификацию изменений в органе, что позволяет наряду с такими методами как УЗД, КТ и МРТ оценить характер поражения, исключить злокачественный процесс, обеспечивая выбор адекватного метода лечения.
Процедура проводится в условиях стационара, под местной анестезией или, при желании пациента, под наркозом, строго после получения консультации гастроэнтеролога или хирурга.
Подготовка к процедуре проводится в стационаре.
№AN504, Гистологическое заключение патологов (Европа, США, Канада) (приготовление препарата (костные фрагменты) + сканирование срезов + описательная часть) : показатели, норма
Анализ гистологии биопсионного материала является лучшим методом дифференциальной диагностики. Микроскопическое исследование проводится для небольших фрагментов ткани или органов, полученных при биопсии, удаленные хирургическим путем.
- Подготовка пациента
- Показания и противопоказания
- Форма выдачи результата
Гистологический анализ начинается с визуальной оценки биоматериала и вырезки фрагментов биоматериала для проведения исследования. Микроскопическое исследование проводится для небольших фрагментов ткани или органов, полученных при биопсии, удаленные хирургическим путем. Гистологический анализ начинается с визуальной оценки биоматериала и вырезки фрагментов биоматериала для проведения исследования. Следующим этапом гистологического исследования является проводка биоматериала. Для костных фрагментов она отличается, материалу необходимо растворить соли кальция на этом этапе биоматериал проводят декальцинацию. Декальцинация происходит после полной фиксации ткани, обычно в некислых фиксаторах. После декальцинации в кислотах необходимо проводить очистку материала от кислот с помощью щелочных растворов или по крайней мере путем промывания в двух сменных спиртах. Специальная подготовка и обработка биоптата проводится для того чтобы произвести заливку материала в парафиновый блок. Для этого проводятся манипуляции в виде пропитывания гистологического материала специальными средами, которые в последующем застывают с образованием однородной плотной массы, в результате которого получается парафиновый блок. Затем проводится нарезка этого блока на микротоме (микротомирование). В результате микротомирования готового парафинового блока с биоматериалом полученный тонкие срезы толщиной в несколько десятых миллиметра (около 1 микрона), готовые срезы помещаются на стекло и сушатся. Потом осуществляется этап воздействия на гистологический препарат различными красителями, для стандартного окрашивания используют краситель Гематоксилин-Эозин, для более сложных и конкретных случаев существуют различные способы окраски. Окраска производится с целью контрастирования и визуализации гистологических структур. После этого образцы сканируют и отправляются к зарубежным патологам. Для каждого случая индивидуально подбирается патолог в соответствии с его специализацией. Хранение и обработка данных производится на защищенных серверах, при этом один и тот же образец могут одновременно изучать несколько специалистов, советуясь друг с другом и приходя к общему решению. Каждый гистологический препарат смотрит по крайней мере два специалиста. После того, как они пришли к общему выводу, формируется заключение.
Сроки исполнения: 30 рабочих дней.
Исследуемый аналит: биопсийный материал, готовые парафиновые блоки и стекла.
Методы забора материала для исследования: забор биоптата может производиться различными способами:
- Щипковая биопсия – метод забора материала, который чаще проводится во время эндоскопии, специальными щипчиками.
- Пункционная биопсия – метод забора материала клеток, таких как печень или простата. Забор материала производится толстой иглой.
- Аспирационная биопсия – метод забора материала путем отсасывания маленькой трубкой образцов ткани, этот способ применяется для узлов щитовидной железы и т.д.
- Эксцизионная биопсия – метод забора материала путем хирургического иссечения пораженных тканей и органов и исследование их в последующем.
- Трепан-биопсия – метод забора материала жидкости из костной ткани.
- Кюретаж – метода забора материала соскабливание материала из полости с помощью специальных инструментов с острыми краями.
Показания:
- Новообразование.
- Определение и характер злокачественности.
- Заболеваний неопухолевой этиологии.
- Для установления причин гибели животного.
- Послеоперационная диагностика.
- Диагностика и оценка состояния органов и/ или системы органов.
Противопоказания: не выявлено.
Подготовка пациента: зависит от способа и локализации места забора биоматериала. Обычно эту процедуру проводят под местный анестезией или седацией. Если материал берется с кожи, она должна быть очищена механически от грязи.
Метод отбора: в гистологии чаще используют методы световой микроскопии, также используется электронная микроскопия и другие методы микроскопии.
Преаналитика: для теста AN504 необходимы определенные параметры для взятия материал, выбранный участок должен быть без некроза и кровоизлияния, на нем необходимо сделать надрезы через 0,5см-1,0см (для более глубокого проникновения формалина в ткани). Затем поместить кусочек в контейнер(-ы) с формалином подходящего размера (соотношением 1:10). Если в одном контейнере находятся образцы тканей из разных локализаций, отмечайте фрагменты лигатурами или чернилами с пояснением отметок в бланке-направлении. Также этот тест подходит для биоптатов при неопухолевых заболеваниях кожи.
Для неопухолевых заболеваний кожи требуются дополнительные требования. Необходимо отметить направление роста волос на биоптате или разрезать вдоль направления роста волос.
На контейнере необходимо написать (вид, кличка, фамилия владельца, номер истории болезни, локализация фрагмента ткани, помещенного в контейнер).
Также нужно заполнить направление (код клиента, вид, порода, возраст, пол, половой статус, кличка, фамилия владельца, фамилия и контакты лечащего врача, код теста, локализация, внешний вид поражений, анамнез).
В лабораторию отправляются только заполненный направительный бланк и гистопод с материалом в синем пакете. (температурный режим транспортировки в лабораторию +2℃…+8℃).
Форма выдачи результата: макроскопическое и микроскопическое описание биоптата с диагностическим заключением патомарфолога.
Список источников:
- https://www.kp.ru/guide/gistologicheskoe-issledovanie.html
- https://www.niioncologii.ru/patients/screening-and-diagnosis/research-types/pi
Биопсия печени | ГБУ РО
Биопсией называется процедура, при которой производится забор небольшого фрагмента ткани органа для уточнения диагноза.
ПОКАЗАНИЯ К БИОПСИИ ПЕЧЕНИ
Показания для выполнения чрескожной пункционной биопсии печени определяет лечащий врач. Биопсия помогает установить диагноз на морфологическом уровне и уточнить степень поражения органа.
Выполняется чрескожная пункционная биопсия при диффузных и очаговых заболеваниях печени.
К диффузным заболеваниям относятся хронические вирусные и невирусные гепатиты и т.д.
К очаговым заболеваниям относятся доброкачественные и злокачественные (первичные и вторичные) образования печени.
В настоящее время наибольшее распространение получила чрескожная пункционная биопсия печени под ультразвуковым контролем, так как позволяет выполнить прицельную биопсию при очаговых образованиях печени, и свести к минимуму риск развития возможных осложнений. Выполняется данная инвазивная процедура опытным врачом-хирургом, владеющим ультразвуковой диагностикой.
В целом чрескожная пункционная биопсия печени считается безопасной процедурой, однако как любое инвазивное вмешательство, она сопряжена с определенным риском развития возможных осложнений, поэтому важно, правильно к ней подготовиться, чтобы максимально снизить риск развития осложнений. На сегодняшний день при соблюдении всех условий выполнения чрескожной пункционной биопсии печени под ультразвуковым контролем риск развития тяжелых осложнений (внутреннего кровотечения) составляет 1:18000.
КАК ПОДГОТОВИТЬСЯ К БИОПСИИ ПЕЧЕНИ?
Если вам назначили проведение данного метода исследования, то во время консультации следует сообщить врачу, есть ли у вас сердечные или легочные заболевания, аллергия, в том числе на лекарственные препараты.
В случае необходимости постоянного приема препаратов, разжижающих кровь, об этом обязательно нужно сообщить врачу-хирургу который будет выполнять биопсию.
За неделю до проведения биопсии необходимо прекратить прием аспирина и противовоспалительных средств, но только после консультации врача назначавшего вам данные препараты, не рекомендуется самостоятельно отказываться от них.
До выполнения биопсии необходимо сдать общий анализ крови, определить группу крови, а также оценить свертывающую систему крови.
Последний прием пищи должен быть за 10 – 12 часов до процедуры. Можно принимать назначенные врачом лекарственные препараты, запивая их небольшим количеством воды.
Желательно сделать очистительную клизму.
КАК ДЕЛАЮТ БИОПСИЮ ПЕЧЕНИ?
Чрескожная пункционная биопсия печени, как правило выполняется амбулаторно в условиях дневного стационара под местной анестезией. Перед процедурой врач выполняет ультразвуковое исследование (предоперационную маркировку) чтобы точно определить место пункции.
Процедура заключается в следующем, после обработки места пункции дезинфицирующим раствором, выполняется обезболивание местным анестетиком, затем специальной иглой выполняется прокол и забор небольшого фрагмента (биоптата) ткани печени. Биопсия выполняется лежа на спине, с заведенной за голову правой рукой. Во время выполнения биопсии больного просят задержать дыхание на 15-20 секунд и не двигаться. Сама биопсия производится очень быстро – за несколько секунд. Для выполнения биопсии печени наиболее часто используется автоматическая биопсийная система с одноразовой стерильной иглой, позволяющая в 100% случаев произвести забор фрагмента ткани печени достаточного для гистологического исследования. После биопсии больной находится под наблюдением в течении 2 часов, с целью оказания немедленной медицинской помощи при развитии возможных осложнениях. На область пункции прикладывается холод.
Через два часа после биопсии больному выполняют УЗИ с целью выявления возможных осложнений, а так же определяют давление и пульс. Если процедура прошла успешно больной может быть отпущен домой. После процедуры больному не разрешается водить автомобиль, поэтому просим Вас заранее договориться с родственником или знакомым, чтобы вас отвезли домой. Дома больной должен в течении суток соблюдать постельный режим, можно пить и принимать пищу. Еще сутки больной проводит в щадящем режиме, при этом не рекомендуется заниматься физическими упражнениями и исключить тяжелую физическую нагрузку. В течение недели больному противопоказан прием препаратов, содержащих ацетилсалициловую кислоту и противовоспалительные нестероидные средства.
Полученный во время биопсии фрагмент ткани печени (биоптат) будет направлен в лабораторию на морфологическое (гистологическое) исследование. При использовании автоматической биопсийной системы размеры фрагмента ткани печени составляют от 1,5 до 2,5 см длиной и от 1 до 1,5 мм в диаметре, что составляет приблизительно 1/50 000 часть массы печени. Гистологическое исследование выполняется в течение 5-7 дней. Результаты гистологического исследования позволяют поставить точный диагноз, а следовательно назначить правильное лечение. Степень правильности поставленного диагноза составляет 98-99 %.
По всем вопросам связанных с выполнением процедуры звоните по телефону 8 (863) 250-80-87.
Что происходит с образцами биопсии и цитологии?
Стандартные процедуры и методы используются для обработки почти всех типов образцов биопсии. Эти процедуры представляют собой обычные способы подготовки образца в лаборатории. Другие процедуры, описанные ниже, также могут выполняться на определенных типах образцов (например, на лимфатических узлах и костном мозге).
Как обычно обрабатываются биопсии
После извлечения образец биопсии помещается в контейнер со смесью воды и формальдегида (формалина) или другой жидкости для его сохранения.На контейнере указано имя пациента и другая идентифицирующая информация (например, номер больницы и дата рождения) и место проведения биопсии (где именно на теле она была взята). Затем его отправляют в лабораторию патологии. Затем патологоанатом или обученный лаборант смотрит на образец без микроскопа. Это называется брутто-экзамен . (В медицине «брутто» означает , видимое без микроскопа .) Это делается для записи того, что можно увидеть, просто глядя на ткань, измеряя ее или ощущая на ощупь.Макросъемка включает размер, цвет, консистенцию и другие характеристики образца ткани. Персонал лаборатории может даже сфотографировать образец как часть записи. Общий осмотр важен, поскольку патолог может увидеть признаки, указывающие на рак. Это также помогает патологу решить, какие части большой биопсии наиболее важны для просмотра под микроскопом.
Для небольших биопсий, таких как пункционная биопсия или стержневая биопсия, обычно исследуют весь образец под микроскопом.Салфетки помещаются в небольшие контейнеры, называемые кассетами . Кассеты надежно удерживают ткань во время обработки. После обработки, которая может занять несколько часов (но обычно проводится в течение ночи), образец ткани помещают в форму с горячим парафином. Воск остывает, образуя твердый блок, который защищает ткань.
Этот парафиновый восковой блок с заделанной тканью разрезают на очень тонкие срезы с помощью инструмента, называемого микротомом . Эти тонкие срезы образца помещают на предметные стекла и погружают в серию пятен или красителей, чтобы изменить цвет ткани.Благодаря цвету клетки легче увидеть под микроскопом. Для большинства образцов биопсии рутинная обработка — это все, что необходимо. На этом этапе (обычно на следующий день после проведения биопсии) патолог смотрит на ткань под микроскопом. Такой взгляд на твердые образцы называется гистология , которая представляет собой исследование структур клеток и тканей.
Специальная биопсия: замороженный участок (во время операции)
Иногда информация об образце ткани необходима во время операции, чтобы принять немедленное решение.Если хирург не может дождаться дня или более, необходимого для рутинной обработки и гистологии, он или она запросит во время операции (во время операции) консультацию по патологии. Это часто называется экзаменом замороженного раздела .
Как делается замороженный участок?
Когда выполняется исследование замороженного среза, свежая ткань отправляется из операционной прямо к патологоанатому. Поскольку пациент часто находится под общей анестезией (засыпает лекарствами), важно быстро осмотреть ткань.Обычно это занимает от 10 до 20 минут. Патолог тщательно исследует свежую ткань, чтобы решить, какую ее часть следует рассматривать под микроскопом. Вместо того, чтобы обрабатывать ткань восковыми блоками, ткань быстро замораживается в специальном растворе, который образует вокруг ткани нечто похожее на кубик льда. Затем его тонко разрезают (нарезают) на специальной машине, быстро окрашивают (погружают в ряд красителей) и рассматривают под микроскопом. Замороженные срезы обычно не показывают особенности ткани так четко, как срезы ткани, залитые воском, но они достаточно хороши, чтобы помочь хирургу принимать решения во время операции.
Когда готово замороженное сечение?
Чтобы узнать, является ли опухоль раком: Иногда тип необходимой операции зависит от того, является ли опухоль раковой (злокачественной). Например, простого удаления опухоли может быть достаточно для лечения опухоли, которая не является раковой (доброкачественной), но может потребоваться удаление большего количества ткани и / или лимфатических узлов, если опухоль является раковой. В таком случае хирург может отправить опухоль на исследование замороженного среза. Часто это может дать достаточно информации, чтобы помочь хирургу решить, какой тип операции лучше всего подходит для пациента.Однако иногда замороженный участок не дает однозначного ответа, и для получения четкого ответа кусочек ткани должен пройти обычную или даже специальную обработку. Когда это происходит, хирург обычно останавливает операцию и закрывает хирургический разрез (разрез). После получения результатов может потребоваться еще одна операция.
Чтобы убедиться, что рак полностью удален: Хирургическое лечение рака часто представляет собой сложный баланс между удалением достаточного количества ткани, чтобы почувствовать, что рак полностью удален, и оставлением достаточного количества нормальной ткани, чтобы ограничить повреждение.Если хирург обеспокоен тем, что рак не был удален полностью, срез края ткани, который был удален (называемый полем ), отправляется на диагностику замороженного среза. Если на границе нет раковых клеток, дополнительная операция обычно не требуется. Но если раковые клетки обнаружены, можно предположить, что некоторые из них еще остались в ткани пациента. Если это происходит, хирург обычно удаляет больше ткани, чтобы попытаться удалить все раковые клетки и снизить вероятность повторного рака.Если невозможно удалить больше ткани, могут быть другие варианты, такие как облучение, чтобы убить оставшиеся раковые клетки.
Процесс для хирургии Мооса (хирургия под микроскопом)
Эта процедура используется для лечения некоторых видов рака кожи. В хирургии Мооса хирург удаляет тонкий слой кожи, в который могла проникнуть опухоль, а затем проверяет образец под микроскопом. Если раковые клетки видны, удаляются другие слои и проверяются до тех пор, пока в образцах кожи не будут обнаружены раковые клетки.Этот процесс идет медленно, но это означает, что можно сохранить более здоровую кожу рядом с опухолью. Хирургия Мооса — это узкоспециализированная методика, которую должны использовать только обученные врачи.
Как обрабатываются образцы цитологии
Порядок обработки цитологических образцов зависит от типа образца. Некоторые образцы размазываются на предметных стеклах микроскопа врачом, который получает образец. Эти слайды, которые называются мазками , затем отправляются в цитологическую лабораторию, где их окунают в серию пятен (цветных красителей), очень похожих на те, которые используются для образцов биопсии.
Другие образцы, такие как биологические жидкости, нельзя легко поместить на предметное стекло микроскопа, потому что они слишком разбавлены (в большом объеме жидкости слишком мало клеток). Процедуры используются для концентрирования этих клеток на предметном стекле до того, как они будут окрашены.
После обработки и окрашивания образцы исследуют под микроскопом. Аномальные клетки обнаруживаются и помечаются специальной ручкой. Затем патолог исследует отмеченные клетки, чтобы поставить диагноз.
Как долго хранятся образцы патологии?
Федеральный закон под названием CLIA (Поправки по улучшению клинических лабораторий) регулирует регулирование и сертификацию клинических лабораторий.Чтобы получить аккредитацию CLIA, лаборатории должны хранить человеческие образцы в течение минимального времени. Например, CLIA говорит, что лаборатории должны хранить:
- Цитологические препараты минимум 5 лет
- Гистопатологические слайды за не менее 10 лет
- Блоки парафиновые не менее 2 лет
В некоторых штатах действуют собственные законы, согласно которым лаборатории должны хранить образцы патологий дольше, чем время, указанное в правилах CLIA. А в некоторых лабораториях есть правила хранения образцов дольше, чем это требуется федеральными законами или законами штата.
Что это значит для вас
Некоторые люди хотят получить второе мнение по поводу диагноза, сделанного на их образце ткани (образце). Это называется обзором патологии. Это означает, что нужно попросить другого врача взглянуть на вашу биопсийную ткань и поставить диагноз на основании увиденного.
Образцы тканей человека не выбрасываются сразу после тестирования. Поэтому в большинстве случаев, если ткани достаточно, образец можно отправить другому врачу или в лабораторию.
Иногда более длительное хранение образцов может быть полезным и по другим причинам.Например, если у пережившего рак развивается опухоль через несколько лет после удаления первой, врачи захотят узнать, является ли эта новая опухоль старой, возвращающейся (рецидив), или совершенно новым раком.
Это часто можно определить, основываясь на расположении двух опухолей и сравнивая гистопатологические слайды обоих образцов. Но иногда также могут помочь дополнительные тесты (например, иммуногистохимические окрашивания), которые можно провести с использованием ткани из парафинового блока исходного образца.
После биопсии: постановка диагноза
Во время биопсии врач удаляет небольшое количество ткани для исследования. Это важный способ диагностики многих различных типов рака. После биопсии ваша медицинская бригада выполнит несколько шагов, прежде чем патолог поставит диагноз. Патолог — это врач, который специализируется на чтении лабораторных тестов и изучении клеток, тканей и органов для диагностики заболевания.
Глядя на образец ткани
Образец ткани, взятый во время биопсии, называется образцом.Медицинский персонал, выполняющий биопсию, помещает образец в контейнер с жидкостью, чтобы сохранить его. Они маркируют контейнер своим именем и другими данными. Затем патологоанатом описывает, как это выглядит невооруженным глазом. Это включает в себя цвет, размер и другие особенности. Это называется макроскопическим или макроскопическим исследованием. Общее описание включает следующую информацию:
Образец может потребоваться для других анализов, основанных на предположении врача о заболевании до биопсии, что называется предполагаемым диагнозом.Молекулярные тесты находят гены, которые могут быть активными, измененными или отсутствующими. Могут потребоваться другие тесты на гены или белки, чтобы определить, какое лечение подействует. Патологоанатом или техник подготовит часть образца для этих тестов.
Изготовление слайда
Перед исследованием ткани под микроскопом патологоанатом или техник готовит предметное стекло. Во время этого процесса образец разрезается на тонкие срезы, называемые гистологическими срезами. Затем их окрашивают различными красителями, на которых видны части клеток.Патологоанатом или техник помещает срезы на предметное стекло. Затем они помещают сверху тонкое покрытие, называемое покровным стеклом, чтобы удерживать образец на месте. Затем патологоанатом просмотрит срезы под микроскопом.
Вот типы слайдов, которые может подготовить ваш патологоанатом или техник:
Постоянный участок. Для создания постоянного среза лаборант помещает образец в фиксатор на несколько часов. Фиксатор — это вещество, которое удерживает образец «фиксированным», чтобы он не изменялся.Продолжительность пребывания образца в фиксаторе зависит от его размера. Наиболее часто используемым фиксатором является формалин. Это приводит к тому, что белки в клетках становятся твердыми, так что они не изменяются.
Затем техник помещает фиксированный образец в машину. Эта машина удаляет воду из ткани и заменяет ее парафином. После этого техник заливает образец в кусок парафина большего размера. Парафиновые блоки долговечны и могут храниться неограниченное время. Когда парафиновый блок затвердевает, технический специалист разрезает образец на очень тонкие срезы с помощью устройства, называемого микротомом.Затем тонкие ломтики опускают в воду, чтобы их можно было зачерпнуть на предметное стекло.
После того, как срез окажется на предметном стекле, парафин растворяется в ткани и снова добавляется вода. Затем техник окрашивает части клетки красителями. В центре клетки, называемом ядром, находятся гены. Это окрашено в темно-синий цвет. Содержимое клетки между ядром и клеточной мембраной называется цитоплазмой. Это окрашено в розовый или оранжевый цвет.
Замороженный участок. Для создания замороженного среза образец быстро замораживается после того, как хирург извлекает его из тела пациента. Затем техник может разрезать образец на тонкие слои с помощью специального устройства, называемого криостатом. Эти срезы помещаются на предметное стекло и окрашиваются тем же методом, что и постоянный срез. Качество замороженного участка часто уступает постоянному. Но процесс идет быстрее. Доктору требуется всего несколько минут, чтобы определить, является ли ткань злокачественной.Врачи чаще всего используют его во время операции, чтобы быстро выяснить, нужно ли человеку удалить больше раковой ткани.
Мазок. Если образец представляет собой жидкость или если в жидкости находятся небольшие кусочки ткани, предметное стекло готовят по-другому. Врач размазывает образец на предметном стекле микроскопа и дает ему высохнуть на воздухе. Затем на него распыляют фиксатор или помещают в жидкость для фиксации. Затем фиксированные клетки окрашивают и просматривают под микроскопом.
Просмотр слайдов под микроскопом
Патологоанатом просматривает слайды с срезами образца под микроскопом.Затем патологоанатом составляет отчет о патологии на основе того, что видно под микроскопом. Отчет носит очень технический характер, в нем используются термины, которые имеют значение для других патологов и врачей. Обычно патологоанатом описывает:
Типы ячеек
Как устроены ячейки
Являются ли клетки ненормальными
Другие характеристики, важные для диагностики
Иногда патолог может захотеть увидеть больше тканей, прежде чем поставить диагноз.Это будет отмечено в отчете.
Проведение диагностики
В дополнение к описанию, упомянутому выше, отчет о патологии включает описание диагноза. Диагноз часто бывает коротким. Он основан на комбинированных результатах биопсии, макроскопического исследования, обработки и микроскопического исследования. Существует общий формат диагнозов:
Биопсия органа или ткани
Определенная часть органа или тела, из которой взят образец
Процедура биопсии
Особенности тканей
Другие важные результаты
Необходимы ли другие тесты
Диагностические слова
Пациенты могут просматривать отчеты о патологии вместе со своей медицинской бригадой.Полезно иметь некоторую базовую информацию о технических словах, используемых в отчете. Вот несколько слов, которые можно использовать. Узнайте больше о чтении отчета о патологии.
Атипичные: клетки, которые не являются нормальными, но не злокачественными. Атипичные клетки могут со временем перерасти в рак или могут повысить риск рака у человека.
Карцинома: раковые клетки, возникшие из клеток, выстилающих органы, называемые эпителиальными клетками
Саркома: раковые клетки, возникшие в клетках, отличных от эпителиальных клеток
Лимфома: раковые клетки, возникшие в лимфатической системе
Лейкоз: раковые клетки, возникшие в крови или костном мозге
Гиперплазия: аномальное увеличение клеток в ткани или органе.Гиперплазия может увеличить риск развития некоторых видов рака. Это также может быть реакцией организма на различные заболевания.
Дисплазия: увеличение количества аномальных или атипичных клеток в органе. Дисплазия — это реакция на вирусную инфекцию или состояние между нормальными и раковыми клетками.
Неоплазия: Неконтролируемый рост клеток. Клетки могут быть доброкачественными, то есть доброкачественными, или злокачественными, то есть злокачественными.
Молекулярные или генетические тесты для диагностики
Иногда другие тесты помогают врачу дополнительно классифицировать опухоль.Например, чтобы диагностировать некоторые типы лейкемии, патолог ищет определенные генетические изменения в раковых клетках крови. BCR-ABL — это 1 такой модифицированный ген, обнаруженный при хроническом миелолейкозе. Патологоанатом перечисляет результаты этих тестов в отчете о патологии или в отдельных отчетах. Узнайте больше о типах генетических тестов.
Молекулярные тесты для планирования лечения
После того, как врач поставит диагноз, другие тесты могут помочь ему или ей спланировать наилучшие варианты лечения.Онкомаркеры могут помочь предсказать, насколько эффективно лечение конкретного рака. Онкомаркеры — это вещества, уровень которых выше нормы в крови, моче или тканях организма некоторых больных раком. Их можно определить путем тестирования конкретного гена или белка. Например, при раке груди часто рекомендуются тесты на белок HER2 и ген HER2 . Результаты помогают врачу выяснить, могут ли определенные препараты, нацеленные на HER2, быть вариантом лечения.
Связанные ресурсы
Биопсия
Биопсия: 5 вещей, которые должен знать каждый пациент
Близкое и личное знакомство с патологией вашего рака
Что такое персонализированная противораковая медицина?
Дополнительная информация
Колледж американских патологов: как читать отчет о патологии
Национальный институт рака: отчеты о патологии
Что такое биопсия?
Биопсия — это медицинская процедура, при которой берется небольшой образец ткани для исследования под микроскопом.Образец ткани можно взять практически из любого места или в теле, включая кожу, желудок, почки, печень и легкие. Термин биопсия часто используется для обозначения как самого процесса взятия образца, так и самого образца ткани.
Для чего нужна биопсия?
Биопсию можно использовать для исследования причины симптомов человека или для диагностики ряда различных состояний здоровья. Если заболевание уже было диагностировано, можно использовать биопсию, чтобы определить, насколько оно серьезно или на какой стадии.Например, результаты биопсии могут показать, насколько сильно воспален такой орган, как печень.
Невозможно с уверенностью сказать, является ли опухоль или опухоль на коже или внутри тела злокачественной (злокачественной) или доброкачественной, просто взглянув на нее или почувствовав ее.
Эту информацию может предоставить биопсия. Исключить диагноз намного сложнее и может потребоваться несколько тестов, включая несколько биопсий.
Виды биопсии
Существуют различные типы биопсии, с помощью которых можно определить широкий спектр заболеваний.Способ проведения биопсии будет зависеть от того, откуда берется образец ткани.
Операция может начаться с биопсии с тестированием образца сразу же, чтобы хирург мог провести соответствующую операцию, используя предоставленный диагноз.
Роль гистопатолога
Гистопатологи — это врачи, которые диагностируют рак и другие серьезные заболевания, но у них также часто есть хорошие новости, например, обнаружение шишки или родинки совершенно доброкачественными.Некоторые гистопатологи также проводят вскрытия (вскрытия), чтобы выяснить, почему кто-то умер. Гистопатологи также находятся в авангарде исследований многих распространенных заболеваний, таких как рак.
Гистопатологи исследуют биопсии (ткани или клетки), взятые у пациентов в клинике или во время операции.
Гистопатолог исследует биопсию тканей невооруженным глазом, чтобы найти любые видимые отклонения и выбрать части для более детального изучения под микроскопом.Эти маленькие кусочки обрабатываются химикатами, чтобы можно было разрезать очень тонкие ломтики. Срезы окрашивают, чтобы показать различные части клеток, и исследуют под микроскопом, чтобы увидеть, есть ли аномалии в ткани. Если это так, цель состоит в том, чтобы определить природу проблемы. Часто это означает, что поставлен точный диагноз. Они также исследуют клетки в жидкостях организма (цитопатология), таких как моча, а также в больших образцах, например, из хирургических вмешательств по поводу рака кишечника или груди. Эти образцы препарируются («разрезаются и обрезаются»), чтобы выбрать наиболее подходящие области для исследования под микроскопом.
После того, как образец ткани был удален, его можно протестировать с использованием различных химикатов, чтобы увидеть, как он реагирует, и выяснить, что в нем содержится. Тип используемых тестов будет зависеть от исследуемых медицинских условий и характеристик образца ткани.
Патологоанатомы посещают собрания мультидисциплинарных групп (MDT), на которых результаты патологии интерпретируются в контексте всего лечения и ухода за пациентом и обсуждаются с другими клиницистами, такими как хирурги и онкологи.Затем для каждого пациента составляются планы лечения.
Встреча команды MDT — это встреча группы профессионалов из нескольких клинических дисциплин, которые вместе принимают решения относительно рекомендованного лечения отдельных пациентов. MDT могут специализироваться на определенных условиях, например, на конкретном раке.
Моими интересами являются патология печени / поджелудочной железы, головы и шеи, поэтому я могу рассматривать печень, удаленную при трансплантации, частичную резекцию печени или резекцию поджелудочной железы по поводу опухоли.
Понимание вашего отчета о патологии | Отделение патологии UIC
Что такое отчет о патологии?
Отчет о патологии — это письменная медицинская карта диагноза ткани. Тканевый диагноз — это диагноз, который ставится, когда кусок ткани исследуется патологом, врачом, обученным исследовать ткани. Он или она интерпретирует результаты в тканях и ставит диагноз. В большей степени, чем что-либо другое, отчет о патологии определяет лечение рака и сильно влияет на лечение других заболеваний.
Кто такой патолог?
Патолог — это врач, который не менее четырех лет после окончания медицинской школы обучает исследованию тканей и постановке диагнозов. Большинство патологоанатомов проходят обучение более четырех лет и специализируются на постановке диагнозов в различных областях заболеваний человека. Например, ткань груди может быть исследована патологом, специализирующимся на хирургической патологии и патологии груди.
Какие ткани исследуют патологи?
Патологоанатомы обучены исследовать ткани размером от дюжины клеток.Обычно ткань удаляется хирургом, радиологом или другим врачом и отправляется на патологоанатомическое обследование. Тканью могут быть клетки, взятые с помощью тонкоигольной аспирации, биопсии с помощью небольшой стержневой иглы, большего кусочка ткани, предназначенного для удаления поражения, или очень большого фрагмента ткани, который представляет собой целый орган, такой как целая грудь или легкое.
Как патологи исследуют ткани?
Патологи исследуют ткани на двух уровнях. Сначала патологоанатом исследует ткань глазами и пальцами, чтобы найти аномалии.Если кусок ткани большой, патологоанатом разрежет его на множество срезов, чтобы найти небольшие поражения, которые могут быть скрыты в ткани. Патолог ищет и прощупывает части ткани, которые не соответствуют норме. Он или она смотрит на расположение аномалий и на то, как далеко поражение находится от краев образца ткани. Края называются «полями». Для очень маленьких образцов ткани вся ткань обрабатывается для получения микроскопических слайдов. Для более крупных образцов ткани патологоанатом выбирает те части ткани, которые выглядят и / или кажутся ненормальными, а также некоторые нормальные ткани для обработки, чтобы сделать микроскопические слайды.В большинстве случаев патолог может поставить диагноз на основании этого первого уровня исследования тканей. Однако патолог подтверждает диагноз, исследуя срезы под микроскопом, чтобы поставить окончательный или микроскопический диагноз.
Какие типы тканей исследуют патологи?
Ткани, удаленные для патологического диагноза, делятся на две общие категории: Ткань, которая удаляется для постановки диагноза, но не для лечения поражения, называется биопсией. Биопсия может представлять собой очень маленькие кусочки ткани, например, полученные с помощью иглы, или они могут быть большего размера с наложением швов, необходимых для закрытия отверстия, оставшегося от удаления ткани.Ткань, удаленная для лечения поражения, называется резекцией. Обычно резекции представляют собой большие куски ткани, иногда целую часть тела, такую как желудок, толстый кишечник или грудь. Иногда кусок ткани удаляется как для постановки диагноза, так и для лечения поражения. Лампэктомия груди может как удалить, так и диагностировать образование, вызывающее образование.
Какие виды биопсии?
Распространенные типы биопсии:
Аспирация тонкой иглой: Клетки из поражения отсасываются через небольшую иглу и помещаются на предметное стекло.Эта форма биопсии может идентифицировать злокачественные клетки, но не независимо от того, является ли поражение инвазивным или in situ.
Биопсия стержневой иглой: ткань вырезается из очага поражения большой иглой. Ткань называется сердцевиной, потому что это размер и форма внутренней части иглы, используемой для получения ткани.
Основные биопсии полностью отправлены на микроскопическое исследование. Чаще всего биопсия удаляет только часть поражения.
Проволочная или игольная биопсия или иссечение: эта процедура используется, когда поражение невозможно нащупать.Радиолог помещает очень тонкую проволоку рядом с поражением или через него, чтобы направлять хирурга, который удаляет поражение. Чаще всего эту процедуру проводят при поражениях груди. Радиолог получает изображение груди и удаленного фрагмента ткани. Удаляемая ткань обычно достаточно велика, чтобы патолог должен разрезать ткань для поиска аномалий.
«_» -скопическая биопсия: биопсия, полученная с помощью оптоволоконных или жестких телескопов, которые позволяют врачам просматривать внутреннюю часть желудочно-кишечного тракта (желудок, пищевод, толстую кишку, называемые эндоскопией), легких (называемых бронхоскопией), мочевого пузыря. (цистоскопия), матки (кольпоскопия) и верхних дыхательных путей (называемая ларингоскопией).Биопсии получают с помощью специальных режущих щипцов и удаляют через оптоволоконный зонд.
Послеоперационная биопсия: это образец ткани, при котором хирург удаляет часть поражения. Поражение четко очерчено, и есть высокие клинические подозрения, что поражение является раком. Ткань берется только для постановки диагноза и, возможно, для проведения специальных тестов, которые помогут определить, какая терапия будет подходящей.
Эксцизионная биопсия: это ткань, которая представляет собой полное поражение, такое как образование, в котором еще не был поставлен патологический диагноз.Этот тип биопсии сочетает в себе лечение и диагностику.
Второй тип образцов тканей — это более крупные куски ткани, которые удаляются для лечения поражения и / или для определения стадии рака. Опять-таки, для постановки диагноза, лечения и определения стадии рака берут несколько больших образцов ткани. Эти более крупные образцы ткани требуют, чтобы ткань была исследована для обнаружения поражения, затем для определения стадии поражения, а затем для определения того, полностью ли удалено поражение. Патолог определит, какая часть ткани должна быть исследована под микроскопом, чтобы поставить диагноз и, в случае рака, определить стадию рака.Ниже приведены несколько примеров больших образцов:
Мастэктомия: вся грудь удаляется для лечения рака или другого поражения. Существуют разные виды мастэктомий. Некоторые удаляют очень мало кожи, чтобы помочь в реконструкции груди. Некоторые удаляют лимфатические узлы вместе с тканью груди.
Колэктомия: удаляется часть или вся толстая кишка для лечения рака или воспалительного состояния.
Нефрэктомия: удаляется вся почка для лечения рака или из-за того, что почка больше не функционирует из-за инфекции или длительного заболевания почек.
Как ткань подготавливается к микроскопическому исследованию?
Ткань, которая обрабатывается для получения микроскопических срезов, должна быть стабилизирована (зафиксирована), обезвожена, а затем пропитана материалом, который укрепляет ткань, чтобы можно было вырезать очень тонкие срезы, которые можно было исследовать под микроскопом. Сначала фиксируются образцы тканей, предназначенные для микроскопического исследования. Это означает, что все клеточные химические вещества, которые могут вызвать разрушение или деградацию ткани, остановлены. Самый распространенный способ исправить ткань — поместить ее в химический раствор, называемый формальдегидом.Как только формальдегид закрепил ткань, вода удаляется из ткани химическими веществами, такими как спирт. После удаления воды ткань пропитывается парафином или пластиком, чтобы сделать ее достаточно твердой, чтобы можно было разрезать очень тонкие срезы на предметные стекла.
Ткань разрезается на ультратонкие срезы специально обученными технологами, которые также окрашивают тонкие срезы, чтобы патологи могли исследовать срезы под микроскопом.
Сколько времени нужно, чтобы исследовать и обработать ткань для микроскопического исследования?
Изготовление микроскопических препаратов из ткани может занять от 4 до 48 часов в зависимости от типа ткани и используемой обработки.Более короткий период времени требует, чтобы один технолог полностью посвятил свое время изучению одного или двух образцов тканей.
Более длительные периоды времени позволяют лаборатории систематизировать ткани по размеру, типу и приоритету. Некоторые ткани требуют более длительной обработки для получения хороших микроскопических срезов. Очень маленькие образцы тканей требуют особого обращения, чтобы гарантировать, что они не будут повреждены или разрушены при обработке, необходимой для создания микроскопических слайдов. Большинство гистологических лабораторий ежедневно обрабатывают сотни образцов тканей и выпускают слайды для изучения патологами.
Что делать, если у меня рак? Что должно быть указано в моем отчете о патологии для постановки диагноза «Рак»?
Чтобы поставить и подтвердить диагноз рака, патолог должен всегда смотреть на микроскопические слайды поражения. Если есть рак, патолог попросит другого патологоанатома подтвердить диагноз. Если вашим врачом была взята только крошечная часть раковой опухоли (например, мазок, ссадина, бритье, жидкости, аспираты или биопсия), в отчете о патологии может быть указано только то, что рак присутствует.Если было удалено больше ткани, в отчете будет информация.
Отчет о патологии должен правильно идентифицировать вас, с вашим именем и по крайней мере одним другим уникальным идентификатором, таким как дата вашего рождения или номер медицинской карты. В отчете будет указана дата сбора и отправки вашей ткани в патологоанатомическое отделение и номер лабораторного образца. Самая важная часть вашего отчета о патологии — это диагноз, который иногда называют окончательным или микроскопическим диагнозом. В этой части будет указан ваш диагноз рака.Если ваша операция также вылечила ваш рак, ваш отчет о патологии также должен содержать краткое изложение рака. В этом резюме собрана вся патологическая информация о вашем раке, полученная при исследовании образца ткани. В резюме следует указать тип рака, особенности рака и то, распространился ли рак за пределы органа, в котором он возник. Эта информация поможет вашему врачу и вам решить, нуждается ли ваш рак в дополнительном лечении и какое.
Есть много разных видов рака.Карцинома — это рак клеток, которые покрывают или выстилают такие органы, как легкие, желудок и толстую кишку; это самый распространенный вид рака. Саркома — это рак структурных частей тела (кости, хрящи, мышцы и т. Д.). Лейкемия и лимфомы — это рак крови и лимфатической системы.
Обычно также указывается, насколько плохо может вести себя рак, умеренно или слабо дифференцированный или как степень 1, 2, 3, причем степень 1 является лучшей. Стадия или степень распространения рака указывается с помощью системы определения стадии TNM.Т обозначает опухоль; цифры от 1 до 4 и буквы a, b, c и т. д. используются точно так же, как размеры одежды, при этом T1a является наименьшим размером и, скорее всего, излечивается, а T4c — очень большой опухолью, которая почти всегда требует дополнительного нехирургического лечения. N обозначает распространение лимфатических узлов, а M — распространение другого рака (метастатазы) с нумерацией и буквами, начинающимися с нуля (лучший вариант), и чем выше число или буква, тем хуже распространение. N0 (ноль) означает отсутствие метастазов в лимфатических узлах. M0 (ноль) означает отсутствие метастазов.
Иногда сводка по раку не проводится, потому что было удалено недостаточно ткани для определения стадии рака. Иногда точный диагноз не может быть установлен на образце ткани. Патологу может потребоваться запросить дополнительную ткань, провести тесты на ткани и / или попросить другого патолога исследовать ткань. Патолог может также провести тесты вашей ткани (например, активность рецепторов эстрогена в ткани рака груди), чтобы определить, какое дальнейшее лечение следует использовать.
Если у вас было более одной операции с удалением ткани, патолог должен изучить ваш предыдущий патологический материал перед исследованием вашей новой ткани.Это предотвращает ошибки при диагностике и постановке. Если ваш врач удалил меланому, а затем другой врач удалил больше ткани, ваши ткани могли исследовать два разных патолога. Если второй патологоанатом не просмотрел ваш первый отчет о патологии и слайды, он / она может поставить неправильный диагноз или неправильно определить стадию вашей меланомы.
Если небольшие различия в типе или стадии рака могут повлиять на лечение рака, вы можете попросить, чтобы ваши патологические материалы были рассмотрены патологом, который специализируется на вашем типе рака.В большинстве практик крупных патологоанатомов онкологические заболевания автоматически передаются специалистам, а в отделениях мелких патологий специалистов может не быть. Специальное обследование вашей патологии может предоставить дополнительную полезную информацию при планировании лечения рака.
Отчет о патологии предоставляет вашему врачу результаты исследования тканей. Отчеты о патологии ткани, удаленной по поводу рака, должны содержать информацию о типе, степени и стадии рака, чтобы вы и ваш врач могли спланировать наилучшее лечение.Ни один врач не может этично лечить рак, пока не будет поставлен патологический диагноз этого рака.
Цитология и биопсия: сравнение точности
Эндрю С. Лоар, DVM, DACVIM (онкология и внутренняя медицина)
Опубликовано 2017-09-05 в Клиническая патология
Оценка клинически аномальных тканей, представленных на цитологический анализ, на протяжении десятилетий оставалась простой и недорогой диагностической методикой. В отличие от взятия образцов биопсии, материал, полученный для цитологического исследования, обычно требует меньшего количества осложнений, времени и планирования.Лишь небольшое количество исследований продемонстрировало относительную ценность цитологического диагноза по сравнению с гистологическим (биопсия) у одного и того же пациента. В приведенном ниже обсуждении в качестве первой части статьи, состоящей из нескольких частей, рассматриваются исследования, проведенные клиническими и анатомическими патологами в помощь клиницистам, которые должны определить точность результатов, полученных на цитологических образцах.
Диагностическая точность — это частота, с которой тест правильно определяет пациента как имеющего или не имеющего интересующее заболевание; тест с высокой диагностической точностью выявляет относительно мало ложноположительных (высокоспецифичный ) и мало ложноотрицательных (высокочувствительный ) результатов.Поскольку индексный тест часто выполняется для выявления более чем одного болезненного процесса, полезно определить диагностическую точность теста, определив, как часто индексный тест согласуется или коррелирует с эталонным стандартом. Таким образом, во многих исследованиях обсуждается частота совпадения (корреляции) или несогласованности. Другие исследования указывают на долю частичного или полного согласия , что отражает долю случаев, в которых цитологический диагноз совпадает с биопсийным.
Есть несколько неточностей, связанных с выполнением и оценкой цитологических и гистопатологических анализов.Качество обоих тестов и этих сравнительных исследований, очевидно, зависит от опыта клинических и анатомических патологов, читающих слайды. Могут быть значительные различия в диагнозах между разными патологами, оценивающими одни и те же ткани. Действительно, похожие, если не менее существенные различия были выявлены, когда один и тот же человек просматривал одни и те же слайды в разное время. В нескольких гистопатологических исследованиях были рассмотрены вариации между наблюдателями, в основном представляющие различия между первым и вторым мнениями, в диагностике смеси представленных биопсий.Значительные диагностические расхождения наблюдались в 10-20% случаев, при этом клинически значимое частичное (несогласие) отмечалось почти в 50%. Кроме того, изменение типа образца, полученного для биопсии, было связано с противоречивыми результатами; Гистологические образцы иглы или керна обычно показывают меньшую точность, чем материал, полученный с помощью эксцизионной или клиновидной резекции. Эти и другие несоответствия ставят под сомнение термин «золотой стандарт» применительно к гистопатологическому анализу и трудность подтверждения истинно положительных и истинно отрицательных результатов.
Тем не менее, методологии цитологического тестирования могут быть несовместимыми. Каждый цитологический образец должен интерпретироваться с предположением, что представленный материал не может быть репрезентативным для аспирированного поражения. Это очевидно, когда образец бесклеточный или состоит только из элементов периферической крови; однако в большем количестве клеточных образцов клинический патолог может идентифицировать отдельные цитологические результаты, которые являются отрицательными для конкретного заболевания, но не может предположить, что результаты могут быть неубедительными.Это очень важно при сравнении ценности цитологии и биопсии, потому что в большинстве исследований исключение неубедительных цитологических диагнозов заметно улучшает определение диагностической точности. Результаты цитологического исследования, которые не подтверждают опухоль или какой-либо другой окончательный диагноз, не обязательно следует рассматривать как отрицательный результат, если он выполнен на нерепрезентативном образце или идентифицирован как нерепрезентативный.
Другие ограничения при цитологической оценке включают распространение и доступность рассматриваемого поражения.Аспирация очаговых, особенно наружных масс, как правило, дает более репрезентативные результаты по сравнению с материалом, полученным из более диффузных поражений или с помощью внутриполостных игл. Аналогичным образом доказано, что аспираты под ультразвуковым контролем более точны, чем когда игла направлена в меньшем направлении. Наконец, размер используемой иглы, методика аспирации и количество подготовленных слайдов — все это связано с вариациями в диагностической точности, и читателю рекомендуется ознакомиться со стандартными текстами по цитологии, чтобы разработать подходящие методы отбора образцов.
Вернитесь на следующей неделе, чтобы увидеть сообщение, в котором обсуждается относительная точность цитологического исследования по сравнению с биопсией в отношении поражений кожи, желудочно-кишечного тракта, дыхательных путей и костной ткани.
Изображение предоставлено: На основе фотографии ВМС США Тома Ватанабе. [Общественное достояние], через Wikimedia Commons
Об автореДоктор Эндрю Лоар окончил Университет Джорджии. Он прошел стажировку в Государственном университете Луизианы и резидентуру по онкологии в Медицинском центре животных в Нью-Йорке.Он работал в клиническом штате в ветеринарных школах Технологического института Вирджинии и Университета Висконсина, а также в Ветеринарном медицинском центре Западного Лос-Анджелеса. Он получил сертификат совета ACVIM (внутренняя медицина и онкология). Он был первым ветеринарным онкологом, практикующим в южной Калифорнии, и руководил онкологической клиникой в Сан-Диего с 1985 по 1995 год. Доктор Лоар прошел дополнительное обучение в области клинической патологии в Государственном университете Оклахомы и работал консультантом по онкологии / внутренней медицине и цитологом в справочной ветеринарной лаборатории, профессиональной лаборатории животных, теперь ANTEC, и лабораториях IDEXX.Вернувшись в Медицинский центр для животных в качестве клинического цитолога, он позже стал соучредителем ALX Laboratory, небольшой амбициозной лаборатории клинической патологии на Манхэттене. |
Как использовать правила кодирования гистологии
Мы рассмотрели большую часть информации о правилах кодирования гистологии 2007 г. ранее в этом учебном модуле. Ознакомиться с этими руководящими принципами в том виде, в каком они напечатаны в Общих инструкциях MPH 2007 г.
Сейчас:
- Вы ознакомились с Общими инструкциями MPH.
- Вы определили, что является основным сайтом, и просмотрели Эквивалентные термины и определения для этого сайта или основной системы. Определения могут дать вам важную информацию о конкретных типах клеток или взаимосвязях между различными гистологиями.
- Вы использовали модули правил Multiple Primaries для этого сайта, чтобы определить, сколько рефератов нужно подготовить.
- Вы готовы присвоить гистологический код первому реферату. (Позже вы повторите этот процесс, чтобы присвоить гистологический код последующим выпискам для этого случая.)
Где получить информацию о гистологии
В Общих инструкциях в конце правил гистологического кодирования есть примечание, которое определяет порядок приоритета для документов, которые могут содержать гистологический диагноз.
Лучшими документами для получения гистологической информации являются отчет о патологии, цитологический отчет и другая клиническая документация в медицинской карте в указанном порядке.
Отчет о патологии
Отчет о патологии — самый важный документ, к которому у вас есть доступ. Следует запомнить два важных понятия:
- Возьмите гистологическую информацию о наиболее репрезентативном исследованном образце опухоли. Определение «наиболее репрезентативный образец» — это патологический образец хирургической процедуры, в ходе которой было удалено наибольшее количество опухолевой ткани. Другими словами, если пациенту была сделана пункционная биопсия поражения молочной железы с последующей лампэктомией, лампэктомия будет иметь наиболее репрезентативный образец, поскольку она удаляла больше опухолевой ткани, чем пункционная биопсия.Напротив, если у пациента была лампэктомия с последующей мастэктомией, и мастэктомия показала только микроскопический остаток, лампэктомия была бы наиболее репрезентативной, потому что, опять же, она дала больше всего опухолевой ткани.
Обратите внимание, что это правило кодирования гистологии значительно отличается от правил лечения, которые говорят о кодировании наиболее обширной процедуры. Не путайте и не смешивайте правила кодирования нескольких основных цветов и гистологии с правилами кодирования других частей реферата.
- Взять гистологическую информацию из окончательного диагноза и связанных приложений и комментариев. Это новое правило является большим изменением для опытных регистраторов, которым в прошлом предлагалось кодировать наиболее конкретную гистологию и внимательно читать микроскопическое описание (если оно доступно), чтобы собрать лакомые кусочки данных, которые можно было бы использовать для правильного присвоения гистологического кода. или неправильно.
Причина этого нового правила в том, что в процессе разработки правил патологи из целевой группы заявили, что, документируя микроскопическое описание, они говорят о том, что они видят от слайда к слайду.Когда они просмотрели все слайды, они собрали собранную информацию и использовали свои знания и опыт, чтобы поставить окончательный диагноз. Их комментарий заключался в том, что в микроскопическом описании может быть более конкретный диагноз, но это могла быть небольшая часть образца, видимая только на одном слайде. Из-за этого они решили не включать его в окончательный диагноз, потому что он не был репрезентативным для всего образца; они никогда бы не поставили окончательный диагноз на такой маленькой территории.
Обычно гистологический диагноз является окончательным диагнозом, как написано. Есть несколько исключений:
- В некоторых случаях в окончательном диагнозе может быть указано «см. Комментарий», и в этом случае информация в комментарии или примечании может использоваться для кодирования гистологии.
- Дополнения к окончательному диагнозу, такие как дополнительная информация из отсроченного лабораторного отчета, также могут использоваться для кодирования гистологии.
- Пересмотренный или измененный диагноз заменяет исходный окончательный диагноз, а гистология должна быть закодирована на основе пересмотренного или измененного диагноза.Пересмотренный или измененный диагноз обычно ставится патологоанатомом, который первоначально выписал случай. Если есть заключение патологоанатома, в котором содержится другой диагноз, но первоначальный патолог не исправляет и не пересматривает свой окончательный диагноз, следует закодировать исходный окончательный диагноз.
- В некоторых случаях информация из микроскопического описания может быть использована для определения гистологического кода. Такие случаи будут четко указаны в правилах для конкретных сайтов.Например, для толстой кишки важно знать, что рак развился из уже существующего полипа. Информация о полипе может отсутствовать в окончательном диагнозе, но может быть представлена в виде макроскопического или микроскопического описания.
Прочие документы
- Вторым по важности медицинским документом для кодирования гистологии является отчет цитологического исследования. Если отчета о патологии нет, введите код из отчета цитологического исследования. Цитология во многих случаях менее специфична, чем патология, потому что цитолог смотрит на отдельные клетки, а не на массу опухоли, но, тем не менее, это надежный источник гистологической информации.
- Если нет ни отчета о патологии, ни отчета о цитологии, введите код из медицинской документации, который ссылается либо на патологию, либо на цитологию. Другими словами, если вы видите запись в медицинской карте, в которой говорится, что пациенту была сделана биопсия в офисе до поступления и что биопсия показала аденокарциному, врач ссылается на патологию.
- Самый низкий приоритет — это упоминание в медицинской карте вида рака. Например, это может быть анамнез и физикальное обследование, где есть сведения о том, что у пациента имеется аденокарцинома левого легкого.В медицинской карте упоминается тип или гистология рака, но не делается конкретных ссылок на отчет о патологии или цитологический отчет.
Модули кодирования гистологии
Помня об этих общих правилах о том, где получить гистологическую информацию в медицинской карте, перейдите к разделу «Правила кодирования гистологии» в правильном наборе правил для сайта, который вы рефератируете. Вы заметите, что, подобно модулям в разделе «Правила множественных первичных», есть два отдельных модуля правил кодирования гистологии (за исключением меланомы кожи).
- Одиночная опухоль (один первичный очаг)
- Множественные опухоли выделены как единый первичный сайт
Каждый модуль представляет собой независимый полный набор правил. Правила пронумерованы последовательно, чтобы избежать путаницы, но каждый модуль стоит отдельно.
- Модуль «Одна опухоль» используется, когда у вас есть одно поражение, гистологию которого необходимо закодировать. Единственная опухоль может перекрывать смежные участки, или она может иметь смесь типов клеток, или это может быть смесь инвазивного рака и рака in situ.Все эти вопросы решаются в приоритетах модуля правил «единой опухоли».
- Модуль «Множественные опухоли, абстрагированные как одна первичная» используется, когда правила множественных первичных указали, что множественные опухоли рассматривались как единое целое и должен быть подготовлен только один реферат. (Если в правилах нескольких основных вариантов указано, что вы должны подготовить более одного реферата для случая, с этого момента работайте только с одним рефератом за раз.) Например, правила нескольких основных вариантов говорят, что пациент с множественными злокачественными полипами и В анамнезе семейный полипоз кишечной палочки (наследственное заболевание) является единичным первичным.Чтобы определить гистологический код для этого случая, используйте модуль «Множественные опухоли, выделенные как одна первичная».
Правила кодирования приоритета гистологии
- Как только вы войдете в соответствующий модуль, начните чтение с первого правила в этом модуле.
- Продолжайте читать, пока не найдете правило, применимое к вашему случаю.
- Используйте первое применимое правило и остановитесь. Не пропускайте остальные правила, чтобы узнать, применимо ли другое правило.
Почти всегда первые два правила кодирования гистологии одинаковы в каждом модуле. Правило h2 в модуле «Одна опухоль» и соответствующее первое правило в модуле «Множественные опухоли» подтверждают приоритет гистологической информации, когда нет патологии или цитологического образца (без резекции или биопсии) или когда нет отчета о патологии или цитологии. доступны (биопсия или резекция, выполненные в другом месте): укажите гистологию, задокументированную врачом. Документация может быть в медицинской карте в виде заявления, относящегося к патологическим или цитологическим находкам, в качестве ссылки врача на конкретный тип рака или даже в отчете о КТ, МРТ или ПЭТ.Если в любом из этих источников упоминается конкретная гистология, закодируйте ее так. Если не задокументировано ничего более специфичного, чем «рак» или «карцинома», введите код 8000 Злокачественное новообразование, БДУ или 8010 Карцинома, БДУ, в зависимости от ситуации.
Правило h3 в модуле «Одна опухоль» и соответствующее второе правило в модуле «Множественные опухоли» устанавливают, что допустимо кодировать гистологию из метастатического участка, когда нет патологии или цитологического образца из первичного участка.
Однако почти во всех случаях будет микроскопическое подтверждение опухоли в виде ткани (патология) или жидкостей и клеток (цитология).Реально зависящие от сайта приоритеты имеют приоритет после первых двух базовых правил.
Теория, лежащая в основе приоритезации правил гистологического кодирования, заключается в том, чтобы в первую очередь иметь дело с наиболее распространенными ситуациями. По мере того как правила идут дальше по списку, они применяются к все меньшему количеству случаев. Например, при раке головы и шеи во многих случаях идентифицируется только одна гистология (плоскоклеточная карцинома), независимо от того, охватывает ли реферат одну опухоль или несколько опухолей, выделенных как одну первичную.В таком случае вам нужно только прочитать пару правил, прежде чем вы найдете подходящее («Закодируйте гистологию, когда идентифицирован только один гистологический тип»), и все готово. Если идентифицировано более одного гистологического типа, последующие правила говорят, какой код использовать, когда присутствует как инвазивный, так и in situ рак, когда одна опухоль более инвазивна, чем другая, когда один из типов является более конкретным термином, чем другой, и и так далее в порядке убывания приоритета.
В общем, правил гистологического кодирования намного больше, чем правил множественных основных, потому что для большинства сайтов существует широкий диапазон гистологических кодов на выбор.Многие правила относятся к одному или нескольким конкретным гистологическим кодам. Эти конкретные гистологические коды расположены в соответствии с типами клеток, которые являются наиболее важными с точки зрения прогноза. Например, при карциноме молочной железы in situ неинфильтрирующая комедокарцинома имеет худший прогноз, чем другие типы карциномы in situ, поэтому одним из наиболее приоритетных правил является кодирование случая со смесью внутрипротоковой карциномы и неинфильтрирующей комедокарциномы до 8501. / 2 Неинфильтрирующая комедокарцинома. Таким образом, гистологический код реферата может частично отражать прогноз пациента.
В других наборах правил есть конкретные инструкции, когда и когда не использовать определенные гистологические коды. У патологов есть особые критерии для определения муцинозной опухоли или аденокарциномы из перстневых клеток толстой кишки, аденокарциномы в сравнении с крупноклеточной карциномой в легких или регрессирующей меланомы кожи. Аденокарцинома кишечного типа — это диагноз, который не следует использовать при раке толстой кишки. Правила MPH 2007 года были тщательно разработаны и протестированы, чтобы дать должный приоритет многим гистологиям, которые могут развиваться на данном первичном участке.
В каждом модуле правил кодирования гистологии самое последнее правило «Закодируйте гистологию с более высоким числовым кодом МКБ-О-3» предназначено для охвата любой ситуации, не описанной в правилах с более высоким приоритетом. Это последнее универсальное правило будет применяться очень редко; это также правило «последней инстанции» в МКБ-О-3.
Подготовка образца
Получение достаточного количества ткани и правильное обращение с образцами (которое начинается еще до того, как образец поступает в лабораторию патологии) являются важными компонентами для точной патологической диагностики.В следующем разделе рассматриваются различные типы биопсии, в том числе жидкие биопсии, используемые для взятия образцов опухолей, и важные аспекты фиксации тканей.
Взятие образца опухоли
Хотя многие типы тестов могут использоваться для оценки , указывающих на рака, только биопсия может использоваться для подтверждения диагноза рака.
Методы получения образца опухоли
Биопсия ткани
Биопсия — это удаление небольшого количества ткани для оценки патологии.Цель биопсии ткани — получить диагностическую ткань, минимизируя заболеваемость, ограничивая возможное распространение опухоли и избегая вмешательства в будущие методы лечения.
Игольная биопсия
- Если опухоль пальпируется вблизи поверхности, игла направляется пальпаторно.
- Если опухоль глубже в теле, то игла направляется визуализацией (обычно ультразвуком или компьютерной томографией).
Аспирация тонкой иглой (FNA)
Источник: Shutterstock
- Использует тонкую (обычно калибра 22 или меньше) полую иглу, прикрепленную к шприцу.Используемая игла даже меньше, чем те, которые используются для анализа крови.
- Удаляет отдельные клетки, очень маленькие кусочки опухолевой ткани или жидкости для патологической оценки.
- Несколько проходов FNA можно сделать из одной большой опухоли, чтобы взять образцы из разных срезов.
- В клеточных образцах материал может быть сконцентрирован в клеточном блоке для дополнительных исследований, таких как иммуногистохимия.
- Преимущества: простой, быстрый, малоинвазивный метод, который можно проводить амбулаторно.Он хорошо переносится с низким риском осложнений.
- Ограничения: ошибки отбора проб из-за низкой клеточности или неадекватного отбора проб опухоли.
- Патолог может присутствовать во время процедуры FNA под визуальным контролем. В этом случае аспират FNA немедленно обрабатывается на предметном стекле и окрашивается для предварительного просмотра клеток, чтобы гарантировать получение адекватного образца. Это называется быстрая оценка адекватности на месте .
Биопсия стержневой иглой
Источник: Национальный институт диабета, болезней органов пищеварения и почек, Национальные институты здравоохранения.
.
- Использует полую иглу, которая немного больше той, что используется в FNA.
- Удаляет небольшой цилиндр ткани (около 1/16 дюйма в диаметре и около 1/2 дюйма в длину).
- Менее инвазивно, чем хирургическое вмешательство, но часто требует местной анестезии.
- Преимущества: В большинстве случаев получается больше ткани по сравнению с FNA, что позволяет проводить более подробные дополнительные исследования. Гистологическая архитектура сохранена по сравнению с FNA.
- Ограничения: ограниченный отбор проб и недоступность некоторых масс (в зависимости от размера, глубины, плотности или местоположения).
Хирургическая биопсия
Источник: Национальный институт рака, Линда Бартлетт (фотограф)
- Требуется местная или общая анестезия.
- Более инвазивный, чем биопсия иглы.
- Требуется время восстановления, повышенная заболеваемость и стоимость по сравнению с игольной биопсией.
Послеоперационная биопсия
- Удаляется часть большой опухоли.
- Обычно выполняется только в том случае, если опухоль слишком велика или слишком инвазивна для полного удаления или попытки игольной биопсии не были диагностическими.
- Эксцизионная биопсия — Удаляется вся опухоль или подозрительная область.
Эксцизионная биопсия
- Удаляется вся опухоль или подозрительная область.
- Обычно также удаляется часть окружающей нормальной ткани (так называемый хирургический край).
- Если образец эксцизионной биопсии оказывается злокачественным, патолог исследует хирургический край, чтобы убедиться, что опухоль была удалена полностью. Это определяется на основании того, имеется ли достаточно широкий ободок нормальной ткани вокруг опухоли.
Другие виды биопсий
Цитология соскоба или щетки
- Небольшой шпатель или кисть используется для соскабливания клеток с исследуемой ткани.
- Самый распространенный пример — мазок Папаниколау.
- Другие ткани, обычно отбираемые таким образом, включают пищевод, желудок, бронхи и ротовую полость.
Эндоскопическая биопсия
- Эндоскоп — это тонкая гибкая трубка с подсветкой, на конце которой есть линза или камера.
- Щипцы также могут быть прикреплены к концу трубки и использованы для удаления небольшого образца ткани из подозрительной области, идентифицированной с помощью камеры.
- Эндоскоп используется для визуализации и биопсии различных частей тела, включая нос, носовые пазухи, горло, пищевод, желудок и верхнюю часть кишечника.
- Некоторые эндоскопы называются по-другому, когда они используются в определенной анатомической области. Бронхоскоп используется для визуализации и биопсии легких и бронхов. Колоноскоп используется для визуализации и биопсии толстой и прямой кишки. Лапараскоп используется для визуализации и биопсии брюшной полости.
Аспирация и биопсия костного мозга
- Используется для диагностики гематологического рака, включая лимфому, лейкоз и множественную миелому.
- Обычно выполняется одновременно с исследованием костного мозга.
- Аспирация костного мозга используется для отбора небольшого количества жидкого компонента костного мозга. Биопсия костного мозга используется для удаления небольшого количества твердого тканевого компонента костного мозга.
- В кость воткнута широкая игла. Образец жидкой части удаляется с помощью шприца, прикрепленного к игле. Затем игла вращается, чтобы удалить образец кости.
- Чаще всего выполняется на тазовой кости.
Картирование и биопсия сторожевых лимфатических узлов
- Названные дозорные лимфатические узлы, потому что они «наблюдают» за опухолью. Это лимфатические узлы, отводящие лимфатическую жидкость из опухолевой ткани. Сторожевой лимфатический узел определяется как первый узел или группа узлов, в которые раковые клетки с наибольшей вероятностью распространятся из первичной опухоли. Биопсия сторожевого лимфатического узла чаще всего используется для определения стадии рака груди и злокачественной меланомы, но ее применяли при различных типах рака.
- Картирование включает использование цветного красителя и / или радиоактивного материала для отслеживания путей оттока лимфы из опухоли с целью идентификации сторожевого узла (ов).
- Сторожевые узлы затем удаляются и исследуются под микроскопом, чтобы определить, содержат ли они раковые клетки. Отрицательный результат биопсии сигнальных лимфатических узлов свидетельствует о том, что рак не распространился на региональные лимфатические узлы или другие органы. Если сторожевые лимфатические узлы отрицательны, то дополнительные региональные лимфатические узлы не удаляются во время операции, потому что опухоль еще не метастазировала в лимфатические узлы.При обнаружении раковых клеток оставшиеся лимфатические узлы в этой области могут быть удалены в процессе, называемом диссекцией лимфатических узлов .
Жидкая биопсия
Технология жидкостной биопсии — быстро развивающаяся область. Терминология «жидкая биопсия» возникла потому, что мы быстро движемся в эпоху, когда некоторые из традиционных оценок, проводимых с помощью биопсии ткани (например, тестирование молекулярных маркеров), теперь могут быть выполнены в крови, моче или другой жидкости организма, которая является менее инвазивной, чем биопсия ткани.В настоящее время около 40 компаний разработали анализы для обнаружения внеклеточной циркулирующей ДНК (вкДНК), циркулирующей опухолевой ДНК (цтДНК) или циркулирующих опухолевых клеток (ЦКО).
Опухоли выделяют клетки (СТК) в кровоток, которые можно выделить для анализа. Проблема в том, что опухолевых клеток очень мало, но их выделение для анализа дает ряд преимуществ. Наиболее очевидным преимуществом является то, что пациенту не нужно будет проходить процедуру инвазивной биопсии, а только будет взят образец крови.Это позволяет упростить серийный анализ с течением времени для отслеживания изменений опухоли, чтобы лучше направлять изменения в терапии по мере прогрессирования опухоли. Кроме того, опухоли неоднородны, что затрудняет получение молекулярного представления опухоли из небольшого образца биопсии (например, из тонкоигольной аспирации или биопсии стержневой иглой). Лечение пациента с опухолью на основе анализа небольшой биопсии может привести к эффективному нацеливанию только на часть клеток. Использование ЦКО позволяет лучше представить гетерогенность опухоли, поскольку клетки могут поступать из нескольких мест внутри опухоли, а также из нескольких опухолей в случае метастатического заболевания.Исследования показали, что количество ЦОК отражает состояние болезни — чем больше ЦКО, тем больше заболевание. Выделенные циркулирующие опухолевые клетки также можно секвенировать индивидуально или в группе для определения действенных мишеней для лечения. Несколько компаний, например CellSearch, Biocept и др., Внедрили анализ ЦОК на коммерческую основу. Проблемой при использовании ЦОК для диагностики является их небольшое количество в крови в любое время. Хотя эти цифры увеличиваются при метастатическом состоянии, их все еще мало по сравнению с количеством красных и белых кровяных телец.Компании разработали собственные методы сбора для стабилизации CTCS в образцах, отправленных им на ночь для изоляции по прибытии в лабораторию. Для улучшения этого подхода необходимы дальнейшие исследования.
Умирающие клетки выделяют ДНК в кровоток (вкДНК). Опухолевые клетки тоже делают это (втДНК), но обычно в крови обнаруживается лишь небольшая часть общей ДНК. Количество опухолевой ДНК, обнаруженной в крови, обычно коррелирует со стадией, увеличиваясь со стадией и количеством метастазов.Различные компании используют несколько подходов для молекулярного анализа ктДНК, но наиболее часто используются полимеразная цепная реакция или секвенирование следующего поколения для выявления молекулярных изменений в ДНК. Те же преимущества выделения ЦОК для анализа по сравнению с биопсией применимы к цТДНК, но часто можно получить более высокие количества цТДНК, чем ЦОК.
В настоящее время несколько компаний расширяют понятие жидкой биопсии, используя другие жидкости организма, такие как моча и спинномозговая жидкость (при опухолях и метастазах головного мозга).Моча представляет собой интересный вариант, если он окажется успешным, потому что образец может быть собран дома и отправлен пациентом, что является наиболее удобным и наименее инвазивным вариантом из всех. Для получения дополнительной информации см. Раздел «Жидкие биопсии».
Вафик Эль-Дейри, доктор медицины, обсуждает плюсы и минусы биопсии ткани и жидкости.
Сравнение тканевых и жидких биопсий
Сокращения: ЦКО, циркулирующая опухолевая клетка; втДНК, циркулирующая опухолевая ДНК; EGFR, рецептор эпидермального фактора роста.
Тканевая фиксация
Фиксация ткани служит нескольким целям во время патологической оценки образцов. Фиксация сохраняет ткань, предотвращая автолиз клеточными ферментами, помогает предотвратить разложение ткани бактериями и плесенью, укрепляет ткань, облегчая рассечение, инактивирует инфекционные агенты и повышает жадность тканей к красителям. Фиксация также оказывает нежелательное воздействие на ткань, такое как изменение структуры белка (потеря антигенности), потеря растворимых компонентов ткани и деградация ДНК и РНК.
Типы фиксаторов
- Формалин: Стандартный фиксатор, используемый в лаборатории патологии, представляет собой 10% -ный формалин с фосфатным буфером. Он хорошо фиксирует большинство тканей и совместим с большинством дополнительных тестов, таких как иммуногистохимия и молекулярные тесты.
- Раствор Bouin (пикриновая кислота, формальдегид и уксусная кислота): Фиксация в растворе Bouin приводит к резкому окрашиванию гематоксилином и эозином, что отдается предпочтениям некоторых патологов.К недостаткам можно отнести пониженную чувствительность иммуногистохимических тестов и повышенную деградацию ДНК и РНК пикриновой кислотой.
- B5 (хлорид ртути, ацетат натрия и формалин): B5 часто используется для рутинной фиксации лимфатических узлов, селезенки и других тканей при подозрении на лимфопролиферативный процесс. B5 обеспечивает быструю фиксацию с превосходными цитологическими данными и сохранением антигена для лимфоидных маркеров. Ткань может стать хрупкой, если происходит чрезмерная фиксация B5, и необходимы специальные процедуры для удаления из-за присутствия ртути.
- Глутаральдегид: Фиксирующий глутаральдегид используется для ткани, которая должна быть оценена с помощью электронной микроскопии.
Создание фиксированных формалином залитых парафином тканевых блоков
После соответствующей фиксации ткань в виде блоков помещается в процессор, который обезвоживает ткань через серию градуированных спиртовых ванн и пропитывает ткань парафиновым воском, в результате чего образуется формалин -фиксированный тканевый блок, залитый парафином. Затем ткань из этих блоков разрезается на тонкие (0.От 4 мкм до 0,5 мкм) с помощью микротома и поместили на предметное стекло. Ткань на предметных стеклах окрашивается гематоксилином и эозином и закрывается покровным стеклом перед осмотром патологоанатома.
Влияние времени на фиксацию
Несколько факторов, связанных с фиксацией ткани, могут повлиять на результаты дополнительных исследований, таких как иммуногистохимические и молекулярные тесты. Автолиз начинается сразу после удаления ткани у пациента. Хотя автолиз можно уменьшить путем охлаждения, задержки перед фиксацией могут отрицательно повлиять на диагностическое качество ткани.Время между извлечением образца из организма пациента и его контактом с формалином называется временем холодовой ишемии. Увеличенное время холодовой ишемии (более 1 часа) может привести к ложноотрицательному анализу на такие маркеры, как рецептор эстрогена, рецептор прогестерона и HER-2. Важно, чтобы образцы доставлялись в лабораторию своевременно, чтобы избежать увеличения времени холодовой ишемии. Считается, что адекватное количество фиксатора в контейнере для образца в 15-20 раз превышает объем ткани.Однако даже за это короткое время происходят изменения в фосфорилировании важных белков (было отмечено как увеличение, так и уменьшение на определенных участках).
Процесс фиксации — это химическая реакция, которая обычно требует минимум 6 часов (даже для небольших биоптатов) для достижения достаточной фиксации ткани. Определенные типы тканей, например, содержащие большое количество жировой ткани, и более крупные образцы требуют более длительного времени фиксации. Более крупные ткани после резекции также могут потребовать вскрытия, чтобы фиксатор мог проникнуть во все области и обеспечить равномерную фиксацию.Как недостаточная фиксация, так и чрезмерная фиксация ткани могут привести к потере антигенности и деградации РНК и ДНК. Существуют специальные рекомендации ASCO / Коллегии американских патологов по фиксации образцов молочной железы для сохранения антигенности ткани в отношении рецепторов гормонов и тестирования HER-2.
