Беременность и трихомониаз: Трихомониаз
Особенности трихомонадной инфекции у беременных и новорожденных: клиника и лечение
Трихомониаз — одно из наиболее частых заболеваний, передающихся половым путем. В мире ежегодно регистрируется около 170 млн случаев инфицирования мужчин и женщин трихомонадами, в Украине — в среднем около 250 тыс. больных в год [1–9].
Несмотря на интенсивное изучение этой урогенитальной инфекции, у нас в стране нет достаточных сведений и обобщающих данных о закономерностях ее распространения, формах проявления у беременных женщин и рожденных ими детей. По разным оценкам, трихомониаз у женщин детородного возраста колеблется в пределах 30 %. В России трихомониаз беременных обнаруживают в 0,98–32 %, в тропических странах — до 40 %, а угроза прерывания беременности отмечается в 36,7 % случаев. Примерно 5 % детей, родившихся oт инфицированных матерей, Т.vaginalis заражаются интранатально. В Украине среди детей ежегодно регистрируется около 500 случаев трихомониаза в возрастной группе от 0 до 14 лет и около 4 тыс. случаев — у детей от 15 до 17 лет. В России трихомониаз у детей, преимущественно у девочек, выявляют в 0,12 % от уровня общей заболеваемости. Больные девочки от матерей с урогенитальным трихомониазом, по разным источникам, составляют около 23 %. Среди девочек до 12 лет с трихомониазом заболевание среди их матерей обнаруживают у 94,3 %. Распространенность трихомониаза в группе детей до 12 лет с половыми контактами в анамнезе колеблется в пределах от 0 до 19,2 %. Заражение детей контактно-бытовым путем при трихомониазе составляет 26,1 % [1, 2, 4, 6, 8, 16–18].
случаев — у детей от 15 до 17 лет. В России трихомониаз у детей, преимущественно у девочек, выявляют в 0,12 % от уровня общей заболеваемости. Больные девочки от матерей с урогенитальным трихомониазом, по разным источникам, составляют около 23 %. Среди девочек до 12 лет с трихомониазом заболевание среди их матерей обнаруживают у 94,3 %. Распространенность трихомониаза в группе детей до 12 лет с половыми контактами в анамнезе колеблется в пределах от 0 до 19,2 %. Заражение детей контактно-бытовым путем при трихомониазе составляет 26,1 % [1, 2, 4, 6, 8, 16–18].
Мочеполовой трихомониаз является многоочаговым заболеванием, при котором урогенитальные трихомонады могут локализоваться во всех мочеполовых органах, однако не исключается их экстрагенитальное обнаружение: в верхнечелюстной пазухе (гайморовой), лакунах и глоточных миндалинах, в конъюнктиве, ушных раковинах, в прямой кишке, а также в легких новорожденных. Наиболее частым проявлением трихомониаза у женщин являются вагиниты, вульвиты, уретриты, циститы, бартолиниты, эндоцервициты, эрозии шейки матки, эндометриты, аднекситы, что увеличивает риск развития бесплодия и рака шейки матки [1, 4, 8].
В то же время роль трихомонад в патологии беременных, рожениц, родильниц, плода и новорожденных изучена недостаточно. Впервые у родильниц урогенитальные трихомонады были выявлены И.П. Лазаревичем в 1870 г. в послеродовом периоде без клинических проявлений. Трихомонадная инфекция у беременных — многоочаговое заболевание, при котором инфицируются мочеиспускательный канал, нередко мочевой пузырь, вульва, влагалище и прямая кишка. Возможность трихомонадной инвазии внутренних половых органов зависит от срока беременности, в который произошло инфицирование. С одной стороны, все анатомо-физиологические процессы, происходящие во время беременности, направлены на защиту плода от восходящей инфекции: резко возрастает активность материнских иммунных механизмов, включая стимуляцию фагоцитарного ответа; формируются дополнительные защитно-биологические барьеры; меняется характер цервикальной слизи, она становится вязкой, труднопроходимой для инфекционных агентов. Начиная с 16-й недели функционирует второй барьер — хориоамниотические оболочки, которые закрывают внутренний маточный зев канала шейки матки. Следует учитывать и то, что послед также выполняет весьма сложные и многообразные функции барьерного органа и является своеобразным экстракорпоральным органом иммунитета плода. С другой стороны, защитные oт инфекции механизмы во время беременности ослабевают, особенно к ее концу (39–40-я неделя) [8, 12, 17].
Следует учитывать и то, что послед также выполняет весьма сложные и многообразные функции барьерного органа и является своеобразным экстракорпоральным органом иммунитета плода. С другой стороны, защитные oт инфекции механизмы во время беременности ослабевают, особенно к ее концу (39–40-я неделя) [8, 12, 17].
Нередко беременность в случае заражения трихомонадами до формирования хориоамниотических оболочек прерывается в результате самопроизвольного выкидыша или мертворождения. Если заражение трихомониазом произошло позже, восходящая инфекция развивается редко. Внутренний зев шейки матки является своего рода границей распространения урогенитальных трихомонад вверх благодаря циркуляторному сжатию мускулатуры шейки матки и резко щелочной реакции секрета эндометрия. Трихомонады, проявляя себя как тканевые паразиты, вызывают деструкцию и метаплазию эпителия и тканей. Возможно, такой механизм играет существенную роль в процессе преждевременного разрыва околоплодных оболочек у рожениц, провоцируя тем самым преждевременные роды и рождение детей с низкой массой тела. Физиологические входные ворота для инфекционного процесса в послеродовом периоде — это отторжение децидуальной оболочки. Заражение трихомониазом в послеродовом периоде приводит к инфицированию сразу нескольких отделов мочеполовой системы, включая нижний отдел прямой кишки. Нередко диагностируют эндомиометриты, сальпингиты, циститы, возможен тазовый перитонит. Урогенитальный трихомониаз беременных представляет собой большей частью смешанный протозойно-бактериальный процесс с частым присоединением грибковой инфекции [1–4, 8, 12, 17].
Физиологические входные ворота для инфекционного процесса в послеродовом периоде — это отторжение децидуальной оболочки. Заражение трихомониазом в послеродовом периоде приводит к инфицированию сразу нескольких отделов мочеполовой системы, включая нижний отдел прямой кишки. Нередко диагностируют эндомиометриты, сальпингиты, циститы, возможен тазовый перитонит. Урогенитальный трихомониаз беременных представляет собой большей частью смешанный протозойно-бактериальный процесс с частым присоединением грибковой инфекции [1–4, 8, 12, 17].
Имеющиеся недостаточные и противоречивые данные литературы не дают четкого представления об особенностях реализации трихомониаза у рожденных от инфицированных матерей детей в период новорожденности и более старшем возрасте. В силу анатомо-физиологических особенностей детского организма заболеваемость трихомониазом и его течение зависят от пола (преимущественно болеют девочки) и возраста ребенка. Эта проблема более изучена у девочек. Инфицирование новорожденных трихомонадами происходит во время прохождения ребенка через родовые пути матери (интранатально), чаще всего при преждевременном разрыве плодных оболочек и по мере удлинения безводного промежутка, или бытовым путем через предметы обихода (общая постель, предметы туалета и т. п.). Возможны семейные очаги. Некоторые авторы допускают возможность проникновения урогенитальных трихомонад в полость матки, в том числе и гематогенным путем. Данных о внутриутробном заражении плода нет, хотя в литературе имеются единичные сообщения о влиянии трихомонад на его развитие, а также обнаружение Т.vaginalis в околоплодной жидкости и легких новорожденных [1, 3–8, 17].
п.). Возможны семейные очаги. Некоторые авторы допускают возможность проникновения урогенитальных трихомонад в полость матки, в том числе и гематогенным путем. Данных о внутриутробном заражении плода нет, хотя в литературе имеются единичные сообщения о влиянии трихомонад на его развитие, а также обнаружение Т.vaginalis в околоплодной жидкости и легких новорожденных [1, 3–8, 17].
Некоторые авторы считают, что заболеваемость трихомониазом у детей в период новорожденности и первых двух лет жизни невысока, что объясняется, в частности, у девочек особенностями эпителиального покрова вульвы и влагалища, не содержащего гликоген в достаточном количестве, транзиторной экстрагенизацией, и даже допускают спонтанное излечивание. Однако паразиты иногда долго сохраняются в цервикальном канале девочек (от 3 до 9 мес.). Наиболее частая локализация манифестной трихомонадной инфекции у детей — наружные половые органы и влагалище (у девочек), реже мочеиспускательный канал и прямая кишка. В среднем на долю трихомонадного вульвовагинита у детей приходится от 0,8 до 3,8 % случаев.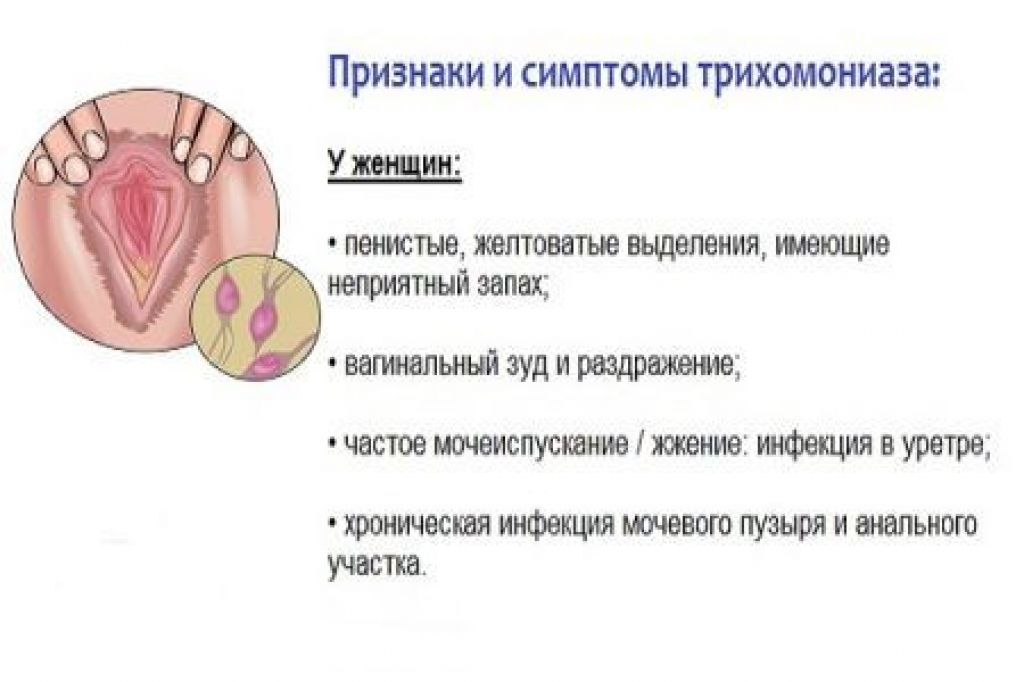 У новорожденных девочек в возрасте до 2–3 недель практически не встречаются ярко выраженные симптомы вульвовагинита, что, очевидно, связано с влиянием материнских эстрогенов, приводящих к «самоочищению» влагалища, а также с участием материнских антител, прошедших через плацентарный барьер. Начиная с возраста 3–4 недель трихомонадный вульвовагинит протекает остро, с выраженными признаками воспаления. Наблюдаются яркая гиперемия, отек слизистой оболочки области наружных половых органов, гименального кольца. Характерны обильные желто-зеленые пенистые гноевидные выделения, которые раздражают кожу промежности и бедер. Дети возбуждены, беспокойны, отказываются от еды [1, 6, 8, 15, 16].
У новорожденных девочек в возрасте до 2–3 недель практически не встречаются ярко выраженные симптомы вульвовагинита, что, очевидно, связано с влиянием материнских эстрогенов, приводящих к «самоочищению» влагалища, а также с участием материнских антител, прошедших через плацентарный барьер. Начиная с возраста 3–4 недель трихомонадный вульвовагинит протекает остро, с выраженными признаками воспаления. Наблюдаются яркая гиперемия, отек слизистой оболочки области наружных половых органов, гименального кольца. Характерны обильные желто-зеленые пенистые гноевидные выделения, которые раздражают кожу промежности и бедер. Дети возбуждены, беспокойны, отказываются от еды [1, 6, 8, 15, 16].
Дети младшего возраста, не живущие половой жизнью, инфицируются трихомонадами, как правило, в очагах семейного трихомониаза, а также при попытке физического насилия над ними. Чаще у девочек в возрасте 3–8 лет развивается трихомонадный вульвовагинит. В отличие от слизистой оболочки влагалища взрослой женщины, где имеется многослойный ороговевший эпителий, препятствующий внедрению урогенитальных трихомонад, у девочек нежный мягкий эпителий со щелочной реакцией влагалища легко доступен для поражений простейшими. В этом возрасте чаще встречаются выраженные субъективные симптомы. Превалирующие жалобы: выделения из половых путей, зуд, жжение; болезненность в области вульвы встречается лишь у половины больных. Вульвовагиниты характеризуются гиперемией и отечностью вульвы, слизистой оболочки влагалища, выраженных в разной степени в зависимости от течения воспалительного процесса. При острой форме — гиперемия яркая, «сочная», отечность значительная, площадь распространения более обширная, с переходом на область промежности, паховых и пахово-бедренных складок, с возможным развитием эрозивных форм. При развитии у детей острого трихомонадного уретрита губки уретры отечны, гиперемированы, при надавливании на них появляется гнойная капля. Болезненное мочеиспускание беспокоит только половину пациентов с острым течением воспалительного процесса и около 5 % — с хроническим. Считается, что постоянный зуд половых органов у детей при трихомониазе может приводить к инфицированию их рук, с последующим заносом этих простейших в полость носа, глаз и ушей [1, 5, 6, 11, 15, 18].
В этом возрасте чаще встречаются выраженные субъективные симптомы. Превалирующие жалобы: выделения из половых путей, зуд, жжение; болезненность в области вульвы встречается лишь у половины больных. Вульвовагиниты характеризуются гиперемией и отечностью вульвы, слизистой оболочки влагалища, выраженных в разной степени в зависимости от течения воспалительного процесса. При острой форме — гиперемия яркая, «сочная», отечность значительная, площадь распространения более обширная, с переходом на область промежности, паховых и пахово-бедренных складок, с возможным развитием эрозивных форм. При развитии у детей острого трихомонадного уретрита губки уретры отечны, гиперемированы, при надавливании на них появляется гнойная капля. Болезненное мочеиспускание беспокоит только половину пациентов с острым течением воспалительного процесса и около 5 % — с хроническим. Считается, что постоянный зуд половых органов у детей при трихомониазе может приводить к инфицированию их рук, с последующим заносом этих простейших в полость носа, глаз и ушей [1, 5, 6, 11, 15, 18].
Самые высокие показатели заболеваемости трихомониазом у детей отмечаются в пубертатном возрасте. В Украине регистрируется около 4 тыс. случаев в год, причем девочки болеют в 7,5 раза чаще. Заражение в большинстве случаев происходит половым путем, хотя нельзя полностью исключать варианты бытового заражения. Особенность течения трихомониаза в этом возрастном периоде заключается в снижении общей способности к ограничению воспалительного очага, обусловленном дисбалансом иммунной системы на фоне пика роста и дифференцировки всех тканей детского организма, а также началом активной половой жизни. У девочек в этом периоде резко возрастает активность яичников, повышается уровень эстрогенов в крови, претерпевает физиологические изменения эпителий влагалища, происходит накопление гликогена, необходимого для обеспечения процессов жизнедеятельности влагалищных трихомонад. Течение трихомонадного вульвовагинита, как правило, острое, с выраженными клиническими признаками воспаления. В воспалительный процесс вовлечен эктоцервикс, эндоцервикс в пубертатном возрасте крайне редко вовлекается в инфекционный процесс в связи с узостью внутреннего и наружного маточного зева. Однако воспаление быстро распространяется на другие отделы мочеполовой системы — уретру и мочевой пузырь, ампулу прямой кишки, инфицируются бартолиновы железы и железы Skene. При хронизации воспалительного процесса в области половых органов могут развиваться нарушения менструального цикла, поражения матки и придатков, угрожающие правильному становлению репродуктивной функции девочки в будущем [1, 5, 6, 11, 15, 18].
Однако воспаление быстро распространяется на другие отделы мочеполовой системы — уретру и мочевой пузырь, ампулу прямой кишки, инфицируются бартолиновы железы и железы Skene. При хронизации воспалительного процесса в области половых органов могут развиваться нарушения менструального цикла, поражения матки и придатков, угрожающие правильному становлению репродуктивной функции девочки в будущем [1, 5, 6, 11, 15, 18].
В силу анатомо-физиологических процессов периода беременности, родов, а также возрастных особенностей детского организма клинические проявления не являются надежными критериями для верификации диагноза трихомонадной инфекции. Залог успешной диагностики трихомониаза — сочетание различных методик, как классических, так и альтернативных (микроскопический, культуральный, серологический методы, метод молекулярной генетики). Микроскопический метод считается отборочным со специфичностью 36 % и базируется на обнаружении Т.vaginalis в нативных или окрашенных препаратах. Культуральный метод — золотой стандарт, наиболее приемлем для верификации диагноза у беременных и обязателен для детей, так как является высокочувствительным и специфичным (более 90 %). К существенным недостаткам его применения у данного контингента больных относится длительный период инкубации (до 17 дней), что препятствует необходимости наиболее раннего выявления и санирования инфекции. Серологический метод диагностики для определения антитрихомонадных антител не получил практического применения в качестве скринингового теста для беременных и их новорожденных. Реакции дают высокий процент ложноположительных результатов из-за наличия нескольких сероваров трихомонад, низкого уровня иммунного ответа, длительного сохранения положительных серологических реакций у излечившихся. Весьма перспективным, но требующим дальнейшей разработки может стать метод флюоресцентного иммуноферментного анализа (ИФА) с использованием моноклональных антител к различным структурам простейших для прямого выявления антигенов Т.
Культуральный метод — золотой стандарт, наиболее приемлем для верификации диагноза у беременных и обязателен для детей, так как является высокочувствительным и специфичным (более 90 %). К существенным недостаткам его применения у данного контингента больных относится длительный период инкубации (до 17 дней), что препятствует необходимости наиболее раннего выявления и санирования инфекции. Серологический метод диагностики для определения антитрихомонадных антител не получил практического применения в качестве скринингового теста для беременных и их новорожденных. Реакции дают высокий процент ложноположительных результатов из-за наличия нескольких сероваров трихомонад, низкого уровня иммунного ответа, длительного сохранения положительных серологических реакций у излечившихся. Весьма перспективным, но требующим дальнейшей разработки может стать метод флюоресцентного иммуноферментного анализа (ИФА) с использованием моноклональных антител к различным структурам простейших для прямого выявления антигенов Т. vaginalis в соскобах слизистых оболочек. Считается, что эти тест-системы обладают чувствительностью, аналогичной таковой при использовании культурального метода, что допускает их применение в качестве отборочного теста у беременных, рожениц и дальнейшего обследования их новорожденных детей. Также активно внедряется в практику и метод молекулярной генетики (ПЦР-анализ, ДНК-гибридизация и др.). Для данного контингента пациентов востребованы основные преимущества метода: высокая чувствительность (97 %) и специфичность (98 %), прямая детекция возбудителя, идентификация единичных микроорганизмов, в частности погибших, частично разрушенных или подвергнутых фиксации, быстрое получение результатов и возможность одновременного выявления в биопробе нескольких возбудителей [1, 6–9, 10, 13, 15, 18].
vaginalis в соскобах слизистых оболочек. Считается, что эти тест-системы обладают чувствительностью, аналогичной таковой при использовании культурального метода, что допускает их применение в качестве отборочного теста у беременных, рожениц и дальнейшего обследования их новорожденных детей. Также активно внедряется в практику и метод молекулярной генетики (ПЦР-анализ, ДНК-гибридизация и др.). Для данного контингента пациентов востребованы основные преимущества метода: высокая чувствительность (97 %) и специфичность (98 %), прямая детекция возбудителя, идентификация единичных микроорганизмов, в частности погибших, частично разрушенных или подвергнутых фиксации, быстрое получение результатов и возможность одновременного выявления в биопробе нескольких возбудителей [1, 6–9, 10, 13, 15, 18].
Исследования последних лет свидетельствуют об обоснованности и необходимости лечения трихомониаза в период беременности, так как своевременно назначенная специфическая терапия приводит к клинико-этиологическому излечению, санации родовых путей, нормальному течению беременности, родов и послеродового периода, а также рождению здорового ребенка. Однако терапия трихомониаза во время беременности остается сложной проблемой из-за возможного неблагоприятного воздействия этиотропных препаратов на плод. В доступной нам литературе нет сообщений о лечении трихомонадной инфекции в I триместре беременности в период органогенеза и плацентации, что связано с недостаточной информацией об отсутствии тератогенного действия этиотропных препаратов на эмбрион. В то же время лечение трихомониаза в ранние сроки беременности, родов и послеродовом периоде необходимо. Поэтому поиск эффективных и безопасных для эмбриона препаратов является актуальной задачей современной фармакологии. В I триместре рекомендуют ежедневное смазывание мочеиспускательного канала и влагалища 4% водным раствором метиленового синего, бриллиантового зеленого или раствором марганцового калия (1 : 10 000). Во II триместре беременности при местном лечении допустимо применение вагинальных свечей с метронидазолом, клотримазолом, комбинированных препаратов (мератин комби, тержинан и др.
Однако терапия трихомониаза во время беременности остается сложной проблемой из-за возможного неблагоприятного воздействия этиотропных препаратов на плод. В доступной нам литературе нет сообщений о лечении трихомонадной инфекции в I триместре беременности в период органогенеза и плацентации, что связано с недостаточной информацией об отсутствии тератогенного действия этиотропных препаратов на эмбрион. В то же время лечение трихомониаза в ранние сроки беременности, родов и послеродовом периоде необходимо. Поэтому поиск эффективных и безопасных для эмбриона препаратов является актуальной задачей современной фармакологии. В I триместре рекомендуют ежедневное смазывание мочеиспускательного канала и влагалища 4% водным раствором метиленового синего, бриллиантового зеленого или раствором марганцового калия (1 : 10 000). Во II триместре беременности при местном лечении допустимо применение вагинальных свечей с метронидазолом, клотримазолом, комбинированных препаратов (мератин комби, тержинан и др. ) в течение 10 дней, так как в этом периоде уже развиваются окислительно-восстановительные реакции плода, связанные с инактивацией лекарственных средств. Лечение метронидазолом перорально можно назначать только в III триместре беременности. Однако при его назначении необходимо учитывать характерные для беременности снижение дезинтоксикационной и выделительной функций почек, замедление метаболизма и выведения химических соединений из организма. Метронидазол во время беременности назначают по 0,25 г 2 раза в сутки в течение 8 дней (курсовая доза 3–4 г). Обязательному лечению подлежат источники заражения и контакты [1, 7, 8, 10, 11, 13].
) в течение 10 дней, так как в этом периоде уже развиваются окислительно-восстановительные реакции плода, связанные с инактивацией лекарственных средств. Лечение метронидазолом перорально можно назначать только в III триместре беременности. Однако при его назначении необходимо учитывать характерные для беременности снижение дезинтоксикационной и выделительной функций почек, замедление метаболизма и выведения химических соединений из организма. Метронидазол во время беременности назначают по 0,25 г 2 раза в сутки в течение 8 дней (курсовая доза 3–4 г). Обязательному лечению подлежат источники заражения и контакты [1, 7, 8, 10, 11, 13].
В силу анатомо-физиологических особенностей детского организма лечение трихомониаза у детей зависит от пола и возраста инфицированного ребенка и представляет собой до конца не разрешенную задачу. Лечение новорожденных девочек, согласно приказу МЗ Украины № 286, заключается в механическом извлечении трихомонад путем промывания влагалища через тонкий катетер настоем ромашки, шалфея, раствором фурацилина. Положительный результат санирования детей старшего возраста может быть получен только при назначении системных препаратов — производных имидазола. Местное лечение девочек (теплые сидячие ванночки и промывание влагалища настоем ромашки, шалфея, раствором марганцовокислого калия) носит лишь вспомогательный характер. Согласно методическим материалам по лечению трихомонадной инфекции (Украина, 2004 г.; Россия, 2001 г.), рекомендуемым препаратом для лечения детей до 12 лет (с массой тела до 45 кг) является орнидазол в суточной дозе 25 мг/кг за 1 прием перорально в течение 5–10 дней. Этиологическая эффективность лечения орнидазолом детей, страдающих трихомониазом, составляет 95–97 %. Тинидазол принимают в дозе 50–60 мг/кг массы тела 1 раз в сутки перорально в течение 3–5 дней. Метронидазол назначают в суточной дозе 15 мг/кг, разделенной на 2 приема, в течение 7–10 дней. Для детей старше 12 лет (с массой тела больше 45 кг) используют схемы лечения для взрослых. При осложненном трихомониазе назначают лечение как и при неосложненном, однако курс должен составлять не менее 14 дней.
Положительный результат санирования детей старшего возраста может быть получен только при назначении системных препаратов — производных имидазола. Местное лечение девочек (теплые сидячие ванночки и промывание влагалища настоем ромашки, шалфея, раствором марганцовокислого калия) носит лишь вспомогательный характер. Согласно методическим материалам по лечению трихомонадной инфекции (Украина, 2004 г.; Россия, 2001 г.), рекомендуемым препаратом для лечения детей до 12 лет (с массой тела до 45 кг) является орнидазол в суточной дозе 25 мг/кг за 1 прием перорально в течение 5–10 дней. Этиологическая эффективность лечения орнидазолом детей, страдающих трихомониазом, составляет 95–97 %. Тинидазол принимают в дозе 50–60 мг/кг массы тела 1 раз в сутки перорально в течение 3–5 дней. Метронидазол назначают в суточной дозе 15 мг/кг, разделенной на 2 приема, в течение 7–10 дней. Для детей старше 12 лет (с массой тела больше 45 кг) используют схемы лечения для взрослых. При осложненном трихомониазе назначают лечение как и при неосложненном, однако курс должен составлять не менее 14 дней. Клинико-лабораторный контроль излеченности мочеполового трихомониаза проводят через 7–10 дней после завершения лечения протистоцидными препаратами с помощью микроскопического и культурального методов исследования. Пациенты находятся на диспансерном наблюдении в течение 3 месяцев. Контрольные обследования переболевших детей проводят ежемесячно в течение 2 месяцев, с обязательным использованием культурального метода диагностики [1–3, 6–8, 12, 15].
Клинико-лабораторный контроль излеченности мочеполового трихомониаза проводят через 7–10 дней после завершения лечения протистоцидными препаратами с помощью микроскопического и культурального методов исследования. Пациенты находятся на диспансерном наблюдении в течение 3 месяцев. Контрольные обследования переболевших детей проводят ежемесячно в течение 2 месяцев, с обязательным использованием культурального метода диагностики [1–3, 6–8, 12, 15].
Для профилактики неонатальных заболеваний, снижения частоты трихомонадных поражений среди беременных, новорожденных, детей раннего и подросткового возраста применяют организационные формы, принципы общих и индивидуальных лечебно-профилактических мероприятий, как и при других инфекциях, приобретенных половым путем. С учетом своеобразия этиопатогенеза и эпидемиологических особенностей данного контингента мероприятия включают: устранение факторов риска и предупреждение инфицирования; раннее выявление на этапе планирования беременности с формированием групп риска; лечение заболевших и половых партнеров для предотвращения прогрессирования болезни и неблагоприятного влияния на исход беременности; определение групп перинатального риска и обеспечение их репродуктивного здоровья [1, 5, 6, 11, 15, 18].
Таким образом, изучение проблемы урогенитального трихомониаза в системе «мать — ребенок» будет способствовать разработке и внедрению в практику оптимальных методов диагностики и терапии, что позволит снизить уровень заболеваемости, а также совершенствовать профилактические мероприятия по предупреждению и распространению инфекций, передающихся половым путем, среди родителей и их детей.
Список літератури
1. Дмитриев Г.А., Сюч Н.Н. Мочеполовой трихомониаз. — М., 2005 — 128 с.
2. Иванов О.Л. Кожные и венерические болезни. — М.: Медицина, 1997. — 352 с.
3. Казначеев В.П., Непомнящих Г.М. Мысли о проблемах общей патологии на рубеже XXI века / НИИ общей патологии и экологии человека НЦ КЗМ СО РАМН; НИИ региональной патологии и патоморфологии НЦ КЗМ СОРАМН. — Новосибирск, 2000. — 47 с.
4. Клименко Б.В., Авазов З.Р., Барановская В.Б., Степанова М.С. Трихомониаз мужчин, женщин и детей. — СПб.: Питер, 2001. — 134 с.
5. Коколина В.Н. Гинекология детского возраста. — М.: Медпрактика, 2003. — 268 с.
Коколина В.Н. Гинекология детского возраста. — М.: Медпрактика, 2003. — 268 с.
6. Кисина Б.И. Урогенитальные инфекции, передаваемые половым путем, у детей: клинические аспекты диагностики и лечение // Лечащий врач. — 2004. — № 5.
7. Мавров Г.И., Никитенко И.Н., Клетной А.Г. Проблема трихомониаза (современные подходы к диагностике, этиотропной и патогенетической терапии // Дерматологія та венерологія. — 2003. — № 2(20). — С. 7-11.
8. Мавров Г.Л., Степаненко B.I., Чинов Г.А. та ін. Урогенітальний трихомоніаз: новітні підходи до дiагностики i лікування (методичні рекомендації). — К., 2004. — 22 с.
9. Мавров И.И. Половые болезни: Руководство для врачей, интернов и студентов. — Харьков: Факт, 2002. — 783 с.
10. Малова И.О. Влагалищные выделения у девочек: этиология, клиника, диагностика, лечение. — Mediа/Consilium, 2004.
11. Руководство по лечению заболеваний, передаваемых половым путем. Центры по контролю и предупреждению заболеваний США, 2002. — М.: Санам, 2003. — 72 с.
— М.: Санам, 2003. — 72 с.
12. Серов В.Н., Стрижаков А.Н., Маркин С.Л. Практическое акушерство: Руководство для врачей. — М.: Медицина, 1989. — 512 с.
13. Стандартные принципы обследования и лечения детей и подростков с гинекологическими заболеваниями и нарушениями полового развития / Под ред. академика РАМН, проф. В.И. Кулакова, проф. Е.В. Увровой. — М.: Триада, 2004. — С. 50-56.
14. Хаммерсилаг М.Р. Заболевания, передаваемые половым путем, у детей // ИППП. — 1999. — Т. 3. — С. 4-11.
15. Fouts A., Kraus S.I. Trichomonas vaginalis: revaluation of its clinical presentation and laboratory diagnosis // J. Infect. Dis. — 1980. — 141. — P. 137-143.
16. Madico G., Quinn T.C., Rompalo A. еt al. Diagnosis of Trichomonas vaginalis infection by PCR usingvaginal sw. Samplas // J. Clin. Microbiol. — 1998. — Vol. 36(11). — P. 3205-3210.
17. Shuter J., Bell D. et al. Rates of and risk factors for trichomoniasis among pregnant in New York City // Sex. Trensm. Dis. — 1998. — Vol. 25(6). — P. 303-307.
Trensm. Dis. — 1998. — Vol. 25(6). — P. 303-307.
18. Waldman H.В. Sexually transmitted diseases and children: there is good news, bud // J. Dent. Child. — 1998. —Vol. 65(1) — P. 60-64.
Трихомониаз: Вопрос 7222 | Арт-Мед
Лечебно-диагностический центр
Более 15 лет заботимся о вашем здоровье !
Записаться на прием
+7(495)636-29-46
Вопросы и ответы
О клинике
Врачи
Диагностика
Приемы специалистов
Программы
Акции
Контакты
Срок беременности у меня был 9 недель, в бак. посеве обнаружены рост трихомонад активно подвижных и грибок кандида. Врач назначил мне Метронидазол в таблетках по 2 т. 3 раза в день и 1 капсулу Дифлюкана. Существует ли риск пороков развития? Мне сказали, что эти препараты из категории В по ФДА. Что мне делать, если я уже пропила их? Теперь срок уже 12 недель и аборт делать поздно. Мой врач говорит, что риск маловероятен и беременность на фоне лекарств лучше чем на фоне трихомониаза.
Галя
Ответ
Если ситуация с приемом препаратов уже произошла, то прерывать беременность после 12 недель, конечно не стоит, да и достаточных медицинских оснований для этого нет. Хотя представляется более целесообразным использование данных препаратов после 12 недель беременности, небольшой риск для плода все же существует. Что-либо конкретно предсказать невозможно. Обычно для таких назначения таких препаратов существует формулировка «если польза от применения превышает риск для плода». Очевидно, Ваш врач руководствовался именно такими соображениями. Для исключения грубых аномалий развития плода сделайте УЗИ 3-4 раза за беременность, тройной тест в 16-20 недель.
Врачи клиники «Арт-Мед»
Наши специалисты:
Комова Ольга Александровна
Врач гинеколог-эндокринолог первой категории
Планирование и ведение простой и осложненной беременности
Стаж: 19 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне и клиника на Щукинской
Кравцова Марина Николаевна
Врач акушер-гинеколог высшей категории, к. м.н.
м.н.
Ведение беременности после ЭКО, многоплодных случаев. Планирование беременностей при невынашивании
Стаж: 34 года
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Одареева Елена Владимировна
Врач акушер-гинеколог
Ведение беременности после ЭКО, многоплодных случаев. Планирование беременностей при невынашивании. Женское здоровье
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Быстрова Ирина Глебовна
Врач гинеколог-эндокринолог высшей категории
Занимается проблемами менопаузы, нарушениями цикла, бесплодием, невынашиванием
Стаж: 35 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Гершанов Евгений Александрович
Врач уролог-андролог
Лечение заболеваний органов мочеполовой системы
Стаж: 15 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Мацаев Адам Борисович
Врач-уролог
Врач-уролог, высшей квалификационной категории, кандидат медицинских наук
Стаж: 19 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Суровова Дарья Александровна
Врач-рентгенолог
рентгенография и компьютерная томография (органов грудной клетки, брюшной полости и забрюшинного пространства, придаточных пазух носа, сердца, сосудов головы и шеи, артерий нижних конечностей).
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Мальцева Татьяна Викторовна
Врач офтальмолог, первой квалификационной категории.
Офтальмология. Диагностика и лечение воспалительных заболеваний глаз. Подбор очков любой сложности.
Стаж: 8 лет
Задать вопрос
Записаться
Место работы:
Черкас Елена Игоревна
Врач ультразвуковой диагностики
УЗИ в акушерстве, гинекологии, молочных желез, щитовидной железы, органов брюшной полости, органов забрюшинного пространства и органов малого таза у мужчин.
Стаж: 20 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Баранов Роман Александрович
Врач акушер-гинеколог, врач УЗИ
Обследование при бесплодии, планирование и ведение беременности
Стаж: 9 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне
Кузьмина Татьяна Евгеньевна
Врач УЗИ высшей категории, к. м.н.
м.н.
Врач высшей квалификационной категории, к.м.н. Выполняет УЗИ экспертного класса.
Стаж: 20 лет
Задать вопрос
Записаться
Место работы: клиника на Красной Пресне и клиника на Щукинской
Имеются противопоказания. Необходимо проконсультироваться со специалистами.
Трихомониаз и неблагоприятные исходы родов: систематический обзор и метаанализ
1. Rowley J, Vander Hoorn S, Korenromp E, Low N, Unemo M, Aub-Raddad LJ, et al.
Хламидиоз, гонорея, трихомониаз и сифилис: оценки глобальной распространенности и заболеваемости, 2016 г. Bull World Health Organ
2019;97:548–62с. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2. Hamilton BE, Martin JA, Ostermak MJK, Rossen LM. Рождения: предварительные данные за 2018 год. Natl Vital Stat Rapid Release
2019;007. [Google Scholar]
3. Martin JA, Hamilton EB, Osterman MJK, Driscoll AK, Drake P. Births: Final Data for 2017. Natl Vital Stat Rep.
Natl Vital Stat Rep.
2018;67(8):1–10. [PubMed] [Google Scholar]
4. Херон М.
Смерти: основные причины в 2015 году. Представитель Natl Vital Stat
2017;66(5):1–74. [PubMed] [Google Scholar]
5. Разрыв плодных оболочек перед родами: практический бюллетень ACOG, номер 217. Obstet Gynecol
2020;135(3):e80–e97. [PubMed] [Google Scholar]
6. Minkoff H, Grunebaum AN, Schwarz RH, Feldman J, Cummings M, Crombleholme W, et al. Факторы риска недоношенности и преждевременного разрыва плодных оболочек: проспективное исследование вагинальной флоры во время беременности. Am J Obstet Gynecol
1984;150(8):965–72. [PubMed] [Google Scholar]
7. Cotch M PI, Nugent R. Trichomonas vaginalis связана с низкой массой тела при рождении и преждевременными родами. Секс Трансм Дис
1997;24(6):353–60. [PubMed] [Google Scholar]
8. Hardy PH, Hardy JB, Nell EE, Graham DA, Spence MR, Rosenbaum RC. Распространенность шести возбудителей заболеваний, передающихся половым путем, среди беременных подростков из городских районов и исход беременности. Ланцет
Ланцет
1984; 2 (8398): 333–7. [PubMed] [Google Scholar]
9. Руководство по лечению инфекций, передающихся половым путем: Всемирная организация здравоохранения;
2003 г. Доступно по адресу https://www.who.int/hiv/pub/sti/en/STIGuidelines2003.pdf. По состоянию на 1 ноября 2019 г.. [Google Scholar]
10. Саурина Г.Р., Маккормак В.М. Трихомониаз при беременности. Секс Трансм Дис
1997;24(6):361–2. [PubMed] [Google Scholar]
11. Klebanoff MA, Carey JC, Hauth JC, Hillier SL, Nugent RP, Thom EA, et al.
Неспособность метронидазола предотвратить преждевременные роды у беременных женщин с бессимптомной трихомонадной инфекцией влагалища. N Engl J Med
2001;345(7):487–93. [PubMed] [Google Scholar]
12. Окун Н., Гронау К.А., Ханна М.Э. Антибиотики при бактериальном вагинозе или Trichomonas vaginalis при беременности: систематический обзор. Акушерство Гинеколь
2005;105(4):857–68. [PubMed] [Академия Google]
13. Ворковский К.А. Руководство по лечению заболеваний, передающихся половым путем, Центров по контролю и профилактике заболеваний. Клин заразить Dis
Клин заразить Dis
2015;61
Приложение 8: S759–62. [PubMed] [Google Scholar]
14. Ван Дер Пол Б., Уильямс Дж. А., Орр Д. П., Баттейгер Б. Э., Фортенберри Д. Д. Распространенность, заболеваемость, естественное течение и ответ на лечение инфекции Trichomonas vaginalis среди женщин-подростков. J заразить Dis
2005;192(12):2039–44. [PubMed] [Google Scholar]
15. Sutton M, Sternberg M, Koumans EH, McQuillan G, Berman S, Markowitz L. Распространенность инфекции Trichomonas vaginalis среди женщин репродуктивного возраста в США, 2001–2004 гг. Клин заразить Dis
2007;45(10):1319–26. [PubMed] [Google Scholar]
16. Peterman TA, Tian LH, Metcalf CA, Malotte CK, Paul SM, Douglas JM, et al.
Стойкие, необнаруженные инфекции Trichomonas vaginalis?
Клин заразить Dis
2009;48(2):259–60. [PubMed] [Google Scholar]
17. Silver BJ, Guy RJ, Kaldor JM, Jamil MS, Rumbold AR. Trichomonas vaginalis как причина перинатальной заболеваемости: систематический обзор и метаанализ. Секс Трансм Дис
2014;41(6):369–76. [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
18. Бертон А.Е., Томас С. Инфекции, передающиеся половым путем, и преждевременные роды среди женщин из числа коренного населения Северной территории, Австралия: исследование случай-контроль. Aust N Z J Obstet Gynaecol
2019;59(1):147–53. [PubMed] [Google Scholar]
19. Warr AJ, Pintye J, Kinuthia J, Drake AL, Unger JA, McClelland RS, et al.
Инфекции, передающиеся половым путем, во время беременности и последующий риск мертворождения и младенческой смертности в Кении: проспективное исследование. Секс Трансм Заражение
2019;95(1):60–6. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Schonfeld A, Feldt T, Tufa TB, Orth HM, Fuchs A, Musfun MG, et al.
Распространенность и влияние инфекций, передающихся половым путем, на беременных женщин в центральной Эфиопии. Int J ЗППП СПИД
2018;29(3): 251–8. [PubMed] [Google Scholar]
21. Камаль А.М., Ахмед А.К., Мовафи Н.М.Э., Шавки Х.Е., Санад А.С., Хассан Э.Э. Заболеваемость антенатальным трихомониазом и оценка его роли как причины преждевременных родов у беременных женщин, обратившихся в университетскую больницу Миниа, Египет. Иран
Иран
Дж Паразитол
2018;13(1):58–66. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Tellapragada C, Eshwara VK, Bhat P, Kamath A, Aletty S, Mukhopadhyay C. Скрининг вульвовагинальных инфекций во время беременности в условиях ограниченных ресурсов: влияние на преждевременные роды. J заразить общественное здравоохранение
2017;10(4):431–437. [PubMed] [Академия Google]
23. Хосни А., Эль-Хаят В., Кашеф М.Т., Фахри М.Н. Связь между преждевременными родами и инфекциями мочеполового тракта, вызванными Trichomonas vaginalis, Mycoplasma hominis, грамотрицательными бациллами и коринеформами. J Chin Med Assoc
2017;80(9):575–81. [PubMed] [Google Scholar]
24. Moodley D, Sartorius B, Madurai S, Chetty V, Maman S. Исходы беременности в связи с ЗППП, включая выделение генитального HSV-2 в когортном исследовании в Южной Африке. Секс Трансм Заражение
2017;93(7):460–6. [PubMed] [Академия Google]
25. Натеги Ростами М., Хоссейн Рашиди Б., Хабиби А., Назари Р., Долати М. Генитальные инфекции и репродуктивные осложнения, связанные с Trichomonas vaginalis, Neisseria gonorrhoeae и Streptococcus agalactiae у женщин в Куме, центральный Иран. Int J Reprod Biomed
Генитальные инфекции и репродуктивные осложнения, связанные с Trichomonas vaginalis, Neisseria gonorrhoeae и Streptococcus agalactiae у женщин в Куме, центральный Иран. Int J Reprod Biomed
2017;15(6):357–66. [Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Nakubulwa S, Kaye DK, Bwanga F, Tumwesigye NM, Mirembe FM. Генитальные инфекции и риск преждевременного разрыва плодных оболочек в больнице Мулаго, Уганда: исследование случай-контроль. Заметки об исследованиях BMC
2015;8:573. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Элеже Г.У., Адинма Д.И., Угвуаньи Д.К., Икечебелу Д.И. Микробный изолят генитального тракта у женщин с преждевременным разрывом плодных оболочек перед родами в условиях сообщества с ограниченными ресурсами. J Obstet Gynecol
2014;35:465–8. [PubMed] [Google Scholar]
28. Мохер Д., Либерати А., Тацлафф Дж., Альтман Д.Г. Предпочтительные элементы отчетности для систематических обзоров и метаанализов: заявление PRISMA. Плос Мед
2009;6(7):e1000097. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Stroup DF, Berlin JA, Morton SC, Olkin I, Williamson GD, Rennie D, et al.
Метаанализ обсервационных исследований в эпидемиологии: предложение для отчета. Группа метаанализа обсервационных исследований в эпидемиологии (MOOSE). ДЖАМА
2000;283(15):2008–2012. [PubMed] [Академия Google]
30. ВОЗ: рекомендуемые определения, терминология и формат статистических таблиц, относящихся к перинатальному периоду и использованию нового сертификата причин перинатальной смерти. Модификации, рекомендованные FIGO в редакции от 14 октября 1976 г. Acta Obstet Gynecol Scand
1977; 56: 247–53. [PubMed] [Google Scholar]
31. Миддлтон П., Шеперд Э., Фленади В., Макбейн Р.Д., Кроутер, Калифорния. Запланированные ранние роды по сравнению с выжидательной тактикой (ожидание) при дородовом разрыве плодных оболочек в сроке (37 недель и более). Системная версия базы данных Cochrane
2017;1(1):CD005302. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Саари Т.Н. Иммунизация недоношенных и маловесных детей. Комитет по инфекционным заболеваниям Американской академии педиатрии. Педиатрия
Саари Т.Н. Иммунизация недоношенных и маловесных детей. Комитет по инфекционным заболеваниям Американской академии педиатрии. Педиатрия
2003; 112 (1 часть 1): 193–8. [PubMed] [Google Scholar]
33. Schlaudecker EP, Munoz FM, Bardají A, Boghossian NS, Khalil A, Mousa H
и другие.
Маленький для гестационного возраста: определение случая и рекомендации по сбору данных, анализу и представлению данных о безопасности материнской иммунизации. вакцина
2017; 35 (48 часть А): 6518–28. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Станг А.
Критическая оценка шкалы Ньюкасла-Оттавы для оценки качества нерандомизированных исследований в метаанализах. Евр J Эпидемиол
2010;25:603–5. [PubMed] [Google Scholar]
35. Sterne JAC, Savovic J, Page MJ, et al.
RoB 2: пересмотренный инструмент для оценки риска систематической ошибки в рандомизированных исследованиях. БМЖ
2019;366:14898. [PubMed] [Google Scholar]
36. Rothman KJ, Greenland S, Lash TL. Современная эпидемиология. 3-е изд. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2008. [Google Академия]
3-е изд. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2008. [Google Академия]
37. Каммингс П.
Относительные достоинства отношения риска и отношения шансов. Arch Pediatr Adolesc Med
2009;163(5):438–45. [PubMed] [Google Scholar]
38. Huedo-Medina TB, Sanchez-Meca J, Marin-Martinez F, Botella J. Оценка неоднородности в метаанализе: статистика Q или индекс I2?
Психологические методы
2006;11(2):193–206. [PubMed] [Google Scholar]
39. Higgins JP, Thompson SG. Количественная неоднородность в метаанализе. Стат Мед
2002;21(11):1539–58. [PubMed] [Академия Google]
40. Эггер М., Дэйви Смит Г., Шнайдер М., Миндер С. Смещение в метаанализе, обнаруженное с помощью простого графического теста. БМЖ
1997;315(7109):629–34. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Begg CB, Mazumdar M. Рабочие характеристики теста ранговой корреляции для предвзятости публикации. Биометрия
1994; 50(4):1088–101. [PubMed] [Google Scholar]
42. StataCorp. 2011. Статистическое программное обеспечение Stata: выпуск 12. College Station TSL. [Google Scholar]
2011. Статистическое программное обеспечение Stata: выпуск 12. College Station TSL. [Google Scholar]
43. Johnson HL, Ghanem KG, Zenilman JM, Erbelding EJ. Инфекции, передающиеся половым путем, и неблагоприятные исходы беременности среди женщин, посещающих городские венерологические диспансеры. Секс Трансм Дис
2011;38(3):167–71. [PubMed] [Академия Google]
44. Азаргун А., Дарвишзаде С. Ассоциация бактериального вагиноза, вагинальной трихомонады и вагинальной кислотности с исходом беременности. Арх Иран Мед
2006;9(3):213–7. [PubMed] [Google Scholar]
45. Buchmayer S, Sparen P, Cnattingius S. Признаки инфекции в мазках Папаниколау и риск неблагоприятного исхода беременности. Педиатр Перинат Эпидемиол
2003;17(4):340–6. [PubMed] [Google Scholar]
46. Stratton P, Tuomala RE, Abboud R, Rodriguez E, Rich K, Pitt J, et al.
Акушерские исходы и исходы у новорожденных в когорте ВИЧ-инфицированных беременных женщин: отчет об исследовании передачи инфекции женщинам и младенцам. J Acquir Immune Defic Syndr Hum Retrovirol
J Acquir Immune Defic Syndr Hum Retrovirol
1999;20(2):179–86. [PubMed] [Google Scholar]
47. Mathai E, Muthaiah A, Mathai M, Jasper P. Распространенность и последствия трихомониаза при беременности. Natl Med J Индия
1998;11(3):151. [PubMed] [Google Scholar]
48. Meis PJ, Goldenberg RL, Mercer B, Moawad A, Das A, McNellis D, et al.
Исследование по прогнозированию преждевременных родов: значение вагинальных инфекций. Сеть отделений медицины матери и плода Национального института здоровья ребенка и человеческого развития. Am J Obstet Gynecol
1995;173(4):1231–5. [PubMed] [Академия Google]
49. McGregor JA, French JI, Parker R, Draper D, Patterson E, Jones W, et al.
Профилактика преждевременных родов путем скрининга и лечения распространенных инфекций половых путей: результаты проспективной контролируемой оценки. Am J Obstet Gynecol
1995;173(1):157–67. [PubMed] [Google Scholar]
50. Грайс А.
Вагинальная инфекция, вызывающая спонтанный разрыв плодных оболочек и преждевременные роды. Aust N Z J Obstet Gynaecol
Aust N Z J Obstet Gynaecol
1974; 14: 156–158. [Google Scholar]
51. Hu CY, Li FL, Hua XG, Jiang W, Zhang XJ. Продольная траектория вульвовагинального кандидоза, трихомониаза и бактериального вагиноза во время беременности, а также влияние на исходы беременности: предварительное исследование. J Matern Fetal Neonatal Med
2019;32:3612–7. [PubMed] [Google Scholar]
52. Lokken EM, Mandaliya K, Srinivasan S, Richardson BA, Kinuthia J, Lannon S, et al.
Влияние микробиоты влагалища до зачатия на риск спонтанных преждевременных родов у женщин: протокол проспективного когортного исследования. БМЖ Открытый
2020;10(2):e035186. [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Olson-Chen C, Balaram K, Hackney DN. Chlamydia trachomatis и неблагоприятные исходы беременности: метаанализ пациентов с инфекцией и без нее. Здоровье матери и ребенка J
2018;22(6):812–21. [PubMed] [Академия Google]
54. Vallely LM, Egli-Gany D, Pomat W, Se Homer C, Guy R, Wand H, et al.
Неблагоприятные исходы беременности и новорожденных, связанные с Neisseria gonorrhoeae, Mycoplasma genitalium, M. hominis, Ureaplasma urealyticum и U. parvum: систематический обзор и протокол метаанализа. БМЖ Открытый
hominis, Ureaplasma urealyticum и U. parvum: систематический обзор и протокол метаанализа. БМЖ Открытый
2018;8(11):e024175. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Уокер Г.
Вмешательства при трихомониазе у беременных: Комментарий БРЗ
Женева, Швейцария: Библиотека репродуктивного здоровья ВОЗ; 2004. [Google Академия]
56. Simhan HN, Anderson BL, Krohn MA, Heine RP, Martinez de Tejada B, Landers DV, et al.
Иммунные последствия бессимптомной трихомонадной инфекции во время беременности. Am J Obstet Gynecol
2007;196(1):59.e1–.e5. [PubMed] [Google Scholar]
57. Mielczarek E, Blaszkowska J. Trichomonas vaginalis: патогенность и потенциальная роль в репродуктивной недостаточности человека. Инфекционное заболевание
2016;44(4):447–58. [PubMed] [Google Scholar]
58. Balu RB, Savitz DA, Ananth CV, Hartmann KE, et al.
Бактериальный вагиноз, дефенсины нейтрофилов вагинальной жидкости и преждевременные роды. Акушерство Гинеколь
2003; 101 (5 часть 1): 862–8. [PubMed] [Академия Google]
[PubMed] [Академия Google]
59. Фихорова Р.Н. Влияние инфекции T. vaginalis на врожденные иммунные реакции и репродуктивный исход. J Репрод Иммунол
2009;83(1–2):185–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
60. Tanaka Y, Narahara H, Takai N, Yoshimatsu J, Anai T, Miyakawa I. Интерлейкин-1β и интерлейкин-8 в цервиковагинальной жидкости во время беременности. Am J Obstet Gynecol
1998; 179 (3 часть 1): 644–9. [PubMed] [Google Scholar]
61. Ван Гервен OT, Muzny CA. Последние достижения в эпидемиологии, диагностике и лечении инфекции Trichomonas vaginalis. F1000рез
2019;8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Mann JR, McDermott S, Zhou L, Barnes TL, Hardin J. Лечение трихомониаза при беременности и преждевременных родах: обсервационное исследование. J Женское здоровье (Larchmt)
2009;18:493–7. [PubMed] [Google Scholar]
Как лечить и многое другое
Трихомониаз (также называемый «трих») — это инфекция, передающаяся половым путем (ИППП), вызываемая паразитом. По оценкам, в Соединенных Штатах ею страдают 3,7 миллиона человек, что делает ее наиболее распространенной ИППП.
По оценкам, в Соединенных Штатах ею страдают 3,7 миллиона человек, что делает ее наиболее распространенной ИППП.
Трихомониаз можно лечить антибиотиками, при этом инфекция обычно проходит через неделю. Однако, если его не лечить, трихомониаз может длиться несколько месяцев или лет. Его симптомы могут сделать секс неприятным. Но у беременных это также может вызвать серьезные осложнения при родах.
Читайте дальше, чтобы узнать больше о симптомах, причинах, факторах риска и о том, что вам следует делать, если вы подозреваете, что у вас трихомониаз. (Спойлер: как можно скорее обратитесь к врачу). Беременные женщины также подвержены более высокому риску преждевременных родов или до 37 недель.
Дети матерей, больных трихомониазом, с большей вероятностью будут иметь вес при рождении менее 5 1/2 фунтов. В крайне редких случаях младенцы женского пола могут заразиться инфекцией при прохождении через родовые пути.
Преждевременные роды и низкая масса тела при рождении являются двумя из трех основных причин детской смертности. Тем не менее, трихомониаз можно лечить антибиотиками во время беременности, при этом инфекции исчезают до родов.
Тем не менее, трихомониаз можно лечить антибиотиками во время беременности, при этом инфекции исчезают до родов.
По данным Центров по контролю и профилактике заболеваний (CDC), от 70 до 85 процентов людей с трихомониазом не испытывают никаких симптомов.
У женщин трихомониаз может вызывать:
- рыбный запах половых органов
- большое количество белых, серых или зеленых выделений из влагалища
- зуд половых органов
- боль при мочеиспускании или половом акте
900 02 Симптомы у мужчин встречаются редко, но они могут испытывать:
- раздражение внутри полового члена
- жжение во время мочеиспускания или после эякуляции
- выделения из полового члена
Трихомониаз вызывается микроскопическим паразитом под названием Вагинальная трихомонада . Он передается от человека к человеку во время полового акта. Инкубационный период между воздействием и заражением составляет от 5 до 28 дней.
Некоторые люди подвержены большему риску заражения трихомониазом, чем другие. К группе наибольшего риска относятся люди:
- имеющие несколько половых партнеров
- перенесшие другие ИППП в прошлом
- переболевшие трихомониазом в прошлом
- занимающиеся сексом без барьерных методов, таких как презервативы
Для проверки на трихомониаз врач будет использовать микроскоп для поиска паразита в образце. Для женщин источником проб являются выделения из влагалища. Для мужчин источником образца является моча.
Затем врач может провести дополнительные анализы образца, чтобы подтвердить присутствие паразита. К ним относятся культуральный тест, тест амплификации нуклеиновых кислот или экспресс-тест на антиген.
Беременные женщины с любыми симптомами трихомониазной инфекции должны немедленно обратиться к врачу. Поскольку при регулярных посещениях акушера-гинеколога вас обычно не проверяют на трихомониаз, инфекция может остаться незамеченной и нанести вред вашему ребенку.
Беременные с трихомониазом подвергаются повышенному риску:
- преждевременных родов и родов
- рождения ребенка с низкой массой тела при рождении
- передачи трихомониаза ребенку женского пола во время родов (крайне редко) трихомониаз могут с большей вероятностью заразиться ВИЧ.
Врачи обычно лечат трихомониаз антибиотиками. Обычно используется один из двух антибиотиков: метронидазол (Флагил) или тинидазол (Тиндамакс). Вам и вашему партнеру потребуется лечение. Кроме того, вы оба должны избегать половых контактов до тех пор, пока инфекция трихомониаза не пройдет.
Вы не должны употреблять алкоголь в течение 24 часов после приема метронидазола или 72 часов после приема тинидазола. Это может привести к сильной тошноте и рвоте.
После лечения обычно проходит около недели, прежде чем инфекция трихомониаза исчезнет. Большинство людей полностью выздоравливают.
Как и при всех ИППП, единственный способ полностью предотвратить трихомониаз – воздержание от секса.

