Андростендион повышен у женщин: Андростендион анализ цена в Москве
Гиперандрогения у женщин: причины, диагностика, лечение
Все жизненно важные процессы в организме человека контролируются гормонами. Их вырабатывают железы внутренней или смешанной секреции. Некоторые их них продуцируют половые гормоны. Они присутствуют в крови и женщин, и мужчин, но в женском организме больше эстрогенов, а в мужском – андрогенов. Когда нарушается соотношение половых гормонов либо некоторые ткани начинают их неадекватно воспринимать, у женщин развивается гиперандрогения. По имеющимся данным, эта патология встречается в половины женского населения.
Роль андрогенов в организме человека
Андрогены – это вещества, которые относятся к стероидным гормонам. Они синтезируются яичками у мужчин, яичниками у женщин и надпочечниками. К ним относят тестостерон, прогестерон, ДГЭА-сульфат. Гипофиз вырабатывает фолликулостимулирующий и лютеинизирующий гормоны, которые регулируют продукцию андрогенов. Дигидротестостерон и прогестерон – главные андрогены, которые циркулируют в крови женщины с нормальным овариально-менструальным циклом. ДГЭА и андростендион являются прогормонами, потому что их андрогенные свойства проявляются только после трансформации в тестостерон. Ежедневно гормонопродуцирующие ткани женского организма синтезируют до 300 мкг тестостерона. Из этого количества ¼ вырабатывается яичниками, ¼ корой надпочечников, а половина трансформируется из проанростеронов. Если же в крови женщины будет больше тестостерона, у неё развивается гиперандрогения.
ДГЭА и андростендион являются прогормонами, потому что их андрогенные свойства проявляются только после трансформации в тестостерон. Ежедневно гормонопродуцирующие ткани женского организма синтезируют до 300 мкг тестостерона. Из этого количества ¼ вырабатывается яичниками, ¼ корой надпочечников, а половина трансформируется из проанростеронов. Если же в крови женщины будет больше тестостерона, у неё развивается гиперандрогения.
Андрогены также оказывают влияние на жировой обмен у женщины, снижая количество липопротеидов высокой плотности. Они улучшают минерализацию костной ткани женщины и снижают вероятность развития остеопороза в постменопаузе. При снижении уровня андрогенов увеличивается заболеваемость сердечно-сосудистыми заболеваниями. Андрогены влияют на процесс формирования вторичных половых признаков, их повышение вызывает такое заболевание, как гиперандрогения у женщин.
Нормальные показатели андрогенов в крови человека
В организме женщины определяется несколько андрогенов.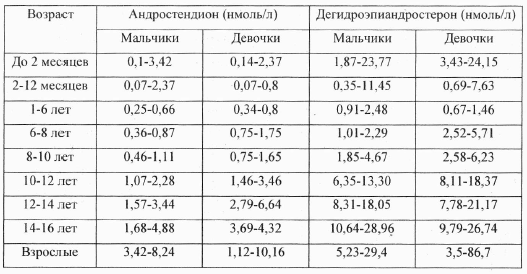 Так, в норме тестостерона у женщины 0,2-2,0 нг/мл, кортизола от 190 до 750 нг/мл, а альдостерона не больше пятнадцати нанограмм в одном миллилитре. Уровень прогестерона и эстрадиола меняется в зависимости от фазы цикла. Так, в фолликулиновую фазу эстрадиола должно быть 0,17, а прогестерона 1,59 нмоль/л. Во время овуляции их концентрация возрастает соответственно до 1,2 и 4,77 нмоль/л. В лютеиновую фазу количество этих гормонов максимальное: эстрадиола 0,57, а прогестерона 29,6 моль/мл.
Так, в норме тестостерона у женщины 0,2-2,0 нг/мл, кортизола от 190 до 750 нг/мл, а альдостерона не больше пятнадцати нанограмм в одном миллилитре. Уровень прогестерона и эстрадиола меняется в зависимости от фазы цикла. Так, в фолликулиновую фазу эстрадиола должно быть 0,17, а прогестерона 1,59 нмоль/л. Во время овуляции их концентрация возрастает соответственно до 1,2 и 4,77 нмоль/л. В лютеиновую фазу количество этих гормонов максимальное: эстрадиола 0,57, а прогестерона 29,6 моль/мл.
Гиперандрогения у женщин. Причины, признаки
Гиперандрогения у женщин бывает в случае резкого повышения уровня андрогенов в сыворотке крови либо при повышении чувствительности к ним клеток сальных и потовых желез и яичников. Это происходит тогда, когда у женщины диагностируются такие заболевания:
- заболевания органов эндокринной системы;
- опухоли вилочковой либо щитовидной железы, надпочечников;
- патология поджелудочной железы;
- андреногенитальный синдром;
- повышенная реакция на андрогены рецепторов кожи, потовых и сальных желез либо яичников.
Гиперандрогения у женщин отмечается при таких заболеваниях: множественные кисты яичников; синдром Штейна-Левенталя, Иценко-Кушинга, врождённое утолщение коры надпочечников, некоторые опухоли, которым свойственна гиперпродукция андрогенов.
Гиперандрогения имеет соответствующие признаки. В пубертатном возрасте у девочек оволосение происходит по мальчиковому типу: волосы начинают расти на лице, грудной клетке, по средней линии живота. Отмечается сильное шелушение кожи (акне, себорея). На голове начинают появляться глубокие залысины. Для таких девушек проблемой становится лишний вес. Месячные начинаются довольно поздно, они и вовсе могут отсутствовать. В ряде случаев менструации очень короткие и перерыв между ними довольно большой.
У таких женщин слабо развита мускулатура, в молодом возрасте начинается вымывание кальция из костей и формируется остеопороз. У них снижена толерантность к глюкозе и повышена восприимчивость к простудным заболеваниям.
Диагностика гиперандрогении
Учитывая то, что гиперандрогения характерна для различных заболеваний, к обследованию надо подходить индивидуально в каждом конкретном случае. При синдроме поликистозных яичников особое внимание надо уделить сбору анамнеза, осмотру и гинекологическому обследованию. В анализах крови можно увидеть изменение уровня фолликулостимулирующего гормона, нарушение принятых за норму пропорций тестостерона и лютеинизирующего гормона, увеличение концентрации пролактина и гиперглюкоземию. Обязательным исследованием является вагинальное УЗИ: на нём можно увидеть резко увеличенные в размерах яичники, в которых имеются множественные фолликулы.
При синдроме поликистозных яичников особое внимание надо уделить сбору анамнеза, осмотру и гинекологическому обследованию. В анализах крови можно увидеть изменение уровня фолликулостимулирующего гормона, нарушение принятых за норму пропорций тестостерона и лютеинизирующего гормона, увеличение концентрации пролактина и гиперглюкоземию. Обязательным исследованием является вагинальное УЗИ: на нём можно увидеть резко увеличенные в размерах яичники, в которых имеются множественные фолликулы.
В случае синдрома Иценко-Кушинга будут соответствующие изменения в гемограмме: увеличенное количество лейкоцитов, снижение содержания эозинофилов и лимфоцитов. Обязательно выполнить УЗИ надпочечников для уточнения локализации и величины опухоли. Если же оно будет не достаточно информативным либо возникнет подозрение на опухоль Вильямса, стоит сделать компьютерную томографию. Для исключения патологического процесса гипофиза следует произвести рентгенологическое исследование черепа.
Особое внимание следует уделить гиперплазии надпочечников, ведь эту патологию можно выявить и ещё внутриутробно. У взрослой женщины при данной патологии в сыворотке крови находят избыток 17-гидроксипрогестерона, а 21-гидролазы будет намного меньше нормы. У беременной женщины определяют андростендион и прогестерон в околоплодных водах. Лечение гиперандрогении врождённой проводится гормонами коры надпочечников.
У взрослой женщины при данной патологии в сыворотке крови находят избыток 17-гидроксипрогестерона, а 21-гидролазы будет намного меньше нормы. У беременной женщины определяют андростендион и прогестерон в околоплодных водах. Лечение гиперандрогении врождённой проводится гормонами коры надпочечников.
Опухоли яичников и надпочечников могут продуцировать избыточное количество андрогенов и вызывать гиперандрогению у женщин. В этом случае при локализации процесса в яичниках можно обнаружить избыточное количество тестостерона, а для опухоли надпочечников характерно повышение концентрации дигидроэпинтестостерона. При подозрении на опухоль яичников следует выполнить УЗИ, а новообразование в надпочечниках лучше искать с помощью компьютерной томографии.
В случае гиперплазии яичников обследование надо начать с определения уровня гормонов: концентрация гонадотропных гормонов будет в пределах интеркурентных показателей, а вот уровень андрогенов станет как у мужчин.
Гиперандрогения.
 Лечение
Лечение
Женщину, прежде всего, беспокоит, как она выглядит. Для того чтобы избавить пациентку от симптомов гиперандрогении, надо назначить лечение основного заболевания, которое вызвало соответствующие изменения. Если ей поставили диагноз «синдром поликистозных яичников», то прописывают, прежде всего, медроксипрогестерон, который особенно показан при гирсутизме. Гормональные комбинированные контрацептивы у большинства пациенток уменьшают рост волос, излечивают акне.
Под воздействием этих препаратов выравниваются месячные, уменьшается кровопотеря во время менструации. Также лечение гиперандрогении проводят такими препаратами: кортикостероидами, кетокеназолом, спироналактоном. При гиперандрогении с СПКЯ применяют оперативное лечение. Чаще всего выполняют прижигание кист с помощью электрокоагулятора.
Лечение гиперандрогении фармакологическими препаратами при синдроме Иценко-Кушинга считается подготовительным этапом перед операцией. Хирургическим путём удаляется аденома. Лучевая терапия показана при опухоли гипофиза, и она не очень эффективна. В случае врождённой гиперплазии надпочечников единственным препаратом, который используют для того, чтобы провести лечение гиперандрогении, является дексаметазон.
Лучевая терапия показана при опухоли гипофиза, и она не очень эффективна. В случае врождённой гиперплазии надпочечников единственным препаратом, который используют для того, чтобы провести лечение гиперандрогении, является дексаметазон.
Если гиперандрогения у женщин вызвана гормоносинтезирующими опухолями, то лечение проводят, как правило, в онкологических центрах. Опухоль удаляют хирургическим путём. Оперативное лечение сочетают с лучевой и химиотерапией. Обязательно назначают гормональные препараты. При гиперплазии яичников следует выполнить их клиновидную резекцию. В тяжёлых случаях удаляют оба яичника.
Что делать, если вы обнаружили признаки гиперандрогении
Каждая женщина, которая обнаружила симптомы гиперандрогении, должна сразу же обратиться к врачу. Ни в коем случае не стоит заниматься самолечением. Выявить причину гиперандрогении, пройти необходимое обследование и лечение вы можете в Центр ЭКО Тамбов. Наши специалисты окажут не только медицинскую, но и так необходимую каждой женщине в этой ситуации психологическую поддержку.
НОВЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ. АНДРОСТЕНДИОН
Дата публикации: .
врач клинической лабораторной
диагностики централизованной городской
гормональной лаборатории Капустина Е.В.
Андростендион (АСД) — стероидный гормон, который вырабатывается половыми железами: яичками у мужчин и яичниками у женщин, а также в сетчатой зоне коркового вещества надпочечников у людей обоих полов. Образуется на промежуточном этапе биосинтеза половых гормонов тестостерона и эстрона. Относится к группе андрогенов. Андрогены стимулируют рост и развитие мужских половых органов, способствуют формированию вторичных половых признаков по мужскому типу, участвуют в регуляции процессов, не связанных с половой системой: оказывают анаболический эффект, влияют на обмен углеводов, липидов, холестерина. Андрогенное действие андростендиона значительно слабее, чем у тестостерона, однако его значение возрастает при развитии синдромов гиперандрогении у женщин. Измерение концентрации андростендиона применяется для дифференциальной диагностики и контроля лечения этих состояний. Кроме того, «слабые» андрогены играют ведущую роль в метаболизме пациентов с низкой концентрацией тестостерона в норме (например, мальчиков до периода полового созревания). Андростендион также является основным стероидным гормоном женщин в постменопаузе.
Измерение концентрации андростендиона применяется для дифференциальной диагностики и контроля лечения этих состояний. Кроме того, «слабые» андрогены играют ведущую роль в метаболизме пациентов с низкой концентрацией тестостерона в норме (например, мальчиков до периода полового созревания). Андростендион также является основным стероидным гормоном женщин в постменопаузе.
Продукция андростендиона надпочечниками регулируется адренокортикотропным гормоном (АКТГ) гипофиза, тогда как выработка андростендиона половыми железами регулируется посредством выработки лютеинизирующего гормона(ЛГ).
Уровень андростендиона в крови начинает увеличиваться у детей примерно в возрасте 6-8 лет, он служит основным источником андрогенов у детей. С наступлением полового созревания выработка андростендиона увеличивается, а после 30 лет плавно снижается. Уровень андростендиона в плазме имеет суточные колебания с максимумом в утренние часы и подвержен циклическим изменениям, связанным с менструальным циклом.-2010/64/3.jpg) Концентрация андростендиона повышается при беременности.
Концентрация андростендиона повышается при беременности.
Физиологическая роль:
У мужчин отвечает за формирование внешних половых признаков , работу репродуктивной системы, за обмен веществ.
В женском организме мужской гормон выполняет следующие функции:
- способствует расщеплению жиров;
- увеличивает синтез белков; стимулирует набор мышечной массы;
- снижает уровень глюкозы;
- участвует в выработке половых гормонов;
- отвечает за работу сальных желез.
- повышает либидо.
Показания к определению:
- признаки гиперандрогении у женщин (гирсутизм, акне, снижение тембра голоса, андрогенная алопеция, угревая сыпь, себорея)
- бесплодие, невынашивание беременности
- нарушения менструального цикла
- нарушение полового развития у детей
- признаки нарушения половой дифференцировки у новорожденных
- подозрение на андрогенпродуцирующие опухоли надпочечников, яичников и яичек
- подозрение на синдром поликистозных яичников (СПКЯ)
- врожденная гиперплазия коры надпочечников (диагностика и мониторинг лечения)
Определение уровней андростендиона в комплексе с другими исследованиями применяется для оценки
функции коры надпочечников, синтеза андрогенов и функции
яичников/яичек, а также для выявления причин гиперандрогенных состояний у женщин, сопровождающихся симптомами вирилизации : акне, гирсутизм (избыточный рост волос на лице и теле по мужскому типу), изменение тембра голоса и др.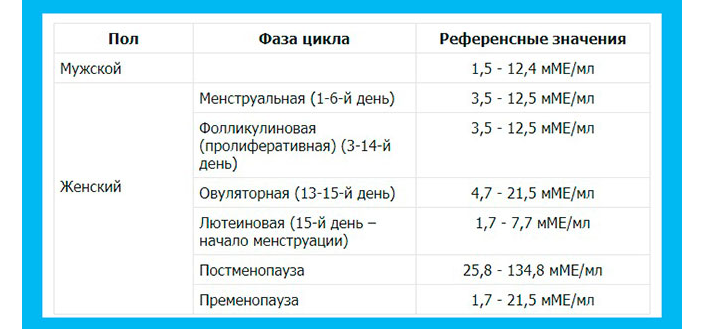 Самыми частыми причинами такой вирилизации являются: гиперпродукция андрогенов яичниками (синдром поликистозных яичников, гипертекоз и андрогенпродуцирующие опухоли) и гипрепродукция андрогенов надпочечниками (синдром Кушинга, врождённая дисфункция коры надпочечников).
Самыми частыми причинами такой вирилизации являются: гиперпродукция андрогенов яичниками (синдром поликистозных яичников, гипертекоз и андрогенпродуцирующие опухоли) и гипрепродукция андрогенов надпочечниками (синдром Кушинга, врождённая дисфункция коры надпочечников).
У мужчин, как правило, умеренное увеличение концентрации андростендиона не сопровождается клиническими признаками. Однако возможность превращения андростендиона в эстрогены может иногда привести к появлению у мужчин легких симптомов гиперэстрогении (например, гинекомастии).
Пониженные значения отмечаются при надпочечниковой недостаточности, недостаточности яичников, серповидноклеточной анемии, физиологическом (возрастном) снижении половой функции у мужчин.
Подготовка к исследованию:
Исследование проводится утром натощак. Накануне следует отказаться от алкоголя, физических нагрузок. Женщинам рекомендуется сдавать кровь на 2-3 день менструального цикла. За 30 дней до сдачи анализа следует отменить прием пероральных контрацептивов.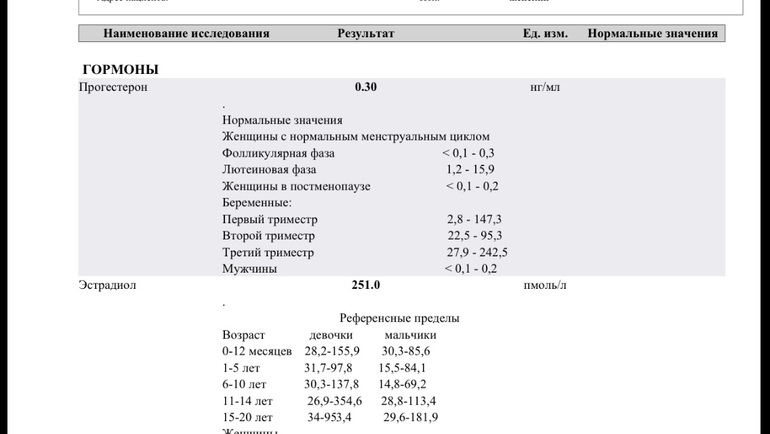
Повышенный уровень андростендиона в крови не является диагностическим критерием конкретного заболевания, а учитывается лечащим врачом при постановке диагноза и назначении лечения в комплексе с данными анамнеза и результатами других обследований.
Повышенный уровень андростендиона у молодых взрослых, но не ранних подростковых пренатально андрогенизированных самок крыс
1. Franks S. Синдром поликистозных яичников. N Engl J Med. 1995;333(13):853–61. дои: 10.1056/NEJM199509283331307 . [PubMed] [Google Scholar]
2. March WA, Moore VM, Willson KJ, Phillips DI, Norman RJ, Davies MJ. Распространенность синдрома поликистозных яичников в выборке сообщества оценивали по контрастным диагностическим критериям. Хум Репрод. 2010;25(2):544–51. дои: 10.1093/humrep/dep399 . [PubMed] [Google Scholar]
3. Агапова С.Е., Камео Т., Софер А.Б., Оберфилд С.Е. Диагностика и проблемы синдрома поликистозных яичников в подростковом возрасте. Семин репрод мед. 2014;32(3):194–201. Эпб 2014/04/08. doi: 10.1055/s-0034-1371091; Центральный PMCID PubMed: PMCPMC4426828. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Эпб 2014/04/08. doi: 10.1055/s-0034-1371091; Центральный PMCID PubMed: PMCPMC4426828. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Rosenfield RL. Диагностика синдрома поликистозных яичников у подростков. Педиатрия. 2015;136(6):1154–65. doi: 10.1542/пед.2015-1430. [Бесплатная статья PMC] [PubMed] [Google Scholar]
5. Гибсон-Хелм М.Э., Лукас И.М., Бойл Дж.А., Тиде Х.Дж. Женский опыт диагностики синдрома поликистозных яичников. Фам Практ. 2014;31(5):545–9. Эпб 2014/06/12. doi: 10.1093/fampra/cmu028. [PubMed] [Google Scholar]
6. Гибсон-Хелм М., Тиде Х., Дунайф А., Докрас А. Задержка диагностики и недостаток информации, связанные с неудовлетворенностью у женщин с синдромом поликистозных яичников. J Clin Endocrinol Metab. 2017;102(2):604–12. doi: 10.1210/jc.2016-2963. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Миссо М., Бойл Дж., Норман Р., Тиде Х. Разработка основанных на фактических данных рекомендаций по СПКЯ и последствиям для здоровья населения. Семин репрод мед. 2014;32(3):230–40. Эпб 2014/04/08. doi: 10.1055/s-0034-1371095. [PubMed] [Google Scholar]
Семин репрод мед. 2014;32(3):230–40. Эпб 2014/04/08. doi: 10.1055/s-0034-1371095. [PubMed] [Google Scholar]
8. Сэм С., Дунайф А. Синдром поликистозных яичников: синдром XX?
Тенденции Эндокринол Метаб. 2003;14(8):365–70. . [PubMed] [Google Scholar]
9. Teede H, Deeks A, Moran L. Синдром поликистозных яичников: сложное состояние с психологическими, репродуктивными и метаболическими проявлениями, которое влияет на здоровье на протяжении всей жизни. БМС Мед. 2010;8:41
doi: 10.1186/1741-7015-8-41; Центральный PMCID в PubMed: PMCPMC2909929. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Welt CK, Carmina E. Клинический обзор: Жизненный цикл синдрома поликистозных яичников (СПКЯ): от внутриутробного развития до менопаузы. J Clin Endocrinol Metab. 2013;98(12):4629–38. doi: 10.1210/jc.2013-2375; Центральный PMCID PubMed: PMCPMC3849665. [Бесплатная статья PMC] [PubMed] [Google Scholar]
11. Scaruffi E, Gambineri A, Cattaneo S, Turra J, Vettor R, Mioni R. Личностные и психические расстройства у женщин, страдающих синдромом поликистозных яичников. Фронт Эндокринол (Лозанна). 2014;5:185
Фронт Эндокринол (Лозанна). 2014;5:185
дои: 10.3389/fendo.2014.00185 ; Центральный PMCID PubMed: PMCPMC4228916. [Бесплатная статья PMC] [PubMed] [Google Scholar]
12. Эрманн Д.А. Синдром поликистоза яичников. N Engl J Med. 2005;352(12):1223–36. doi: 10.1056/NEJMra041536. [PubMed] [Google Scholar]
13. Gambineri A, Patton L, Altieri P, Pagotto U, Pizzi C, Manzoli L, et al.
Синдром поликистозных яичников является фактором риска развития диабета 2 типа: результаты долгосрочного проспективного исследования. Диабет. 2012;61(9):2369–74. Эпб 2012/06/14. дои: 10.2337/db11-1360 ; Центральный PMCID PubMed: PMCPMC3425413. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Моран Л.Дж., Норман Р.Дж., Тиде Х.Дж. Метаболический риск при СПКЯ: влияние фенотипа и ожирения. Тенденции Эндокринол Метаб. 2015;26(3):136–43. doi: 10.1016/j.tem.2014.12.003 . [PubMed] [Google Scholar]
15. Группа REA-SPCW. Пересмотренный консенсус 2003 г. по диагностическим критериям и долгосрочным рискам для здоровья, связанным с синдромом поликистозных яичников. Фертил Стерил. 2004;81(1):19–25. . [PubMed] [Google Scholar]
Фертил Стерил. 2004;81(1):19–25. . [PubMed] [Google Scholar]
16. Azziz R, Carmina E, Dewailly D, Diamanti-Kandarakis E, Escobar-Morreale HF, Futterweit W, et al.
Критерии Общества избытка андрогенов и СПКЯ для синдрома поликистозных яичников: полный отчет целевой группы. Фертил Стерил. 2009 г.;91(2):456–88. doi: 10.1016/j.fertnstert.2008.06.035. [PubMed] [Google Scholar]
17. Дунайф А. Синдром поликистозных яичников. Бостон, Сент-Луис, Миссури: Научные публикации Блэквелла; Дистрибьюторы, США и Канада, Mosby-Year Book; 1992.
XVIII, 392 с. п. [Google Scholar]
18. Pasquali R, Zanotti L, Fanelli F, Mezzullo M, Fazzini A, Morselli Labate AM, et al.
Определение гиперандрогении у женщин с синдромом поликистозных яичников: сложная перспектива. J Clin Endocrinol Metab. 2016;101(5):2013–22. Эпб 2016/03/10. doi: 10.1210/jc.2015-4009. [PubMed] [Google Scholar]
19. Ксита Н., Цацулис А. Обзор: фетальное программирование синдрома поликистозных яичников избытком андрогенов: данные экспериментальных, клинических и генетических ассоциативных исследований. J Clin Endocrinol Metab. 2006;91(5):1660–6. doi: 10.1210/jc.2005-2757. [PubMed] [Google Scholar]
J Clin Endocrinol Metab. 2006;91(5):1660–6. doi: 10.1210/jc.2005-2757. [PubMed] [Google Scholar]
20. Forsdike RA, Hardy K, Bull L, Stark J, Webber LJ, Stubbs S, et al.
Нарушение развития фолликулов в яичниках пренатально андрогенизированных овец. J Эндокринол. 2007;192(2):421–8. дои: 10.1677/Джо.1.07097 . [PubMed] [Google Scholar]
21. Abbott DH, Zhou R, Bird IM, Dumesic DA, Conley AJ. Фетальное программирование избытка андрогенов надпочечников: уроки из модели синдрома поликистозных яичников у нечеловеческих приматов. Эндокр Дев. 2008; 13: 145–58. дои: 10.1159/000134831; Центральный PMCID PubMed: PMCPMC2531212. [Бесплатная статья PMC] [PubMed] [Google Scholar]
22. Abbott DH, Tarantal AF, Dumesic DA. Фетальные, младенческие, подростковые и взрослые фенотипы синдрома поликистозных яичников у пренатально андрогенизированных самок макак-резусов. Am J Приматол. 2009 г.;71(9):776–84. doi: 10.1002/ajp.20679; Центральный PMCID PubMed: PMCPMC2916860. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Abbott DH, Bruns CR, Barnett DK, Dunaif A, Goodfriend TL, Dumesic DA, et al.
Abbott DH, Bruns CR, Barnett DK, Dunaif A, Goodfriend TL, Dumesic DA, et al.
Экспериментально индуцированный гестационный избыток андрогенов нарушает глюкорегуляцию у самок макак-резусов и их потомства женского пола. Am J Physiol Endocrinol Metab. 2010;299(5):E741–51. Эпубликовано 03.08.2010. doi: 10.1152/ajpendo.00058.2010; Центральный PMCID PubMed: PMCPMC2980359. [Бесплатная статья PMC] [PubMed] [Google Scholar]
24. Роланд А.В., Нунемакер К.С., Келлер С.Р., Моэнтер С.М. Пренатальное воздействие андрогенов программирует метаболическую дисфункцию у самок мышей. J Эндокринол. 2010;207(2):213–23. doi: 10.1677/JOE-10-0217; Центральный PMCID PubMed: PMCPMC3612271. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Tyndall V, Broyde M, Sharpe R, Welsh M, Drake AJ, McNeilly AS. Влияние лечения андрогенами в течение жизни плода и/или новорожденного на функцию яичников у препубертатных и взрослых крыс. Репродукция. 2012;143(1):21–33. Эпублик 20.10.2011. дои: 10.1530/REP-11-0239; Центральный PMCID PubMed: PMCPMC3245827. [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]
26. Padmanabhan V, Veiga-Lopez A, Abbott DH, Recabarren SE, Herkimer C. Программирование развития: влияние пренатального избытка тестостерона и постнатального увеличения веса на индекс чувствительности к инсулину и передача признаков потомству самок с избыточным весом. Эндокринология. 2010;151(2):595–605. Эпублик 2009/12/04. doi: 10.1210/en.2009-1015; Центральный PMCID PubMed: PMCPMC2817622. [Бесплатная статья PMC] [PubMed] [Google Scholar]
27. Lu C, Cardoso RC, Puttabyatappa M, Padmanabhan V. Программирование развития: пренатальный избыток тестостерона и нарушение передачи сигналов инсулина у самок овец. Биол Репрод. 2016;94(5):113 Epub 06.04.2016. doi: 10.1095/biolreprod.115.136283; Центральный PMCID PubMed: PMCPMC4939741. [Бесплатная статья PMC] [PubMed] [Google Scholar]
28. Nohara K, Waraich RS, Liu S, Ferron M, Waget A, Meyers MS, et al.
Избыток андрогенов в процессе развития программирует симпатический тонус и дисфункцию жировой ткани и предрасполагает к кардиометаболическому синдрому у самок мышей. Am J Physiol Endocrinol Metab. 2013;304(12):E1321–30. doi: 10.1152/ajpendo.00620.2012; Центральный PMCID PubMed: PMCPMC3680697. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Am J Physiol Endocrinol Metab. 2013;304(12):E1321–30. doi: 10.1152/ajpendo.00620.2012; Центральный PMCID PubMed: PMCPMC3680697. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29. Wu XY, Li ZL, Wu CY, Liu YM, Lin H, Wang SH, et al.
Эндокринные признаки синдрома поликистозных яичников у пренатально андрогенизированных самок крыс Sprague-Dawley. Эндокр Дж. 2010;57(3):201–9. . [PubMed] [Google Scholar]
30. Yan X, Dai X, Wang J, Zhao N, Cui Y, Liu J. Избыток андрогенов в пренатальном периоде программирует метаболические расстройства у половозрелых самок крыс. J Эндокринол. 2013;217(1):119–29. Эпб 2013/03/19. doi: 10.1530/JOE-12-0577. [PubMed] [Академия Google]
31. Mannerås L, Cajander S, Holmäng A, Seleskovic Z, Lystig T, Lönn M, et al.
Новая крысиная модель, демонстрирующая как яичниковые, так и метаболические характеристики синдрома поликистозных яичников. Эндокринология. 2007;148(8):3781–91. Эпублик от 10 мая 2007 г. doi: 10.1210/en.2007-0168. [PubMed] [Google Scholar]
32. Ван Хаутен Э.Л., Крамер П., Макласки А., Карелс Б., Теммен А.П., Виссер Дж.А. Репродуктивный и метаболический фенотип мышиной модели СПКЯ. Эндокринология. 2012;153(6):2861–9. Эпб 2012/02/14. doi: 10.1210/en.2011-1754. [PubMed] [Академия Google]
Ван Хаутен Э.Л., Крамер П., Макласки А., Карелс Б., Теммен А.П., Виссер Дж.А. Репродуктивный и метаболический фенотип мышиной модели СПКЯ. Эндокринология. 2012;153(6):2861–9. Эпб 2012/02/14. doi: 10.1210/en.2011-1754. [PubMed] [Академия Google]
33. Caldwell AS, Middleton LJ, Jimenez M, Desai R, McMahon AC, Allan CM, et al.
Характеристика репродуктивных, метаболических и эндокринных особенностей синдрома поликистозных яичников на моделях самок гиперандрогенных мышей. Эндокринология. 2014;155(8):3146–59. doi: 10.1210/en.2014-1196. [PubMed] [Google Scholar]
34. Demissie M, Lazic M, Foecking EM, Aird F, Dunaif A, Levine JE. Кратковременное пренатальное воздействие андрогенов вызывает метаболический синдром у взрослых самок крыс. Am J Physiol Endocrinol Metab. 2008;295 (2): E262–8. doi: 10.1152/ajpendo.
- .2008; Центральный PMCID PubMed: PMCPMC2519755. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- . [Бесплатная статья PMC] [PubMed] [Google Scholar]
53. Staley K, Scharfman H. Прерогатива женщины. Нат Нейроски. 2005;8(6):697–9. doi: 10.1038/nn0605-697. [PubMed] [Google Scholar]
54. Леброн-Милад К., Милад М.Р. Половые различия, гонадные гормоны и сеть угасания страха: значение для тревожных расстройств. Биол Тревожное расстройство настроения. 2012;2:3 Epub 2012/02/07. doi: 10.1186/2045-5380-2-3; Центральный PMCID PubMed: PMCPMC3384233. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55. Маликео М., Бенрик А., Стенер-Викторин Э. Модели синдрома поликистозных яичников у грызунов: фенотипические проявления, патофизиология и эффекты различных вмешательств. Семин репрод мед. 2014;32(3):183–93. Эпб 2014/04/08. doi: 10.1055/s-0034-1371090 . [PubMed] [Google Scholar]
56. Норуззаде М., Рамезани Техрани Ф., Седагат К., Години А., Азизи Ф. Влияние пренатального воздействия однократной дозы тестостерона на резистентность к инсулину, толерантность к глюкозе и липидный профиль самок крыс.
 потомство во взрослом возрасте. Дж Эндокринол Инвест. 2015;38(5):489–95. doi: 10.1007/s40618-014-0198-y. [PubMed] [Google Scholar]
потомство во взрослом возрасте. Дж Эндокринол Инвест. 2015;38(5):489–95. doi: 10.1007/s40618-014-0198-y. [PubMed] [Google Scholar]57. Ресслер И.Б., Грейсон Б.Е., Ульрих-Лай Ю.М., Сили Р.Дж. Ожирение, вызванное диетой, усугубляет метаболические и поведенческие эффекты синдрома поликистозных яичников в модели грызунов. Am J Physiol Endocrinol Metab. 2015;308(12):E1076–84. doi: 10.1152/ajpendo.00182.2014; Центральный PMCID PubMed: PMCPMC4469809. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Уолтерс К.А., Аллан К.М., Handelsman DJ. Модели грызунов для синдрома поликистозных яичников человека. Биол Репрод. 2012;86(5):149, 1–12. doi: 10.1095/biolreprod.111.097808. [PubMed] [Google Scholar]
59. Amalfi S, Velez LM, Heber MF, Vighi S, Ferreira SR, Orozco AV, et al.
Пренатальная гиперандрогенизация вызывает метаболические и эндокринные изменения, которые зависят от уровня воздействия тестостерона. ПЛОС Один. 2012;7(5):e37658
doi: 10.1371/journal.pone.0037658 ; Центральный PMCID PubMed: PMCPMC3360026.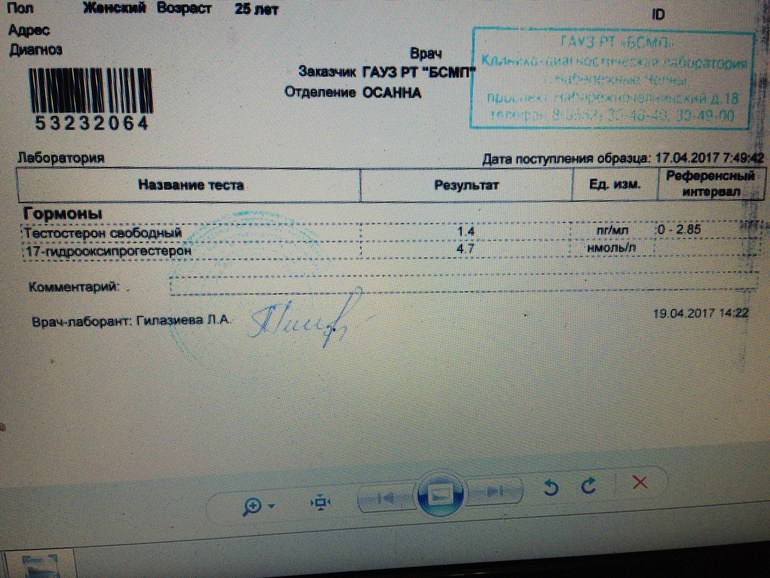 [Бесплатная статья PMC] [PubMed] [Google Scholar]
[Бесплатная статья PMC] [PubMed] [Google Scholar]60. Ramezani Tehrani F, Noroozzadeh M, Zahediasl S, Piryaei A, Hashemi S, Azizi F. Время пренатального воздействия андрогенов влияет на развитие фенотипа, подобного синдрому поликистозных яичников. во взрослом возрасте у самок крыс. Int J Endocrinol Metab. 2014;12(2):e16502
doi: 10.5812/ijem.16502; Центральный PMCID PubMed: PMCPMC4030220. [Бесплатная статья PMC] [PubMed] [Google Scholar]61. Уорд И.Л., Уорд О.Б., Аффузо Д.Д., Лонг В.Д., Френч Д.А., Хендрикс С.Э. Всплеск тестостерона у плода: специфические модуляции, вызванные у самцов крыс материнским стрессом и/или употреблением алкоголя. Хорм Бехав. 2003;43(5):531–9. . [PubMed] [Google Scholar]
62. Сенгупта П. Лабораторная крыса: связь ее возраста с человеческим. Int J Prev Med. 2013;4(6):624–30. ; Центральный PMCID PubMed: PMCPMC3733029. [Бесплатная статья PMC] [PubMed] [Google Scholar]
63. Лонг Дж., Эванс А. О достижении половой зрелости и характере первого эстрального цикла у крыс.
 Ана Рек.1920. с. 244. [Google Scholar]
Ана Рек.1920. с. 244. [Google Scholar]64. Андерсон А.Д., Солорзано К.М., Маккартни К.Р. Детское ожирение и его влияние на развитие СПКЯ у подростков. Семин репрод мед. 2014;32(3):202–13. Эпб 2014/04/08. doi: 10.1055/s-0034-1371092; Центральный PMCID PubMed: PMCPMC4103796. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Misichronis G, Georgopoulos NA, Marioli DJ, Armeni AK, Katsikis I, Piouka AD, et al.
Влияние ожирения на соотношение андростендиона и тестостерона у женщин с синдромом поликистозных яичников (СПКЯ) и гиперандрогенемией. Гинекол Эндокринол. 2012;28(4):249–52. дои: 10.3109/09513590.2011.613965 . [PubMed] [Google Scholar]Андростендион — Объяснение лабораторных результатов
Оптимальный результат:
3,93–13,53 мкг/г креатинина.
Андростендион является эндогенным андрогенным стероидным гормоном и промежуточным звеном в биосинтезе эстрона и тестостерона из дегидроэпиандростерона (ДГЭА). Он тесно связан с андростендиолом.
 Было обнаружено, что андростендион обладает некоторой эстрогенной активностью, как и другие метаболиты ДГЭА. Однако, в отличие от андростендиола, его сродство к рецепторам эстрогена очень низкое.
Было обнаружено, что андростендион обладает некоторой эстрогенной активностью, как и другие метаболиты ДГЭА. Однако, в отличие от андростендиола, его сродство к рецепторам эстрогена очень низкое.ДГЭА сам по себе не является андрогенным, поскольку он не связывается с клеточными андрогенными рецепторами, такими как тестостерон и ДГТ, но является предшественником андростендиона, который затем превращается в тестостерон.
Что означает слишком низкий результат анализа на Андростендион?
У женщин в пременопаузе около половины андростендиона вырабатывается яичниками, а другая половина — надпочечниками. В период менопаузы большая часть андростендиона образуется из ДГЭА(С), вырабатываемого надпочечниками. ДГЭА синтезируется в надпочечниках и быстро сульфатируется до ДГЭА-сульфата (ДГЭАС), что увеличивает время его полужизни в крови. Андростендион, нижележащий метаболит ДГЭА, далее превращается в тестостерон и эпи-тестостерон в почти равных количествах у большинства людей или в эстрон.
 Большее превращение в эстроген, эстрон, происходит у людей с большим количеством жировой ткани.
Большее превращение в эстроген, эстрон, происходит у людей с большим количеством жировой ткани.Низкие уровни этих предшественников андрогенов связаны с симптомами низкого уровня андрогенов, о которых сообщают сами пациенты. DHEA обычно используется в качестве добавки для повышения уровня тестостерона у женщин. Если симптомы низкого уровня андрогенов сохраняются, рассмотрите возможность дополнительного приема ДГЭА для повышения уровня тестостерона, особенно если уровень тестостерона или его нижестоящего и более мощного метаболита ДГТ находится в среднем диапазоне или ниже.
Что означает слишком высокий результат анализа на Андростендион?
Уровень ДГЭА(С), а также его нижестоящих метаболитов, андростендиона и тестостерона, чаще повышен у женщин с резистентностью к инсулину и синдромом поликистозных яичников (СПКЯ). Эти люди обычно имеют более высокие уровни инсулина и ЛГ (соотношение ЛГ/ФСГ обычно > 2,5 у 75% женщин с СПКЯ), что стимулирует высокий синтез ДГЭА(С) надпочечниками и высокий синтез тестостерона яичниками.

10 000+
довольные клиенты100%
удовлетворение★ ★ ★ ★ ★
поддержка клиентовРасширенный план
- ✓ Годовая подписка
- ✓ Пять бесплатных загрузок
- ✓ Отменить в любое время
- ✓ Мгновенные переводы
- ✓ Воспользуйтесь бесплатной формой самостоятельной загрузки
- ✓ Объяснение более 3000 биомаркеров
- ✓ Рекомендации по питанию
- ✓ Специальная поддержка
- ✓ Годовая подписка
- ✓ Пять бесплатных загрузок
- ✓ Отменить в любое время
79 долларов США в год
- ✓ Мгновенные переводы
- ✓ Воспользуйтесь бесплатной формой самостоятельной загрузки
- ✓ Объяснение более 3000 биомаркеров
- ✓ Рекомендации по питанию
- ✓ Специальная поддержка
Безлимитный план
- ✓ Без подписки
- ✓ Десять бесплатных загрузок
- ✓ Неограниченный доступ
- ✓ Мгновенные переводы
- ✓ Воспользуйтесь бесплатной формой самостоятельной загрузки
- ✓ Объяснение более 3000 биомаркеров
- ✓ Рекомендации по питанию
- ✓ Специальная поддержка
- ✓ Без подписки
- ✓ Десять бесплатных загрузок
- ✓ Неограниченный доступ
Полная версия за 250 долларов
Добро пожаловать в Healthmatters Pro.

Экономьте время на интерпретации результатов лабораторных исследований с помощью крупнейшей онлайн-базы данных биомаркеров. Углубленное исследование любого теста у вас под рукой, все хранится и отслеживается в одном месте.
Узнать больше- ✓ Отслеживание результатов нескольких клиентов
- ✓ Плата за установку не взимается
- ✓ Никаких скрытых затрат
- ✓ Отменить в любое время
- ✓ Мгновенные интерпретации
- ✓ Используйте бесплатные шаблоны форм
- ✓ Объяснение более 3000 биомаркеров
- ✓ Дополнительный член команды $25
- ✓ Персональное обучение и поддержка
45 долларов в месяц
Мы применяем проверенные меры для обеспечения безопасности ваших данных.
Мы в HealthMatters стремимся обеспечивать безопасность и конфиденциальность вашей личной информации.

35. Tehrani FR, Noroozzadeh M, Zahediasl S, Piryaei A, Azizi F. Представляем крысиную модель пренатального андроген-индуцированного синдрома поликистозных яичников во взрослом возрасте. Опыт физиол. 2014;99(5):792–801. doi: 10.1113/expphysiol.2014.078055. [PubMed] [Google Scholar]
Представляем крысиную модель пренатального андроген-индуцированного синдрома поликистозных яичников во взрослом возрасте. Опыт физиол. 2014;99(5):792–801. doi: 10.1113/expphysiol.2014.078055. [PubMed] [Google Scholar]
36. Paixão L, Ramos RB, Lavarda A, Morsh DM, Spritzer PM. Животные модели гиперандрогении и изменения морфологии яичников как признаки синдрома поликистозных яичников: систематический обзор. Репрод Биол Эндокринол. 2017;15(1):12 Epub 2017/02/10. дои: 10.1186/с12958-017-0231-з; Центральный PMCID PubMed: PMCPMC5301391. [PMC free article] [PubMed] [Google Scholar]
37. Георгопулос Н.А., Пападакис Э., Армени А.К., Кацикис И., Рупас Н.Д., Панидис Д. Повышенное содержание андростендиона в сыворотке связано с более тяжелым фенотипом у женщин с синдромом поликистозных яичников. (СПКЯ). Гормоны (Афины). 2014;13(2):213–21. . [PubMed] [Google Scholar]
38. Guzel AI, Kuyumcuoğlu U, Celik Y. Факторы, влияющие на степень гирсутизма у пациенток с синдромом поликистозных яичников. Arch Gynecol Obstet. 2012;285(3):767–70. Эпублик 2011/09/10. doi: 10.1007/s00404-011-2077-5. [PubMed] [Google Scholar]
Arch Gynecol Obstet. 2012;285(3):767–70. Эпублик 2011/09/10. doi: 10.1007/s00404-011-2077-5. [PubMed] [Google Scholar]
39. Радж С.Г., Томпсон И.Е., Бергер М.Дж., Талерт Л.М., Таймор М.Л. Диагностическое значение измерения андрогенов при синдроме поликистозных яичников. Акушерство Гинекол. 1978;52(2):169–71. . [PubMed] [Google Scholar]
40. Köşüş N, Köşüş A, Kamalak Z, Hızlı D, Turhan N. Влияние соотношения андрогенов надпочечников и яичников на признаки и симптомы синдрома поликистозных яичников. Гинекол Эндокринол. 2012;28(8):611–4. Эпублик 2012/02/01. дои: 10.3109/09513590.2011.650770 . [PubMed] [Google Scholar]
41. Goodarzi MO, Carmina E, Azziz R. ДГЭА, ДГЭАС и СПКЯ. J Steroid Biochem Mol Biol. 2015;145:213–25. doi: 10.1016/j.jsbmb.2014.06.003. [PubMed] [Google Scholar]
42. Rosenfield RL. Функция яичников и надпочечников при синдроме поликистозных яичников. Эндокринол Метаб Клин Норт Ам. 1999;28(2):265–93. . [PubMed] [Google Scholar]
43. Quinkler M, Sinha B, Tomlinson JW, Bujalska IJ, Stewart PM, Arlt W. Генерация андрогенов в жировой ткани у женщин с простым ожирением — роль 17-бета-гидроксистероиддегидрогеназы в конкретном месте тип 5. J Endocrinol. 2004;183(2):331–42. doi: 10.1677/joe.1.05762 . [PubMed] [Академия Google]
Генерация андрогенов в жировой ткани у женщин с простым ожирением — роль 17-бета-гидроксистероиддегидрогеназы в конкретном месте тип 5. J Endocrinol. 2004;183(2):331–42. doi: 10.1677/joe.1.05762 . [PubMed] [Академия Google]
44. Махаджан Д.К. Стероидогенез при поликистозе яичников человека. Эндокринол Метаб Клин Норт Ам. 1988;17(4):751–69. . [PubMed] [Google Scholar]
45. Pinola P, Piltonen TT, Puurunen J, Vanky E, Sundström-Poromaa I, Stener-Victorin E, et al.
Андрогенный профиль на протяжении жизни у женщин с синдромом поликистозных яичников: Северное многоцентровое совместное исследование. J Clin Endocrinol Metab. 2015;100(9):3400–7. Эпб 2015/07/20. doi: 10.1210/jc.2015-2123. [PubMed] [Google Scholar]
46. Barth JH, Field HP, Yasmin E, Balen AH. Определение гиперандрогении при синдроме поликистозных яичников: измерение тестостерона и андростендиона методом жидкостной хроматографии-тандемной масс-спектрометрии и анализ графиков характеристик оператора-приемника. Евр Дж Эндокринол. 2010;162(3):611–5. Электронная книга 2009 г./12/14. дои: 10.1530/EJE-09-0741. [PubMed] [Google Scholar]
Евр Дж Эндокринол. 2010;162(3):611–5. Электронная книга 2009 г./12/14. дои: 10.1530/EJE-09-0741. [PubMed] [Google Scholar]
47. O’Reilly MW, Taylor AE, Crabtree NJ, Hughes BA, Capper F, Crowley RK, et al.
Гиперандрогенемия предсказывает метаболический фенотип при синдроме поликистозных яичников: полезность андростендиона в сыворотке. J Clin Endocrinol Metab. 2014;99(3):1027–36. doi: 10.1210/jc.2013-3399; Центральный PMCID PubMed: PMCPMC3955250. [Бесплатная статья PMC] [PubMed] [Google Scholar]
48. Lerchbaum E, Schwetz V, Rabe T, Giuliani A, Obermayer-Pietsch B. Гиперандрогенемия при синдроме поликистозных яичников: исследование роли свободного тестостерона и андростендиона в метаболизме фенотип. ПЛОС Один. 2014;9(10):e108263
doi: 10.1371/journal.pone.0108263 ; Центральный PMCID PubMed: PMCPMC4195601. [Бесплатная статья PMC] [PubMed] [Google Scholar]
49. Miri M, Karimi Jashni H, Alipour F. Влияние интенсивности упражнений на изменение веса и половые гормоны (андростендион и свободный тестостерон) у самок крыс с индуцированным эстрадиола валератом СПКЯ. J Яичник Res. 2014;7:37
J Яичник Res. 2014;7:37
doi: 10.1186/1757-2215-7-37; Центральный PMCID PubMed: PMCPMC3997229. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Yang X, Zhang Y, Wu X, Bae CS, Hou L, Kuang H, et al.
Криптотаншинон устраняет репродуктивные и метаболические нарушения у пренатально андрогенизированных крыс посредством регуляции сигнальных механизмов яичников и синтеза андрогенов. Am J Physiol Regul Integr Comp Physiol. 2011;300(4):R869–75. Эпублик 12.01.2011. doi: 10.1152/ajpregu.00334.2010. [PubMed] [Google Scholar]
51. Маркондес Ф.К., Бьянки Ф.Дж., Танно А.П. Определение фаз эстрального цикла крыс: некоторые полезные соображения. Браз Дж. Биол. 2002;62(4А):609–14. Эпублик 11 февраля 2003 г. . [PubMed] [Google Scholar]
52. McLean AC, Valenzuela N, Fai S, Bennett SA. Проведение вагинального лаважа, окрашивание кристаллическим фиолетовым и вагинальная цитологическая оценка для определения стадии эстрального цикла у мышей. J Vis Exp. 2012;(67):e4389Эпб 2012/09/15. дои: 10.3791/4389; Центральный PMCID PubMed: PMCPMC34
дои: 10.3791/4389; Центральный PMCID PubMed: PMCPMC34
