Прививка от столбняка при беременности: Союз педиатров России
Планируем беременность — прививки — ЕМЦ
Вакцинация женщин при подготовке к планируемой беременности
Часто у женщин возникают вопрос, необходимо ли проводить вакцинацию до наступления и во время беременности, от каких инфекций и как это сделать правильно.
Вакцинация при подготовке к беременности обусловлена необходимостью создания иммунного барьера от инфекций. Что дает профилактику первичного инфицирования беременной и плода, и связанные с этим осложнения.
С точки зрения иммунной системы беременность является серьезным потрясением. Во время беременности по-иному работают все органы и системы, что также влияет на иммунитет. Беременность — это состояние, которое может привести к значительному снижению иммунитета.
Важно провести вакцинацию до наступления беременности против следующих инфекций: краснуха, вирусный гепатит В, полиомиелит, дифтерия, столбняк, грипп
Краснуха
Для беременных и их будущих детей опасны практически любые вирусы, размер и свойства которых позволяют им проникать через плацентарный барьер. Среди них особо опасна краснуха. Следствием болезни беременной женщины, не имеющей иммунитета, с 75–95% вероятностью становятся врожденные уродства у плода. Врожденная краснуха является причиной около 20% уродств и встречается с частотой более 2 на 1000 живых новорожденных.
Среди них особо опасна краснуха. Следствием болезни беременной женщины, не имеющей иммунитета, с 75–95% вероятностью становятся врожденные уродства у плода. Врожденная краснуха является причиной около 20% уродств и встречается с частотой более 2 на 1000 живых новорожденных.
Если женщина не болела краснухой, то прививку необходимо сделать как минимум за 2 месяца до начала планируемой беременности. Проверить наличие иммунитета к краснухе можно иммунологическими методами.
Все современные противокраснушные вакцины обладают 95–100% эффективностью. Иммунитет после вакцинации сохраняется более 20 лет. Вакцина содержит живой вирус, курс вакцинации состоит из всего одной прививки, т.е. иммунитет образуется сразу. Еще один положительный эффект вакцинации — это передача антител против краснухи с материнским молоком будущему ребенку.
Прививку против краснухи ни в коем случае нельзя делать во время беременности из-за пусть теоретической, но все же вероятности повреждения плода вакцинным вирусом.
NB! В течение, как минимум, 2 мес. после прививки против краснухи необходимо предохраняться!
Вирусный гепатит В
Строго говоря, вакцинация против вирусного гепатита В необходима всем. Вирус гепатита В не обладает свойством повреждать плод, как вирус краснухи.
Вирус гепатита В передается с кровью и другими биологическими жидкостями. Все беременные женщины подвергаются инъекциям, обследованиям, манипуляциям. Роды и вероятные переливания крови и ее препаратов — все это также представляет собой дополнительный риск возможного инфицирования вирусом гепатита В.
Стандартная схема вакцинации против гепатита В выглядит как 0 – 1 – 6 мес., т.е. выбранный день (0) – через месяц (1) – через 6 мес. (3) после первой прививки. В идеале вакцинацию лучше начать с таким расчетом, чтобы успеть сделать все три прививки до начала беременности — т.е. за 6 месяцев.
Однако при подготовке к планируемой беременности на практике (к сожалению, редко кто думает о прививках за полгода до беременности) эта схема скорее всего будет выглядеть как: выбранный день (0) — через месяц (1) – через 6 – 12 мес. (3) после первой. Другими словами, две прививки с интервалом в 1 мес. обеспечивают иммунитет длительностью до 1 года, третья прививка (сделанная уже после родов) формирует иммунитет длительностью более 15 лет (современные вакцины применяются лишь с 1986 г., поэтому полная длительность иммунитета не выяснена).
(3) после первой. Другими словами, две прививки с интервалом в 1 мес. обеспечивают иммунитет длительностью до 1 года, третья прививка (сделанная уже после родов) формирует иммунитет длительностью более 15 лет (современные вакцины применяются лишь с 1986 г., поэтому полная длительность иммунитета не выяснена).
Вакцина против гепатита В представляет собой чистый «австралийский антиген», то есть лишь часть, а вернее только один из белков вируса. Эффективность вакцинации у взрослых в среднем составляет 85–90%, побочные реакции несущественны (возможны незначительное повышение температуры примерно у 2% привитых и легкая болезненность в месте укола) у 5 – 10% получивших прививку.
Полиомиелит
Риск заражения естественно циркулирующим полиомиелитом и в Европе, и в России ничтожен — последний раз «дикий» вирус полиомиелита в центральных регионах РФ был замечен лет 10 – 15 лет назад. Но есть более чем реальный риск заражения живым вакцинным вирусом, поскольку дети в целях искоренения полиомиелита в стране поголовно получают ОПВ — живую вирусную вакцину.
Во многих странах перед беременностью рекомендуют сделать прививку (ревакцинацию) инактивированной поливакциной (ИПВ). Одной прививки вполне достаточно для «напоминания» иммунитету о существовании вируса.
Дифтерия, столбняк
Прививка против дифтерии и столбняка нужна, если подошел срок очередной вакцинации или если Вы пропустили предыдущую вакцинацию. По календарю прививка против дифтерии и столбняка делается каждые 10 лет после прививки в 16 лет, то есть в 26 лет, 36 лет и т.д. до 60 лет. 90% взрослых об этом не помнят и не знают. Прививка нужна, прежде всего будущему ребенку, которого нужно защищать от такой патологии, как столбняк новорожденных — абсолютно смертельной инфекции. Собственных антител к столбнячной палочке у ребенка нет, и материнские, переданные с молоком в первые дни кормления, окажут малышу неоценимую услугу.
Грипп
Беременным, у кого 2 – 3-й триместр по времени совпадет с эпидемией гриппа, желательно за 2 – 3 месяца до эпидемии сделать прививку против гриппа. Эти рекомендации основаны на свидетельствах более высокой подверженности беременных тяжелым осложнениям гриппа. Помимо этого, прививка особенно настоятельно рекомендуется беременным (равно как и другим взрослым и детям), имеющим хронические заболевания.
Эти рекомендации основаны на свидетельствах более высокой подверженности беременных тяжелым осложнениям гриппа. Помимо этого, прививка особенно настоятельно рекомендуется беременным (равно как и другим взрослым и детям), имеющим хронические заболевания.
Прививку против гриппа лучше сделать до планируемой беременности, если на этот момент доступны вакцины обновленного состава (обычно, они появляются в сентябре), для защиты в текущем эпидемическом сезоне. Современные инактивированные гриппозные вакцины, относящиеся к классам расщепленных (сплит-) и субъединичных препаратов, не противопоказаны и даже рекомендованы к применению во время беременности.
Календарь прививок при подготовке к беременности
| Месяцев до планируемой беременности | Вакцинация |
|
3 месяца
|
гепатит В*(1), краснуха
|
|
2 месяца
|
гепатит В(2), полиомиелит (ИПВ)
|
|
1 месяц
|
дифтерия-столбняк (АДС-М**), грипп***
|
|
1 месяц после родов
|
гепатит В (3)
|
* — если нет возможности начать курс прививок против гепатита В (см. ниже) за 6 мес. до начала планируемой беременности, т.е. полностью закончить вакцинацию до ее начала
ниже) за 6 мес. до начала планируемой беременности, т.е. полностью закончить вакцинацию до ее начала
** — если 2 или 3 триместр беременности совпадают по времени с ежегодной эпидемией гриппа
*** — если подошел срок плановой вакцинации (раз в 10 лет, после 16-летнего возраста) или была пропущена предыдущая вакцинация
В любом случае, во время подготовки к материнству посоветуйтесь с Вашим врачом насчёт необходимых и желательных прививок.
Имеются противопоказания. Ознакомьтесь с инструкцией или проконсультируйтесь у специалиста.
Посетите другие разделы сайта:
- Программа ведения беременности
- Планирование беременности в Екатеринбурге
Ученые: прививки во время беременности не вызывают аутизм у детей
Прививки во время беременности не повышают риск развития аутизма у ребенка, выяснили американские специалисты. Они надеются, что эти данные позволят будущим матерям принять верное решение и защитить ребенка от возможных инфекций.
В США беременные женщины получают вакцину Tdap, призванную защитить их и ребенка в первые месяцы жизни от коклюша, дифтерии и столбняка. Вакцинация проводится на 27-30 неделе беременности.
Несмотря на то, что миф о связи прививок с аутизмом был развенчан практически сразу после своего появления еще в XX веке, многие женщины и сегодня продолжают бояться, что вакцинация может привести к появлению у ребенка расстройства аутистического спектра.
Однако волноваться не о чем, выяснили специалисты американской медицинской организации Kaiser Permanente. Проанализировав десятки тысяч случаев вакцинации во время беременности, они не выявили никакой связи между прививками и развитием аутизма. Результаты исследования были опубликованы в журнале Pediatrics.
«Если какая-то женщина колеблется насчет того, делать ли ей прививку, эти данные должны ее успокоить,
— считает доктор Трейси Бекерра-Калки, ведущий автор исследования. — Риск без вакцинации заболеть коклюшем намного выше, чем гипотетическая возможность осложнений после прививки, поэтому глупо от нее отказываться».
Пик смертности от коклюша приходится на возраст до года, поэтому для младенцев он наиболее опасен. Кроме того, заболевание может привести к воспалению легких, судорогам и поражению головного мозга.
У детей грудного возраста во время приступа кашля за счет сильного напряжения может сформироваться грыжа, выпасть прямая кишка. Причиной смерти, как правило, являются тяжелые проявления коклюша с нарушением мозгового кровообращения, осложненные пневмонией. Крайне неблагоприятно наслоение острых респираторных, стафилококковой инфекций, которые усиливают патологические процессы, развившиеся в результате коклюша, что в свою очередь приводит к более тяжелому течению воспалительных процессов.
«Любая беременная женщина может быть обеспокоена возможными последствиями для еще не рожденных детей, — поясняет Бекерра-Калки. — Мы хотели развенчать мифы, вызывающие это беспокойство. Один из вопросов, которые волнуют женщин, — может ли у ребенка развиться аутизм?»
Гипотеза о связи прививок с развитием аутизма появилась в 1998 году, когда британский исследователь Эндрю Уэйкфилд опубликовал работу, в которой описал несколько случаев аутизма у детей, получавших прививки от кори, краснухи и паротита. Его быстро поймали на подтасовке данных — так, например, у части детей симптомы аутизма проявились еще до прививок, для других же указанные Уэйкфилдом сроки начала заболевания не совпадали с данными, которые предоставляли родители.
Его быстро поймали на подтасовке данных — так, например, у части детей симптомы аутизма проявились еще до прививок, для других же указанные Уэйкфилдом сроки начала заболевания не совпадали с данными, которые предоставляли родители.
Когда медицинский совет Великобритании запросил медицинскую документацию по всем детям, участвовавшим в исследовании Уэйкфилда, обнаружились и другие несостыковки. Ко всему прочему обнаружилось, что пациентов набирали по знакомству, преимущественно среди противников прививок. Уэйкфилд тем временем подчеркивал, что не следует прививать детей от кори, краснухи и паротита одновременно; необходимо использовать отдельные вакцины.
Одну такую вакцину от кори он как раз запатентовал перед проведением исследования.
«Скептическое отношение к вакцинации и прямой отказ от прививок в последние годы привели к появлению мест, где есть целые сообщества с непривитыми детьми, которые более восприимчивы к заболеваниям и представляют угрозу для здоровья более широкой общественности», — поясняют ученые.
Последующие исследования показали, что среди привитых и непривитых детей аутизм развивается у одинакового процента. Такие же результаты получили и исследователи из Kaiser Permanente.
Они проанализировали данные о 82 тыс. детей из Южной Калифорнии, чтобы выяснить, сколько малышей с аутизмом среди тех, чьи матери получили вакцину во время беременности, и тех, чьи отказались.
Оказалось, что среди первых количество детей с расстройствами аутистического спектра составило 1,5%, а среди вторых — 1,8%.
«Никакой связи между вакциной Tdap, полученной во время беременности, и аутизмом у детей обнаружено не было», — резюмирует Бекерра-Калки.
Медицинские эксперты единогласно сходятся во мнении, что вакцинация необходима еще до рождения ребенка, чтобы защитить его в первые месяцы жизни. Предоставление вакцин беременным женщинам позволяет обеспечить детям защиту до того времени, как им будут сделаны первые прививки.
Вопреки еще одному распространенному заблуждению, не способны прививки и подорвать иммунитет против других болезней. Весной 2018 года было опубликовано исследование, опровергающее этот миф.
Весной 2018 года было опубликовано исследование, опровергающее этот миф.
Исследователи изучили медицинские данные 944 детей от двух до четырех лет. В дозе вакцины для ребенка содержится от 1 до 93 антигенов. Таким образом, привитые дети в исследовании в среднем подвергались воздействию 193-435 антигенов. Оказалось, что прививки отнюдь не делают детей более восприимчивыми к другим инфекционным агентам:
между детьми, которые получили все прививки, и теми, кто не получил ни одной, не было никакой разницы в подверженности заболеваниям.
В будущем же, рассчитывают ученые, широкое распространение вакцин позволит сократить потребность в использовании антибиотиков и поможет бороться с ростом распространения так называемых супербактерий, которые особенно устойчивы к лекарствам. Использование антибиотиков способствует развитию и распространению инфекций, которые устойчивы к лекарствам, но вакцины уменьшают число заражений инфекциями и потребность в антибиотиках.
Прививки при планировании беременности
В частности, привиться от особо опасных инфекций, которые могут причинить серьезный вред вашему будущему ребенку. Какие прививки являются необходимыми для того, чтобы обезопасить своего будущего ребенка и саму себя от опасности заражения?
Какие прививки являются необходимыми для того, чтобы обезопасить своего будущего ребенка и саму себя от опасности заражения?
Краснуха
Если вы не болели краснухой, т.е. у вас нет справки, подтверждающей этот факт — лучше не полагаться на память родителей, и сделать прививку как минимум за 2 месяца до начала планируемой беременности. Если хотите, можете проверить наличие иммунитета к краснухе, сдав анализ на антитела, но необязательно. Как показывают зарубежные и российские исследования, прививка, сделанная тем, у кого изначально имелись антитела к краснухе, является безопасной и позволяет усилить иммунитет к инфекции.
Все современные противокраснушные вакцины обладают 95-100-процентной эффективностью, а иммунитет, созданный ими, сохраняется более 20 лет. Поскольку вакцина являет собой живой вирус, курс вакцинации состоит всего из одной прививки, т.е. иммунитет образуется сразу, без ревакцинаций. Еще один положительный эффект вакцинации — это передача антител против краснухи с материнским молоком будущему ребенку.
Прививку против краснухи ни в коем случае нельзя делать во время беременности из-за пусть теоретической, но все же вероятности повреждения плода вакцинным вирусом. То есть необходимо предохраняться, в течение, как минимум, 2 месяцев после прививки от краснухи.
Гепатит В
Хотя вирус гепатита В не обладает свойством повреждать плод, как вирус краснухи, он передается с кровью и другими биологическими жидкостями. Беременные женщины подвергаются инъекциям, обследованиям, манипуляциям. Собственно роды, вероятные переливания крови и ее препаратов — все это также представляет собой дополнительный риск инфицирования матери и ребенка вирусом гепатита В.
Стандартная схема вакцинации против гепатита В выглядит как 0–1–6 мес., т.е. выбранный день(0)-через месяц(1)-через 6 мес.(3) после первой прививки. В идеале вакцинацию лучше начать с таким расчетом, чтобы успеть сделать все три прививки до начала беременности — т.е. за 6 месяцев. Это позволит гарантировать защиту в среднем у 85-90% привитых.
Однако при подготовке к планируемой беременности на практике (к сожалению, редко кто думает о прививках за полгода до беременности) эта схема скорее всего будет выглядеть как: выбранный день(0)-через месяц(1)-через 6-12 месяцев(3) после первой. Другими словами, две прививки с интервалом в 1 мес. обеспечивают иммунитет длительностью до 1 года, третья прививка (сделанная уже после родов) формирует иммунитет длительностью более 15 лет. К недостаткам такого подхода следует отнести тот факт, что гарантировать защиту между 2 и 3 прививками можно у несколько меньшего (75%) числа привитых.
Существующая альтернативная схема иммунизации против гепатита В (0–1–2-12 мес.) используется, в основном, ввиду экстренных показаний и отличается более интенсивным и надежным формированием иммунитета через два месяца от начала прививок. Относительными недостатками этой схемы следует признать ее более высокую стоимость, большее число прививок и визитов к врачу.
Вакцина против гепатита В представляет собой лишь часть, а вернее только один из белков вируса. Эффективность вакцинации у взрослых в среднем составляет 85-90%, а побочные реакции несущественны — возможны незначительное повышение температуры (у 2% привитых) и легкая болезненность в месте укола.
Эффективность вакцинации у взрослых в среднем составляет 85-90%, а побочные реакции несущественны — возможны незначительное повышение температуры (у 2% привитых) и легкая болезненность в месте укола.
Дополнительные прививки
- Прививка против дифтерии и столбняка желательна, если подошел срок очередной вакцинации, или если Вы пропустили предыдущую вакцинацию. По календарю прививка против дифтерии и столбняка делается каждые 10 лет после прививки в 16 лет, то есть в 26 лет, 36 лет и т.д. до 60 лет. 90% взрослых об этом не помнят или не знают. Собственных антител к столбнячной палочке у ребенка нет, и материнские, переданные с молоком в первые дни кормления, окажут малышу неоценимую услугу.
- В некоторых европейских странах практикуется обязательная прививка против полиомиелита для женщин, планирующих беременность. Объясняется это тем, что существует опасность вирусной инфекции, если рядом с беременной женщиной находится ребенок, которого только что привили от полиомиелита живой полиомиелитной вакциной (ОПВ).
 В России эта вакцина входит в календарь обязательных прививок. Вакцинный вирус размножения в кишечнике привитого, и выделяется в окружающую среду. Именно поэтому во Франции и ряде других стран перед беременностью рекомендуют сделать прививку (ревакцинацию) инактивированной полиовакциной (ИПВ).
В России эта вакцина входит в календарь обязательных прививок. Вакцинный вирус размножения в кишечнике привитого, и выделяется в окружающую среду. Именно поэтому во Франции и ряде других стран перед беременностью рекомендуют сделать прививку (ревакцинацию) инактивированной полиовакциной (ИПВ). - Перед прогнозируемой эпидемией врачи рекомендуют беременным сделать прививку от гриппа. Современные прививки содержат инактивированный (убитый) вирус гриппа, поэтому считается, что он безопасен для ребенка. Однако если срок вашей беременности меньше, чем 14 недель, то эту прививку делать не следует. Кроме того, следует иметь в виду, что ни одна прививка от гриппа не гарантирует, что вы не заболеете. Все равно остается пусть маленькая, но неприятная возможность перенести грипп, часто в стертой форме.
При подготовке к беременности рекомендуется следующий календарь прививок
| Число месяцев до планируемой беременности | Вакцинация | Условие |
|---|---|---|
| 3 месяца | гепатит В (1), краснуха | если нет возможности начать курс прививок против гепатита В за 6 мес.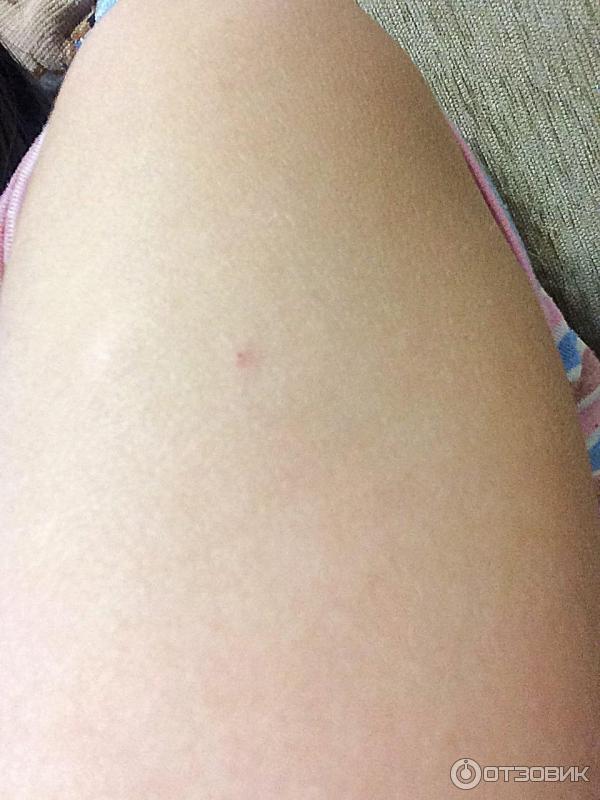 до начала планируемой беременности, т.е. полностью закончить вакцинацию до ее начала до начала планируемой беременности, т.е. полностью закончить вакцинацию до ее начала |
| 2 месяца | гепатит В (2), полиомиелит (ИПВ) | |
| 1 месяц | дифтерия-столбняк (АДС-М), грипп | если подошел срок плановой вакцинации (раз в 10 лет, после 16-летнего возраста) или была пропущена предыдущая вакцинация |
| 1 месяц | грипп | если эпидемия гриппа приходится на второй-третий триместр |
| 1 месяц после родов | гепатит В (3) |
Источники
- Chervenak FA., McCullough LB., Bornstein E., Johnson L., Katz A., McLeod-Sordjan R., Nimaroff M., Rochelson BL., Tekbali A., Warman A., Williams K., Grünebaum A. Professionally responsible coronavirus disease 2019 vaccination counseling of obstetrical and gynecologic patients. // Am J Obstet Gynecol — 2021 — Vol — NNULL — p.; PMID:33539825
- Demissie SD., Kozuki N., Olorunsaiye CZ., Gebrekirstos P., Mohammed S.
 , Kiapi L., Chantler T., Karafillakis E., Landegger J. Community engagement strategy for increased uptake of routine immunization and select perinatal services in north-west Ethiopia: A descriptive analysis. // PLoS One — 2020 — Vol15 — N10 — p.e0237319; PMID:33119604
, Kiapi L., Chantler T., Karafillakis E., Landegger J. Community engagement strategy for increased uptake of routine immunization and select perinatal services in north-west Ethiopia: A descriptive analysis. // PLoS One — 2020 — Vol15 — N10 — p.e0237319; PMID:33119604 - Mellucci C., Tamburrano A., Cassano F., Galletti C., Sguera A., Damiani G., Laurenti P. Vaccine Hesitancy among Master’s Degree Students in Nursing and Midwifery: Attitude and Knowledge about Influenza Vaccination. // Int J Environ Res Public Health — 2020 — Vol17 — N19 — p.; PMID:33019559
- Kaya ÇA., Akman M., Ünalan PC., Çifçili S., Uzuner A., Akdeniz E. Comparison of preventive health service provision before and after reorganization of primary care in Turkey: a community-based study. // Prim Health Care Res Dev — 2019 — Vol20 — NNULL — p.e119; PMID:32323643
- Bechini A., Moscadelli A., Pieralli F., Sartor G., Seravalli V., Panatto D., Amicizia D., Bonanni P., Boccalini S. Impact assessment of an education course on vaccinations in a population of pregnant women: a pilot study.
 // J Prev Med Hyg — 2019 — Vol60 — N1 — p.E5-E11; PMID:31041404
// J Prev Med Hyg — 2019 — Vol60 — N1 — p.E5-E11; PMID:31041404 - Ghimire PR., Agho KE., Ezeh OK., Renzaho AMN., Dibley M., Raynes-Greenow C. Under-Five Mortality and Associated Factors: Evidence from the Nepal Demographic and Health Survey (2001⁻2016). // Int J Environ Res Public Health — 2019 — Vol16 — N7 — p.; PMID:30965556
- Braczkowska B., Kowalska M., Barański K., Gajda M., Kurowski T., Zejda JE. Parental Opinions and Attitudes about Children’s Vaccination Safety in Silesian Voivodeship, Poland. // Int J Environ Res Public Health — 2018 — Vol15 — N4 — p.; PMID:29662022
- Pazol K., Robbins CL., Black LI., Ahrens KA., Daniels K., Chandra A., Vahratian A., Gavin LE. Receipt of Selected Preventive Health Services for Women and Men of Reproductive Age — United States, 2011-2013. // MMWR Surveill Summ — 2017 — Vol66 — N20 — p.1-31; PMID:29073129
- Ozaki T., Ono K., Gyouten M., Mizuta J., Fujita Y., Inoshita H., Seto H., Ohasi I., Mino M., Kokudo S., Ikeda H.
 , Kawata K., Hamano H., Fukuoka H. Prevention of Lifestyle-related Diseases by Utilization of Newly Developed Health Record Booklet "My Karte" in Mitoyo and Kanonji Areas. // Nihon Eiseigaku Zasshi — 2017 — Vol72 — N1 — p.10-14; PMID:28154353
, Kawata K., Hamano H., Fukuoka H. Prevention of Lifestyle-related Diseases by Utilization of Newly Developed Health Record Booklet "My Karte" in Mitoyo and Kanonji Areas. // Nihon Eiseigaku Zasshi — 2017 — Vol72 — N1 — p.10-14; PMID:28154353 - Weiner JL., Fisher AM., Nowak GJ., Basket MM., Gellin BG. Childhood immunizations: First-time expectant mothers’ knowledge, beliefs, intentions, and behaviors. // Vaccine — 2015 — Vol33 Suppl 4 — NNULL — p.D92-8; PMID:26615175
Исходы у младенцев после введения вакцины Tdap во время беременности: обсервационное исследование
Текст статьи
Меню статьи
- Статья
Текст - Артикул
информация - Цитата
Инструменты - Поделиться
- Быстрое реагирование
- Артикул
метрика - Оповещения
Педиатрия
Исследования
Infant outcomes after exposure to Tdap vaccine in pregnancy: an observational study
- Tony Walls1,
- Patricia Graham1,2,
- Helen Petousis-Harris3,
- Linda Hill4,
- Nicola Austin1,2
- 1 Кафедра педиатрии Университета Отаго, Крайстчерч, Новая Зеландия
- 2 Районный совет здравоохранения Кентербери, Крайстчерч, Новая Зеландия
- 3 Кафедра общей практики и первичной медико-санитарной помощи Оклендского университета, Окленд, Новая Зеландия
- 4 Центр последипломного обучения сестринскому делу, Университет Отаго, Крайстчерч, Новая Зеландия
- доктор Тони Уоллс; tony.
 walls{at}otago.ac.nz
walls{at}otago.ac.nz
Abstract
Цель Вакцинация против коклюша во время беременности недавно была рекомендована как в США, так и в Великобритании для предотвращения коклюшной инфекции у младенцев. Несмотря на отсутствие явных опасений по поводу безопасности введения вакцины Tdap во время беременности, имеются лишь ограниченные данные о безопасности. Мы стремились внимательно следить за детьми, подвергшимися воздействию Tdap во время беременности, чтобы выявить любые неблагоприятные последствия, которые могут быть связаны с вакциной.
Дизайн Это было проспективное обсервационное исследование, в ходе которого собиралась информация для оценки безопасности вакцины Tdap для младенцев, подвергшихся воздействию вакцины во время беременности. Младенцы наблюдались в течение от 6 до 12 месяцев после рождения, при этом 84% завершили 12 месяцев наблюдения. Информация была получена из объективных источников, включая регулярные визиты к врачу и записи о прививках, где это возможно, а также частые отчеты родителей.
Настройка Район Кентербери в Новой Зеландии.
Пациенты Группа из 403 младенцев, матери которых получили вакцину Tdap.
Основные показатели исхода Гестационный возраст при рождении, параметры роста, врожденные аномалии, статус иммунизации и своевременность иммунизации, развитие коклюшной инфекции.
Результаты Не было никаких существенных различий в массе тела при рождении, гестационном возрасте при рождении, врожденных аномалиях или росте младенцев по сравнению с исходными данными о населении. Младенцы матерей, получивших вакцину, с большей вероятностью получали прививки вовремя в младенчестве. В этой когорте не было случаев коклюша, несмотря на высокий уровень заболеваемости среди населения. Мы не обнаружили каких-либо побочных эффектов, связанных с воздействием вакцины.
Выводы Эти данные дополняют растущее количество доказательств того, что введение вакцины Tdap во время беременности является подходящей стратегией для снижения бремени коклюша у младенцев.
Регистрация клинических испытаний Австралия Новая Зеландия Реестр клинических испытаний ACTRN12613001045707.
- ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ
- ОБЩЕСТВЕННОЕ ЗДРАВООХРАНЕНИЕ
Это статья с открытым доступом, распространяемая в соответствии с некоммерческой лицензией Creative Commons Attribution (CC BY-NC 4.0), которая разрешает другим распространять, ремикшировать, адаптировать, строить на ее основе работать в некоммерческих целях и лицензировать свои производные работы на других условиях, при условии, что оригинальная работа правильно процитирована и использование является некоммерческим. См.: http://creativecommons.org/licenses/by-nc/4.0/
http://dx.doi.org/10.1136/bmjopen-2015-009536
Статистика с сайта Altmetric.com
Запрос разрешений
направит вас к службе RightsLink Центра защиты авторских прав. Вы сможете получить быструю цену и мгновенное разрешение на повторное использование контента различными способами.
- ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ
- ОБЩЕСТВЕННОЕ ЗДРАВООХРАНЕНИЕ
Сильные стороны и ограничения данного исследования
Мы часто контактировали с родителями, чтобы определить неблагоприятные события, используя различные способы общения.
Везде, где это было возможно, показатели состояния здоровья младенцев были получены из объективных исходных данных.
Наша исследуемая популяция вряд ли будет действительно репрезентативной для общей популяции из-за наших методов набора.
Мы не включили группу сравнения младенцев, не подвергшихся вакцинации во время беременности.
Введение
Младенцы раннего возраста подвергаются наибольшему риску осложнений от коклюша в случае его заражения. В отсутствие материнской иммунизации младенцы в возрасте до 2 месяцев, как правило, не защищены от коклюша до тех пор, пока их не вакцинируют, так как через плаценту переносится мало защитных антител или они вообще не переносятся. Это связано с относительно низкими титрами антител у большинства беременных женщин, поскольку в целом происходит активный плацентарный перенос материнских коклюшных антител, что приводит к более высоким уровням коклюшно-специфических IgG у младенцев, чем у матери.1 В 2012 г. Консультативный комитет США по практике иммунизации (ACIP) рекомендовал вводить бесклеточную коклюшную вакцину (Tdap) любому лицу, которое может быть в контакте с младенцами в возрасте до 12 месяцев, включая беременных женщин, независимо от предыдущей вакцинации Tdap2. Аналогичным образом, в 2012 г. Комитет по вакцинации и иммунизации Великобритании согласился ввести программу иммунизации женщин с Tdap на более поздних сроках беременности.3 Рекомендуется введение вакцины беременным женщинам, поскольку она не только защищает мать от коклюша, но и индуцирует антитела. которые передаются младенцу до рождения и обеспечивают защиту в течение первых недель жизни2. ACIP признал, что безопасность Tdap imm унификация во время беременности систематически не изучалась, а единственные доступные данные получены из небольших исследований, постмаркетингового наблюдения и Системы отчетности о побочных эффектах вакцин (VAERS) США.
Это связано с относительно низкими титрами антител у большинства беременных женщин, поскольку в целом происходит активный плацентарный перенос материнских коклюшных антител, что приводит к более высоким уровням коклюшно-специфических IgG у младенцев, чем у матери.1 В 2012 г. Консультативный комитет США по практике иммунизации (ACIP) рекомендовал вводить бесклеточную коклюшную вакцину (Tdap) любому лицу, которое может быть в контакте с младенцами в возрасте до 12 месяцев, включая беременных женщин, независимо от предыдущей вакцинации Tdap2. Аналогичным образом, в 2012 г. Комитет по вакцинации и иммунизации Великобритании согласился ввести программу иммунизации женщин с Tdap на более поздних сроках беременности.3 Рекомендуется введение вакцины беременным женщинам, поскольку она не только защищает мать от коклюша, но и индуцирует антитела. которые передаются младенцу до рождения и обеспечивают защиту в течение первых недель жизни2. ACIP признал, что безопасность Tdap imm унификация во время беременности систематически не изучалась, а единственные доступные данные получены из небольших исследований, постмаркетингового наблюдения и Системы отчетности о побочных эффектах вакцин (VAERS) США. 4 Они пришли к выводу, что «имеющиеся данные этих исследований не предполагают какой-либо повышенной частоты или необычные модели побочных эффектов у беременных женщин, получивших Tdap, и что несколько серьезных побочных эффектов, о которых сообщалось, вряд ли были вызваны вакциной».
4 Они пришли к выводу, что «имеющиеся данные этих исследований не предполагают какой-либо повышенной частоты или необычные модели побочных эффектов у беременных женщин, получивших Tdap, и что несколько серьезных побочных эффектов, о которых сообщалось, вряд ли были вызваны вакциной».
В небольшом рандомизированном контролируемом исследовании (РКИ) фазы 1–2 Munoz et al 5 продемонстрировали, что вакцину Tdap можно безопасно вводить женщинам во время беременности без значительных побочных эффектов у матери или ребенка. В исследование были включены 33 младенца, подвергшихся внутриутробному воздействию вакцины Tdap. Учитывая трудности, связанные с клиническими испытаниями вакцин, вводимых во время беременности, маловероятно, что будут проведены достаточно мощные РКИ для оценки безопасности вакцины Tdap. Поэтому мы полагаемся на постепенное накопление данных небольших испытаний и обсервационных исследований.
Целью данного исследования было описание любых нежелательных явлений после иммунизации, связанных с введением вакцины Tdap во время беременности, с акцентом на исходы у младенцев.
Пациенты и методы
Календарь иммунизации Новой Зеландии (НЗ) включает в себя трехдозовый календарь бесклеточной коклюшной вакцины, вводимой детям в возрасте 6 недель, 3 и 5 месяцев, с ревакцинацией в возрасте 4 и 11 лет. В ответ на недавнюю эпидемию коклюша в Новой Зеландии в 2012 году Министерство здравоохранения ввело вакцину Tdap во время беременности для женщин в сроке от 28 до 38 недель беременности. Финансируемой вакциной была Boostrix (GSK). В Новой Зеландии все прививки предоставляются родителям бесплатно через врачей общей практики (ВОП) и регистрируются в Национальном регистре иммунизации (NIR). В период с октября по декабрь 2014 г. национальные показатели охвата иммунизацией составили 94% для обоих младенцев в возрасте 8 и 24 месяцев6. год). Он является частью более крупного общенационального исследования, посвященного неблагоприятным событиям после вакцинации Tdap во время беременности, и уделяет особое внимание лонгитюдным исходам у младенцев.
Женщины были включены в исследование, если они получили вакцину Tdap между 28 и 38 неделями беременности. Они должны были соблюдать стандартную дородовую помощь, включая как минимум одно ультразвуковое исследование на ранних сроках беременности. Это должно было гарантировать, что любые серьезные врожденные аномалии, выявленные на ранних сроках беременности, не будут позже связаны с вакцинацией. Мы исключили женщин, плод которых имел врожденные аномалии, тяжелые структурные и/или хромосомные аномалии, выявленные в ходе пренатального скрининга.
Они должны были соблюдать стандартную дородовую помощь, включая как минимум одно ультразвуковое исследование на ранних сроках беременности. Это должно было гарантировать, что любые серьезные врожденные аномалии, выявленные на ранних сроках беременности, не будут позже связаны с вакцинацией. Мы исключили женщин, плод которых имел врожденные аномалии, тяжелые структурные и/или хромосомные аномалии, выявленные в ходе пренатального скрининга.
Женщины заполнили форму согласия со своим терапевтом перед введением Tdap, спросив, согласны ли они с тем, что исследовательская группа свяжется с ними. Заявления врачей общей практики о возмещении расходов использовались для выявления женщин, получивших вакцину, и с теми, кто дал согласие, связывались по телефону в течение 2 недель после введения. Наблюдение за младенцами планировалось до 1 года. Первая регистрация была проведена в сентябре 2012 г., а последующее наблюдение за младенцами продолжалось до ноября 2014 г.
16 сентября 2103 г. исследованию был присвоен универсальный номер испытания (U1111-1148-0718) и оно было зарегистрировано в Реестре клинических испытаний Австралии и Новой Зеландии ( ACTRN12613001045707) от 19Сентябрь 2013 г.
исследованию был присвоен универсальный номер испытания (U1111-1148-0718) и оно было зарегистрировано в Реестре клинических испытаний Австралии и Новой Зеландии ( ACTRN12613001045707) от 19Сентябрь 2013 г.
Финансирование осуществлялось за счет неограниченного гранта Кентерберийского окружного совета здравоохранения.
Информация о беременности и исходах у младенцев была собрана из рассказов матерей и подтверждена различными объективными источниками, включая записи о рождении, заметки ведущей акушерки (LMC; главный медицинский работник, ответственный за новорожденного до 6 недельного возраста) и рутинные Младенческий 6-недельный осмотр у врача общей практики. К ним относятся любые неблагоприятные события у женщин во время беременности, гестационный возраст младенцев при рождении, масса тела при рождении, длина тела и окружность головы, врожденные аномалии и любые события, связанные с медицинским обслуживанием младенцев после рождения.
Гестационный возраст определяли по последнему менструальному периоду, а там, где он был недоступен, для его оценки использовали УЗИ на ранних сроках беременности. Преждевременные роды определялись как любой ребенок, рожденный до 37 недель гестации, а дети, рожденные <32 недель гестации, определялись как очень недоношенные. Низкая масса тела при рождении определялась как <2500 г с очень низкой массой тела при рождении <1500 г, независимо от гестационного возраста при рождении. Консенсусный список Брайтонского сотрудничества терминов и определений ключевых событий для мониторинга иммунизации во время беременности использовался для классификации значимых медицинских событий и врожденных аномалий.7
Преждевременные роды определялись как любой ребенок, рожденный до 37 недель гестации, а дети, рожденные <32 недель гестации, определялись как очень недоношенные. Низкая масса тела при рождении определялась как <2500 г с очень низкой массой тела при рождении <1500 г, независимо от гестационного возраста при рождении. Консенсусный список Брайтонского сотрудничества терминов и определений ключевых событий для мониторинга иммунизации во время беременности использовался для классификации значимых медицинских событий и врожденных аномалий.7
Данные об иммунизации младенцев были получены из NIR6, и мы задокументировали как получение вакцины, так и своевременность вакцинации. Своевременная иммунизация определялась как вакцинация младенца в течение 1 месяца от рекомендованной даты. Параметры роста младенцев были получены во время рутинных посещений клиник по уходу за детьми по месту жительства (Plunket Nurse) вплоть до посещения в возрасте около 5–7 месяцев.
Все эти услуги бесплатно предоставляются семьям в рамках плановой медицинской помощи младенцам. Z-показатели использовались для всех измерений роста, где это уместно, с использованием диаграмм роста ВОЗ.
Z-показатели использовались для всех измерений роста, где это уместно, с использованием диаграмм роста ВОЗ.
Ежемесячно матерям рассылали анкету по почте, электронной почте или смс, в которой спрашивали, были ли младенцы в тесном контакте с кем-либо с доказанной коклюшной инфекцией или необъяснимым кашлем, длящимся > 2 недель, или был ли у ребенка постоянный кашель продолжительностью >10 дней. В каждом случае было предпринято не менее трех попыток связаться с родителями, используя несколько методов контакта, чтобы обеспечить полное последующее наблюдение за младенцами. Клинический осмотр был организован для любого ребенка, имевшего значительный контакт с больным коклюшем или симптомами, характерными для коклюша. Подробная информация о любых медицинских осмотрах, необходимых детям и не проведенных исследовательским персоналом, была получена из больничных или семейных записей.
Сообщения о серьезных нежелательных явлениях, которые наблюдались с медицинской точки зрения у матери или их младенцев, были зарегистрированы в Центре мониторинга побочных реакций при Новозеландском центре фармакологического надзора Университета Отаго.
Это описательный анализ, и результаты представлены в цифрах и процентах. Было проведено сравнение показателей и своевременности иммунизации младенцев между изучаемой популяцией и общей популяцией младенцев региона Кентербери в течение периода исследования с использованием коэффициентов риска.
Результаты
Мы были уведомлены о 1211 женщинах, получивших вакцину Tdap во время беременности, и набрали 470. Причины отказа от участия перечислены на рисунке 1. Средний возраст женщин на момент вакцинации Tdap составлял 32 года (диапазон 15 лет). –45 лет), а средний срок беременности составил 33,9 недель. Восемьдесят шесть процентов женщин были европейками Новой Зеландии, из них 4% маори и 8% азиатки. Шестьдесят две женщины также получили трехвалентную вакцину против гриппа во время беременности, часто одновременно с вакциной Tdap.
Рисунок 1
Зачисление в исследование (FU, последующее наблюдение).
Последующие данные были получены от 403 женщин и 408 младенцев (403 одноплодных, 6 близнецов и 1 мертворожденный), 345 из них в возрасте до 12 месяцев и 63 — в возрасте до 6–12 месяцев. Мы решили включить в анализ младенцев, наблюдавшихся как минимум до 6 месяцев, так как мы чувствовали, что к этому времени должно произойти большинство значимых с медицинской точки зрения событий, связанных с материнской вакцинацией. В 67 случаях были доступны только материнские данные, которые не были включены в анализ. Из исследования было исключено 28 младенцев.
Мы решили включить в анализ младенцев, наблюдавшихся как минимум до 6 месяцев, так как мы чувствовали, что к этому времени должно произойти большинство значимых с медицинской точки зрения событий, связанных с материнской вакцинацией. В 67 случаях были доступны только материнские данные, которые не были включены в анализ. Из исследования было исключено 28 младенцев.
Триста восемьдесят пять наблюдаемых новорожденных родились в срок (94%). Средний гестационный возраст при родах составлял 39,2 недели (диапазон 33–42 недели). Было шесть пар близнецов (3 пары родились в срок, 2 пары родились на 36 неделях и 1 на 33 неделях беременности). Только 23 (6%) младенца родились на сроке менее 37 недель беременности. Средняя масса тела при рождении составила 3490 г, только один ребенок весил <1500 г и восемь младенцев весили от 1500 до 2500 г.
У десяти младенцев (2,5%) были выявлены значимые медицинские события или врожденные аномалии, как указано в блоке 1. Один младенец родился мертвым (0,2%), и, несмотря на патологоанатомическое исследование (врожденных аномалий выявлено не было), причина этого неизвестно. В анамнезе у матери были мертворождения.
В анамнезе у матери были мертворождения.
Вставка 1
Медицинские события и врожденные аномалии у детей, подвергшихся воздействию TDAP во время беременности
Gastroschisis
Малротация кишечника
СОЗДАНИЯ НОВАЛА.
Дисплазия тазобедренного сустава
Аномалия правой руки
Ларингомаляция
В общей сложности 303 ребенка завершили 6-недельный осмотр, а 278 — 5-месячный. На рисунке 2 показаны z-показатели массы тела при рождении, при 6-недельной проверке и в возрасте от 5 до 7 месяцев, каждый из которых имеет нормальное распределение.
Рисунок 2
Z-показатели массы тела младенцев при рождении, в возрасте 6 недель и 5–7 месяцев.
Только девять младенцев имели контакт с подтвержденным случаем коклюша в течение периода наблюдения. Шестьдесят семь младенцев находились в домашнем контакте с человеком с длительным кашлем, и 64 младенца, как сообщается, сами страдали кашлем, продолжающимся более 10 дней. Ни у одного из этих младенцев впоследствии не был диагностирован коклюш. Только девять младенцев были госпитализированы в течение периода наблюдения. У троих из них было заболевание дыхательных путей, у одного из них была доказана инфекция гриппа, и все трое дали отрицательный результат на коклюш.
Ни у одного из этих младенцев впоследствии не был диагностирован коклюш. Только девять младенцев были госпитализированы в течение периода наблюдения. У троих из них было заболевание дыхательных путей, у одного из них была доказана инфекция гриппа, и все трое дали отрицательный результат на коклюш.
Доля младенцев в когорте SMART VIP, получивших своевременную иммунизацию, составила 97,8%, 98,5% и 94,2% в возрасте 6 недель, 3 и 5 месяцев соответственно. Для каждого события вакцинации это было значительно лучше, чем для всей когорты младенцев Кентербери за тот же период времени (таблица 1). Таблица 10003
Обсуждение
Несмотря на широкое применение вакцины Tdap в США и Великобритании, данные о безопасности применения вакцины Tdap во время беременности ограничены. На сегодняшний день это крупнейшее исследование, посвященное изучению индивидуальных последствий для здоровья и проспективному мониторингу нежелательных явлений у младенцев, чьи матери получали вакцину Tdap во время беременности.
В этом исследовании изучались исходы у младенцев, и не было обнаружено свидетельств учащения побочных эффектов у младенцев, подвергшихся внутриутробному воздействию вакцины Tdap, по сравнению с исходными показателями в популяции. Исходы родов, параметры роста и частота врожденных аномалий были очень похожи на исходные показатели в Новой Зеландии. В отчете Министерства здравоохранения Новой Зеландии о клинических показателях родовспоможения8 сообщается, что 8% всех живых младенцев рождаются между 32 и 36 неделями беременности в регионе Кентербери. Это было выше, чем 6% уровень недоношенности в нашей когорте.
В реестре врожденных пороков Новой Зеландии9 указана частота врожденных аномалий в диапазоне от 4000 до 6000 на 100 000 родов в больнице (от 4% до 6%) за 2000–2012 годы. В нашей когорте показатели были значительно ниже этого показателя — 2,7%. Эти сравнения следует проводить с осторожностью, учитывая избирательный характер нашей исследуемой популяции. В частности, вполне вероятно, что частота врожденных аномалий в нашей исследуемой популяции будет ниже, чем сравнительные данные, учитывая, что наша когорта не включала младенцев, родившихся до 33 недель беременности. Тем не менее, обнадеживает тот факт, что эти данные не указывают на потенциальные неблагоприятные последствия.
Тем не менее, обнадеживает тот факт, что эти данные не указывают на потенциальные неблагоприятные последствия.
Единственным исходом для младенцев, который значительно отличался в нашей когорте от популяции младенцев в Кентербери, была своевременность иммунизации младенцев. Своевременная иммунизация детей раннего возраста является одним из ключевых мероприятий общественного здравоохранения, рекомендуемых для снижения риска заболевания коклюшем у детей раннего возраста во время эпидемии. Отсроченная иммунизация неоднократно ассоциировалась с более высокими показателями заболеваемости коклюшем у младенцев и госпитализаций по поводу коклюша.10
Младенцы, рожденные от матерей из нашей когорты, получивших вакцину Tdap, с большей вероятностью получали вакцины вовремя по сравнению с показателями населения Кентербери. Одно из возможных объяснений этого заключается в том, что женщины, которые решили пройти вакцинацию и согласились участвовать в исследовании, были лучше осведомлены о продолжающейся эпидемии коклюша в обществе и, следовательно, с большей вероятностью решат вовремя вакцинировать своих детей. В Новой Зеландии большинство LMC являются акушерками, которые не могут вводить вакцины. Если женщины хотят пройти вакцинацию, они должны посетить своего врача общей практики, что не является обычной частью дородового наблюдения. Этот дополнительный визит к врачу общей практики даст возможность обсудить преимущества иммунизации как для них самих, так и для их детей с практикующим врачом. Внедрение вакцины могло непреднамеренно привести к большему количеству контактов будущих матерей со своими врачами и большему количеству дискуссий об иммунизации.
В Новой Зеландии большинство LMC являются акушерками, которые не могут вводить вакцины. Если женщины хотят пройти вакцинацию, они должны посетить своего врача общей практики, что не является обычной частью дородового наблюдения. Этот дополнительный визит к врачу общей практики даст возможность обсудить преимущества иммунизации как для них самих, так и для их детей с практикующим врачом. Внедрение вакцины могло непреднамеренно привести к большему количеству контактов будущих матерей со своими врачами и большему количеству дискуссий об иммунизации.
В общем, нет никаких теоретических проблем безопасности при введении субъединичных вакцин беременным женщинам. Некоторые вакцины, такие как вакцина против столбняка, широко используются в этой группе без признаков серьезных побочных эффектов у матери или ребенка.11 Сроки иммунизации матери также являются важным фактором безопасности вакцины. Когда вакцина Tdap вводится между 28 и 38 неделями беременности, риск врожденных аномалий, вероятно, будет низким, учитывая, что период основного эмбриогенеза плода был завершен к этой беременности.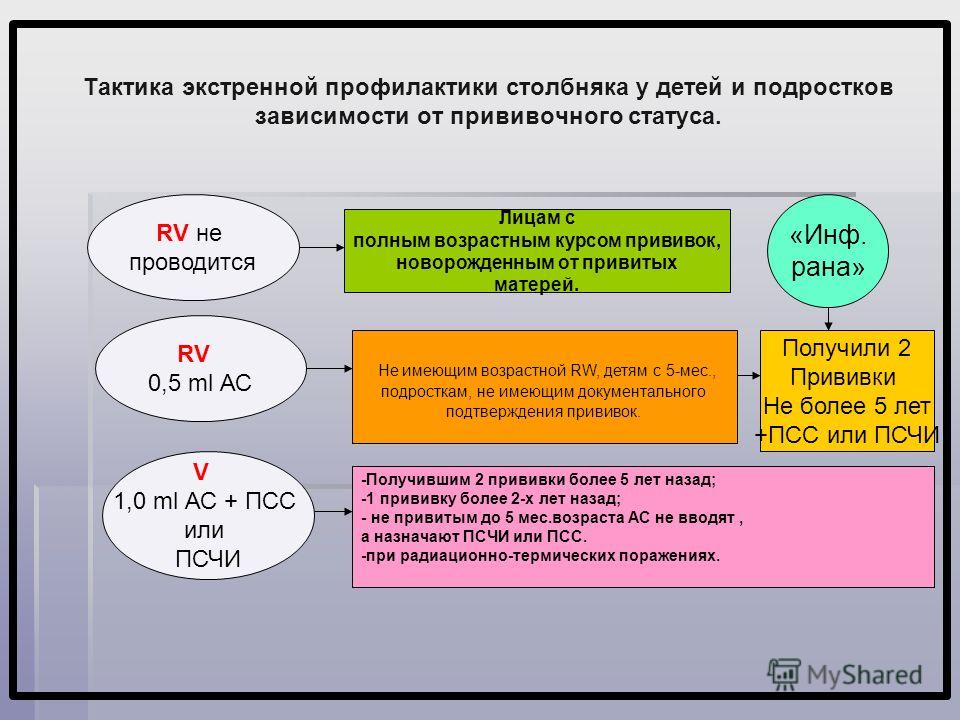 Однако по сравнению с вакцинами, вводимыми вне беременности, данные о безопасности часто ограничены из-за отсутствия крупных РКИ для их оценки. В отсутствие данных РКИ накопление информации из хорошо спланированных обсервационных исследований становится все более важным. Это исследование расширяет наши знания о безопасности вакцины Tdap, вводимой во время беременности, и мы согласились включить данные исследования в международную базу данных о воздействии Tdap во время беременности.
Однако по сравнению с вакцинами, вводимыми вне беременности, данные о безопасности часто ограничены из-за отсутствия крупных РКИ для их оценки. В отсутствие данных РКИ накопление информации из хорошо спланированных обсервационных исследований становится все более важным. Это исследование расширяет наши знания о безопасности вакцины Tdap, вводимой во время беременности, и мы согласились включить данные исследования в международную базу данных о воздействии Tdap во время беременности.
Недавние оценки эффективности вакцины показывают, что вакцинация женщин в конце третьего триместра беременности на 91% защищает от коклюша у младенцев в первые 2 месяца жизни.12,13 Ни у одного из младенцев в нашей когорте не развился коклюш. Это было обсервационное исследование, в котором участвовали только младенцы, подвергшиеся вакцинации, поэтому мы не можем делать какие-либо выводы об эффективности вакцины. Однако, учитывая высокие показатели заболеваемости коклюшем в сообществе на протяжении всего исследования, очень обнадеживает тот факт, что случаев заболевания не было. Это согласуется с предполагаемой эффективностью вакцины.
Это согласуется с предполагаемой эффективностью вакцины.
Одной из сильных сторон этого исследования было то, что благодаря частым контактам с родителями с использованием различных способов общения у нас было большое количество младенцев, завершивших последующее наблюдение. Мы решили использовать объективные показатели данных из обычных источников, таких как NIR, чтобы обеспечить оптимальное качество данных.
Несмотря на то, что мы смогли получить данные о большом количестве женщин и младенцев, однако план наблюдения означал, что наша выборка не является действительно репрезентативной для всего населения в регионе. Например, в нашей когорте было меньше женщин маори и женщин с тихоокеанских островов, чем в остальной части Кентербери, и было показано, что в обеих этих этнических группах показатели заболеваемости коклюшем значительно выше, чем среди европейцев Новой Зеландии.14 Мы также должны подчеркнуть, что женщины К участию в этом исследовании подошла подгруппа вакцинированных, давших согласие на то, чтобы исследовательская группа связалась с ними. Из-за нехватки ресурсов мы не смогли связаться со всеми этими женщинами, и, к сожалению, у нас нет данных для сравнения вакцинированных женщин, которые не участвовали в исследовании, с нашей исследуемой популяцией.
Из-за нехватки ресурсов мы не смогли связаться со всеми этими женщинами, и, к сожалению, у нас нет данных для сравнения вакцинированных женщин, которые не участвовали в исследовании, с нашей исследуемой популяцией.
Небольшая часть женщин в этом исследовании также получила вакцину против сезонного гриппа, часто одновременно с вакциной Tdap. Учитывая наблюдательный характер исследования, мы не могли это контролировать; однако не было статистически значимых различий в исходах для женщин, получивших обе вакцины, по сравнению с теми, кто не получил противогриппозную вакцину (данные не представлены).
Наконец, несмотря на то, что это крупнейшее на сегодняшний день исследование с подробным наблюдением за младенцами, подвергшимися воздействию вакцины Tdap во время беременности, число участников все еще слишком мало, чтобы выявить менее распространенные побочные эффекты, связанные с вакциной.
Выводы
Ранее было показано, что введение вакцины Tdap во время беременности обеспечивает защиту младенцев от коклюша во время эпидемий. Мы не показали различий в исходах у младенцев у тех, кто подвергся воздействию вакцины во время беременности, по сравнению с населением в целом. Это дает дополнительные доказательства, подтверждающие рекомендации по вакцинации беременных женщин Tdap для предотвращения коклюша у их детей. Однако данные о безопасности вакцины остаются ограниченными, и сохраняется необходимость в постоянном наблюдении и отчетности о нежелательных явлениях, связанных с вакцинацией Tdap во время беременности.
Мы не показали различий в исходах у младенцев у тех, кто подвергся воздействию вакцины во время беременности, по сравнению с населением в целом. Это дает дополнительные доказательства, подтверждающие рекомендации по вакцинации беременных женщин Tdap для предотвращения коклюша у их детей. Однако данные о безопасности вакцины остаются ограниченными, и сохраняется необходимость в постоянном наблюдении и отчетности о нежелательных явлениях, связанных с вакцинацией Tdap во время беременности.
Благодарности
Авторы благодарят доктора Джонатана Уиллимана за советы по статистическому анализу. Они также благодарят CDHB за финансовую поддержку этого исследования.
Ссылки
- ↵
- Healy CM,
- Munoz FM,
- Rench MA, и др.
. Распространенность коклюшных антител в материнских родах, пуповине и детской сыворотке. J Infect Dis 2004;190:335–40. дои: 10.1086/421033
- ↵
Центры по контролю и профилактике заболеваний CDC.
 Обновленные рекомендации по использованию противостолбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) у беременных женщин — Консультативный комитет по практике иммунизации (ACIP), 2012 г. MMWR Morb Mortal Wkly Rep 2013; 62:131–5.
Обновленные рекомендации по использованию противостолбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной коклюшной вакцины (Tdap) у беременных женщин — Консультативный комитет по практике иммунизации (ACIP), 2012 г. MMWR Morb Mortal Wkly Rep 2013; 62:131–5. - ↵
Заседание JCVI по иммунизации против коклюша: август 2012 г. https://www.gov.uk/government/groups/joint-committee-on-vaccination-and-immunisation
- ↵
- Жетеева Ю.А.,
- Моро П.Л.,
- Теппер Н.К. и др.
. Сообщения о нежелательных явлениях после введения столбнячного анатоксина, редуцированного дифтерийного анатоксина и бесклеточной вакцины против коклюша у беременных женщин. Am J Obstet Gynecol 2012;207:59.e1–7. doi:10.1016/j.ajog.2012.05.006
- ↵
- Munoz FM,
- Bond NH,
- Maccato M, et al
1
.
 Безопасность и иммуногенность иммунизации против столбняка, дифтерии и бесклеточного коклюша (Tdap) во время беременности у матерей и младенцев: рандомизированное клиническое исследование. JAMA 2014; 311:1760–9. doi:10.1001/jama.2014.3633
Безопасность и иммуногенность иммунизации против столбняка, дифтерии и бесклеточного коклюша (Tdap) во время беременности у матерей и младенцев: рандомизированное клиническое исследование. JAMA 2014; 311:1760–9. doi:10.1001/jama.2014.3633 - ↵
Публикации Национального регистра иммунизации. http://www.health.govt.nz/our-work/preventative-health-wellness/immunisation/national-immunisation-register/national-immunisation-register-publications (по состоянию на 9 марта 2015 г.).
- ↵
- Муньос Ф.М.,
- Эккерт Л.О.,
- Кац М.А. и др.
. Ключевые термины для оценки безопасности вакцин при беременности: результаты глобального консультативного процесса по инициированию гармонизации определений нежелательных явлений. Вакцина 2015;33:6441–52. doi:10.1016/j.vaccine.2015.07.112
- ↵
Клинические показатели родовспоможения Новой Зеландии.
 http://www.health.govt.nz/publication/new-zealand-maternity-clinical-indicators-2012 (по состоянию на 9 марта 2015 г.).
http://www.health.govt.nz/publication/new-zealand-maternity-clinical-indicators-2012 (по состоянию на 9 марта 2015 г.). - ↵
Реестр врожденных дефектов Новой Зеландии. http://nzbdr.ac.nz (по состоянию на 9 марта 2015 г.).
- ↵
- Grant CC,
- Roberts M,
- Scragg R, et al
. Отсроченная иммунизация и риск коклюша у младенцев: непревзойденное исследование случай-контроль. BMJ 2003;326:852–3. doi:10.1136/bmj.326.7394.852
- ↵
- Линдси Б,
- Кампманн Б,
- Джонс С
. Иммунизация матери как стратегия снижения восприимчивости к инфекциям у новорожденных. Curr Opin Infect Dis 2013;26:248–53. doi: 10.1097/QCO.0b013e3283607a58
- ↵
- Амирталингам Г.,
- Эндрюс Н.,
- Кэмпбелл Х. и др.
.
 Эффективность материнской вакцинации против коклюша в Англии: обсервационное исследование. Ланцет 2014; 384:1521–8. doi:10.1016/S0140-6736(14)60686-3
Эффективность материнской вакцинации против коклюша в Англии: обсервационное исследование. Ланцет 2014; 384:1521–8. doi:10.1016/S0140-6736(14)60686-3 - ↵
- Dabrera G,
- Amirthalingam G,
- Andrews N, et al
5
- Исследование случай-контроль для оценки эффективности вакцинации матерей против коклюша для защиты новорожденных в Англии и Уэльсе, 2012–2013 гг. Clin Infect Dis 2015;60:333–7. doi:10.1093/cid/ciu821
- ↵
- Somerville RL,
- Grant CC,
- Grimwood K, et al
. Младенцы, госпитализированные с коклюшем: оценка истинного бремени болезни. J Paediatr Child Health 2007;43:617–22. doi:10.1111/j.1440-1754.2007.01154.x
Сноски
Twitter Следите за Хелен Петусис-Харрис на @PetousisH
Авторы TW разработали концепцию и дизайн исследования, подготовили рукопись и утвердили окончательный вариант рукописи в представленном виде.
 PG разработала инструмент для сбора данных, собрала и сопоставила большую часть данных. Она помогла с составлением рукописи и одобрила окончательный вариант. HP-H участвовала в разработке и дизайне концепции исследования, а также в первоначальной заявке на финансирование. Она помогла с составлением рукописи и одобрила окончательный вариант рукописи в представленном виде. LH участвовала в сборе данных и анализе данных, касающихся статуса иммунизации младенцев. Она помогла с составлением рукописи и одобрила окончательный вариант рукописи в представленном виде. NA участвовала в планировании и разработке исследования, а также в первоначальной заявке на финансирование. Она помогла с составлением рукописи и одобрила окончательный вариант.
PG разработала инструмент для сбора данных, собрала и сопоставила большую часть данных. Она помогла с составлением рукописи и одобрила окончательный вариант. HP-H участвовала в разработке и дизайне концепции исследования, а также в первоначальной заявке на финансирование. Она помогла с составлением рукописи и одобрила окончательный вариант рукописи в представленном виде. LH участвовала в сборе данных и анализе данных, касающихся статуса иммунизации младенцев. Она помогла с составлением рукописи и одобрила окончательный вариант рукописи в представленном виде. NA участвовала в планировании и разработке исследования, а также в первоначальной заявке на финансирование. Она помогла с составлением рукописи и одобрила окончательный вариант.Финансирование Департамента здравоохранения округа Кентербери.
Конкурирующие интересы Компания TW провела исследования под руководством исследователей, финансируемых GSK. Компания HP-H провела исследования под руководством исследователей, финансируемых GSK, CSL и Sanofi.

Согласие пациента Получено.
Утверждение этики Верхний Юг Региональный комитет по этике — одобрение URA/12/EXP/021.
Происхождение и рецензирование Не введен в эксплуатацию; рецензируется внешними экспертами.
Заявление о совместном использовании данных Дополнительные данные отсутствуют.
Читать полный текст или скачать PDF:
Подписаться
Войти под своим именем пользователя и паролем
Пароль *
Забыли данные для входа? Зарегистрировать новую учетную запись?
Забыли имя пользователя или пароль?
Безопасность вакцинации против столбняка, дифтерии и коклюша во время беременности: систематический обзор
Обзор
. 2017 март; 129(3):560-573.
doi: 10.1097/AOG.0000000000001888.
Марк Макмиллан
1
, Мишель Кларк, Адриана Паррелла, Дешайн Б. Фелл, Гаятри Амирталингам, Хелен С. Маршалл
Фелл, Гаятри Амирталингам, Хелен С. Маршаллпринадлежность
- 1 Отдел исследований вакцинологии и иммунологии, Женская и детская больница, Медицинский факультет и Научно-исследовательский институт Робинсона, Университет Аделаиды, Северная Аделаида, Австралия; Детская больница Научно-исследовательского института Восточного Онтарио и Оттавского университета, Оттава, Онтарио, Канада; и Департамент иммунизации, гепатита и безопасности крови, Общественное здравоохранение Англии, Лондон, Соединенное Королевство.
PMID:
28178054
DOI:
10.1097/АОГ.0000000000001888
Обзор
Марк Макмиллан и др.
Акушерство Гинекол.

2017 март
. 2017 март; 129(3):560-573.
дои: 10.1097/АОГ.0000000000001888.
Авторы
Марк Макмиллан
1
, Мишель Кларк, Адриана Паррелла, Дешайн Б. Фелл, Гаятри Амирталингам, Хелен С. Маршаллпринадлежность
- 1 Отдел исследований вакцинологии и иммунологии, Женская и детская больница, Медицинский факультет и Научно-исследовательский институт Робинсона, Университет Аделаиды, Северная Аделаида, Австралия; Детская больница Научно-исследовательского института Восточного Онтарио и Оттавского университета, Оттава, Онтарио, Канада; и Департамент иммунизации, гепатита и безопасности крови, Общественное здравоохранение Англии, Лондон, Соединенное Королевство.

PMID:
28178054
DOI:
10.1097/АОГ.0000000000001888
Абстрактный
Задача:
Оценить антенатальные, родовые и младенческие исходы для беременных женщин, плодов и младенцев после антенатальной вакцинации любым антигеном, присутствующим в комбинированных коклюшных вакцинах.
Источники данных:
PubMed, EMBASE, Литература в области медицинских наук в Латинской Америке и Карибском бассейне, ClinicalTrials.gov, Кокрейновская библиотека и Всемирная организация здравоохранения (от начала до 5 мая 2016 г.).
Методы отбора исследований:
Исследования, сообщающие об исходах для беременных женщин, их плода или младенца после антенатального воздействия либо моновалентной, либо комбинированной вакцины против столбняка, редуцированного дифтерийного анатоксина и бесклеточной коклюшной (Tdap) или инактивированной вакцины против полиомиелита, рассматривались для включения.

Полученные результаты:
Всего в этот обзор было включено 21 исследование. Баллы варьировали от 0,47 до 1,50 для преждевременных родов (менее 37 недель беременности), 0,65-1,00 для малых для гестационного возраста (масса тела при рождении менее 10-го процентиля), 0,36-0,85 для мертворождений, 0,16-1,00 для неонатальной смерти, 0,76-1,20 при низкой массе тела при рождении (менее 2500 г) и 0,20-0,91 при врожденных аномалиях. Все нижние 95% доверительные интервалы (ДИ) были меньше 1,0. Из трех ретроспективных исследований, оценивающих хориоамнионит после вакцинации, одно показало небольшое, но статистически значимое увеличение. Точечные оценки всех аномалий после антенатальной вакцинации столбнячным анатоксином колебались от 1,20 до 1,60 и имели 95% ДИ, которые превысили 1,0. Существовала значительная клиническая и методологическая неоднородность в основном ретроспективных обсервационных исследований с общим высоким риском систематической ошибки.
 Объективные показатели лихорадки были низкими, 3% или ниже, и более распространенными системными явлениями были головная боль, недомогание и миалгия.
Объективные показатели лихорадки были низкими, 3% или ниже, и более распространенными системными явлениями были головная боль, недомогание и миалгия.
Вывод:
Имеющиеся данные свидетельствуют о том, что антенатальное комбинированное введение Tdap во втором или третьем триместре беременности не связано с клинически значимым вредом для плода или новорожденного. Медицинские мероприятия у беременных женщин одинаковы в вакцинированных и невакцинированных группах.
Похожие статьи
Оценка связи вакцинации матери против коклюша с акушерскими событиями и исходами родов.
Харбанда Э.О., Васкес-Бенитес Г., Липкинд Х.С., Кляйн Н.П., Читам Т.К., Нейлуэй А., Омер С.Б., Хэмбидж С.Дж., Ли Г.М., Джексон М.Л., Маккарти Н.Л., ДеСтефано Ф., Нордин Д.Д.
Харбанда Э.О. и др.
ДЖАМА. 2014 12 ноября; 312 (18): 1897-904. дои: 10.1001/jama.2014.14825.
2014 12 ноября; 312 (18): 1897-904. дои: 10.1001/jama.2014.14825.
ДЖАМА. 2014.PMID: 25387187
Бесплатная статья ЧВК.Акушерские и перинатальные исходы после вакцинации против коклюша во время беременности в Онтарио, Канада: ретроспективное когортное исследование.
Фахраи Р., Кроукрофт Н., Болотин С., Суча Э., Хокен С., Уилсон К., Годе Л., Амирталингам Г., Бирингер А., Кук Дж., Дубей В., Гальперин С.А., Джеймисон Ф., Квонг Дж.С., Садарангани М., Уокер М.С., Лаверти М., Фелл Д.Б.
Фахраи Р. и соавт.
ЦМАЖ открытый. 2021 13 апр;9(2):E349. doi: 10.9778/cmajo.20200239. Печать 2021 апрель-июнь.
ЦМАЖ открытый. 2021.PMID: 33849984
Бесплатная статья ЧВК.Безопасность и эффективность бесклеточной вакцинации против коклюша во время беременности: систематический обзор.

Выген-Бонне С., Хелленбранд В., Гарбе Э., фон Крис Р., Богдан С., Хайнингер У., Рёбл-Матье М., Хардер Т.
Выген-Бонне С. и соавт.
BMC Infect Dis. 2020 13 февраля; 20 (1): 136. дои: 10.1186/s12879-020-4824-3.
BMC Infect Dis. 2020.PMID: 32054444
Бесплатная статья ЧВК.Лечение заболеваний пародонта для предотвращения неблагоприятных исходов родов у беременных.
Ихеозор-Эджиофор З., Миддлтон П., Эспозито М., Гленни А.М.
Ихеозор-Эджиофор З. и соавт.
Cochrane Database Syst Rev. 2017 Jun 12;6(6):CD005297. doi: 10.1002/14651858.CD005297.pub3.
Кокрановская система базы данных, ред. 2017 г.PMID: 28605006
Бесплатная статья ЧВК.Обзор.
Вакцины для женщин для профилактики столбняка новорожденных.

Демикели В., Барале А., Риветти А.
Демичели В. и соавт.
Cochrane Database Syst Rev. 6 июля 2015 г.; 2015(7):CD002959. doi: 10.1002/14651858.CD002959.pub4.
Кокрановская система базы данных, ред. 2015 г.PMID: 26144877
Бесплатная статья ЧВК.Обзор.
Посмотреть все похожие статьи
Цитируется
Барьеры и факторы, способствующие вакцинации от COVID-19, коклюша и гриппа во время беременности: протокол комплексного обзора.
Никол Б., Симонетти В., Маккриди Дж., Стин М., Ансворт Дж., Томьетто М.
Никол Б. и др.
ПЛОС Один. 2022, 26 сентября; 17(9):e0275105. doi: 10.1371/journal.pone.0275105. Электронная коллекция 2022.
ПЛОС Один. 2022.PMID: 36156084
Бесплатная статья ЧВК.Охват материнской вакцинацией против гриппа и коклюша и влияющие факторы в Испании: исследование, основанное на реестре записей первичной медико-санитарной помощи.

Фернандес-Кано М.И., Арресиадо Мараньон А., Рейес-Лакалье А., Фейхоо-Сид М., Манреса-Домингес Х.М., Монтеро-Понс Л., Кабедо-Феррейро Р.М., Торан-Монсеррат П., Фальгера-Пуч Г.
Фернандес-Кано М.И. и соавт.
Общественное здравоохранение Int J Environ Res. 2022 6 апр;19(7):4391. doi: 10.3390/ijerph2- 91.
Общественное здравоохранение Int J Environ Res. 2022.PMID: 35410075
Бесплатная статья ЧВК. Всесторонний обзор вакцинации во время беременности в Европе.
Симионеску А.А., Стрейну-Черчел А., Попеску Ф.Д., Станеску А.М., Виеру М., Данчу Б.М., Мирон В.Д., Сэндулеску О.
Симионеску А.А. и соавт.
J Pers Med. 2021 13 ноября; 11 (11): 1196. дои: 10.3390/jpm11111196.
J Pers Med. 2021.PMID: 34834548
Бесплатная статья ЧВК.Обзор.
Защитные прививки во время беременности — знания взрослых поляков в этой области.

Домбек Я., Серка О., Кулик Х., Гонсиор З.
Домбек Дж. и соавт.
Общественное здравоохранение BMC. 2021 13 июля; 21 (1): 1392. doi: 10.1186/s12889-021-11336-0.
Общественное здравоохранение BMC. 2021.PMID: 34256706
Бесплатная статья ЧВК.Изменяется ли вирусная реакция хозяина и иммуногенность вакцин во время беременности?
Саид З., Грир О., Шах Н.М.
Саид З. и др.
Антитела (Базель). 2020 4 августа; 9 (3): 38. дои: 10.3390/антиб38.
Антитела (Базель). 2020.PMID: 32759839
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
использованная литература
Somerville RL, Grant CC, Scragg RK, Thomas MG. Госпитализации из-за коклюша в Новой Зеландии в эпоху до иммунизации и массовой иммунизации.
 J Paediatr Child Health 2007;43:147–53.
J Paediatr Child Health 2007;43:147–53.
Спицы П.Дж., Куинн Х.Э., Маканулти Дж.М. Обзор эпидемии коклюша в Новом Южном Уэльсе в 2008–2009 гг.: уведомления и госпитализации. N S W Public Health Bull 2010; 21: 167–73.
Танака М., Витек Ч.Р., Паскуаль Ф., Бисгард К.М., Тейт Дж.Э., Мерфи Т.В. Тенденции заболеваемости коклюшем среди младенцев в США, 1980–1999 гг. ЯМА 2003;290: 2968–75.
Хранилище данных Глобальной обсерватории здравоохранения. Женева (Швейцария): Всемирная организация здравоохранения; 2016. Доступно по адресу: http://apps.who.int/gho/data/view.main.CM1002015WORLD-Ch5?lang=en. Проверено 27 июня 2016 г.
ван Хук А.
 Дж., Кэмпбелл Х., Амирталингам Г., Эндрюс Н., Миллер Э. Количество смертей от коклюша среди младенцев в возрасте до одного года в Англии: результаты анализа захвата/повторного захвата за период с 2001 по 2011 год. Euro Surveill 2013; 18. пий: 20414.
Дж., Кэмпбелл Х., Амирталингам Г., Эндрюс Н., Миллер Э. Количество смертей от коклюша среди младенцев в возрасте до одного года в Англии: результаты анализа захвата/повторного захвата за период с 2001 по 2011 год. Euro Surveill 2013; 18. пий: 20414.
Типы публикаций
термины MeSH
вещества
Вакцинация во время беременности: обращение за помощью ко всем поставщикам медицинских услуг
Обзор
Джонатан Д. Эмери, доктор медицинских наук, и Даниэль Мусса, бакалавр медицины
Cleveland Clinic Journal of Medicine, март 2021 г., 88 (3) 157–162; Doi: https://doi.org/10.3949/ccjm.88a.20111
- Статья
- Рисунки и данные
- Информация и метрики
Аннотация
- Вместе медицинской помощи, но показатели материнской иммунизации по-прежнему ниже национальных контрольных показателей.
 Было показано, что прививки от гриппа и столбняка, редуцированного дифтерийного анатоксина и бесклеточного коклюша (Tdap) безопасны и обеспечивают важную защиту беременных женщин, плода и новорожденных. Хотя акушеры-гинекологи обеспечивают большую часть ухода за беременными, терапевты общего профиля и врачи-специалисты часто встречаются с роженицами и должны помогать в обучении и проведении иммунизации.
Было показано, что прививки от гриппа и столбняка, редуцированного дифтерийного анатоксина и бесклеточного коклюша (Tdap) безопасны и обеспечивают важную защиту беременных женщин, плода и новорожденных. Хотя акушеры-гинекологи обеспечивают большую часть ухода за беременными, терапевты общего профиля и врачи-специалисты часто встречаются с роженицами и должны помогать в обучении и проведении иммунизации.ОСНОВНЫЕ ПОЛОЖЕНИЯ
Прививки от сезонного гриппа и Tdap рекомендуются беременным или планирующим беременность женщинам.
Обе вакцины безопасны для большинства женщин и приносят значительную пользу матери и ребенку.
Беременным женщинам следует вводить инактивированную форму противогриппозной вакцины, а не живую вакцину.
Вакцинация Tdap рекомендуется в третьем триместре, но ее можно делать в любое время беременности.
Рекомендация поставщика медицинских услуг является фактором номер один, который неизменно повышает уровень вакцинации матерей.

Вакцину против COVID-19 не следует отказывать беременным пациенткам, которые соответствуют критериям для вакцинации, но решение остается на усмотрение пациентки после информированного обсуждения.
Вакцинация во время беременности является приоритетом общественного здравоохранения, которым часто пренебрегают, тем более сегодня, когда внимание уделяется COVID-19.вакцинация. Вакцинация во время беременности важна для защиты матери (которая особенно уязвима из-за физиологических изменений во время беременности), плода (из-за рисков развития и недоношенности) и новорожденного (путем создания пассивного иммунитета).
В этой статье рассматриваются 2 вакцины, которые чаще всего вводят во время беременности: инактивированная вакцина против сезонного гриппа и столбнячный анатоксин, редуцированный дифтерийный анатоксин и бесклеточная вакцина против коклюша (Tdap), а также доказательства их пользы и безопасности, рекомендации по их применению, и ведение беременных женщин, заболевших гриппом или коклюшем или подвергшихся их воздействию.

ВАКЦИНАЦИЯ РЕКОМЕНДУЕТСЯ ВО ВРЕМЯ БЕРЕМЕННОСТИ
Американский колледж акушеров и гинекологов (ACOG) сообщает, что не только акушеры-гинекологи, но и другие поставщики медицинских услуг рекомендуют и вводят вакцину против гриппа женщинам, которые беременны или планируют забеременеть в сезон гриппа . 1 Они также рекомендуют вакцинировать женщин против столбняка, дифтерии и коклюша во время каждой беременности. 2
Несмотря на рекомендации национальных и международных обществ, уровень вакцинации во время беременности остается ниже целевых показателей. 3 Терапевты и врачи-специалисты играют решающую роль в повышении уровня вакцинации беременных женщин. Поскольку эти поставщики обеспечивают постоянный уход и наблюдение за сопутствующими заболеваниями, такими как астма, диабет, волчанка и болезни сердца, во время беременности, их действия по рекомендации и проведению иммунизации беременным или планирующим беременность женщинам необходимы для повышения уровня вакцинации.

В таблице 1 приведены рекомендации по иммунизации матерей.
ТАБЛИЦА 1
Сводная информация о прививках во время беременности
ВАКЦИНАЦИЯ ОТ ГРИППА
Хотя показатели вакцинации против гриппа увеличились после пандемии h2N1 2009 г. до пика чуть более 50% в 2016 г. в США, 4 показатели при беременности снижаются .
Иммунизация беременных против сезонного гриппа имеет решающее значение. Во время пандемии гриппа h2N1 в США в 2009 г. 5% всех смертей от гриппа приходилось на беременных женщин, хотя беременные женщины составляют лишь 1% населения. 4
Грипп во время беременности подвергает мать более высокому риску пневмонии, госпитализации, дыхательной недостаточности и госпитализации в отделение интенсивной терапии по сравнению с небеременными женщинами. Эти риски связаны с иммунологическими изменениями во время беременности, такими как измененный Т-клеточный иммунитет, и физиологическими изменениями, такими как сдавливание беременной матки в грудную клетку, вызывающее снижение функциональной остаточной емкости легких.
 Грипп также может привести к преждевременным родам и преждевременным родам, потенциально подвергая плод воздействию преждевременных родов или вызывая мертворождение. 5
Грипп также может привести к преждевременным родам и преждевременным родам, потенциально подвергая плод воздействию преждевременных родов или вызывая мертворождение. 5 Преимущества вакцинации против гриппа для матери и ребенка
Вакцинация во время беременности полезна как для матери, так и для ребенка. Эффективность вакцинации против сезонного гриппа у беременных и небеременных женщин одинакова. 6 Хотя эффективность сезонной вакцины варьируется от года к году, вакцинированные беременные реже госпитализируются, чем непривитые. 1,4
Вакцинация матери также может иметь существенные преимущества для новорожденного после рождения благодаря пассивному иммунитету, обеспечиваемому трансплацентарным проникновением материнских антител. Рандомизированное исследование показало, что титры антител в пуповинной крови более чем в 1,5 раза выше, чем в материнской крови после вакцинации. 7 Клинические преимущества включают меньшее количество госпитализаций и более низкие показатели лабораторно подтвержденного заболевания гриппом у младенцев, рожденных вакцинированными матерями.
 В 2 исследованиях лабораторно подтвержденное заболевание гриппом развилось у 93 из 2873 (3,24%) младенцев вакцинированных женщин по сравнению с 142 из 2869 (4,95%) младенцев невакцинированных женщин (коэффициент риска 0,66, 95% доверительный интервал 0,50–0,85). 8 На основании этих данных мы рассчитали снижение абсолютного риска на 1,71% и число, необходимое для лечения 58.
В 2 исследованиях лабораторно подтвержденное заболевание гриппом развилось у 93 из 2873 (3,24%) младенцев вакцинированных женщин по сравнению с 142 из 2869 (4,95%) младенцев невакцинированных женщин (коэффициент риска 0,66, 95% доверительный интервал 0,50–0,85). 8 На основании этих данных мы рассчитали снижение абсолютного риска на 1,71% и число, необходимое для лечения 58.Нет данных о проблемах безопасности
Многочисленные исследования показали, что вакцинация против гриппа безопасна и эффективна во время беременности, с небольшим неблагоприятным воздействием на мать. 1,4,5 Общие побочные эффекты, связанные с вакцинацией, включают реакцию в месте инъекции, лихорадку, головную боль и миалгию.
Также были изучены возможные побочные эффекты вакцины против сезонного гриппа на плод и новорожденного. Систематические обзоры вакцинации матери инактивированным вирусом гриппа не обнаружили корреляции с повышенным риском для плода. 9,10 Проспективное когортное исследование более чем 10 000 беременных женщин не выявило связи между вакцинацией против гриппа во время беременности и неблагоприятными исходами родов.
 11 Хотя были высказаны опасения по поводу безопасности ртутьсодержащего консерванта тимеросала и его возможной связи с аутизмом, нет научных доказательств связи между введением вакцин, содержащих тиомерсал, матери и неблагоприятными последствиями для здоровья или развития ребенка когда-либо был найден. 1
11 Хотя были высказаны опасения по поводу безопасности ртутьсодержащего консерванта тимеросала и его возможной связи с аутизмом, нет научных доказательств связи между введением вакцин, содержащих тиомерсал, матери и неблагоприятными последствиями для здоровья или развития ребенка когда-либо был найден. 1 Рекомендации по применению
Беременным женщинам следует использовать только инактивированную противогриппозную вакцину. Живая аттенуированная гриппозная вакцина показана небеременным пациенткам в возрасте от 2 до 49 лет и может применяться у женщин в послеродовом периоде, в том числе кормящих грудью.
Противопоказания . Предшествующая опасная для жизни реакция на вакцину против гриппа или любой из ее компонентов является абсолютным противопоказанием для получения вакцины. Даже женщинам с аллергией на яйца или синдромом Гийена-Барре в анамнезе следует рассмотреть вопрос о вакцинации, если потенциальные преимущества перевешивают риски.
 12
12 Время . Беременные женщины могут получить инактивированную противогриппозную вакцину в любое время в течение сезона гриппа (обычно с октября по май), хотя лучшее время — в начале сезона, в идеале до конца октября. Невакцинированную беременную женщину, обратившуюся к своему лечащему врачу или врачу-специалисту, следует поощрять к получению вакцины независимо от стадии ее беременности.
Вакцину следует вводить женщинам репродуктивного возраста, планирующим беременность в сезон гриппа или не использующим активно противозачаточные средства.
Документация о прививках должна быть предоставлена пациенту, чтобы обеспечить актуальность ее записей о прививках.
Члены семьи беременной женщины также должны быть вакцинированы. Хотя эта стратегия рекомендуется для снижения заболеваемости новорожденных, данные о ее эффективности неоднозначны. 5
Лечение гриппа и возможное заражение
Независимо от того, вакцинированы они или нет, женщинам, у которых в любой момент беременности развилось гриппоподобное заболевание, должны быть назначены противовирусные препараты, т.
 е. одна из следующих схем, в зависимости от местной резистентности вируса гриппа 13 :
е. одна из следующих схем, в зависимости от местной резистентности вируса гриппа 13 :Осельтамивир 75 мг два раза в день в течение 5 дней (рекомендовано Центрами по контролю и профилактике заболеваний США)
Занамивир 10 мг (2 ингаляции по 5 мг) два раза в день в течение 5 дней
6 мг
Перамивир 900 (однократная внутривенная инфузия).
- ↵
Мнение комитета ACOG № 732: вакцинация против гриппа во время беременности. Обстет Гинекол 2018; 131(4):e109–e114. doi:10.1097/AOG.
 0000000000002588
0000000000002588 - ↵
Мнение комитета ACOG № 741: иммунизация матерей. Акушерство Гинекол 2018; 131(6):e214–e217. doi: 10.1097/aog.0000000000002662
- ↵
- Sakala IG,
- Honda-Okubo Y,
- Fung J,
- Petrovsky N
. Иммунизация против гриппа во время беременности: преимущества для матери и ребенка. Hum Vaccin Immunother 2016; 12(12):3065–3071. doi:10.1080/21645515.2016.1215392
- ↵
- Rasmussen SA,
- Jamieson DJ
. Грипп и беременность: не время для самоуспокоенности. Акушерство Гинекол 2019; 133(1):23–26. doi:10.1097/AOG.0000000000003040
- ↵
- Маршалл Х,
- Макмиллан М,
- Эндрюс Р.М.,
- Эдвардс К,
9009
. Вакцины при беременности: двойная польза для беременных женщин и младенцев.
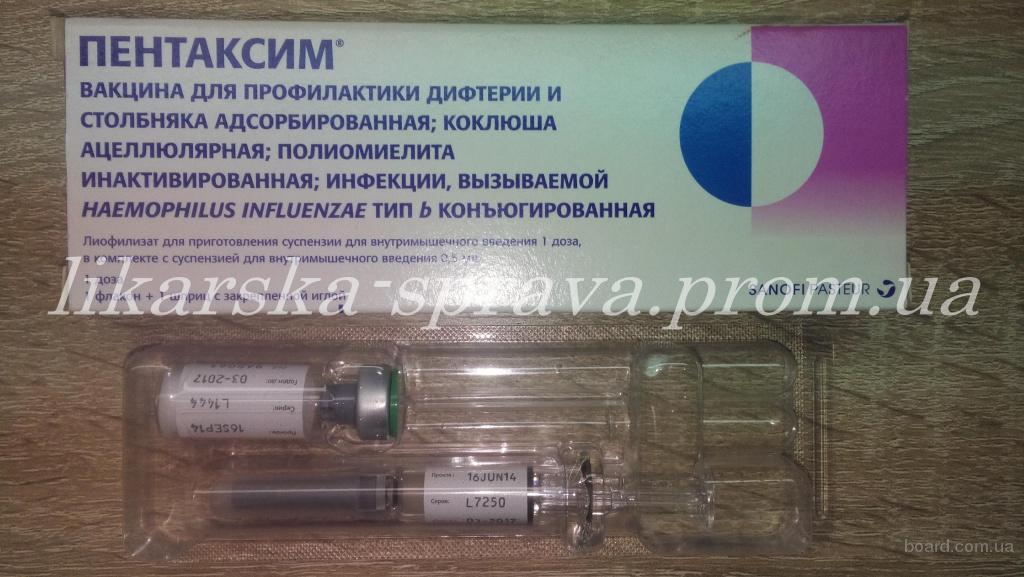 Hum Vaccin Immunother 2016; 12(4):848–856. doi:10.1080/21645515.2015.1127485
Hum Vaccin Immunother 2016; 12(4):848–856. doi:10.1080/21645515.2015.1127485 - ↵
- Thompson MG,
- Li DK,
- Shifflett P, et al 90
9
- Эффективность сезонной трехвалентной противогриппозной вакцины для профилактики заболевания вирусом гриппа среди беременных женщин: популяционное исследование случай-контроль в сезоны гриппа 2010–2011 и 2011–2012 гг. Clin Infect Dis 2014; 58(4):449–457. doi:10.1093/cid/cit750
- ↵
- Весикари Т.,
- Вирта М.,
- Хейнонен С., и др.
9003. Иммуногенность и безопасность четырехвалентной инактивированной противогриппозной вакцины у беременных: рандомизированное слепое наблюдательное исследование. Вакцина Hum Immunother 2020; 16(3):623–629. doi:10.1080/21645515.2019.1667202
- ↵
- Джарвис Дж.Р.,
- Дори Р.Б.,
- Warricker FDM,
- Alwan NA,
- Jones CE
.
 Эффективность вакцинации против гриппа во время беременности по отношению к состоянию здоровья ребенка: систематический обзор и метаанализ. Вакцина 2020; 38 (7): 1601–1613. doi:10.1016/j.vaccine.2019.12.056
Эффективность вакцинации против гриппа во время беременности по отношению к состоянию здоровья ребенка: систематический обзор и метаанализ. Вакцина 2020; 38 (7): 1601–1613. doi:10.1016/j.vaccine.2019.12.056 - ↵
- Беднарчик Р.А.,
- Аджайе-Гбевоньо Д,
- Омер С.Б.
5
1
1
1 Безопасность иммунизации против гриппа во время беременности для плода и новорожденного. Am J Obstet Gynecol 2012; 207 (3 доп): S38–S46. doi: 10.1016/j.ajog.2012.07.002
- ↵
- Giles ML,
- Krishnaswamy S,
- Macartney K,
- Cheng A
. Безопасность инактивированных вакцин против гриппа при беременности для исходов родов: систематический обзор. Hum Vaccin Immunother 2019; 15(3):687–699. doi:10.1080/21645515.2018.1540807
- ↵
- Офудзи С,
- Дегучи М.,
- Татибана Д. и др.

. Безопасность вакцинации против гриппа в отношении неблагоприятных исходов родов среди беременных женщин: проспективное когортное исследование в Японии. Int J Infect Dis 2020; 93:68–76. doi:10.1016/j.ijid.2020.01.033
- ↵
- Psarris A,
- Sindos M,
- Daskalakis G, et al
9
1 9 0. Прививки во время беременности: как, когда и зачем. Eur J Obstet Gynecol Reprod Biol 2019; 240:29–35. doi:10.1016/j.ejogrb.2019.06.019
- ↵
Заключение Комитета ACOG № 753 Резюме: обследование и лечение беременных женщин с подозрением или подтвержденным диагнозом гриппа. Акушерство Гинекол 2018; 132 (4): 1077–1079. doi:10.1097/AOG.0000000000002873
- ↵
- Liang JL,
- Tiwari T,
- Moro P, et al
3
90. Профилактика коклюша, столбняка и дифтерии с помощью вакцин в США: рекомендации Консультативного комитета по практике иммунизации (ACIP).
 MMWR Recomm Rep 2018; 67(2):1–44. doi:10.15585/mmwr.rr6702a1
MMWR Recomm Rep 2018; 67(2):1–44. doi:10.15585/mmwr.rr6702a1 - ↵
- Vittucci AC,
- Spuri Vennarucci V,
- Grandin A, et al
4 90. Коклюш у детей раннего возраста: недооцененное заболевание. BMC Infect Dis 2016; 16(1):414. doi:10.1186/s12879-016-1710-0
- ↵
- Smallenburg LC,
- van Welie NA,
- Elvers LH,
- JC 9007 van Huisseling
- Teunis PF,
- Versteegh FG
. Снижение коклюшного токсина IgG, измеренное в пуповинной крови, а также в сыворотке новорожденных и детей раннего возраста. Eur J Clin Microbiol Infect Dis 2014; 33 (9): 1541–1545. doi: 10.1007/s10096-014-2110-2
- ↵
- FORSYTH K,
- PLOTKIN S,
- TAN T,
- Wirsing von König CH
. Стратегии снижения передачи коклюша младенцам.
 Педиатрия 2015; 135(6):e1475–e1482. doi: 10.1542/PEDS.2014-3925
Педиатрия 2015; 135(6):e1475–e1482. doi: 10.1542/PEDS.2014-3925 - ↵
- McMillan M,
- Clarke M,
- Parrella A,
- DB,
- Amirthalingam G,
- Marshall HS
9
- 9913.
- 9913.
- 9913.
- 91919913.
- 9913.
- 9913.
- 9913. Безопасность вакцинации против столбняка, дифтерии и коклюша во время беременности: систематический обзор. Акушерство Гинекол 2017; 129(3):560–573. doi:10.1097/AOG.0000000000001888
- ↵
- Furuta M,
- Sin J,
- Ng ESW,
- Wang K
. Эффективность и безопасность вакцинации беременных против коклюша — систематический обзор рандомизированных контролируемых испытаний и обсервационных исследований. BMC Беременность Роды 2017; 17(1):390. doi:10.1186/s12884-017-1559-2
- ↵
- Тивари Т.,
- Мерфи Т.В.,
- Моран Дж.
 ; Национальная программа иммунизации, CDC
; Национальная программа иммунизации, CDC
. Рекомендуемые противомикробные препараты для лечения и постконтактной профилактики коклюша: Руководство CDC 2005 г. MMWR Recomm Rep 2005; 54 (RR-14): 1–16. pmid:16340941
- ↵
- Healy CM
. Прививка от коклюша беременным. Hum Vaccin Immunother 2016; 12(8):1972–1981. doi:10.1080/21645515.2016.1171948
- ↵
- O’Leary ST,
- Riley LE,
- Lindley MC, et al
. Практика иммунизации беременных женщин акушерами-гинекологами США. Am J Prev Med 2018; 54(2):205–213. doi:10.1016/j.amepre.2017.10.016
- ↵
- Ahluwalia IB,
- Jamieson DJ,
- Rasmussen SA,
- D’Angelo D,
- Goodman D,
- Kim H
.
 Корреляции охвата вакцинацией против сезонного гриппа среди беременных женщин в Джорджии и Род-Айленде. Акушерство Гинекол 2010; 116(4):949–955. doi:10.1097/AOG.0b013e3181f1039f
Корреляции охвата вакцинацией против сезонного гриппа среди беременных женщин в Джорджии и Род-Айленде. Акушерство Гинекол 2010; 116(4):949–955. doi:10.1097/AOG.0b013e3181f1039f - ↵
- O’Leary ST,
- Riley LE,
- Lindley MC, et al
9
1 9. Стратегии акушеров-гинекологов по решению проблемы отказа от вакцин среди беременных женщин. Акушерство Гинекол 2019; 133(1):40–47. doi:10.1097/AOG.0000000000003005
- ↵
- Моссад СБ
. Как реагировать на тех, кто сомневается в прививке от гриппа. Cleve Clin J Med 2019; 86 (12): 782–788. doi:10.3949/ccjm.86a.19139
- ↵
- Юдин М.Х.,
- Мистри Н,
- Де Соуза Л.Р., и др.
4 . Текстовые сообщения для вакцинации против гриппа среди беременных женщин: рандомизированное контролируемое исследование.
 Вакцина 2017; 35(5):842–848. doi:10.1016/j.vaccine.2016.12.002
Вакцина 2017; 35(5):842–848. doi:10.1016/j.vaccine.2016.12.002 - ↵
- Goodman K,
- Mossad SB,
- Taksler GB,
- Эмери Дж,
- Шрамм С,
- Ротберг МБ
. Влияние видеообучения на вакцинацию против гриппа во время беременности. J Reprod Med 2015; 60 (11–12): 471–479. pmid:26775454
- ↵
- Shavell VI,
- Moniz MH,
- Gonik B,
- Beigi RH
4 90. Иммунизация беременных против гриппа: преодоление барьеров между пациентами и медицинскими работниками. Am J Акушерство Gynecol 2012; 207 (3 доп): S67–S74. doi:10.1016/j.ajog.2012.06.077
- ↵
- Американский колледж акушеров и гинекологов
. Вакцинация беременных и кормящих пациентов против COVID-19. Консультативная практика. Декабрь 2020.
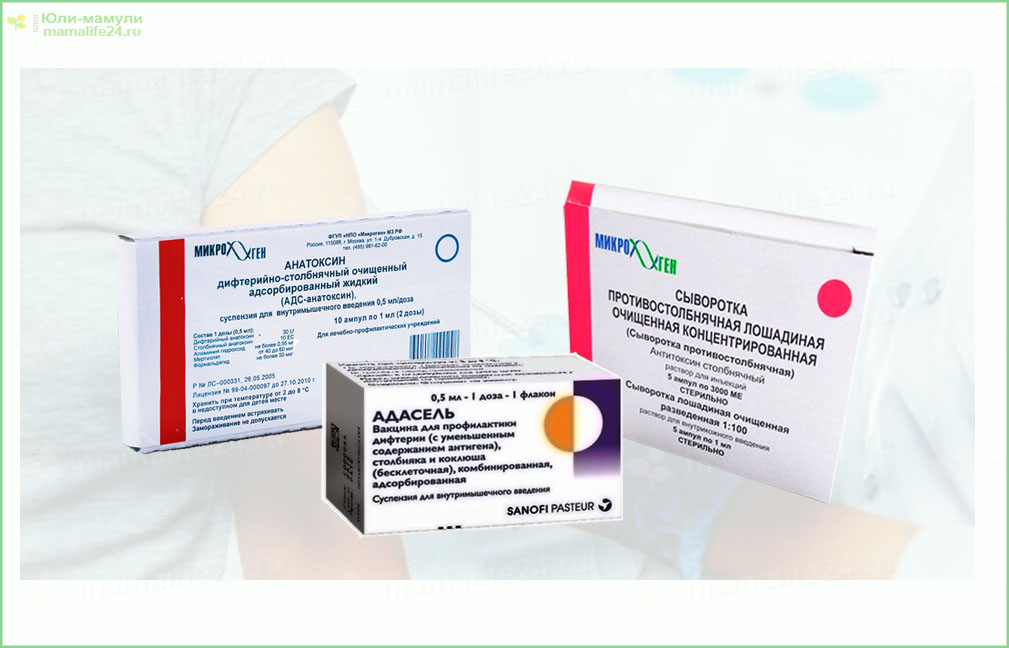
413913.
Лечение следует начинать как можно раньше после начала заболевания.
Противовирусную профилактику после контакта следует рассматривать для беременных и родильниц по одному из следующих режимов:
Терапия должна назначаться предположительно без лабораторного подтверждения, если подозрения высоки у беременных женщин и женщин в сроке до 2 недель после родов, включая женщин, перенесших потерю плода.
ВАКЦИНАЦИЯ TDAP
Вакцинация Tdap рекомендуется во время беременности Консультативным советом по практике иммунизации (ACIP) и ACOG в первую очередь для защиты новорожденных от высококонтагиозных бактерий Bordetella pertussis . 14 Несмотря на это, уровень иммунизации Tdap во время беременности колеблется чуть выше 50%.
14 Несмотря на это, уровень иммунизации Tdap во время беременности колеблется чуть выше 50%.
Младенцы в возрасте до 1 года подвергаются наибольшему риску тяжелых симптомов и последствий коклюша; это основная причина предотвратимой с помощью вакцины смерти в этой возрастной группе. 15
Вакцинация очень эффективна для защиты младенцев от коклюшной инфекции, предотвращая более 90% госпитализаций и 95% смертей от коклюша в первые 2–3 месяца жизни. 16 Вакцинация во время беременности особенно важна, так как она усиливает материнские коклюшно-специфические IgG-антитела, которые пассивно приобретаются плодом во время беременности. 17 Без вакцинации матери возникает пробел в защите после родов, поскольку младенцы не могут получить свою первую вакцинацию против коклюша до 6-недельного возраста, когда они начинают курс из 5 доз с установленными интервалами между 2 месяцами и 6 годами жизни. возраст. 14
Сроки иммунизации Tdap
Tdap следует вводить беременным женщинам в начале третьего триместра каждой беременности, в идеале между 27 и 36 неделями беременности, независимо от сроков предыдущей вакцинации Tdap. Его можно вводить на ранних сроках беременности для пользы матери (например, при воздействии столбняка), и в таких случаях его не нужно повторять позже во время беременности или после родов. Женщинам, которые не получали Tdap до родов, его можно назначать после родов. Не следует давать предубеждения, если пациенту не назначена запланированная вакцинация.
Его можно вводить на ранних сроках беременности для пользы матери (например, при воздействии столбняка), и в таких случаях его не нужно повторять позже во время беременности или после родов. Женщинам, которые не получали Tdap до родов, его можно назначать после родов. Не следует давать предубеждения, если пациенту не назначена запланированная вакцинация.
Вакцинация против коклюша противопоказана пациентам, у которых развилась тяжелая аллергическая реакция после предыдущей дозы или энцефалопатия без идентифицируемой причины в течение 7 дней после получения вакцины против коклюша.
Вакцинация членов семьи
С 2005 г. ACIP рекомендует стратегию «коконирования» (т. е. вакцинации людей, вступающих в тесный контакт с новорожденным), чтобы обеспечить наилучшую защиту от коклюша до тех пор, пока не начнется рекомендуемый график вакцинации детей. 14 Однако программы, использующие эту стратегию, дали противоречивые результаты из-за проблем с вакцинацией других членов семьи. Кроме того, данные свидетельствуют о том, что иммунизация Tdap не может полностью предотвратить передачу бактерий. Тем не менее, ACIP продолжает рекомендовать эту практику, и врачи первичного звена, которые могут ухаживать за несколькими членами семьи, могут продвигать эту политику.
Кроме того, данные свидетельствуют о том, что иммунизация Tdap не может полностью предотвратить передачу бактерий. Тем не менее, ACIP продолжает рекомендовать эту практику, и врачи первичного звена, которые могут ухаживать за несколькими членами семьи, могут продвигать эту политику.
Решение проблем безопасности
Безопасность вакцинации Tdap для матери и плода хорошо документирована, 18 и не увеличивает риски беременности, такие как преэклампсия, задержка роста плода, мертворождение или преждевременные роды. 19 Рисков для развития плода или новорожденного не выявлено. Как и в случае вакцины против сезонного гриппа, общие реакции на введение матери Tdap включают боль в месте инъекции, головную боль и утомляемость.
Лечение коклюша
Несмотря на то, что коклюш в основном лечится посредством вакцинации в Соединенных Штатах, заражение все же происходит. Коклюш имеет 3 стадии: катаральную стадию с симптомами инфекции верхних дыхательных путей, пароксизмальную стадию с кашлевыми спазмами и реконвалесцентную стадию с медленным исчезновением частоты и тяжести кашля. Больные наиболее заразны в катаральной и пароксизмальной стадиях. 20
Больные наиболее заразны в катаральной и пароксизмальной стадиях. 20
Если беременная пациентка или контактировавшая с ней в домашнем хозяйстве женщина заразилась коклюшем, лечение следует начать в течение 21 дня после контакта, чтобы уменьшить симптоматическую инфекцию и ее распространение. Лечение беременных взрослых проводится по одной из следующих схем 21 :
Лечение матери особенно важно в послеродовой период для снижения риска передачи инфекции новорожденному. Любой режим безопасен во время лактации.
ВСЕ ВРАЧИ ДОЛЖНЫ пропагандировать вакцинацию
Поставщики первичной медико-санитарной помощи и медицинские специалисты должны регулярно оценивать статус вакцинации своих пациентов, особенно беременных женщин, а также рекомендовать и вводить соответствующие вакцины. Хотя акушеры-гинекологи несут основную ответственность за вакцинацию беременных и проведение вакцинации, не все из них имеют в своих кабинетах вакцины против гриппа или Tdap по финансовым или логистическим причинам, таким как хранение или отслеживание вакцин.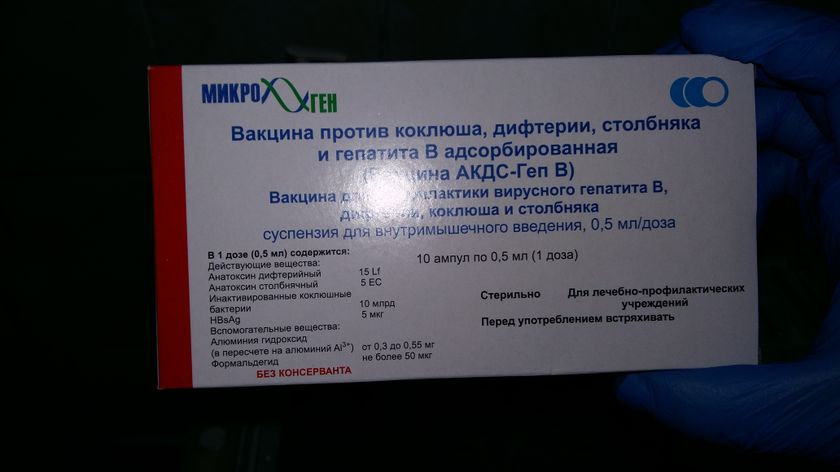 22 Национальный опрос акушеров-гинекологов в США показал, что среди тех, в чьей практике не было необходимой вакцины, 56% «всегда или часто» направляли пациентов к своему лечащему врачу для получения вакцины, реже обращаясь в отделы общественного здравоохранения. (32%) или аптеки (25%). 22
22 Национальный опрос акушеров-гинекологов в США показал, что среди тех, в чьей практике не было необходимой вакцины, 56% «всегда или часто» направляли пациентов к своему лечащему врачу для получения вакцины, реже обращаясь в отделы общественного здравоохранения. (32%) или аптеки (25%). 22
Многие беременные женщины отказываются от вакцины Tdap и вакцины против гриппа 23 по разным причинам, 24 включая распространенные заблуждения («от этого мне станет плохо»), опасения за безопасность плода или новорожденного и личные убеждения в отношении здоровья («Я никогда не делаю прививку от гриппа»). Обзор Mossad 25 содержит рекомендации по консультированию пациентов, которые сомневаются в ценности иммунизации.
Исследования различных методов продвижения вакцин, таких как обмен текстовыми сообщениями или видеоуроки, показали, что они приводят лишь к незначительному повышению согласия матерей на вакцинацию. 26,27 Многочисленные исследования показали, что рекомендация поставщика медицинских услуг является единственным наиболее влиятельным фактором, влияющим на согласие беременных женщин на вакцинацию во время беременности. 4,23,28
4,23,28
ВАКЦИНАЦИЯ ОТ COVID-19 ПРИ БЕРЕМЕННОСТИ
В декабре 2020 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США выдало разрешение на экстренное использование двух вакцин против SARS-CoV-2 (COVID-19).
Вскоре после этого ACOG 29 выпустила заявление о вакцинации против COVID-19 во время беременности, в котором говорилось: «ACOG рекомендуетне следует отказывать в вакцинации беременным женщинам, которые соответствуют критериям для вакцинации, основанным на приоритетных группах, рекомендованных ACIP». С аналогичным заявлением выступили Центры по контролю и профилактике заболеваний США (CDC). 30 Рекомендуется, но не обязательно, чтобы беременные и кормящие пациенты обсуждали со своим лечащим врачом свои особые обстоятельства и риски, а также необходимость принятия вакцины.
Хотя ни одна беременная пациентка не была включена в критические испытания безопасности вакцины, известно, что беременная женщина, заразившаяся COVID-19подвергается более высокому риску осложнений по сравнению с ее небеременными коллегами, 31 , и CDC отреагировали, включив беременность в качестве фактора риска для группы высокого риска для здоровья. Таким образом, беременным пациенткам, особенно работающим с повышенным риском, следует предлагать вакцину после соответствующего консультирования, как указано в руководстве ACOG и CDC.
Таким образом, беременным пациенткам, особенно работающим с повышенным риском, следует предлагать вакцину после соответствующего консультирования, как указано в руководстве ACOG и CDC.
Однако решение о вакцинации принимается исключительно по усмотрению пациентки, и обсуждение ее решения о вакцинации с лечащим врачом рекомендуется, но не является обязательным. Наконец, врачам рекомендуется быть в курсе имеющихся данных о COVID-19.вакцин с точки зрения рисков и преимуществ, а также потенциальных осложнений, чтобы они могли предоставлять наиболее точную информацию и консультировать своих пациентов.
РАСКРЫТИЕ ИНФОРМАЦИИ
Авторы не сообщают о соответствующих финансовых отношениях, которые в контексте их взносов могли бы быть восприняты как потенциальный конфликт интересов.
