После родов тромбоз: Тромбоз вен нижних конечностей в акушерской практике
Тромбоз вен нижних конечностей в акушерской практике
При беременности частота венозных тромбоэмболических осложнений (ВТЭО) составляет 0,2—1% [1—3], а риск тромбообразования повышается в 5—6 раз [2]. И при физиологически протекающей беременности имеются составляющие триады, описанной Р. Вирховым — изменения свойств крови, создающие благоприятные условия для тромбообразования, снижение скорости кровотока, изменение сосудистой стенки. Во время беременности развивается гиперкоагуляция, обусловленная повышением уровня факторов свертывания и агрегации тромбоцитов и снижением активности системы фибринолиза [3, 4]. Снижается концентрация физиологических антикоагулянтов, в частности растворимого протеина S [5]. Возникающее и прогрессирующее по мере развития беременности сдавление нижней полой вены ведет к повышению гидродинамического давления в ее системе и увеличению диаметра глубоких вен в нижних конечностях на фоне снижения в них кровотока [6, 7]. У беременных фактором, повреждающим внутреннюю выстилку вен, могут быть сопутствующие аутоиммунные заболевания, повышенная концентрация циркулирующих эстрогенов, вирусные инфекции [7]. Предпосылки для тромбообразования сохраняются и в послеродовом периоде — вены малого таза перерастянуты, кровоток в матке резко снижен, что приводит к формированию венозного стаза. Вероятность ВТЭО в послеродовом периоде повышается в 2—9 раз [7].
Предпосылки для тромбообразования сохраняются и в послеродовом периоде — вены малого таза перерастянуты, кровоток в матке резко снижен, что приводит к формированию венозного стаза. Вероятность ВТЭО в послеродовом периоде повышается в 2—9 раз [7].
В акушерстве выделяют группы очень высокой, высокой и умеренной степени риска развития ВТЭО [8, 9]. Группы очень высокого и высокого риска составляют беременные с различными формами тромбофилии и с ВТЭО в анамнезе — рецидив при беременности отмечен у 2—10% ранее перенесших ВТЭО [10]. При ряде тромбофилических состояний риск венозных тромбозов повышается более чем в 100 раз, особенно при наличии гомозиготных, мультигенных форм тромбофилии или комбинированных форм — сочетания антифосфолипидного синдрома (АФЛС) с генетическими тромбофилиями [2]. В группу умеренного риска развития ВТЭО входят беременные без тромбозов в прошлом, но с дополнительными факторами — осложнениями беременности, сопряженными с гиперкоагуляцией: тяжелым течением раннего токсикоза с дегидратацией, преэклампсией, соматической патологией (ревматические пороки сердца, оперированное сердце, системные заболевания, нефротический синдром, ожирение), оперативным родоразрешением, острыми и хроническими инфекциями. Выделяется значимая роль иммобилизации при беременности [11]. В группу умеренного риска должны быть включены и беременные с варикозным расширением подкожных вен нижних конечностей, которой страдает от 25 до 33% женщин, и с хронической венозной недостаточностью, имеющейся, по разным данным [12], у 3,7—15% женщин. У 50—95% женщин с патологией вен заболевание впервые возникло во время беременности [13, 14]. Хроническая венозная недостаточность, кроме создания условий для тромбообразования, может способствовать нарушению маточно-плацентарного, а затем и плодово-плацентарного кровотока, ухудшая перинатальный прогноз [15]. Повышают риск тромбоэмболических осложнений длительные статичные нагрузки и ожирение [10, 11].
Выделяется значимая роль иммобилизации при беременности [11]. В группу умеренного риска должны быть включены и беременные с варикозным расширением подкожных вен нижних конечностей, которой страдает от 25 до 33% женщин, и с хронической венозной недостаточностью, имеющейся, по разным данным [12], у 3,7—15% женщин. У 50—95% женщин с патологией вен заболевание впервые возникло во время беременности [13, 14]. Хроническая венозная недостаточность, кроме создания условий для тромбообразования, может способствовать нарушению маточно-плацентарного, а затем и плодово-плацентарного кровотока, ухудшая перинатальный прогноз [15]. Повышают риск тромбоэмболических осложнений длительные статичные нагрузки и ожирение [10, 11].
Клинические проявления тромбоза, независимо от его локализации, обычно представлены общими, болевыми симптомами и симптомами застоя. Диагностика тромбоза глубоких вен при беременности осложняется исходной венозной гипертензией в нижних конечностях с лимфовенозной недостаточностью, особенно слева, а также перераспределением болевой импульсации в связи с беременностью. Дифференциальная диагностика может быть затруднена, если сосудистая патология развивается на фоне других осложнений беременности — угрожающего прерывания, преэклампсии, многоводия [6].
Дифференциальная диагностика может быть затруднена, если сосудистая патология развивается на фоне других осложнений беременности — угрожающего прерывания, преэклампсии, многоводия [6].
Основным методом диагностики венозного тромбоза является компрессионное ультразвуковое дуплексное ангиосканирование (УЗАС), при отрицательных результатах — определение D-димера и повторное УЗАС в динамике. При подозрении на распространение тромбоза на илиокавальный сегмент и невозможности определения его проксимальной границы и характера рекомендуется компьютерная томография (КТ), магнитно-резонансная томография (МРТ) [8, 16]. Тест на D-димер рассматривается при беременности как вспомогательный метод, так как уровень D-димера возрастает при физиологической беременности по мере увеличения сроков гестации, а также при наличии акушерских осложнений, протекающих с развитием ДВС-синдрома [16]. Отмечено повышение уровня D-димера при преэклампсии [17] и гестационном сахарном диабете [18]. Есть мнение, что показатель D-димера информативен для оценки протромботической готовности до назначения низкомолекулярных гепаринов (НМГ), но менее показателен в процессе мониторинга эффективности назначенной терапии [19].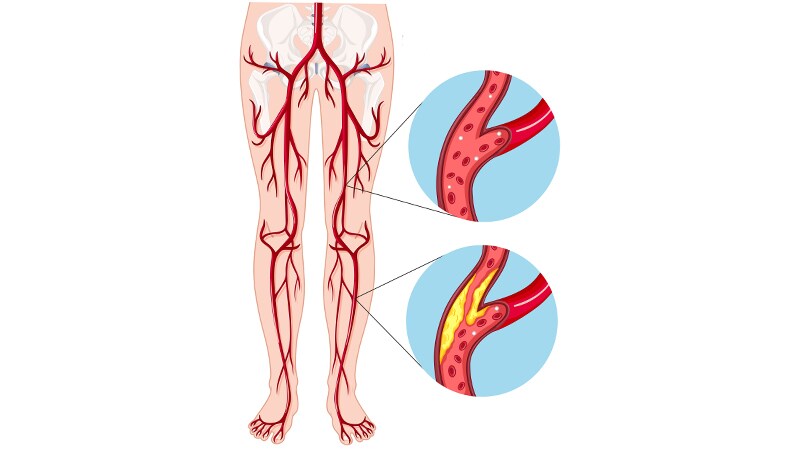
Цель исследования — анализ 10-летнего опыта лечения и родоразрешения беременных с тромбозом вен нижних конечностей для оценки выбора лечебной тактики.
Материал и методы
Материалом настоящего исследования послужили результаты обследования, лечения, динамического наблюдения и исхода беременности 96 женщин с тромбозом вен нижних конечностей, которые находились на лечении в многопрофильной больнице Саратова. В состав лечебного учреждения, помимо других отделений, входят родильный дом, гинекологические отделения, отделение лучевой диагностики и отделение сосудистой хирургии.
Все пациентки были разделены на три группы соответственно триместру беременности, в котором началось заболевание: 1-я группа (n=24, 25%) — I триместр, 2-я группа (n=26, 27%) — II триместр, 3-я группа (n=46, 47,9%) — III триместр.
Особенности ведения беременных с ВТЭО обусловлены необходимостью минимизации негативного воздействия на плод и тщательного постоянного контроля за его состоянием. До установления диагноза пациентки госпитализировались в отделение интенсивной терапии для совместного наблюдения акушерами-гинекологами и ангиохирургами до выяснений характера тромбоза. В срочном порядке выполнялось ультразвуковое дуплексное ангиосканирование (УЗАС) вен нижних конечностей, исследование гемостаза, определение D-димера. В ряде наблюдений назначалась магнитно-резонансная томография (II, III триместры). Проводилось акушерское обследование с эхографическим исследованием матки и плода с допплерометрией и кардиотокографией. После уточнения локализации и характера тромбоза и состояния плода избиралась тактика — хирургическая или консервативная. При исключении эмбологенного тромбоза и при достижении положительной динамики в состоянии гемостаза беременные продолжали лечение в сосудистом отделении либо, при наличии показаний, в акушерском или гинекологическом отделении в зависимости от срока гестации. Больным назначалась компрессия — применение компрессионного трикотажа 2—3-го класса или бинтование эластичным бинтом.
До установления диагноза пациентки госпитализировались в отделение интенсивной терапии для совместного наблюдения акушерами-гинекологами и ангиохирургами до выяснений характера тромбоза. В срочном порядке выполнялось ультразвуковое дуплексное ангиосканирование (УЗАС) вен нижних конечностей, исследование гемостаза, определение D-димера. В ряде наблюдений назначалась магнитно-резонансная томография (II, III триместры). Проводилось акушерское обследование с эхографическим исследованием матки и плода с допплерометрией и кардиотокографией. После уточнения локализации и характера тромбоза и состояния плода избиралась тактика — хирургическая или консервативная. При исключении эмбологенного тромбоза и при достижении положительной динамики в состоянии гемостаза беременные продолжали лечение в сосудистом отделении либо, при наличии показаний, в акушерском или гинекологическом отделении в зависимости от срока гестации. Больным назначалась компрессия — применение компрессионного трикотажа 2—3-го класса или бинтование эластичным бинтом. Антикоагулянтная терапия осуществлялась терапевтическими дозами НМГ. В последние годы мы с успехом применяем эноксапарин натрия — эниксум в рекомендуемых для лечения при беременности дозах [8, 9]. Препарат вводился в терапевтической дозе по 1 мг/кг через 12 ч. При достижении положительной динамики в течение тромботического процесса доза снижалась до профилактической — в зависимости от массы тела по 40—60 мг/сут вплоть до родоразрешения. Подкожное введение препарата прекращали не менее чем за 24 ч до планируемого завершения беременности — прерывания беременности, кесарева сечения или родовозбуждения. Антикоагулянтная терапия возобновлялась через 6—12 ч после вмешательства или родоразрешения. После выписки из стационара всем пациенткам рекомендовано ношение компресионного трикотажа и продленное использование НМГ (эноксапарина) — беременным до родоразрешения, родильницам — до 4—6 нед послеродового периода в зависимости от наличия факторов, предрасполагающих к рецидиву.
Антикоагулянтная терапия осуществлялась терапевтическими дозами НМГ. В последние годы мы с успехом применяем эноксапарин натрия — эниксум в рекомендуемых для лечения при беременности дозах [8, 9]. Препарат вводился в терапевтической дозе по 1 мг/кг через 12 ч. При достижении положительной динамики в течение тромботического процесса доза снижалась до профилактической — в зависимости от массы тела по 40—60 мг/сут вплоть до родоразрешения. Подкожное введение препарата прекращали не менее чем за 24 ч до планируемого завершения беременности — прерывания беременности, кесарева сечения или родовозбуждения. Антикоагулянтная терапия возобновлялась через 6—12 ч после вмешательства или родоразрешения. После выписки из стационара всем пациенткам рекомендовано ношение компресионного трикотажа и продленное использование НМГ (эноксапарина) — беременным до родоразрешения, родильницам — до 4—6 нед послеродового периода в зависимости от наличия факторов, предрасполагающих к рецидиву.
Результаты и обсуждение
Большая часть наших пациенток — 72 (76%) из 96 имели 2 фактора риска и более развития ВТЭО и входили в группу умеренного риска. У 59 имело место варикозное расширение вен нижних конечностей (рис. 1), Рис. 1. Факторы риска развития тромбофлебитических осложнений. у 21 — нарушение жирового обмена II—III степени, артериальной гипертензией страдали 17 беременных, сахарным диабетом — 2. Курили 9 пациенток и до беременности и во время нее, у 5 профессиональные обязанности были связаны с длительным статичным положением, 2 (2,08%) пациентки во II триместре беременности были оперированы по поводу флегмонозного аппендицита, 4 (4,16%) беременных в прошлом получали консервативную терапию по поводу тромбоза поверхностных (n=3) и глубоких (n=1) вен нижних конечностей, судя по анамнестическим данным, ничем не спровоцированного. Последние 6 пациенток входили в группу высокого риска развития тромбоэмболических осложнений (см. рис. 1). Беременных с тромбофилией среди наших пациенток не было, тогда как по статистическим данным 15% всех случаев тромбозов глубоких вен нижних конечностей приходится на АФС [20].
У 59 имело место варикозное расширение вен нижних конечностей (рис. 1), Рис. 1. Факторы риска развития тромбофлебитических осложнений. у 21 — нарушение жирового обмена II—III степени, артериальной гипертензией страдали 17 беременных, сахарным диабетом — 2. Курили 9 пациенток и до беременности и во время нее, у 5 профессиональные обязанности были связаны с длительным статичным положением, 2 (2,08%) пациентки во II триместре беременности были оперированы по поводу флегмонозного аппендицита, 4 (4,16%) беременных в прошлом получали консервативную терапию по поводу тромбоза поверхностных (n=3) и глубоких (n=1) вен нижних конечностей, судя по анамнестическим данным, ничем не спровоцированного. Последние 6 пациенток входили в группу высокого риска развития тромбоэмболических осложнений (см. рис. 1). Беременных с тромбофилией среди наших пациенток не было, тогда как по статистическим данным 15% всех случаев тромбозов глубоких вен нижних конечностей приходится на АФС [20].
У 30 (31,25%) беременных патологический процесс локализовался в поверхностных, у 66 (68,75%) — в глубоких венах нижних конечностей (рис. 2). Рис. 2. Частота возникновения глубокого и поверхностного тромбозов нижних конечностей в различные триместры беременности.
2). Рис. 2. Частота возникновения глубокого и поверхностного тромбозов нижних конечностей в различные триместры беременности.
В 56 (58,4%) наблюдениях тромбоз имел проксимальную, в 40 (41,6%) дистальную локализацию (рис. 3). Рис. 3. Частота возникновения дистального и проксимального тромбозов нижних конечностей в различные триместры беременности.
Госпитализированы в I триместре беременности 24 (25%) пациентки 1-й группы (рис. 4). Рис. 4. Распределение больных по триместрам беременности (n=96). В этой группе в 15 (62,5%) наблюдениях имел место тромбофлебит поверхностных вен голени и бедра, сочетавшийся с варикозным расширением вен. У 6 (25%) пациенток с проксимальной границей тромбоза большой подкожной вены на уровне верхней трети бедра выполнена кроссэктомия (перевязка большой подкожной вены и ее мелких ветвей), остальные получали консервативную терапию. У 9 (37,5%) пациенток, госпитализированных в I триместре, диагностирован проксимальный неэмбологенный тромбоз глубоких вен. Проведенная консервативная терапия была эффективной. 5 больным, госпитализированным в I триместре и пожелавшим прервать беременность, был произведен искусственный аборт. Кроме того, в 2 наблюдениях диагностирована неразвивающаяся беременность, что потребовало опорожнения матки. Внутриматочное вмешательство производилось после достижения положительной динамики показателей гемостаза на фоне антикоагулянтной терапии, продолженной после операции. Остальные 17 (70,8%) пациенток 1-й группы благополучно доносили беременность (см. таблицу). Исход беременности при тромбозе вен нижних конечностей Повторных эпизодов тромбоза до родов у них не было. В 2 наблюдениях в раннем послеродовом периоде выполнялось ручное обследование стенок полости матки в связи с гипотоническим кровотечением. Абдоминально родоразрешена только одна беременная в связи с преждевременной отслойкой плаценты при сроке гестации 36—37 нед.
Проведенная консервативная терапия была эффективной. 5 больным, госпитализированным в I триместре и пожелавшим прервать беременность, был произведен искусственный аборт. Кроме того, в 2 наблюдениях диагностирована неразвивающаяся беременность, что потребовало опорожнения матки. Внутриматочное вмешательство производилось после достижения положительной динамики показателей гемостаза на фоне антикоагулянтной терапии, продолженной после операции. Остальные 17 (70,8%) пациенток 1-й группы благополучно доносили беременность (см. таблицу). Исход беременности при тромбозе вен нижних конечностей Повторных эпизодов тромбоза до родов у них не было. В 2 наблюдениях в раннем послеродовом периоде выполнялось ручное обследование стенок полости матки в связи с гипотоническим кровотечением. Абдоминально родоразрешена только одна беременная в связи с преждевременной отслойкой плаценты при сроке гестации 36—37 нед.
У 26 (27,1%) пациенток (2-я группа) тромбоз вен нижних конечностей развился во II триместре беременности. В 10 (38,5%) наблюдениях процесс локализовался в поверхностных венах, в 16 (61,5%) наблюдениях — в глубоких венах. 15 (57,7%) беременных, госпитализированных во II триместре с неэмбологенным тромбозом, получили консервативную терапию. Лечение было эффективным, беременности пролонгированы до доношенного срока. Самопроизвольные, неосложненные роды произошли у 12 пациенток, в 3 наблюдениях выполнено кесарево сечение по акушерским показаниям — острый дистресс плода (2), преэклампсия (1). У 3 (11,5%) беременных с тромбозом большой подкожной вены бедра во II триместре была произведена кроссэктомия. В этих наблюдениях беременности были пролонгированы и завершились родами через естественные родовые пути без осложнений. В 6 (23%) наблюдениях был выявлен эмболоопасный характер тромбоза глубоких вен бедра (флотирующий тромб), что явилось показанием к оперативному вмешательству — пликации вены (наложение 1—3 П-образных швов с захватом обеих стенок вены) на уровне верхней трети бедра (рис. 5). Рис.
В 10 (38,5%) наблюдениях процесс локализовался в поверхностных венах, в 16 (61,5%) наблюдениях — в глубоких венах. 15 (57,7%) беременных, госпитализированных во II триместре с неэмбологенным тромбозом, получили консервативную терапию. Лечение было эффективным, беременности пролонгированы до доношенного срока. Самопроизвольные, неосложненные роды произошли у 12 пациенток, в 3 наблюдениях выполнено кесарево сечение по акушерским показаниям — острый дистресс плода (2), преэклампсия (1). У 3 (11,5%) беременных с тромбозом большой подкожной вены бедра во II триместре была произведена кроссэктомия. В этих наблюдениях беременности были пролонгированы и завершились родами через естественные родовые пути без осложнений. В 6 (23%) наблюдениях был выявлен эмболоопасный характер тромбоза глубоких вен бедра (флотирующий тромб), что явилось показанием к оперативному вмешательству — пликации вены (наложение 1—3 П-образных швов с захватом обеих стенок вены) на уровне верхней трети бедра (рис. 5). Рис. 5. Ультразвуковые сканограммы, В-режим. а — продольный срез, б — поперечный срез. Флотирующий тромб в бедренной вене (указан стрелками).
5. Ультразвуковые сканограммы, В-режим. а — продольный срез, б — поперечный срез. Флотирующий тромб в бедренной вене (указан стрелками).
Пациентки выписаны из стационара в удовлетворительном состоянии с прогрессирующей беременностью, двое из них родоразрешены абдоминально при 37—38 нед беременности по поводу сосудистой патологии. У 4 произошли произвольные срочные роды без осложнений. Неблагополучно завершилась беременность у пациентки, пликация у которой выполнялась на фоне инфарктной пневмонии — на 6-е сутки после операции произошел поздний выкидыш. Одной больной параллельно с пликацией была выполнена гистерэктомия, показанием к которой явилась неразвивающаяся при 18 нед беременность в сочетании с фибромиомой матки больших размеров.
Из 46 (47,9%) беременных 3-й группы, госпитализированных в III триместре, процесс локализовался в поверхностных венах голени и бедра у 5 (10,9%) пациенток. У 17 (36,1%) тромбоз произошел в глубоких венах голени и не носил флотирующего характера.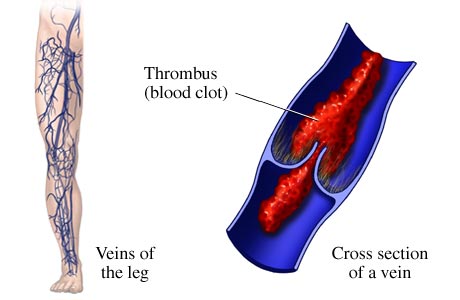 Этим 22 беременным проведена антикоагулянтная терапия. Из них 17 (77,3%) рожали самостоятельно, у 2 пациенток этой группы роды осложнились гипотоническим кровотечением. Кесарево сечение было выполнено 5 (22,7%) при доношенной беременности по акушерским показаниям (преэклампсия — 2 наблюдения, фетоплацентарная недостаточность в сочетании с задержкой роста плода — 2, нарушение сократительной деятельности матки — 1) с благополучным перинатальным исходом. У 24 (52%) беременных 3-й группы был диагностирован тромбоз глубоких вен бедра. В 9 наблюдениях выявлен флотирующий тромб, что потребовало экстренного хирургического вмешательства. Шести беременным со сроком гестации 35—36 нед, произведены кесарево сечение и хирургический этап операции — пликация бедренной вены проксимальнее места тромбоза. Недоношенные дети родились с оценкой по шкале Апгар 6—7 баллов, 2 детей в дальнейшем были переведены на 2-й этап выхаживания с последующей выпиской из стационара. В 3 наблюдениях флотирующий тромбоз глубокой вены бедра диагностирован в сроки беременности 26, 28 и 31 нед, что не позволяло с уверенностью рассчитывать на хороший перинатальный исход.
Этим 22 беременным проведена антикоагулянтная терапия. Из них 17 (77,3%) рожали самостоятельно, у 2 пациенток этой группы роды осложнились гипотоническим кровотечением. Кесарево сечение было выполнено 5 (22,7%) при доношенной беременности по акушерским показаниям (преэклампсия — 2 наблюдения, фетоплацентарная недостаточность в сочетании с задержкой роста плода — 2, нарушение сократительной деятельности матки — 1) с благополучным перинатальным исходом. У 24 (52%) беременных 3-й группы был диагностирован тромбоз глубоких вен бедра. В 9 наблюдениях выявлен флотирующий тромб, что потребовало экстренного хирургического вмешательства. Шести беременным со сроком гестации 35—36 нед, произведены кесарево сечение и хирургический этап операции — пликация бедренной вены проксимальнее места тромбоза. Недоношенные дети родились с оценкой по шкале Апгар 6—7 баллов, 2 детей в дальнейшем были переведены на 2-й этап выхаживания с последующей выпиской из стационара. В 3 наблюдениях флотирующий тромбоз глубокой вены бедра диагностирован в сроки беременности 26, 28 и 31 нед, что не позволяло с уверенностью рассчитывать на хороший перинатальный исход. Поэтому была выполнена только пликация вены с последующей консервативной терапией. Эти беременные после завершения лечения в отделении сосудистой хирургии находились под наблюдением акушеров до 37—38 нед беременности и были родоразрешены в плановом порядке абдоминально. Кесаревым сечением завершилась беременность и у 15 женщин с неэмбологенным тромбозом, развившимся после 34 нед беременности. Им проводилась антикоагулянтная терапия до срока гестации 37—38 нед, после чего было выполнено кесарево сечение с продолжением антикоагулянтной терапии в послеродовом периоде. Случаев массивной кровопотери в родах не было. Не было и случаев перинатальной смерти. После родоразрешения продолжалось проведение антикоагулянтной терапии в сочетании с ранней активизацией родильниц и использованием компрессионного трикотажа. Считается, что в тех наблюдениях, когда острые явления тромбоза к моменту родоразрешения купировались не полностью, безопаснее выполнить кесарево сечение, поскольку активная родовая деятельность может привести к фрагментации тромба и его проксимальной миграции [6].
Поэтому была выполнена только пликация вены с последующей консервативной терапией. Эти беременные после завершения лечения в отделении сосудистой хирургии находились под наблюдением акушеров до 37—38 нед беременности и были родоразрешены в плановом порядке абдоминально. Кесаревым сечением завершилась беременность и у 15 женщин с неэмбологенным тромбозом, развившимся после 34 нед беременности. Им проводилась антикоагулянтная терапия до срока гестации 37—38 нед, после чего было выполнено кесарево сечение с продолжением антикоагулянтной терапии в послеродовом периоде. Случаев массивной кровопотери в родах не было. Не было и случаев перинатальной смерти. После родоразрешения продолжалось проведение антикоагулянтной терапии в сочетании с ранней активизацией родильниц и использованием компрессионного трикотажа. Считается, что в тех наблюдениях, когда острые явления тромбоза к моменту родоразрешения купировались не полностью, безопаснее выполнить кесарево сечение, поскольку активная родовая деятельность может привести к фрагментации тромба и его проксимальной миграции [6].
На 1—2-е сутки после родов через естественные родовые пути тромбоз глубоких вен нижней конечности рецидивировал у 3 (3,1%) наших пациенток. Эти родильницы имели варикозную болезнь нижних конечностей и другие факторы риска (нарушение жирового обмена, умеренная преэклампсия) и перенесли тромбоз глубоких вен во II триместре беременности. Рекомендованная дородовая антикоагулянтная терапия им выполнялась бессистемно. После проведенной консервативной терапии родильницы выписаны из отделения сосудистой хирургии в удовлетворительном состоянии.
Таким образом, наиболее тромбоопасным периодом при беременности является ее III триместр. Оперативное лечение по поводу венозной патологии перенесли 25% беременных, остальные получали консервативную терапию с хорошим эффектом. Благополучно завершилась беременность у 87 (90,6%) пациенток, из них абдоминально родоразрешены 35 (40,2%) беременных. Показанием для кесарева сечения в 9 наблюдениях послужила акушерская патология, в 26 наблюдениях оперативное родоразрешение предпринято в связи с сосудистой патологией.
Выбор метода и сроков разрешения определяется и особенностями тромботического процесса и акушерской ситуацией [20]. Такая тактика позволила избежать не только материнской и перинатальной смертности, но и тяжелых осложнений.
Выводы
1. Наиболее тромбоопасным периодом при беременности является ее III триместр — почти 48% обследованных пациенток госпитализированы в III триместре.
2. Эмболоопасный тромбоз, потребовавший хирургического вмешательства, имел место у 25% беременных.
3. При отсутствии угрозы развития опасных осложнений и стабильном состоянии жизнеспособного плода при ВТЭО у беременных показано консервативное лечение.
4. Консервативная терапия, основой которой являлись НМГ (в последние годы эниксум), дала хороший результат у 75% пациенток.
5. Избранная лечебная тактика способствовала благополучному завершению желанной беременности в 95,6% наблюдений; абдоминальное родоразрешение произведено у 40,23% беременных. В большинстве наблюдений (26 из 35) кесарево сечение выполнено с учетом характера сосудистой патологии. Тромбоз вен нижних конечностей при беременности существенно увеличивает число абдоминальных родоразрешений.
В большинстве наблюдений (26 из 35) кесарево сечение выполнено с учетом характера сосудистой патологии. Тромбоз вен нижних конечностей при беременности существенно увеличивает число абдоминальных родоразрешений.
Сведения об авторах
Салов Игорь Аркадьевич — докт. мед. наук, проф., зав. кафедрой акушерства и гинекологии лечебного факультета Саратовского государственного медицинского университета. 410012, Саратов, ул. Большая Казачья, 112. Засл. врач России, главный врач городской клинической больницы №1 Саратова. 410017, Саратов ул. им. Хользунова, 19; e-mail: [email protected]; https://orcid.org/0000-0002-1926-5418
Tурлупова Татьяна Ивановна — кандидат медицинских наук, доцент кафедры акушерства и гинекологии лечебного факультета Саратовского государственного медицинского университета. 410012, Саратов, ул. Большая Казачья, 112; e-mail: [email protected]; https//orcid.org.0000-0002-8439-8254
Морозова Виктория Анатольевна — канд.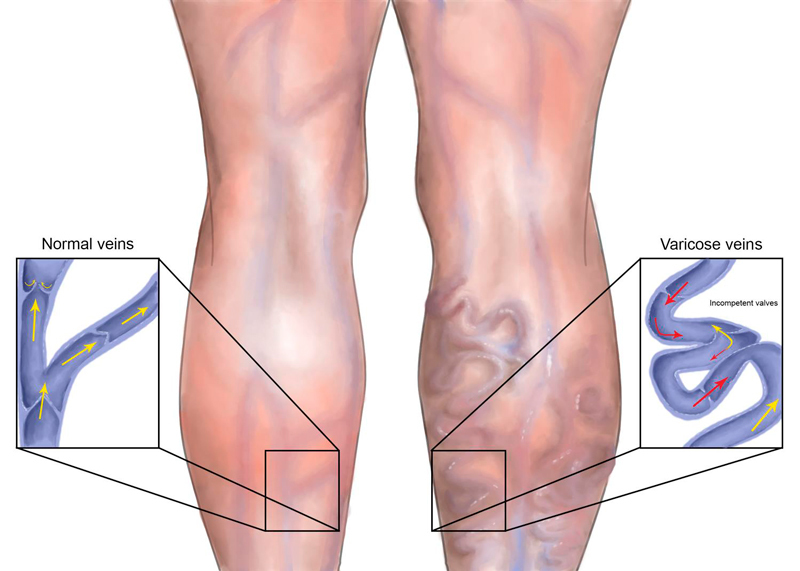 мед. наук, доцент кафедры акушерства и гинекологии лечебного факультета Саратовского государственного медицинского университета; 410012, Саратов, ул. Большая Казачья, 112; e-mail: [email protected]; https//orcid.org/0000-0002-6892-4272
мед. наук, доцент кафедры акушерства и гинекологии лечебного факультета Саратовского государственного медицинского университета; 410012, Саратов, ул. Большая Казачья, 112; e-mail: [email protected]; https//orcid.org/0000-0002-6892-4272
*e-mail: [email protected], https://orcid.org/0000-0002-1926-5418
Риск тромбоза при беременности
Тромбоз глубоких вен — это образование сгустка (тромба) в просвете сосуда (в данном случае глубоких вен, расположенных в толще мышц нижних конечностей), который вызывает нарушение кровообращения. Болезнь проявляется распирающей болью, покраснением и отеком в месте тромбоза. Болезнь может протекать как бессимптомно, так и привести к жизнеугрожающему осложнению – тромбоэмболии легочной артерии1.
Женщины в меньшей степени подвержены риску развития венозного тромбоза, однако, во время беременности вероятность его возникновения значительно возрастает. Виной тому изменение гормонального фона, сдавление вен таза увеличенной маткой, нарушение баланса свертывающей системы крови, что может привести к патологическому тромбообразованию в венах2.
С первых дней беременности организм будущей мамы претерпевает серьезные изменения: происходит гормональная перестройка, могут снижаться показатели гемоглобина, ферритина, витамина В12, увеличиваются показатели холестерина, инсулина, щелочной фосфатазы, изменяется объем циркулирующей крови (таким образом организм адаптируется к развитию плода и последующим родам), перестраивается кровеносная система, а органы начинают работать «за двоих».
Тромботические осложнения – основная прямая причина материнской смертности во время беременности и в послеродовый период: 12,8% от всех смертей рожениц3,6. Поэтому необходимо пристально следить за здоровьем женщины во время беременности.
Основные факторы риска развития тромбоза у беременных
Врожденные аномалии сосудов и системы свертывания крови
Применение оральных контрацептивов и гормональная терапия
Онкологические заболевания
Варикозное расширение вен
Cдавление вен малого таза
Хронические заболевания сердечно-сосудистой системы
Беременность и послеродовый период
Возраст более 35 лет
Малоподвижный образ жизни
Основные факторы риска развития тромбоза у беременных
Основные факторы риска развития тромбоза у беременных
Ключевые симптомы тромбоза4
Почти всегда заболевание на ранних стадиях протекает без симптомов. Однако, можно выделить некоторые распространенные признаки тромбоза:
Однако, можно выделить некоторые распространенные признаки тромбоза:
Как обезопасить себя?
Отказаться за 6 месяцев до планируемой беременности от оральных контрацептивов и других препаратов, влияющих на свертываемость крови для снижения риска тромбообразования.
Во время планирования и протекания беременности регулярно консультироваться с врачом, тщательно выполняя все его рекомендации, направленные на укрепление здоровья мамы и малыша4.
График посещения врача беременными3,5
Подготовка к визиту3
При планировании беременности помимо лечащего врача вы можете также проконсультироваться с врачом-гематологом или любым другим специалистом, который занимается проблемой тромбоза и гемостаза во время беременности. Стоит вспомнить, какие из анализов вы сдавали в последние пару месяцев: это поможет доктору отследить динамику вашего состояния.
Лабораторное исследование системы гемостаза
Для профилактики тромботических осложнений во время беременности в ряде случаев врачи некоторым беременным пациенткам могут порекомендовать пройти лабораторное исследование с оценкой свертывающей системы крови — Коагулограмма с показателями таких факторов свертываемости как2-4:
- Фибриноген — фактор свертывания крови, превращается в фибрин, последний впоследствии образует тромб.

- Количество тромбоцитов – клеток, непосредственно участвующих в процессе свертывания крови.
- Активированное частичное тромбопластиновое время (АЧТВ) — время, за которое формируется сгусток в крови, после добавления к ней специальных активаторов этого процесса.
- МНО (международное нормализованное отношение) — используется для комплексной оценки кровеносной системы пациента, показывает, насколько “жидкая” кровь.
Продемонстрируйте врачу список всех препаратов, которые вы регулярно принимали в течение последних двух месяцев. Эта информация очень важна!
Необходимо заранее изучить, болели ли ваши родственники какими-либо заболеваниями, связанными с повышенной свертываемостью крови и образованием тромбов в венозном русле, а также болезнями почек и сердечно-сосудистой системы.
Если вы ведете трекинг фитнес-активности, можно предоставить эти данные своему лечащему врачу.
Советы беременным
Во время беременности при отсутствии противопоказаний при возможности стоит сохранять достаточно активный образ жизни. Небольшие физические нагрузки, такие как плавание и длительные пешие прогулки, только помогут вам и вашему будущему малышу быть здоровыми.
Небольшие физические нагрузки, такие как плавание и длительные пешие прогулки, только помогут вам и вашему будущему малышу быть здоровыми.
В качестве диеты рекомендуется употреблять в пищу продукты с низким содержанием холестерина, например: отруби, рыба, овощи, фрукты, в пище также должны присутствовать животные жиры.
Необходим тщательный сбор гинекологического анамнеза: истории предыдущих родов, процедур ЭКО или абортов.
Однако, эти данные почти всегда фиксируются в ваших амбулаторных картах и стоят отдельного уточнения только в случае, если ваши медицинские данные так или иначе были утеряны
Самое главное — регулярно посещайте врачей и медицинские центры, сдавайте все необходимые анализы, следуйте всем назначенным рекомендациям. Помните, что на ранних этапах можно предотвратить серьезные осложнения.
Во что бы то ни стало стоит отказаться от всех вредных привычек.
Получить консультацию профильного специалиста
И пройти специализированное обследование системы гемостаза можно в медицинских центрах, представленных на карте
Найти клинику
Илеофеморальный тромбоз после родов — Болезни сосудов — 22.
 08.2011
08.2011
/
анонимно
Уважаемый доктор! Посоветуйте, пожалуйста! И извините за объёмное сообщение.
Мой диагноз: илеофеморопоплитеальный тромбоз левой ноги.
Мне 31 год (рост 172см, вес 66кг), живу в Словении (бывш. Югославия). До недавнего времени была здорова, хронических заболеваний не было, никаких лекарств не принимала, аналаизы в норме. Родила второго ребёнка в конце июня этого года, роды и беременность без осложнений. (Первые роды шесть лет назад, также без особ. Выкидышей не было. В семье: бабушка умерла от ТЭЛА, мама страдает тромбофлебитом, у дяди — тромбоз голени.)
После родов поднялась высокая температура (до 39, держалась неделю). Обследование показало воспалительный процесс. Где он — врачи определить не смогли, под вопросом был диагноз эндометрита из-за стрептокока пиогенес (группа А), обнаруженного в мазке из влагалища. В больнице в/в давали Амоксиксициллин, затем ещё курс того же антибиотика в таблетках 3 недели. Кололи фраксипарин 7 дней (пока была в роддоме). Всё это время была практически иммобилизована из-за высокой температуры, слабости, низкого давления. Домой отпустили без предупреждения о возможном тромбозе, без лекарств, «разжижающих» кровь. Кол-во тромбоцитов вышло за пределы нормы после прекращения уколов фраксипарина.
Всё это время была практически иммобилизована из-за высокой температуры, слабости, низкого давления. Домой отпустили без предупреждения о возможном тромбозе, без лекарств, «разжижающих» кровь. Кол-во тромбоцитов вышло за пределы нормы после прекращения уколов фраксипарина.
12 июля (через 2 недели после родов) появились боли в бедре левой ноги, нижнем отделе позвоночника, анализы, на фоне высокого СОЭ показывали повышенное число тромбоцитов (до 700). На это гинекологи не обращали внимания и не назначили доп.обследования.
27 июля (через месяц после родов) внезапно отказала левая нога, слегка посинела и отекла (на тот момент разница в голени 2,5 см), наступить на неё не могла. Дальше: скорая, больница, Гепарин с переходом на варфарин. Неделю я лежала. Д-димер 5,924, СОЭ 57, тромбоциты 324.
Доплер (перевела, как смогла): Область илеофеморопоплитеально, сразу над инвагинальным лигаментом: гиперэхогенное включение в вене iliaki, которое продолжается в вену femoralis, не реканализирано. Вход вены safena magne заполнен — виден тромб, который продолжается 3-4 см над входом в вену safena magne. Затем тромб продолжается в дистальный отдел, где вена сужается. Тромб меньший по размеру, сжатие вены более-менее. Затем снова виден тромб, который расширяется в поплитеальную вену.
Затем тромб продолжается в дистальный отдел, где вена сужается. Тромб меньший по размеру, сжатие вены более-менее. Затем снова виден тромб, который расширяется в поплитеальную вену.
На 5тый день (1-го августа) отправили домой. Отёк спал, боли (от бедра до колена ) появлялись при опускании ноги вниз и при ходьбе. Хромая постепенно увеличивала время и дистанцию передвижения. МНО достигло отметки 2,32.
Анализы крови на 08 августа: Д-димер 0,585, фибриноген 6,28,, протромбиновое время 0,47, МНО 1,65, тромбиновое время 19,7.
14 августа опять появилась боль, очень острая, теперь только в голени. Пять дней не могла наступить на ногу, болело и в покое, появился небольшой отёк. Сейчас опять медленно могу передвигаться по квартире, стоять выдерживаю минуты 2-3, затем появляется боль и вынуждена придавать ноге горизонтальное положение. Повторный цветной допплер изменений не выявил.
Сейчас принимаю только варфарин. Иногда наклофен дуо и начала пить Детралекс. Ношу компрессионный чулок 2 степ. только на больной ноге. Дома, с помощью портативного аппарата делаю сеансы магнитотерапии. Планирую ходить в бассейн.
Дома, с помощью портативного аппарата делаю сеансы магнитотерапии. Планирую ходить в бассейн.
С маткой в данный момент всё в порядке, но ТРОМБОЦИТЫ — 460, СОЭ — 38, лейкоциты в норме.
Гематолог мог только догадываться о причине увеличенного числа тромбоцитов. Сказал, что диагностику на тромбофилию и миелопролиферативные заболевания (лейкемия) он провести не может из-за приёма варфарина. Назначил какие-то анализы, но результатов пока нет.
Нахожусь в глубокой депрессии из-за всего случившегося. Физически не могу ухаживать за грудным ребёнком, пришлось прекратить грудное вскармливание. Начиталась о последствиях ГВТ… Врачи здесь ничего не объясняют, лечение варфарином они назначили, на этом всё. Говорят, через полгода будет видно, что делать. Понимаю, жизнь моя круто поменялась, а детей надо растить…
Подскажите:
1. Конца тромба (выше промежности) на доплере не видно, опасно ли это, надо ли проводить доп. обследование, например МРТ ангиографию?
2. Понимаю, что всё зависит от конкретного больного, но есть хотя бы маленькая надежда на то, что такой длинный тромб как у меня, рассосётся?
3. Как поступать с нагрузкой? Упражнения для ног я делаю несколько раз в день. А как с передвижением: терпеть и ходить через боль или лучше садиться, когда боль усиливается?
Как поступать с нагрузкой? Упражнения для ног я делаю несколько раз в день. А как с передвижением: терпеть и ходить через боль или лучше садиться, когда боль усиливается?
4. Имеет ли смысл пить Детралекс?
5. Компрессионная терапия только на больной ноге — это нормально или стоит носить чулок и на здоровой тоже?
6. И самое главное, что ещё я могу сделать для скорейшего восстановления???? Альтернативные методы лечения (гомеопатия), зарядка, физиотерапия (какая?)….. Традиционная медицина может ещё что-то сделать, кроме варфарина? Тромболизинг — почему уже поздно?
Заранее огромное спасибо!
Отвечает Невольских Алексей Алексеевич
хирург-флеболог
Здравствуйте.
Тактика в принципе правильная. Беспокоит из анализов низкий уровень МНО — 1,65. На фоне непрямых антикоагулянтов он должен колебаться в пределах 2-3. Второе: доплерография — не метод диагностики тромбоза глубоких вен. Речь видимо идет о дуплексном ангиосканировании. Если все же была доплерография, то вам обязательно необходимо выполнить ангиосканирование. МРТ ангиография — по желанию. Речь идет об илеофеморальном тромбозе, а при таком диагнозе все же необходимо видеть верхушку тромба и степень ее фиксации к стенке вены.
МРТ ангиография — по желанию. Речь идет об илеофеморальном тромбозе, а при таком диагнозе все же необходимо видеть верхушку тромба и степень ее фиксации к стенке вены.
При условии адекватной компрессионной терапии (трикотаж 3 класса компрессии) и адекватной антикоагулянтной терапии (непрямые коагулянты под контролем МНО) тромб обязательно рассосется, наступит реканализация вены. Однако клапанный аппарат вены не восстановится никогда. Поэтому в той или иной степени нога отекать будет .
По поводу нагрузки: если флотации тромба нет, то ходить в чулке можно и нужно. Интенсивность нагрузок — по собственным ощущениям. Для снятия болей и уменьшения воспалительных реакций следует принимать нестероидные противовоспалительные препараты (найз, вольтарен, диклофенак, метиндол и т.д.), лучше в виде пролонгированных форм (ретард — диклофенак-ретард, метиндол-ретард). Можно свечи наклофен-дуо с диклофенаком. Чулок 3 класса компрессии необходимо носить только на больной ноге. На здоровой — хуже не будет, однако большого смысла в этом нет. Детралекс или другие венотоники (венорутон, троксерутин, флебодиа-600) — также хуже не будет, хотя на антикоагулянтную активность крови влияния они не оказывают. Если будете принимать — курс — 1,5-2 месяца.
Детралекс или другие венотоники (венорутон, троксерутин, флебодиа-600) — также хуже не будет, хотя на антикоагулянтную активность крови влияния они не оказывают. Если будете принимать — курс — 1,5-2 месяца.
Альтернативных методов лечения тромбоза глубоких вен не существует. Тромболизис не проводится и более того, опасен, так как может привести к тромбоэмболии и фатальному исходу. Нетрадиционная медицина не заменит антикоагулянтную терапию и должна применяться по принципу «не навреди».
Рад, если смог ответить на все ваши вопросы.
Всего вам доброго.
Похожие вопросы
анонимно (Женщина, 27 лет)
Илеофеморальный тромбоз
Здравствуйте! 3 недели назад диагностировали илеофеморальный тромбоз глубоких вен после родов(кесарево сечение). Выписали домой с улучшением(под коленом началась реканализация). Врач прописала продолжать колоть фраксипарин, пока кормлю грудью. Далее, как только…
Мария Ракина (Женщина, 27 лет)
Илео феморальный тромбоз глубоких вен
Здравствуйте! Через 3 недели после родов диагностировали илеофеморальный тромбоз. Началось всё с боли в пояснице, затем поднялась температура до 38 и дальше началась боль в ноге и в итоге она…
Началось всё с боли в пояснице, затем поднялась температура до 38 и дальше началась боль в ноге и в итоге она…
анонимно (Женщина, 33 года)
Терапия после тромбоза
Здравствуйте! На 10 неделе беременности был Илеофеморальный тромбоз. Всю беременность была На Клексане и месяц после ер. После родов прошло уже 3.5 месяца и я ничего не пью, тк гематолог…
Alina Striped (Женщина, 22 года)
Окклюзивный тромбоз
Здравствуйте. На сроке беременности 28 недель проснулась утром с опухшей левой ногой и болью в паху при движении. Так как в семье никто о тромбозах до этого не знал, решили…
анонимно (Женщина, 21 год)
Илеофеморальный тромбоз нижнией левой конечности
Здравствуйте. 12.12 я родила, роды были ер и без осложнений, где то с 23 начала болеть и отекать, но как то не обращалась в больницу, т.к ребёнок маленький. А числа…
анонимно (Женщина, 25 лет)
Перенесенный илеофеморальный флеботромбоз
Доброго дня. Мне 25 лет,два года назад был перенесен илеофеморальный флеботромбоз сосудов левой ноги. Через неделю после родов. На данный момент со свертываемостью все в порядке,врач назначает курсами детралекс и кардиомагнил….
Через неделю после родов. На данный момент со свертываемостью все в порядке,врач назначает курсами детралекс и кардиомагнил….
анонимно (Женщина, 25 лет)
Илеофеморальный тромбоз восстановление ноги
Здравствуйте! Месяц назад поставлен диагноз острый илеофеморальный тромбоз левой конечности (после родов). 5 Дней кололи гепарин, после узд (позитивная динамика, частичная реканализация) приписали ксарелто (3 недели 2 р. В день…
Послеродовая венозная тромбоэмболия: частота и факторы риска
. 2014 май; 123(5):987-996.
doi: 10.1097/AOG.0000000000000230.
Наоми К Теппер
1
, Шери Л. Буле, Маура К. Уайтман, Майкл Монсур, Полли А. Марчбэнкс, В. Крейг Хупер, Кэтрин М. Кертис
принадлежность
- 1 Отдел репродуктивного здоровья, Национальный центр профилактики хронических заболеваний и укрепления здоровья и Отдел болезней крови, Национальный центр врожденных дефектов и нарушений развития, Центры по контролю и профилактике заболеваний, Атланта, Джорджия.
PMID:
24785851
DOI:
10.1097/АОГ.0000000000000230
Наоми К. Теппер и др.
Акушерство Гинекол.
2014 май.
. 2014 май; 123(5):987-996.
doi: 10.1097/AOG.0000000000000230.
Авторы
Наоми К Теппер
1
, Шери Л. Буле, Маура К. Уайтман, Майкл Монсур, Полли А. Марчбэнкс, В. Крейг Хупер, Кэтрин М. Кертис
принадлежность
- 1 Отдел репродуктивного здоровья, Национальный центр профилактики хронических заболеваний и укрепления здоровья и Отдел болезней крови, Национальный центр врожденных дефектов и отклонений в развитии, Центры по контролю и профилактике заболеваний, Атланта, Джорджия.

PMID:
24785851
DOI:
10.1097/АОГ.0000000000000230
Абстрактный
Задача:
Рассчитать частоту послеродовой венозной тромбоэмболии по неделям после родов и изучить потенциальные факторы риска венозной тромбоэмболии в целом и в разные сроки в послеродовом периоде.
Методы:
Обезличенная информационная база данных о заявлениях о медицинском обслуживании от работодателей, планов медицинского страхования, больниц и программ Medicaid в Соединенных Штатах использовалась для выявления случаев госпитализации при родах среди женщин в возрасте 15–44 лет в течение 2005–2011 годов. Международная классификация болезней, 9-й пересмотр, клиническая модификация, диагноз и коды процедур использовались для выявления случаев венозной тромбоэмболии и связанных с ней характеристик и состояний у женщин с недавними родами. Доля заболеваемости венозной тромбоэмболией от недели после родов до 12 недели рассчитывалась на 10 000 родов. Логистическую регрессию использовали для расчета отношения шансов для выбранных факторов риска среди женщин с послеродовой венозной тромбоэмболией и среди женщин с венозной тромбоэмболией в раннем или позднем послеродовом периоде.
Международная классификация болезней, 9-й пересмотр, клиническая модификация, диагноз и коды процедур использовались для выявления случаев венозной тромбоэмболии и связанных с ней характеристик и состояний у женщин с недавними родами. Доля заболеваемости венозной тромбоэмболией от недели после родов до 12 недели рассчитывалась на 10 000 родов. Логистическую регрессию использовали для расчета отношения шансов для выбранных факторов риска среди женщин с послеродовой венозной тромбоэмболией и среди женщин с венозной тромбоэмболией в раннем или позднем послеродовом периоде.
Полученные результаты:
Доля заболеваемости послеродовой венозной тромбоэмболией была самой высокой в течение первых 3 недель после родов, снижаясь с 9 на 10 000 в течение первой недели до 1 на 10 000 через 4 недели после родов и неуклонно снижаясь в течение 12-й недели. Определенные акушерские процедуры и осложнения, такие как кесарево сечение, преэклампсия, кровотечение и послеродовая инфекция, приводили к повышенному риску венозной тромбоэмболии (отношение шансов от 1,3 до 6,4), который сохранялся в течение 12-недельного периода по сравнению с женщинами без этих факторов риска.
Вывод:
Риск послеродовой венозной тромбоэмболии наиболее высок в течение первых 3 недель после родов. Женщины с акушерскими осложнениями подвергаются наибольшему риску послеродовой венозной тромбоэмболии, и этот риск остается повышенным в течение первых 12 недель после родов.
Уровень доказательств:
II.
Похожие статьи
Связь между перипартальной гистерэктомией и венозной тромбоэмболией.
Мони Л., Барт У.Х. младший, Клапп М.А.
Мани Л. и соавт.
Am J Obstet Gynecol. 2022 Январь; 226(1):119.e1-119.e11. doi: 10.1016/j.ajog.2021.06.091. Epub 2021 2 июля.
Am J Obstet Gynecol. 2022.PMID: 34224689
Повторная госпитализация по поводу послеродовой венозной тромбоэмболии в США.

Вен Т., Райт Дж. Д., Гоффман Д., Д’Алтон М. Е., Мак В. Дж., Аттенелло Ф. Дж., Фридман А. М.
Вен Т и др.
Am J Obstet Gynecol. 2018 окт; 219(4):401.e1-401.e14. doi: 10.1016/j.ajog.2018.07.001. Epub 2018 11 июля.
Am J Obstet Gynecol. 2018.PMID: 30017675
Разработка и валидация модели прогнозирования риска венозной тромбоэмболии у женщин в послеродовом периоде: многонациональное когортное исследование.
Султан А.А., Уэст Дж., Грейндж М.Дж., Райли Р.Д., Тата Л.Дж., Стефанссон О., Флеминг К.М., Нельсон-Пирси С., Людвигссон Дж.Ф.
Султан А.А. и др.
БМЖ. 2016 5 декабря; 355: i6253. дои: 10.1136/bmj.i6253.
БМЖ. 2016.PMID: 27919934
Бесплатная статья ЧВК.Тенденции заболеваемости венозной тромбоэмболией во время беременности или после родов: 30-летнее популяционное исследование.

Heit JA, Kobbervig CE, James AH, Petterson TM, Bailey KR, Melton LJ 3rd.
Хейт Дж.А. и соавт.
Энн Интерн Мед. 2005 15 ноября; 143(10):697-706. doi: 10.7326/0003-4819-143-10-200511150-00006.
Энн Интерн Мед. 2005.PMID: 16287790
Риск венозной тромбоэмболии в послеродовом периоде: систематический обзор.
Джексон Э., Кертис К.М., Гаффилд М.Э.
Джексон Э. и др.
Акушерство Гинекол. 2011 март; 117(3):691-703. doi: 10.1097/AOG.0b013e31820ce2db.
Акушерство Гинекол. 2011.PMID: 21343773
Обзор.
Посмотреть все похожие статьи
Цитируется
Четвертый триместр: время для улучшения переходов в сердечно-сосудистой помощи.
Чой Э.
 , Каззи Б., Варма Б., Ортенгрен А.Р., Минхас А.С., Воут А.Дж., Беннетт В.Л., Льюи Дж., Мичос Э.Д.
, Каззи Б., Варма Б., Ортенгрен А.Р., Минхас А.С., Воут А.Дж., Беннетт В.Л., Льюи Дж., Мичос Э.Д.
Чой Э. и др.
Представитель Curr Cardiovasc Risk Rep. 2022, сентябрь 21:1–11. doi: 10.1007/s12170-022-00706-x. Онлайн перед печатью.
Curr Cardiovasc Risk Rep. 2022.PMID: 36159207
Бесплатная статья ЧВК.Обзор.
Связь между увеличением веса матери в разные периоды беременности и риском венозной тромбоэмболии: ретроспективное исследование случай-контроль.
У И, Пей Дж, Донг Л, Чжоу З, Чжоу Т, Чжао Х, Че Р, Хань З, Хуа Х.
У Ю и др.
Фронт Эндокринол (Лозанна). 2022 18 июля; 13:858868. doi: 10.3389/fendo.2022.858868. Электронная коллекция 2022.
Фронт Эндокринол (Лозанна). 2022.PMID: 35923618
Бесплатная статья ЧВК.Анестезиологические аспекты и антикоагулянтная терапия у беременных с механическими клапанами сердца.
Бхатия К., Шехата Н., Д’Суза Р.
Бхатия К. и др.
BJA Образование. 2022 июль; 22 (7): 273-281. doi: 10.1016/j.bjae.2022.01.004. Epub 2022 24 марта.
BJA Образование. 2022.PMID: 35754854
Обзор.
Аннотация недоступна.
Воспалительные заболевания кишечника и тромбоэмболические осложнения: есть чему поучиться.
Карвалью А.С., Пиньо Х., Кансела Э., Виейра Х.М., Силва А., Министро П.
Карвалью А.С. и соавт.
Терапия Adv Гастроэнтерол. 2022 25 мая; 15:17562848221100626. дои: 10.1177/17562848221100626. Электронная коллекция 2022.
Терапия Adv Гастроэнтерол. 2022.PMID: 35651649
Бесплатная статья ЧВК.Предотвращение послеродовой венозной тромбоэмболии в 2022 году: описательный обзор.
Блондон М.
 , Скит Л.
, Скит Л.
Блондон М. и др.
Front Cardiovasc Med. 2022 12 апр;9:886416. doi: 10.3389/fcvm.2022.886416. Электронная коллекция 2022.
Front Cardiovasc Med. 2022.PMID: 35498021
Бесплатная статья ЧВК.Обзор.
Просмотреть все статьи «Цитируется по»
использованная литература
Джеймс АХ. Тромбоз, связанный с беременностью. Гематология Am Soc Hematol Educ Program 2009: 277–85.
Торнтон П., Дуглас Дж. Коагуляция при беременности. Best Pract Res Clin Obstet Gynaecol 2010; 24: 339–52.
Джексон Э., Кертис К., Гаффилд М. Риск венозной тромбоэмболии в послеродовом периоде: систематический обзор. Obstet Gynecol 2011;117:691–703.

Epiney M, Boehlen F, Boulvain M, Reber G, Antonelli E, Morales M и др. Уровни D-димера во время родов и после родов. Дж. Тромб Хемост 2005; 3: 268–71.
Хеллгрен М. Гемостаз при нормальной беременности и послеродовом периоде. Семин Тромб Хемост 2003; 29: 125–30.
термины MeSH
Профилактика послеродовой венозной тромбоэмболии в 2022 г.: описательный обзор
Введение
Связанная с беременностью венозная тромбоэмболия (ЛА-ВТЭ) является причиной около 10% ВТЭ у женщин (1). Активация системы свертывания крови, эндотелиальная травма и венозный застой — все это способствует повышенному риску во время беременности.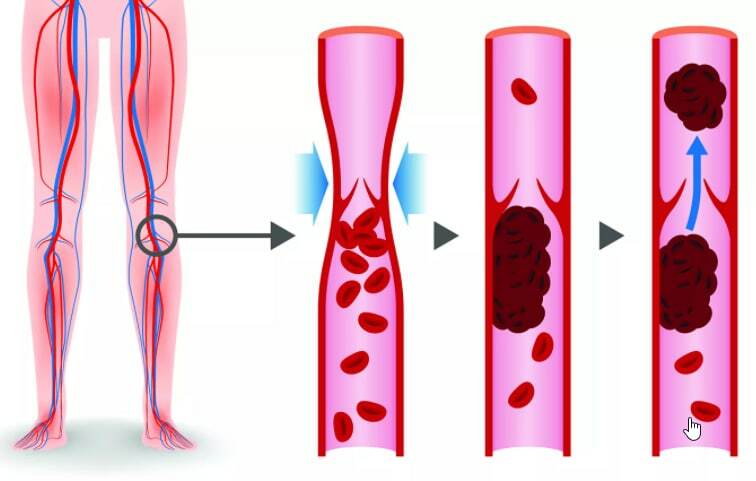 Эндогенные гормоны вызывают гиперкоагуляцию, характеризующуюся повышением уровня факторов свертывания крови (фибриноген, факторы VII, VIII, X и фактор фон Виллебранда), снижением уровня антитромботических факторов (протеин S, протеин С), приобретенной резистентностью к ингибированию протеином С, и снижение фибринолитической активности (снижение активности тканевого активатора плазминогена и увеличение ингибиторов активатора плазминогена 1 и 2) (1). Застой крови опосредован венозным расширением и сдавлением подвздошных вен (2), особенно левой общей подвздошной вены. Наконец, повреждение сосудов возникает при родах.
Эндогенные гормоны вызывают гиперкоагуляцию, характеризующуюся повышением уровня факторов свертывания крови (фибриноген, факторы VII, VIII, X и фактор фон Виллебранда), снижением уровня антитромботических факторов (протеин S, протеин С), приобретенной резистентностью к ингибированию протеином С, и снижение фибринолитической активности (снижение активности тканевого активатора плазминогена и увеличение ингибиторов активатора плазминогена 1 и 2) (1). Застой крови опосредован венозным расширением и сдавлением подвздошных вен (2), особенно левой общей подвздошной вены. Наконец, повреждение сосудов возникает при родах.
Клиническая значимость ЛА-ВТЭ подчеркивается его смертностью и заболеваемостью. Примерно 1/100 000 беременных женщин умирает от легочной эмболии в западном мире (3). По сравнению с небеременными тромбозы глубоких вен (ТГВ) чаще возникают проксимальнее с вовлечением подвздошно-бедренных вен. Послеродовой ТГВ осложняется высокой частотой развития посттромботического синдрома, снижающего отдаленное качество жизни (4, 5). Кроме того, поскольку прямые пероральные антикоагулянты противопоказаны во время грудного вскармливания, необходимо использовать низкомолекулярные гепарины или антагонисты витамина К в послеродовом периоде, каждый из которых имеет свои ограничения.
Кроме того, поскольку прямые пероральные антикоагулянты противопоказаны во время грудного вскармливания, необходимо использовать низкомолекулярные гепарины или антагонисты витамина К в послеродовом периоде, каждый из которых имеет свои ограничения.
Наибольшее потенциальное влияние профилактики ЛА-ВТЭ (тромбопрофилактика) наблюдается в послеродовом периоде, определяемом как 6 недель после родов, с пиком заболеваемости ЛА-ВТЭ в первые 2 недели после родов (6). По сравнению с небеременными женщинами у женщин в послеродовом периоде риск ВТЭ повышен в 22–60 раз (7, 8). Однако, поскольку абсолютный риск ВТЭ остается низким в краткосрочной перспективе, необходимо выявление лиц, которым могут помочь профилактические меры, но это может быть сложным, например, путем стратификации риска. В этом описательном обзоре мы обобщим современные знания о факторах риска и стратификации риска послеродовой ВТЭ, о наших знаниях о пользе и риске механической и фармакологической тромбопрофилактики, а также о предпочтениях и ценностях пациенток в отношении послеродовой тромбопрофилактики. Эти темы будут рассмотрены в перспективе гипотетической послеродовой ситуации.
Эти темы будут рассмотрены в перспективе гипотетической послеродовой ситуации.
Описание клинического случая
35-летняя женщина родила сегодня своего первого новорожденного весом 3600 граммов на сроке беременности 39 недель. Из-за дистресса плода во время родов было выполнено экстренное кесарево сечение (кесарево сечение). У матери в анамнезе или семейном анамнезе не было ВТЭ, и, кроме ожирения (ИМТ 32,7, исходя из веса до беременности 89 кг и роста 165 см), других заболеваний не было. И мать, и новорожденный чувствуют себя хорошо через несколько часов после родов. Мать спрашивает о необходимости профилактики венозной тромбоэмболии.
Общий риск послеродовой ВТЭ
Абсолютный риск ВТЭ в течение 6 недель после родов низок на основании популяционных исследований, проведенных в нескольких странах. Основным преимуществом популяционных исследований является их большой размер выборки и обобщаемость, но определение ВТЭ обычно основывается на административных кодексах и/или некоторых признаках использования антикоагулянтов без вынесения решения по ВТЭ, поэтому существует возможность неправильной классификации.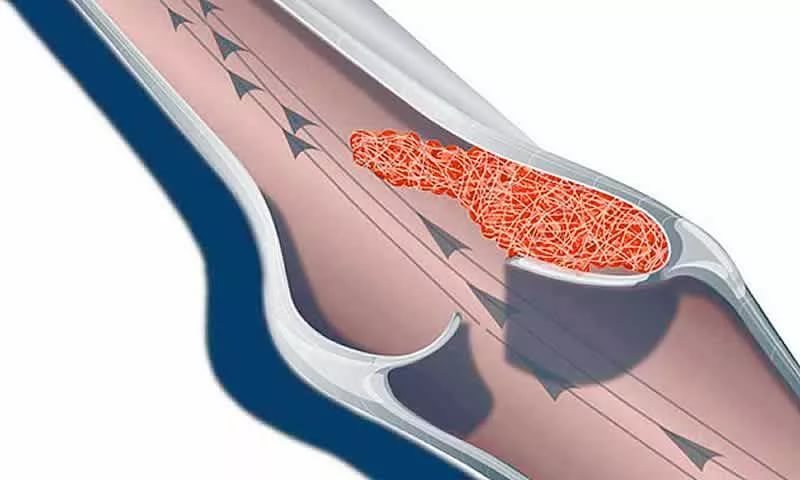 В Великобритании более 200 000 беременностей без предшествующей истории ВТЭ были выявлены в сети из 255 врачей общей практики между 1987 и 2004, с риском послеродовой ВТЭ 0,5/1000 родов (8). В Дании общенациональная проспективная когорта изучила >900 000 беременностей в период с 1995 по 2009 г., и после исключения женщин с ВТЭ в анамнезе риск составил 0,35/1000 родов (9). В Калифорнии в период с 2005 по 2010 год среди >1 600 000 беременностей риск составлял 2,8 на 1000 родов (10). В Канаде среди >3 800 000 беременностей риск составлял 1,2 на 1000 родов в период с 1991 по 2006 г. (11). Наконец, когорта Medicaid и частных страховых компаний в Соединенных Штатах в период с 2005 по 2011 год выявила риск 1,6 на 1000 родов (12). Вероятна недооценка рисков в первых 2 исследованиях (0,35–0,5/1000 родов) из-за исключения женщин с ВТЭ в анамнезе и неизвестной чувствительности алгоритма выявления исходов ВТЭ. Завышение возможно в 2 последних исследованиях (1,2–2,8/1000 родов) из-за широких диагностических кодов с субоптимальной положительной прогностической ценностью.
В Великобритании более 200 000 беременностей без предшествующей истории ВТЭ были выявлены в сети из 255 врачей общей практики между 1987 и 2004, с риском послеродовой ВТЭ 0,5/1000 родов (8). В Дании общенациональная проспективная когорта изучила >900 000 беременностей в период с 1995 по 2009 г., и после исключения женщин с ВТЭ в анамнезе риск составил 0,35/1000 родов (9). В Калифорнии в период с 2005 по 2010 год среди >1 600 000 беременностей риск составлял 2,8 на 1000 родов (10). В Канаде среди >3 800 000 беременностей риск составлял 1,2 на 1000 родов в период с 1991 по 2006 г. (11). Наконец, когорта Medicaid и частных страховых компаний в Соединенных Штатах в период с 2005 по 2011 год выявила риск 1,6 на 1000 родов (12). Вероятна недооценка рисков в первых 2 исследованиях (0,35–0,5/1000 родов) из-за исключения женщин с ВТЭ в анамнезе и неизвестной чувствительности алгоритма выявления исходов ВТЭ. Завышение возможно в 2 последних исследованиях (1,2–2,8/1000 родов) из-за широких диагностических кодов с субоптимальной положительной прогностической ценностью. В целом, эти исследования показывают, что около 1/1000 женщин испытывают ВТЭ в послеродовом периоде, при этом у 40% пациенток возникает легочная эмболия (6). Это означает, что у женщин без каких-либо факторов риска ВТЭ и у женщин, сочетающих несколько факторов риска, риск будет ниже и >0,1% соответственно.
В целом, эти исследования показывают, что около 1/1000 женщин испытывают ВТЭ в послеродовом периоде, при этом у 40% пациенток возникает легочная эмболия (6). Это означает, что у женщин без каких-либо факторов риска ВТЭ и у женщин, сочетающих несколько факторов риска, риск будет ниже и >0,1% соответственно.
Риск послеродовой ВТЭ 0,1% в 10–50 раз ниже, чем у стационарных больных с высоким риском ВТЭ (1–5%), которым показана тромбопрофилактика (13). Это также более чем в 10 раз ниже, чем частота ВТЭ после эндопротезирования тазобедренного или коленного сустава (14). Несмотря на то, что фактическое число случаев послеродовой ВТЭ велико из-за огромного знаменателя, превышающего 10 миллионов родов в год в Европе и Северной Америке, универсальная послеродовая тромбопрофилактика не может быть рекомендована для этого редкого события: при оптимистичном сценарии относительного снижения ВТЭ с помощью низкомолекулярного гепарина короткого действия (НМГ), необходимо пролечить около 1500 женщин, чтобы предотвратить 1 случай ВТЭ. Это число, необходимое для профилактики, вероятно, слишком велико с точки зрения затрат на здравоохранение и, вероятно, самих женщин. Ключевым моментом является стратификация женщин с разным уровнем риска, чтобы избежать лечения женщин с очень низким риском и снизить риск тромбообразования у женщин с высоким риском, чтобы найти оптимальный баланс снижения ВТЭ при минимизации затрат и возможных побочных эффектов фармакологической тромбопрофилактики.
Это число, необходимое для профилактики, вероятно, слишком велико с точки зрения затрат на здравоохранение и, вероятно, самих женщин. Ключевым моментом является стратификация женщин с разным уровнем риска, чтобы избежать лечения женщин с очень низким риском и снизить риск тромбообразования у женщин с высоким риском, чтобы найти оптимальный баланс снижения ВТЭ при минимизации затрат и возможных побочных эффектов фармакологической тромбопрофилактики.
Стратификация риска
Удивительно мало прямых данных для количественной оценки абсолютного послеродового риска ВТЭ среди пациенток с дополнительными преходящими или специфическими для беременности факторами риска. Большая часть доступных данных, используемых для поддержки руководств по клинической практике, была получена из крупных популяционных регистров или исследований случай-контроль. Хотя это и не исчерпывающий список, мы выделяем тип и уровень доступных данных при попытке предсказать послеродовой риск ВТЭ.
Предыдущий VTE
Несомненно, любая предшествовавшая ВТЭ представляет собой наиболее важный фактор риска с относительным риском >20–50 и абсолютным риском послеродовой ВТЭ 6–8% без тромбопрофилактики (15, 16).
Кесарево сечение
В комплексном метаанализе, в котором оценивались как исследования случай-контроль, так и когортные исследования, опубликованные до 2015 г., послеродовой риск ВТЭ после кесарева сечения был увеличен более чем в 3 раза по сравнению с вагинальными родами (17). Абсолютный риск по результатам проспективных исследований составил 2,6–4,3/1000 родов, или примерно 1 случай на 230–380 родов. Этот риск был выше при срочных/экстренных кесаревых сечениях, чем при плановых/элективных кесаревых сечениях. В метаанализе наблюдалась значительная неоднородность, отражающая не только различия в методологии исследования, но также в клинических контекстах и наличии других факторов риска.
Повышенный ИМТ
Существует положительная постепенная связь между риском послеродовой ВТЭ и ИМТ. В стационарном исследовании случай-контроль, в котором сравнивали женщин с объективно подтвержденной ВТЭ во время беременности или в послеродовом периоде с контрольной группой, риск послеродовой ВТЭ был несколько выше среди женщин с ИМТ ≥ 25 кг/м 2 в начале беременности. скорректированное отношение шансов (aOR) 2,4, 95% ДИ, 1,7–3,3] (18). В других исследованиях рассматривались различные пороговые значения ИМТ до беременности. Было обнаружено, что по сравнению с нормальным ИМТ категории с повышенным ИМТ прогрессивно повышают риск ВТЭ с ожирением III степени (ИМТ ≥40 кг/м 9 ).0007 2 ), имеющих самый высокий риск (aOR 4,0, 95% ДИ, 2,7–6,3) (19). Избыточное увеличение массы тела во время беременности менее изучено, и вопрос о том, является ли он фактором риска послеродовой ВТЭ или нет, остается спорным (18, 19). Из-за растущей распространенности и сильной связи с ВТЭ ожирение несет в себе значительный популяционный риск послеродовой ВТЭ.
скорректированное отношение шансов (aOR) 2,4, 95% ДИ, 1,7–3,3] (18). В других исследованиях рассматривались различные пороговые значения ИМТ до беременности. Было обнаружено, что по сравнению с нормальным ИМТ категории с повышенным ИМТ прогрессивно повышают риск ВТЭ с ожирением III степени (ИМТ ≥40 кг/м 9 ).0007 2 ), имеющих самый высокий риск (aOR 4,0, 95% ДИ, 2,7–6,3) (19). Избыточное увеличение массы тела во время беременности менее изучено, и вопрос о том, является ли он фактором риска послеродовой ВТЭ или нет, остается спорным (18, 19). Из-за растущей распространенности и сильной связи с ВТЭ ожирение несет в себе значительный популяционный риск послеродовой ВТЭ.
Маркеры плацентарной болезни
Задержка внутриутробного развития плода (ЗВУР), преждевременные роды и преэклампсия являются общепризнанными факторами риска послеродовой ВТЭ. В популяционном исследовании методом «случай-контроль» у женщин в послеродовом периоде, родивших новорожденных с низкой массой тела при рождении (<2500 г), риск ВТЭ был повышен в 3 раза, и этот риск сохранялся после поправки на возможные вмешивающиеся переменные (aOR 2,9). 8, 95% ДИ 1,80–4,93) (20). В других исследованиях, ЗВУР, преждевременные роды (определяемые как <37 недель) и преэклампсия показали аналогичный риск ВТЭ (18, 21, 22). Как определяется преэклампсия или ЗВУР, в том числе какой референтный стандарт ограничения роста или какие пороговые процентили используются, остается неясным и может меняться в разных странах.
8, 95% ДИ 1,80–4,93) (20). В других исследованиях, ЗВУР, преждевременные роды (определяемые как <37 недель) и преэклампсия показали аналогичный риск ВТЭ (18, 21, 22). Как определяется преэклампсия или ЗВУР, в том числе какой референтный стандарт ограничения роста или какие пороговые процентили используются, остается неясным и может меняться в разных странах.
Дополнительные факторы риска ВТЭ
Существует множество других факторов ВТЭ с незначительной или промежуточной связью с послеродовой ВТЭ, таких как послеродовое кровотечение, инфекция, текущее или недавнее курение или заболевания, включая диабет. Хотя постельный режим во время беременности является известным фактором риска ВТЭ, показания к строгому постельному режиму в настоящее время встречаются редко (18). Кроме того, взаимосвязь тромбофилии и семейного анамнеза с ВТЭ сложна и выходит за рамки данного обзора, но недавно была подвергнута метаанализу (23) и подробно описана в руководствах (24).
Стоит обсудить две области неопределенности. Во-первых, сроки послеродовой ВТЭ могут варьироваться в зависимости от типа факторов риска ВТЭ. В исследовании базы данных Великобритании у женщин с преждевременными родами или послеродовым кровотечением частота ВТЭ была выше только в первые 3 недели после родов. Для сравнения, у женщин с повышенным ИМТ ≥30 кг/м 2 или у женщин, перенесших кесарево сечение, риск сохранялся до 6 недель после родов (22). Учитывая множество факторов риска, которые необходимо оценить, а также необходимое количество пациентов и случаев ВТЭ, по-прежнему мало информации о сроках послеродовых событий ВТЭ для различных факторов риска. Во-вторых, необходимо уточнить влияние комбинированных факторов риска, особенно потому, что почти половина женщин являются носителями множественных факторов риска в послеродовом периоде (25). Например, когда у пациента повышенный ИМТ ≥ 25 кг/м 2 и со строгой дородовой иммобилизацией, aOR для послеродовой ВТЭ может быть в 40 раз выше по сравнению с пациенткой с нормальным ИМТ и отсутствием дородовой иммобилизации.
Во-первых, сроки послеродовой ВТЭ могут варьироваться в зависимости от типа факторов риска ВТЭ. В исследовании базы данных Великобритании у женщин с преждевременными родами или послеродовым кровотечением частота ВТЭ была выше только в первые 3 недели после родов. Для сравнения, у женщин с повышенным ИМТ ≥30 кг/м 2 или у женщин, перенесших кесарево сечение, риск сохранялся до 6 недель после родов (22). Учитывая множество факторов риска, которые необходимо оценить, а также необходимое количество пациентов и случаев ВТЭ, по-прежнему мало информации о сроках послеродовых событий ВТЭ для различных факторов риска. Во-вторых, необходимо уточнить влияние комбинированных факторов риска, особенно потому, что почти половина женщин являются носителями множественных факторов риска в послеродовом периоде (25). Например, когда у пациента повышенный ИМТ ≥ 25 кг/м 2 и со строгой дородовой иммобилизацией, aOR для послеродовой ВТЭ может быть в 40 раз выше по сравнению с пациенткой с нормальным ИМТ и отсутствием дородовой иммобилизации.
В настоящее время в руководствах предлагается проводить стратификацию риска с использованием эмпирических схем уровней или комбинации факторов риска по нескольким категориям: отсутствие тромбопрофилактики или только механическая тромбопрофилактика, краткосрочная фармакологическая тромбопрофилактика (дни) и 6-недельная фармакологическая тромбопрофилактика. Важно отметить, что такие рекомендации (ACOG (26), RCOG (27), ASH (24)), подробно изложенные в другом месте, резко различаются по доле женщин, которым рекомендована тромбопрофилактика, от 7 до 40% для всех родов (28) и 0,2 –73% при кесаревом сечении (29). Логично, что более высокая распространенность применения тромбопрофилактики связана с более низкими рисками среди пациентов, получающих тромбопрофилактику, и большим числом пациентов, нуждающихся в лечении для предотвращения 1 ВТЭ.
Недавней инновацией в этой области является разработка шкалы риска послеродовой ВТЭ («Риск материнского сгустка»), объединяющей в сложных формах следующие 11 материнских и акушерских факторов: возраст, ИМТ, варикозное расширение вен, сопутствующие заболевания, курение. , преэклампсия, кровотечение, инфекция, способ родоразрешения, паритет и масса тела при рождении (30). Шкала позволяет оценить послеродовой риск ВТЭ у отдельных женщин с факторами риска ВТЭ и, таким образом, может помочь сосредоточить усилия по профилактике на женщинах выше определенного порога риска. Эта оценка не применяется к женщинам с ВТЭ в анамнезе и не учитывает тромбофилию. Он прошел внешнюю проверку с использованием шведской базы данных и базы данных первичной медико-санитарной помощи Великобритании (31), однако с некоторыми ограничениями (32). Будут приветствоваться дальнейшие усилия по валидации, и пока они еще не включены в руководства по клинической практике.
, преэклампсия, кровотечение, инфекция, способ родоразрешения, паритет и масса тела при рождении (30). Шкала позволяет оценить послеродовой риск ВТЭ у отдельных женщин с факторами риска ВТЭ и, таким образом, может помочь сосредоточить усилия по профилактике на женщинах выше определенного порога риска. Эта оценка не применяется к женщинам с ВТЭ в анамнезе и не учитывает тромбофилию. Он прошел внешнюю проверку с использованием шведской базы данных и базы данных первичной медико-санитарной помощи Великобритании (31), однако с некоторыми ограничениями (32). Будут приветствоваться дальнейшие усилия по валидации, и пока они еще не включены в руководства по клинической практике.
Обсуждение случая
У пациента два промежуточных фактора риска ВТЭ: ожирение (ИМТ = 32,7 кг/м 2 ) с относительным риском 2,5 (19) и экстренное кесарево сечение с относительным риском около 4 , Предполагая, что базовый риск среди женщин без каких-либо факторов риска составляет 0,05%, мы могли бы в общих чертах оценить, с комбинацией факторов риска от 5,5 (аддитивная модель) до 10 (мультипликативная модель), что ее личный послеродовой риск ВТЭ составляет около 0,3–0,5. %. Использование калькулятора риска материнского сгустка дает более низкую оценку риска в 0,1%. Мы сообщаем пациентке, что ее риск послеродовой ВТЭ составляет около 0,1–0,5%, или примерно 1 случай на 200–1000 родов.
%. Использование калькулятора риска материнского сгустка дает более низкую оценку риска в 0,1%. Мы сообщаем пациентке, что ее риск послеродовой ВТЭ составляет около 0,1–0,5%, или примерно 1 случай на 200–1000 родов.
Как мы можем предотвратить послеродовую ВТЭ в ситуациях высокого риска?
Убедительные доказательства показывают, что низкие дозы гепарина, будь то нефракционированный гепарин или НМГ, снижают риск ТГВ и тромбоэмболии легочной артерии у терапевтических или хирургических стационарных пациентов примерно на 50–70% (33). В акушерских условиях уровень доказательности близок к нулю и недавно был резюмирован в обновленном Кокрейновском систематическом обзоре как имеющий «весьма неопределенный эффект» (34). Действительно, все доступные рандомизированные испытания включали небольшие размеры выборки, а некоторые из них были только пилотными рандомизированными испытаниями для проверки осуществимости. Нельзя сделать никаких выводов относительно эффективности и безопасности гепаринов в этой популяции. Кроме того, большинство пришло к выводу, что осуществимость крупномасштабного рандомизированного исследования была низкой из-за барьеров и низкого набора участников в послеродовом периоде (таблица 1).
Кроме того, большинство пришло к выводу, что осуществимость крупномасштабного рандомизированного исследования была низкой из-за барьеров и низкого набора участников в послеродовом периоде (таблица 1).
Таблица 1 . Опубликованные (псевдо) рандомизированные исследования гепаринов по сравнению с плацебо или отсутствием лечения для предотвращения послеродовой венозной тромбоэмболии.
Крупное моноцентровое исследование в Ираке, несмотря на то, что оно не было рандомизированным, последовательно распределяло 6-дневный курс низких доз бемипарина или эноксапарина или отсутствие лечения среди женщин после вагинальных родов или кесарева сечения, которые были отнесены к промежуточному риску послеродовой ВТЭ в соответствии с рекомендациями RCOG ( Таблица 1) (41). Совершенно удивительно, что исследователи сообщили о включении 7020 участников с чрезвычайно низким показателем 0,5% отказов от участия и 0% потерь для последующего наблюдения. Эноксапарин и бемипарин были связаны с 89Относительное снижение риска симптоматической ВТЭ на 95%, которое не было подтверждено. Это соответствовало снижению абсолютного риска на 0,3% (нужно лечить 333 человека). Это исследование вселяет надежду на то, что краткосрочное введение НМГ может эффективно снижать послеродовую ВТЭ, но не следует делать четких интерпретаций на основании его методологических ограничений, неизвестной внешней валидности и отсутствия отчетов о безопасности (кровотечения).
Это соответствовало снижению абсолютного риска на 0,3% (нужно лечить 333 человека). Это исследование вселяет надежду на то, что краткосрочное введение НМГ может эффективно снижать послеродовую ВТЭ, но не следует делать четких интерпретаций на основании его методологических ограничений, неизвестной внешней валидности и отсутствия отчетов о безопасности (кровотечения).
У нас есть ограниченные данные обсервационных исследований. Недавно два моноцентровых исследования, проведенных в США, не показали снижения случаев ВТЭ после внедрения стандартизированных послеродовых протоколов НМГ у родильниц с факторами риска ВТЭ, несмотря на увеличение использования послеродового эноксапарина с <1–>30% среди 9766 родов (42) и от 1 до 16% среди 24 299 родов (43). Важно отметить, что в одном из исследований также отмечался повышенный риск раневых гематом и незапланированных процедур в группе после применения протокола НМГ (43). Ограничения этих исследований включают ретроспективный дизайн исследования, оценивающий до и после вмешательства с течением времени, который не является рандомизированным, а также отсутствие независимого решения по ВТЭ и кровотечению. Эти противоречивые исследования подчеркивают все еще существующую неопределенность и необходимость дополнительных исследований в этой области.
Эти противоречивые исследования подчеркивают все еще существующую неопределенность и необходимость дополнительных исследований в этой области.
Другим интересным препаратом является аспирин в низких дозах. Его основными преимуществами являются его пероральный путь введения и известный профиль безопасности, в том числе при грудном вскармливании, с продемонстрированной пользой ВТЭ в других условиях [хирургическая тромбопрофилактика (14), вторичная профилактика ВТЭ (44)], хотя с потенциально более низким снижением риска ВТЭ, чем это НМГ. В настоящее время аспирин не рекомендуется в послеродовом периоде, но он является предметом продолжающихся испытаний (пилотное исследование PARTUM, описанное ниже).
Кормящим женщинам следует избегать применения прямых пероральных антикоагулянтов из соображений безопасности, и в настоящее время нет данных о профилактике ВТЭ у женщин, не кормящих грудью, в послеродовом периоде. С предыдущими сообщениями о безопасности в отношении учащения обильных менструальных кровотечений у женщин, принимающих пероральные антикоагулянты прямого действия для лечения ВТЭ, все еще необходимы дальнейшие исследования безопасности этого подхода у женщин, не кормящих грудью, в послеродовом периоде.
Механическая тромбопрофилактика, в частности прерывистая пневматическая компрессия (ИПК), также может снизить риск ВТЭ после операции (45). К сожалению, поскольку отсутствуют клинические данные для оценки ИПК в послеродовом периоде, роль механической тромбопрофилактики в этих условиях неясна. Кроме того, одно исследование указало на низкую приверженность к ношению компрессионных чулок после выписки из больницы, подчеркнув их бремя, несмотря на их безопасность (46).
Обсуждение случая
При кратковременном применении НМГ (до 10 дней) мы полагаем, что риск послеродовой ВТЭ у нашей пациентки может быть снижен вдвое, однако истинные преимущества НМГ до сих пор неизвестны. Другими словами, для предотвращения 1 случая ВТЭ необходимо лечение 400–2000 женщин. Мы сообщаем эти оценки пациентке, включая большую неопределенность, возможные побочные эффекты НМГ и предложение некоторых руководств (но не всех) назначать НМГ в ее ситуации. Мы также признаем, что у каждого из авторов свой подход, в том числе вариации продолжительности НМГ от пребывания в больнице (47) до 10 дней после родов (27).
Что женщины думают о послеродовой фармакологической тромбопрофилактике?
Взгляды и мнения пациентов имеют решающее значение в этой области текущей неопределенности. Поразительно, но мы очень мало знаем о предпочтениях и ценностях женщин в отношении стратегий тромбопрофилактики и о том, какой порог риска ВТЭ, по их мнению, должен оправдывать использование НМГ для краткосрочного введения в послеродовом периоде, но это может оказаться критически полезным.
В международном многоцентровом исследовании изучались предпочтения и ценности пациентов для принятия решения о дородовой тромбопрофилактике (40, 48). Используя ряд различных упражнений (прямой выбор, полезность для состояния здоровья и компромисс вероятности), авторы опросили 123 женщины с ВТЭ в анамнезе, которые были беременны или планировали беременность. Только около 80% женщин рассматривали возможность приема НМГ в дородовой период при риске ВТЭ 10%, что выше порога, при котором большинство врачей рекомендовали бы тромбопрофилактику. Это подчеркивает контраст между видением специалистов по ВТЭ и женщин с ВТЭ в анамнезе. Хотя это исследование не относится к решению о первичной тромбопрофилактике (женщины без ВТЭ в анамнезе) в послеродовом периоде, оно подчеркивает важность совместного принятия решений о риске ВТЭ.
Это подчеркивает контраст между видением специалистов по ВТЭ и женщин с ВТЭ в анамнезе. Хотя это исследование не относится к решению о первичной тромбопрофилактике (женщины без ВТЭ в анамнезе) в послеродовом периоде, оно подчеркивает важность совместного принятия решений о риске ВТЭ.
Насколько нам известно, и это весьма удивительно, ценность и предпочтения женщин в отношении послеродовой тромбопрофилактики или исследований послеродовой ВТЭ не изучались. Мы не знаем о предпочтительном пороге риска ВТЭ, который оправдывал бы использование НМГ в послеродовом периоде, по мнению беременных женщин, о том, как принимаются решения, учитывающие бремя и побочные эффекты НМГ, и как эти взгляды могут отличаться от их медицинских работников. . Кроме того, в значительной степени неизвестно, как мнения пациентов должны быть включены в руководства по клинической практике.
Сегодня существует большая разница между рисками ВТЭ для оправдания применения НМГ в послеродовом периоде между мнением экспертов (разработка рекомендаций) и фактической практикой, основанной на этих рекомендациях. При использовании риска образования тромбов у беременных для косвенной оценки риска ВТЭ, используемого в рекомендациях, в выборке рожениц из университетских больниц Женевы (28) мы обнаружили, что рекомендации RCOG 2015 г. и рекомендации ACOG 2018 г. предлагают профилактику тромбообразования при риске 0,12 и 0,20%. , соответственно. Это резко контрастирует с мнением экспертов, которые выступают за то, чтобы риск ВТЭ составлял 1–3%, чтобы оправдать послеродовую ВТЭ (24). Очевидно, что в этой области необходимы дополнительные исследования, чтобы лучше понять предпочтения и ценности женщин и гарантировать, что использование послеродовых НМГ достигает приемлемого количества, необходимого для предотвращения события ВТЭ, при минимизации вреда.
При использовании риска образования тромбов у беременных для косвенной оценки риска ВТЭ, используемого в рекомендациях, в выборке рожениц из университетских больниц Женевы (28) мы обнаружили, что рекомендации RCOG 2015 г. и рекомендации ACOG 2018 г. предлагают профилактику тромбообразования при риске 0,12 и 0,20%. , соответственно. Это резко контрастирует с мнением экспертов, которые выступают за то, чтобы риск ВТЭ составлял 1–3%, чтобы оправдать послеродовую ВТЭ (24). Очевидно, что в этой области необходимы дополнительные исследования, чтобы лучше понять предпочтения и ценности женщин и гарантировать, что использование послеродовых НМГ достигает приемлемого количества, необходимого для предотвращения события ВТЭ, при минимизации вреда.
Также представляет интерес приверженность послеродовой тромбопрофилактике, которая может быть субоптимальной. В исследовании, проведенном в 2018 г. в Израиле в специализированном центре, 250 родильниц прошли телефонное интервью в конце запланированной послеродовой тромбопрофилактики (48). В то время как приверженность НМГ в стационаре составляла 100 %, 33 % ввели <80 % от запланированного среднего значения НМГ в течение 7 дней после выписки, а 18 % не вводили ничего. Женщины с большей вероятностью соблюдали режим, если они использовали НМГ в прошлом или в дородовой период, а женщины, которые чувствовали, что получили хорошие технические разъяснения по поводу инъекций, с большей вероятностью соблюдали режим. Двумя основными причинами несоблюдения режима лечения были убеждение в том, что НМГ не нужен, и проблемы с инъекциями в домашних условиях. Эти причины были аналогичны причинам, описанным для неучастия в пилотном рандомизированном исследовании PROSPER, посвященном осуществимости, в котором оценивалась роль НМГ в течение 10–21 дня после выписки по сравнению с отсутствием НМГ для женщин с промежуточными факторами риска ВТЭ (40).
В то время как приверженность НМГ в стационаре составляла 100 %, 33 % ввели <80 % от запланированного среднего значения НМГ в течение 7 дней после выписки, а 18 % не вводили ничего. Женщины с большей вероятностью соблюдали режим, если они использовали НМГ в прошлом или в дородовой период, а женщины, которые чувствовали, что получили хорошие технические разъяснения по поводу инъекций, с большей вероятностью соблюдали режим. Двумя основными причинами несоблюдения режима лечения были убеждение в том, что НМГ не нужен, и проблемы с инъекциями в домашних условиях. Эти причины были аналогичны причинам, описанным для неучастия в пилотном рандомизированном исследовании PROSPER, посвященном осуществимости, в котором оценивалась роль НМГ в течение 10–21 дня после выписки по сравнению с отсутствием НМГ для женщин с промежуточными факторами риска ВТЭ (40).
Три проспективных исследования в Великобритании предлагают более оптимистичные оценки приверженности (46). Среди 51 женщины, заполнившей проспективный дневник послеродовых инъекций НМГ в течение от 7 дней до 6 недель, 82% не пропускали более одной дозы. Среди 95 женщин, которым были показаны как антенатальные, так и постнатальные НМГ, в основном в профилактической дозе, 98% в дородовом периоде и 93% в послеродовом периоде имели приверженность ≥80% (49). Точно так же другая проспективная когорта из Великобритании указывает на 83% долю полного соблюдения послеродового режима НМГ (50). Отбор высоко мотивированных женщин, желающих участвовать в клинических исследованиях в двух первых исследованиях, и общий проспективный дизайн, вероятно, повысили уровень приверженности. Сомнительно, является ли такая высокая приверженность репрезентативной для населения в целом. Вместе эти исследования подчеркивают важность обсуждения преимуществ НМГ и техники инъекций НМГ перед выпиской для тех, кому это полезно.
Среди 95 женщин, которым были показаны как антенатальные, так и постнатальные НМГ, в основном в профилактической дозе, 98% в дородовом периоде и 93% в послеродовом периоде имели приверженность ≥80% (49). Точно так же другая проспективная когорта из Великобритании указывает на 83% долю полного соблюдения послеродового режима НМГ (50). Отбор высоко мотивированных женщин, желающих участвовать в клинических исследованиях в двух первых исследованиях, и общий проспективный дизайн, вероятно, повысили уровень приверженности. Сомнительно, является ли такая высокая приверженность репрезентативной для населения в целом. Вместе эти исследования подчеркивают важность обсуждения преимуществ НМГ и техники инъекций НМГ перед выпиской для тех, кому это полезно.
Разрешение случая
Пациентка осознала свои риски, возможные преимущества НМГ и общую неопределенность в отношении принятия решения о тромбопрофилактике. Хотя она соответствовала бы критериям включения в пилотное исследование PARTUM (описано ниже), это исследование не проводилось в ее центре. После совместного принятия решения она решает использовать низкие дозы НМГ в течение 10 дней, чтобы еще больше снизить риск ВТЭ. Она проходит обучение по подкожным инъекциям.
После совместного принятия решения она решает использовать низкие дозы НМГ в течение 10 дней, чтобы еще больше снизить риск ВТЭ. Она проходит обучение по подкожным инъекциям.
Обсуждение
В этом обзоре мы попытались выделить несколько областей, остро нуждающихся в высококачественных данных.
Что касается стратификации риска, то появление метода оценки индивидуальных рисков (риска материнского тромба) может оказать большую помощь клиницистам в будущем, но, по нашему мнению, нуждается в дальнейшей проверке, в идеале на популяции женщин с промежуточные факторы риска ВТЭ, не получавшие послеродовую тромбопрофилактику. Метаанализ данных отдельных пациентов обсервационных исследований может помочь увеличить мощность для выявления клинически значимых взаимодействий общих факторов риска. Идентификация типа комбинации (аддитивной, мультипликативной, сверхаддитивной) требует больших размеров выборки, которая может исходить из метаанализа анализа отдельных пациентов. Наконец, необходимы дальнейшие исследования, чтобы лучше понять опыт пациента и связанные с ним предпочтения и ценности, чтобы лучше направлять исследования и клинические рекомендации в области послеродовой тромбопрофилактики.
Явный парадокс, что только в Великобритании около 300 000 женщин получают послеродовую тромбопрофилактику каждый год, но это пилотное рандомизированное исследование подкожного введения НМГ показало невозможность проведения крупномасштабного исследования с участием 10 000–20 000 женщин. Пандемия COVID-19 высветила проблемы набора, но также и возможность международного сотрудничества, которое может дать ответы на клинически важные вопросы с помощью крупных рандомизированных испытаний, и мы не должны прекращать наши усилия по послеродовой ВТЭ. Прекрасным примером такого глобального усилий (https://partumtrial.ca; Clinicaltrials.gov ID: NCT04153760). Рандомизированные испытания низких доз НМГ по сравнению с отсутствием лечения по-прежнему крайне необходимы для получения высококачественных данных, подтверждающих современные модели практики тромбопрофилактики у родильниц с промежуточным риском ВТЭ. Такие рандомизированные исследования позволят сделать выводы не только об эффективности этих различных препаратов, но и об их безопасности и фактических рисках ВТЭ в контрольных группах.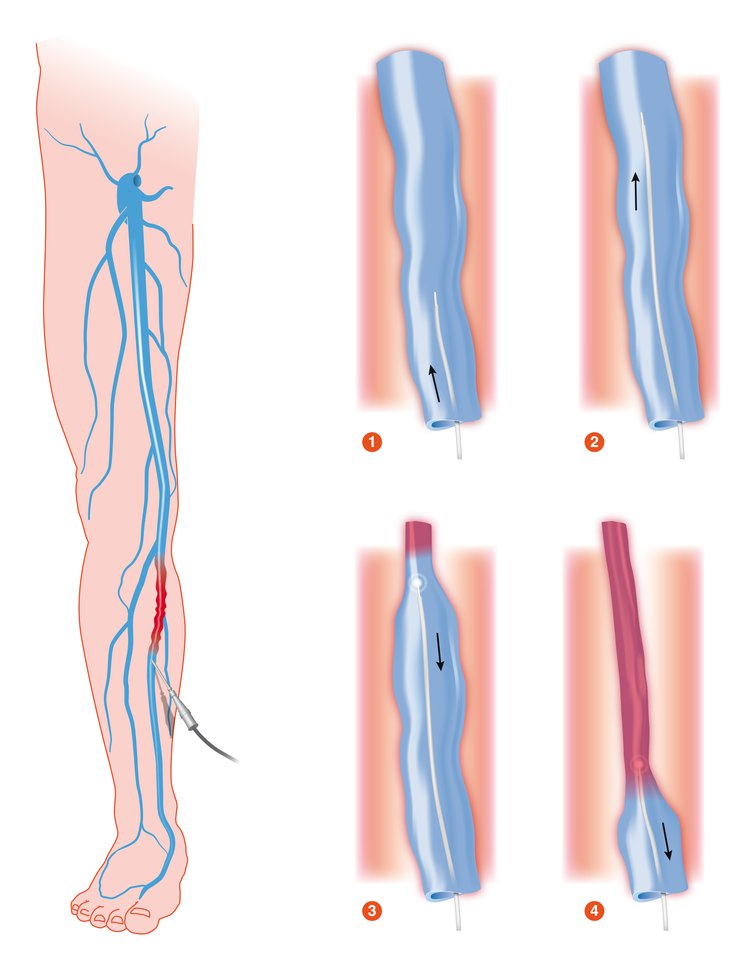
Вклад авторов
MB и LS подготовили обзор, критически отредактировали его и одобрили публикацию его содержания.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Примечание издателя
Все претензии, изложенные в этой статье, принадлежат исключительно авторам и не обязательно представляют претензии их дочерних организаций или издателя, редакторов и рецензентов. Любой продукт, который может быть оценен в этой статье, или претензии, которые могут быть сделаны его производителем, не гарантируются и не поддерживаются издателем.
Ссылки
1. Секси П.Б., Йоргенсен М., Клайнбард А., Андерсен М.Р., Колов Н.П., Стендер С. Контрольные интервалы гемостаза при беременности. Тромб Гемост. (2010) 103:718–27. doi: 10.1160/TH09-10-0704
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. S MN, A GI, Bowman AW. Ультразвуковое исследование гестационных и постуральных изменений глубокой венозной системы голени при беременности. Br J Obstet Gynaecol . (1997) 104:191–7. дои: 10.1111/j.1471-0528.1997.tb11043.x
S MN, A GI, Bowman AW. Ультразвуковое исследование гестационных и постуральных изменений глубокой венозной системы голени при беременности. Br J Obstet Gynaecol . (1997) 104:191–7. дои: 10.1111/j.1471-0528.1997.tb11043.x
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
3. Creanga AA, Syverson C, Seed K, Callaghan WM. Смертность, связанная с беременностью, в США, 2011–2013 гг. Акушер-гинеколог. (2017) 130:366–73. doi: 10.1097/AOG.0000000000002114
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
4. Wik HS, Enden TR, Jacobsen AF, Sandset PM. Долгосрочное качество жизни после тромбоза глубоких вен, связанного с беременностью, и влияние социально-экономических факторов и сопутствующих заболеваний. J Тромб Гемост. (2011) 9:1931–6. doi: 10.1111/j.1538-7836.2011.04468.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
5. Wik HS, Jacobsen AF, Sandvik L, Sandset PM. Распространенность и предикторы посттромботического синдрома в период от 3 до 16 лет после венозного тромбоза, связанного с беременностью: популяционное перекрестное исследование случай-контроль. J Тромб Гемост. (2012) 10:840–7. doi: 10.1111/j.1538-7836.2012.04690.x
Распространенность и предикторы посттромботического синдрома в период от 3 до 16 лет после венозного тромбоза, связанного с беременностью: популяционное перекрестное исследование случай-контроль. J Тромб Гемост. (2012) 10:840–7. doi: 10.1111/j.1538-7836.2012.04690.x
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
6. Jacobsen A, Skjeldestad F, Sandset P. Частота и модели риска венозной тромбоэмболии во время беременности и послеродового периода — исследование случай-контроль на основе регистров. Am J Obstet Gynecol . (2008) 198:233.e1–7. doi: 10.1016/j.ajog.2007.08.041
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
7. Pomp ER, Lenselink AM, Rosendaal FR, Doggen CJM. Беременность, послеродовой период и протромботические дефекты: риск венозного тромбоза в исследовании MEGA. J Тромб Гемост. (2008) 6:632–7. doi: 10.1111/j.1538-7836.2008.02921.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
8. Султан А.А., Уэст Дж., Тата Л.Дж., Флеминг К.М., Нельсон-Пирси С., Грейндж М.Дж. Риск первой венозной тромбоэмболии во время беременности и во время беременности: популяционное когортное исследование. Бр Ж Гематол. (2012) 156:366–73. doi: 10.1111/j.1365-2141.2011.08956.x
Султан А.А., Уэст Дж., Тата Л.Дж., Флеминг К.М., Нельсон-Пирси С., Грейндж М.Дж. Риск первой венозной тромбоэмболии во время беременности и во время беременности: популяционное когортное исследование. Бр Ж Гематол. (2012) 156:366–73. doi: 10.1111/j.1365-2141.2011.08956.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
9. Virkus RA, Løkkegaard E, Lidegaard Ø, Langhoff-Roos J, Nielsen AK, Rothman KJ, et al. Факторы риска венозной тромбоэмболии у 13 миллионов беременностей: общенациональная проспективная когорта. ПЛОС ОДИН. (2014) 9:e96495. doi: 10.1371/journal.pone.0096495
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
10. Камел Х., Нави Б.Б., Шрирам Н., Ховсепян Д.А., Деверо Р.Б., Элкинд М.С.В. Риск тромботического события после 6-недельного послеродового периода. N Английский J Med . (2014) 370:1307–15. doi: 10.1056/NEJMoa1311485
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
11. Liu S, Rouleau J, Joseph KS, Sauve R, Liston RM, Young D, et al. Эпидемиология венозной тромбоэмболии, связанной с беременностью: популяционное исследование в Канаде. J Акушерство Gynaecol Can. (2009) 31:611–20. doi: 10.1016/S1701-2163(16)34240-2
Liu S, Rouleau J, Joseph KS, Sauve R, Liston RM, Young D, et al. Эпидемиология венозной тромбоэмболии, связанной с беременностью: популяционное исследование в Канаде. J Акушерство Gynaecol Can. (2009) 31:611–20. doi: 10.1016/S1701-2163(16)34240-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
12. Tepper NK, Boulet SL, Whiteman MK, Monsour M, Marchbanks PA, Hooper WC, et al. Послеродовая венозная тромбоэмболия: частота и факторы риска. Акушер-гинеколог. (2014) 123:987–96. doi: 10.1097/AOG.0000000000000230
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
13. Блондон М., Спирк Д., Кучер Н., Ауески Д., Хайоз Д., Бир Дж. Х. и др. Сравнительная эффективность моделей оценки клинического риска внутрибольничной венозной тромбоэмболии у пациентов. Тромб Гемост. (2018) 118:82–9. doi: 10.1160/Th27-06-0403
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
14. Андерсон Д. Р., Данбар М., Мурнаган Дж., Кан С.Р., Гросс П., Форсайт М. и другие. Аспирин или ривароксабан для профилактики ВТЭ после эндопротезирования тазобедренного или коленного сустава. N Engl J Med. (2018) 378: 699–707. doi: 10.1056/NEJMoa1712746
Р., Данбар М., Мурнаган Дж., Кан С.Р., Гросс П., Форсайт М. и другие. Аспирин или ривароксабан для профилактики ВТЭ после эндопротезирования тазобедренного или коленного сустава. N Engl J Med. (2018) 378: 699–707. doi: 10.1056/NEJMoa1712746
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
15. Pabinger I, Grafenhofer H, Kaider A, Kyrle PA, Quehenberger P, Mannhalter C, et al. Риск рецидивирующей венозной тромбоэмболии, связанной с беременностью, у женщин с венозным тромбозом в анамнезе. J Тромб Гемост. (2005) 3:949–54. doi: 10.1111/j.1538-7836.2005.01307.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
16. Стефано В.Д., Мартинелли И., Росси Э., Баттальоли Т., За Т., Маннуччи П.М. и др. Риск рецидива венозной тромбоэмболии при беременности и в послеродовом периоде без антитромботической профилактики. Бр Ж Гематол. (2006) 135:386–91. doi: 10.1111/j.1365-2141.2006.06317.x
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
17.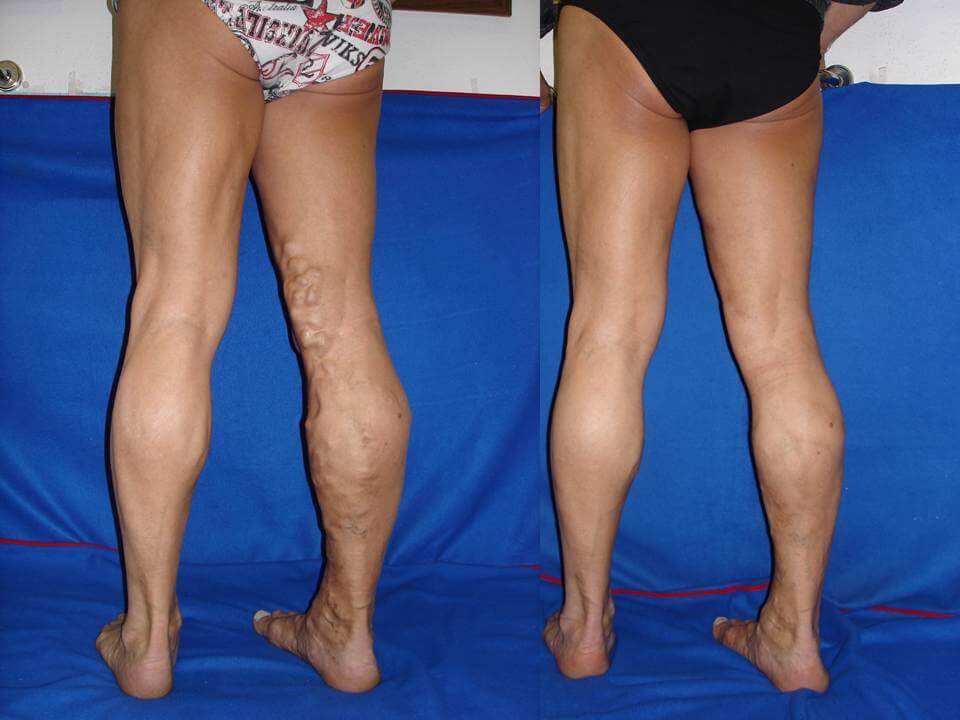 Блондон М., Казини А., Хоппе К.К., Болен Ф., Ригини М., Смит Н.Л. Риски венозной тромбоэмболии после кесарева сечения: метаанализ. Сундук. (2016) 150:572–96. doi: 10.1016/j.chest.2016.05.021
Блондон М., Казини А., Хоппе К.К., Болен Ф., Ригини М., Смит Н.Л. Риски венозной тромбоэмболии после кесарева сечения: метаанализ. Сундук. (2016) 150:572–96. doi: 10.1016/j.chest.2016.05.021
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
18. Якобсен А.Ф., Скьельдестад Ф.Е., Сандсет П.М. Дородовые и постнатальные факторы риска венозного тромбоза: исследование случай-контроль в больнице. J Тромб Гемост. (2008) 6:905–12. doi: 10.1111/j.1538-7836.2008.02961.x
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
19. Блондон М., Харрингтон Л.Б., Боелен Ф., Роберт-Эбади Х., Ригини М., Смит Н.Л. ИМТ до беременности, ИМТ при родах, увеличение массы тела во время беременности и риск послеродового венозного тромбоза. Рез. тромба. (2016) 145:151–6. doi: 10.1016/j.thromres.2016.06.026
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
20. Блондон М., Куон Б.С., Харрингтон Л. Б., Бунамо Х., Смит Н.Л. Связь между весом новорожденного при рождении и риском послеродовой венозной тромбоэмболии у матери: популяционное исследование случай-контроль. Тираж . (2015) 131:1471–6; обсуждение 1476. doi: 10.1161/CIRCULATIONAHA.114.012749
Б., Бунамо Х., Смит Н.Л. Связь между весом новорожденного при рождении и риском послеродовой венозной тромбоэмболии у матери: популяционное исследование случай-контроль. Тираж . (2015) 131:1471–6; обсуждение 1476. doi: 10.1161/CIRCULATIONAHA.114.012749
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
21. Султан А.А., Тата Л.Дж., Уэст Дж., Фиаски Л., Флеминг К.М., Нельсон-Пирси С. и соавт. Факторы риска первой венозной тромбоэмболии во время беременности: популяционное когортное исследование в Соединенном Королевстве. Кровь. (2013) 121:3953–61. doi: 10.1182/blood-2012-11-469551
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
22. Султан А.А., Грейндж М.Дж., Уэст Дж., Флеминг К.М., Нельсон-Пирси С., Тата Л.Дж. Влияние факторов риска на сроки первой послеродовой венозной тромбоэмболии: популяционное когортное исследование в Англии. Кровь. (2014) 124:2872–80. doi: 10.1182/blood-2014-05-572834
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
23.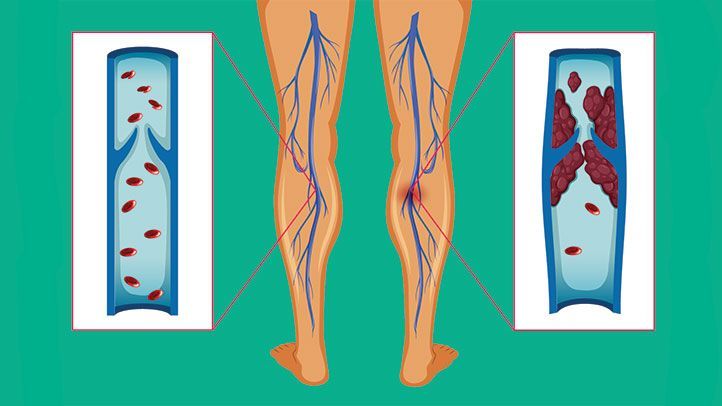 Кролес Ф.Н., Нассеринеджад К., Дувекот Дж.Дж., Круип М.Дж., Мейер К., Либик Ф.В. Беременность, тромбофилия и риск первого венозного тромбоза: систематический обзор и байесовский метаанализ. БМЖ. (2017) 359:j4452. doi: 10.1136/bmj.j4452
Кролес Ф.Н., Нассеринеджад К., Дувекот Дж.Дж., Круип М.Дж., Мейер К., Либик Ф.В. Беременность, тромбофилия и риск первого венозного тромбоза: систематический обзор и байесовский метаанализ. БМЖ. (2017) 359:j4452. doi: 10.1136/bmj.j4452
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
24. Бейтс С.М., Раджасекар А., Мидделдорп С., Маклинток С., Роджер М.А., Джеймс А.Х. и другие. Рекомендации Американского общества гематологов 2018 года по лечению венозной тромбоэмболии: венозная тромбоэмболия в контексте беременности. Кровь Adv. (2018) 2:3317–59. doi: 10.1182/bloodadvances.2018024802
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
25. О’Шонесси Ф., Доннелли Дж. К., Беннетт К., Дамкиер П., Айнле Ф. Н., Клири Б. Дж. Распространенность факторов риска послеродовой венозной тромбоэмболии в городской акушерской популяции Ирландии. J Тромб Гемост. (2019) 17:1875–85. doi: 10.1111/jth.14568
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
26. Практический бюллетень ACOG № 196: Тромбоэмболия при беременности . (2018) Доступно в Интернете по адресу: http://Insights.ovid.com/crossref?an=00006250-201807000-00054 (по состоянию на 20 сентября 2021 г.).
Практический бюллетень ACOG № 196: Тромбоэмболия при беременности . (2018) Доступно в Интернете по адресу: http://Insights.ovid.com/crossref?an=00006250-201807000-00054 (по состоянию на 20 сентября 2021 г.).
Google Scholar
27. Королевский колледж акушеров Снижение риска венозной тромбоэмболии во время беременности и послеродового периода. Руководство Green-Top №37a . (2015). Доступно в Интернете по адресу: https://www.rcog.org.uk/globalassets/documents/guidelines/gtg-37a.pdf (по состоянию на 20 сентября 2021 г.).
Google Scholar
28. Гассманн Н., Вивиано М., Ригини М., Фонтана П., Техада Б.М. де, Блондон М. Оценка порогов риска, используемых в рекомендациях по послеродовой тромбопрофилактике. J Тромб Гемост. (2021) 19: 452–9. doi: 10.1111/jth.15166
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
29. Federspiel JJ, Wein LE, Addae-Konadu KL, Darwin KC, Talamo LE, Myers ER, et al. Частота венозной тромбоэмболии среди пациенток, которым рекомендована фармакологическая профилактика тромбоэмболии после кесарева сечения в отдельных руководствах. J Тромб Гемост. (2021) 19:830–8. doi: 10.1111/jth.15218
J Тромб Гемост. (2021) 19:830–8. doi: 10.1111/jth.15218
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
30. Султан А.А., Вест Дж., Грейндж М.Дж., Райли Р.Д., Тата Л.Дж., Стефанссон О. и соавт. Разработка и валидация модели прогнозирования риска венозной тромбоэмболии у женщин в послеродовом периоде: многонациональное когортное исследование. БМЖ. (2016) 355:i6253. doi: 10.1136/bmj.i6253
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
31. Ban L, Sultan AA, West J, Tata LJ, Riley RD, Nelson-Piercy C, et al. Внешняя проверка модели для прогнозирования женщин, наиболее подверженных риску послеродовой венозной тромбоэмболии: риск образования тромбов у беременных. Тромб Res . (2021) 208: 202–10. doi: 10.1016/j.thromres.2021.05.020
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
32. Блондон М., Бейер-Вестендорф Дж. Каждые 6 секунд в Европе. Тромб Рес . (2021) 208: 211–2. doi: 10.1016/j.thromres.2021.07.012
(2021) 208: 211–2. doi: 10.1016/j.thromres.2021.07.012
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
33. Алихан Р., Беденис Р., Коэн А.Т. Гепарин для профилактики венозной тромбоэмболии у пациентов с острыми заболеваниями (за исключением инсульта и инфаркта миокарда). Cochrane Database Syst Rev . (2014) 2014:CD003747. doi: 10.1002/14651858.CD003747.pub4
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
34. Миддлтон П., Шеперд Э., Гомерсолл Дж. К. Профилактика венозных тромбоэмболий у женщин группы риска во время беременности и в раннем послеродовом периоде. Cochrane Db Syst Rev. (2021) 2021:CD001689. doi: 10.1002/14651858.CD001689.pub4
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
35. Сегал С., Садовский Э., Вайнштейн Д., Полищук В.З. Профилактика послеродового венозного тромбоза низкими дозами гепарина. Eur J Obstet Gynecol Reprod Biol . (1975) 5:273. 6.
6.
Реферат PubMed | Google Scholar
36. Hill NCW, Hill JG, Sargent JM, Taylor CG, Bush PV. Влияние низких доз гепарина на кровопотерю при кесаревом сечении. Br Medical J Clin Res Ed. (1988) 296:1505. doi: 10.1136/bmj.296.6635.1505-a
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
37. Берроуз Р.Ф., Ган Э.Т., Галлус А.С., Уоллес Э.М., Берроуз Э.А. Рандомизированное двойное слепое плацебо-контролируемое исследование низкомолекулярного гепарина в качестве профилактического средства для предотвращения венозных тромботических событий после кесарева сечения: пилотное исследование. БЖОГ. (2001) 108:835–9. doi: 10.1111/j.1471-0528.2001.00198.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
38. Гейтс С. Броклхерст П. Айерс С. Боулер У.; Тромбопрофилактика в консультативной группе по беременности. Тромбопрофилактика и беременность: два рандомизированных контролируемых пилотных исследования, в которых использовался низкомолекулярный гепарин. Am J Акушер-гинеколог. (2004) 191:1296–303. doi: 10.1016/j.ajog.2004.03.039
Am J Акушер-гинеколог. (2004) 191:1296–303. doi: 10.1016/j.ajog.2004.03.039
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
39. Роджер М.А., Филлипс П., Кан С.Р., Джеймс А.Х., Конкл Б.А.; ПРОСПЕР Следователи. Низкомолекулярный гепарин для профилактики послеродовой венозной тромбоэмболии. Тромб Гемост. (2015) 113:212–6. doi: 10.1160/Th24-06-0485
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
40. Роджер М.А., Филлипс П., Кан С.Р., Бейтс С., Макдональд С., Курана Р. и другие. Низкомолекулярный гепарин для предотвращения послеродовой венозной тромбоэмболии: пилотное исследование для оценки возможности проведения рандомизированного открытого исследования. Рез. тромба. (2016) 142:17–20. doi: 10.1016/j.thromres.2016.04.004
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
41. Алалаф С.К., Джавад Р.К., Мухаммад П.Р., Али М.С., Тавил НГА. Бемипарин против эноксапарина в качестве тромбопрофилактики после вагинальных и абдоминальных родов: проспективное клиническое исследование. BMC Беременность Роды. (2015) 15:72. doi: 10.1186/s12884-015-0515-2
BMC Беременность Роды. (2015) 15:72. doi: 10.1186/s12884-015-0515-2
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
42. Robison E, Heyborne K, Allshouse AA, Valdez C, Metz TD. Внедрение риск-ориентированного гепаринового протокола для профилактики послеродовой венозной тромбоэмболии. Акушер-гинеколог. (2017) 130:262–9. doi: 10.1097/AOG.0000000000002050
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
43. Мишель Ю.Л., Кристина Т.Б., Элизабет Б.А., Кейси Р.О., Маргарет Р.П., Эллисон Д.Л. и др. Оценка протокола акушерской тромбопрофилактики на основе гепарина со стратифицированным риском. Акушерство Гинекол . (2021) 138: 530–8. doi: 10.1097/AOG.0000000000004521
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
44. Блондон М., Бунамо Х. Вторичная профилактика венозной тромбоэмболии: один режим может не подойти всем. Тираж. (2015) 132:1856–9. doi: 10. 1161/CIRCULATIONAHA.115.019310
1161/CIRCULATIONAHA.115.019310
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
45. Хо К.М., Тан Дж.А. Стратифицированный метаанализ прерывистой пневматической компрессии нижних конечностей для предотвращения венозной тромбоэмболии у госпитализированных пациентов. Тираж. (2013) 128:1003–20. doi: 10.1161/CIRCULATIONAHA.113.002690
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
46. Гуймичева Б., Патель Дж. П., Робертс Л. Н., Субраманиан Д., Арья Р. Взгляды женщин, приверженность и опыт постнатальной тромбопрофилактики. Рез. тромба. (2019) 173:85–90. doi: 10.1016/j.thromres.2018.11.020
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
47. Chan WS, Rey E, Kent NE, Kent NE, Rey E, Corbett T, et al. Венозная тромбоэмболия и антитромботическая терапия при беременности. J Obstet Gynaecol Can. (2014) 36:527–53. doi: 10.1016/S1701-2163(15)30569-7
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
48. Роттенстрейх А., Карлин А., Калиш Ю., Левин Г., Роттенстрейх М. Факторы, связанные с приверженностью женщин к послеродовой тромбопрофилактике. J Тромб Тромболизис. (2020) 49: 304–11. doi: 10.1007/s11239-019-01952-4
Роттенстрейх А., Карлин А., Калиш Ю., Левин Г., Роттенстрейх М. Факторы, связанные с приверженностью женщин к послеродовой тромбопрофилактике. J Тромб Тромболизис. (2020) 49: 304–11. doi: 10.1007/s11239-019-01952-4
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
49. Patel JP, Auyeung V, Patel RK, Marsh MS, Green B, Arya R, et al. Мнение женщин и приверженность к терапии низкомолекулярными гепаринами во время беременности и в послеродовом периоде. J Тромб Гемост. (2012) 10:2526–34. doi: 10.1111/jth.12020
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
50. Хордерн К.Э., Бирчер К.В., Проссер-Снеллинг Э.К., Фрейзер Ф.К., Смит Р.П. Соблюдение пациентом постнатальной тромбопрофилактики: обсервационное исследование. J Акушерство гинеколог. (2015) 35:793–6. doi: 10.3109/01443615.2015.1009878
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Тромбоз глубоких вен при беременности
Тромбоз глубоких вен (ТГВ) — это серьезное заболевание, при котором в глубокой вене тела, обычно в ноге, образуется тромб.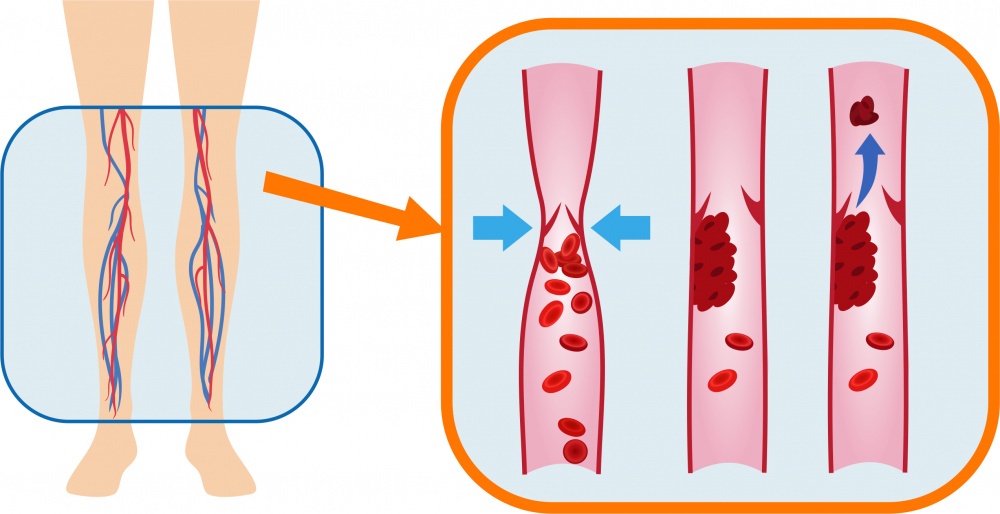
Срочный совет: Немедленно позвоните своему врачу общей практики, акушерке или 111, если у вас:
- боль, отек и болезненность в 1 ноге, обычно в задней части голени (голени) – боль может усиливаться при ходьбе
- сильная боль или повышение температуры кожи в пораженной области
- покраснение кожи, особенно на задней части ноги ниже колена
Это может быть признаком тромбоза глубоких вен. Обычно это происходит только в 1 ноге, но не всегда.
Если тромб оторвется в кровоток, он может закупорить 1 кровеносный сосуд в легких. Это называется легочной эмболией (ТЭЛА) и требует неотложного лечения.
Требуются немедленные действия: Немедленно позвоните по номеру 999, если вы:
- внезапное затруднение дыхания
- боль или скованность в груди или верхней части спины
- кашель с кровью
Это может быть признаком тромба в легких (тромбоэмболия легочной артерии).
ТЭЛА может быть фатальной, но риск развития ТЭЛА очень мал, если ТГВ диагностирован и лечится.
Подробнее о ТГВ
ТГВ не характерен для беременных. Но у вас больше шансов развить ТГВ на любой стадии беременности и в течение 6 недель после родов, чем у небеременных людей того же возраста.
ТГВ не всегда имеет симптомы.
Во время беременности часто возникают отеки или дискомфорт в ногах, так что это само по себе не всегда означает наличие серьезной проблемы.
Вы в опасности?
Ваш риск развития ТГВ во время беременности еще выше, если у вас:
- или у близкого члена семьи был тромб до
- вам больше 35 лет
- страдаете ожирением (имеете индекс массы тела 30 или более)
- перенесли тяжелую инфекцию или недавнюю серьезную травму, например, перелом ноги
- имеют состояние, при котором повышается вероятность образования тромбов (тромбофилия)
- вынашивают близнецов или многодетных детей
- прошли курс лечения бесплодия
- перенесли кесарево сечение
- курите – получите поддержку, чтобы бросить курить
- имеют тяжелое варикозное расширение вен (болезненные или выше колена с покраснением или отеком)
- обезвожены
Лечение ТГВ во время беременности
Если у вас разовьется ТГВ во время беременности, вам, вероятно, потребуются инъекции лекарства, чтобы предотвратить увеличение кровяного сгустка, чтобы ваше тело могло его растворить.
Лекарство под названием гепарин не влияет на вашего развивающегося ребенка.
Подробнее о лечении ТГВ
Инъекции также снижают риск возникновения ТЭЛА и образования нового тромба.
Инъекции обычно требуются до конца беременности и по крайней мере до 6 недель после рождения ребенка.
Хотя лечение ТГВ необходимо, есть вещи, которые вы можете сделать, чтобы помочь себе.
К ним относятся:
- как можно больше вести активный образ жизни – об этом вам может посоветовать акушерка или врач
- ношение предписанных компрессионных чулок для улучшения кровообращения в ногах
Путешествия и ТГВ
Путешествие продолжительностью более 4 часов (дальние поездки) увеличивает риск развития ТГВ.
