Перитонит у детей: Перитонит у детей. Что такое Перитонит у детей?
Перитонит у детей. Что такое Перитонит у детей?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Перитонит у детей — это воспаление брюшины, которое сопровождается интоксикацией и полиорганными нарушениями. Развивается под действием патогенных бактерий при прободении полых пищеварительных органов, гематогенном распространении инфекции, осложнении аппендицита, других острых хирургических болезней. Симптомы перитонита включают мучительные боли и напряжение мышц живота, многократную рвоту, ухудшение общего состояния (спутанность сознания, обезвоживание, гипертермию). Для диагностики проводят УЗИ и рентгенографию брюшных органов, лапароскопию, лабораторные исследования. Назначается оперативное лечение, которое дополняют антибиотиками, инфузионной терапией.
МКБ-10
К65.0 Острый перитонит
- Причины
- Патогенез
- Классификация
- Симптомы перитонита у ребенка
- Осложнения
- Диагностика
- Лечение
- Консервативная терапия
- Хирургическое лечение
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Частота встречаемости перитонита составляет 3-4% среди всех острых хирургических заболеваний у детей. Симптомы чаще развиваются у пациентов младшего возраста, что связано с анатомо-функциональными особенностями брюшины и желудочно-кишечного тракта. Перитонит представляет серьезную угрозу для жизни и здоровья ребенка. Несмотря на усовершенствование техники лечения, летальность остается высокой и составляет от 4,5% при ранней диагностике до 50% при запущенных и осложненных случаях.
Перитонит у детей
Причины
Этиологическая структура перитонитов у детей значительно отличается от таковой у взрослых и напрямую связана с возрастом пациентов. Непосредственная причина патологии — попадание в стерильную полость брюшины патогенных грамотрицательных или грамположительных микроорганизмов, которые вызывают воспалительный процесс. Основными этиологическими факторам заболевания у детей служат:
Непосредственная причина патологии — попадание в стерильную полость брюшины патогенных грамотрицательных или грамположительных микроорганизмов, которые вызывают воспалительный процесс. Основными этиологическими факторам заболевания у детей служат:
- Перфорация стенки кишечника. Составляет до 80% случаев перитонита у новорожденных и детей грудного возраста. Симптомы возникают в результате прободения стенки при некротическом энтероколите (более характерном для недоношенных) или врожденных аномалиях.
- Гематогенное или лимфогенное инфицирование. Бактерии переносятся по сосудистому руслу из отдаленных очагов или циркулируют при генерализованном процессе, вызывая заражение брюшины. Фактор особо значим для маленьких детей, у которых недостаточно развит клеточный и гуморальный иммунитет, более высокая склонность к сепсису.
- Аппендицит. До 5-6 лет у детей не полностью сформирован сальник, которые должен прикрывать воспаленный червеобразный отросток и препятствовать генерализации процесса.
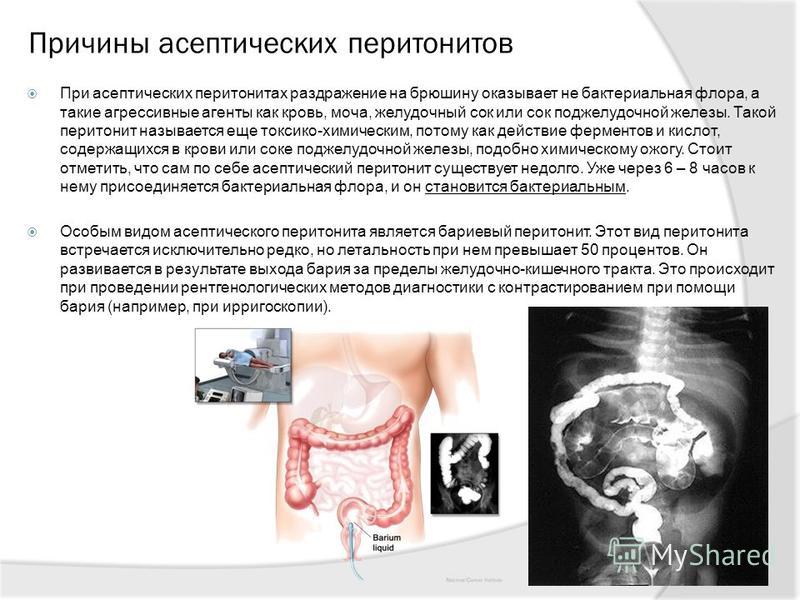 Этот фактор и трудности диагностики аппендицита у больных раннего возраста провоцируют осложненные формы болезни с развитием перитонита.
Этот фактор и трудности диагностики аппендицита у больных раннего возраста провоцируют осложненные формы болезни с развитием перитонита. - Заболевания ЖКТ. У подростков симптомы перитонеального воспаления зачастую вызваны типичными «взрослыми» причинами: прободением язвы желудка или двенадцатиперстной кишки, обострением холецистита или панкреатита. У маленьких детей эти факторы встречаются крайне редко.
Патогенез
Симптомы развиваются как при первичном проникновении микроорганизмов, так и вследствие инфицирования реактивного выпота. У детей отмечается незрелость резорбтивной функции брюшины, способствующая быстрому распространению воспалительного процесса по всем отделам перитонеальной полости и развитию разлитых форм. Недостаточная функциональная активность иммунитета приводит к активному размножению бактерий.
В патогенезе важную роль играют нарушения гомеостаза, которые проявляются изменением концентраций электролитов, эксикозом, гипертермическим синдромом. Водно-солевой дисбаланс происходит на фоне патологических потерь жидкости с рвотой и диареей, пареза кишечника и накоплении транссудата в его полости. Начинается массивная эндогенная интоксикация организма, выявляются симптомы негативного влияния на центр терморегуляции.
Водно-солевой дисбаланс происходит на фоне патологических потерь жидкости с рвотой и диареей, пареза кишечника и накоплении транссудата в его полости. Начинается массивная эндогенная интоксикация организма, выявляются симптомы негативного влияния на центр терморегуляции.
Классификация
По этиологическому фактору различают бактериальные и абактериальные перитониты. Последние вызваны раздражением брюшины желчью, мочой или кровью, но они быстро переходят в микробную форму вследствие присоединения условно-патогенной флоры. По распространенности выделяют местный, диффузный и разлитой вариант. Для детских хирургов большое значение имеет характер развития заболевания, согласно которому существует 3 формы процесса:
- Первичный перитонит. Составляет около 5% в структуре заболеваемости у детей, обусловлен гематогенным переносом бактерий из отдаленных инфекционных очагов. Предрасполагающие факторы у детей — нефротический синдром, системные аутоиммунные болезни.

- Вторичный перитонит. Возникает вследствие проникновения болезнетворных организмов из поврежденных органов пищеварительного тракта. Выявляется почти в 90% случаев воспалительного поражения брюшины в детской хирургии.
- Третичный перитонит. Тяжелое состояние, при котором происходит повторное перитонеальное воспаление спустя 48 часов и более после успешного оперативного лечения предшествующего перитонита.
Симптомы перитонита у ребенка
В начальной (реактивной) стадии болезни сильнее выражены локальные симптомы. Ребенок жалуется на резкую, нестерпимую боль в животе, начинает кричать или плакать, ложится, подтянув колени к животу. Возникаю рвота желудочным содержимым с примесями желчи, задержка стула и газов. Больной становится вялым и заторможенным, кожные покровы бледные, сухие, губы трескаются. Температура тела поднимается до субфебрильных или фебрильных цифр.
С переходом перитонита в токсическую стадию симптомы усугубляются. Родители замечают страдальческое выражение лица, холодный пот и синюшность дистальных отделов конечностей. Ребенок лежит неподвижно на спине или боку, при попытке его перевернуть начинает плакать из-за усиления боли. В терминальной стадии сознание спутано, боли стихают, что является прогностически неблагоприятным признаком.
Родители замечают страдальческое выражение лица, холодный пот и синюшность дистальных отделов конечностей. Ребенок лежит неподвижно на спине или боку, при попытке его перевернуть начинает плакать из-за усиления боли. В терминальной стадии сознание спутано, боли стихают, что является прогностически неблагоприятным признаком.
У новорожденных клиническая картина перитонита отличается. На первый план выходят общие симптомы, которые включают патологическую сонливость, отказ от еды, бледность или цианоз кожи. У ребенка быстро нарастает интоксикация, появляются нарушения сердечной деятельности и расстройства дыхания. Живот сильно вздут, на попытки прикоснутся к нему новорожденный реагирует криком.
Осложнения
Частые последствия запущенного перитонита у детей — абдоминальный сепсис и полиорганная недостаточность. Их развитие вызвано несколькими факторами: интоксикацией организма бактериями и продуктами их жизнедеятельности, нарушениями гомеостаза, повреждением тканей головного мозга и расстройствами периферической нервной регуляции. Без лечения эти осложнения заканчиваются смертью ребенка.
Без лечения эти осложнения заканчиваются смертью ребенка.
Вторую группу составляют послеоперационные осложнения перитонита, возникающие в раннем или позднем периоде и встречающиеся с частотой 10-23%. Среди них выделяют спаечную кишечную непроходимость (5%), нагноение шва на передней брюшной стенке (4,8%), межкишечные и тазовые абсцессы (2,5%). К редким последствиям операции у детей относят кишечные свищи (1%) и острые воспалительные поражения органов ЖКТ (0,6%).
Диагностика
При осмотре детский хирург выявляет напряженные мышцы («доскообразный живот»), проверяет перитонеальные симптомы, проводит перкуссию и аускультацию. Обязательно производится ректальное исследование, чтобы исключить воспаление брюшины малого таза. Для уточнения диагноза назначаются инструментальные и лабораторные методы исследования:
- УЗИ брюшной полости. Ультразвуковая диагностика показывает наличие и примерное количество жидкости в полости брюшины, патологии внутренних органов, которые могли быть причиной перитонита.
 Исследование информативно в 85% случаев, поскольку его проведению мешает вздутый живот, двигательное беспокойство ребенка, вызванное сильным болевым синдромом.
Исследование информативно в 85% случаев, поскольку его проведению мешает вздутый живот, двигательное беспокойство ребенка, вызванное сильным болевым синдромом. - Рентгенография. На обзорной рентгенограмме врачи могут обнаружить скопление воздуха, что свидетельствует о желудочной или кишечной перфорации. Косвенные рентгенологические симптомы перитонита — высокое стояние диафрагмы, наличие выпота в плевральных синусах.
- Дополнительные методы. Если состояние ребенка стабильное и симптомы не прогрессируют, целесообразно сделать КТ. Исследование показывает изменения во всех внутренних органах брюшной полости, поэтому врачу удается точно определить причину перитонита. При затруднениях в диагностическом поиске рекомендована лапароскопия.
- Анализы. Основные лабораторные симптомы болезни — высокий лейкоцитоз или лейкопения, повышение лейкоцитарного индекса интоксикации в гемограмме. Обязательно выполняется биохимический анализ крови, исследование острофазовых показателей.
 Современный метод подтверждения гнойного перитонита и абдоминального сепсиса у детей — оценка уровня прокальцитонина.
Современный метод подтверждения гнойного перитонита и абдоминального сепсиса у детей — оценка уровня прокальцитонина.
Лечение
Консервативная терапия
Учитывая тяжелые симптомы заболевания, перед хирургическим лечением необходима интенсивная подготовка. Она включает медикаменты для поддержания общего состояния и профилактики послеоперационных осложнений. В ургентном порядке проводится зондирование желудка и катетеризация мочевого пузыря, установка доступа к центральной и периферической вене. Для стабилизации объема циркулирующей крови вводятся коллоидные и кристаллоидные растворы.
Чтобы прекратить размножение патогенных микроорганизмов, ребенку назначают комбинированную антибиотикотерапию. Используются препараты из 2-3 групп для парентерального введения, которые обладают широким спектром действия. В постоперационном периоде схему терапии дополняют антихолинэстеразными лекарствами для стимуляции кишечника, ганглиоблокаторами, физиопроцедурами — диадинамотерапией, лекарственным электрофорезом, электростимуляцией.
Хирургическое лечение
Оперативное вмешательство спустя 2-4 часа подготовки — стандарт в лечении перитонита у детей. Объем операции и тактика хирургов определяются распространенностью процесса, причинами заболевания, наличием пороков или сопутствующих патологий ЖКТ. Доступом выбора является срединная лапаротомия, которая дает врачу широкий простор для выполнения манипуляций и осмотра состояния брюшной полости.
Ключевой момент хирургического вмешательства — нахождение и устранение источника перитонита. По окончании этого этапа врачи переходят к тщательной ревизии и санации брюшной полости, постановке дренажей. Обязательно обеспечивается декомпрессия кишечника путем аспирации содержимого через назогастральный зонд, чтобы снизить эндогенную интоксикацию.
Прогноз и профилактика
Вероятность полного выздоровления зависит от своевременности диагностики перитонита, объема терапии, возраста ребенка и состояния его иммунной системы. Прогноз более благоприятный при неосложненном течении болезни и проведении адекватного хирургического лечения на ранней стадии. Вызывают опасения симптомы воспаления брюшины у детей с множественными врожденными пороками ЖКТ, тяжелыми нарушениями иммунного статуса.
Прогноз более благоприятный при неосложненном течении болезни и проведении адекватного хирургического лечения на ранней стадии. Вызывают опасения симптомы воспаления брюшины у детей с множественными врожденными пороками ЖКТ, тяжелыми нарушениями иммунного статуса.
Профилактика перитонита в период новорожденности заключается в антенатальной охране плода, рациональном ведении беременности, раннем начале грудного вскармливания. Для предупреждения патологии у детей старшего возраста назначаются вторичные меры профилактики: своевременное обнаружение и лечение гастроэнтерологических заболеваний, ликвидация хронических очагов инфекции.
Вы можете поделиться своей историей болезни, что Вам помогло при лечении перитонита у детей.
Источники
- Клинические рекомендации МОЗ РФ «Острый перитонит». — 2017
- Детская хирургия: национальное руководство / под ред. Ю.Ф. Исакова, А.Ф. Дронова. — 2009
- Абсцедирующие формы аппендикулярного перитонита у детей.
 Автореферат диссертации / О.В. Карасева. — 2005
Автореферат диссертации / О.В. Карасева. — 2005 - О первичном перитоните у детей. К.К. Федоров, М.К. Беляев // Мать и Дитя. — 2004
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
404 Cтраница не найдена
- Университет
- Руководство
- Ректорат
- Обращение к ректору
- Ученый совет
- Университету 90 лет
- Телефонный справочник
- Документы
- Структура
- СМИ о вузе
- Символика БГМУ
- Электронный ящик доверия
- Комплексная программа развития БГМУ
- Антитеррор
- Сведения об образовательной организации
- Абитуриенту
- Обращение граждан
- Фотогалерея
- Карта сайта
- Видеогалерея
- Оплата банковской картой
- Реорганизация вуза
- Календарь мероприятий
- Образование
- Учебно-методическое управление
- Центр практических навыков
- Факультеты
- Кафедры
- Институт дополнительного профессионального образования
- Приемная комиссия
- Медицинский колледж
- Деканат по работе с иностранными обучающимися
- Управление международной деятельности
- Отдел ординатуры
- Расписание
- Менеджмент качества
- Федеральный аккредитационный центр
- Научно-образовательный медицинский кластер «Нижневолжский»
- Государственная итоговая аттестация
- Первичная аккредитация
- Первичная специализированная аккредитация
- Внутренняя оценка качества образования
- Информация для инвалидов и лиц с ограниченными возможностями здоровья
- Информация для студентов
- Я-профессионал
- Всероссийская студенческая олимпиада по хирургии с международным участием
- Медицинский инспектор
- Онлайн обучение
- Социальная работа в системе здравоохранения
- Новые образовательные программы
- Электронная учебная библиотека
- Периодическая аккредитация
- Независимая оценка качества образования
- Профессиональное обучение
- Наука и инновации
- Наука и университеты
- Структура и документы
- Указ Президента Российской Федерации «О стратегии научно-технологического развития Российской Федерации»
- Стратегия развития медицинской науки до 2025 года
- Научно-исследовательские подразделения
- Клинические исследования и испытания, ЛЭК
- Диссертационные советы
- Докторантура
- Аспирантура
- Грантовая политика БГМУ
- Актуальные гранты, стипендии, конкурсы
- Конференции и форумы
- Гранты, премии, конкурсы, конференции для молодых ученых
- Полезные интернет-ссылки
- Научные издания
- Проблемные научные комиссии
- Патентная деятельность
- БГМУ в рейтингах университетов
- Публикационная активность
- НИИ кардиологии
- Биобанк
- Репозиторий БГМУ
- Евразийский НОЦ
- Лечебная работа
- Клиника БГМУ
- Всероссийский центр глазной и пластической хирургии
- Уф НИИ ГБ
- Клиническая стоматологическая поликлиника
- Клинические базы
- Отчеты по лечебной работе
- Договорная работа с клиническими базами
- Отделения клиники БГМУ
- Лицензии
- Санаторий-профилакторий БГМУ
- Жизнь БГМУ
- Воспитательная и социальная работа
- Отдел по культурно-массовой работе
- Отдел по связям с общественностью
- Общественные объединения и органы самоуправления
- Отдел по воспитательной и социальной работе
- Творческая жизнь
- Спортивная жизнь
- Профсоюз обучающихся БГМУ
- Профсоюзный комитет
- Совет кураторов
- Совет обучающихся
- Ассоциация выпускников
- Работа музеев на кафедрах
- Выпускники БГМУ – ветераны ВОВ
- Золотой фонд БГМУ
- Медиа центр
- БГМУ — ВУЗ здорового образа жизни
- Юбиляры
- Жизнь иностранных студентов БГМУ
- Университету 90 лет
- Университету 85 лет
- Празднование 75-летия Победы в Великой Отечественной войне
- Научная библиотека
- Приоритет 2030
- О программе
- Проектный офис
- Стратегические проекты
- Миссия и стратегия
- Цифровая кафедра
- Конкурсы для студентов
- Отчетность
- Публикации в СМИ
- Программа развития
- Научные семинары для студентов и ученых БГМУ
- Новости
Диализ-ассоциированный перитонит у детей — ПМК
1. Александр С.Р., Варади Б.А. Демография диализа у детей. В: Варади Б.А., Шефер Ф.С., Файн Р.Н., Александр С.Р., редакторы. Детский диализ. Дордрехт: Клювер; 2004. С. 35–46. [Google Scholar]
Александр С.Р., Варади Б.А. Демография диализа у детей. В: Варади Б.А., Шефер Ф.С., Файн Р.Н., Александр С.Р., редакторы. Детский диализ. Дордрехт: Клювер; 2004. С. 35–46. [Google Scholar]
2. North American Pediatric Pediatric Renal Trials and Cooperative Studies (NAPRTCS) (2007) Годовой отчет за 2007 г. EMMES Corp, Rockville
3. Сето К.С., Чоу К.М., Вонг Т.И., Леунг К.Б., Ли П.К. Влияние климата на заболеваемость перитонитом, связанным с перитонеальным диализом. Перит Наберите внутр. 2003; 23: 580–586. [PubMed] [Академия Google]
4. Варади Б.А., Салливан Э.К., Александр С.Р. Уроки из базы данных пациентов на перитонеальном диализе: отчет Североамериканского кооперативного исследования педиатрической почечной трансплантации. почки инт. 1996; 53:S68–S71. [PubMed] [Google Scholar]
5. Tranaeus A. Перитонит у детей на непрерывном перитонеальном диализе. В: Fine RN, Александр С., Варади Б.А., редакторы. ПАПД/ХЦПД у детей. Норвелл: Клувер; 1998. С. 301–347. [Google Scholar]
6. U.S. Renal Data System (USRDS) (2007) Годовой отчет за 2007 год: атлас терминальной стадии почечной недостаточности в США. Национальный институт здоровья, Национальный институт диабета, болезней органов пищеварения и почек, Bethesda
U.S. Renal Data System (USRDS) (2007) Годовой отчет за 2007 год: атлас терминальной стадии почечной недостаточности в США. Национальный институт здоровья, Национальный институт диабета, болезней органов пищеварения и почек, Bethesda
7. Кин В.Ф., Эверетт Э.Д., Голпер Т.А., Гокал Р., Халстенсон С., Кавагути Ю., Риэлла М., Вас С., Вербру Х.А. Рекомендации по лечению перитонита, связанного с перитонеальным диализом: обновление 1993 г. Специальный консультативный комитет по лечению перитонита. Международное общество перитонеального диализа. Перит Наберите внутр. 1993; 13:14–28. [PubMed] [Google Scholar]
8. Кин В.Ф., Александр С.Р., Бэйли Г.Р., Бошотен Э., Гокал Р., Голпер Т.А., Холмс С.Дж., Хуанг К.С., Кавагути И., Пираино Б., Риэлла М., Шефер Ф., Вас С. Рекомендации по лечению перитонита, связанного с перитонеальным диализом: 1996 обновление. Перит Наберите внутр. 1996; 16: 557–573. [PubMed] [Google Scholar]
9. Keane WF, Bailie GR, Boeschoten E, Gokal R, Golper TA, Holmes CJ, Kawaguchi Y, Piraino B, Riella M, Vas S. Рекомендации по лечению перитонита, связанного с перитонеальным диализом у взрослых: обновление 2000 года. Перит Наберите внутр. 2000; 20:828–829. [PubMed] [Google Scholar]
Рекомендации по лечению перитонита, связанного с перитонеальным диализом у взрослых: обновление 2000 года. Перит Наберите внутр. 2000; 20:828–829. [PubMed] [Google Scholar]
10. Пираино Б., Бэйли Г.Р., Бернардини Дж., Бошотен Э., Гупта А., Холмс С., Куиджпер Э.Дж., Ли ПКТ, Лай В.К., Муджайс С., Патерсон Д.Л., Фонтан М.П., Рамос А., Schaefer F, Uttley L. Рекомендации по инфекциям, связанным с перитонеальным диализом: обновление 2005 г. Перит Наберите внутр. 2005; 25:107–131. [PubMed] [Академия Google]
11. Варади Б.А., Шефер Ф., Холлоуэй М., Александр С., Кандерт М., Пираино Б., Салуски И., Транеус А., Дивино Дж., Хонда М., Муджайс С., Веррина Э., для Международного общества перитонеального диализа (ISPD) Консультативный комитет по лечению перитонита у детей: согласованные рекомендации по лечению перитонита у детей, получающих перитонеальный диализ. Перит Наберите внутр. 2000;20:610–624. [PubMed] [Google Scholar]
12. Фенеберг Р., Варади Б.А., Александр С.Р., Шефер Ф. , члены Международного педиатрического перитонеального регистра Международный педиатрический перитонеальный регистр: глобальная интернет-инициатива в области педиатрического диализа. Перит Наберите внутр. 2004; 24:S130–S134. [PubMed] [Академия Google]
, члены Международного педиатрического перитонеального регистра Международный педиатрический перитонеальный регистр: глобальная интернет-инициатива в области педиатрического диализа. Перит Наберите внутр. 2004; 24:S130–S134. [PubMed] [Академия Google]
13. Шефер Ф., Фенеберг Р., Аксу Н., Донмез О., Садикоглу Б., Александр С.Р., Мир С., Ха И.С., Фишбах М., Симкова Е., Уотсон А.Р., Моллер К., Баум Х., Варади Б.А. Всемирная вариация перитонита, связанного с диализом, у детей. почки инт. 2007; 72: 1374–1379. [PubMed] [Google Scholar]
14. Warady BA, Feneberg R, Verrina E, Flynn JT, Muller-Wiefel DE, Besbas N, Zurowska A, Aksu N, Fischbach M, Sojo E, Donmez O, Sever L, Sirin A, Александр С.Р., Шефер Ф. Перитонит у детей, находящихся на длительном диализе: проспективная оценка терапевтических рекомендаций. J Am Soc Нефрол. 2007; 18: 2172–2179. [PubMed] [Google Scholar]
15. Zurowska A, Feneberg R, Warady BA, Zimmering M, Monteverde M, Testa S, Calyskan S, Drozdz D, Salusky I, Kemper MJ, Ekim M, Verrina E, Misselwitz J, Шефер Ф. Грамотрицательный перитонит у детей, находящихся на длительном перитонеальном диализе. Am J почек Dis. 2008; 51: 455–462. [PubMed] [Google Scholar]
Грамотрицательный перитонит у детей, находящихся на длительном перитонеальном диализе. Am J почек Dis. 2008; 51: 455–462. [PubMed] [Google Scholar]
16. Burkart J, Hylnader B, Durnell-Figel T, Roberts D. Сравнение частоты перитонита при длительном использовании стандартного спайка и Ultraset при непрерывном амбулаторном перитонеальном диализе (CAPD) Perit Dial Int . 1990;10:41–43. [PubMed] [Google Scholar]
17. Burkart J, Jordan JR, Durnell TA, Case LD. Сравнение инфекций в месте выхода в разъединяемых и неразъемных системах для перитонеального диализа. Перит Наберите внутр. 1992; 12: 317–320. [PubMed] [Google Scholar]
18. Валери А., Радхакришнан Дж., Верноччи Л., Кармайкл Л.Д., Стерн Л. Эпидемиология перитонита при остром перитонеальном диализе: сравнение открытых и закрытых дренажных систем. Am J почек Dis. 1993; 21: 300–309. [PubMed] [Академия Google]
19. Монтеон Ф., Корреа-Роттер Р., Паниагуа Р., Амато Д., Уртадо М.Е., Медина Дж.Л., Сальседо Р.М., Гарсия Э. , Матос М., Каджи Дж., Васкес Р., Рамос А., Скеттино М.А., Моран Дж. Профилактика перитонит с отключенными системами при ПАПД: рандомизированное контролируемое исследование. почки инт. 1998;54:2123–2128. [PubMed] [Google Scholar]
, Матос М., Каджи Дж., Васкес Р., Рамос А., Скеттино М.А., Моран Дж. Профилактика перитонит с отключенными системами при ПАПД: рандомизированное контролируемое исследование. почки инт. 1998;54:2123–2128. [PubMed] [Google Scholar]
20. Li PK, Law MC, Chow KM, Chan WK, Szeto CC, Cheng YL, Wong TY, Leung CB, Wang AY, Lui FS, Yu AW. Сравнение клинических результатов и простоты обращения с двумя системами двойного мешка при непрерывном амбулаторном перитонеальном диализе: проспективное рандомизированное контролируемое многоцентровое исследование. Am J почек Dis. 2002; 40: 373–380. [PubMed] [Академия Google]
21. Kim DK, Yoo TH, Ryu DR, Xu ZG, Kim HJ, Choi KH, Lee HY, Han DS, Kang SW. Изменения возбудителей и их антимикробной чувствительности при перитоните ПАПД: опыт одного центра за одно десятилетие. Перит Наберите внутр. 2004; 24:424–432. [PubMed] [Google Scholar]
22. Benfield MR, McDonald R, Sullivan EK, Stablein DM, Tejani A. Ежегодная трансплантация почки у детей в 1997 г. : отчет Североамериканского кооперативного исследования по трансплантации почек у детей (NAPRTCS) Pediatr Transplant. 1999;2:152–167. [PubMed] [Google Scholar]
: отчет Североамериканского кооперативного исследования по трансплантации почек у детей (NAPRTCS) Pediatr Transplant. 1999;2:152–167. [PubMed] [Google Scholar]
23. Verrina E, Bassi S, Perfumo F, Edefonti A, Zacchello G, Andreetta B, Pela I, Penza R, Piaggio G, Picca M. Анализ осложнений при хроническом перитонеальном диализе у детей популяция пациентов. Итальянский регистр педиатрической популяции пациентов. Перит Наберите внутр. 1993; 13: С257–С259. [PubMed] [Google Scholar]
24. Schaefer F, Klaus G, Muller-Wiefel DE, Mehls O. Текущая практика перитонеального диализа у детей: результаты продольного исследования. Перит Наберите внутр. 1999;2:S445–S449. [PubMed] [Google Scholar]
25. Хонда М., Иитака К., Кавагути Х., Хошии С., Акаши С., Косака Т., Тузуки К., Ямаока К., Йошивака Н., Карашима С., Ито Ю., Хатаэ К. Гражданин Японии регистрационные данные о педиатрических больных ПАПД: десятилетний опыт. Доклад исследовательской группы педиатрической конференции PD. Перит Наберите внутр. 1996; 16: 269–275. [PubMed] [Google Scholar]
1996; 16: 269–275. [PubMed] [Google Scholar]
26. Schaefer F, Kandert M, Feneberg R. Методологические вопросы оценки заболеваемости перитонитом у детей. Перит Наберите внутр. 2002; 22: 234–238. [PubMed] [Академия Google]
27. Рамалакшми С., Бернардини Дж., Пираино Б. Ночной прерывистый перитонеальный диализ для начала перитонеального диализа. Adv Perit Dial. 2003; 19: 111–114. [PubMed] [Google Scholar]
28. Vas S, Oreopoulos DG. Инфекции у пациентов, находящихся на перитонеальном диализе. Заразить Dis Clin North Am. 2001; 15: 743–774. [PubMed] [Google Scholar]
29. Зеленицкий С., Барнс Л., Финдли И., Альфа М., Ариано Р., Файн А., Хардинг Г. Анализ микробиологических тенденций перитонита, связанного с перитонеальным диализом, из 19с 91 по 1998 год. Am J Kidney Dis. 2000;36:1009–1013. [PubMed] [Google Scholar]
30. Piraino B, Bernardin J, Florio T, Fried L. Профилактика золотистого стафилококка и тенденции грамотрицательных инфекций у пациентов на перитонеальном диализе. Перит Наберите внутр. 2003; 23: 456–459. [PubMed] [Google Scholar]
Перит Наберите внутр. 2003; 23: 456–459. [PubMed] [Google Scholar]
31. Mujais S. Микробиология и исходы перитонита в Северной Америке. Почки Int Suppl. 2006; 103:S55–S62. [PubMed] [Google Scholar]
32. MacGinley R, Cooney K, Alexander G, Cohen S, Goldsmith JA. Рецидивирующий культурально-негативный перитонит у пациентов на перитонеальном диализе, подвергшихся воздействию раствора икодекстрина. Am J почек Dis. 2002;40:1030–1035. [PubMed] [Академия Google]
33. Бур В.Х., Вос П.Ф., Фиерен М.В. Отрицательный культуральный перитонит, связанный с использованием диализата, содержащего икодекстрин, у двенадцати пациентов, получавших перитонеальный диализ. Перит Наберите внутр. 2003; 23:33–38. [PubMed] [Google Scholar]
34. Toure F, Lavaud S, Mohajer M, Lavaud F, Canivet E, Nguyen P, Chanard J, Rieu P. Икодекстрин-индуцированный перитонит: изучение пяти случаев и сравнение с бактериальным перитонитом. почки инт. 2004; 65: 654–660. [PubMed] [Google Scholar]
35. Мартис Л., Патель М., Гертич Дж., Монговен Дж., Таминн М., Перрье М.А., Мендоса О., Гоуд Н., Костиган А., Данджой Н., Вергер С., Оуэн В.Ф., младший Асептический перитонит из-за загрязнения пептидогликанами стандартного диализирующего раствора фармакопеи. Ланцет. 2005; 365: 588–59.4. [PubMed] [Google Scholar]
Мартис Л., Патель М., Гертич Дж., Монговен Дж., Таминн М., Перрье М.А., Мендоса О., Гоуд Н., Костиган А., Данджой Н., Вергер С., Оуэн В.Ф., младший Асептический перитонит из-за загрязнения пептидогликанами стандартного диализирующего раствора фармакопеи. Ланцет. 2005; 365: 588–59.4. [PubMed] [Google Scholar]
36. Вичитил А., Ремон С., Мишель С., Вильямс П., Родригес-Кармона А., Маррон Б., Вонеш Э., Хейден С., Филхо Дж. К. (от имени исследования экстранеального перитонита). Группа) Икодекстрин не влияет на частоту инфекционных и культурально-негативных перитонитов у пациентов на перитонеальном диализе: 2-летнее многоцентровое сравнительное проспективное когортное исследование. Трансплантация нефролового циферблата. 2008; 23:3711–3719. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Goldie SJ, Kiernan-Troidle L, Torres C, Gorban-Brennan N, Dunne D, Kliger AS, Finkelstein FO. Грибковый перитонит в большой популяции пациентов с хроническим перитонеальным диализом: отчет о 55 эпизодах. Am J почек Dis. 1996;28:86–91. [PubMed] [Google Scholar]
Am J почек Dis. 1996;28:86–91. [PubMed] [Google Scholar]
38. Ван AYM, Yu AWY, Li PKT, Lam PKW, Leung CB, Lai KN, Lui SF. Факторы, предопределяющие исход грибкового перитонита при перитонеальном диализе: анализ 9-летнего опыта лечения грибкового перитонита в одном центре. Am J почек Dis. 2000;36:1183–1192. [PubMed] [Google Scholar]
39. Варади Б.А., Башир М., Дональдсон Л.А. Грибковый перитонит у детей, находящихся на перитонеальном диализе: отчет НАПРТКС. почки инт. 2000; 58: 384–389. [PubMed] [Академия Google]
40. Луи С.Л., Ло С.И., Чой Б.Я., Чан Т.М., Ло В.К., Ченг И.К. Оптимальное лечение и отдаленные исходы туберкулезного перитонита, осложняющего непрерывный амбулаторный перитонеальный диализ. Am J почек Dis. 1996; 28: 747–751. [PubMed] [Google Scholar]
41. Пираино Б. Перитонеальные инфекции. Adv Ren Заменить Ther. 2000; 7: 280–288. [PubMed] [Google Scholar]
42. Тройдл Л., Килгер А.С., Горбан-Бреннан Н., Фикриг М., Голден М., Финкельштейн Ф. О. Девять эпизодов ХПД-ассоциированного перитонита с ванкомицин-резистентными энтерококками. почки инт. 1996;50:1368–1372. [PubMed] [Google Scholar]
О. Девять эпизодов ХПД-ассоциированного перитонита с ванкомицин-резистентными энтерококками. почки инт. 1996;50:1368–1372. [PubMed] [Google Scholar]
43. Baum H, Schehl J, Geiss HK, Schaefer F. Распространенность энтерококков, устойчивых к ванкомицину, среди детей с терминальной стадией почечной недостаточности. Клин Инфекция Дис. 1999; 29: 912–916. [PubMed] [Google Scholar]
44. Holtta TM, Ronnholm KA, Holmberg C. Влияние возраста, времени и перитонита на кинетику перитонеального транспорта у детей. Перит Наберите внутр. 1998; 18: 590–597. [PubMed] [Google Scholar]
45. Андреоли С.П., Лейзер Дж., Варади Б.А., Шлихтинг Л., Брюэр Э.Д., Уоткинс С.Л. Неблагоприятное влияние перитонита на функцию перитонеальной мембраны у детей на диализе. Педиатр Нефрол. 1999;13:1–6. [PubMed] [Google Scholar]
46. Warady BA, Fivush B, Andreoli SP, Kohaut E, Salusky I, Schlichting L, Pu K, Watkins S. Продольная оценка транспортной кинетики у детей, получающих перитонеальный диализ. Педиатр Нефрол. 1999; 13: 571–576. [PubMed] [Google Scholar]
Педиатр Нефрол. 1999; 13: 571–576. [PubMed] [Google Scholar]
47. Aflaiw A, Vas S, Oreopoulos DG. Перитонит у больных на автоматизированном перитонеальном диализе. Внести нефрол. 1999; 129: 213–228. [PubMed] [Google Scholar]
48. Schaefer F. Лечение перитонита у детей, находящихся на хроническом перитонеальном диализе. Педиатрические препараты. 2003; 5: 315–325. [PubMed] [Академия Google]
49. Warchol S, Roszkowska-Blaim M, Sieniawska M. Престернальный перитонеальный диализный катетер «лебединая шея»: пятилетний опыт лечения детей. Перит Наберите внутр. 1998; 18: 183–187. [PubMed] [Google Scholar]
50. Чадха В., Джонс Л.Л., Рамирес З.Д., Варади Б.А. Размещение катетера перитонеального диализа на грудной клетке у младенцев с колостомией. Adv Perit Dial. 2000;16:318–320. [PubMed] [Google Scholar]
51. Warady BA, Hebert D, Sullivan EK, Alexander SR, Tejani A. Трансплантация почки, хронический диализ и хроническая почечная недостаточность у детей и подростков. 1995 ежегодный отчет североамериканского педиатрического кооперативного исследования трансплантата почки. Педиатр Нефрол. 1997; 11:49–64. [PubMed] [Google Scholar]
1995 ежегодный отчет североамериканского педиатрического кооперативного исследования трансплантата почки. Педиатр Нефрол. 1997; 11:49–64. [PubMed] [Google Scholar]
52. Furth SL, Donaldson LA, Sullivan EK, Watkins SL, North American Pediatric Renal Transplant Cooperative Study Инфекции перитонеального диализного катетера и перитонит у детей: отчет о Североамериканском педиатрическом совместном исследовании по пересадке почек . Педиатр Нефрол. 2000; 15: 179–182. [PubMed] [Google Scholar]
53. Twardowski ZJ, Dobbie JW, Moore HL, Nichols WK, DeSpain JD, Anderson PC, Khanna R, Nolph KD, Loy TS. Морфология туннеля катетера перитонеального диализа: макроскопия и световая микроскопия. Перит Наберите внутр. 1991;11:237–251. [PubMed] [Google Scholar]
54. Эклунд Б., Хонканен Э., Киллонен Л., Салмела К., Кала А.Р. Доступ к перитонеальному диализу: проспективное рандомизированное сравнение прямых катетеров Tenckhoff с одной и двумя манжетами. Трансплантация нефролового циферблата. 1997; 12: 2664–2666. [PubMed] [Google Scholar]
1997; 12: 2664–2666. [PubMed] [Google Scholar]
55. Стрипполи Г.Ф., Тонг А., Джонсон Д., Шена Ф.П., Крейг Дж.К. (2004) Тип катетера, методы размещения и введения для предотвращения перитонита у пациентов на перитонеальном диализе. Кокрановская база данных Syst Rev (4): CD004680 [PubMed]
56. Crabtree JH, Burchette RJ. Перспективное сравнение нисходящего и латерального перитонеального диализного катетера в направлении туннельного тракта и места выхода. Перит Наберите внутр. 2006; 26: 677–683. [PubMed] [Google Scholar]
57. Smith CA. Снижение частоты перитонита за счет использования «промывки перед заполнением» при APD. Adv Perit Dial. 1997; 13: 224–226. [PubMed] [Google Scholar]
58. Варади Б.А., Эллис Э.Н., Фивуш Б.А., Кум Г.М., Александр С.Р., Брюэр Э.Д., Огринк Ф., Уоткинс С. Промойте перед введением детям, получающим автоматический перитонеальный диализ. Перит Наберите внутр. 2003;23:493–498. [PubMed] [Google Scholar]
59. Веррина Э., Хонда М. , Варади Б.А., Пираино Б. Профилактика перитонита у детей на перитонеальном диализе. Перит Наберите внутр. 2000;20:625–630. [PubMed] [Google Scholar]
, Варади Б.А., Пираино Б. Профилактика перитонита у детей на перитонеальном диализе. Перит Наберите внутр. 2000;20:625–630. [PubMed] [Google Scholar]
60. Gadallah MF, Ramdeen G, Mignone J, Patel D, Mitchell L, Tatro S. Роль предоперационной антибиотикопрофилактики в предотвращении послеоперационного перитонита при недавно установленных катетерах для перитонеального диализа. Am J почек Dis. 2000;36:1014–1019. [PubMed] [Google Scholar]
61. Strippoli GF, Tong A, Johnson D, Schena FP, Craig JC (2004) Противомикробные средства для профилактики перитонита у пациентов на перитонеальном диализе. Кокрановская база данных, системная редакция (4): CD004679[PubMed]
62. Bonifati C, Pansini F, Torres DD, Navaneethan SD, Craig JC, Strippoli GF. Антимикробные агенты и вмешательства, связанные с катетером, для предотвращения перитонита при перитонеальном диализе: использование фактических данных в контексте клинической практики. Int J Artif Organs. 2006; 29:41–49. [PubMed] [Google Scholar]
63. Sardegna KM, Beck AM, Strife CF. Оценка периоперационной антибиотикотерапии во время установки диализного катетера. Педиатр Нефрол. 1998; 12: 149–152. [PubMed] [Академия Google]
Sardegna KM, Beck AM, Strife CF. Оценка периоперационной антибиотикотерапии во время установки диализного катетера. Педиатр Нефрол. 1998; 12: 149–152. [PubMed] [Академия Google]
64. Катял А., Махале А., Ханна Р. Антибиотикопрофилактика перед установкой катетера для перитонеального диализа. Adv Perit Dial. 2002; 18:112–115. [PubMed] [Google Scholar]
65. Пираино Б. Лечение инфекций, связанных с катетером. Am J почек Dis. 1996; 27: 754–758. [PubMed] [Google Scholar]
66. Пираино Б. Инфекционные осложнения перитонеального диализа. Перит Наберите внутр. 1997; 17: С15–С18. [PubMed] [Google Scholar]
67. Пираино Б. Перитонит как осложнение перитонеального диализа. J Am Soc Нефрол. 1998;9:1956–1964. [PubMed] [Google Scholar]
68. Szeto CC, Chow KM, Leung CB, Wong TYH, Wu AKL, Wang AYM, Lui SF, Li PKT. Клиническое течение перитонита, вызванного видами Pseudomonas, осложняющими перитонеальный диализ: обзор 104 случаев. почки инт. 2001; 59: 2309–2315. [PubMed] [Google Scholar]
69. Twardowski ZJ, Prowant BF. Современный подход к инфекциям места выхода у пациентов на перитонеальном диализе. Трансплантация нефролового циферблата. 1997; 12:1284–1295. [PubMed] [Академия Google]
Twardowski ZJ, Prowant BF. Современный подход к инфекциям места выхода у пациентов на перитонеальном диализе. Трансплантация нефролового циферблата. 1997; 12:1284–1295. [PubMed] [Академия Google]
70. Аурон А., Саймон С., Эндрюс В., Джонс Л., Джонсон С., Мушараф Г., Варади Б.А. Профилактика перитонита у детей, находящихся на перитонеальном диализе. Педиатр Нефрол. 2007; 22: 578–585. [PubMed] [Google Scholar]
71. Luzar MA, Coles GA, Faller B, Slingeneyer A, Dah GD, Briat C, Wone C, Knefati Y, Kessier M, Peluso F. Назальное носительство Staphylococcus aureus и инфекция у пациентов на непрерывный амбулаторный перитонеальный диализ. N Engl J Med. 1990; 322: 505–559. [PubMed] [Академия Google]
72. Piraino B, Perlmutter JA, Holley JL, Bernardini J. Перитонит, вызванный золотистым стафилококком, связан с назальным носительством золотистого стафилококка у пациентов на перитонеальном диализе. Перит Наберите внутр. 1993; 13:S332–S334. [PubMed] [Google Scholar]
73. Блоуи Д.Л., Варади Б.А., Макфарланд К.С. Лечение назального носительства золотистого стафилококка у детей, находящихся на перитонеальном диализе. Adv Perit Dial. 1994; 10: 297–299. [PubMed] [Google Scholar]
Блоуи Д.Л., Варади Б.А., Макфарланд К.С. Лечение назального носительства золотистого стафилококка у детей, находящихся на перитонеальном диализе. Adv Perit Dial. 1994; 10: 297–299. [PubMed] [Google Scholar]
74. Кингватанакул П., Варади Б.А. Назальное носительство золотистого стафилококка у детей, находящихся на длительном перитонеальном диализе. Adv Perit Dial. 1997;13:281–284. [PubMed] [Google Scholar]
75. Oh J, Baum H, Klaus G, Schaefer F, Европейская исследовательская группа по перитонеальному диализу у детей (EPPS) Назальное носительство Staphylococcus aureus в семьях, если дети находятся на перитонеальном диализе. Adv Perit Dial. 2000; 16: 324–327. [PubMed] [Google Scholar]
76. Bernardini J, Piraino B, Holley J, Johnston JR, Lutes R. Рандомизированное исследование профилактики золотистого стафилококка у пациентов на перитонеальном диализе: 2% кальциевая мазь мупироцина наносится на место выхода по сравнению с циклический пероральный рифампин. Am J почек Dis. 1996;27:695–700. [PubMed] [Google Scholar]
1996;27:695–700. [PubMed] [Google Scholar]
77. Группа по изучению мупироцина Назальный мупироцин предотвращает инфицирование места выхода Staphylococcus aureus во время перитонеального диализа. J Am Soc Нефрол. 1998; 11:2403–2408. [PubMed] [Google Scholar]
78. Миллер М.А., Даскаль А., Портной Дж., Мендельсон Дж. Развитие устойчивости к мупироцину среди метициллин-резистентных золотистых стафилококков после широкого применения назальной мупироциновой мази. Краткое коммун. 1996;17:811. [PubMed] [Академия Google]
79. Томас Д.Г., Уилсон Дж.М., Дэй М.Дж., Рассел А.Д. Устойчивость к мупироцину у стафилококков: развитие и передача устойчивости, опосредованной изолейцил-тРНК-синтетазой, in vitro. J Appl Microbiol. 1999; 86: 715–722. [PubMed] [Google Scholar]
80. Annigeri R, Conly J, Vas S, Dedier H, Praskashan KP, Bargman JM, Jassal V, Oreopoulos D. Возникновение мупироцин-резистентного Staphylococcus aureus у пациентов с хроническим перитонеальным диализом, использующих мупироциновую профилактику. для предотвращения инфекции на выходе. Перит Наберите внутр. 2001; 21: 554–559.. [PubMed] [Google Scholar]
для предотвращения инфекции на выходе. Перит Наберите внутр. 2001; 21: 554–559.. [PubMed] [Google Scholar]
81. Бернардини Дж., Бендер Ф., Флорио Т., Слоанд Дж., Пальммонтальбано Л., Фрид Л., Пираино Б. Рандомизированное двойное слепое исследование антибиотика крема для места выхода для предотвращения инфекции места выхода у пациентов на перитонеальном диализе. J Am Soc Нефрол. 2005; 16: 539–545. [PubMed] [Google Scholar]
82. Холлоуэй М., Муджейс С., Кандерт М., Варади Б.А. Обучение педиатрическому перитонеальному диализу: характеристики и влияние на частоту перитонита. Перит Наберите внутр. 2001; 21: 401–404. [PubMed] [Академия Google]
83. Zaruba K, Peters J, Jungbluth H. Успешная профилактика грибкового перитонита у пациентов на непрерывном амбулаторном перитонеальном диализе: шестилетний опыт. Am J почек Dis. 1991; 17:43–46. [PubMed] [Google Scholar]
84. Robitaille P, Merouani A, Clermont MJ, Hebert E. Успешная противогрибковая профилактика при хроническом перитонеальном диализе: педиатрический опыт. Перит Наберите внутр. 1995; 15:77–79. [PubMed] [Google Scholar]
Перит Наберите внутр. 1995; 15:77–79. [PubMed] [Google Scholar]
85. Lo WK, Chan CY, Cheng SW, Poon JF, Chan DT, Cheng IK. Проспективное рандомизированное контрольное исследование пероральной профилактики нистатином кандидозного перитонита, осложняющего непрерывный амбулаторный перитонеальный диализ. Am J почек Dis. 1996;28:549–552. [PubMed] [Google Scholar]
86. Тодис Э., Вас С.И., Баргман Дж.М., Сингхал М., Чу М., Ореопулос Д.Г. Профилактика нистатином: его неспособность предотвратить грибковый перитонит у пациентов, находящихся на постоянном амбулаторном перитонеальном диализе. Перит Наберите внутр. 1998; 18: 583–589. [PubMed] [Google Scholar]
87. Williams PF, Moncrieff N, Marriott J. Нет пользы от использования нистатина для профилактики грибкового перитонита у пациентов на перитонеальном диализе. Перит Наберите внутр. 2000; 20: 352–353. [PubMed] [Академия Google]
88. Прасад К.Н., Прасад Н., Гупта А., Шарма Р.К., Верма А.К., Айягари А. Грибковый перитонит у пациентов на непрерывном амбулаторном перитонеальном диализе: опыт Индии в одном центре. J заразить. 2004; 48:96–101. [PubMed] [Google Scholar]
J заразить. 2004; 48:96–101. [PubMed] [Google Scholar]
89. Schaefer F, Klaus G, Mueller-Wiefel DE, Mehls O, Mid-European Pediatric Peritoneal Study Group (MEPPS) Прерывистое и непрерывное внутрибрюшинное лечение гликопептидами/цефтазидимом у детей с перитонеальным диализом. сопутствующий перитонит. J Am Soc Нефрол. 1999;10:136–145. [PubMed] [Google Scholar]
90. Boyce NW, Wood C, Thomson NM, Kerr P, Atkins RC. Внутрибрюшинная (IP) ванкомициновая терапия перитонита ПАПД — проспективное рандомизированное сравнение прерывистой и непрерывной терапии. Am J почек Dis. 1988; 12: 304–306. [PubMed] [Google Scholar]
91. Low CL, Bailie GR, Evans A, Eisle G, Venezia RA. Фармакокинетика внутрибрюшинного введения гентамицина один раз в сутки у пациентов с ПАПД. Перит Наберите внутр. 1996; 16: 379–384. [PubMed] [Академия Google]
92. Лоу С.Л., Гопалакришна К., Лай В.К. Фармакокинетика внутрибрюшинного цефазолина один раз в сутки у пациентов с постоянным амбулаторным перитонеальным диализом. J Am Soc Нефрол. 2000; 11:1117–1121. [PubMed] [Google Scholar]
J Am Soc Нефрол. 2000; 11:1117–1121. [PubMed] [Google Scholar]
93. Блоуи Д.Л., Варади Б.А., Абдель-Рахман С., Фрай Р.Ф., Мэнли Х.Дж. Распределение ванкомицина после внутрибрюшинного введения у детей, получающих перитонеальный диализ. Перит Наберите внутр. 2007; 27:79–85. [PubMed] [Google Scholar]
94. Jorres A, Topley N, Witowski J. Влияние растворов для перитонеального диализа на перитонеальную иммунную защиту. Перит Наберите внутр. 1993;13:S291–S294. [PubMed] [Google Scholar]
95. Кэмерон Дж.С. Защитные силы хозяина при постоянном амбулаторном перитонеальном диализе и генез перитонита. Педиатр Нефрол. 1995; 9: 647–662. [PubMed] [Google Scholar]
96. Бур А.В., Леви М., Реддингиус Р.Е., Виллемс Дж.Л., Бош С., Шредер С.Х., Монненс Л.А. Внутрибрюшинная гиперкоагуляция и гипофибринолиз присутствуют при детском перитоните. Педиатр Нефрол. 1999; 13: 284–287. [PubMed] [Google Scholar]
97. Баутс А.Х.М., Дэвин Дж.К., Кредиет Р.Т., Вил М.Б., Шредер К.Х. , Монненс Л., Наута Дж., Аут Т.А. Иммуноглобулины при хронической почечной недостаточности у детей: влияние методов диализа. почки инт. 2000;58:629–637. [PubMed] [Google Scholar]
, Монненс Л., Наута Дж., Аут Т.А. Иммуноглобулины при хронической почечной недостаточности у детей: влияние методов диализа. почки инт. 2000;58:629–637. [PubMed] [Google Scholar]
98. Neu AM, Furth SL, Lederman HM, Warady BA, Fivush B. Гипогаммаглобулинемия у младенцев на перитонеальном диализе. Перит Наберите внутр. 1998; 18:440–443. [PubMed] [Google Scholar]
99. Flanigan MJ, Lim VS. Начальное лечение перитонита, связанного с диализом: контролируемое исследование ванкомицина по сравнению с цефазолином. Перит Наберите внутр. 1991; 11:31–37. [PubMed] [Google Scholar]
100. Милликен С.П., Мацке Г.Р., Кин В.Ф. Антимикробное лечение перитонита, связанного с постоянным амбулаторным перитонеальным диализом. Перит Наберите внутр. 1991;11:252–260. [PubMed] [Google Scholar]
101. Мюллер-Вифель, Германия. Лечение перитонита у детей на непрерывном перитонеальном диализе. Перит Наберите внутр. 1999; 19: С450–С457. [PubMed] [Google Scholar]
102. Консультативный комитет по практике больничного инфекционного контроля (HICPAC) Рекомендации по предотвращению распространения резистентности к ванкомицину. Infect Control Hosp Epidemiol. 1995; 16:105–113. [PubMed] [Google Scholar]
Infect Control Hosp Epidemiol. 1995; 16:105–113. [PubMed] [Google Scholar]
103. Smith TL, Pearson ML, Wilcox KR, Cruz C, Lancaster MV, Robinson-Dunn B, Tenover FC, Zervos MJ, Band JD, White E, Jarvis WR. Возникновение устойчивости к ванкомицину у Staphylococcus aureus. N Engl J Med. 1999;316:927–931. [PubMed] [Google Scholar]
104. Sieradzki K, Roberts RB, Haber SW, Tomasz A. Развитие устойчивости к ванкомицину у пациента с метициллин-резистентной инфекцией Staphylococcus aureus. N Engl J Med. 1999; 340: 517–523. [PubMed] [Google Scholar]
105. Warady BA, Reed L, Murphy G, Kastetter S, Karlsen E, Alon U, Hellerstein S. Ототоксичность аминогликозидов у детей, получающих длительный перитонеальный диализ. Педиатр Нефрол. 1993; 7: 178–181. [PubMed] [Академия Google]
106. Шемин Д., Мааз Д., Сен-Пьер Д., Кан С.И., Чазан Дж.А. Влияние применения аминогликозидов на остаточную функцию почек у больных на перитонеальном диализе. Am J почек Dis. 1999; 31:14–20. [PubMed] [Google Scholar]
107. Singhal MK, Bhaskaran S, Vidgen E, Bargman JM, Vas SI, Oreopoulos DG. Скорость снижения остаточной функции почек у больных на непрерывном перитонеальном диализе и факторы, влияющие на нее. Перит Наберите внутр. 2000; 20:429–438. [PubMed] [Google Scholar]
Singhal MK, Bhaskaran S, Vidgen E, Bargman JM, Vas SI, Oreopoulos DG. Скорость снижения остаточной функции почек у больных на непрерывном перитонеальном диализе и факторы, влияющие на нее. Перит Наберите внутр. 2000; 20:429–438. [PubMed] [Google Scholar]
108. Чадха В., Блоуи Д.Л., Варади Б.А. Является ли рост достоверным показателем исхода диализа у детей на перитонеальном диализе? Перит Наберите внутр. 2001;21:S179–С184. [PubMed] [Google Scholar]
109. Boeschoten EW, Ter Wee PM, Divinho J. Рекомендации по инфекциям, связанным с перитонеальным диализом, 2005 г. — важный инструмент для улучшения качества. Трансплантация нефролового циферблата. 2006; 21: Sii31–Sii33. [PubMed] [Google Scholar]
110. Baker RJ, Senior H, Clemenger M, Brown EA. Эмпирические аминогликозиды при перитоните не влияют на остаточную функцию почек. Am J почек Dis. 2003; 41: 670–675. [PubMed] [Google Scholar]
111. Грейди Р. Профиль безопасности хинолоновых антибиотиков у детей. Педиатр Infect Dis. 2003; J22: 1128–1132. [PubMed] [Академия Google]
2003; J22: 1128–1132. [PubMed] [Академия Google]
112. Ноэль Г.Дж., Брэдли Д.С., Кауфман Р.Э., Даффи К.М., Гербино П.Г., Аргедас А., Багчи П., Балис Д.А., Блумер Д.Л. Сравнительный профиль безопасности левофлоксацина у 2523 детей с акцентом на четыре специфических заболевания опорно-двигательного аппарата. Педиатр Infect Dis. 2007; 26: 879–891. [PubMed] [Google Scholar]
113. Гокал Р., Александр С.Р., Эш С., Чен Т.В., Дэниэлсон А., Холмс С., Джоффе П., Монкриф Дж., Николс К., Пираино Б., Провант Б., Слингенейер А., Стегмайр Б., Твардовски З., Вас С. Перитонеальные катетеры и практика места выхода. На пути к оптимальному перитонеальному доступу: 1998 обновление. Педиатр Наберите внутр. 1998; 18:11–13. [PubMed] [Google Scholar]
114. Vychytil A, Lorenz M, Schneider B, Horl WH, Haag-Weber M. Новые критерии лечения катетерных инфекций у пациентов на перитонеальном диализе с использованием ультразвукового исследования. J Am Soc Нефрол. 1998; 9: 290–296. [PubMed] [Google Scholar]
115. Фрид Л., Пираино Б. Перитонит. В: Гокал Р., Ханна Р., Кредиет Р., Нолф К., редакторы. Учебник перитонеального диализа. Норвелл: Клувер; 2000. стр. 545–564. [Академия Google]
Фрид Л., Пираино Б. Перитонит. В: Гокал Р., Ханна Р., Кредиет Р., Нолф К., редакторы. Учебник перитонеального диализа. Норвелл: Клувер; 2000. стр. 545–564. [Академия Google]
116. Блоуи Д.Л., Гарг У.К., Кернс Г.Л., Варади Б.А. Перитонеальное проникновение липидного комплекса амфотерицина В и флуконазола у ребенка с грибковым перитонитом. Adv Perit Dial. 1998; 14: 247–250. [PubMed] [Google Scholar]
117. Даль Н.В., Фут Э.Ф., Сирсон К.М., Фейн Дж.Л., Капоян Т., Стюард К.А., Шерман Р.А. Фармакокинетика внутрибрюшинного флуконазола при непрерывном циклическом перитонеальном диализе. Энн Фармакотер. 2000; 32: 1284–1289. [PubMed] [Google Scholar]
118. Klaus G, Schaer F, Querfeld U, Soergel M, Wolf S, Mehls O. Лечение рецидивирующего перитонита у детей на перитонеальном диализе. Adv Perit Dial. 1992;8:302–305. [PubMed] [Google Scholar]
119. Plum J, Sudkamp S, Grabensee B. Результаты ультразвуковой диагностики туннельных инфекций при непрерывном амбулаторном перитонеальном диализе. Am J почек Dis. 1994; 23:99–104. [PubMed] [Google Scholar]
Am J почек Dis. 1994; 23:99–104. [PubMed] [Google Scholar]
120. Majkowski NL, Mendley SR. Одновременное удаление и замена инфицированных катетеров для перитонеального диализа. Am J почек Dis. 1997; 29: 706–711. [PubMed] [Google Scholar]
121. Posthuma N, Borgstein PJ, Eijsbouts Q, ter Wee PM. Одновременное введение и удаление катетера для перитонеального диализа при инфекциях, связанных с катетером, без прерывания перитонеального диализа. Трансплантация нефролового циферблата. 1998;13:700–703. [PubMed] [Google Scholar]
122. Lui SL, Li FK, Lo CY, Lo WK. Одновременное удаление и повторная установка катетеров Tenckhoff для лечения рефрактерной инфекции в месте выхода. Adv Perit Dial. 2000; 16: 195–197. [PubMed] [Google Scholar]
123. Lui SL, Yip T, Tse KC, Lam MF, Lai KN, Lo WK. Лечение рефрактерной инфекции места выхода Pseudomonas aeruginosa путем одновременного удаления и повторной установки катетера для перитонеального диализа. Перит Наберите внутр. 2005; 25: 560–563. [PubMed] [Академия Google]
[PubMed] [Академия Google]
124. Шварц Р.Д., Мессана Дж.М. Одновременное удаление и замена катетера при перитонеальных диализных инфекциях: обновление и текущие рекомендации. Adv Perit Dial. 1999; 15: 205–208. [PubMed] [Google Scholar]
125. Warady BA, Schaefer FS. Перитонит. В: Варади Б.А., Шефер Ф.С., Файн Р.Н., Александр С.Р., редакторы. Детский диализ. Дордрехт: Клювер; 2004. стр. 393–414. [Google Scholar]
126. Honda M, Warady B (2008) Длительный перитонеальный диализ и инкапсулирующий перитонеальный склероз у детей. Педиатр Нефрол doi:10.1007/s00467-008-0982-z [бесплатная статья PMC] [PubMed]
127. Маруяма Ю., Накаяма М. Инкапсулирующий перитонеальный склероз в Японии. Перит Наберите внутр. 2008; 28:S201–S204. [PubMed] [Google Scholar]
История болезни: Первичный перитонит как начало детской болезни Менетрие
Введение
брюшной источник. На его долю приходится 1–3% острых абдоминальных неотложных состояний у детей (1–4). Болезнь Менетрие (БМ) относительно распространена среди взрослых, но крайне редко встречается у детей: на сегодняшний день в научной литературе описано около 150 случаев (5–7). Мы представляем необычный случай ПП как начало БМ у мальчика.
Мы представляем необычный случай ПП как начало БМ у мальчика.
История болезни
11-летний мальчик был осмотрен в педиатрическом отделении неотложной помощи в связи с 3-дневной историей боли и вздутия живота. Он был правильно вакцинирован, и в анамнезе у него не было интереса, за исключением самокупирующегося гастроэнтерита за 14 дней до начала этого эпизода.
Больной имел обычный вид за счет спонтанных болей, усиливающихся при движении, лихорадки (38,3°С) и тахикардии (124 уд/мин) при нормальном АД (104/62 мм рт.ст.). Было оценено увеличение на 3,5 кг по сравнению с его обычным весом. Физикальное обследование выявило незудящие эритематозные бляшки на животе, лобке и проксимальных сегментах обеих нижних конечностей (рис. 1). При осмотре брюшной полости отмечалось вздутие живота, диффузная боль и болезненность. Нижняя часть спины болезненна при пальпации. У него имелись ямочные отеки на брюшной стенке, поясничной области и дистальных сегментах нижних конечностей. При аускультации легких выявлено ослабление везикулярного дыхания справа.
При аускультации легких выявлено ослабление везикулярного дыхания справа.
Рисунок 1 . Физикальное обследование: вздутие живота и незудящие эритематозные бляшки на брюшной стенке (А) , лобке и проксимальных сегментах обеих нижних конечностей (В) .
Выполнена рентгенограмма брюшной полости, показывающая вероятное масс-эффект на петлях поперечной и нисходящей ободочной кишки без признаков обструкции. Рентгенограмма грудной клетки выявила правосторонний плеврит. КТ брюшной полости с контрастом была приоритетнее УЗИ, чтобы лучше охарактеризовать предполагаемое образование в брюшной полости. Он показал асцит, двусторонний плеврит, поясничный подкожный отек и ателектаз правой нижней доли с нормальным размером сердца (рис. 2). Анализ крови выявил повышенное количество лейкоцитов 37,48 × 10 9 .0277 9 /л (нейтрофилы 34,30 × 10 9 /л), количество гемоглобина и тромбоцитов в пределах нормы, аномалий в мазке периферической крови нет. Повышение реагентов острой фазы (С-реактивный белок 345 мг/л, прокальцитонин 2,77 нг/мл), гипопротеинемия с гипоальбуминемией (4,2 г общего белка/дл при 1,9 г альбумина/дл) и гипогаммаглобулинемия (IgG 137 мг/дл, IgG -1 1060 мг/л, IgG-2 317 мг/л, IgG-3 139 мг/л, IgA 43 мг/л, другие изотипы в пределах нормы). Ионы, уровень амилазы, ферменты печени, показатели функции почек были в пределах нормы. Биологические параметры сердечной функции, такие как тропонины и N-концевой прогормон натрийуретического пептида головного мозга (NT-pro-BNP), также были протестированы при обследовании асцита и плеврального выпота с нормальными результатами. Исследование мочи не выявило значительной протеинурии или гематурии.
Повышение реагентов острой фазы (С-реактивный белок 345 мг/л, прокальцитонин 2,77 нг/мл), гипопротеинемия с гипоальбуминемией (4,2 г общего белка/дл при 1,9 г альбумина/дл) и гипогаммаглобулинемия (IgG 137 мг/дл, IgG -1 1060 мг/л, IgG-2 317 мг/л, IgG-3 139 мг/л, IgA 43 мг/л, другие изотипы в пределах нормы). Ионы, уровень амилазы, ферменты печени, показатели функции почек были в пределах нормы. Биологические параметры сердечной функции, такие как тропонины и N-концевой прогормон натрийуретического пептида головного мозга (NT-pro-BNP), также были протестированы при обследовании асцита и плеврального выпота с нормальными результатами. Исследование мочи не выявило значительной протеинурии или гематурии.
Рисунок 2 . КТ брюшной полости: асцит (A) , двусторонний плевральный выпот (B) и поясничный подкожный отек (A) .
При первоначальном диагнозе перитонита и плеврального выпота было принято решение о госпитализации и начата внутривенная антибиотикотерапия цефотаксимом. Через 24 ч после госпитализации была проведена диагностическая лапароскопия, в ходе которой была обнаружена гнойная перитонеальная жидкость и исключен аппендицит или висцеральные перфорации. Рутинная аппендэктомия была выполнена без каких-либо аномальных анатомо-патологических данных. Таким образом, вторичный перитонит был исключен. Образцы асцитической жидкости исследовали на цитобиохимический анализ (562 клетки/мкл, 57% полиморфноядерных, рН 7,34, глюкоза 31 мг/дл, белок 0,12 г/дл, ЛДГ 32 ЕД/мл, триглицериды 54 мг/дл) и микробиологические исследования ( Окрашивание по Граму и аурамину, бактериальные и микобактериальные культуры, а также полимеразная цепная реакция на 9ДНК 0293 Mycobacterium tuberculosis были отрицательными). В связи с преобладанием в нашей среде метициллин-резистентного Staphylococcus aureus (~15%), был добавлен ванкомицин и назначено ограничение жидкости со строгим контролем водного баланса и суточного веса. При подозрении на ПП с гипопротеинемией дополнительные обследования исключали нефротический синдром, печеночную недостаточность, дефицит альфа-1-антитрипсина (α1-АТ), сахарный диабет, красную волчанку, лямблиоз, целиакию, туберкулез и иммунодефициты.
Через 24 ч после госпитализации была проведена диагностическая лапароскопия, в ходе которой была обнаружена гнойная перитонеальная жидкость и исключен аппендицит или висцеральные перфорации. Рутинная аппендэктомия была выполнена без каких-либо аномальных анатомо-патологических данных. Таким образом, вторичный перитонит был исключен. Образцы асцитической жидкости исследовали на цитобиохимический анализ (562 клетки/мкл, 57% полиморфноядерных, рН 7,34, глюкоза 31 мг/дл, белок 0,12 г/дл, ЛДГ 32 ЕД/мл, триглицериды 54 мг/дл) и микробиологические исследования ( Окрашивание по Граму и аурамину, бактериальные и микобактериальные культуры, а также полимеразная цепная реакция на 9ДНК 0293 Mycobacterium tuberculosis были отрицательными). В связи с преобладанием в нашей среде метициллин-резистентного Staphylococcus aureus (~15%), был добавлен ванкомицин и назначено ограничение жидкости со строгим контролем водного баланса и суточного веса. При подозрении на ПП с гипопротеинемией дополнительные обследования исключали нефротический синдром, печеночную недостаточность, дефицит альфа-1-антитрипсина (α1-АТ), сахарный диабет, красную волчанку, лямблиоз, целиакию, туберкулез и иммунодефициты. Биохимический анализ кала показал повышенный уровень α1-АТ (1,9мг/г стула; референтное значение <0,3 мг/г) и повышенный клиренс α1-АТ (107,7 мл/24 ч; референтное значение <27 мл/24 ч), что совместимо с энтеропатией с потерей белка (ЭБЭ).
Биохимический анализ кала показал повышенный уровень α1-АТ (1,9мг/г стула; референтное значение <0,3 мг/г) и повышенный клиренс α1-АТ (107,7 мл/24 ч; референтное значение <27 мл/24 ч), что совместимо с энтеропатией с потерей белка (ЭБЭ).
У него было благоприятное клиническое течение с постепенным снижением воспалительных параметров, прогрессивным улучшением уровня сывороточного белка и гамма-глобулина, полной реабсорбцией плеврального выпота и перитонеальной жидкости при поступлении. Пациент прошел 21-дневную антибактериальную терапию (14 дней внутривенного введения цефотаксима и 10 дней внутривенного введения ванкомицина, а после выписки — 7 дней перорального приема амоксициллина-клавулановой кислоты).
Дальнейшие исследования для выявления причины этого ЭПБ включали нормальную колоноскопию и гастроскопию, которые показали очень эритематозную и дискретно отечную слизистую оболочку и увеличенные желудочные складки в теле и дне желудка. Биопсия слизистой оболочки желудка выявила обширную и значительную гиперплазию фовеолярного слизисто-секреторного эпителия, что привело к удлинению и извитости фовеолярных желез с потерей париетальных клеток и отечностью собственной пластинки. Признаков лимфоплазмоцитарного или нейтрофильного инфильтрата, внутриэпителиального лимфоцитоза, включений патогенной микрофлоры или внутриклеточного цитомегаловируса (ЦМВ) не выявлено. Слизистая двенадцатиперстной кишки сохранена. Эти результаты были совместимы с MD. Гистохимическое исследование на Helicobacter pylori и иммуногистохимическое исследование на ЦМВ были отрицательными (рис. 3). Серология ЦМВ также была отрицательной.
Признаков лимфоплазмоцитарного или нейтрофильного инфильтрата, внутриэпителиального лимфоцитоза, включений патогенной микрофлоры или внутриклеточного цитомегаловируса (ЦМВ) не выявлено. Слизистая двенадцатиперстной кишки сохранена. Эти результаты были совместимы с MD. Гистохимическое исследование на Helicobacter pylori и иммуногистохимическое исследование на ЦМВ были отрицательными (рис. 3). Серология ЦМВ также была отрицательной.
Рисунок 3 . (A) Удлиненные и извилистые (штопорообразные) фовеолярные железы с отечной ведущей пластинкой (H-E x200). (B) Кистозные и расширенные железы с потерей париетальных клеток (H-E x100). (C, D) Исследование на H. pilory и CMV у нашего пациента было отрицательным. (3. Уортин-Старри х100, 4. ЦМВ х100).
Несмотря на первоначальную гипогаммаглобулинемию у нашего пациента, внутривенные иммуноглобулины не вводились для предотвращения риска новых гнойных бактериальных инфекций, поскольку у него наблюдалось хорошее клиническое развитие, а уровни гаммаглобулина и белка в его плазме спонтанно медленно увеличивались в течение следующих недель. Аналитический контроль, проведенный через 6 месяцев, показал полное восстановление уровня общего белка плазмы и альбумина. Уровень иммуноглобулинов нормализовался через 10 месяцев после госпитализации. После 12 мес наблюдения рецидива заболевания у пациентки не было. Краткое описание его клинического течения показано на рис. 4.9.0003
Аналитический контроль, проведенный через 6 месяцев, показал полное восстановление уровня общего белка плазмы и альбумина. Уровень иммуноглобулинов нормализовался через 10 месяцев после госпитализации. После 12 мес наблюдения рецидива заболевания у пациентки не было. Краткое описание его клинического течения показано на рис. 4.9.0003
Рисунок 4 . График в днях появления клинических симптомов, лабораторных данных, процедур и лечения ПП и МД.
Обсуждение и заключение
Первичный перитонит, также называемый спонтанным бактериальным перитонитом (СБП), определяемый как бактериальный перитонит при отсутствии явного интраабдоминального очага инфекции, такого как перфорация кишечника, является нечастой причиной острого живота в педиатрической популяции (1, 2, 8–11). По данным ряда педиатрических исследований, чаще встречается у женщин (85–9 лет).5%) и в возрастной группе 4–9 лет (1, 2, 4, 12). Однако в данном случае речь шла о 11-летнем мальчике. Хотя большинство случаев у детей возникают спонтанно без какой-либо патологии (1, 2, 8, 12), они связаны с заболеваниями, вызывающими гипопротеинемию и/или иммунодефицит, такими как нефротический синдром, заболевания печени, кишечная лимфома или дефицит α1-АТ (1, 2, 8, 12). 9, 11–13). Пациенты с вентрикулоперитонеальным шунтом, по-видимому, имеют более высокий риск развития СБП, поскольку спинномозговая жидкость может снижать бактериостатическую активность перитонеальной жидкости посредством различных механизмов (14). ПП также связан с расстройствами, вызывающими ЭПБ у взрослых (15). Наш случай – нечастый дебют МД с ПП у мальчика.
9, 11–13). Пациенты с вентрикулоперитонеальным шунтом, по-видимому, имеют более высокий риск развития СБП, поскольку спинномозговая жидкость может снижать бактериостатическую активность перитонеальной жидкости посредством различных механизмов (14). ПП также связан с расстройствами, вызывающими ЭПБ у взрослых (15). Наш случай – нечастый дебют МД с ПП у мальчика.
Наиболее частым клиническим проявлением ПП является острое начало болей в животе с перитонизмом или без него; в то время как лихорадка, рвота и диарея встречаются реже (1, 3, 9, 12). Околопупочная эритема является редким признаком перитонита (12), однако у нашего пациента изначально были эритематозные бляшки на животе, лобке и проксимальных сегментах обеих конечностей. Диагноз обычно подтверждается лапароскопией. В нашем случае были исключены панкреатит и поражение внутренних органов; гнойная перитонеальная жидкость исследовалась с ≥250 полиморфноядерных клеток/мм 3 и посев асцитической жидкости был отрицательным, вероятно, из-за предшествующего лечения антибиотиками. Все эти находки, при отсутствии в анамнезе лечения антибиотиками в течение последних 30 дней, были определены как культуральный негативный нейтрофилезный асцит (CNNA), разновидность СБП (16).
Все эти находки, при отсутствии в анамнезе лечения антибиотиками в течение последних 30 дней, были определены как культуральный негативный нейтрофилезный асцит (CNNA), разновидность СБП (16).
Культура асцитической жидкости отрицательна более чем в 50% образцов, на что может повлиять тот факт, что большинство пациентов получают антибиотики до диагностической хирургической процедуры (4, 8), как и в нашем случае. В детском возрасте Streptococcus pneumoniae является наиболее часто выделяемым микроорганизмом, за которым следует стрептококк группы А (GAS) (3, 10, 12). ГАС ПП был идентифицирован как очаг 5% инвазивной инфекции ГАС у детей в Финляндии (17), и другие исследования показывают, что возможная связь между ГАС фарингитом и ПП у детей может существовать (3, 10). У пациента мазок из горла экспресс-тест на обнаружение антигена (RADT) для GAS и культура были отрицательными. Исследование показало высокую чувствительность и специфичность RADT для GAS, выполненного на глубоких тканях, включая перитонеальную жидкость (18), хотя в данном случае оно не проводилось. Другие описанные микроорганизмы Escherichia coli, Klebsiella pneumoniae, Enterococcus spp., Staphylococcus aureus и некоторые вирусы (1, 9, 13, 19). Измерение кальпротектина и микроРНК-155 в асцитической жидкости можно использовать в качестве биомаркеров бактериальной инфекции асцитической жидкости (20). Обнаружение антигенов пневмококковой капсулы с помощью иммунохроматографии и полимеразной цепной реакции (традиционная или мультиплексная для бактерий и вирусов, а также амплификация и секвенирование 16S рРНК) использовались для микробиологического анализа в образцах с отрицательной культурой (21, 22). но в нашем случае эти приемы не применялись.
Другие описанные микроорганизмы Escherichia coli, Klebsiella pneumoniae, Enterococcus spp., Staphylococcus aureus и некоторые вирусы (1, 9, 13, 19). Измерение кальпротектина и микроРНК-155 в асцитической жидкости можно использовать в качестве биомаркеров бактериальной инфекции асцитической жидкости (20). Обнаружение антигенов пневмококковой капсулы с помощью иммунохроматографии и полимеразной цепной реакции (традиционная или мультиплексная для бактерий и вирусов, а также амплификация и секвенирование 16S рРНК) использовались для микробиологического анализа в образцах с отрицательной культурой (21, 22). но в нашем случае эти приемы не применялись.
Цефотаксим считается антибиотиком выбора (1, 9, 12). В нашем случае, в связи с отрицательным посевом перитонеальной жидкости и 15%-ным преобладанием метициллин-резистентного Staphylococcus aureus в нашем районе, к цефотаксиму был добавлен ванкомицин. Рекомендуемая продолжительность лечения антибиотиками составляет 10–14 дней для Streptococcus (9, 10, 19) и 10 дней–3 недели для грамотрицательных микроорганизмов (19). В данном случае, поскольку микробиологическая характеристика была невозможна, пациент получил 3 недели лечения антибиотиками. Клиническое течение при своевременном выявлении и лечении в большинстве случаев благоприятное (8, 12).
В данном случае, поскольку микробиологическая характеристика была невозможна, пациент получил 3 недели лечения антибиотиками. Клиническое течение при своевременном выявлении и лечении в большинстве случаев благоприятное (8, 12).
Болезнь Менетрие — очень редкое ЛЭ у детей. Со времени первого случая БМ, представленного в 1888 г. (23), было зарегистрировано около 150 случаев в детском возрасте (5–7). МД характеризуется гипоальбуминемией, вторичной по отношению к потере белка через слизистую оболочку желудочно-кишечного тракта, что приводит к периферическим отекам, асциту или даже анасарке (7, 23, 24). Асцит в сочетании с гипогаммаглобулинемией создает благоприятную обстановку для развития ПП. Во многих ранее зарегистрированных случаях БМ, включая этот, продромальный период болей в животе, анорексии и рвоты описывается примерно за 1 или 2 недели до поступления (5, 6, 25). Считается, что это связано с раздражением слизистой оболочки желудка и гибелью эпителиальных клеток во время первоначального воздействия неизвестного повреждающего агента (5). Большинство педиатрических исследований, по-видимому, указывают на инфекционную этиологию, основанную на наличии антител к ЦМВ в сыворотке или их идентификации в биопсии желудка, и на самокупирующееся течение (средняя продолжительность 5 недель) (5, 6, 24–26). ).
Большинство педиатрических исследований, по-видимому, указывают на инфекционную этиологию, основанную на наличии антител к ЦМВ в сыворотке или их идентификации в биопсии желудка, и на самокупирующееся течение (средняя продолжительность 5 недель) (5, 6, 24–26). ).
Повышенные значения α1-АТ и его клиренс в изолированных образцах фекалий указывают на диагноз ЭПБ, причем последний является более точным методом. α1-АТ представляет собой антипротеолитический белок плазмы, отсутствует в пищевых продуктах, за исключением грудного молока, и синтезируется в печени. Хотя он может быть разрушен при pH ниже 3 (27), как это происходит в желудке, он не расщепляется кишечными протеазами и не реабсорбируется, поэтому его определение в кале является точным маркером проникновения альбумина в кишечник. просвет кишечника, являясь отличным маркером PLE (28). Определение α1-АТ не считается подходящим методом у детей, находящихся на грудном вскармливании, и его значение может быть ложно заниженным, если ранитидин или ингибиторы протонной помпы (ИПП) не используются, когда утечка белка происходит в основном через слизистую оболочку желудка (27, 28). Наш пациент не получал ранитидин или ИПП, что свидетельствует об очень высокой потере белка желудочным соком или его просачивании через другие участки желудочно-кишечного тракта.
Наш пациент не получал ранитидин или ИПП, что свидетельствует об очень высокой потере белка желудочным соком или его просачивании через другие участки желудочно-кишечного тракта.
Окончательный диагноз БМ ставится с помощью визуализирующих исследований, таких как эндоскопия, исследования с барием или УЗИ, показывающих фовеолярную гиперплазию с железистой атрофией, связанной с увеличением складок желудка, а также биопсию желудка с гипертрофией желудка и гиперплазией эпителия при микроскопии, преимущественно на дне и желудке тело (5, 7, 29), как и в нашем случае. Другие данные включают утолщение слизистой оболочки желудка с уменьшением основных и париетальных клеток наряду с базальной кистозной дилатацией желудочных желез, что может способствовать потере белка на желудочно-кишечном уровне и впоследствии привести к глубокой гипоальбуминемии (5, 7, 29).). Изменения, описанные в гистологии, могут быть вызваны некоторыми инфекционными агентами. Наиболее частым является ЦМВ (5–7, 25, 26), за которым следует H. pylori (7, 26, 30). Другими менее распространенными являются Mycoplasma pneumoniae (31), Giardia lamblia и вирус герпеса (29). Однако у нашего пациента не было обнаружено никаких признаков заражения ЦМВ, H. pylori или другими микроорганизмами.
pylori (7, 26, 30). Другими менее распространенными являются Mycoplasma pneumoniae (31), Giardia lamblia и вирус герпеса (29). Однако у нашего пациента не было обнаружено никаких признаков заражения ЦМВ, H. pylori или другими микроорганизмами.
КТ брюшной полости обычно показывает трансмуральное утолщение желудка в области дна и тела с аномально утолщенными желудочными складками (7, 24). После постановки окончательного диагноза БМ КТ-изображения были тщательно просмотрены радиологами, которые заметили некоторые выступающие желудочные складки в области большой кривизны желудка, но они также отметили, что КТ не была выполнена в идеальных условиях для оценки типичных изображений. МД.
В педиатрической популяции лечение БД является поддерживающим и включает высокобелковую диету и анальгетики (5–7, 24). Некоторым пациентам могут потребоваться ИПП, антихолинергические стероиды, диуретики (5–7, 24), внутривенные иммуноглобулины (30) и даже инфузии альбумина в случаях тяжелой и длительной гипоальбуминемии (24, 32). Противовирусное лечение валганцикловиром или ганцикловиром может быть рассмотрено при доказанной ЦМВ-инфекции у детей с иммунодефицитом или если заболевание сохраняется более 2-4 недель (5, 6, 24, 32). Кроме того, цетуксимаб, моноклональное антитело, которое блокирует передачу сигналов рецептора эпидермального фактора роста (EGFR), успешно применялся у взрослых пациентов (33).
Противовирусное лечение валганцикловиром или ганцикловиром может быть рассмотрено при доказанной ЦМВ-инфекции у детей с иммунодефицитом или если заболевание сохраняется более 2-4 недель (5, 6, 24, 32). Кроме того, цетуксимаб, моноклональное антитело, которое блокирует передачу сигналов рецептора эпидермального фактора роста (EGFR), успешно применялся у взрослых пациентов (33).
Учитывая благоприятное течение и частое самопроизвольное разрешение заболевания, прогрессивное восстановление уровня белка и иммуноглобулинов в крови и отсутствие новых инвазивных инфекций, от внутривенного введения иммуноглобулинов в нашем случае отказались (34, 35). В педиатрической популяции МД является самокупирующимся, с хорошим прогнозом и отсутствием тенденции к рецидивам. В нашем случае пациент не нуждался в дополнительном лечении и до настоящего времени не предъявлял новых симптомов. С другой стороны, МД у взрослых обычно протекает хронически, с тенденцией к малигнизации, иногда требуя агрессивного лечения, такого как гастрэктомия (5–7, 26, 33).
В заключение, хотя и редко встречающийся у здоровых детей, ПП представляет собой потенциально опасный для жизни процесс, который следует включать в дифференциальную диагностику острой боли в животе, особенно если она связана с отеком. Как показано в этом клиническом случае, ПП и МД могут сосуществовать у детей, хотя клиническое начало в этом случае, по-видимому, связано с ПП. Знание МД и его в целом доброкачественной природы у детей важно, чтобы избежать ненужных дополнительных тестов или лечения.
Заявление о доступности данных
Первоначальные материалы, представленные в исследовании, включены в статью/дополнительные материалы. Дальнейшие запросы можно направлять соответствующему автору/авторам.
Заявление об этике
От законного опекуна несовершеннолетнего было получено письменное информированное согласие на публикацию любых потенциально идентифицируемых изображений или данных, включенных в эту статью.
Вклад авторов
JB-M, EC-G и CM-C разработали первоначальную рукопись, критически рассмотрели и отредактировали окончательную рукопись. AB-F, AP-L и CF-L подготовили первоначальную рукопись, рассмотрели и отредактировали окончательную рукопись. CQ-T и AM-N составили исходную рукопись, выполнили биохимические и патологические процедуры соответственно, а также рассмотрели и отредактировали рукопись. Все авторы предоставили критические отзывы, одобрили окончательный вариант представленной рукописи, согласились нести ответственность за все аспекты работы и обеспечили надлежащее расследование и решение вопросов, связанных с точностью или целостностью любой части работы.
AB-F, AP-L и CF-L подготовили первоначальную рукопись, рассмотрели и отредактировали окончательную рукопись. CQ-T и AM-N составили исходную рукопись, выполнили биохимические и патологические процедуры соответственно, а также рассмотрели и отредактировали рукопись. Все авторы предоставили критические отзывы, одобрили окончательный вариант представленной рукописи, согласились нести ответственность за все аспекты работы и обеспечили надлежащее расследование и решение вопросов, связанных с точностью или целостностью любой части работы.
Конфликт интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Мы благодарим пациента и его семью за разрешение использовать данные.
Дополнительный материал
Дополнительный материал к этой статье можно найти в Интернете по адресу: https://www.frontiersin. org/articles/10.3389/fped.2020.589853/full#supplementary-material
org/articles/10.3389/fped.2020.589853/full#supplementary-material
Сокращения
PP, Первичный перитонит; MD, болезнь Менетрие; КТ, Компьютерная томография; NT-pro-BNP, N-концевой прогормон натрийуретического пептида головного мозга; PLE, энтеропатия с потерей белка; ЦМВ, цитомегаловирус; СБП, спонтанный бактериальный перитонит; CNNA, нейтрофильный асцит с отрицательным посевом; ГАС, стрептококк группы А; RADT, экспресс-тест на обнаружение антигена; α1-АТ, альфа-1-антитрипсин; ИПП, ингибиторы протонной помпы; EGFR, рецептор эпидермального фактора роста.
Литература
1. Хилджи М.Ф. Первичный перитонит — забытое явление. Eur J Pediatric Surg Rep. (2015) 3:27–9. doi: 10.1055/s-0034-1374544
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
2. Мараки С., Спатопулу Т., Нтаукакис М., Влачакис Дж. Первичный пневмококковый перитонит у иммунокомпетентного ребенка. Braz J Infect Dis. (2012) 16:107–8. doi: 10.1016/S1413-8670(12)70287-8
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
3. Sharp EA, Linn A, Zitelli BJ. Стрептококковый фарингит группы А, ассоциированный с первичным перитонитом. BMJ Case Rep. (2019) 12:e229186. doi: 10.1136/bcr-2019-229186
Sharp EA, Linn A, Zitelli BJ. Стрептококковый фарингит группы А, ассоциированный с первичным перитонитом. BMJ Case Rep. (2019) 12:e229186. doi: 10.1136/bcr-2019-229186
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
4. Фаулер Р. Первичный перитонит: изменяющиеся аспекты, 1956–1970 гг. J Педиатр Детское здоровье. (1971) 7:73–83. doi: 10.1111/j.1440-1754.1971.tb02202.x
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
5. Williamson K, Park HK, Schacht R, Kaistha A. Случай болезни Менетрие у ребенка. Неотложная помощь педиатру. (2012) 28:277–9. doi: 10.1097/PEC.0b013e31824957b8
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
6. Blackstone MM, Mittal MK. Отечный малыш: случай педиатрической болезни Менетрие. Неотложная помощь педиатру. (2008) 24:682–4. doi: 10.1097/PEC.0b013e3181887e89
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
7. Barbati F, Marrani E, Indolfi G, Lionetti P, Trapani S. Болезнь Менетрие и цитомегаловирусная инфекция в педиатрическом возрасте: отчет о трех случаях и обзор литературы. Eur J Pediatr. (2020). doi: 10.1007/s00431-020-03782-6. [Epub перед печатью].
Barbati F, Marrani E, Indolfi G, Lionetti P, Trapani S. Болезнь Менетрие и цитомегаловирусная инфекция в педиатрическом возрасте: отчет о трех случаях и обзор литературы. Eur J Pediatr. (2020). doi: 10.1007/s00431-020-03782-6. [Epub перед печатью].
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
8. Кимбер С.П., Хатсон Дж.М. Первичный перитонит у детей. ANZ J Surg. (1996) 66:169–70. doi: 10.1111/j.1445-2197.1996.tb01149.x
Резюме PubMed | Полный текст перекрестной ссылки | Google Scholar
9. Johnson CC, Baldessarre J, Levison ME. Перитонит: обновленная информация о патофизиологии, клинических проявлениях и лечении. Clin Infect Dis. (1997) 24:1035–45. doi: 10.1086/513658
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
10. Haskett H, Delair S, Neemann K. Первичный стрептококковый перитонит группы А у ранее здоровой девочки-подростка. Глоб Педиатр Здоровье. (2020) 7:2333794X2095764. doi: 10.1177/2333794X20957647
doi: 10.1177/2333794X20957647
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
11. Гошал У.К., Поддар У., Ячха С.К. Спонтанный бактериальный перитонит у ребенка с абдоминальной лимфомой. Акта Онкол. (1995) 34:531. doi: 10.3109/02841869509094019
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
12. Zhou H, Cheng W. Первичный перитонит у детей. Энн Колл Сур Гонконг. (2000) 4:53–6. дои: 10.1046/j.1442-2034.2000.00049.x
Полнотекстовая перекрестная ссылка | Google Scholar
13. Грэм Дж. К., Мосс П. Дж., МакКендрик М. В. Первичный стрептококковый перитонит группы А. Scand J Infect Dis. (1995) 27:171–2. doi: 10.3109/0036554950
01
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
14. Гаскилл С.Дж., Марлин А.Е. Спонтанный бактериальный перитонит у больных с вентрикулоперитонеальными шунтами. Детский нейрохирург. (1997) 26:115–9. дои: 10. 1159/000121175
1159/000121175
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
15. Плодди А., Атисук К., Харгроув Н.С. Кишечные лимфангиэктазии при интраабдоминальном туберкулезе. J Med Assoc Thai. (1988) 71:518–23.
Реферат PubMed | Google Scholar
16. Руньон Б.А., Хофс Дж.К. Культурально-негативный нейтрофильный асцит: вариант спонтанного бактериального перитонита. Гепатология. (1984) 4:1209–11. doi: 10.1002/hep.1840040619
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
17. Tapiainen T, Launonen S, Renko M, Saxen H, Salo E, Korppi M, et al. Инвазивные стрептококковые инфекции группы А у детей: общенациональное исследование в Финляндии. Pediatr Infect Dis J . (2016) 35:123–8. doi: 10.1097/INF.0000000000000945
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
18. Газзано В., Бергер А., Бенито Ю., Фрейдьер А.М., Тристан А., Буассет С. и др. Переоценка роли экспресс-тестов для обнаружения антигена в диагностике инвазивных стрептококковых инфекций группы А. Дж Клин Микробиол . (2016) 54:994–9. doi: 10.1128/JCM.02516-15
Дж Клин Микробиол . (2016) 54:994–9. doi: 10.1128/JCM.02516-15
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
19. Кларк Дж. Х., Фитцджеральд Дж. Ф., Клейман М. Б. Спонтанный бактериальный перитонит. J Педиатр. (1984) 104:495–500. doi: 10.1016/S0022-3476(84)80536-3
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
20. Nabiel Y, Barakat G, Abed S. Сывороточный CD64 и асцитическая жидкость кальпротектин и микроРНК-155 как потенциальные биомаркеры спонтанного бактериального перитонита. Eur J Гастроэнтерол Гепатол. (2019) 31:1064–9. doi: 10.1097/MEG.0000000000001443
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
21. Молинос Л. Обнаружение антигенов в моче. Арка Бронконеумол. (2006) 42:101–3. doi: 10.1016/S1579-2129(06)60126-2
PubMed Abstract | CrossRef Full Text
22. Dagan R, Shriker O, Hazan I, et al. Проспективное исследование для определения клинической значимости выявления ДНК пневмококка в сыворотке крови детей методом ПЦР. J Clin Microbiol. (1998) 36:669–73. doi: 10.1128/JCM.36.3.669-673.1998
J Clin Microbiol. (1998) 36:669–73. doi: 10.1128/JCM.36.3.669-673.1998
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
23. Ménétrier P. Des polyadenomes gastriques et de leurs rapports avec le Cancer de Estomac. Арка Физиол Норм Патол. (1888) 32: 236–62.
Google Scholar
24. Fouda A., Kamath B., Chung C., Punnett A. Болезнь Менетрие (гастропатия с потерей белка) у ребенка с острым лимфобластным лейкозом. Int J Pediatr Adolesc Med. (2019) 6:38–40. doi: 10.1016/j.ijpam.2019.01.002
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
25. Sferra TJ, Pawel BR, Qualman SJ, Li BUK. Детская болезнь Менетрие: роль цитомегаловируса и трансформирующего фактора роста альфа. J Педиатр. (1996) 128:213–9. doi: 10.1016/S0022-3476(96)70392-X
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
26. Кирберг Б.А., Родригес В.Б., Доносо В.Ф., Кирхман Т. М., Нориэль В.М. Гипертрофическая гастропатия с потерей белка: болезнь Менетрие. Клинический случай. Преподобный Чил Педиатрия . (2014) 85:80–5. doi: 10.4067/S0370-41062014000100011
М., Нориэль В.М. Гипертрофическая гастропатия с потерей белка: болезнь Менетрие. Клинический случай. Преподобный Чил Педиатрия . (2014) 85:80–5. doi: 10.4067/S0370-41062014000100011
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
27. Reinhart WH, Weigand K, Kappeler M, Roesler H, Halter F. Сравнение желудочно-кишечных потерь альфа-1-антитрипсина и хром-51-альбумина при болезни Менетрие и влияние ранитидина. Пищеварение. (1983) 26:192–6. doi: 10.1159/000198889
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
28. Sierra C, Vicioso M, Barco A. Enteropatía pierde-proteínas. Detección у causas más frecuentes. Анальная педиатрия . (2001) 54:36–8.
29. Фернандес Кааманьо Б., Рамос Болуда Э., Мартинес-Охинага Нодаль Э., Молина Ариас М., Сарриа Осес Дж., Прието Бозано Г. Энфермедад де Менетриер, ассоциированный с инфекцией, вызываемой цитомегаловирусом. Анальная педиатрия . (2015) 82: e113–6. doi: 10.1016/j.anpedi.2014.02.019
doi: 10.1016/j.anpedi.2014.02.019
PubMed Abstract | Полный текст перекрестной ссылки | Академия Google
30. Iwama I, Kagimoto S, Takano T, Sekijima T, Kishimoto H, Oba A. Случай педиатрической болезни Менетрие с цитомегаловирусом и коинфекцией Helicobacter pylori . Педиатр Междунар. (2010) 52:200–3. doi: 10.1111/j.1442-200X.2010.03130.x
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
31. Бен Амитай Д., Захави И., Динари Г., Гарти Б.З. Транзиторная гипертрофическая гастропатия с потерей белка, связанная с инфекцией Mycoplasma pneumoniae в детском возрасте. J Pediatr Gastroenterol Nutr. (1992) 14:237–9. doi: 10.1097/00005176-199202000-00021
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
32. Faure C, Besnard M, Hirsch A, Mougenot JF, Peuchmaur M, Cezard JP, et al. Хроническая гипертрофическая гастропатия у ребенка, напоминающая болезнь Менетрие у взрослых. J Pediatr Gastroenterol Nutr.
