Открытый артериальный проток 2 мм у детей: Открытый артериальный проток у детей (ОАП)
Открытый артериальный проток у детей (ОАП)
Открытый артериальный проток (ОАП) — сосуд, соединяющий грудную аорту с легочной артерией. В норме ОАП обязательно в 100% присутствует у плода, но закрывается вскоре после рождения, превращаясь в артериальную связку. Условно полагают, что в норме ОАП должен закрыться в течение первых двух недель жизни. Если же этого не происходит, то говорят о наличии порока сердца. Наличие данного протока и его значимость для гемодинамики в значительной мере зависит от доношенности ребенка, чем меньше вес при рождении, тем чаще встречается данная патология.
Наличие небольшого протока (менее 3 мм) обычно протекает благоприятно, совместимо с длительной активной жизнью, но имеется высокий риск развития инфекционного эндокардита или наступление резкого ухудшения на фоне любого инфекционного заболевания, чаще всего пневмонии. Протоки большого диаметра могут привести к развитию тяжелого состояния и даже гибели ребенка в первые месяцы жизни. Группой риска по длительному незакрытию протока являются прежде всего недоношенные дети, родившиеся путем операции кесарева сечения, перенесшие острую гипоксию в родах или хроническую гипоксию во время беременности.
! Ребенок с ОАП должен обязательно наблюдаться специалистом — кардиологом с контролем гемодинамических показателей по ЭХОДКГ на аппарате экспертного класса 1 раз в 3 месяца, обязательной является консультация кардиохирурга с целью определения тактики наблюдения, сроков и способе коррекции порока.
Если ОАП выявлен на этапе родильного дома и его размер более 3 мм — консультация кардиохирурга на 1-м месяце жизни ребенка является обязательной, даже при отсутствии жалоб со стороны родителей на состояние малыша. Если размер ОАП 3 мм и менее — контроль ЭХОДКГ на аппарате экспертного класса в 3 месяца, консультация кардиохирурга.
При наблюдении за ребенком родители должны обращать внимание на его физическую активность (младенцы — активность сосания), потливость, появление «посинения» в области носогубного треугольника на фоне сосания, купания, плача, натуживания; важными показателями также являются нормальный набор веса, темпы нервно — психического развития ребенка.
Открытый артериальный проток — цены на лечение, симптомы и диагностика заболевания в клинике «Мать и дитя» в Москве
Клинические проявления
В период новорожденности, как правило, диагноз «открытый артериальный проток устанавливается по результатам осмотра (аускультации) ребенка и проведенного эхографического исследования сердца.
У детей более старшего возраста, как правило, открытый артериальный проток бывает небольшого диаметра и основная жалоба в таком случае — частые респираторные заболевания у ребенка, отставание в физическом развитии (на первом году жизни).
Длительно существующий открытый артериальный проток большого диаметра (более 5 мм) — причина развития одного из самых грозных осложнений — легочной гипертензии.
Диагностика открытого артериального протока в Клиническом госпитале «Лапино»
Способ закрытия открытого артериального протока определяет хирург после проведенного диагностического обследования. Диагноз открытый артериальный проток устанавливается по данным выполненного ЭхоКГ экспертного уровня.
Лечение открытого артериального протока в Клиническом госпитале «Лапино»
В настоящее время развитие медицинских технологий позволяет в большинстве случаев (97%) устранить артериальный проток, не прибегая к торакотомии, а выполнить операцию пункционно, через бедренные сосуды.
При артериальном протоке диаметром не более 3.0 мм возможна имплантация небольшой спирали, а при диаметре от 3 до 20 мм — проток закрывают специальными механическими окклюдерами. Продолжительность операции составляет 15-25 минут и выполняется под внутривенной анестезией, что позволяет сразу после операции перевести ребенка в палату к маме и на следующий день выписать из госпиталя. О проведенном оперативном лечении будет напоминать спираль или окклюдер выявляемый каждый раз, когда Вашему ребенку будет выполняться рентгенография грудной клетки. Шрамов и следов операции на теле ребенка не остается. Имплантируемые спирали и окклюдеры полностью МРТ-совместимы и позволяют путешествовать по всему миру, свободно проходя через рамки металлодетекторов.
Имплантируемые спирали и окклюдеры полностью МРТ-совместимы и позволяют путешествовать по всему миру, свободно проходя через рамки металлодетекторов.
Открытый артериальный проток
Анатомически этот проток — короткий сосуд, соединяющий нисходящую аорту с легочной артерией. Поскольку это физиологический шунт, он необходим для внутриутробной жизни плода. Сразу после первого вдоха он больше не нужен, и через несколько часов или дней он самостоятельно закрывается. Если этого не происходит, то сообщение остается, и кровь продолжает шунтироваться из большого в малый круг кровообращения.
За редким и исключением, открытый артериальный проток (Боталлов), пожалуй, самый безобидный, «незловредный» из всех врожденных пороков сердца. Сердце, хотя и увеличивается, достаточно легко справляется с нагрузкой. Давление в системе легочной артерии повышено незначительно. Дети с этим пороком нормально развиваются и растут и, за исключением «шума» в сердце, обычно ничем от сверстников не отличаются. Однако при большом протоке могут появиться признаки перегрузки сердца и клинические признаки в виде более частых простуд, одышки про нагрузке. Тогда надо что-то делать. Здесь оговоримся, что при огромных протоках, 9 мм, и даже больше, когда их диаметр превышает размер самой аорты — главной артерии организма, то новорожденные крайне тяжелы по своему клиническому состоянию, прогрессирующей сердечной недостаточности, огромное сердечко занимает почти всю грудную клетку, смещая легкие, мешая их нормальному функционированию. Операция экстренная, выполняется по жизненным показаниям.
Особая картина развивается при сохраняющемся открытом артериальном протоке у недоношенных новорожденных. Ситуация может развиваться по разным сценариям. При небольшом диаметре протока и массе тела более 2 кг обычно ситуация не экстренная, проток имеет шансы самостоятельного закрытия, ребенок справляется с нагрузкой по сердечку, достаточно бывает наблюдения. Но при массе ребеночка менее килограмма, находящемся в кювезе (специальной медицинской кровати для выхаживания нововрожденных) и не способному к самостоятельному дыханию, т.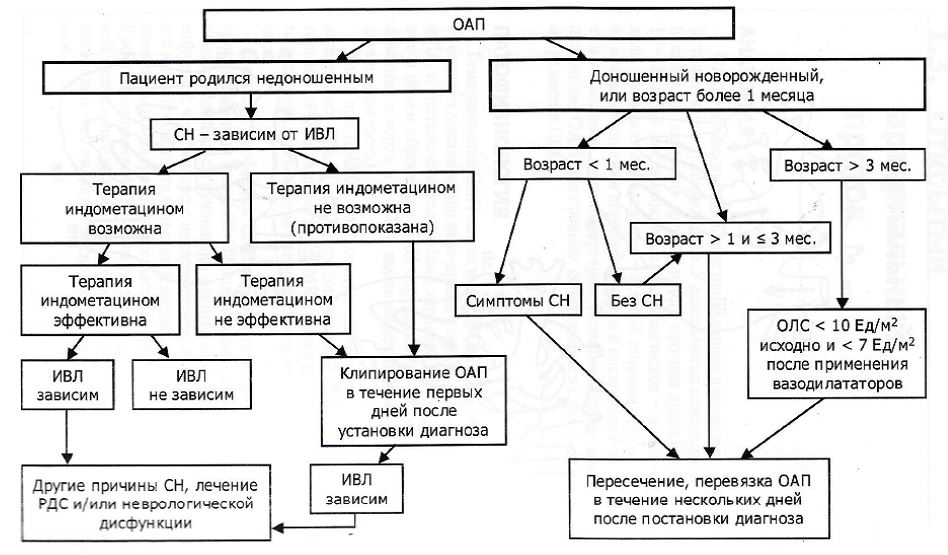 е. постоянно дышащему с помощью аппарата искусственного дыхания, даже проток диаметром 3-4 мм вызывает огромные гемодинамические нарушения. Транспортировка таких деток в кардиохирургический стационар (да и в любой другой) сопряжена с огромным для них риском, и поэтому нередко кардиохирурги выезжают в роддома и стационары, где выхаживаются детки с такой экстремальной низкой массой тела, и там, на месте проводят операцию по устранению протока.
е. постоянно дышащему с помощью аппарата искусственного дыхания, даже проток диаметром 3-4 мм вызывает огромные гемодинамические нарушения. Транспортировка таких деток в кардиохирургический стационар (да и в любой другой) сопряжена с огромным для них риском, и поэтому нередко кардиохирурги выезжают в роддома и стационары, где выхаживаются детки с такой экстремальной низкой массой тела, и там, на месте проводят операцию по устранению протока.
После операции, риск которой практически равен нулю, дети отлично себя чувствуют, и они, и родители быстро забывают неприятный момент их жизни. Перевязка открытого артериального протока — радикальная, т.е. полностью излечивающая операция, и после нее человек практически здоров.
Строго говоря, открытый артериальный проток врожденным пороком сердца не является, т.к. сердце при нем нормально. Он отнесен к этой группе из-за его значения в кровообращении плода и из-за тех нарушений, к которым он может привести при несвоевременном закрытии. В старых, «дохирургических», учебниках указывают, что прожить с этим пороком можно только до 35-40 лет.
В последние годы благодаря появлению нового инструментария и накоплению опыта, открытый артериальный проток все чаще закрывают с применением рентгенохирургической техники. Это производится не в обычной операционной, а в рентгенохирургическом кабинете, и о том, как проходит процедура и подготовка ребенка, вы можете прочитать выше, где описаны катеризация и зондирование сердца.
В данном случае ребенку путем пункции (прокола) артерии на бедре, в самом верху, введут особый катетер с устройством на кончике, которое закроет проток из просвета нисходящей грудной аорты. Процедура занимает 1-1,5 часа и выгодно отличается от операции, при которой все-таки надо открывать грудную клетку путем достаточно большого разреза, оставлять дренаж (трубочку для удаления воздуха и жидкости), которую уберут только на следующий день. Сейчас с помощью различных устройств (спирали, окклюдеры) можно закрыть проток практически любого диаметра и формы. Но операция, даже такая, — это операция, и если ее можно избежать, получив тот же эффект, то так и следует сделать.
Но операция, даже такая, — это операция, и если ее можно избежать, получив тот же эффект, то так и следует сделать.
К слову сказать, операция перевязки открытого артериального протока была впервые сделана в 1938 году, и эта дата считается годом рождения хирургии врожденных пороков сердца.
Открытый артериальный проток
Диагноз
Открытый артериальный (Баталлов) проток с малым сбросом – гемодинамически незначимый. По месту жительства рекомендована операция.
Пациент:
Ребенок, 1 год 6 месяцев, Казахстан
Врач:
Профессор Йоханнес Бройер, главный врач отделения детской кардиологии университетской клиники Бонн
Ответ детского хирурга кардиолога, проф. Йоханнеса Бройер
В соответствии с предоставленными медицинскими заключениями у ребенка обнаружен открытый артериальный проток. Если при этом слышны шумы сердца, то необходимо провести закрытие артериального протока. В заключении сказано, что диаметр протока составляет 2мм, но шумы сердца отсутствуют. Однако при протоке такого размера шумы сердца должны быть слышны. Для установления точного диагноза нам необходимо провести дополнительное обследование.
Вопросы родителей пациента
В случае необходимости хирургического лечения, каким способом вы проводите подобные операции?
Ответ врача
Операция – чрезкожная транслюменальная сосудистая окклюзия, проводится эндоваскулярным способом. С помощью специального катетера вводится и имплантируется спираль, которая закрывает незаращеный артериальный проток. Риск при такой операции практически равен нулю. Длительность пребывания в клиники около 4 дней.
Предварительная стоимость обследования: 350 Евро
Проведенное обследование, оценка состояния, рекомендации
Результат проведенного нами обследования свидетельствует о том, что сердце ребенка имеет нормальную структуру и выполняет все необходимые функции. Обнаружено незаращение крошечного артериального (Баталлова) протока без характерных шумов в сердце. В этом случае показания к хирургическому или интервенционному лечению артериального протока отсутствуют. В настоящий момент никаких дальнейших процедур не требуется. В соответствии с новым протоколом немецкого общества Кардиологов, также нет необходимости в проведении профилактики эндокардита.
Обнаружено незаращение крошечного артериального (Баталлова) протока без характерных шумов в сердце. В этом случае показания к хирургическому или интервенционному лечению артериального протока отсутствуют. В настоящий момент никаких дальнейших процедур не требуется. В соответствии с новым протоколом немецкого общества Кардиологов, также нет необходимости в проведении профилактики эндокардита.
Рекомендован эхокардиографический контроль через 2 года.
Фактическая стоимость обследования: 290 Евро
Открытый артериальный проток — лечение в отделении института Амосова.
Что такое открытый артериальный проток (боталлов проток)?
Боталлов проток (Рис 1, Видео 1) – это сосуд, который в норме функционирует у плода и соединяет два магистральных сосуда сердца – аорту и легочную артерию. Существует он для того, что бы кровь могла обойти мимо легкие, которые у внутриутробно не функционируют. В течение первых дней жизни новорожденного малыша боталлов проток в норме закрывается. Иногда случается, что открытый артериальный проток не закрывается, что приводит к ряду неприятных проблем. Проток, который не закрылся в течение месяца жизни ребенка, считается врожденным пороком сердца.
Естественное течение порока. Или к чему приведет открытый боталов проток?
Дело в том, что этот сосуд все еще соединяет два больших сосуда сердца – аорту и легочную артерию. Давление в аорте намного превышает давление в легочной артерии. Поэтому через открытый артериальный проток с аорты в легкие попадает избыточное количество крови, что сначала приведет к частым бронхолегочным заболеваниям, а при очень больших боталловых протоках – к необратимым изменениям в сосудах легких и неоперабельности. Кроме того, большой боталлов проток значительно увеличивает нагрузку на сердце, особенно на левый желудочек. Поэтому затягивать с лечением этого порока нельзя.
Лечение открытого артериального протока.
В настоящее время не существует такого боталлова протока, который нельзя было бы закрыть нетравматичным эндоваскулярным методом, который позволит избежать разреза, шрамов и длительной реабилитации. Хирургическое лечение этого порока осталось в прошлом, хирурги закрывают боталлов проток только недоношенным детям или в странах, где медицина имеет недостаточное финансирование. Во всех развитых странах Европы и Америки этот порок устраняется исключительно эндоваскулярно в ренгеноперационных. К тому же вероятность осложнений при эндоваскулярном лечении намного меньше.
Хирургическое лечение этого порока осталось в прошлом, хирурги закрывают боталлов проток только недоношенным детям или в странах, где медицина имеет недостаточное финансирование. Во всех развитых странах Европы и Америки этот порок устраняется исключительно эндоваскулярно в ренгеноперационных. К тому же вероятность осложнений при эндоваскулярном лечении намного меньше.
Процедура эндоваскулярного закрытия.
|
Рис 2 – Внешний вид окклюдера
|
|
Рис 3 — Внешний вид спирали
|
При эндоваскулярном закрытии через маленький прокол в бедренные сосуды в сосуды сердца и в боталлов проток заводятся тоненькие трубочки, так называемые катетеры. Используя рентген и контрастное вещество, доктор оценивает размер и форму боталлова протока, после чего он выбирает самое подходящее окклюзирующее (от англ. Occlusion – закупорка) устройство. В качестве таких устройств могут использоваться окклюдеры (рис 2; Видео 1, 2, 3) или спирали (рис 3; Видео 4, 5, 6).
Выбор устройства для закрытия происходит во время операции, и зависит от размера и формы боталлова протока. Как правило, для больших протоков используются окклюдеры, для маленьких — спирали. В течение полугода окклюзирующие устройства полностью обрастают собственными клеточками сердца, происходит, так называемая, эндотелизация. Сброс через боталлов проток в 90% случаев прекращается сразу же после процедуры, в остальных случаях – по окончанию периода эндотелизации устройства.
Реабилитация после процедуры
1. Пациентов выписывают, как правило, на следующий день после процедуры.
2. В течении 6 месяцев рекомендуется проводить антибиотикопрофилактику инфекционного эндокардита.
У нас наибольший в Украине опыт по эндоваскулярному лечению открытых артериальных протоков – более 300 операций. Мы имеем доступ к оборудованию для закрытия боталлового протока любого размера и формы.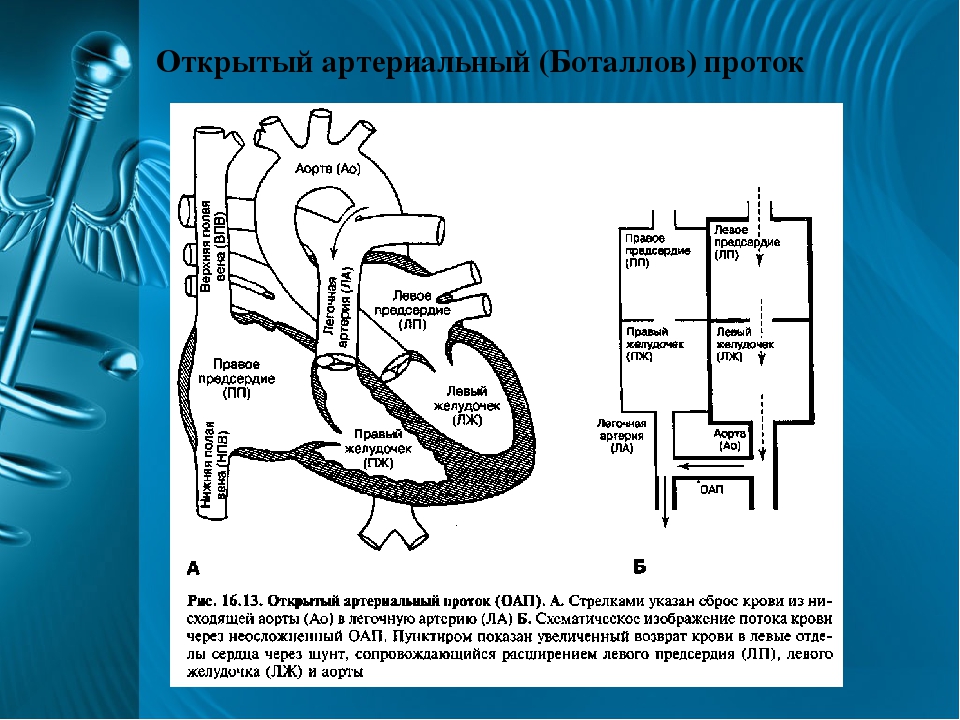 Также, специализируемся на лечении дефектов межпредсердной и межжелудочковой перегородок. Для того чтобы попасть к нам на консультацию или госпитализироваться позвоните по одному из телефонов или запишитесь на прием онлайн.
Также, специализируемся на лечении дефектов межпредсердной и межжелудочковой перегородок. Для того чтобы попасть к нам на консультацию или госпитализироваться позвоните по одному из телефонов или запишитесь на прием онлайн.
Врач поставил Вашему ребенку диагноз
Если вашему ребенку поставили диагноз врожденный порок сердца, не стоит опускать руки, нужно узнать все способы поддержания здоровья таких детей, а также причины развития данного заболевания, пройти необходимое обследование, чтобы врач назначил соответствующее лечение.
Сердце человека состоит из четырех камер: правое предсердие (ПП) и правый желудочек (ПЖ), левое предсердие (ЛП) и левый желудочек (ЛЖ). Правые и левые отделы сердца между собой никак не сообщаются. В этом нет необходимости, так как они обеспечивают движение крови каждый по своему кругу. Левые отделы сердца отвечают за движение крови по большому кругу кровообращения. Из левого предсердия через левый желудочек в аорту (Ао) поступает артериальная кровь, богатая кислородом. Из аорты по многочисленным артериям, а потом и по капиллярам она разносится по всему организму, доставляя клеткам кислород. В свою очередь, «отработанная» организмом венозная кровь собирается в мелкие вены, которые сливаются в более крупные венозные сосуды – верхнюю и нижнюю полые вены (ВПВ и НПВ). Конечная точка путешествия венозной крови – правое предсердие. Оттуда через правый желудочек кровь попадает в легочную артерию (ЛА). Малый круг кровообращения проходит через легкие, где венозная кровь обогащается кислородом и вновь становится артериальной. Отток обновленной крови осуществляется по легочным венам (ЛВ), впадающим, в свою очередь, в левое предсердие.
Особенности кровообращения у плода и новорожденного
Находясь в утробе матери, плод не дышит самостоятельно и его легкие не функционируют. Кровообращение осуществляется через плаценту. Насыщенная кислородом кровь матери поступает к плоду через пуповину: в венозный проток, откуда через систему сосудов в правое предсердие. У плода между правым и левым предсердием имеется отверстие – овальное окно. Через него кровь попадает в левое предсердие, затем в левый желудочек, аорту – и ко всем органам плода. Малый круг кровообращения отключен. В легкие плода кровь поступает через артериальный проток – соединение между аортой и легочной артерией. Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями».
У плода между правым и левым предсердием имеется отверстие – овальное окно. Через него кровь попадает в левое предсердие, затем в левый желудочек, аорту – и ко всем органам плода. Малый круг кровообращения отключен. В легкие плода кровь поступает через артериальный проток – соединение между аортой и легочной артерией. Венозный проток, овальное окно и артериальный проток имеются только у плода. Они называются «фетальными сообщениями».
Когда ребенок рождается и пуповину перевязывают, схема кровообращения радикально изменяется. С первым вдохом ребенка его легкие расправляются, давление в сосудах легких снижается, кровь притекает в легкие. Малый круг кровообращения начинает функционировать. Фетальные сообщения больше не нужны ребенку и постепенно закрываются (венозный проток – в течение первого месяца, артериальный проток и овальное окно – через два-три месяца). В некоторых случаях своевременного закрытия не происходит, тогда у ребенка диагностируют врожденный порок сердца (ВПС).
Иногда при развитии плода возникает аномалия и ребенок рождается с анатомически измененными структурами сердца, что также считается врожденным пороком сердца. Из 1000 детей с врожденными пороками рождается 8-10, и эта цифра увеличивается в последние годы (развитие и совершенствование диагностики позволяет врачам чаще и точнее распознавать пороки сердца, в том числе, когда ребенок еще в утробе матери).
«Синие» и «бледные» пороки сердца
Аномалии могут быть очень разнообразными, наиболее часто встречающиеся имеют названия и объединяются в группы. Например, пороки разделяют на «синие» (при которых кожные покровы ребенка синюшные, «цианотичные») и «бледные» (кожные покровы бледные). Для жизни и развития ребенка более опасны «синие» пороки, при которых насыщение крови кислородом очень низкое. К «синим» порокам относятся Тетрада Фалло, транспозиция магистральных сосудов, атрезия легочной артерии. К «бледным» порокам относятся дефекты перегородок – межпредсердной, межжелудочковой.
В некоторых случаях порок может частично компенсироваться за счет открытого артериального протока (в норме он закрывается, как только легкие ребенка расправляются с первым криком). Также у ребенка может недоразвиться клапан сердца – сформируется клапанный порок (наиболее часто, аортальный клапан или клапан легочной артерии).
Причины развития врожденного порока сердца
У плода формирование структур сердца происходит в первом триместре, на 2-8 неделе беременности. В этот период развиваются пороки, которые являются следствием наследственных генетических причин или воздействия неблагоприятных внешних факторов (например, инфекция или отравления). Иногда у ребенка имеется несколько пороков развития, в том числе и порок сердца.
Риск рождения ребенка с врожденным пороком сердца очень высок, если:
— ранее у женщины были выкидыши или мертворожденные
— возраст женщины более 35 лет
— женщина во время беременности принимает алкоголь, психоактивные вещества (наркотики), курит
— в семье женщины есть история рождения детей с пороками или мертворождения
— женщина живет в экологически неблагоприятной местности (радиация, отравляющие вещества)
или работает на экологически неблагоприятном производстве
— во время беременности (особенно первые 2 месяца) женщина перенесла инфекционные, вирусные заболевания
— женщина принимала во время беременности лекарственные препараты
с тератогенным эффектом (приводящие к развитию уродств у плода) или
эндокринные препараты для сохранения беременности (гормоны).
Можно ли поставить диагноз ВПС у плода?
Возможность выявить у плода врожденный порок сердца существует, хотя ее нельзя назвать абсолютно информативной. Это зависит от многих причин, основные их которых — наличие высококлассной аппаратуры и квалифицированного специалиста, имеющего опыт перинатальной диагностики. Диагностика возможна начиная с 14-й недели беременности. Если при обследовании у плода выявляется аномалия развития, родителям сообщают о тяжести патологических изменений, возможностях лечения и о том, насколько будет ребенок жизнеспособен. Женщина может принять решение о прерывании беременности. Если есть надежда на успешные роды и лечение, женщина наблюдается у специалиста, роды принимают в специализированном роддоме (чаще всего женщине предлагают кесарево сечение).
Если при обследовании у плода выявляется аномалия развития, родителям сообщают о тяжести патологических изменений, возможностях лечения и о том, насколько будет ребенок жизнеспособен. Женщина может принять решение о прерывании беременности. Если есть надежда на успешные роды и лечение, женщина наблюдается у специалиста, роды принимают в специализированном роддоме (чаще всего женщине предлагают кесарево сечение).
Врожденный порок сердца у новорожденных
При рождении ребенка или в первые дни его жизни врачи могут заподозрить врожденный порок сердца.
На чем они основывают свои предположения?
— Шум в сердце. В первые несколько дней жизни ребенка шум в сердце нельзя расценивать как достоверный симптом врожденного порока сердца. Такого ребенка наблюдают, при сохранении шумов более 4-5 суток – обследуют. Само появление сердечного шума объясняется нарушением тока крови через сосуды и полости сердца (например, при наличии аномальных сужений, отверстий, резкой смены направления кровотока).
— синюшность кожных покровов (цианоз). В норме артериальная кровь богата кислородом и придает коже розовую окраску. Когда к артериальной крови примешивается бедная кислородом венозная кровь (в норме не происходит), кожа приобретает синюшный оттенок. В зависимости от типа порока цианоз может быть разной степени выраженности. Однако, врачам приходится уточнять причины цианоза, так как он может быть симптомом болезней органов дыхания и центральной нервной системы.
— проявления сердечной недостаточности. Сердце перекачивает кровь, работая как насос. Когда снижается насосная способность сердца, кровь начинает застаиваться в венозном русле, питание органов артериальной кровью снижается. Учащаются сердечные сокращения и дыхание, появляется увеличение печени и отечность, быстрая утомляемость и одышка. К сожалению, эти признаки очень трудно распознать у новорожденных. Высокая частота сердечных сокращений и дыхания наблюдается у маленьких детей в нормальном состоянии. Только при значительных отклонениях можно с достаточной уверенностью говорить о развитии у малыша сердечной недостаточности. Часто следствием развития сердечной недостаточности является спазм периферических сосудов, что проявляется похолоданием конечностей и кончика носа, их побледнением. Эти признаки помогают косвенно судить о недостаточности сердца.
Только при значительных отклонениях можно с достаточной уверенностью говорить о развитии у малыша сердечной недостаточности. Часто следствием развития сердечной недостаточности является спазм периферических сосудов, что проявляется похолоданием конечностей и кончика носа, их побледнением. Эти признаки помогают косвенно судить о недостаточности сердца.
— нарушения электрической функции сердца (сердечного ритма и проводимости), проявляющиеся аритмиями и, иногда, потерей сознания. Врач может услышать неровное сердцебиение при аускультации (выслушивании фонендоскопом) или увидеть на записи электрокардиограммы.
Как сами родители могут заподозрить у ребенка врожденный порок сердца?
Если порок сердца приводит к серьезным нарушениям гемодинамики (кровотока), как правило, его диагностируют уже в роддоме. При отсутствии выраженных проявлений ребенка могут выписать домой. Родители могут заметить, что малыш вялый, плохо сосет и часто срыгивает, во время кормления и при крике — синеет. Может проявиться выраженная тахикардия (частота сердечных сокращений выше 150 ударов в минуту). В этом случае нужно обязательно сообщить о жалобах педиатру и пройти специальные обследования.
Подтверждение диагноза врожденного порока сердца
В настоящее время наиболее доступным, простым, безболезненным для ребенка и высокоинформативным методом диагностики пороков сердца является эхокардиография. Во время исследования с помощью ультразвукового датчика врач видит толщину стенок, размеры камер сердца, состояние клапанной системы и расположение крупных сосудов. Допплеровский датчик позволяет увидеть направления кровотока и измерить его скорость. Во время исследования можно выполнить снимки, подтверждающие заключение специалиста.
Также ребенку обязательно запишут электрокардиограмму. При необходимости более точного исследования (как правило, для определения тактики хирургического лечения порока) врач порекомендует зондирование сердца. Это инвазивная методика, для выполнения которой ребенок госпитализируется в стационар. Зондирование проводится врачем-рентгенхирургом в рентгеноперационной, в присутствии врача-анестезиолога, под внутривенным наркозом. Через прокол в вене или артерии специальные катетеры вводятся в сердце и магистральные сосуды, позволяя точно измерить давление в полостях сердца, аорте, легочной артерии. Введение специального рентген-контрастного препарата позволяет получить точное изображение внутреннего строения сердца и крупных сосудов (см. рисунок).
Диагноз – не приговор. Лечение ВПС (врожденного порока сердца)
Современная медицина позволяет не только своевременно диагностировать, но и лечить врожденные пороки сердца. Лечением ВПС занимаются кардиохирурги. При выявлении порока, сопровождающегося серьезным нарушением гемодинамики, влияющего на развитие ребенка и угрожающего жизни малыша, операция проводиться как можно раньше, иногда в первые дни жизни ребенка. При пороках, которые не влияют значительно на рост и развитие ребенка, операция может проводиться позже. Выбор сроков операции определяется хирургом. Если ребенку рекомендовали хирургическое вмешательство и его не удалось выполнить своевременно (часто из-за отказа родителей, непонимания серьезности проблемы), у ребенка может начаться патологическое изменение гемодинамики, приводящее к развитию и прогрессированию сердечной недостаточности. На определенном этапе изменения становятся необратимыми, операция уже не поможет.
Отнеситесь внимательно к советам и рекомендациям врачей, не лишайте своего ребенка возможности расти и развиваться, не быть инвалидом на всю жизнь!
Операция при врожденных пороках сердца
Многие годы операции при врожденных пороках сердца выполнялись только на открытом сердце, с использованием аппарата искусственного кровообращения (АИК), который берет на себя функции сердца во время его остановки. Сегодня при некоторых пороках такой операции существует альтернатива – устранение дефекта структур сердца с помощью системы AMPLATZER.
Такие операции значительно безопаснее, не требуют раскрытия грудной клетки, не отличаясь по эффективности от «большой» хирургии.
Если операция выполнена своевременно и успешно, ребенок полноценно развивается и растет, и часто – навсегда забывает о существовании порока. После операции обязательным является наблюдение педиатра, контрольные эхокардиографические исследования. Дети с врожденными пороками сердца часто болеют простудными заболеваниями из-за снижения иммунитета, поэтому в послеоперационном периоде проводится общеукрепляющее лечение и ограничиваются физические нагрузки. В дальнейшем у многих детей эти ограничения снимают и даже разрешают посещать спортивные секции.
Если Вы считаете, что у Вашего ребенка есть проблемы с сердцем, то Вы можете пройти эхокардиографическое исследование и обратиться за консультацией к детскому кардиологу.
Статья была опубликована сотрудниками нашего Центра ранее на «Сибирском медицинском портале».
Эндоваскулярное закрытие открытого артериального протока с помощью окклюдера
Закарян Н.В., Панков А.С.
Введение
Открытый артериальный проток (ОАП) – это врождённый порок сердца (ВПС), характеризующийся наличием аномального сосудистого сообщения между аортой и лёгочной артерией
Во внутриутробном периоде ОАП есть у всех, это нормальный компонент кровообращения плода. После первого вдоха родившегося ребенка лёгочные сосуды раскрываются, давление в правом желудочке падает, ОАП постепенно перестает функционировать и закрывается (облитерируется). Облитерация протока происходит в различные сроки. У 1/3 детей он закрывается к двум неделям, у остальных – в течение восьми недель жизни.
Нарушения гемодинамики связаны с аномальным сбросом крови из аорты в лёгочную артерию, так как давление в аорте гораздо выше, чем в лёгочной артерии.
Объём сбрасываемой крови зависит от размеров протока. В результате нарушений кровообращения в большой круг кровообращения поступает меньший, чем положено, объём крови, от чего страдают жизненно важные органы (мозг, почки), скелетная мускулатура. Проходя через сосуды лёгких, эта кровь возвращается в левое предсердие, левый желудочек, которые, испытывая чрезмерную нагрузку, увеличиваются в размерах (гипертрофируются), затем под влиянием всё возрастающего объёма перенасыщенной кислородом крови происходят изменения сосудов лёгких и возникает лёгочная гипертензия.
Проявления и естественное течение порока
Дети рождаются с нормальной массой и длиной тела. Дальнейшие проявления заболевания связаны с размерами протока. Чем короче и шире ОАП, тем больший объём крови сбрасывается по нему и тем более выражена клиника заболевания. При узких и длинных ОАП больные дети ничем не отличаются от здоровых. Единственным признаком, указывающим на наличие ВПС, является шум, выслушиваемый врачом-педиатром над областью сердца. При широких и узких ОАП уже в первые месяцы и даже дни жизни ребенка могут обнаруживаться все симптомы (проявления) порока. У таких детей наблюдается постоянная бледность, при физической нагрузке (натуживание, сосание, крик) отмечается преходящий цианоз (синий оттенок кожи) преимущественно на ногах. Дети отстают в физическом развитии. У них отмечается склонность к повторяющимся бронхитам, пневмониям.
Наиболее тяжёлыми периодами в течении порока являются фаза адаптации в период новорождённости и фаза терминальной лёгочной гипертензии у детей старшего возраста. В эти периоды дети погибают от сердечной недостаточности, нарушений мозгового кровообращения (инсульт), пневмоний, инфекционного эндокардита. Средняя продолжительность жизни при ОАП без оперативного лечения – 25 лет, хотя многие больные при узком и длинном ОАП доживают до пожилого возраста. Если у взрослого пациента с ОАП развиваются признаки декомпенсации кровообращения — также рекомендовано выполнение операции по закрытию протока.
Лечение
Существует два метода лечения ОАП: консервативный, или медикаментозный, и оперативный. Медикаментозное лечение ОАП применяется только в родильном доме у новорождённых в течение двух первых недель жизни, позже оно становится неэффективным. Данный метод далеко не всегда результативен, имеет много противопоказаний, поэтому основным лечением является механическое закрытие протока.
Раньше наиболее распространённым вмешательством была перевязка протока после торакотомии. Сейчас операция перевязки ОАП выполняется очень редко. На ведущие роли вышла эндоваскулярная окклюзия ОАП. Суть вмешательства заключается в окклюзии (закрытии) протока специально изготовленными спиралями и окклюдерами. Методика почти не имеет осложнений, выполняется маленьким детям под наркозом, а подросткам и взрослым – под местной анестезией. Доступ осуществляется пункционным путем, через бедренную артерию. Эффективность операции почти стопроцентная, изредка наблюдается реканализация ОАП, которая впоследствии устраняется таким же образом. При широких и коротких ОАП, когда эндоваскулярная окклюзия ОАП спиралями технически невозможна, применяется закрытие ОАП с помощью специально разработанных окклюдеров, которые также доставляются через бедренную артерию.
Описание клинического случая.
Больная С, 67 лет, поступила в стационарное отделение скорой медицинской помощи 18.09.2017 г. с диагнозом: Врожденный порок сердца: открытый артериальный проток (диаметр 4мм, длина 13 мм). При поступлении предъявляет жалобы на слабость и одышку при ходьбе. В анамнезе ГБ с максимальным повышением АД до 200/100 мм.рт.ст., адаптирована к 140/80 мм.рт.ст. Принимает конкор, амлодипин, торвакард. В течение года отмечает появление одышки при ходьбе. При обследовании по данным ЭХО КГ обнаружен ВПС: открытый артериальный проток, признаки умеренной легочной гипертензии. По данным МСКТ диаметр артериального протока составил 4 мм.
Учитывая ухудшение самочуствия и появление легочной гипертензии, принято решение о выполнении транскатетерного закрытия ОАП.
Описание операции (22.09.2017)
Под местной анестезией пунктированы правые общая бедренная артерия и общая бедренная вена. Диагностический катетер проведен в грудой отдел аорты. Выполнена ангиография, визуализируется открытый артериальный проток, соединяющий аорту и легочную артерию. Далее через интродъюсер в правой ОБВ по проводнику через артериальный проток в нисходящую часть аорты заведен катетер. Катетер заменен на доставляющее устройство окклюдера. Выполнена имплантация окклюдера «Amplatzer Duct Occluder» с расположением дистального диска окклюдера со стороны аорты, проксимального — со стороны легочной артерии. На контрольной ангиографии позиция окклюдера в артериальном протоке оптимальна, отмечается редукция кровотока по артериальному протоку. Получен хороший ангиографический результат.
На следующий день пациентка выписана из стационара в удовлетворительном состоянии.
Статья добавлена 9 октября 2017 г.
Патентный артериальный проток (КПК)
Когда бывает КПК?
КПК может случиться с любым здоровым ребенком, но КПК может быть более распространенным в:
- Недоношенные (слишком рано родившиеся дети).
- Девочки (КПК в два раза чаще встречается у девочек, чем у мальчиков).
- Младенцы с другими генетическими заболеваниями, такими как синдром Дауна.
- Младенцы, матери которых заболели краснухой во время беременности.
Признаки и симптомы
Шум в сердце (дополнительный или необычный звук, слышимый во время сердцебиения) может быть единственным признаком того, что у ребенка есть КПК.Другие признаки или симптомы, по которым сердце работает слишком тяжело:
- Учащенное дыхание, тяжелая работа, чтобы дышать, или одышка.
- Низкий уровень кислорода у недоношенных детей. Для этого может потребоваться кислородная или искусственная вентиляция легких.
- Плохо питается.
- Плохая прибавка в весе.
- Легко устаю.
- Потливость во время кормления.
Диагностика
У доношенных новорожденных врач сначала ищет КПК, услышав шум в сердце при осмотре.Обычно врач просит детского кардиолога (детского кардиолога) провести обследование. Недоношенные дети могут не иметь тех же признаков КПК, что и доношенные. Врачи могут искать КПК у младенцев, у которых возникают проблемы с дыханием вскоре после рождения.
Для диагностики КПК используются два безвредных и безболезненных теста:
- Эхокардиограмма. В этом тесте используются звуковые волны, чтобы создать движущуюся картину сердца и основных кровеносных сосудов вашего ребенка и того, как кровь течет по ним.Тест позволяет врачу увидеть любые проблемы, связанные с формированием сердца и его работой. Этот тест позволит диагностировать проблему и проследить ее с течением времени. Он показывает, насколько велик КПК и насколько хорошо с ним работает сердце.
- ЭКГ (электрокардиограмма). Этот тест регистрирует электрическую активность сердца. Он может показать, насколько велики камеры сердца, и любые другие небольшие изменения, которые могут быть признаками ОАП.
Лечение
Иногда КПК сжимается и полностью уходит без лечения.В других случаях может потребоваться лечение, чтобы закрыть отверстие. Лечение может отличаться в зависимости от проблем и возраста вашего ребенка. Врач вашего ребенка обсудит с вами варианты лечения и поможет принять решение. Доктор может обсудить 3 варианта лечения:
- Медицина
- Катетерная процедура
- Хирургия
Если ваш ребенок родился с определенными типами сердечных заболеваний, при которых КПК должен оставаться открытым, можно использовать лекарства, чтобы КПК оставался открытым до тех пор, пока не будет сделана операция по исправлению порока сердца.
Лекарства
- Индометацин (in doh METH ah sin) — это лекарство, которое помогает закрыть КПК у недоношенных детей, поскольку оно заставляет КПК сжиматься (сжиматься), закрывая отверстие. Обычно это не помогает доношенным младенцам.
- Ибупрофен (EYE boo pro fen) — это лекарство, подобное индометацину. Его часто используют для закрытия КПК у недоношенных детей.
- Если КПК маленький, врач может не сразу его лечить.
- В некоторых случаях будут назначены антибиотики, чтобы предотвратить инфекцию сердца, пока КПК не будет закрыт.Этот вид инфекции называется эндокардитом.
Катетерная процедура
- Процедура называется катетеризацией сердца (KATH i ter i ZA shun).
- Эта процедура является наиболее распространенным способом закрытия артериального протока и может проводиться для детей старшего возраста и пациентов. Вашему ребенку дадут лекарство, чтобы он заснул, и он не будет чувствовать боли или дискомфорта.
- Врач вставит длинную тонкую трубку, называемую катетером, в большой кровеносный сосуд в верхней части бедра (пах).Врач будет использовать камеры для перемещения катетера из паха в артериальный проток. Во время процедуры грудную клетку вашего ребенка открывать не нужно.
- Маленькая металлическая спираль или другое блокирующее устройство пропускается через катетер и помещается в артериальный проток. Это устройство заблокирует кровоток по сосуду.
- Проблемы с этой процедурой случаются нечасто. Если они действительно случаются, то длятся недолго и могут включать кровотечение, инфекцию и перемещение устройства.
Хирургия
- Операция не может быть сделана до достижения 6-месячного возраста младенцам, у которых нет проблем со здоровьем из-за КПК.
- Вашему ребенку дадут лекарство, чтобы он заснул. Он или она не будет чувствовать боли во время операции.
- Хирург сделает небольшой разрез между ребрами вашего ребенка, чтобы достать КПК. КПК закрывается швами или зажимами.
- Проблемы с этой процедурой случаются нечасто. Если они действительно случаются, то длятся недолго и могут включать охриплость голоса, инфекцию, кровотечение или образование жидкости вокруг легких.Ребенку может понадобиться аппарат, чтобы на короткое время помочь ему дышать, но это случается редко.
- Операция на КПК может быть выполнена, если катетерная процедура не работает или невозможна. Это также может быть сделано, если ребенку уже запланирована операция по поводу других проблем с сердцем.
После операции
- Ваш ребенок будет находиться в больнице несколько дней. Большинство детей отправляются домой через 2 дня после операции.
- Выдадут лекарства от боли или беспокойства.Если вы считаете, что ваш ребенок испытывает боль или дискомфорт дома, поговорите с врачом или медсестрой о том, что можно сделать от боли.
- Врачи и медсестры в больнице научат вас ухаживать за ребенком дома. Вы также узнаете, как давать ребенку лекарство в случае необходимости.
- Нормальная повседневная активность разрешена. Однако ваш ребенок не может заниматься контактными видами спорта, пока врач не разрешит ему это.
- Запланированы повторные визиты к врачам вашего ребенка.
- Долгосрочные проблемы после операции случаются нечасто. Врач расскажет вам об этих возможных проблемах.
Жизнь с КПК
- Если ваш ребенок родился доношенным и не имел других проблем с сердцем, вполне вероятно, что он или она будет жить здоровой и нормальной жизнью после лечения КПК.
- Если ваш ребенок родился недоношенным, жизнь после лечения КПК зависит от других факторов. Это включает в себя то, как рано родился ребенок, есть ли у ребенка другие проблемы, и уровень необходимого ухода.
- Все дети с открытым ОАП имеют более высокий риск заражения сердца, называемого бактериальным эндокардитом. Вашему ребенку потребуются антибиотики перед любой стоматологической работой и определенными процедурами для предотвращения этой инфекции. Важно заботиться о зубах вашего ребенка, чтобы предотвратить кариес и инфекцию.
- После закрытия КПК вашему ребенку не потребуются антибиотики перед стоматологической работой или хирургическими вмешательствами. Если КПК закрыт хирургическим вмешательством или катетером и остается полностью закрытым, антибиотики потребуются только в течение 6 месяцев после операции.
- Если у вас есть вопросы, спросите своего врача или медсестру.
Патентный артериальный проток (PDF)
HH-I-274 12/14 Copyright 2014, Национальная детская больница
Патентный артериальный проток (КПК) | Американская кардиологическая ассоциация
Что это?
Незакрытое отверстие в аорте.
Перед рождением ребенка кровь плода не должна попадать в легкие для насыщения кислородом. Артериальный проток — это отверстие, через которое кровь не попадает в легкие.Однако, когда ребенок рождается, кровь должна получать кислород в легких, и это отверстие должно закрываться. Если артериальный проток все еще открыт (или открыт), кровь может пропустить этот необходимый этап циркуляции. Открытое отверстие называется открытым артериальным протоком.
Дополнительная информация для родителей детей с КПК
Что вызывает это?
Артериальный проток — это нормальная артерия плода, соединяющая основную артерию тела (аорту) и главную легочную артерию (легочную артерию).Проток позволяет крови отводиться от легких до рождения.
Каждый ребенок рождается с артериальным протоком. После родов отверстие больше не нужно, и оно обычно сужается и закрывается в течение первых нескольких дней.
Иногда проток не закрывается после рождения. Отсутствие закрытия протока часто встречается у недоношенных детей, но редко у доношенных детей. У большинства детей причина КПК неизвестна. У некоторых детей наряду с КПК могут быть и другие пороки сердца.
Как это влияет на сердце?
Обычно левая сторона сердца перекачивает кровь только к телу, а правая сторона только перекачивает кровь к легким.У ребенка с ОАП лишняя кровь перекачивается из артерии тела (аорты) в легочные (легочные) артерии. Если ОАП большой, дополнительная кровь, закачиваемая в легочные артерии, заставляет сердце и легкие работать тяжелее, и легкие могут быть перегружены.
Как КПК влияет на моего ребенка?
Если КПК маленький, он не вызовет симптомов, потому что сердце и легкие не должны работать интенсивнее. Единственным отклонением от нормы может быть характерный шум (шум, слышимый с помощью стетоскопа).
Если КПК большой, ребенок может дышать быстрее и тяжелее, чем обычно. У младенцев могут быть проблемы с кормлением и нормальным ростом. Симптомы могут проявиться только через несколько недель после рождения. В кровеносных сосудах легких может возникнуть высокое давление, потому что туда перекачивается больше крови, чем обычно. Со временем это может привести к необратимому повреждению кровеносных сосудов легких.
Что можно сделать с КПК?
Если ОАП (проток) маленький, это не заставляет сердце и легкие работать тяжелее.Хирургия и другие виды лечения могут не понадобиться. Маленькие КПК часто закрываются сами по себе в течение первых нескольких месяцев жизни.
У большинства детей КПК можно закрыть, вставив катетеры (длинные тонкие трубки) в кровеносные сосуды на ноге, чтобы добраться до сердца и КПК, а катетер или другое устройство можно ввести через катетеры в КПК, как заглушку. На рисунке ниже слева показан один из примеров использования катетеризации для закрытия протока. Если необходимо хирургическое вмешательство, делается разрез на левой стороне груди между ребрами.Проток закрывают, связывая его швом (нитевидным материалом) или постоянно помещая небольшой металлический зажим вокруг протока, чтобы сжать его. Если других пороков сердца нет, кровообращение у ребенка восстанавливается. У недоношенных новорожденных лекарство часто помогает закрыть проток. После первых нескольких недель жизни лекарства для закрытия протока перестают работать, и может потребоваться операция.
Чем может заниматься мой ребенок?
Если КПК маленький или если он был закрыт катетеризацией или хирургическим вмешательством, вашему ребенку могут не потребоваться какие-либо особые меры предосторожности в отношении физической активности и он сможет участвовать в обычных занятиях без повышенного риска.
Что касается последующего наблюдения в будущем, в зависимости от типа закрытия КПК детский кардиолог вашего ребенка может периодически осматривать его, чтобы искать необычные проблемы. Долгосрочная перспектива отличная, и обычно не требуются никакие лекарства, дополнительная операция или катетеризация.
Идентификационный лист врожденного порока сердца
Дополнительная информация для взрослых с КПК
Что вызывает это?
Артериальный проток — это нормальная артерия плода, соединяющая основную артерию тела (аорту) и главную легочную артерию (легочную артерию).Проток позволяет крови отводиться от легких до рождения.
Каждый ребенок рождается с артериальным протоком. После рождения отверстие больше не нужно, и обычно оно сужается и закрывается в течение первых нескольких дней жизни.
Иногда проток не закрывается после рождения. Невозможность закрытия протока часто встречается у недоношенных детей, но редко у доношенных детей, и причина обычно не известна. У некоторых пациентов наряду с КПК могут быть и другие пороки сердца.
Как это влияет на сердце?
Обычно левая сторона сердца перекачивает кровь только к телу, а правая сторона только перекачивает кровь к легким.У человека с ОАП лишняя кровь перекачивается из артерии тела (аорты) в легкие (легочные) артерии. Если ОАП большой, дополнительная кровь, закачиваемая в легочные артерии, заставляет сердце и легкие работать тяжелее, и легкие могут быть перегружены.
Как на меня влияет КПК?
Если КПК маленький, он не вызовет симптомов или проблем, потому что кровоток и давление в сердце и легких существенно не изменятся по сравнению с нормальными. Единственным отклонением от нормы может быть характерный шум (шум, слышимый с помощью стетоскопа), иногда называемый «машинным» шумом.
Если КПК большой, одышка может быть связана с нарушением функции сердца или проблемами, связанными с высоким давлением в легких. В сосудах легких может возникнуть высокое давление, потому что туда перекачивается больше крови, чем обычно. Со временем это может вызвать необратимое повреждение кровеносных сосудов легких (легочная гипертензия).
Что делать, если дефект все еще присутствует? Стоит ли его ремонтировать в зрелом возрасте?
Если КПК маленький, его не нужно закрывать, потому что это не заставляет сердце и легкие работать тяжелее.
У пациентов с ОАП среднего или большого размера могут развиться проблемы, связанные с усилением кровотока в легких. У этих пациентов может быть улучшение, если КПК закрыт. Закрытие КПК теперь обычно можно выполнить путем размещения катетерной катетеры или введения другого устройства для устранения аномального обмена данными (так называемая интервенционная или терапевтическая катетеризация (PDF)).
Хирургия может быть лучшим вариантом лечения для некоторых пациентов. Хирургу не нужно открывать сердце, чтобы исправить КПК.На левой стороне груди между ребрами делается разрез. КПК закрывается путем завязывания его швом (нитевидным материалом) или путем постоянного размещения небольшого металлического зажима вокруг КПК, чтобы сжать его. Иногда у взрослых используется хирургический пластырь. Если нет другого порока сердца, это восстанавливает нормальное кровообращение.
Если у меня еще есть КПК, что я могу делать?
Если КПК небольшой или если КПК был закрыт катетеризацией или хирургическим вмешательством, вам могут не потребоваться какие-либо особые ограничения, и вы сможете участвовать в обычных занятиях без повышенного риска.
Пациентам с умеренным или большим ОАП и пациентам с легочной гипертензией может потребоваться ограничение активности. Им следует обсудить это со своим кардиологом.
Текущее обслуживание
Что мне понадобится в будущем?
В зависимости от типа закрытия КПК ваш кардиолог может периодически осматривать его, чтобы искать необычные проблемы. Долгосрочная перспектива отличная, и обычно не требуются никакие лекарства, дополнительная операция или катетеризация.
Медицинское наблюдение
Пациентам с маленьким ОАП необходимо периодическое наблюдение у кардиолога.Пациенты с успешно закрытым КПК редко нуждаются в длительном кардиологическом наблюдении, если нет других сердечных заболеваний. Лишь в редких случаях им нужно будет принимать лекарства после хирургического вмешательства или закрытия устройства. При необходимости ваш кардиолог может контролировать вас с помощью неинвазивных тестов.
Ограничения деятельности
Большинство пациентов с небольшим неповрежденным КПК или восстановленным КПК не нуждаются в каких-либо специальных мерах предосторожности и могут заниматься обычной деятельностью без повышенного риска. После операции или закрытия катетера ваш кардиолог может посоветовать некоторые ограничения вашей физической активности на короткое время, даже если легочной гипертензии нет.
Ограничение физических упражнений рекомендуется пациентам с легочной гипертензией, связанной с КПК.
Профилактика эндокардита
Профилактика эндокардита обычно не требуется более чем через шесть месяцев после закрытия КПК. Тем не менее, профилактика эндокардита рекомендуется пациентам с ОАП с эндокардитом в анамнезе, пациентам с тканевым протезом клапана, а также для неоперированных ОАП с легочной гипертензией и цианозом. См. Дополнительную информацию в разделе об эндокардите.
Беременность
Если нет легочной гипертензии или признаков сердечной недостаточности, у пациенток с КПК риск беременности низкий.
Вам понадобится дополнительная операция?
После закрытия КПК маловероятно, что потребуется дополнительная операция. В редких случаях у пациента может быть остаточное отверстие. Потребуется ли его закрывать, зависит от его размера.
Патентный артериальный проток | Детская больница CS Mott
Что такое открытый артериальный проток?
Открытый артериальный проток (PDA) возникает, когда кровеносный сосуд в норме, когда ребенок в утробе матери не может закрыться после рождения ребенка.Причина проблемы неизвестна, и она поражает одного из 2000 новорожденных ежегодно. Это чаще встречается у девочек и гораздо чаще у недоношенных детей. Это может произойти у детей с нормальным сердцем и обычно возникает в связи со сложными пороками сердца, такими как синдром гипоплазии левых отделов сердца, транспозиция магистральных артерий, коарктация аорты и атрезия легких. Информация на этой странице в первую очередь относится к пациентам с открытым артериальным протоком и здоровым сердцем.
Пока ребенок находится в утробе матери, мать обеспечивает кислородом, а легкие ребенка наполнены жидкостью. Кровоток в это время обходит легкие через кровеносный сосуд, соединяющий легочную артерию (1) с аортой (2). Этот кровеносный сосуд называется артериальным протоком (3). Когда он остается открытым после рождения, он называется открытым артериальным протоком. У большинства младенцев он остается открытым в течение короткого периода времени после рождения, но 90% закрывается к 8-недельному возрасту. Большинство остальных закроются в течение первого года жизни.
Пока ребенок находится в утробе матери, жидкость в легких вызывает высокое давление, поэтому кровь, попадающая в легочную артерию, идет по пути наименьшего сопротивления, минуя легкие и вытекает в аорту через артериальный проток. После рождения легкие наполняются кислородом, поэтому давление в легких и легочной артерии снижается. При этом зажимается пуповина и давление в аорте увеличивается. В результате давление в легочной артерии ниже, чем давление в аорте, поэтому часть крови в аорте течет через проток обратно в легкие.Это приводит к дополнительному притоку крови к легким. Если проток небольшой, дополнительный кровоток минимален, но если проток большой, может быть большое количество крови, возвращающееся в легкие, что приведет к значительному увеличению нагрузки на сердце.
Как эта проблема влияет на здоровье моего ребенка?
Эффекты открытого артериального протока в значительной степени зависят от размера протока. Младенцы, рожденные очень недоношенными, более чувствительны к внелегочному кровотоку, поэтому у них больше шансов иметь сердечные симптомы.Если дополнительный кровоток слишком сильно нагружает сердце, развиваются симптомы застойной сердечной недостаточности. Это не редкость у недоношенных детей, но довольно редко у доношенных детей или детей старшего возраста. Симптомы застойной сердечной недостаточности включают учащенное дыхание, проблемы с кормлением, медленное увеличение веса, низкий уровень энергии и холодное липкое потоотделение.
Если ОАП остается большим, со временем дополнительный кровоток повреждает легочные артерии, и они становятся жесткими и утолщенными. Это состояние, называемое заболеванием легочных сосудов, представляет собой очень серьезную проблему, от которой в настоящее время не существует эффективного лечения.
Дети с открытым артериальным протоком также подвержены повышенному риску подострого бактериального эндокардита (ВБЭ). Это инфекция сердца, вызванная бактериями в кровотоке. Это может произойти после стоматологической или другой медицинской процедуры, но обычно его можно предотвратить с помощью дозы антибиотика перед процедурой. Дети с маленькими КПК подвергаются даже большему риску СБЭ, чем дети с большими КПК. По этой причине многие врачи рекомендуют закрывать даже небольшие КПК.
Рекомендации по упражнениям: рекомендации по упражнениям лучше всего делать врачом пациента, чтобы все соответствующие факторы могли быть учтены при принятии решения.В общем, ограничения физических упражнений для пациентов с открытым артериальным протоком не требуются, и дети могут участвовать в соревновательной и активной спортивной деятельности.
Как диагностируется эта проблема?
Клинические данные: У большинства детей с КПК нет сердечных симптомов. Если проток большого размера, могут развиться симптомы застойной сердечной недостаточности. Застойная сердечная недостаточность может развиться в любое время, но чаще проявляется в течение первых 2–3 месяцев жизни.Симптомы включают учащенное дыхание, плохое питание, медленный рост и холодное липкое потоотделение.
Физические данные: Шум в сердце часто является единственным признаком того, что у ребенка есть КПК. Если у ребенка застойная сердечная недостаточность, он не прибавит в весе, частота сердечных сокращений и частота дыхания будут выше нормы, а печень увеличится.
Медицинские анализы: Медицинские анализы, которые предоставляют полезную информацию, включают электрокардиограмму, тест на сатурацию кислорода и рентген грудной клетки.Диагноз подтверждается эхокардиограммой.
Как решается проблема?
Как описано ранее, маленькие КПК не вызывают симптомов, поэтому обычно лечение (кроме профилактики SBE) не требуется. У многих детей в течение первого года жизни происходит самопроизвольное закрытие протока. Если у ребенка развивается застойная сердечная недостаточность, могут быть назначены лекарства, в том числе дигоксин и / или диуретики. Эти лекарства часто контролируют симптомы до тех пор, пока ребенок не станет больше, а КПК не станет меньше или полностью не закроется.
Если открытый проток не закрывается самопроизвольно к одному или двум годам, или если есть симптомы застойной сердечной недостаточности, которые не контролируются лекарствами, рекомендуется закрытие дефекта. Также может быть рекомендовано закрытие очень маленького или «тихого» открытого артериального протока для снижения риска бактериального эндокардита. Варианты лечения включают закрытие через катетеризацию сердца или хирургическое закрытие. Лекарство под названием индометацин часто используется для закрытия протока у недоношенных детей.
Транскатетерное закрытие открытого артериального протока: Транскатетерное закрытие открытого артериального протока оказалось отличным вариантом лечения детей с открытым артериальным протоком. Впервые описанная в 1967 году, эта процедура проводится в лаборатории катетеризации сердца с применением седативных средств, не требующих хирургического вмешательства. Во время процедуры катетеры (тонкие пластиковые трубки) вводятся в крупные кровеносные сосуды ног и осторожно направляются к сердцу. Эти катетеры используются для размещения небольших металлических спиралей внутри протока.Спирали препятствуют току крови по сосуду, отчасти за счет стимуляции образования тромба в этом месте. Эта процедура дает отличный результат у большинства пациентов. Осложнения возникают редко и включают кровотечение, инфекцию и раннее смещение спирали. Если катушка смещается, ее обычно можно извлечь во время процедуры и переставить или заменить катушкой большего размера. Процедура проводится в амбулаторных условиях, и дети могут возобновить все занятия в течение 48 часов.
Хирургическое закрытие открытого артериального протока: Хирургические результаты также превосходны.Хирургическое вмешательство является предпочтительным методом лечения большого ОАП и / или если закрытие требуется в младенчестве. Это делается через небольшой разрез между ребрами с левой стороны. Проток идентифицируется и либо перевязан, либо разделен. Хирургические осложнения возникают редко и включают охриплость голоса или паралич диафрагмы, инфекцию, кровотечение и скопление жидкости вокруг легких. Большинство детей уходят домой через два-три дня после операции.
Клиники
Уход и услуги для пациентов с этой проблемой предоставляются в клиниках врожденного сердца, интервенционной кардиологии и сердечно-сосудистой хирургии при Медицинском центре Мичиганского университета в Анн-Арборе.
Каковы перспективы для детей с этой проблемой?
Перспективы для этих пациентов превосходны, если лечение начато достаточно быстро, чтобы предотвратить обструктивную болезнь легочных сосудов. Возможные отдаленные осложнения включают коарктацию (сужение аорты) или рецидив сосуда, хотя обе проблемы возникают крайне редко.
Список литературы
Ллойд Т.Р., Феддерли Р., Мендельсон А.М. и др. Транскатетерная окклюзия открытого артериального протока.Тираж 1993: 88; 1412-1420.
Mullins CE & Pagotto L. Открытый артериальный проток. В Garson A, Bricker J, Fisher D & Neish S (Eds), Наука и практика детской кардиологии. Уильямс и Уилкинс: Балтимор, Мэриленд, 1181–1197.
Парк МК. Поражения шунта слева направо. В детской кардиологии для практиков. Ежегодник Мосби: Сент-Луис, Миссури, 1996, 142–145.
Shim D и Beekman RH. Чрескатетерное ведение открытого артериального протока. Педиатр Кардиол 1998: 19; 67-71.
Автор: S. LeRoy RN, MSN
Отзыв написан сентябрь 2012 г.
границ | Эхокардиографическая оценка открытого артериального протока у недоношенных детей
Введение
Недоношенные дети составляют 6–12% населения новорожденных и составляют основную группу младенцев, получающих лечение в отделениях интенсивной терапии новорожденных. Среди типичных осложнений, наблюдаемых у недоношенных детей, часто встречается открытый артериальный проток (ОАП). Заболеваемость обратно пропорциональна гестационному возрасту недоношенного ребенка: около 20% у недоношенных детей, родившихся на 32 неделе гестации, по сравнению с примерно 80–90% у младенцев с крайне низкой массой тела при рождении и сроком гестации менее 26. недели (1, 2).Вероятность самопроизвольного закрытия артериального протока (DA) у доношенных детей без врожденных пороков сердца очень высока; у недоношенных новорожденных показатели закрытия ниже (1–3). Однако недавние исследования показали, что ОАП самопроизвольно закрывается к концу первой недели жизни примерно у 73% недоношенных детей со сроком беременности 28 недель (3).
Согласно международной литературе, КПК ассоциируется не только с повышенной смертностью, но и с различными сопутствующими заболеваниями новорожденных (1, 2, 4, 5).К ним относятся сердечная недостаточность, потребность в респираторной поддержке, потребность в дополнительном кислороде, бронхолегочная дисплазия, легочное кровотечение, внутрижелудочковое кровоизлияние, нарушение церебральной перфузии и некротический энтероколит. На этом фоне в 1990-е годы стало обычной практикой следовать стратегии агрессивного медикаментозного или хирургического закрытия ОАП у очень недоношенных детей. В настоящее время мы знаем, что нет реальной доказанной причинно-следственной связи между смертностью, неонатальными заболеваниями и ОАП (2, 5).Показания к близко КПК имеют, таким образом, резко уменьшились, а процедура остается спорной. Текущий подход состоит в том, чтобы ограничить лечение младенцами, которые с наибольшей вероятностью выиграют от вмешательства, то есть младенцами с чрезвычайно низкой массой тела при рождении, особенно теми, которые получают респираторную поддержку и подвержены риску быстрого развития гемодинамически значимого ОАП (hsPDA) (5).
Поскольку клинические признаки ОАП недостаточно чувствительны или специфичны, всем крайне недоношенным детям с риском развития ОАП следует проводить эхокардиографию.Основная цель настоящего обзора — определить и разработать различные этапы эхокардиографической оценки ОАП у недоношенных детей.
Эхокардиографическая оценка КПК
Общие положения
При оценке КПК важно учитывать некоторые общие рекомендации. Хотя DA является основным направлением функциональной эхокардиографии, ребенку всегда следует сначала пройти полную эхокардиограмму. Первоначальная эхокардиограмма позволяет (i) исключить структурные врожденные пороки сердца, (ii) измерить бивентрикулярную функцию и (iii) проверить различные аспекты переходного кровообращения, например, давление в легких.
При выполнении функциональной эхокардиографии также важно помнить о трудностях и проблемах, связанных со сканированием недоношенных детей. Некоторые дети очень маленькие, они могут быть возбужденными или нестабильными, иметь высокую частоту сердечных сокращений, а иногда и плохое эхо-окно, особенно если они находятся на вентиляции и имеют тяжелое основное заболевание легких. Вот несколько простых приемов: поместите ребенка в наиболее удобное положение (слегка повернутый влево и слегка вытянутую шею), по возможности просканируйте ребенка, когда он находится в спокойном и стабильном состоянии, и выделите достаточно времени.
Специальная оценка КПК
Эхокардиографическая оценка КПК недоношенного ребенка поможет врачам ответить на следующие вопросы: Имеется ли патент на DA? Какой у него размер? Какое направление шунта? Является ли КПК гемодинамически значимым?
Проходимость воздуховода
Открытый артериальный проток можно увидеть на каждом из классических эхо-изображений, но наиболее предпочтительными видами являются парастернальный вид по короткой оси (SAX) и надгрудинный вид. С помощью SAX DA визуализируется у основания сердца, слегка перемещая зонд к легочной артерии.Небольшой DA можно легко пропустить на 2D-изображениях, поэтому могут быть полезны импульсный волновой допплер и цветной допплер (рисунок 1). Импульсно-волновой допплер в основной легочной артерии показывает спокойный поток, когда DA закрыт, и турбулентный систолический и диастолический поток, когда DA является очевидным (Рисунок 1). Для надгрудинного обзора датчик следует разместить на сагиттальном уровне по средней линии, чтобы визуализировать легочную артерию слева и нисходящую аорту справа на снимке. DA появляется между обеими крупными артериями (рис. 2).
Рисунок 1 . Визуализация открытого артериального протока в короткой оси (SAX). (A) 2D SAX смещен кпереди, (B) такое же изображение с цветным допплером, (C) допплер в основной легочной артерии по закрытому протоку и (D) допплер в основной легочной артерии по патенту воздуховод. MPA, главная легочная артерия; RPA, правая легочная артерия; LPA, левая легочная артерия; AAo, восходящая аорта.
Рисунок 2 .Визуализация открытого артериального протока (ОАП) в надгрудинной проекции. (A) Нормальная надгрудинная проекция дуги аорты, (B) надгрудинная сагиттальная проекция с легочной артерией и нисходящей аортой и (C) цветной допплер в сагиттальной надгрудинной проекции с ОАП красного цвета.
Помимо SAX и над грудинной проекции, также можно увидеть DA в парастернальной длинной оси (LAX), перемещая зонд от классической LAX кпереди к легочной артерии (рис. 3).Подреберный LAX также позволяет обнаруживать DA. Единственное окно, которое не подходит для обнаружения ДА, — это апикальный четырехкамерный вид.
Рисунок 3 . Визуализация открытого артериального протока в продольной оси (LAX). (A) 2D classic LAX, (B) LAX немного наклонен кпереди в сторону легочной артерии, и (C) главная легочная артерия с легочными ветвями. ПЖ, правый желудочек; LV, левый желудочек; AV, аортальный клапан; PV, легочный клапан; MPA, главная легочная артерия; RPA, правая легочная артерия; LPA, левая легочная артерия.
Размер воздуховода
Наиболее точным видом для измерения размера DA является окно верхней левой парастернальной короткой оси, также называемое «протоковым видом». Сосредоточившись на основной легочной артерии, можно визуализировать начало правой легочной артерии, которая не всегда видна, и левой легочной артерии; DA расположен слева от него. DA следует измерять в самом узком месте до входа в основную легочную артерию (Рисунок 4).
Рисунок 4 .Измерение размера открытого артериального протока (ОАП) в надгрудинной проекции. MPA, главная легочная артерия; RPA, правая легочная артерия; LPA, левая легочная артерия.
Размер протока не очень точный. Не рекомендуется использовать цветной допплер, который может преувеличить размер. Измерения всегда должны выполняться с использованием последовательной техники. КПК считается маленьким при размере <1,5 мм, средним, если он составляет от 1,5 до 3 мм, и большим, если его размер превышает 3 мм.SAX не следует выбирать для измерения размера протока, потому что не всегда можно отличить левую легочную артерию от DA.
Направление шунта через КПК
Направление шунта через КПК может быть справа налево, двунаправленным или слева направо. Чтобы задокументировать это, требуется цветной допплер. Шунт справа налево через ОАП увидеть труднее: цветной доплеровский анализ покажет поток, идущий от легочной артерии к нисходящей аорте.Таким образом, обе магистральные артерии и DA будут отображаться синим цветом на цветном доплеровском изображении, потому что кровь уходит от датчика. Размещение импульсной волны Доплера над DA показывает волну Доплера ниже базовой линии, обычно во время систолы. Реже можно наблюдать непрерывный поток во время систолы и диастолы, представляющий собой чистый шунт справа налево (рис. 5). Когда сопротивление легочных сосудов падает, шунт будет двунаправленным с потоком выше базовой линии во время систолы и ниже базовой линии во время диастолы (рис. 6).Скорости обычно низкие и предполагают одинаковое давление в легочной артерии и нисходящей аорте. Цветной допплер показывает чередование красного и синего цветов. Как только давление в легких еще больше упадет, шунт переместится слева направо и станет красным на цветном доплеровском изображении. С помощью импульсного или непрерывного волнового допплера можно измерить максимальные скорости во время систолы и диастолы, см. Ниже. Также можно продемонстрировать направление шунта на цветном доплеровском режиме с использованием M-режима (рисунок 6).
Рисунок 5 .Шунт справа налево через открытый артериальный проток (ОАП). (A) Вид короткой оси; цвет Допплеровский режим потока синий во время систолы и диастолы, (B) поток через ОАП ниже базовой линии во время систолы, и (C) поток через ОАП ниже базовой линии во время систолы и диастолы в случае « чистый шунт справа налево ». MPA, главная легочная артерия; RPA, правая легочная артерия; LPA, левая легочная артерия.
Рисунок 6 .Надгрудинный вид с двунаправленным шунтом (A), , двунаправленным шунтом (B), , преимущественно слева направо, (C), шунтом слева направо на цветном доплеровском режиме и (D), слева направо правый шунт на цветном доплеровском M-Mode.
Является ли КПК гемодинамически значимым?
В физиологическом состоянии соотношение легочного и системного кровотока (Qp: Qs) равно 1. Выход правого желудочка отражает системный кровоток, тогда как выход левого желудочка отражает поток крови в легких.Шунт через открытое овальное отверстие влияет на выброс правого желудочка, а шунт через ОАП влияет на выброс левого желудочка. Таким образом, измерения желудочкового выброса у новорожденного с открытым DA и овальным отверстием не очень точны.
В случае hsPDA, легочный кровоток увеличивается из-за количества крови, возвращающейся из нисходящей аорты в легочную циркуляцию через PDA; этот паттерн известен как феномен кражи. При этом снижается системный кровоток по той же причине.Соотношение Qp: Qs увеличится.
Нет четкого клинического определения hsPDA. Сосенко и др. (6) упомянули hsPDA при наличии клинических признаков ОАП, связанных либо с легочным кровотечением, либо с кардиомегалией и признаками отека легких, а также с дыхательной недостаточностью и / или артериальной гипотензией, требующей лечения вазопрессорами. McNamara и Sehgal (7) предложили систему стадирования со сравнением клинических и эхокардиографических критериев hsPDA.
Основные эхокардиографические критерии, упомянутые в литературе, включают увеличение левого предсердия с соотношением левого предсердия к аортальному клапану (LA: Ao) ≥1.5, а также отсутствие или ретроградный диастолический поток в нисходящей аорте, отсутствие или ретроградный диастолический поток в верхней брыжеечной артерии и / или в передней мозговой артерии, средний или большой диаметр ОАП ≥ 1,5 мм в самом узком месте и неограниченный пульсирующий трансдуктальный поток (2, 5, 6, 8–12).
Как мы можем измерить эти параметры?
LA: отношение Ao измеряется на парастернальном LAX с использованием M-режима (рис. 7). В левом предсердии на уровне аортального клапана делается разрез, датчик помещается перпендикулярно ему.Аортальный клапан измеряется непосредственно перед его открытием, в конце диастолы, тогда как левое предсердие измеряется при максимальном объеме во время систолы. Отношение LA: Ao не должно превышать 1,5. Это измерение легко выполнить, но оно не очень точное по двум причинам: во-первых, левое предсердие не всегда легко определить, особенно из-за входа в него легочных вен. Во-вторых, предсердный шунт влияет на соотношение LA: Ao, поскольку большое овальное отверстие или дефект межпредсердной перегородки позволяет набухшему левому предсердию стекать в правое.
Рисунок 7 . Измерение отношения LA: Ao в парастернальном виде по длинной оси в M-режиме.
Еще одним признаком hsPDA является отсутствие или ретроградный диастолический кровоток в нисходящей аорте. Чтобы это визуализировать, датчик необходимо поместить в постпротоковую нисходящую аорту; используется импульсный волновой допплер. В физиологической ситуации волна Доплера является антероградной во время систолы и диастолы, при этом волна видна под базовой линией. Когда появляется феномен обкрадывания, конечный диастолический поток будет отсутствовать, и если соотношение Qp: Qs будет увеличиваться, поток будет ретроградным в течение всей диастолы, появляясь выше базовой линии (Рисунок 8).Это измерение является одним из наиболее точных при оценке гемодинамической значимости КПК.
Рисунок 8 . Надгрудинный вид: (A) цветной допплер постдуктальной нисходящей аорты с нормальным антероградным потоком (B) , отсутствием конечного диастолического потока (C) и ретроградным пандиастолическим потоком (D) .
Аналогичным образом измеряется диастолический поток в нисходящей брюшной аорте и в верхней брыжеечной артерии.Опять же, диастолический поток должен быть антероградным и отображаться как доплеровская кривая выше базовой линии. В случае hsPDA он может отсутствовать или даже казаться ретроградным (рис. 9). В этом случае предполагается, что перфузия тонкой кишки нарушена.
Рисунок 9 . Вид подреберья нисходящей части брюшной аорты с визуализацией целлюлозного ствола и верхней брыжеечной артерии, (A) на 2D, (B) на цветном доплеровском изображении, (C) с антероградным потоком, (D) с отсутствие конечного диастолического потока и (E) с ретроградным потоком.TC, truncus coeliacus; SMA, верхняя брыжеечная артерия.
И последнее, но не менее важное: измеряется доплеровский режим потока через КПК. Это покажет один из трех шаблонов (Рисунок 10). Негемодинамически значимый ОАП имеет высокую скорость потока во время систолы и диастолы с максимальной скоростью более 2 м / с в конце диастолы; это называется «ограниченный непрерывный трансдуктальный поток». Если ОАП имеет умеренное гемодинамическое значение, доплеровский режим кровотока имеет максимальную диастолическую скорость менее 2 м / с и называется «неограниченным пульсирующим трансдуктальным потоком».В большом hsPDA поток также является «неограниченным пульсирующим трансдуктным потоком», но максимальная конечная диастолическая скорость ниже 1 м / с. Помимо абсолютных значений, также можно измерить соотношение между систолической и диастолической скоростями. Если пиковая диастолическая скорость составляет более 50% от максимальной систолической скорости, картина потока является ограничительной. Если это соотношение меньше 50%, картина потока пульсирующая, что свидетельствует о гемодинамически значимом ОАП.
Рисунок 10 .Трансдуктальный поток по Допплеру в виде короткой оси или над грудиной: (A, B), неограниченный пульсирующий поток и (C) ограничивающий непрерывный поток.
Сводка эхокардиографических параметров КПК
Наиболее специфические эхокардиографические параметры ОАП можно разделить на три группы: (i) протоковые характеристики, (ii) избыточное кровообращение в легких и (iii) системная гипоперфузия. Последние два наблюдаются в случае hsPDA.
Характеристики КПК
Характеристики ОАП лучше всего оцениваются путем измерения размера протока и скоростей через ОАП, как в надгрудинной сагиттальной проекции.Диаметр протока, измеренный в первый день жизни, имеет высокую чувствительность и специфичность при прогнозировании развития hsPDA (2). Другие авторы также описывают связь между размером протока и необходимостью дальнейшего медикаментозного или хирургического закрытия (13). Измерение скорости потока над грудиной дает информацию о направлении шунта и позволяет оценить легочное давление. Кроме того, количественная оценка систолической и диастолической скоростей потока через ОАП и, в частности, отношения пиковой систолической скорости к конечной диастолической скорости потока является хорошим предиктором проходимости протоков у недоношенных детей, родившихся до 32 недель беременности (14).
Гиперперфузия легких
Легочная гиперперфузия лучше всего документируется при соотношении LA: Ao ≥1,5, повышенном потоке через среднюю легочную артерию, повышенном диастолическом потоке в левой легочной артерии и митральном соотношении E / A> 1,5, что свидетельствует о тяжелом давлении в левой части сердца. загрузка (2, 7). Самым популярным эхокардиографическим параметром является отношение LA: Ao, которое легко измерить. Однако на этот параметр влияет шунт через открытое овальное отверстие.
Системная гипоперфузия
Системную гипоперфузию лучше всего оценивать при наличии ретроградного кровотока в нисходящей аорте, а также в передней мозговой и верхней брыжеечной артериях.
Эти параметры помогают оценить КПК как бессимптомный, или как умеренно, умеренно или сильно гемодинамически значимый. В литературе нет согласия по лучшим параметрам для оценки значимости протоков, но Condo et al. предложенный размер протока и структура потока являются наиболее чувствительными (9).Однако эти параметры должны быть связаны с клиническими симптомами ребенка, а также с его послеродовым возрастом. Гемодинамический переход, характеризующийся повышенным сопротивлением легочных сосудов, будет отражен на эхокардиографии преимущественно шунтом справа налево в первые минуты жизни, за которым следует двунаправленное шунтирование, а затем шунт слева направо с низким протоковым протоком. скорости потока (15). При физиологическом понижении и нормализации легочного давления наблюдается увеличение систолической и диастолической скорости.Кроме того, размер протока, измеренный в первые 2 дня жизни, является хорошим предиктором развития симптоматического ДА, чего не происходит в более позднем возрасте. Таким образом, подход, используемый при оценке hsPDA, варьируется в зависимости от времени появления эха.
Обсуждение
Эхокардиографическая оценка ОАП у очень недоношенных новорожденных является одним из повседневных занятий в отделении интенсивной терапии новорожденных и обычно выполняется не только детскими кардиологами, но также неонатологами или детскими реаниматологами, обученными функциональной эхокардиографии.Выполнение эхокардиограммы у крайне недоношенных новорожденных непросто, и тот факт, что существует вариабельность как внутри, так и между наблюдателями, определенно не является оптимальным. Таким образом, важно соблюдать некоторые основные правила. Во-первых, эхокардиограмма может сфокусироваться на КПК только после того, как предыдущее полное эхо исключило структурный врожденный порок сердца и измерило функцию желудочков. Во-вторых, сканирование недоношенного ребенка может быть сложной задачей, а оценка КПК требует времени, поэтому также важно помнить об общих соображениях, описанных в этом обзоре.
Если эхокардиограмма недоношенного ребенка с ОАП была проведена неонатологом или реаниматологом, результаты эхокардиографии должны быть подтверждены детским кардиологом и должно быть принято совместное решение относительно лечения ОАП и последующего наблюдения за ребенком.
Дискуссия о том, следует ли лечить КПК, выходит за рамки настоящего обзора. Однако многие авторы предлагают лечить только детей с hsPDA и клиническими признаками дыхательной недостаточности.Действительно, ребенку, который чувствует себя очень хорошо и ему не требуется поддержка искусственной вентиляции легких или дополнительный кислород, обычно не приносит пользы закрытие протока. В этом смысле эхокардиографическая оценка КПК должна сопровождаться определением его клинической значимости. Одним из возможных подходов является система стадирования, опубликованная 10 лет назад McNamara и Sehgal (7), в которой подробно описывается корреляция между клиническими и эхокардиографическими признаками. Неонатологи могут найти это полезным при принятии решения о том, следует ли и когда начинать медикаментозное лечение, чтобы закрыть КПК.
Авторские взносы
Р.А. — единственный автор, внесший полный вклад в рукопись.
Заявление о конфликте интересов
Автор заявляет, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Все эхокардиографические снимки были сделаны мной и включены с письменного разрешения родителей пациентов.Я хотел бы поблагодарить их всех за разрешение опубликовать фотографии.
Сокращения
DA, артериальный проток; hsPDA, гемодинамически значимый открытый артериальный проток; ЛА: АО, левое предсердие к аортальному клапану; LAX, вид по длинной оси; PDA, открытый артериальный проток; SAX, вид короткой оси.
Список литературы
2. Хеучан AM, Климан Р.И. Лечение открытого артериального протока: текущие варианты лечения. Arch Dis Child Fetal Neonatal Ed (2014) 99: F431–6.DOI: 10.1136 / archdischild-2014-306176
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Роллан А., Шанкар-Агилера С., Диоманде Д., Зупан-Симунек В., Буало П. Естественная эволюция открытого артериального протока у крайне недоношенных детей. Arch Dis Child Fetal Neonatal Ed (2015) 100: F55–8. DOI: 10.1136 / archdischild-2014-306339
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Клюков М., Джеффри М., Гилл А., Эванс Н.Рандомизированное плацебо-контролируемое исследование раннего лечения открытого артериального протока. Arch Dis Child Fetal Neonatal Ed (2014) 99: F99–104. DOI: 10.1136 / archdischild-2013-304695
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Sosenko IRS, Fajardo MF, Claure N, Bancalari E. Сроки лечения открытого артериального протока и респираторные исходы у недоношенных детей: двойное слепое рандомизированное контролируемое исследование. J Pediatr (2012) 160: 929–35.DOI: 10.1016 / j.jpeds.2011.12.031
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Макнамара П.Дж., Сегал А. К рациональному ведению открытого артериального протока: необходимость определения стадии заболевания. Arch Dis Child Fetal Neonatal Ed (2007) 92: F424–7. DOI: 10.1136 / adc.2007.118117
CrossRef Полный текст | Google Scholar
8. Селлмер А., Бьерре Дж. В., Шмидт М. Р., Макнамара П. Дж., Хьортдал В. Е., Хозяин Б и др. Заболеваемость и смертность недоношенных новорожденных с открытым артериальным протоком на 3-й день. Arch Dis Child Fetal Neonatal Ed (2013) 98: F505–10. DOI: 10.1136 / archdischild-2013-303816
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Кондо М., Эванс Н., Беллу Р., Клюцков М. Эхокардиографическая оценка протокового значения: ретроспективное сравнение двух методов. Arch Dis Child Fetal Neonatal Ed (2012) 97: F35–8. DOI: 10.1136 / adc.2010.207233
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Vanhaesebrouck S, Zonnenberg I., Vandervoort P, Bruneel E, Van Hoestenberghe MR, Theyskens C.Консервативное лечение открытого артериального протока у недоношенных. Arch Dis Child Fetal Neonatal Ed (2007) 92: F244–7. DOI: 10.1136 / adc.2006.104596
CrossRef Полный текст | Google Scholar
11. Ивашима С., Исикава Т. Количественная неинвазивная оценка шунтирующего потока открытого артериального протока путем измерения площади проксимальной изоворотной поверхности на цветном доплеровском изображении. Circ J (2014) 78: 2302–8. DOI: 10.1253 / circj.CJ-14-0229
CrossRef Полный текст | Google Scholar
12.Таузин Л., Жубер С., Ноэль А.С., Буиссу А., Мулис М.Э. Влияние стойкого открытого артериального протока на смертность и заболеваемость у младенцев с очень низкой массой тела при рождении. Acta Paediatr (2012) 101: 419–23. DOI: 10.1111 / j.1651-2227.2011.02550.x
CrossRef Полный текст | Google Scholar
13. Tschuppert S, Doell C, Arlettaz-Mieth R, Baenziger O, Rousson V, Balmer C, et al. Влияние диаметра протока на хирургическое и медицинское закрытие открытого артериального протока у недоношенных новорожденных: размер имеет значение. J Thorac Cardiovasc Surg (2008) 135: 78–82. DOI: 10.1016 / j.jtcvs.2007.07.027
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14. Смит А., Магуайр М., Ливингстон В., Демпси Э.М. Отношение максимальной систолической скорости к конечной диастолической скорости потока связано с проходимостью протоков у младенцев до 32 недель беременности. Arch Dis Child Fetal Neonatal Ed (2014) 100: F132–6. DOI: 10.1136 / archdischild-2014-306439
CrossRef Полный текст | Google Scholar
15.Ван Вондерен Дж. Дж., Те Пас А. Б., Кольстер-Бийдеваате К., ван Лит Дж. М., Блом Н. А., Хупер С. Б. и др. Неинвазивные измерения кровотока в артериальном протоке сразу после рождения. Arch Dis Child Fetal Neonatal Ed (2014) 99: F408–12. DOI: 10.1136 / archdischild-2014-306033
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Рассмотрение подходов, консервативное лечение, фармакологическое управление
Автор
Люк Ким, доктор медицины Доцент кафедры внутренней медицины, отделение кардиологии, Пресвитерианская больница Нью-Йорка, Медицинский центр Вейл Корнелл
Раскрытие: Ничего не разглашать.
Соавтор (ы)
Джеффри Милликен, доктор медицины Руководитель отделения кардиоторакальной хирургии Калифорнийского университета в Медицинском центре Ирвина; Клинический профессор кафедры хирургии Калифорнийского университета в Ирвине, медицинский факультет
Джеффри Милликен, доктор медицинских наук, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская ассоциация торакальной хирургии, Американский колледж кардиологии, Американский колледж Грудные врачи, Американский колледж хирургов, Американская кардиологическая ассоциация, Американское общество искусственных внутренних органов, Калифорнийская медицинская ассоциация, Международное общество трансплантации сердца и легких, Phi Beta Kappa, Общество торакальных хирургов, SWOG, Western Surgical Association
Раскрытие: ничего расскрыть.
Главный редактор
Стюарт Бергер, доктор медицины Исполнительный директор кардиологического центра, временный начальник отделения детской кардиологии детской больницы Лурье; Профессор кафедры педиатрии Северо-Западного университета, Медицинская школа Файнберга
Стюарт Бергер, доктор медицинских наук, является членом следующих медицинских обществ: Американская академия педиатрии, Американский колледж кардиологии, Американский колледж грудных врачей, Американская кардиологическая ассоциация, Общество. по сердечно-сосудистой ангиографии и вмешательствам
Раскрытие информации: нечего раскрывать.
Благодарности
Хью Д. Аллен, доктор медицины Профессор, кафедра педиатрии, кафедра детской кардиологии и кафедра внутренней медицины, Медицинский колледж Университета штата Огайо
Хью Д. Аллен, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии педиатрии, Американского кардиологического колледжа, Американской кардиологической ассоциации, Американского педиатрического общества, Американского общества эхокардиографии, Общества педиатрических исследований, Общества детской эхокардиографии и Western Общество педиатрических исследований
Раскрытие: Ничего не раскрывать.
Дэвид Ф.М. Браун, доктор медицины Адъюнкт-профессор, Отделение неотложной медицины, Гарвардская медицинская школа; Заместитель председателя, отделение неотложной медицины, Массачусетская больница общего профиля
Дэвид Ф.М. Браун, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Стивен Дж. Комптон, доктор медицины, FACC, FACP Директор кардиологической электрофизиологии, Институт сердца Аляски, Региональные больницы Провиденса и Аляски
Стивен Дж. Комптон, доктор медицины, FACC, FACP является членом следующих медицинских обществ: Медицинская ассоциация штата Аляска, Американский колледж кардиологии, Американский колледж врачей, Американская кардиологическая ассоциация, Американская медицинская ассоциация и Общество сердечного ритма
.
Раскрытие: Ничего не раскрывать.
Кристофер И Доти, доктор медицины, FACEP, FAAEM Доцент кафедры неотложной медицины, директор программы резидентуры, Департамент неотложной медицины, Больничный центр округа Кингс, Медицинский центр Нижнего штата Нью-Йорка
Christopher I Doty, MD, FACEP, FAAEM является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации, Совета директоров резидентур по неотложной медицине и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Gehaan D’Souza, MD Медицинский факультет Калифорнийского университета в Ирвине,
Раскрытие: Ничего не раскрывать.
Джастин Галович, доктор медицины Врач-резидент, отделение хирургии, Калифорнийский университет, Ирвин, медицинский факультет
Джастин Галович, доктор медицины, является членом следующих медицинских обществ: American College of Surgeons
Раскрытие: Ничего не раскрывать.
Christopher Johnsrude, MD, MS Начальник отдела детской кардиологии Медицинской школы Университета Луисвилля; Директор Центра врожденных пороков сердца, Детская больница Kosair
Christopher Johnsrude, MD, MS является членом следующих медицинских обществ: Американской академии педиатрии и Американского колледжа кардиологии
Раскрытие информации: Св. Иуда, Медицинская гонорар Говорит и преподает
Стивен Р Нейш, доктор медицинских наук Директор программы стипендий по детской кардиологии, доцент кафедры педиатрии Медицинского колледжа Бейлора
Стивен Р Нейш, доктор медицины, SM является членом следующих медицинских обществ: Американской академии педиатрии, Американского колледжа кардиологии и Американской кардиологической ассоциации
.
Раскрытие: Ничего не раскрывать.
Гириш Сетураман, доктор медицины, магистр здравоохранения Доцент, Медицинский факультет Университета Мэриленда
Гириш Сетураман, доктор медицины, магистр здравоохранения, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации, Американской ассоциации общественного здравоохранения и Общества академической неотложной медицины
Раскрытие: Ничего не раскрывать.
Гэри Сетник, доктор медицины , заведующий отделением неотложной медицины, больница Маунт-Оберн; Доцент отделения неотложной медицины Гарвардской медицинской школы
Гэри Сетник, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей скорой помощи, Национальной ассоциации врачей скорой помощи и Общества академической неотложной медицины
Раскрытие информации: должность в SironaHealth по вопросам заработной платы; Должность менеджера по заработной плате в Консорциуме EMS Южного Миддлсекса; Процедуры Консультации.com Royalty Прочее
Марк С. Слабинский, доктор медицины, FACEP, FAAEM Вице-президент, EMP Medical Group
Марк С. Слабински, доктор медицины, FACEP, FAAEM является членом следующих медицинских обществ: Alpha Omega Alpha, Американской академии экстренной медицины, Американского колледжа врачей скорой помощи, Американской медицинской ассоциации и Медицинской ассоциации штата Огайо
Раскрытие: Ничего не раскрывать.
Франсиско Талавера, фармацевт, доктор философии, Адъюнкт-профессор фармацевтического колледжа Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Reference Salary Employment
Park W Willis IV, MD Сара Грэм Заслуженный профессор медицины и педиатрии Университета Северной Каролины в Медицинской школе Чапел-Хилл
Park W Willis IV, MD является членом следующих медицинских обществ: Американское общество эхокардиографии
Раскрытие: Ничего не раскрывать.
Мэри Л. Виндл, PharmD Адъюнкт-профессор фармацевтического колледжа Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие: Ничего не раскрывать.
Патентный артериальный проток — обзор
Устройство для закрытия незащищенного артериального протока у новорожденных
КПК — относительно частая ИБС, встречающаяся у 1 из 2000 живорожденных у доношенных детей. 94 Кроме того, он чаще встречается у недоношенных новорожденных и может привести к значительной сердечной недостаточности и повышению заболеваемости, включая повышенный риск внутрижелудочкового кровотечения, некротического энтероколита и ХЗП. 95–99
Первое транскатетерное закрытие ОАП было выполнено Porstmann et al. в 1967 году. 100 С тех пор были разработаны различные устройства КПК, оболочки и низкопрофильные системы доставки. В настоящее время транскатетерное закрытие ОАП считается стандартом лечения после неонатального периода. Кроме того, в последнее время его успешно применяют в качестве альтернативы хирургическому закрытию даже у очень маленьких недоношенных детей. 101,102
Транскатетерное закрытие ОАП также может быть выполнено либо антероградным (венозным), либо ретроградным (артериальным) подходом, причем первый предпочтителен у очень маленьких детей, чтобы снизить риск сосудистых осложнений.Всем пациентам выполняется катетеризация сердца под общей анестезией в лаборатории двухплоской катетеризации. Для оценки размера, положения и формы протока выполняется двухплоскостная переднезадняя и боковая нисходящая аортограмма. 4-французский интродьюсер можно проследить по 0,025-дюймовому проводнику через правый желудочек в легочную артерию. Затем им можно манипулировать, чтобы пересечь ОАП с кончиком, расположенным в нисходящей аорте. После определения анатомии и ориентиров КПК (рис.32.7A) выбирается и запускается соответствующее устройство. После развертывания устройства и перед его отсоединением от системы доставки выполняется нисходящая аортограмма для подтверждения положения и устойчивости устройства (см. Рис. 32.7B). Затем через 10 минут после выпуска выполняется повторная аортограмма для оценки степени остаточного шунта (рис. 32.8).
Транскатетерное закрытие ОАП под эхокардиографическим контролем также было недавно описано, когда хирургическое закрытие противопоказано или когда транспортировка нестабильных младенцев сопряжена с высоким риском.Этот подход может выполняться у постели больного с использованием только венозного доступа, что избавляет младенцев от осложнений, потенциально связанных с артериальным доступом. Кроме того, было показано, что он безопасен и применим для недоношенных детей весом менее 1500 г. 101,103
Существует множество различных устройств, которые потенциально могут быть использованы для закрытия КПК у детей и младенцев. К ним относятся катушки, сосудистые пробки и окклюдер Amplatzer Duct Occluder. Решение о том, какое устройство использовать, зависит от предпочтений оператора, доступности устройства, типа КПК, размера ампулы (аортального конца КПК), самого узкого диаметра легочной артерии, длины КПК и нисходящей аорты. размер пациента и размер системы доставки.Практическое правило — использовать наименьшую доступную систему доставки, которой в настоящее время является 4-французская система доставки, и по возможности избегать артериального доступа. Это очень важно, особенно для недоношенных новорожденных, поскольку сосудистые осложнения обратно пропорциональны их весу. 104 В общем, для небольшого КПК с его самой узкой точкой менее 2 мм закрытие может быть достигнуто путем развертывания катушки или устройства Amplatzer Duct Occluder II. Для большого ОАП могут быть предпочтительны другие устройства, такие как сосудистая пробка или окклюдер для протока Occlutech.Эти устройства обычно устанавливаются внутри протока без каких-либо удерживающих дисков, выступающих за пределы ОАП, которые потенциально могут препятствовать потоку в нисходящей аорте или левой легочной артерии. 105–107
Устройства ADO (St. Jude Medical, Плимут, Миннесота), которые, как правило, безопасны для детей старшего возраста, могут быть проблематичными для младенцев меньшего возраста из-за риска закупорки аорты громоздкими удерживающими дисками. Следовательно, для этой группы очень маленьких детей закрытие спирали может быть предпочтительным и безопасным подходом.Катушки могут поставляться целиком внутри КПК без выступающих частей. Фрэнсис и его коллеги описали успешную спиральную окклюзию ОАП у восьми недоношенных новорожденных со средним весом при рождении 1040 г (от 700 до 1700 г) без значительных осложнений. 108
Новый ADO II AS с небольшими сочлененными ретенционными дисками (эти диски всего на 1–1,5 мм больше, чем центральная окклюзионная часть) является многообещающим устройством для использования у маленьких детей, обеспечивая отличную скорость закрытия протока через низкопрофильная система доставки с использованием 4-французских ножен для доставки.Хотя он еще не был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США, он доказал свою эффективность при низком уровне осложнений. Его использование у маленьких детей весом всего 1700 г было продемонстрировано в исследованиях как на животных, так и на людях. 101,102
По сравнению с хирургическим закрытием, транскатетерное закрытие ОАП ассоциируется с меньшим риском и меньшим количеством неблагоприятных исходов, напрямую связанных с вмешательством. Однако в настоящее время неизвестно, возникают ли медицинские осложнения после хирургического перевязки ОАП, включая системную гипотензию и значительное ухудшение легочного статуса пациента, после транскатетерного закрытия ОАП у недоношенных детей.Наиболее частые осложнения, конкретно связанные с устройством, включают эмболизацию устройства или неправильное его положение и обструкцию кровотока в нисходящей аорте и / или левой легочной артерии, вызывая ятрогенную коарктацию и / или стеноз левой легочной артерии. 101,104,107 Следует отметить, что проблемы безопасности при транскатетерном закрытии выше у младенцев меньшего возраста; Осложнения, такие как неправильное положение спирали или устройства, аритмия и / или гипотензия, требующие вмешательства, чаще возникают у младенцев с массой тела менее 6 кг по сравнению с более крупными младенцами (частота нежелательных явлений 27% vs.8%). 104,109 По мере накопления опыта и дальнейшего развития прочных оболочек с более низким профилем и систем доставки транскатетерное закрытие КПК с помощью устройства, вероятно, станет методом выбора при закрытии КПК как у доношенных, так и у недоношенных новорожденных.
Открытый артериальный проток у недоношенного ребенка: лечить или не лечить?
Нури С., Сери I. Новорожденный с очень низкой массой тела с гемодинамически значимым открытым артериальным протоком в течение первой постнатальной недели. В: Kleinman CS, Seri I (ред.). Гемодинамика и кардиология. Неонатальные вопросы и противоречия . Saunders Elsevier: Филадельфия, Пенсильвания, 2008 г., стр. 179.
Google Scholar
Hermes-DeSantis ER, Clyman RI. Открытый артериальный проток: патофизиология и лечение. J Perinatol 2006; 26 : S14 – S18.
Артикул
Google Scholar
Кох Дж., Хенсли Дж., Рой Л., Браун С., Рамачотти С., Розенфельд С. Р..Распространенность спонтанного закрытия артериального протока у новорожденных с массой тела при рождении 1000 грамм или меньше. Педиатрия 2006; 117 : 1113–1121.
Артикул
Google Scholar
Нури С., Сери I. Лечение открытого артериального протока: когда, как и как долго? J Pediatr 2009; 155 : 774–776.
Артикул
Google Scholar
Laughon MM, Simmons MA, Bose CL.Проходимость артериального протока у недоношенного ребенка: патология? Стоит ли лечить? Curr Opin Pediatr 2004; 16 : 146–151.
Артикул
Google Scholar
Bose CL, Laughon MM. Открытый артериальный проток: отсутствие доказательств общепринятых методов лечения. Arch Dis Child Fetal Neonatal Ed 2007; 92 : F498 – F502.
Артикул
Google Scholar
Knight DB, Laughon MM.Доказательства активного закрытия открытого артериального протока у очень недоношенных детей. J Pediatr 2008; 152 : 446–447.
Артикул
Google Scholar
Ван Овермайр Б. Открытый артериальный проток: насколько агрессивными мы должны быть? Неонатология 2007; 91 : 318.
Артикул
Google Scholar
Климан Р.И., Черн Н.Открытый артериальный проток: доказательства за и против лечения. J Pediatr 2007; 150 : 216–219.
Артикул
Google Scholar
Benitz WE. Лечение стойкого открытого артериального протока у недоношенных детей: время принять нулевую гипотезу? J Perinatol 2010; 30 (4): 241–252.
CAS
Статья
Google Scholar
Альпан Г., Шерер Р., Блэнд Р., Климан Р.Открытый артериальный проток увеличивает фильтрацию легочной жидкости у недоношенных ягнят. Pediatr Res 1991; 30 : 616–621.
CAS
Статья
Google Scholar
Маршалл Д.Д., Котельчук М., Янг Т.Э., Бозе К.Л., Крюер Л., О’Ши ТМ. Факторы риска хронических заболеваний легких в эпоху сурфактантов: популяционное исследование младенцев с очень низкой массой тела при рождении в Северной Каролине. Ассоциация неонатологов Северной Каролины. Педиатрия 1999; 104 : 1345–1350.
CAS
Статья
Google Scholar
Рохас М.А., Гонсалес А., Банкалари Е., Клер Н., Пул С., Сильва-Нето Г. Изменение тенденций в эпидемиологии и патогенезе хронических заболеваний легких новорожденных. J Pediatr 1995; 126 : 605–610.
CAS
Статья
Google Scholar
Шимада С., Касаи Т., Кониси М., Фудзивара Т. Влияние открытого артериального протока на выброс левого желудочка и кровоток в органах у недоношенных новорожденных с респираторным дистресс-синдромом, получавших сурфактант. J Pediatr 1994; 125 : 270–277.
CAS
Статья
Google Scholar
Перлман Дж. М., Хилл А, Вольпе Дж. Дж. Влияние открытого артериального протока на скорость кровотока в передних церебральных артериях: протоковый обхват у недоношенного новорожденного. J Pediatr 1981; 99 : 767–771.
CAS
Статья
Google Scholar
Lipman B, Serwer GA, Brazy JE.Аномальная церебральная гемодинамика у недоношенных детей с открытым артериальным протоком. Педиатрия 1982; 69 : 778–781.
CAS
PubMed
Google Scholar
Мартин К.Г., Снайдер А.Р., Кац С.М., Пибоди Дж. Л., Брэди Дж. Патологические паттерны мозгового кровотока у недоношенных детей с большим открытым артериальным протоком. J Pediatr 1982; 101 : 587–593.
CAS
Статья
Google Scholar
Deeg KH, Gerstner R, Brandl U, Bundscherer F, Zeilinger G, Harai G et al .Доплеровский сонографический параметр потока передней мозговой артерии в открытом артериальном протоке новорожденного по сравнению со здоровым контрольным образцом. Клинский Падиатр 1986; 198 : 463–470.
CAS
Статья
Google Scholar
Итихаси К., Сираиси Х, Эндоу Х, Курамацу Т., Яно С., Янагисава М. Церебральная и брюшная артериальная гемодинамика у недоношенных детей с открытым артериальным протоком. Acta Paediatr Jpn 1990; 32 : 349–356.
CAS
Статья
Google Scholar
Lemmers PM, Toet MC, van Bel F. Влияние открытого артериального протока и последующая терапия индометацином на церебральную оксигенацию у недоношенных детей. Педиатрия 2008; 121 : 142–147.
Артикул
Google Scholar
Клуцков М., Эванс Н. Низкий кровоток в верхней полой вене и внутрижелудочковое кровотечение у недоношенных детей. Arch Dis Child Fetal Neonatal Ed 2000; 82 : F188 – F194.
CAS
Статья
Google Scholar
Dykes FD, Lazzara A, Ahmann P, Blumenstein B, Schwartz J, Brann AW. Внутрижелудочковое кровоизлияние: проспективная оценка этиопатогенеза. Педиатрия 1980; 66 : 42–49.
CAS
PubMed
Google Scholar
Evans N, Kluckow M.Раннее протоковое шунтирование и внутрижелудочковое кровотечение у недоношенных детей, находящихся на ИВЛ. Arch Dis Child Fetal Neonatal Ed 1996; 75 : F183 – F186.
CAS
Статья
Google Scholar
Фоули П.В., Дэвис П.Г. Профилактическое внутривенное введение индометацина для предотвращения смертности и заболеваемости недоношенных детей. Кокрановская база данных Syst Rev 2002 г., выпуск 3. Ст. номер: CD000174 ..
Coombs RC, Morgan ME, Durbin GM, Booth IW, McNeish AS.Скорость кровотока в кишечнике новорожденных: влияние открытого артериального протока и парентерального индометацина. Arch Dis Child 1990; 65 : 1067–1071.
CAS
Статья
Google Scholar
Шимада С., Касаи Т., Хоши А, Мурата А, Чида С. Кардиоциркуляторные эффекты открытого артериального протока у младенцев с крайне низкой массой тела при рождении с респираторным дистресс-синдромом. Pediatr Int 2003; 45 : 255–262.
Артикул
Google Scholar
Бейлен Б.Г., Огата Х., Икегами М., Якобс Х.С., Джоб А.Х., Эммануилидес Г.С. Характеристики левого желудочка и региональные кровотоки до и после окклюзии артериального протока у недоношенных ягнят, получавших сурфактант. Тираж 1983 г .; 67 : 837–843.
CAS
Статья
Google Scholar
Климан Р.И., Мори Ф., Хейманн М.А., Роман С.Сердечно-сосудистые эффекты открытого артериального протока у недоношенных ягнят с респираторной недостаточностью. J Pediatr 1987; 111 : 579–587.
CAS
Статья
Google Scholar
Мейерс Р.Л., Альпан Дж., Лин Э., Климан Р.И. Открытый артериальный проток, индометацин и растяжение кишечника: влияние на кровоток в кишечнике и потребление кислорода. Pediatr Res 1991; 29 : 569–574.
CAS
Статья
Google Scholar
McCurnin D, Clyman RI.Влияние открытого артериального протока на перфузию брыжейки после еды у недоношенных бабуинов. Педиатрия 2008; 122 : e1262 – e1267.
Артикул
Google Scholar
Райдер Р. У., Шелтон Дж. Д., Гуинан, Мэн. Некротический энтероколит: проспективное многоцентровое исследование. Am J Epidemiol 1980; 112 : 113–123.
CAS
Статья
Google Scholar
Доллберг С., Луски А., Райхман Б.Артериальный проток, индометацин и некротический энтероколит у младенцев с очень низкой массой тела при рождении: популяционное исследование. J Pediatr Gastroenterol Nutr 2005; 40 : 184–188.
CAS
Статья
Google Scholar
Шмидт Б., Дэвис П., Моддеманн Д., Олссон А., Робертс Р.С., Сайгал С. и др. . Испытание профилактики индометацином у исследователей недоношенных. Долгосрочные эффекты профилактики индометацином у младенцев с крайне низкой массой тела при рождении. N Engl J Med 2001; 344 : 1966–1972.
CAS
Статья
Google Scholar
Clyman RI, Saha S, Jobe A, Oh W. Профилактика индометацином у недоношенных детей: влияние 2 многоцентровых рандомизированных контролируемых испытаний на клиническую практику. J Pediatr 2007; 150 : 46–50.
CAS
Статья
Google Scholar
Аттридж Дж. Т., Кларк Р., Уолкер М. В., Гордон П. В..Новое понимание спонтанной перфорации кишечника с использованием национального набора данных: (1) ГПИ связана с ранним воздействием индометацина. J Perinatol 2006; 26 : 93–99.
CAS
Статья
Google Scholar
Пакетт Л., Фридлих П., Раманатан Р., Сери I. Одновременное применение индометацина и дексаметазона увеличивает риск спонтанной перфорации кишечника у новорожденных с очень низкой массой тела при рождении. J Perinatol 2006; 26 : 486–492.
CAS
Статья
Google Scholar
Watterberg KL, Gerdes JS, Cole CH, Aucott SW, Thilo EH, Mammel MC et al . Профилактика ранней надпочечниковой недостаточности для предотвращения бронхолегочной дисплазии: многоцентровое исследование. Педиатрия 2004; 114 : 1649–1657.
Артикул
Google Scholar
Ambat MT, Ostrea Jr EM, Aranda СП.Влияние L-лизината ибупрофена на связывание билирубина с альбумином, измеренное с помощью анализа индекса насыщения и пероксидазы хрена. J Perinatol 2008; 28 : 287–290.
CAS
Статья
Google Scholar
Gournay V, Roze JC, Kuster A, Daoud P, Cambonie G, Hascoet JM et al . Профилактическое применение ибупрофена по сравнению с плацебо у очень недоношенных детей: рандомизированное двойное слепое плацебо-контролируемое исследование. Lancet 2004; 364 : 1939–1944.
CAS
Статья
Google Scholar
Bellini C, Campone F, Serra G. Легочная гипертензия после терапии L-лизин ибупрофеном у недоношенного ребенка с открытым артериальным протоком. CMAJ 2006; 174 : 1843–1844.
Артикул
Google Scholar
Rheinlaender C, Helfenstein D, Walch E, Berns M, Obladen M, Koehne P.Уровни общего билирубина в сыворотке крови при лечении ингибитором циклооксигеназы открытого артериального протока у недоношенных детей. Acta Paediatr 2009; 98 : 36–42.
CAS
Статья
Google Scholar
Zecca E, Romagnoli C, De Carolis MP, Costa S, Marra R, De Luca D. Увеличивает ли ибупрофен неонатальную гипербилирубинемию? Педиатрия 2009; 124 : 480–484.
Артикул
Google Scholar
Бернс М., Тоеннессен М., Кене П., Альтманн Р., Обладен М.Ибупрофен усиливает токсичность билирубина в культуре корковых нейронов крыс. Pediatr Res 2009; 65 : 392–396.
CAS
Статья
Google Scholar
Ван Овермайр Б., Аллегерт К., Казаер А, Дебауш С., Декалуве В., Йесперс А и др. . Профилактика ибупрофена у недоношенных детей: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. Lancet 2004; 364 : 1945–1949.
CAS
Статья
Google Scholar
Jaillard S, Larrue B, Rakza T, Magnenant E, Warembourg H, Storme L. Последствия отсроченного хирургического закрытия открытого артериального протока у очень недоношенных детей. Ann Thorac Surg 2006; 81 : 231–234.
Артикул
Google Scholar
Климан Р.И. Рекомендации для послеродового использования индометацина: анализ четырех отдельных стратегий лечения. J Pediatr 1996; 128 : 601–607.
CAS
Статья
Google Scholar
Брукс Дж. М., Травади Дж. Н., Патоле С.К., Доэрти Д.А., Симмер К. Необходима ли хирургическая перевязка открытого артериального протока? Западно-австралийский опыт консервативного менеджмента. Arch Dis Child Fetal Neonatal Ed 2005; 90 : F235 – F239.
CAS
Статья
Google Scholar
Нури С., Маккой М., Фридлих П., Брайт Б., Готтипати В., Сери I и др. .Отсутствие закрытия артериального протока связано с повышенной смертностью недоношенных детей. Педиатрия 2009; 123 : e138 – e144.
Артикул
Google Scholar
Херрман К., Бозе К., Льюис К., Лафон М. Самопроизвольное закрытие открытого артериального протока у младенцев с очень низкой массой тела при рождении после выписки из неонатального отделения. Arch Dis Child Fetal Neonatal Ed 2009; 94 : F48 – F50.
CAS
Статья
Google Scholar
Zbar RI, Chen AH, Behrendt DM, Bell EF, Smith RJ. Заболеваемость параличом голосовых складок у младенцев, перенесших перевязку открытого артериального протока. Ann Thorac Surg 1996; 61 : 814–816.
CAS
Статья
Google Scholar
Бенджамин Дж. Р., Смит П. Б., Коттен С. М., Джаггерс Дж., Голдштейн Р.Ф., Малкольм В.Ф.Долгосрочные заболевания, связанные с параличом голосовых связок после хирургического закрытия открытого артериального протока у младенцев с крайне низкой массой тела при рождении. J Perinatol 2010; 30 (6): 408–413.
CAS
Статья
Google Scholar
Moin F, Kennedy KA, Moya FR. Факторы риска, предсказывающие использование вазопрессоров после перевязки открытого артериального протока. Am J Perinatol 2003; 20 : 313–320.
Артикул
Google Scholar
Нури С., Фридлих П., Сери I, Вонг П. Изменения функции миокарда и гемодинамики после перевязки артериального протока у недоношенных детей. J Pediatr 2007; 150 : 597–602.
Артикул
Google Scholar
Тейшейра Л.С., Шивананда С.П., Стивенс Д., Ван Арсделл Г., Макнамара П.Дж. Послеоперационная кардиореспираторная нестабильность после перевязки преждевременного артериального протока связана с ранней необходимостью вмешательства. J Perinatol 2008; 28 : 803–810.
CAS
Статья
Google Scholar
Кабра Н.С., Шмидт Б., Робертс Р.С., Дойл Л.В., Папайл Л., Фанаров А. Испытание профилактики индометацином у исследователей недоношенных. Нарушение нейросенсорных функций после хирургического закрытия открытого артериального протока у новорожденных с крайне низкой массой тела при рождении: результаты исследования профилактики индометацином у недоношенных. J Pediatr 2007; 150 : 229–234.
CAS
Статья
Google Scholar
Чорн Н., Леонард К., Пикуч Р., Климан Р. Открытый артериальный проток и его лечение как факторы риска неонатальных заболеваний и заболеваний нервной системы. Педиатрия 2007; 119 : 1165–1174.
Артикул
Google Scholar
Мадан Дж. К., Кендрик Д., Хагадорн Дж. И., Франц III ID. Терапия открытого артериального протока: влияние на неонатальный и 18-месячный исход. Педиатрия 2009; 123 : 674–681.
Артикул
Google Scholar
Лелигер М., Индер Т.Э., Далиц П.А., Каин С., Камм Э.Дж., Йодер Б. и др. . Онтогенетические и невропатологические последствия перевязки протоков у недоношенного павиана. Pediatr Res 2009; 65 : 209–214.
Артикул
Google Scholar
Кэссиди Дж., Кроуз Д. Т., Кирклин Дж. В., Стрэндж М.Дж., Стойнер СН, Годой Дж. и др. .Рандомизированное контролируемое испытание очень ранней профилактической перевязки артериального протока у младенцев, весивших при рождении не более 1000 г. N Engl J Med 1989; 320 : 1511–1516.
CAS
Статья
Google Scholar
Клайман Р., Кэссиди Дж., Кирклин Дж. К., Коллинз М., Филипс III Дж. Б. Роль перевязки открытого артериального протока в бронхолегочной дисплазии: пересмотр рандомизированного контролируемого исследования. J Pediatr 2009; 154 : 873–876.
Артикул
Google Scholar
McCurnin D, Seidner S, Chang LY, Waleh N, Ikegami M, Petershack J et al . Ибупрофен-индуцированное закрытие открытого артериального протока: физиологические, гистологические и биохимические эффекты на преждевременное легкое. Педиатрия 2008; 121 : 945–956.
Артикул
Google Scholar
Чанг Л.Й., МакКурнин Д., Йодер Б., Шауль П.В., Клайман Р.И.Перевязка артериального протока и рост альвеол у недоношенных бабуинов с открытым артериальным протоком. Pediatr Res 2008; 63 : 299–302.
Артикул
Google Scholar
Клуцков М., Эванс Н. Раннее эхокардиографическое прогнозирование симптоматического открытого артериального протока у недоношенных детей, подвергающихся искусственной вентиляции легких.
