Острая гипоксия плода в родах последствия: Гипоксия плода при беременности — гипоксия во время беременности и при родах. Последствия гипоксии
Гипоксия плода — причины, симптомы, диагностика и лечение
Гипоксия плода – внутриутробный синдром, характеризующийся комплексом изменений со стороны плода, обусловленных недостаточным поступлением кислорода к его тканям и органам. Гипоксия плода характеризуется нарушениями со стороны жизненно-важных органов, в первую очередь, ЦНС. Диагностика гипоксии плода включает проведение кардиотокографии, допплерометрии маточно-плацентарного кровообращения, акушерского УЗИ, амниоскопии. Лечение гипоксии плода направлено на нормализацию маточно-плацентарного кровотока, улучшение реологии крови; иногда данное состояние требует досрочного родоразрешения женщины.
Общие сведения
Гипоксия плода регистрируется в 10,5% случаев от общего числа беременностей и родов. Гипоксия плода может развиваться в различные сроки внутриутробного развития, характеризоваться различной степенью кислородной недостаточности и последствиями для организма ребенка. Гипоксия плода, развившаяся в ранние сроки гестации, вызывает пороки и замедление развития эмбриона. На поздних сроках беременности гипоксия сопровождается задержкой роста плода, поражением ЦНС, снижением адаптационных возможностей новорожденного.
Гипоксия плода, развившаяся в ранние сроки гестации, вызывает пороки и замедление развития эмбриона. На поздних сроках беременности гипоксия сопровождается задержкой роста плода, поражением ЦНС, снижением адаптационных возможностей новорожденного.
Гипоксия плода
Причины гипоксии плода
Гипоксия плода может являться следствием широкого круга неблагоприятных процессов, происходящих в организме ребенка, матери или в плаценте. Вероятность развития гипоксии у плода повышается при заболеваниях материнского организма – анемии, сердечно-сосудистой патологии (пороках сердца, гипертонии), заболеваниях почек, дыхательной системы (хроническом бронхите, бронхиальной астме и др.), сахарном диабете, токсикозах беременности, многоплодной беременности, ИППП. Негативно на снабжении плода кислородом отражается алкоголизм, никотиновая, наркотическая и другие виды зависимости матери.
Опасность гипоксии плода возрастает при нарушениях плодово-плацентарного кровообращения, обусловленных угрозой выкидыша, перенашиванием беременности, патологией пуповины, фетоплацентарной недостаточностью, аномалиями родовой деятельности и других осложнениях беременности и родового процесса.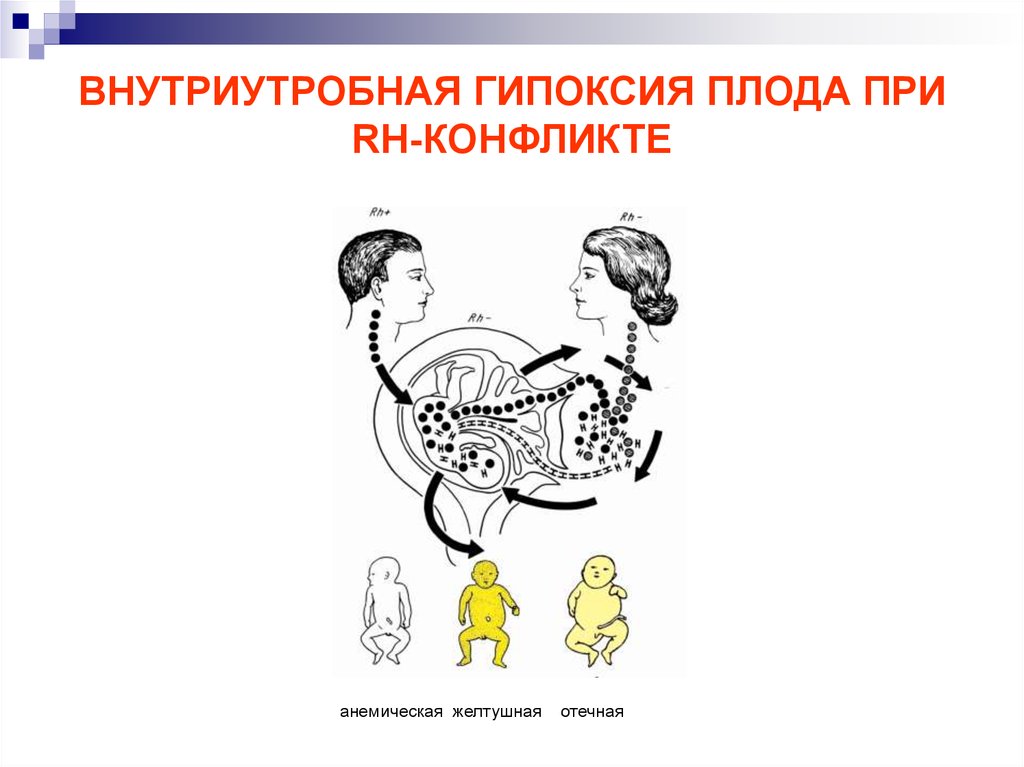 К факторам риска в развитии интранатальной гипоксии относят гемолитическую болезнь плода, врожденные аномалии развития, внутриутробное инфицирование (герпетическая инфекция, токсоплазмоз, хламидиоз, микоплазмоз и др.), многократное и тугое обвитие пуповины вокруг шейки ребенка, длительная по времени компрессия головки в процессе родов.
К факторам риска в развитии интранатальной гипоксии относят гемолитическую болезнь плода, врожденные аномалии развития, внутриутробное инфицирование (герпетическая инфекция, токсоплазмоз, хламидиоз, микоплазмоз и др.), многократное и тугое обвитие пуповины вокруг шейки ребенка, длительная по времени компрессия головки в процессе родов.
В ответ на гипоксию у плода, прежде всего, страдает нервная система, поскольку нервная ткань наиболее чувствительная к дефициту кислорода. Начиная с 6-11 недели развития эмбриона, недостаток кислорода вызывает задержку созревания головного мозга, нарушения в строении и функционировании сосудов, замедление созревания гематоэнцефалического барьера. Также гипоксию испытывают ткани почек, сердца, кишечника плода.
Незначительная гипоксия плода может не вызывать клинически значимых повреждений ЦНС. При тяжелой гипоксии плода развиваются ишемия и некрозы в различных органах. После рождения у ребенка, развивавшегося в условиях гипоксии, может наблюдаться широкий диапазон нарушений – от неврологических расстройств до задержки психического развития и тяжелых соматических отклонений.
Классификация гипоксии плода
По времени течения и скорости возникновения выделяют острую и хронически развивающуюся гипоксию плода.
Возникновение острой гипоксии плода обычно связано с аномалиями и осложнениями родового акта – стремительными или затяжными родами, прижатием или выпадением пуповины, длительным сдавлением головки в родовых путях. Иногда острая гипоксия плода может развиться в ходе беременности: например, в случае разрыва матки или преждевременной отслойки плаценты. При острой гипоксии стремительно нарастают нарушения функций жизненно важных органов плода. Острая гипоксия характеризуется учащением сердцебиения плода (более 160 уд. в мин.) или его урежением (менее 120 уд. в мин.), аритмией, глухостью тонов; усилением или ослаблением двигательной активности и т. д. Нередко на фоне острой гипоксии развивается асфиксия плода.
К хронической гипоксии приводит длительный умеренный дефицит кислорода, в условиях которого развивается плод. При хроническом дефиците кислорода возникает внутриутробная гипотрофия; в случае истощения компенсаторных возможностей плода развиваются те же нарушения, что и при остром варианте течения. Гипоксия плода может развиваться в ходе беременности или родов; отдельно рассматривается гипоксия, возникшая у ребенка после рождения вследствие болезни гиалиновых мембран, внутриутробной пневмонии и т. д.
При хроническом дефиците кислорода возникает внутриутробная гипотрофия; в случае истощения компенсаторных возможностей плода развиваются те же нарушения, что и при остром варианте течения. Гипоксия плода может развиваться в ходе беременности или родов; отдельно рассматривается гипоксия, возникшая у ребенка после рождения вследствие болезни гиалиновых мембран, внутриутробной пневмонии и т. д.
С учетом компенсаторно-адаптационных возможностей плода гипоксия может приобретать компенсированные, субкомпенсированные и декомпенсированные формы. Поскольку при неблагоприятных условиях плод испытывает не только гипоксию, но и целый комплекс сложных нарушений обмена, в мировой практике данное состояние определяется как «дистресс-синдром», который подразделяется на дородовый, развившийся в родах и респираторный.
Проявления гипоксии плода
Выраженность изменений, развивающихся у плода под воздействием гипоксии, определяется интенсивностью и длительностью испытываемой кислородной недостаточности. Начальные проявления гипоксии вызывают у плода учащение сердцебиения, затем — его замедление и приглушенность тонов сердца. В околоплодных водах может появиться меконий. При гипоксии легкой степени увеличивается двигательная активность плода, при тяжелой – движения урежаются и замедляются.
Начальные проявления гипоксии вызывают у плода учащение сердцебиения, затем — его замедление и приглушенность тонов сердца. В околоплодных водах может появиться меконий. При гипоксии легкой степени увеличивается двигательная активность плода, при тяжелой – движения урежаются и замедляются.
При выраженной гипоксии у плода развиваются нарушения кровообращения: отмечается кратковременный тахикардия и подъем АД, сменяющиеся брадикардией и спадом АД. Реологические нарушения проявляются сгущением крови и выходом плазмы из сосудистого русла, что сопровождается внутриклеточным и тканевым отеком. В результате повышенной ломкости и проницаемости сосудистых стенок возникают кровоизлияния. Снижение тонуса сосудов и замедление кровообращение приводит к ишемизации органов. При гипоксии в организме плода развивается ацидоз, изменяется баланс электролитов, нарушается тканевое дыхание. Изменения в жизненно важных органах плода может вызывать его внутриутробную гибель, асфиксию, внутричерепные родовые травмы.
Диагностика гипоксии плода
Подозрение на то, что плод испытывает гипоксию, могут возникнуть при изменении его двигательной активности – беспокойном поведении, усилении и учащении шевелений. Длительная или прогрессирующая гипоксия приводит к ослаблению шевелений плода. Если женщина замечает такие изменения, ей следует немедленно обратиться к гинекологу, осуществляющему ведение беременности. При прослушивании сердцебиения плода акушерским стетоскопом врач оценивает частоту, звучность и ритм сердечных тонов, наличие шумов. Для выявления гипоксии плода современная гинекология использует проведение кардиотокографии, фонокардиографии плода, допплерометрии, УЗИ, амниоскопии и амниоцентеза, лабораторных исследований.
В ходе кардиотокографии удается отследить ЧСС плода и его двигательную активность. По изменению сердцебиения в зависимости от покоя и активности плода судят о его состоянии. Кардиотокография, наряду с фонокардиографией, широко применяется в родах. При допплерографии маточно-плацентарного кровотокаизучается скорость и характер кровотока в сосудах пуповины и плаценты, нарушение которого приводит к гипоксии плода. Кордоцентез под контролем УЗИ проводится для забора пуповинной крови и исследования кислотно-щелочного равновесия. Эхоскопическим признаком гипоксии плода может служить выявляемая задержка его роста. Кроме того, в процессе акушерского УЗИ оценивается состав, объем и цвет околоплодных вод. Выраженное многоводие или маловодие могут сигнализировать о неблагополучии.
При допплерографии маточно-плацентарного кровотокаизучается скорость и характер кровотока в сосудах пуповины и плаценты, нарушение которого приводит к гипоксии плода. Кордоцентез под контролем УЗИ проводится для забора пуповинной крови и исследования кислотно-щелочного равновесия. Эхоскопическим признаком гипоксии плода может служить выявляемая задержка его роста. Кроме того, в процессе акушерского УЗИ оценивается состав, объем и цвет околоплодных вод. Выраженное многоводие или маловодие могут сигнализировать о неблагополучии.
Проведение амниоскопии и амниоцентеза через канал шейки матки позволяет визуально оценить прозрачность, цвет, количество околоплодной жидкости, наличие в ней включений (хлопьев, мекония), провести биохимические пробы (измерение рН, исследование содержания гормонов, ферментов, концентрации CO2). Амниоскопия противопоказана при предлежании плаценты, кольпите, цервиците, угрозе прерывания беременности. Непосредственная оценка амниотической жидкости осуществляется после ее излития в I периоде родов. В пользу гипоксии плода свидетельствует примесь в околоплодных водах мекония и их зеленоватый цвет.
В пользу гипоксии плода свидетельствует примесь в околоплодных водах мекония и их зеленоватый цвет.
Лечение гипоксии плода
В случае выявления гипоксии плода беременная госпитализируется в акушерско-гинекологический стационар. Наличие гипоксии плода требует коррекции имеющейся акушерской и экстрагенитальной патологии матери и нормализации фетоплацентарного кровообращения. Беременной показан строгий покой, оксигенотерапия. Проводится терапия, направленная на снижение тонуса матки (папаверин, дротаверин, эуфиллин, гексопреналин, тербуталин), уменьшение внутрисосудистой свертываемости (дипиридамол, декстран , гемодериват крови телят, пентоксифиллин).
Хроническая гипоксия плода требует введения препаратов, улучшающих клеточную проницаемость для кислорода и метаболизм (эссенциальных фосфолипидов, витаминов Е, С, В6, глутаминовой кислоты, глюкозы), антигипоксантов, нейропротекторов. При улучшении состояния беременной и уменьшении явлений гипоксии плода беременной может быть рекомендована дыхательная гимнастика, аквагимнастика, УФО, индуктотермия. При неэффективности комплексных мер и сохранении признаков гипоксии плода на сроке свыше 28 недель показано родоразрешение в экстренном порядке (экстренное кесарево сечение).
При неэффективности комплексных мер и сохранении признаков гипоксии плода на сроке свыше 28 недель показано родоразрешение в экстренном порядке (экстренное кесарево сечение).
Роды при хронической гипоксии плода ведутся с использованием кардиомниторинга, позволяющего своевременно применять дополнительные меры. При острой гипоксии, развившейся в родах, ребенку требуется реанимационная помощь. Своевременная коррекция гипоксии плода, рациональное ведение беременности и родов позволяют избежать развития грубых нарушений у ребенка. В дальнейшем все дети, развивавшиеся в условиях гипоксии, наблюдаются у невролога; нередко им требуется помощь психолога и логопеда.
Осложнения гипоксии плода
Тяжелая степень гипоксии плода сопровождается тяжелейшими полиорганными дисфункциями у новорожденного. При гипоксическом поражении ЦНС может развиваться перинатальная энцефалопатия, отек мозга, арефлексия, судороги. Со стороны дыхательной системы отмечаются постгипоксическая пневмопатия, легочная гипертензия; сердечно-сосудистые нарушения включают пороки сердца и сосудов, ишемический некроз эндокарда и др.
Влияние гипоксии плода на почки может проявляться почечной недостаточностью, олигурией; на ЖКТ – срыгиваниями, рвотой, энтероколитом. Нередко вследствие тяжелой перинатальной гипоксии у новорожденного развиваются ДВС-синдром, вторичный иммунодефицит. Асфиксия новорожденных в 75-80% случаев развивается на фоне предшествующей гипоксии плода.
Профилактика гипоксии плода
Предупреждение развития гипоксии плода требует от женщины ответственной подготовки к беременности: лечения экстрагенитальной патологии и заболеваний органов репродуктивной системы, отказ от нездоровых привычек, рациональное питание. Ведение беременности должно осуществляться с учетом факторов риска и своевременным контролем за состоянием плода и женщины. Недопущение развития острой гипоксии плода заключается в правильном выборе способа родоразрешения, профилактике родовых травм.
Гипоксия плода последствия для ребенка, кислородное голодание у новорожденного при родах
Гипоксия плода – такой диагноз все чаще ставят будущим мамам. В сущности, она является не болезнью, а состоянием острой нехватки кислорода у ребенка. Когда голодание находится на начальной стадии, его достаточно просто устранить, при этом оно не повлечет каких-либо существенных последствий. Если же меры не будут предприняты вовремя, осложнений будет не избежать. Последствия гипоксии плода для ребенка имеют очень серьезный характер.
В сущности, она является не болезнью, а состоянием острой нехватки кислорода у ребенка. Когда голодание находится на начальной стадии, его достаточно просто устранить, при этом оно не повлечет каких-либо существенных последствий. Если же меры не будут предприняты вовремя, осложнений будет не избежать. Последствия гипоксии плода для ребенка имеют очень серьезный характер.
При сильной нехватке кислорода малыш теряет свои жизненные силы. Долго находиться в таком состоянии нельзя: либо ребенок приобретет серьезное заболевание, либо гипоксия приведет к летальному исходу. Стоит учитывать, что недуг не так сложно распознать. Если женщина будет внимательно прислушиваться к себе и своему малышу, она сможет предупредить развитие этого недуга и изменить ситуацию. Будущая мама должна испытывать только положительные эмоции.
Содержание статьи
- 1 Гипоксия плода и ее последствия
- 2 Причины и признаки гипоксии
- 3 Процессы протекающие в организме плода
Не нужно доводить заботу о ребенке до паранойи, бесконечно выискивая в поведении плода и своем состоянии признаки появления гипоксии. Чтобы избежать этого достаточно знать причины и факторы риска возникновения недуга. Читая статью дальше, можно узнать всю необходимую информацию.
Чтобы избежать этого достаточно знать причины и факторы риска возникновения недуга. Читая статью дальше, можно узнать всю необходимую информацию.
Гипоксия плода и ее последствия
Гипоксия – это кислородное голодание плода. Причины ее появления могут быть разными, в зависимости от ее разновидности: внутриутробная либо интранатальная. Первая получается в процессе беременности и зависит от поведения и состояния матери, а вторая происходит во время родов и, по большей части, зависит от действий врачей. Есть две формы гипоксии: острая и хроническая. Первая из них менее распространена, но имеет более серьезные последствия. ХВГП – это внутриутробное состояние постоянной нехватки кислорода. При этом очень сильно страдает развитие малыша. Существует риск преждевременных родов и появления недоношенного младенца.
При острой гипоксии полностью прекращается поступление кислорода в организм плода. Это может происходить как в утробе матери, так и во время родов. Чаще всего такая ситуация возникает в результате обвития пуповины вокруг шеи ребенка. Уже через 15 секунд отсутствия кислорода клетки мозга начинают отмирать. Врачи должны исправить ситуацию так скоро, как будет возможно. В этом случае полностью избежать серьезных последствий нельзя, но можно свести их к допустимому минимуму. Последствия гипоксии плода у ребенка после рождения в большинстве случаев могут быть диагностированы сразу. Особенно это касается тяжелых случаев.
Уже через 15 секунд отсутствия кислорода клетки мозга начинают отмирать. Врачи должны исправить ситуацию так скоро, как будет возможно. В этом случае полностью избежать серьезных последствий нельзя, но можно свести их к допустимому минимуму. Последствия гипоксии плода у ребенка после рождения в большинстве случаев могут быть диагностированы сразу. Особенно это касается тяжелых случаев.
Кислородное голодание плода при беременности может привести к следующим последствиям для ребенка:
- отставание в физическом развитии;
- задержка умственного развития;
- болезни органов вследствие их недоразвитости;
- заболевания нервной системы, в частности болезни мозга.
Отсутствие кислорода пагубно сказывается на всем организме плода, но больший урон такое состояние наносит его мозгу. За время голодания в нем может случиться кровоизлияние, образоваться отек и произойти другие серьезные процессы. Как следствие этого у ребенка в младенчестве или в старшем возрасте могут проявляться различные неврологические недуги. Серьезным последствием гипоксии является ДЦП. В крайнем случае может произойти остановка сердца и гибель мозга.
Серьезным последствием гипоксии является ДЦП. В крайнем случае может произойти остановка сердца и гибель мозга.
Видео
Самым легким осложнением считается слабый иммунитет. Такие дети больше других подвержены простудным заболеваниям. Независимо от того, какой тяжести была гипоксия, в дальнейшем потребуется соответствующее лечение. Так или иначе, ребенок должен будет наблюдаться у невропатолога, который при необходимости назначит терапию.
Обратите внимание! Устранение последствий гипоксии нужно начинать сразу после родов. В роддоме специалистами будут назначены медикаменты и необходимые процедуры.
Если гипоксию не удается предотвратить, необходимо предпринять все меры, чтобы свести к минимуму ее последствия. В случае, если помимо нарушений функций нервной системы не было обнаружено патологий других органов, лечением ребенка первое время будет заниматься только невропатолог. В процессе развития может потребоваться помощь логопеда и психолога.
В процессе развития может потребоваться помощь логопеда и психолога.
Причины и признаки гипоксии
Внутриутробная гипоксия появляется в процессе вынашивания плода. По сравнению с острой формой, ее последствия не так очевидны. Родовая гипоксия возникает во период с начала схваток до момента перерезания пуповины. Причины образования этого состояния у двух этих форм различны.
Факторы образования гипоксии приведены в таблице:
| Внутриутробная | Родовая |
| Многоплодие | Многоплодие |
| Угроза прерывания беременности, кровотечение | Преждевременная отслойка плаценты |
| Перенашивание | Многоводие |
| Употребление наркотических веществ матерью | Слабая родовая деятельность |
| Курение матери | Обвитие шеи пуповиной |
| Диабет и инфекции | Неоправданная стимуляция родов |
| Серьезные болезни в период вынашивания |
Это неполный перечень причин, которые могут привести к кислородному голоданию. Симптомы возникновения этого состояния, соответственно, отличаются. При внутриутробной гипоксии, женщина может судить о состоянии малыша по его движениям. При снижении количества поступающего кислорода, плод начинает активно двигаться. Через некоторое время его шевеления становятся все слабее. В конечном счете они могут совсем пропасть. Другими признаками этого явления являются задержка в росте и развитии малыша, патологическое уменьшение околоплодной жидкости, опускание матки. Последние признаки невозможно определить без проведения УЗИ. Помимо этого, врачи могут провести ряд других исследований, позволяющих получить более полное представление о состоянии плода. К ним относятся КГТ, БФП, НСТ, ЭГК плода. Так же могут быть проведены исследования крови малыша. В случае обнаружения недуга, женщине назначают необходимое лечение. Хроническую гипоксию можно распознать во время родов. О наличии ее и степени тяжести будет свидетельствовать цвет околоплодных вод.
Симптомы возникновения этого состояния, соответственно, отличаются. При внутриутробной гипоксии, женщина может судить о состоянии малыша по его движениям. При снижении количества поступающего кислорода, плод начинает активно двигаться. Через некоторое время его шевеления становятся все слабее. В конечном счете они могут совсем пропасть. Другими признаками этого явления являются задержка в росте и развитии малыша, патологическое уменьшение околоплодной жидкости, опускание матки. Последние признаки невозможно определить без проведения УЗИ. Помимо этого, врачи могут провести ряд других исследований, позволяющих получить более полное представление о состоянии плода. К ним относятся КГТ, БФП, НСТ, ЭГК плода. Так же могут быть проведены исследования крови малыша. В случае обнаружения недуга, женщине назначают необходимое лечение. Хроническую гипоксию можно распознать во время родов. О наличии ее и степени тяжести будет свидетельствовать цвет околоплодных вод.
Гипоксию, полученную во время родов, распознать проще. Ребенок уже родился, его легче осмотреть и, в случае необходимости, предпринять требуемые меры. Если из-за зажатой пуповины кровь не поступает ребенку, а сам он не задышал, кислород полностью прекращает поступать в его организм. Новорожденный может посинеть, он не кричит и не шевелится. В этом случае врачи начинают реанимировать его.
Ребенок уже родился, его легче осмотреть и, в случае необходимости, предпринять требуемые меры. Если из-за зажатой пуповины кровь не поступает ребенку, а сам он не задышал, кислород полностью прекращает поступать в его организм. Новорожденный может посинеть, он не кричит и не шевелится. В этом случае врачи начинают реанимировать его.
Важно! Частая причина гипоксии – преждевременная неоправданная стимуляция родоразрешения. Организм ребенка не успевает подготовиться и, в результате слишком стремительных родов, получает родовую травму.
Многие акушеры, стремясь как можно быстрее провести роды, прибегают к стимуляции. Часто это происходит и в тех случаях, где подобные меры не являлись необходимостью. О губительности такого подхода было отмечено ранее. Не стоит пугаться всех врачей. Для того чтобы обезопасить себя и малыша, нужно заранее определиться с роддомом и акушером, который будет принимать роды.
Процессы протекающие в организме плода
Не нужно бояться появления гипоксии. Далеко не все дети подвержены этому явлению. Стрессы во время беременности могут негативно сказываться на малыше. Для того чтобы помочь, а не навредить своему ребенку, нужно трезво оценивать ситуацию. Детально изучив вопрос и разобравшись в причинах появления недуга, можно постараться его избежать или предотвратить. Узнать, какие исследования нужно проходить до родов, и как правильно следить за своим самочувствием и поведением плода можно просмотрев это видео:
Далеко не все дети подвержены этому явлению. Стрессы во время беременности могут негативно сказываться на малыше. Для того чтобы помочь, а не навредить своему ребенку, нужно трезво оценивать ситуацию. Детально изучив вопрос и разобравшись в причинах появления недуга, можно постараться его избежать или предотвратить. Узнать, какие исследования нужно проходить до родов, и как правильно следить за своим самочувствием и поведением плода можно просмотрев это видео:
Видео
Не стоит думать, что при малейшем недостатке кислорода развивается хроническая гипоксия. Природа сама защищает плод, и он способен некоторое время противостоять этому состоянию.
Это происходит благодаря тому что:
- кровь, циркулирующая в сосудах плода, содержит больше кислорода, чем у взрослого человека;
- гемоглобин имеет особую структуру;
- строение сердечно-сосудистой системы направлено на защиту от гипоксии;
- при недостатке кислорода надпочечники начинают интенсивно впрыскивать в кровь гормоны, способствующие учащению ритма сердца.

С гипоксией, полученной во время родов организм не сможет бороться таким образом. Все эти процессы помогают плоду нормально развиваться в условиях недостаточности кислорода. Если это время продлится недолго, оно никак не скажется на росте ребенка. В противном случае организм будет истощен и не сможет бороться с кислородным голоданием. Внутриутробная гипоксия может привести к тому, что меконий из кишечника попадет в амниотическую жидкость. Это произойдет в результате недостаточного снабжения кровью мышц заднего прохода.
Это важно! Наличие мекония в околоплодных водах – очень опасное для малыша обстоятельство. Прежде всего, его наличие свидетельствует о наличии кислородного голодания. Кроме того, при тяжелых затяжных родах ребенок может начать дышать, находясь в утробе матери. Вместе с водами он «вдохнет» кал.
В таких случаях врач сразу после родов удаляет из легких жидкость. Частицы первородного кала, оставшиеся в них, могут привести к пневмонии. В любом случае, наличие в амниотической жидкости каких-либо частиц говорит о тяжелой степени гипоксии. В этом случае незамедлительно назначается послеродовое лечение. Мама, заботящаяся о здоровье своего будущего ребенка, должна знать, какие бывают симптомы и последствия гипоксии у новорожденного. Это поможет избежать появление такого серьезного недуга. Кроме того, беременная должна придерживаться здорового образа жизни: соблюдать режим сна, правильно питаться, воздерживаться от употребления алкоголя, сигарет и наркотиков, чаще находится на свежем воздухе. Рождение здорового ребенка – вот к чему она должна стремится. Матерям, чьи дети были подвержены гипоксии до или во время родов, не нужно отчаиваться. Они должны направить все свои силы на исправление последствий, чтобы в будущем здоровье малыша не доставляло ему проблем.
В любом случае, наличие в амниотической жидкости каких-либо частиц говорит о тяжелой степени гипоксии. В этом случае незамедлительно назначается послеродовое лечение. Мама, заботящаяся о здоровье своего будущего ребенка, должна знать, какие бывают симптомы и последствия гипоксии у новорожденного. Это поможет избежать появление такого серьезного недуга. Кроме того, беременная должна придерживаться здорового образа жизни: соблюдать режим сна, правильно питаться, воздерживаться от употребления алкоголя, сигарет и наркотиков, чаще находится на свежем воздухе. Рождение здорового ребенка – вот к чему она должна стремится. Матерям, чьи дети были подвержены гипоксии до или во время родов, не нужно отчаиваться. Они должны направить все свои силы на исправление последствий, чтобы в будущем здоровье малыша не доставляло ему проблем.
Статины и влияние на сохранение мозга плода при гипоксии
Статины и влияние на сохранение мозга плода при гипоксии
Наше время в утробе матери не простое.
 Как растущий плод, наши делящиеся клетки требуют соответствующего количества питательных веществ и кислорода. Ограничение этого запаса может привести к быстрому ухудшению состояния плода, что может привести к летальному исходу или вызвать серьезные долгосрочные последствия. Статины помогают или вредят гипоксическому плоду?
Как растущий плод, наши делящиеся клетки требуют соответствующего количества питательных веществ и кислорода. Ограничение этого запаса может привести к быстрому ухудшению состояния плода, что может привести к летальному исходу или вызвать серьезные долгосрочные последствия. Статины помогают или вредят гипоксическому плоду?
Характеристики
Эндрю Кейн, Эмилио Эррера, Авнеш Такор и Дино Джуссани
Кембриджский университет, Великобритания
https://doi.org/10.36866/pn.92.42
К сожалению, несмотря на достижения в клинической акушерской практике возникновение снижения оксигенации плода или гипоксии представляет собой распространенную серьезную проблему со значительной вероятностью долгосрочной заболеваемости (например, гипоксически-ишемической энцефалопатии и церебрального паралича) или смертности пораженного новорожденного (Low, 2004). Гипоксия плода при неблагоприятном течении беременности может возникнуть при преэклампсии, плацентарной недостаточности, отслойке плаценты или окклюзии пуповины. Гипоксия плода также может возникать из-за состава окружающей среды матери (например, большая высота, загрязненный воздух, дым и угарный газ), сердечно-легочного заболевания матери или в результате анемии матери.
Гипоксия плода при неблагоприятном течении беременности может возникнуть при преэклампсии, плацентарной недостаточности, отслойке плаценты или окклюзии пуповины. Гипоксия плода также может возникать из-за состава окружающей среды матери (например, большая высота, загрязненный воздух, дым и угарный газ), сердечно-легочного заболевания матери или в результате анемии матери.
Индивидуальная стратегия противостояния эпизодам гипоксии различается во внутриутробном и постнатальном периодах жизни. Проще говоря, в постнатальный период нашей физиологической реакцией на острую гипоксию является увеличение скорости альвеолярной вентиляции и сердечного выброса, а также снижение сопротивления периферических сосудов в попытке сохранить доставку кислорода кровью к нашим дышащим тканям. Однако плод не обладает такой способностью повышать легочную оксигенацию и должен выживать при любом снижении доставки кислорода, вызванном плацентой или материнской средой. Используя плод овцы на поздних сроках беременности в качестве предпочтительной животной модели, было показано, что стратегия плода заключается в том, чтобы наилучшим образом использовать доступное снабжение кислородом, перераспределяя сердечный выброс от периферических органов, таких как кишечник и конечности, к периферическим органам. более существенные кровообращения, такие как те, которые перфузируют мозг плода (Cohn и др. 1974). Эта «щадящая мозг» защита от острой гипоксии во время внутриутробного развития достигается за счет скоординированных нервных, эндокринных и метаболических механизмов. Мы знаем, что плод может ощущать гипоксию через хеморецепторы каротидного тела и что эта информация передается в мозг плода через языкоглоточные нервы (Giussani et al. 1993). В свою очередь, происходит активация как симпатического, так и парасимпатического отделов вегетативной нервной системы. Нервный компонент симпатической нервной системы вызывает сужение сосудов периферического кровообращения, что приводит к увеличению периферического сосудистого сопротивления и уменьшению периферического кровотока. Напротив, церебральное сосудистое сопротивление снижается, направляя большую часть кровотока в мозг плода (Rudolph, 19).84; Джуссани и др. 1993 г.). Если период гипоксии длительный и/или тяжелый, плод высвобождает широкий спектр агентов в кровоток плода, включая катехоламины, кортизол, ангиотензин II, вазопрессин и нейропептид Y, которые поддерживают периферическую вазоконстрикцию и, тем самым, перераспределение кровоток (Giussani et al.
более существенные кровообращения, такие как те, которые перфузируют мозг плода (Cohn и др. 1974). Эта «щадящая мозг» защита от острой гипоксии во время внутриутробного развития достигается за счет скоординированных нервных, эндокринных и метаболических механизмов. Мы знаем, что плод может ощущать гипоксию через хеморецепторы каротидного тела и что эта информация передается в мозг плода через языкоглоточные нервы (Giussani et al. 1993). В свою очередь, происходит активация как симпатического, так и парасимпатического отделов вегетативной нервной системы. Нервный компонент симпатической нервной системы вызывает сужение сосудов периферического кровообращения, что приводит к увеличению периферического сосудистого сопротивления и уменьшению периферического кровотока. Напротив, церебральное сосудистое сопротивление снижается, направляя большую часть кровотока в мозг плода (Rudolph, 19).84; Джуссани и др. 1993 г.). Если период гипоксии длительный и/или тяжелый, плод высвобождает широкий спектр агентов в кровоток плода, включая катехоламины, кортизол, ангиотензин II, вазопрессин и нейропептид Y, которые поддерживают периферическую вазоконстрикцию и, тем самым, перераспределение кровоток (Giussani et al. 1994). Кроме того, у плода возникает метаболический ответ. Гипоксия приводит к увеличению анаэробного дыхания с меньшим образованием АТФ на единицу глюкозы. Таким образом, повышение уровня катехоламинов в плазме плода вызывает гипергликемический ответ, возникающий в результате снижения поглощения и утилизации глюкозы периферическими тканями и увеличения продукции глюкозы в печени путем стимуляции гликогенолиза и глюконеогенеза (Jones, 19).77; Джонс и др. . 1983). Молочнокислая ацидемия плода возникает из-за анаэробного метаболизма глюкозы в гипоксических тканях плода, особенно в задних конечностях, где кровоток и доставка кислорода заметно снижаются (Boyle et al , 1990). Интересно, что многие аспекты этой защиты плода от гипоксии хорошо сохраняются у разных видов, от рептилий до птиц и млекопитающих, включая нечеловеческих приматов и человеческий плод (Giussani, 2006).
1994). Кроме того, у плода возникает метаболический ответ. Гипоксия приводит к увеличению анаэробного дыхания с меньшим образованием АТФ на единицу глюкозы. Таким образом, повышение уровня катехоламинов в плазме плода вызывает гипергликемический ответ, возникающий в результате снижения поглощения и утилизации глюкозы периферическими тканями и увеличения продукции глюкозы в печени путем стимуляции гликогенолиза и глюконеогенеза (Jones, 19).77; Джонс и др. . 1983). Молочнокислая ацидемия плода возникает из-за анаэробного метаболизма глюкозы в гипоксических тканях плода, особенно в задних конечностях, где кровоток и доставка кислорода заметно снижаются (Boyle et al , 1990). Интересно, что многие аспекты этой защиты плода от гипоксии хорошо сохраняются у разных видов, от рептилий до птиц и млекопитающих, включая нечеловеческих приматов и человеческий плод (Giussani, 2006).
Плод человека в ближайшем будущем в утробе матери с предлежанием плаценты. Это пластина XII из 9 Уильяма Хантера. 0022 Anatamio uteri humani tabulis illustrata , Анатомия беременной матки человека, представленная в рисунках. Birmingham, John Baskerville, 1774.
0022 Anatamio uteri humani tabulis illustrata , Анатомия беременной матки человека, представленная в рисунках. Birmingham, John Baskerville, 1774.
В последнее время работа в нашей лаборатории была сосредоточена на изучении вклада самой сосудистой сети плода в перераспределение кровотока плода во время острой гипоксии. В дополнение к нейроэндокринному контролю в настоящее время признано, что клеточная оксидантная среда является важным модулятором сосудистого сопротивления (Chen & Keaney, 2004; Valko et al. 9).0023 2007). Установлено, что во взрослой сосудистой системе увеличивается продукция аниона супероксида (·O2–), который будет реагировать с оксидом азота (NO), снижая его биодоступность. Таким образом, увеличение сосудистого соотношения ·O2–:NO будет способствовать вазоконстрикции, а наоборот – расширению сосудов. Активные формы кислорода (АФК) генерируются через прооксидантные системы, включая митохондриальную цепь переноса электронов, несвязанную eNOS, ксантиноксидазу, НАДФН-оксидазу и цитохром Р450. В нормальных физиологических условиях АФК постоянно расщепляются за счет антиоксидантной защиты, включая ферментативную утилизацию супероксиддисмутазой, каталазой и глутатионпероксидазой и/или молекулами, удаляющими свободные радикалы, такими как витамины С и Е, мелатонин и каротины (Valko 9).0022 и др. 2007 г.). Однако при более высоких концентрациях ·O2– может вступать в реакцию с NO вместо того, чтобы разрушаться или связываться с молекулой антиоксиданта, тем самым оказывая влияние на сердечно-сосудистую регуляцию. В кровообращении плода в течение некоторого времени было признано, что NO способствует поддержанию кровотока во многих сосудистых руслах, включая пупочное, мозговое, миокардиальное, бедренное и каротидное кровообращение, поскольку ингибирование синтеза NO приводит к выраженному увеличению сосудистого русла. сопротивление. Также известно, что при острой гипоксии усиленный NO противостоит хеморефлексным и эндокринным вазоконстрикторным влияниям в бедренном сосудистом русле, тем самым тонко настраивая периферический вазоконстрикторный ответ плода на гипоксию (Morrison 9).
В нормальных физиологических условиях АФК постоянно расщепляются за счет антиоксидантной защиты, включая ферментативную утилизацию супероксиддисмутазой, каталазой и глутатионпероксидазой и/или молекулами, удаляющими свободные радикалы, такими как витамины С и Е, мелатонин и каротины (Valko 9).0022 и др. 2007 г.). Однако при более высоких концентрациях ·O2– может вступать в реакцию с NO вместо того, чтобы разрушаться или связываться с молекулой антиоксиданта, тем самым оказывая влияние на сердечно-сосудистую регуляцию. В кровообращении плода в течение некоторого времени было признано, что NO способствует поддержанию кровотока во многих сосудистых руслах, включая пупочное, мозговое, миокардиальное, бедренное и каротидное кровообращение, поскольку ингибирование синтеза NO приводит к выраженному увеличению сосудистого русла. сопротивление. Также известно, что при острой гипоксии усиленный NO противостоит хеморефлексным и эндокринным вазоконстрикторным влияниям в бедренном сосудистом русле, тем самым тонко настраивая периферический вазоконстрикторный ответ плода на гипоксию (Morrison 9). 0022 и др. 2003). Однако роль свободных радикалов и их взаимодействия с NO в контроле кровообращения плода в норме или при патологии до недавнего времени не была установлена.
0022 и др. 2003). Однако роль свободных радикалов и их взаимодействия с NO в контроле кровообращения плода в норме или при патологии до недавнего времени не была установлена.
Работа в нашей лаборатории показала, что лечение плода овцы антиоксидантами витамином С или мелатонином, которые способны гасить кислород в кровотоке, способствует значительной вазодилатации в пупочном сосудистом русле, что приводит к значительному увеличению пуповинного кровотока. (Такор и л. 2010а). В другом исследовании, опубликованном в The Journal of Physiology, лечение плода витамином С приводило к расширению бедренной сосудистой сети плода во время исходных состояний и нарушало реакцию бедренного констриктора плода на острую гипоксию (рис. 1; Thakor et al. 2010b). Данные свидетельствуют о том, что антиоксидантная секвестрация O2– внутри сосудистой сети плода и предотвращение реакции с NO повышают биодоступность NO, способствуя расширению сосудов и, таким образом, увеличивая кровоток в исходных условиях и противодействуя периферическим вазоконстрикторным влияниям во время стимулированных состояний, таких как при гипоксии плода. Позже это было подтверждено лечением плода антиоксидантами в присутствии NO-зажима, in vivo , который блокирует синтез NO, не влияя на базальную сердечно-сосудистую функцию (Gardner & Giussani, 2003), восстанавливал величину периферической вазоконстрикции плода (рис. 1).
Позже это было подтверждено лечением плода антиоксидантами в присутствии NO-зажима, in vivo , который блокирует синтез NO, не влияя на базальную сердечно-сосудистую функцию (Gardner & Giussani, 2003), восстанавливал величину периферической вазоконстрикции плода (рис. 1).
Рис. 1. Сопротивление бедренных сосудов в течение 1 ч нормоксии, 0,5 ч гипоксии (пунктирная рамка) и 1 ч восстановления плода овцы на поздних сроках беременности при инфузии физиологического раствора (n = 6/7), лечении витамином С или правастатином (n = 6/7) или лечение витамином С или правастатином во время клэмпа NO (n = 6/7). Значения представляют собой среднее ± SEM, рассчитываемое каждую минуту. Эксперименты с витамином С или с правастатином взяты из разных исследований. Изменено с Thakor и др. (2010b) и Кейн и др. (2012).
Открытие действия оксидантного тонуса в сосудистой сети плода и его манипуляции с антиоксидантами, вызывающими изменения в кровотоке, имеют важные последствия для использования во время беременности лекарств, повышающих биодоступность NO. Одним из таких примеров являются ингибиторы ГМГ-КоА-редуктазы. Статины подавляют лимитирующую стадию синтеза холестерина и поэтому стали одними из наиболее эффективных и широко назначаемых препаратов для первичной и вторичной профилактики ишемической болезни сердца (Steinberg, 2008). В дополнение к их липидоснижающему действию были отмечены дополнительные положительные эффекты на кровообращение, включая снижение жесткости артерий, снижение агрегации тромбоцитов и улучшение функции эндотелия сосудов. Эти преимущества объясняются вызванным статинами повышением биодоступности NO и усилением функции NO с помощью различных механизмов (Adam & Laufs, 2008). Принимая во внимание растущий уровень ожирения и связанных с ним нарушений липидного обмена у молодых людей (Национальный центр статистики болезней, 2011 г.), а также тот факт, что женщины откладывают рождение ребенка до четвертого или пятого десятилетия жизни (Хеффнер, 2004 г.), клинический интерес к возможности для лечения беременных женщин статинами, если это необходимо.
Одним из таких примеров являются ингибиторы ГМГ-КоА-редуктазы. Статины подавляют лимитирующую стадию синтеза холестерина и поэтому стали одними из наиболее эффективных и широко назначаемых препаратов для первичной и вторичной профилактики ишемической болезни сердца (Steinberg, 2008). В дополнение к их липидоснижающему действию были отмечены дополнительные положительные эффекты на кровообращение, включая снижение жесткости артерий, снижение агрегации тромбоцитов и улучшение функции эндотелия сосудов. Эти преимущества объясняются вызванным статинами повышением биодоступности NO и усилением функции NO с помощью различных механизмов (Adam & Laufs, 2008). Принимая во внимание растущий уровень ожирения и связанных с ним нарушений липидного обмена у молодых людей (Национальный центр статистики болезней, 2011 г.), а также тот факт, что женщины откладывают рождение ребенка до четвертого или пятого десятилетия жизни (Хеффнер, 2004 г.), клинический интерес к возможности для лечения беременных женщин статинами, если это необходимо. Действительно, в одно большое рандомизированное многоцентровое клиническое исследование был начат набор пациентов в Соединенном Королевстве для изучения того, может ли правастатин снижать циркулирующие антиангиогенные факторы, связанные с преэклампсией (исследование «StAmP»; Ahmed, 2011). В другом недавнем исследовании, опубликованном в The Journal of Physiology, вазоконстрикторная реакция плода на острую гипоксию оценивалась в контрольных условиях и после лечения клинически значимой дозой правастатина (Kane 9).0022 и др. 2012). Эксперименты показали, что воздействие правастатина на плод угнетало периферические сосудосуживающие реакции плода на острую гипоксию (см. рис. 1). Кроме того, эти эффекты можно было предотвратить у эмбрионов овец, получавших правастатин в условиях клампирования NO, демонстрируя, что повышение уровней NO при лечении правастатином способствовало подавлению бедренной вазоконстрикции в результате гипоксии. Данные подтверждают гипотезу о том, что статины повышают биодоступность NO и противостоят нейроэндокринным влияниям, которые опосредуют периферическую вазоконстрикцию и метаболические реакции на гипоксический стресс у плода.
Действительно, в одно большое рандомизированное многоцентровое клиническое исследование был начат набор пациентов в Соединенном Королевстве для изучения того, может ли правастатин снижать циркулирующие антиангиогенные факторы, связанные с преэклампсией (исследование «StAmP»; Ahmed, 2011). В другом недавнем исследовании, опубликованном в The Journal of Physiology, вазоконстрикторная реакция плода на острую гипоксию оценивалась в контрольных условиях и после лечения клинически значимой дозой правастатина (Kane 9).0022 и др. 2012). Эксперименты показали, что воздействие правастатина на плод угнетало периферические сосудосуживающие реакции плода на острую гипоксию (см. рис. 1). Кроме того, эти эффекты можно было предотвратить у эмбрионов овец, получавших правастатин в условиях клампирования NO, демонстрируя, что повышение уровней NO при лечении правастатином способствовало подавлению бедренной вазоконстрикции в результате гипоксии. Данные подтверждают гипотезу о том, что статины повышают биодоступность NO и противостоят нейроэндокринным влияниям, которые опосредуют периферическую вазоконстрикцию и метаболические реакции на гипоксический стресс у плода.
На первый взгляд, результаты кажутся тревожными, учитывая клинический интерес к использованию статинов при осложненной беременности. Статины могут нарушать щадящую реакцию мозга плода на гипоксию при рождении. Однако поддержание или увеличение мозгового кровотока и, следовательно, доставки в мозг кислорода и питательных веществ, что щадит мозг плода во время эпизодов гипоксии или асфиксии, зависит не только от вазоконстрикции в периферических сосудистых руслах, но и от активной вазодилатации в мозговое кровообращение. Действительно, это опосредовано механизмами, включающими повышенное содержание NO (зеленый и др. 1996), а в нескольких исследованиях сообщалось о сохранении увеличения цереброваскулярной перфузии при острой гипоксии даже при полном отсутствии периферической вазоконстрикции, например, при денервации каротидного синуса или блокаде α1-адренергических рецепторов (Giussani et al. 1993). Следовательно, в суженных сосудах, таких как бедренные сосуды, повышенная биодоступность NO может уменьшать периферическую вазоконстрикцию. Однако в сосудах, которые расширяются, в частности, за счет NO-зависимых механизмов во время острой гипоксии, таких как церебральное сосудистое русло, повышенная биодоступность NO может фактически увеличить мозговой кровоток. Следовательно, в условиях воздействия на плод статинов или антиоксидантов стратегия защиты сердечно-сосудистой системы плода от гипоксии может измениться, чтобы увеличить сердечный выброс и поддерживать перфузию в большинстве циркуляционных систем. Очевидно, что существует острая необходимость в оценке влияния воздействия антиоксидантов или статинов на изменения мозгового кровотока и доставки кислорода плода, а также на периферическое кровообращение плода во время острой гипоксии плода. На данный момент мы предлагаем рассматривать использование статинов или антиоксидантов во время беременности с особой осторожностью.
Однако в сосудах, которые расширяются, в частности, за счет NO-зависимых механизмов во время острой гипоксии, таких как церебральное сосудистое русло, повышенная биодоступность NO может фактически увеличить мозговой кровоток. Следовательно, в условиях воздействия на плод статинов или антиоксидантов стратегия защиты сердечно-сосудистой системы плода от гипоксии может измениться, чтобы увеличить сердечный выброс и поддерживать перфузию в большинстве циркуляционных систем. Очевидно, что существует острая необходимость в оценке влияния воздействия антиоксидантов или статинов на изменения мозгового кровотока и доставки кислорода плода, а также на периферическое кровообращение плода во время острой гипоксии плода. На данный момент мы предлагаем рассматривать использование статинов или антиоксидантов во время беременности с особой осторожностью.
Ссылки
Adam O & Laufs U (2008). Антиоксидантные эффекты статинов. Arch Toxicol 82 , 885–892.
Ахмед А. (2011 г.). Новый взгляд на этиологию преэклампсии: выявление ключевых неуловимых факторов сосудистых осложнений. Исследование тромбоза: Статьи и тезисы 4-го Международного симпозиума по проблемам женского здоровья при тромбозе и гемостазе 127 , S72–S75.
Бойл Д.В., Херст К., Зербе Г.О., Месхия Г. и Вилкенинг Р.Б. (1990). Потребление кислорода задними конечностями плода и кровоток во время острой гипоксии. Pediatr Res 28 , 94–100.
Чен К. и Кини Дж. Ф. (2004). Опосредованная активными формами кислорода передача сигнала в эндотелии. Эндотелий 11 , 109–121.
Кон Х.Е., Сакс Э.Дж., Хейманн М.А. и Рудольф А.М. (1974). Сердечно-сосудистые реакции на гипоксемию и ацидемию у плодов ягнят. Am J Obstet Gynecol 120 , 817–824.
Гарднер Д.С. и Джуссани Д.А. (2003). Усиление пуповинного кровотока при острой гипоксемии после хронической компрессии пуповины: роль оксида азота. Тираж 108 , 331–335.
Тираж 108 , 331–335.
Джуссани Д.А. (2006 г.). Пренатальная гипоксия: отношение к истокам развития здоровья и болезней. In Development Origins of Health and Disease , ed. Глюкман П.Д. и Хэнсон М.А., стр. 178–190. Издательство Кембриджского университета, Кембридж.
Джуссани Д.А., Спенсер Дж.А. и Хэнсон М.А. (1994). Рефлекторные реакции сердечно-сосудистой системы плода на острую гипоксемию. Fetal Matern Med Rev 6 17–37.
Джуссани Д.А., Спенсер Дж.А., Мур П.Дж., Беннет Л. и Хэнсон М.А. (1993). Афферентные и эфферентные компоненты сердечно-сосудистых рефлекторных ответов на острую гипоксию у доношенных плодов овец. J Physiol 461 , 431–449.
Грин Л.Р., Беннет Л. и Хэнсон М.А. (1996). Роль синтеза оксида азота в сердечно-сосудистых реакциях на острую гипоксию у плода овцы на поздних сроках беременности. J Physiol 497 , 271–277.
Хеффнер Л. Дж. (2004 г.). Преклонный материнский возраст – сколько лет считается слишком старым? N Engl J Med 351 , 1927–1929 гг.
Дж. (2004 г.). Преклонный материнский возраст – сколько лет считается слишком старым? N Engl J Med 351 , 1927–1929 гг.
Джонс CT (1977). Развитие некоторых метаболических реакций на гипоксию у плода овцы. J Physiol 265 , 743–762.
Джонс К.Т., Ричи Дж.В. и Уокер Д. (1983). Влияние гипоксии на обмен глюкозы у эмбрионов овец. J Dev Physiol 5 , 223–235.
Кейн А.Д., Эррера Э.А., Ханселл Дж.А. и Джуссани Д.А. (2012). Лечение статинами снижает защиту плода от острой гипоксии за счет повышения биодоступности оксида азота. J Physiol 590 , 323–334.
Низкий JA (2004 г.). Размышления о возникновении и значении дородовой асфиксии плода. Best Pract Res Clin Obstet Gynaecol 18 , 375–382.
Моррисон С., Гарднер Д.С., Флетчер А.Дж., Блумфилд М.Р. и Джуссани Д.А. (2003). Повышенная активность оксида азота компенсирует периферическую вазоконстрикцию во время острой гипоксемии за счет хеморефлексного и адреномедуллярного действия у плода овцы. J Physiol 547 , 283–291.
J Physiol 547 , 283–291.
Национальный центр статистики здравоохранения (2011 г.). H alth, США, 2010 г.: специальный материал о смерти и умирании . Национальный центр медицинской статистики, Хайяттсвилль, Мэриленд, США.
Рудольф А.М. (1984). Кровообращение плода и его реакция на стресс. J Dev Physiol 6 , 11–19.
Стейнберг Д. (2008 г.). Статины в профилактической кардиологии. N Engl J Med 359 , 1426–1427.
Такор А.С., Эррера Э.А., Серон-Ферре М. и Джуссани Д.А. (2010a). Мелатонин и витамин С увеличивают пуповинный кровоток через механизмы, зависящие от оксида азота. J Pineal Res 49 , 399–406.
Такор А.С., Рихтер Х.Г., Кейн А.Д., Данстер С., Келли Ф.Дж., Постон Л. и Джуссани Д.А. (2010b). Окислительно-восстановительная модуляция сердечно-сосудистой защиты плода от гипоксемии. J Physiol 588 , 4235–4247.
Валко М., Лейбфриц Д., Монкол Дж., Кронин М., Мазур М. и Телсер Дж. (2007). Свободные радикалы и антиоксиданты в нормальных физиологических функциях и заболеваниях человека. Int J Biochem Cell Biol 39 , 44–84.
Интранатальная асфиксия
по
Jan Stener Jørgensen
Газы крови/кислотно-щелочное Неонатология Глюкоза Лактат
Таким образом, EFM используется уже почти полвека. Первоначально предполагалось, что EFM предотвратит интранатальную асфиксию, что, как мы надеемся, сведет к минимуму частоту церебрального паралича (ДЦП) у плодов, рожденных в срок. Однако частота ХП осталась почти неизменной, тогда как частота вмешательств, в основном в виде кесарева сечения (КС), с тех пор резко возросла [4].
Это отчасти связано с тем, что сама по себе EFM имеет низкую специфичность, что приводит к большому количеству ненужных вмешательств (CS). Поэтому исследования и разработки в области интранатального наблюдения были сосредоточены на поиске инструментов для повышения специфичности EFM.
FBS повышает специфичность и дополнительно предотвращает последствия интранатальной асфиксии [5-6].
В Части I этой статьи кратко представлена история мониторинга плода. Описаны различные причины интранатальной асфиксии и их возможное лечение, а также представлены разные стадии асфиксии с точки зрения кислотно-основных изменений.
Асфиксия плода
Наличие кислорода является необходимым условием аэробного метаболизма (РИСУНОК 1) и обеспечения достаточного количества энергии (АТФ) для поддержания здорового состояния плода даже во время родов. Во время эпизодов недостатка кислорода метаболизм становится анаэробным (РИСУНОК 2) , высвобождая очень мало энергии из запасов, которые быстро истощаются. Следовательно, неизбежен риск развития асфиксии и, наконец, повреждения головного мозга плода или его смерти.
РИСУНОК 1: Аэробный метаболизм глюкозы
РИСУНОК 2: Анаэробный метаболизм глюкозы
Термин асфиксия не имеет точного определения в литературе, хотя это состояние хорошо известно акушерам и неонатологам. Для большинства акушеров это состояние означает состояние плода с угнетением жизненно важных функций, обычно определяемое фетальным ацидозом в сочетании с гипоксией/аноксией:
Для большинства акушеров это состояние означает состояние плода с угнетением жизненно важных функций, обычно определяемое фетальным ацидозом в сочетании с гипоксией/аноксией:
Низкий уровень pH и низкий стандартный избыток основания: артерия пуповины (UCA) pH
Ниже этих уровней существует повышенный риск повреждения головного мозга [7].
Признаками асфиксии во время родов являются аномальная частота сердечных сокращений, патологические показатели КТГ, зеленоватые мекониальные амниотические жидкости и низкий рН крови на голове.
Асфиксия — физиология и возможное лечение
Во время родов плод подвержен высокому риску возникновения периодов гипоксии. Здесь решающее значение имеет функция плодно-плацентарной единицы как части оси между материнским и плодным кровообращением. «Части высокого риска» этой оси — оксигенация матери и кровяное давление, функция плаценты во время и между схватками, кровоток пуповины и кровообращение плода.
«Смазанное оборудование» обеспечивает передачу кислорода от матери к плоду, а также передачу CO 2 и других продуктов жизнедеятельности плода в кровоток матери. Плацента, так сказать, служит легким для плода внутриутробно .
Возможные причины гипоксии/асфиксии плода во время родов
Механизмами, которые могут изменить функцию этой оси, являются: физиологические изменения во время родов, такие как страх, боль и стресс, регионарная анестезия с сопутствующими изменениями артериального давления матери, слишком частые сокращения матки — либо спонтанные, либо из-за неправильного использования окситоцина для увеличения схватки (гиперстимуляция), когда роды не развиваются (дистоция), плацентарная недостаточность или отслойка и, наконец, различные аспекты беременности и родов, которые могут изменить или сжать кровоток через пуповину. См. ТАБЛИЦА 1 для обзора.
| Причина | Эффект |
| Гипотензия у матери Положение на спине, анестезия, вазодилатация (эпидуральная) | Маточно-плацентарный поток ↓ Плод p O 2 / с O 2 ↓ |
| Гиповентиляция у матери апноэ/эклампсия | Материнский р О 2 / с О 2 ↓ |
| Гипервентиляция у матери Страх, боль, стресс | Материнский p O 2 / s O 2 ↓ (вентиляция мертвого пространства) |
| Материнские катеколамины ↑ (адреналин ↑) страх, боль, стресс | Маточно-плацентарный поток ↓ (из экспериментов на животных) Плод p O 2 / s O 2 ↓ |
| Гипертонус матки Гиперстимуляция Гиперфункция матки | Маточно-плацентарный поток ↓ Плод p O 2 / с O 2 ↓ |
| Сдавление пуповины Маловодие, (материнское) положение, тазовое предлежание, обвитие пуповины, выпадение | Фето-плацентарный поток ↓ снижен/заблокирован O 2 /CO 2 обмен |
| Отслойка/недостаточность плаценты | Фето-плацентарный поток ↓ снижен/заблокирован O 2 /CO 2 обмен |
ТАБЛИЦА 1: Возможные причины и последствия гипоксии/асфиксии плода во время родов
Асфиксия — возможное лечение
Возможное лечение этих ситуаций с высоким риском для плода во избежание тяжелой асфиксии включает: респираторную поддержку и подачу кислорода матери, замещение объема для улучшения артериального давления матери, изменение положения матери, анестезию, прекращение или отмену окситоцина, острый токолиз (лекарственное торможение сокращений матки), амниоинфузия (введение физиологического раствора в амниотическую полость для уменьшения давления на пуповину) и, в конечном счете, немедленное родоразрешение либо с помощью КС, либо через инструментальное вагинальное родоразрешение. См. ТАБЛИЦА 2 для обзора.
См. ТАБЛИЦА 2 для обзора.
| Причина | Лечение |
| Гипотензия матери положение, анестезия, эпидуральная | Смена положения, замещение объема сосудосуживающие средства (эфедрин) |
| Гиповентиляция у матери апноэ/эклампсия | Свободные дыхательные пути, O 2 доп. (100 %) Инструктаж/поддержка органов дыхания |
| Гипервентиляция у матери (вентиляция мертвого пространства) | Устранить причину (например, боль) |
| Материнские катеколамины ↑ страх, боль, стресс | Обезболивание, анестезия, психологическая поддержка, акушерская помощь |
| Гипертонус/активность матки Гиперстимуляция окситоцином сверхэффективная деятельность матки | Устранить причину (окситоцин ↓) Сменить положение/токолиз Положение на левом боку |
| Компрессия пуповины Маловодие, (материнское) положение, тазовое предлежание, обвитие пуповины, затылочная пуповина/выпадение | Смена положения – амниоинфузия, токолиз «поднять головку плода» (наполнить мочевой пузырь) |
| Отслойка плаценты | Немедленная доставка (CAVE токолиз!!) |
| Плацентарная недостаточность | Кесарево сечение (желательно после токолиза) |
ТАБЛИЦА 2: Асфиксия – возможное лечение
Нормальные значения рН: во время родов
рН кожи головы медленно снижается во время нормальных родов, со значениями от 7,45 до 7,25. Верхние пределы нормального рН кожи головы не описаны. Значения выше 7,50 встречаются редко и, вероятно, из-за артефактов.
Верхние пределы нормального рН кожи головы не описаны. Значения выше 7,50 встречаются редко и, вероятно, из-за артефактов.
pH кожи головы снижается во время нормальных родов [8]:
- Первая стадия: 0,016 единиц pH в час
- Вторая ступень: 0,11 единицы pH в час
– то есть pH падает почти в десять раз быстрее во втором периоде нормальных родов с активными потугами и потугами. Это в первую очередь связано с более высоким и более длительным маточным давлением во время второй стадии схваток, с сопутствующей блокировкой плацентарного кровоснабжения, а также с задержкой дыхания матери. В результате происходит накопление CO 2 и быстрое падение рН.
By аноксия (полное отсутствие подачи кислорода) – напр. полное сдавление пуповины – рН снижается на 0,04 единицы рН в минуту [9] – напр. с 7.20 → 6.80 через 10 минут .
В большинстве европейских родильных отделений установлен 15-минутный лимит времени, затрачиваемого с момента постановки диагноза тяжелой асфиксии до родов.
Крайне важно понимать, что эти цифры относятся к женщинам и плодам при нормальных родах в срок – с нормальными ресурсами, чтобы выдерживать физиологический стресс и бремя родов. При преждевременных родах, задержке роста или перерождении плода; в клинических ситуациях, таких как преэклампсия, инфекция (например, хориоамнионит) или при плацентарной недостаточности или отслойке, у плода гораздо меньше резервов, и риск быстрого развития необратимых повреждений вследствие тяжелой асфиксии значительно выше.
Физиология плода во время родов
Когда плод сталкивается с физиологическими трудностями родов, он имеет различные защитные механизмы, чтобы противостоять риску стресса и возможному развитию гипоксии и асфиксии [10].
Когда нормальные роды становятся патологическими – напр. когда маточные сокращения были усилены окситоцином из-за отсутствия прогресса и слишком часты (> 5/10 минут), между сокращениями есть только короткие интервалы между сокращениями для восстановления нормального фетально-плацентарного газообмена: если есть также олигогидрамнион и развивается компрессия пуповины, плод использует различные механизмы, чтобы противостоять. Можно схематически разделить фазы последовательности на три:
Можно схематически разделить фазы последовательности на три:
| И. | Преацидотический период, |
| II. | период «стресса» с респираторным ацидозом и |
| III. | период «дистресса» с метаболическим ацидозом. |
I. Преацидотический период
- Увеличение использования кислорода (эффект Бора)
- Снижение активности
- Уменьшение роста
РИСУНОК 3: КТГ и типичные значения газов кожи головы и крови в фазе I преацидотический период, когда плод сталкивается с проблемой длительных сокращений и вероятной компрессией пуповины. КТГ можно охарактеризовать как неутешительную (исходная тахикардия и поздние децелерации). Выполнена FBS, pH 7,28, p CO 2 5,8 кПа, SBE –5,5 ммоль/л (лактат 3,5 ммоль/л) – и, поскольку это считается нормальным, роды продолжаются.
Выполнена FBS, pH 7,28, p CO 2 5,8 кПа, SBE –5,5 ммоль/л (лактат 3,5 ммоль/л) – и, поскольку это считается нормальным, роды продолжаются.
II. Период со «стрессом» и респираторным ацидозом
- Выброс гормонов стресса
- Перераспределение плодного потока
- Анаэробный метаболизм в периферических тканях плода
РИСУНОК 4: КТГ и типичные значения газов кожи головы и крови в фазе II щелкните для увеличения
РИСУНОК 4 демонстрирует КТГ и типичные значения газов кожи головы и крови в ситуации стресса плода и респираторного ацидотического периода. Плод осуществляет ауторегуляцию, перераспределяя внутриутробное кровообращение («централизация» или «мозгосберегающая»), обеспечивая приток богатой кислородом крови к жизненно важным органам путем «выключения» притока к периферическим нежизнеспособным органам.
КТГ может быть охарактеризована как патологическая (исходная ЧСС снизилась и длительные сложные замедления), отсутствие регистрации сокращений, но, вероятно, они были бы очень частыми и длительными, оставляя очень короткий промежуток времени между ними, чтобы обеспечить поглощение кислорода и в результате в СО 2 накопление.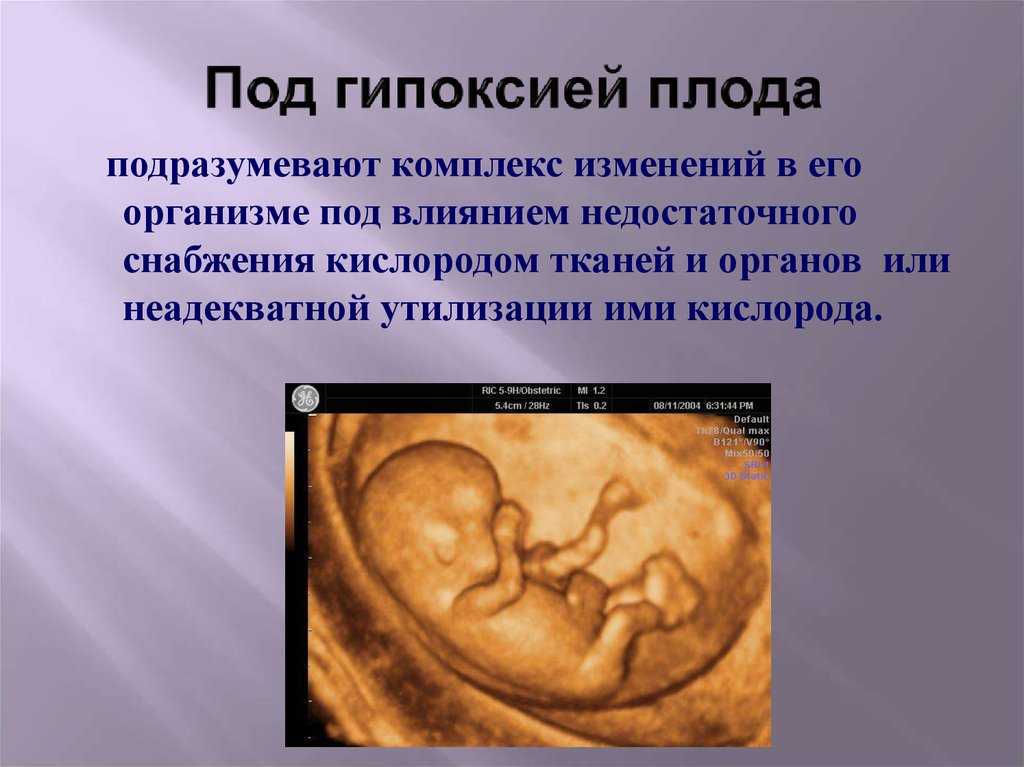
Выполнена FBS: pH 7,11, p CO 2 9,2 кПа , SBE –8,8 ммоль/л (лактат 11 ммоль/л – на самом деле это смешанный респираторно-метаболический ацидоз) – и считается патологический. Выполнен острый токолиз, роженица доставлена в операционную для экстренного КС.
III. Период с «дистрессом» и метаболическим ацидозом. Тяжелая асфиксия.
- Анаэробный метаболизм в жизненно важных органах
- Сердечная и мозговая недостаточность
РИСУНОК 5: КТГ и типичные значения газов скальп-кровь в фазе III щелкните для увеличения
и метаболический ацидоз. Первоначально небольшое улучшение из-за острого токолиза, левого бокового и наклонного положения, замещения объема и 100% кислорода матери.
У матери был ИМТ 44, в связи с чем была предпринята одна попытка проведения регионарной (спинальной) анестезии, но безуспешно. КТГ показывает отсутствие вариабельности, осложненные децелерации и, наконец, претерминальную брадикардию.
Была начата общая анестезия, но интубация не удалась в течение более 4 минут. Наконец, после успешной интубации было начато КС, и ребенок был рожден менее чем через 60 секунд. Первоначально у ребенка была депрессия с низкой оценкой по шкале Апгар и pH 6,9 в UCA.8, p CO 2 13,5 кПа, SBE – 12,4 ммоль/л и лактат 15 ммоль/л ( примечание: p O 2 0,1 кПа и 5 5 0,2 O 2
%!!).
Ребенок быстро выздоровел и через 5 дней был отправлен домой с матерью в добром здравии.
Асфиксия во время родов,
p O 2 , p CO 2 , pH, SBE и лактат
Последовательно описать развитие тяжелой асфиксии плода во время родов, РИСУНОК 6 показывает курсы p O 2 , p CO 2 , pH, SBE ммоль/л и лактата в три периода:
I. (нормальный/предацидный): нормальные роды, плод p O 2 значения обычно находятся в пределах от 2 до 3 кПа (плод s O 2 30-65 %), p CO 2 между 4 и 6,5 кПа, pH: 7,5 кПа -7,45. SBE и лактат ок. 0 ммоль/л.
SBE и лактат ок. 0 ммоль/л.
II. (стресс/респираторный ацидоз): когда плод подвергается стрессу, например, из-за длительная компрессия пуповины или слишком короткие интервалы между сокращениями, p O 2 падает, CO 2 накапливается, и рН быстро падает. Ауторегуляция плода с централизацией притока крови к жизненно важным органам приводит к анаэробному метаболизму и накоплению лактата в периферических тканях. Кислорода еще достаточно для поддержания аэробного метаболизма в жизненно важных органах.
Типичные значения: p O 2 : 1–1,5 кПа, p CO 2 : 7–9 кПа, pH: 7,05–7,15 и SBE: от –5 до –9 ммоль/л, что соответствует лактатный показатель 5-9ммоль/л.
III. (стресс/метаболический ацидоз): снабжение кислородом жизненно важных органов плода в настоящее время недостаточно для поддержания аэробного метаболизма, накапливается лактат, а рН быстро падает ниже 7,00.
