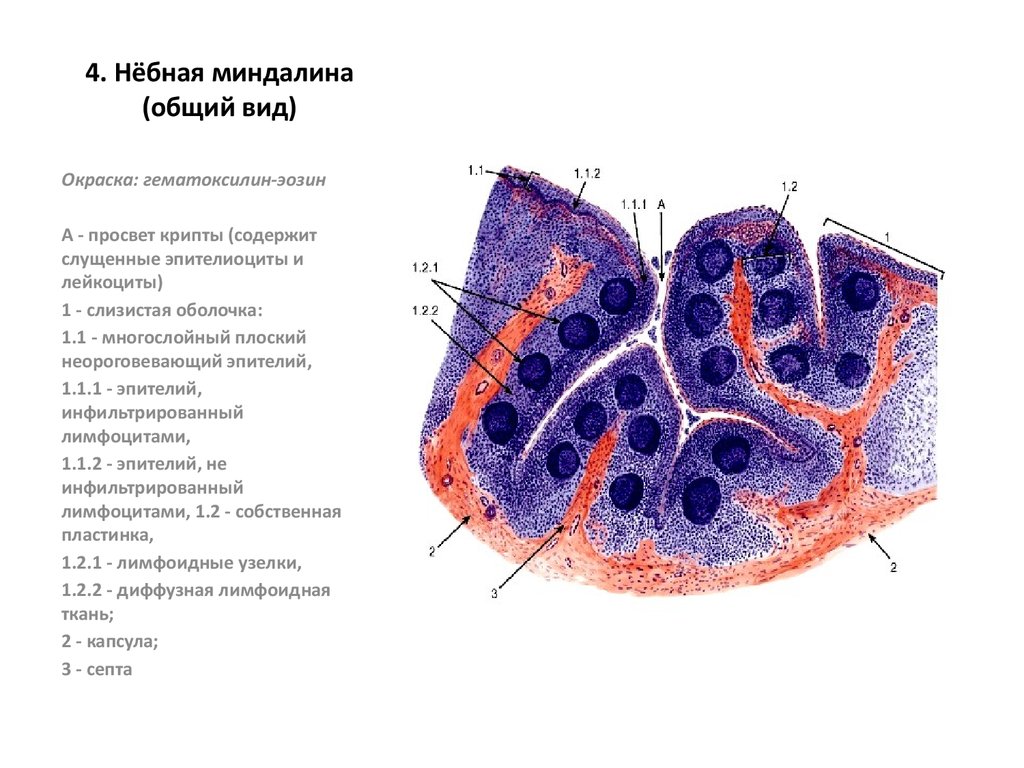
Миндалина гистология: Миндалины, их виды, строение, распределение лимфоцитов и функции:
Миндалины, их виды, строение, распределение лимфоцитов и функции:
Диффузная лимфоидная
ткань, межэпителиальные лимфоциты и
лимфоциты собственной пластинки:
Виды:
трубные, нёбные, глоточные, язычные,
гортанные.
Строение:
Состоит из складок слизистой, в собственной
пластинке находятся лимфоидные узелки.
От поверхности вглубь отходят крипты,
которые затем делятся на вторичные
крипты. Слизистая оболочка миндалин
покрыта многослойным плоским
неороговевающим эпителием, во многих
местах, особенно криптах, богато заселён
лимфоцитами и лейкоцитами.
Функции:
обезвреживают микробов, образуют
лимфоциты.
Слизистая
оболочка миндалин покрыта многослойным
плоским неорог овевающим эпителием, во
многих местах, особенно криптах, богато
заселён лимфоцитами и лейкоцитами. За
счёт фагоцитоза лейкоцитов эпителий
может частично разрушаться, но затем
восстанавливается обратно.
Глотка
и пищевод.
Строение глотки:
Выделяют
3 отдела: носовой, ротовой и гортанный.
В
носовом отделе слизистая покрыта
многорядным реснитчатым эпителием,
содержит смешанные железы.
В
ротовом и гортанном выстлана многослойным
плоским эпителием. В подслизистой
-концевые отделы сложных слизистых
желёз. Мышечная стенка состоит из
внутреннего продольного и наружного
кольцевого слоя.
Оболочки
стенки пищевода; слизистая, её строение
и тканевой состав:
Слизистая:
эпителий — многослойный плоский
неороговевающий, состоит из 20-25
слоев,
плоские клетки содержат немного зёрен
кератогиалина. Собственная пластинка
образует соединительнотканные сосочки,
вдающиеся в эпителий. В ней находятся
большие скопления лимфоцитов,
превращающиеся в лимфатические узелки;
здесь же находятся кардиальные железы
пищевода (простые разветвлённые трубчатые
железы, концевые отделы из кубического
или призматического эпителия, с большим
содержанием эндокринных клеток). Мышечная
Мышечная
пластинка состоит из расположенных
вдоль пищевода пучков гладких мышечных
клеток, окружённых сетью эластических
волокон.
Подслизистая
вместе со слизистой образует складки,
расправляющиеся при глотании пищи.
Содержит собственные железы пищевода.
Мышечная
оболочка состоит из внутреннего
циркулярного и наружного продольного
слоёв. В верхней 1/3 пищевода ткань
поперечнополосатая, в средней — и такая,
и такая, в нижней — только гладкая.
Адвентиция
связана с прослойками соединительной
ткани в мышечной оболочке, а с другой
стороны — с соединительной тканью
средостения. Брюшной отдел покрыт
серозной оболочкой.
Железы пищевода:
Кардиальные
железы пищевода (простые разветвлённые
трубчатые железы, концевые отделы из
кубического или призматического
эпителия, с большим содержанием
эндокринных клеток)
Собственные
железы — сложные сильно разветвлённые
альвеолярно-трубчатые железы. Концевые
Концевые
отделы состоят из слизистых клеток,-
Секрет сливается в мелкие протоки,
которые затем сливаются в более крупные,
которые затем идут через мышечную
пластинку слизистой и образуют там
протоки, открывающиеся на поверхность
эпителия. Эпителий мелких протоков
призматический, крупных — многослойный
плоский с реснитчатыми клетками
4.Особенности
пищевода в верхней, средней и нижней
1/3: Мышечная
оболочка состоит из внутреннего
циркулярного и наружного продольного
слоёв. В верхней 1/3 пищевода ткань
поперечнополосатая, в средней — и такая,
и такая, в нижней — только гладкая.
Иннервация
представлена 4-мя сплетениями:
адвентициальным— развито в средней и нижней 1/3,субадвентициальным— в верхней,межмышечным— между циркулярным и продольным слоями,подслизистым— на всём пищеводе, в местах ветвления
которых лежат нервные узелки.
Васкуляризация
и иннервация: артерии
образуют сплетения в подслизистой,
откуда затем идёт в сплетения собственной
пластинки. Венозный отток начинается
Венозный отток начинается
сетью мелких вен в собственной пластинке,
откуда кровь идёт в сплетение подслизистой,
а оттуда — в адвентицию. Лимфатика
представлена сплетения во всех 3-х
оболочках.
Иннервация
представлена 4-мя сплетениями:
адвентициальным— развито в средней и нижней 1/3,субадвентициальным— в верхней,межмышечным— между циркулярным и продольным слоями,подслизистым— на всём пищеводе, в местах ветвления
которых лежат нервные узелки.
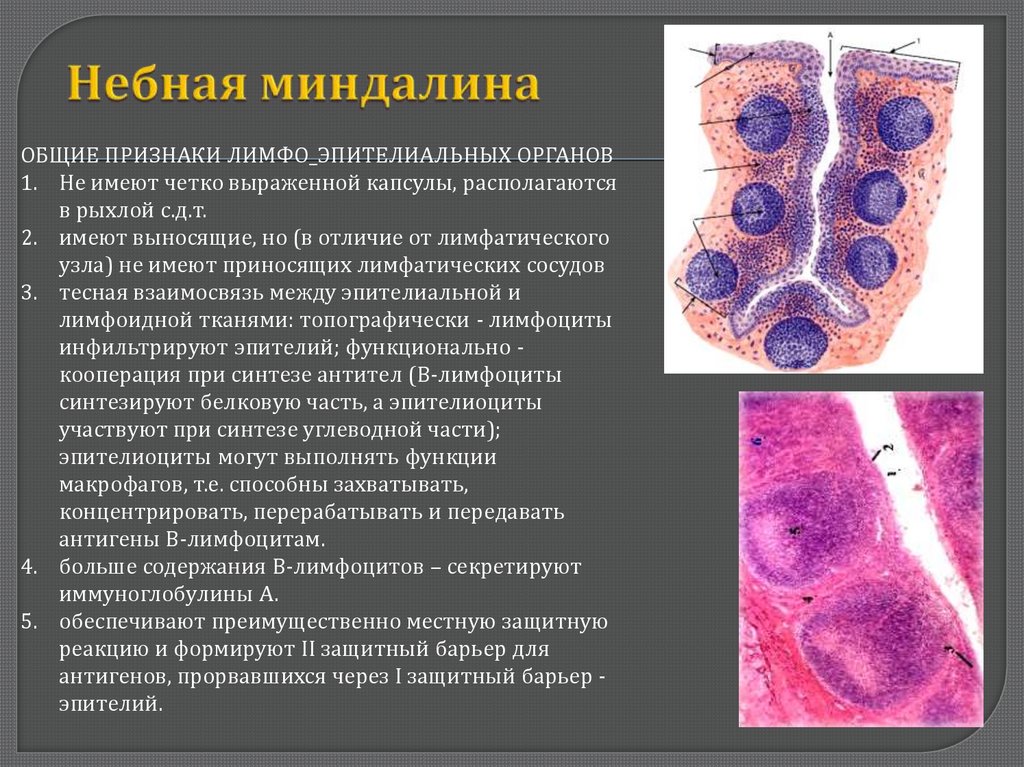
Небные миндалины: физиология и патология
Особое место среди хронических поражений ЛОР-органов занимает хроническая тонзиллярная патология. Это обусловлено как относительно быстрой хронизацией процесса в небных миндалинах, так и возможностью развития генерализованных, вплоть до летальных, осложнений, а также особенностями течения и влияния на организм сопряженных (метатонзиллярных) заболеваний. По данным разных авторов, от 4 до 35% населения страдают хроническим тонзиллитом, при этом в разных регионах Российской Федерации отмечается рост числа пациентов, страдающих данной патологией.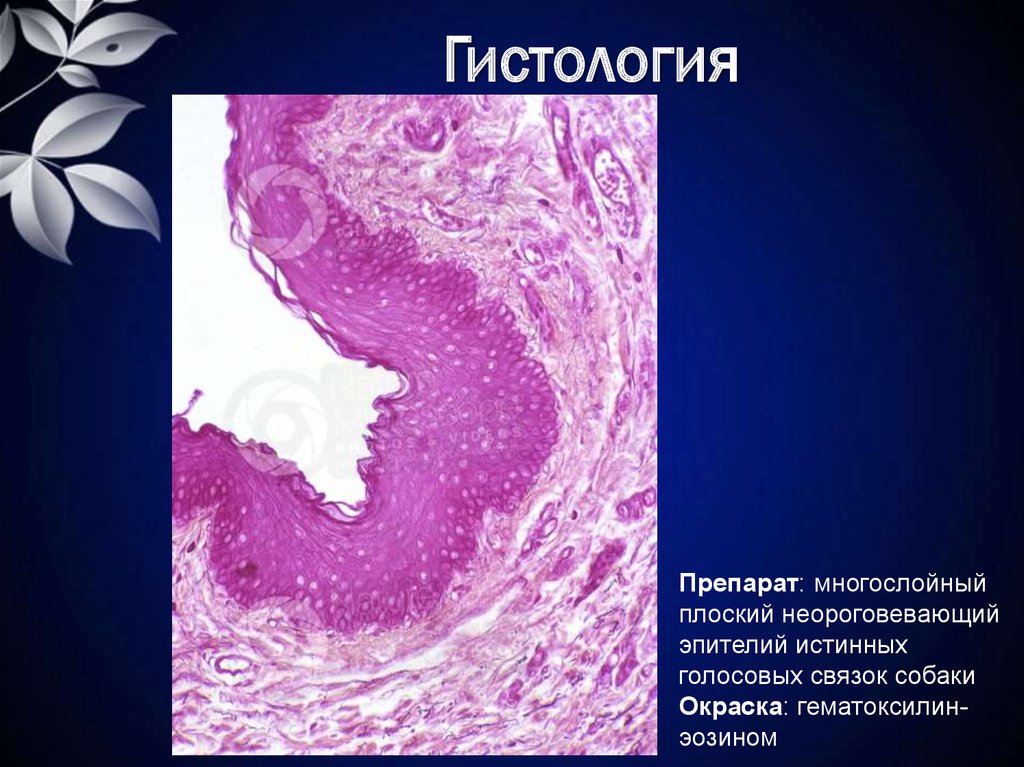
Хронический тонзиллит, являясь классическим примером очаговой инфекции, представляет собой по сути хроническое инфекционно-аллергическое заболевание с местной воспалительной реакцией в небных миндалинах, которое обусловливает возможность развития всей совокупности осложнений, в основе которых лежит активность β-гемолитического стрептококка, его антигенов и различных факторов патогенности, ключевую роль в которых играют стрептолизины.
Известно, что большинство острых воспалительных заболеваний, характеризующихся поражением ЛОР-органов, при отсутствии адекватной терапии склонно к переходу в хронический процесс. Однако патология, связанная с небными миндалинами, имеет выраженные отличительные особенности как в формировании хронического воспаления, так и в строгой этапности развития данного патологического процесса. В естественных физиологических функциях небных миндалин настолько тесно взаимодействуют нормальные и патологические процессы, что, несмотря на большое количество самых разнообразных исследований, которые были проведены по этой проблеме, до настоящего времени практически не удалось установить абсолютно определенную «точку невозврата», когда наступают необратимые патоморфологические изменения в структуре небных миндалин, и уже требуется выполнение радикальных методов лечения, в частности тонзиллэктомии.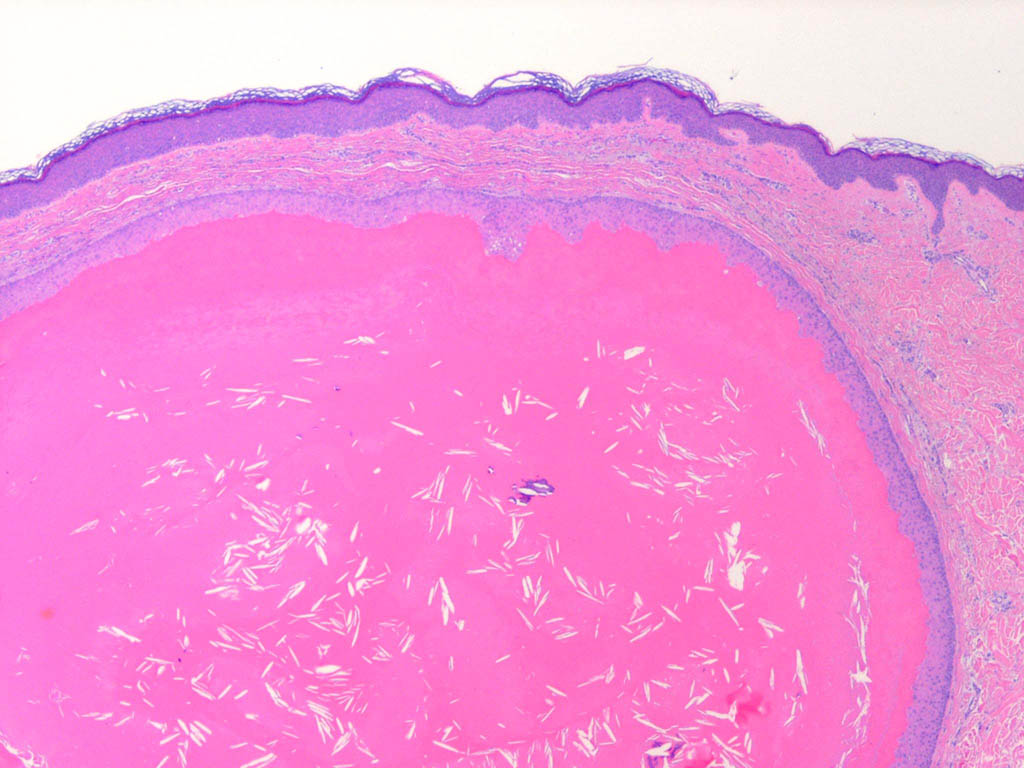 Отсутствие консенсусного решения по данной проблематике в современном медицинском сообществе лишь еще более усугубляет проблему.
Отсутствие консенсусного решения по данной проблематике в современном медицинском сообществе лишь еще более усугубляет проблему.
Так, крайне часто в рутинной клинической практике при выборе дальнейшей тактики ведения пациента врачи руководствуются преимущественно анамнестическими данными о количестве перенесенных ангин и паратонзиллярных абсцессов, ориентируясь при этом больше на субъективные ощущения, нежели на объективную клиническую симптоматику и данные лабораторных методов исследования. Между тем существующая в настоящее время классификация хронического тонзиллита Б.С. Преображенского—В.Т. Пальчуна (и заложенные в ней диагностические критерии), разработанная в свое время на кафедре оториноларингологии РНИМУ им. Н.И. Пирогова, позволяет четко дифференцировать различные формы хронической тонзиллярной патологии и дает ясное указание на дальнейшую тактику ведения данного пациента [1, 2]. В отличие от существующих классификаций хронического тонзиллита, данная классификация отражает этапность развития патологического процесса в структуре небных миндалин и влияние этих процессов на организм в целом в соответствии с основными патогенетическими звеньями данного заболевания. При этом в комментариях к данной классификации прямо прописана необходимость выполнения тонзиллэктомии больным с хроническим тонзиллитом токсико-аллергической формы (ТАФ) II, а также, в случае неэффективности консервативной терапии, пациентам с хроническим тонзиллитом ТАФ I. Однако, несмотря на это, с сожалением приходится констатировать, что во врачебной среде и особенно в терапевтическом сообществе до настоящего времени бытует мнение о необходимости сохранения любыми средствами небных миндалин как иммунокомпетентного органа, даже несмотря на возможную тяжесть общесоматической симптоматики и очевидную несостоятельность небных миндалин в условиях глубоких изменений ее структуры на фоне выраженных хронических изменений.
При этом в комментариях к данной классификации прямо прописана необходимость выполнения тонзиллэктомии больным с хроническим тонзиллитом токсико-аллергической формы (ТАФ) II, а также, в случае неэффективности консервативной терапии, пациентам с хроническим тонзиллитом ТАФ I. Однако, несмотря на это, с сожалением приходится констатировать, что во врачебной среде и особенно в терапевтическом сообществе до настоящего времени бытует мнение о необходимости сохранения любыми средствами небных миндалин как иммунокомпетентного органа, даже несмотря на возможную тяжесть общесоматической симптоматики и очевидную несостоятельность небных миндалин в условиях глубоких изменений ее структуры на фоне выраженных хронических изменений.
Именно поэтому при выборе метода лечения пациента с хронической тонзиллярной патологией необходимо в первую очередь руководствоваться теми знаниями, которые накоплены по данной проблеме в настоящее время, и объективно оценивать риск развития осложнений, которые могут привести к развитию в том числе летальной симптоматики, а классификация хронического тонзиллита Б.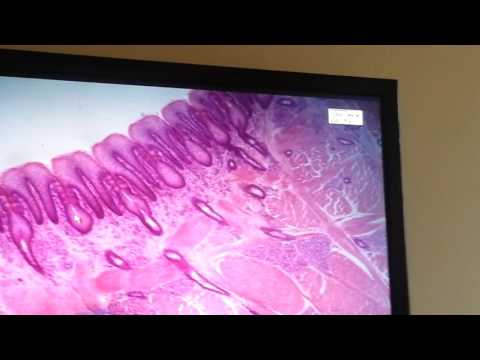 С. Преображенского — В.Т. Пальчуна должна являться основным ориентиром для детализации диагноза и, на этом основании, выбора тактики дальнейшего ведения.
С. Преображенского — В.Т. Пальчуна должна являться основным ориентиром для детализации диагноза и, на этом основании, выбора тактики дальнейшего ведения.
Этапность развития патоморфологических изменений в структуре небных миндалин, а также формирование общих и местных сопряженных заболеваний (метатонзиллярных осложнений), отраженных в классификации Б.С. Преображенского—В.Т. Пальчуна, во многом определены биологическими свойствами основных этиологически значимых микроорганизмов [3].
Согласно результатам многих исследований, проводившихся в последние десятилетия, среди микроорганизмов, претендующих на роль ведущего этиологического фактора в развитии хронического тонзиллита, можно встретить большое количество разнообразных по свойствам возбудителей, среди которых стрептококки, стафилококки, гемофильная палочка, лимфотропные вирусы и др. В соответствии с результатами этих исследований, хронический тонзиллит принято считать полиэтиологическим заболеванием. Рассматривая данный вопрос с позиции клинической микробиологии, следует отметить, что в большинстве случаев причинно значимыми микроорганизмами являются в первую очередь бактерии, вегетирующие в дистальных отделах крипт небных миндалин. Поскольку в данных отделах миндалин крайне низкое содержание кислорода, доминирующей флорой, вегетирующей на поверхности слизистой оболочки крипт миндалин, являются микроорганизмы с анаэробным типом метаболизма, которые представлены пептококками, бактероидами. превотеллами, фузобактериями и др. Однако ведущая роль в развитии хронических изменений в небных миндалинах, а также местных и общих осложнений хронического тонзиллита отводится β-гемолитическому стрептококку серологической группы, А (S. pyogenes) — микроорганизму, который также использует для своей жизнедеятельности анаэробное дыхание. При этом небные миндалины являются единственным природным резервуаром пиогенного стрептококка в макроорганизме [4, 5].
Поскольку в данных отделах миндалин крайне низкое содержание кислорода, доминирующей флорой, вегетирующей на поверхности слизистой оболочки крипт миндалин, являются микроорганизмы с анаэробным типом метаболизма, которые представлены пептококками, бактероидами. превотеллами, фузобактериями и др. Однако ведущая роль в развитии хронических изменений в небных миндалинах, а также местных и общих осложнений хронического тонзиллита отводится β-гемолитическому стрептококку серологической группы, А (S. pyogenes) — микроорганизму, который также использует для своей жизнедеятельности анаэробное дыхание. При этом небные миндалины являются единственным природным резервуаром пиогенного стрептококка в макроорганизме [4, 5].
И именно данный факт в большинстве случаев обусловливает развитие токсико-аллергических проявлений в человеческом организме, приводящих к формированию общих, сопряженных с хроническим тонзиллитом заболеваний. Среди этих заболеваний следует особо выделять острую ревматическую лихорадку и постстрептококковый гломерулонефрит, которые, как правило, приводят к патологии сердечно-сосудистой и мочевыделительной систем, а также ухудшают качество жизни и, в конечном счете, сокращают ее [6—8].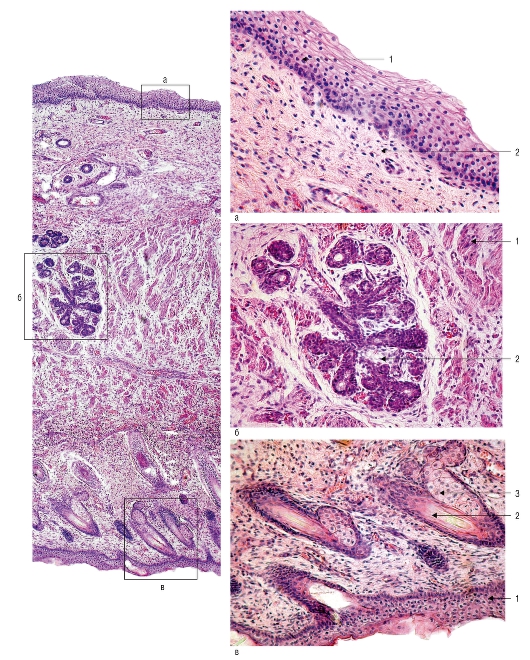
S. pyogenes — микроорганизмы, представляющие собой грамположительные кокки, имеющие классический для стрептококков тип расположения — в виде цепочки, дающие полный лизис эритроцитов (бета-гемолиз) на кровяном агаре и относящиеся к серологической группе, А в антигенной классификации стрептококков Р. Ленсфильд. Пиогенный стрептококк обладает значительной устойчивостью к физическим и химическим факторам внешней среды. Единственным природным резервуаром пиогенного стрептококка в макроорганизме являются дистальные отделы лакун небных миндалин.
Патогенез пиогенных стрептококковых инфекций связан с активацией данных микроорганизмов в глубоких отделах лакун небных миндалин, их последующей инвазией в структуры лимфоидной ткани миндалин за счет наличия большого количества экстрацеллюлярных ферментов — стрептокиназы, катализирующей превращение плазминогена в протеолитический фермент плазмин, гиалуронидазы, разрушающей гиалуроновую кислоту, являющуюся основным компонентом соединительной ткани, стрептодорназы (ДНК-азы), разрушающей элементы генома соединительнотканных клеток, и др. Выработка специфичных для данного возбудителя мембраноповреждающих токсинов О- и S-стрептолизинов приводит к развитию системной интоксикации, кардиотоксичности, которая объясняется подавлением энергетических процессов в митохондриях миокардиальных клеток в условиях активности О-стрептолизина, который обладает также гемолитической активностью и иммуногенными свойствами. Действие S-стрептолизина совместно с антихемотаксическим фактором (пептидаза С5а) связано с подавлением активности фагоцитарных клеток и разрушением мембран митохондрий клеток в очаге поражения. Специфичность клинических симптомов поражения небных миндалин обусловлена в первую очередь действием именно этих факторов патогенности.
Выработка специфичных для данного возбудителя мембраноповреждающих токсинов О- и S-стрептолизинов приводит к развитию системной интоксикации, кардиотоксичности, которая объясняется подавлением энергетических процессов в митохондриях миокардиальных клеток в условиях активности О-стрептолизина, который обладает также гемолитической активностью и иммуногенными свойствами. Действие S-стрептолизина совместно с антихемотаксическим фактором (пептидаза С5а) связано с подавлением активности фагоцитарных клеток и разрушением мембран митохондрий клеток в очаге поражения. Специфичность клинических симптомов поражения небных миндалин обусловлена в первую очередь действием именно этих факторов патогенности.
Помимо этого, особенностью клеточной стенки пиогенного стрептококка можно считать наличие большого количества поверхностных белковых структур, в частности М-протеина, являющегося важным адгезином данных микроорганизмов. М-белок обеспечивает связывание с коллагеном, фибронектином, а также белками сыворотки крови — фибриногеном, компонентами системы комплемента, а также другими элементами различных органов и систем, обусловливая активацию первичной фазы развития метатонзиллярных осложнений.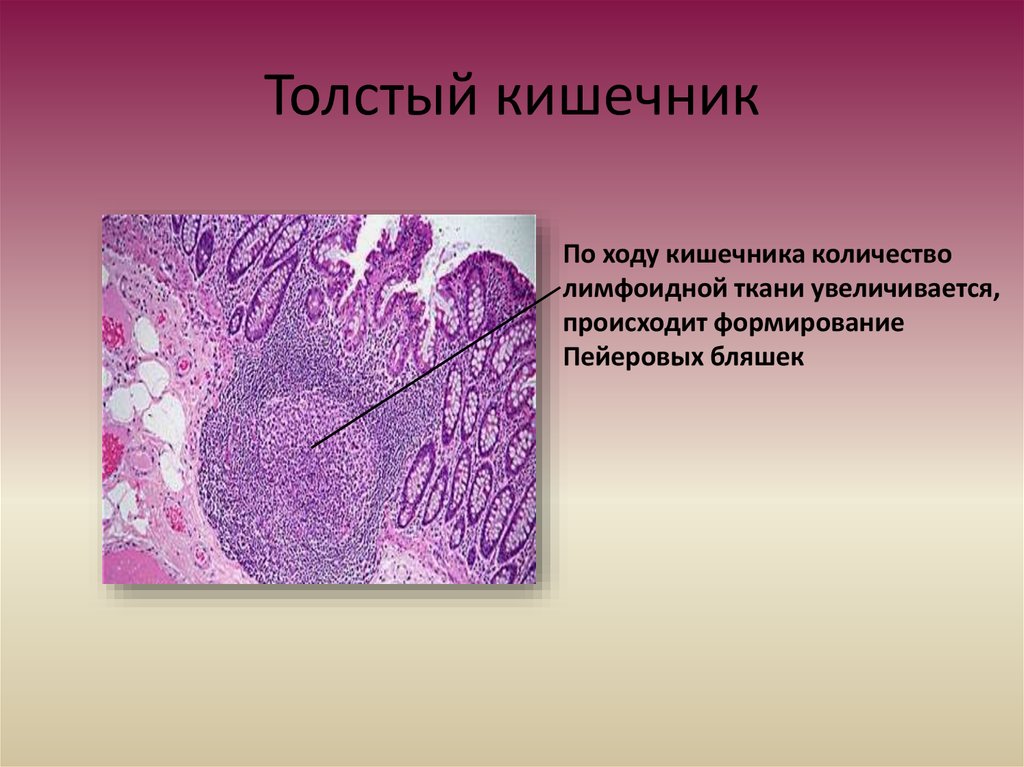 Именно с наличием М-протеина связана способность пиогенного стрептококка проникать внутрь эпителиальных клеток с развитием феномена интернализации. Пиогенный стрептококк имеет гиалуроновую капсулу, защищающую его от органов иммунологического надзора и являющуюся фактором антифагоцитарной активности.
Именно с наличием М-протеина связана способность пиогенного стрептококка проникать внутрь эпителиальных клеток с развитием феномена интернализации. Пиогенный стрептококк имеет гиалуроновую капсулу, защищающую его от органов иммунологического надзора и являющуюся фактором антифагоцитарной активности.
Помимо этого, S. pyogenes имеет и синтезирует большое количество веществ, которые обладают свойствами суперантигенов, обусловливают митогенную активность и приводят к поликлональной пролиферации Т-лимфоцитов. К суперантигенам стрептококков относятся пирогенные экзотоксины (SPE A, SPE B, SPE C, SPE D), митогенный фактор SPE F и, вероятно, типоспецифические М-протеины [2, 9]. Пирогенный токсин, А (Spe A), ген которого локализован на умеренном бактериофаге, связан с наиболее тяжелыми формами стрептококковой инфекции. Ген, кодирующий этот токсин, выявляется в ½ случаев скарлатины и ревматической лихорадки. Ген пирогенного токсина В локализуется в хромосомной ДНК клетки и представляет собой цистеиновую протеиназу, которая способна расщеплять фибронектин в макроорганизме. У больных с инвазивными формами стрептококковой инфекции (целлюлит, пневмония, некротический фасциит) отмечается повышенный уровень антител к пирогенному экзотоксину В (SPE В). Помимо этого, выработка стрептококком SPE B сочеталась с высоким риском развития острого постстрептококкового гломерулонефрита [10, 11].
У больных с инвазивными формами стрептококковой инфекции (целлюлит, пневмония, некротический фасциит) отмечается повышенный уровень антител к пирогенному экзотоксину В (SPE В). Помимо этого, выработка стрептококком SPE B сочеталась с высоким риском развития острого постстрептококкового гломерулонефрита [10, 11].
В настоящее время доказано, что стрептококки могут не только прикрепляться к клеткам макроорганизма, но и проникать в них. Так, A. Osterlund [12], исследуя небные миндалины детей с рецидивирующим тонзиллитом, выявил стрептококки, находящиеся внутри клеток, а 30% неудач в лечении хронического тонзиллита связывают с нахождением возбудителя внутриклеточно.
Необходимо также отметить, что β-гемолитический стрептококк персистирует в структуре слизистой оболочки крипт небных миндалин не в виде планктонных культур, а в форме патологических биопленок, обусловливающих не только защиту от экзогенных факторов окружающей среды, но и резистентность к различным методам терапевтического воздействия [13, 14].
В развитии этапности клинической картины тонзиллита (которые отражены в классификации Б.С. Преображенского – В.Т. Пальчуна) принимают участие несколько факторов, связанных с пиогенным стрептококком: 1) токсический фактор, обусловливающий патологическое воздействие стрептолизинов на сердечно-сосудистую, нервную и эндокринную системы, что проявляется общей интоксикацией, лихорадкой и др.; 2) септический фактор, который связан с воздействием ферментов патогенности бета-гемолитического стрептококка, в результате чего возникает локальная воспалительная реакция в структуре небных миндалин и далее инвазия микроорганизмов вглубь тканей с возможностью дальнейшей генерализации процесса, чаще гематогенным путем, вплоть до развития тонзиллогенного сепсиса, выраженной реакцией лимфатических узлов и др.; 3) аллергический фактор (комплекс поверхностных субстанций пиогенного стрептококка), который вызывает сенсибилизацию макроорганизма к бета-гемолитическому стрептококку и антигенам разрушенных тканей организма, приводящую затем к развитию гломерулонефрита, миокардита и др. [2].
[2].
Анализируя все вышесказанное, приходится констатировать, что факторы патогенности пиогенного стрептококка и его биологические свойства напрямую влияют на характер клинического течения тонзиллярной патологии и ее осложнений, что доказывает ведущую роль данного микроорганизма в генезе хронического тонзиллита.
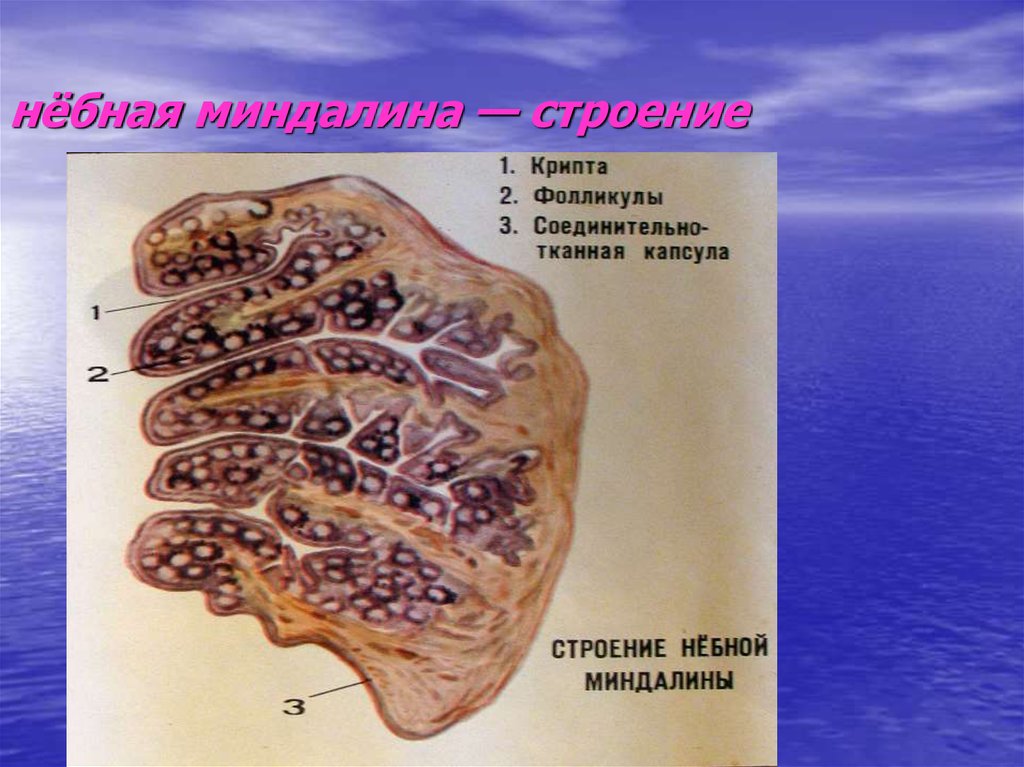
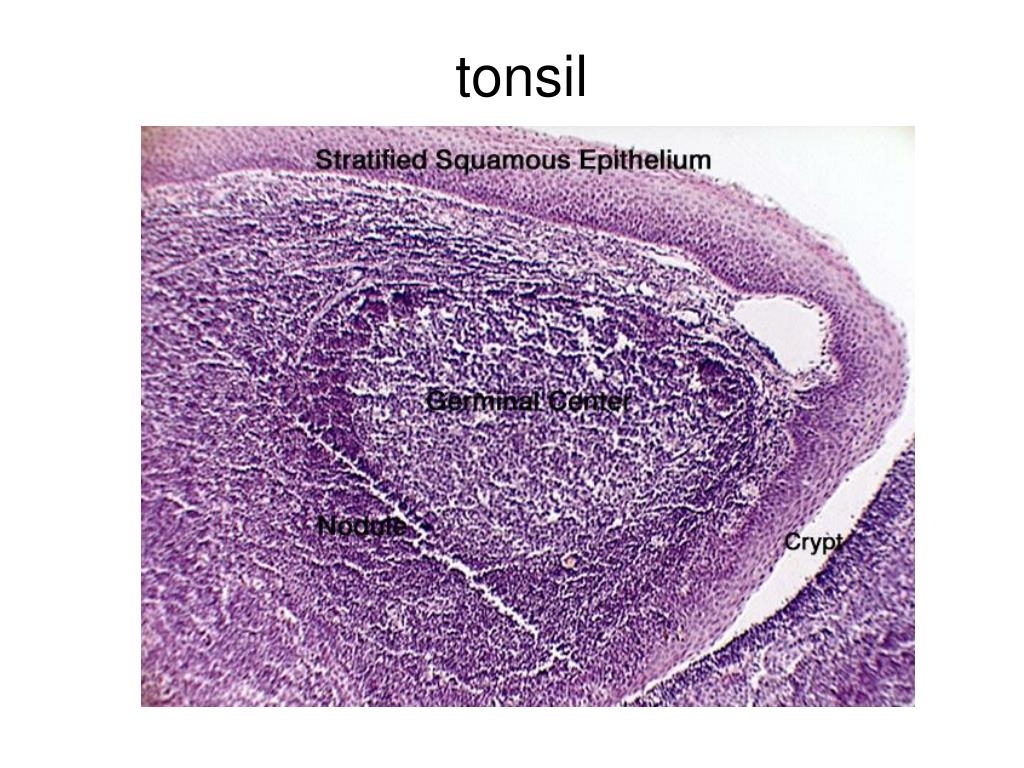
Особенности анатомо-гистологического строения небных миндалин наряду с биологическими свойствами пиогенного стрептококка также привносят существенный вклад в развитие в них хронического воспаления. Являясь частью лимфоэпителиального глоточного кольца, небные миндалины имеют не только самые большие размеры, но и самое сложное строение среди всех элементов данного кольца, которое во многом и предопределяет развитие очага хронической инфекции.
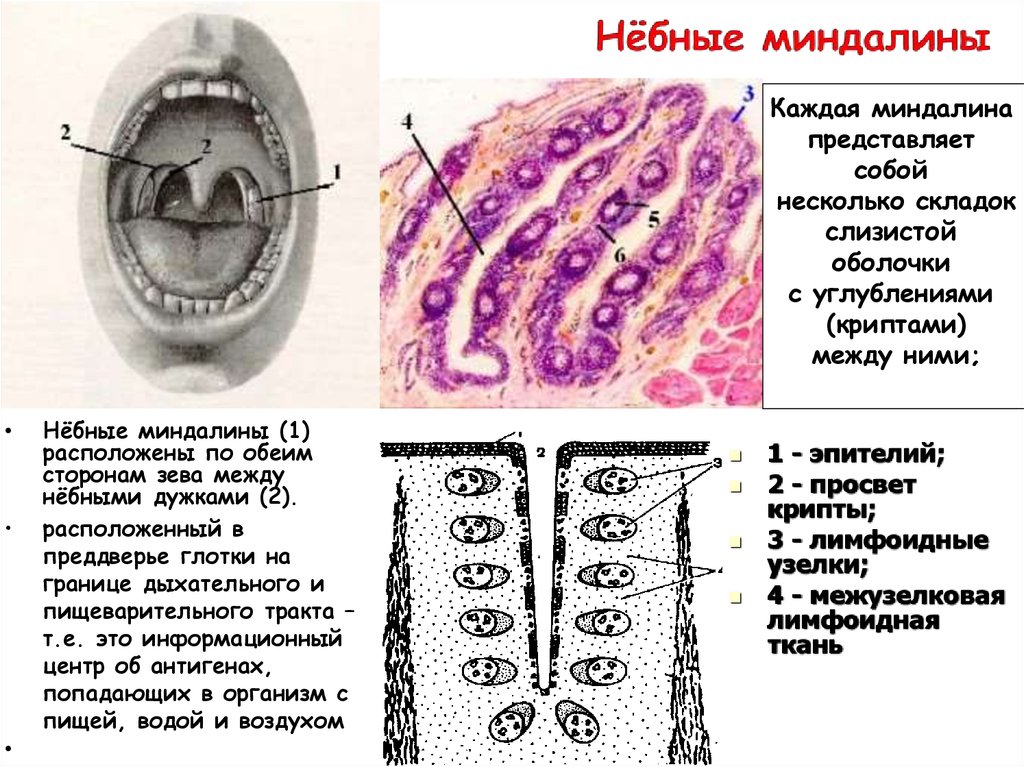
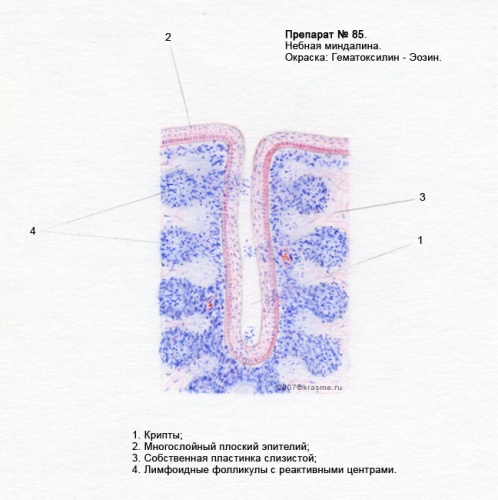
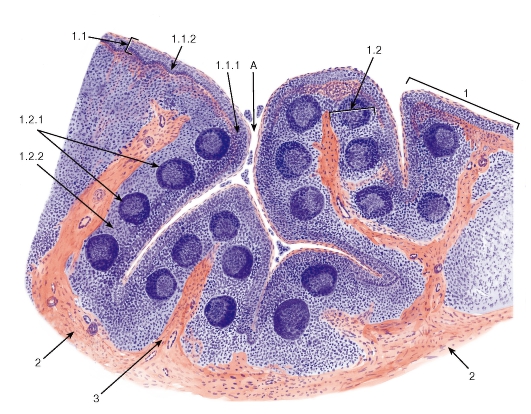
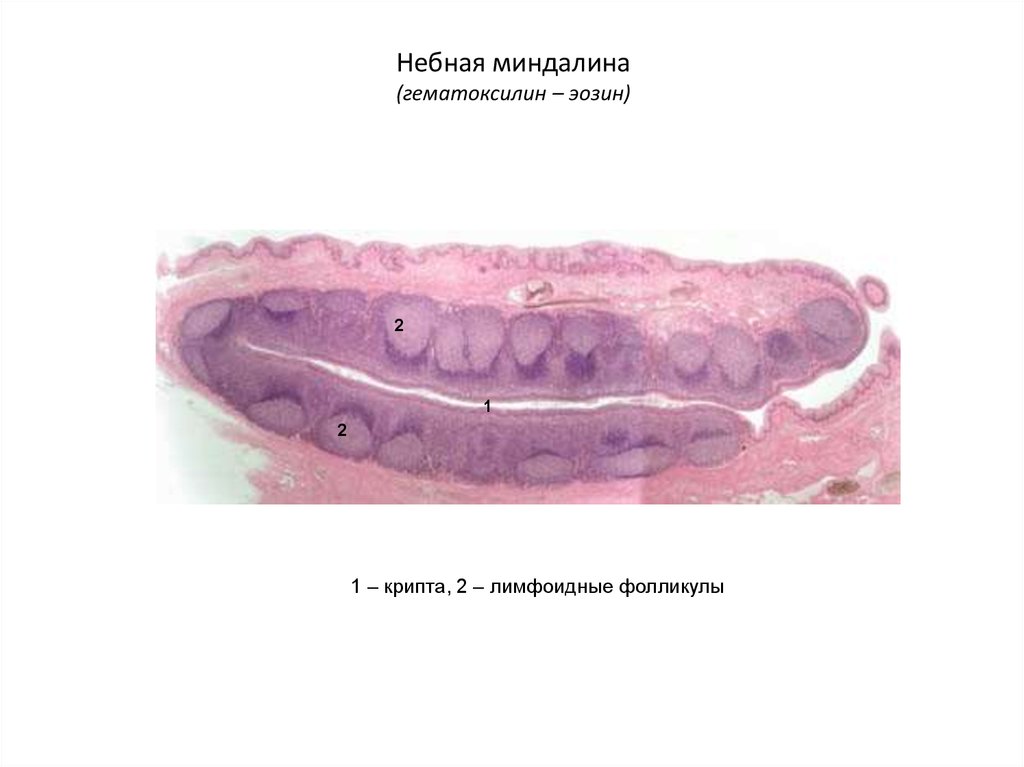
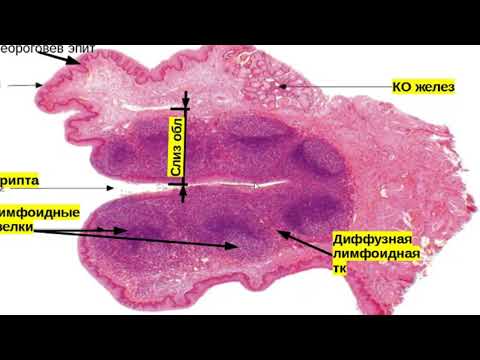
Так, известно, что небная миндалина состоит из долек, которые имеют сложное строение. Из разных участков соединительнотканной капсулы миндалины в направлении к зевной поверхности идут пучки соединительной ткани, образуя основу долек (строму). Затем эти основные тяжи ветвятся на более мелкие, пронизывающие всю миндалину. Паренхима миндалины представляет собой группы лимфоидных фолликулов, находящихся в тонкопетлистой соединительнотканной сети. В центре таких более или менее округлых фолликулов находится зона, имеющая при приготовлении микропрепарата более светлую окраску, — так называемый зародышевый центр, где образуются молодые лимфоциты, которые по мере развития постепенно оттесняются к периферии фолликула. Важной особенностью небных миндалин, обусловливающих и нормальные физиологические, и патологические процессы, является наличие крипт. Они начинаются на зевной поверхности и идут вглубь миндалины, древовидно ветвясь. Крипты, как и вся зевная поверхность миндалины, выстланы многослойным плоским эпителием в 6—8 рядов.
Затем эти основные тяжи ветвятся на более мелкие, пронизывающие всю миндалину. Паренхима миндалины представляет собой группы лимфоидных фолликулов, находящихся в тонкопетлистой соединительнотканной сети. В центре таких более или менее округлых фолликулов находится зона, имеющая при приготовлении микропрепарата более светлую окраску, — так называемый зародышевый центр, где образуются молодые лимфоциты, которые по мере развития постепенно оттесняются к периферии фолликула. Важной особенностью небных миндалин, обусловливающих и нормальные физиологические, и патологические процессы, является наличие крипт. Они начинаются на зевной поверхности и идут вглубь миндалины, древовидно ветвясь. Крипты, как и вся зевная поверхность миндалины, выстланы многослойным плоским эпителием в 6—8 рядов.
В некоторых местах крипт эпителиальный покров прерывается (участки физиологического ангизирования). Здесь происходит контакт микроорганизмов и лимфоцитов. Именно участки физиологического ангизирования обеспечивают контакт микроорганизмов с мантийной зоной фолликулов. В обнаженную в этих разрывах эпителия лимфаденоидную ткань свободно проникают микроорганизмы, вегетирующие на поверхности крипт. Таким образом формируется естественный биологический механизм, обеспечивающий проникновение инфекционного агента из внешней среды в лимфоидную ткань миндалины, что приводит к инициации развития герминативного центра фолликулов небной миндалины, дифференцировке В-лимфоцитов в высокоспецифичные плазматические клетки, способные к синтезу высокоавидных антител. Контроль иммунитета обеспечивает гибель проникших в паренхиму НМ микроорганизмов. В этом случае очаг инфекции инактивируется общими иммунными факторами макроорганизма. Бактерии погибают, однако сохраняют частицы своей антигенной структуры, что является дополнительным стимулом активации местных и общих иммунологических реакций.
В обнаженную в этих разрывах эпителия лимфаденоидную ткань свободно проникают микроорганизмы, вегетирующие на поверхности крипт. Таким образом формируется естественный биологический механизм, обеспечивающий проникновение инфекционного агента из внешней среды в лимфоидную ткань миндалины, что приводит к инициации развития герминативного центра фолликулов небной миндалины, дифференцировке В-лимфоцитов в высокоспецифичные плазматические клетки, способные к синтезу высокоавидных антител. Контроль иммунитета обеспечивает гибель проникших в паренхиму НМ микроорганизмов. В этом случае очаг инфекции инактивируется общими иммунными факторами макроорганизма. Бактерии погибают, однако сохраняют частицы своей антигенной структуры, что является дополнительным стимулом активации местных и общих иммунологических реакций.
Распознавание антигенных структур микроорганизмов происходит и за счет Toll-подобных рецепторов. При этом рядом авторов отмечается, что не только лимфоциты экспрессируют на своей поверхности Toll-подобные рецепторы (TLR), играющие ключевую роль в распознавании микроорганизмов.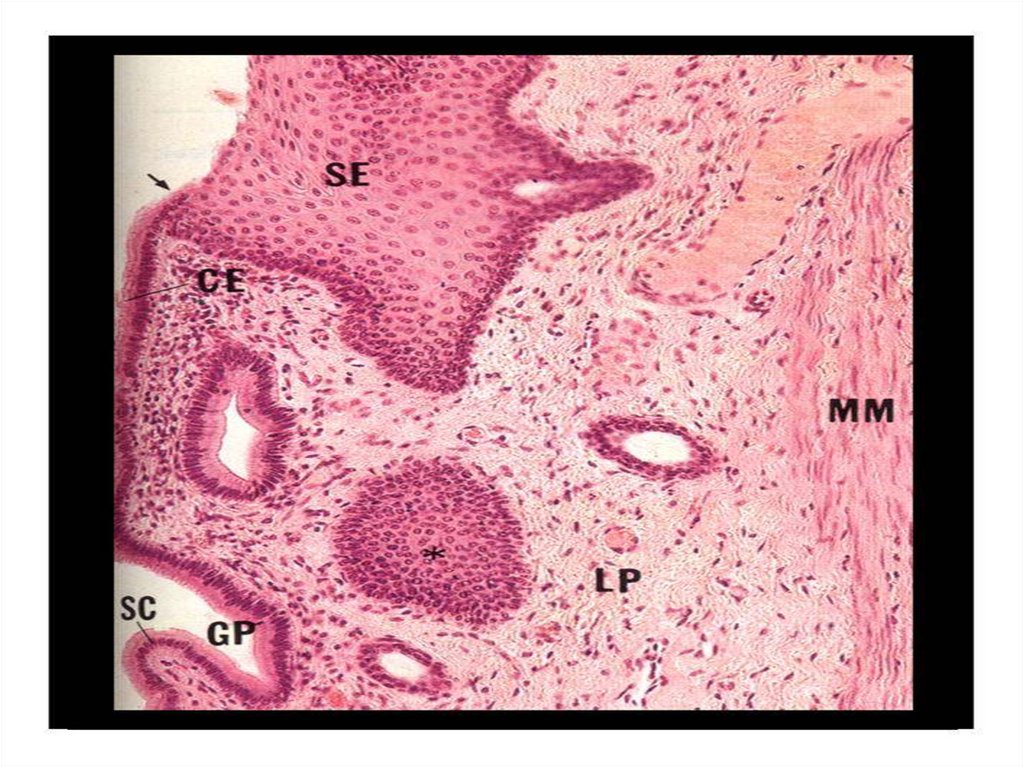 Данные рецепторы обнаруживаются в клетках эпителия миндалин, в первую очередь в криптальном и люминарном [15]. Обнаружение данных рецепторов в эпителии миндалин может свидетельствовать о его функциональной роли в качестве антигенпрезентирующих клеток, и это также служит подтверждением того, что в условиях нормально функционирующей миндалины выстилка крипт не имеет повреждений.
Данные рецепторы обнаруживаются в клетках эпителия миндалин, в первую очередь в криптальном и люминарном [15]. Обнаружение данных рецепторов в эпителии миндалин может свидетельствовать о его функциональной роли в качестве антигенпрезентирующих клеток, и это также служит подтверждением того, что в условиях нормально функционирующей миндалины выстилка крипт не имеет повреждений.
Таким образом, само строение миндалины, а именно древовидно ветвящиеся крипты, имеющие 4—6 порядков, способствует формированию приобретенного иммунитета, увеличивая время контакта возбудителя с иммунными клетками. Однако в тех ситуациях, когда задержка оттока содержимого происходит сверх определенного времени, лакуны приобретают способность к кистозному расширению. В этих условиях на эпителий крипт длительное время начинают воздействовать токсины микроорганизмов, которые впоследствии принимают непосредственное участие в формировании различных токсико-аллергических проявлений. Именно поэтому задержка оттока содержимого лакун является одним из важных механизмов развития хронизации процесса, а также принимает участие в генезе сопряженной патологии, дальнейшем системном воздействии сформированного хронического очага инфекции на макроорганизм и формировании грубых патоморфологических изменений в тканях самих миндалин.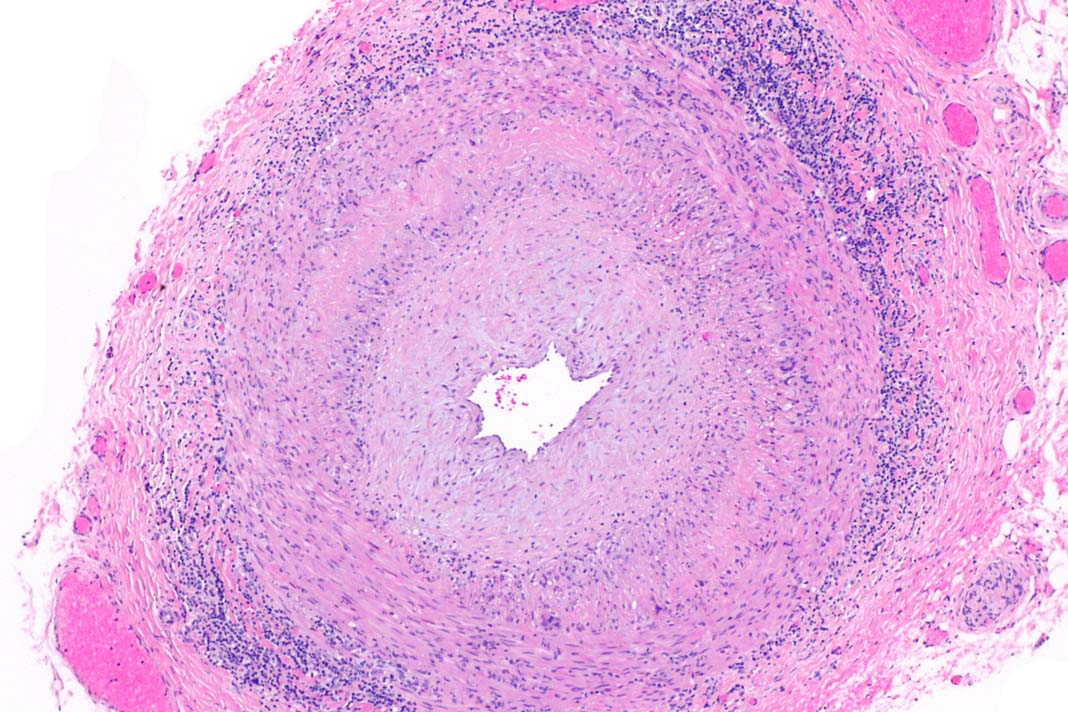
Отправной точкой в развитии хронического тонзиллита является нарушение местного иммунного статуса слизистой оболочки небных миндалин, что в совокупности с воздействием токсинов бактерий, а иногда и лимфотропных вирусов, на эпителий крипт может приводить к его истончению и формированию участков уже не физиологического, а патологического ангизирования. Это позволяет этиологически значимым микроорганизмам проникнуть в глубокие клеточные слои слизистой оболочки, вглубь паренхимы миндалины, в кровеносные сосуды и инициировать дальнейшие патологические процессы.
Необходимо отметить, что в современной литературе мало данных об изменениях, возникающих в небных миндалинах при разных формах и стадиях хронического тонзиллита, на клеточном уровне. Проведенные на нашей кафедре исследования помогли дополнить представления о физиологии и патофизиологии небных миндалин в условиях формирования в них хронического воспаления. В ходе исследования был использован метод авторадиографии, позволяющий оценить гистоархитектонику небных миндалин, а также определить функциональную активность микроорганизмов, находящихся в паренхиме тонзилл, как в норме, так и у пациентов с хроническим тонзиллитом.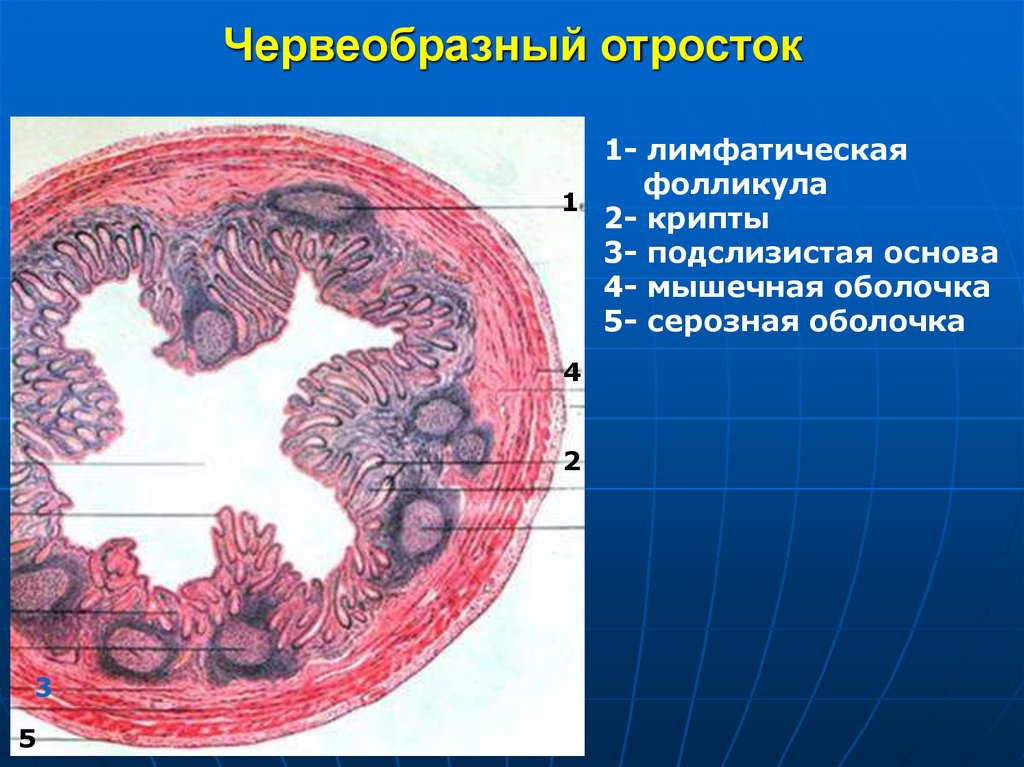 Суть метода состояла в использовании радиоактивных предшественников нуклеиновых кислот (3Н-тимидинa, 3Н-уридинa). Накопление клеткой 3Н-тимидинa демонстрирует возможность данных клеток синтезировать ДНК, т. е. указывает на их пролиферативную активность. Синтез РНК, которая является матричной основой для синтеза протеинов, отражает функциональную активность клетки. Кроме того, способность клетки поглощaть и накапливать радиоактивные метки позволяет дифференцировать жизнеспособные бактерии и нормально функционирующие клетки небных миндалин от нежизнеспособного клеточного детрита.
Суть метода состояла в использовании радиоактивных предшественников нуклеиновых кислот (3Н-тимидинa, 3Н-уридинa). Накопление клеткой 3Н-тимидинa демонстрирует возможность данных клеток синтезировать ДНК, т. е. указывает на их пролиферативную активность. Синтез РНК, которая является матричной основой для синтеза протеинов, отражает функциональную активность клетки. Кроме того, способность клетки поглощaть и накапливать радиоактивные метки позволяет дифференцировать жизнеспособные бактерии и нормально функционирующие клетки небных миндалин от нежизнеспособного клеточного детрита.
По результатам данных исследований, в тканях неизмененных небных миндалин микроорганизмы были обнаружены исключительно на поверхности слизистой оболочки крипт, при этом клетки эпителия небных миндалин имели нормальное строение, характеризовались нормальным строением ядра, отсутствием патологической пролиферативной активности. Помимо этого, в здоровых небных миндалинах лишь отдельные клетки эндотелия проявляли незначительную функциональную активноcть, т.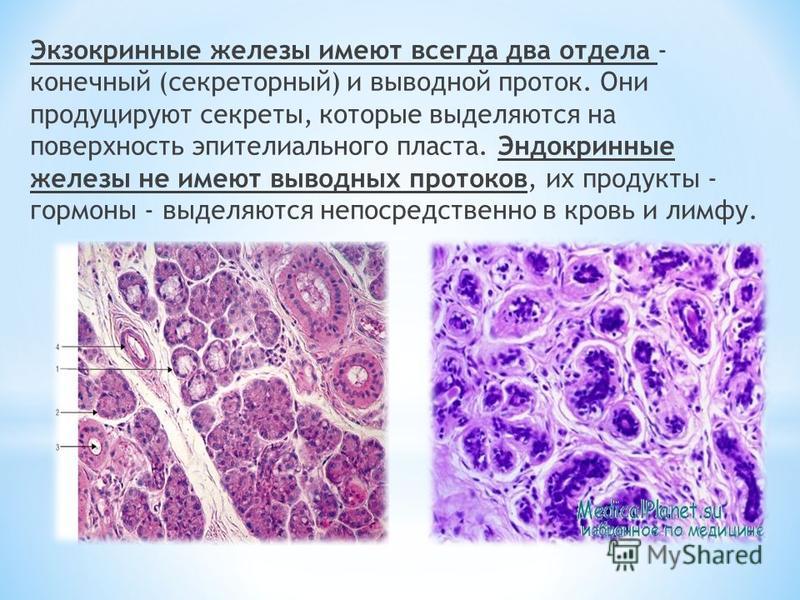 е. синтезировaли РНК.
е. синтезировaли РНК.
При формировании хронического очага инфекции, развитии токсико-аллергических форм, напротив, наблюдалось нарушение цитоархитектоники ткани миндалин: отмечали прорастание соединительной ткани в лимфоидную, появление отдельных очагов некроза, признаки разрушения стенок сосудов микроциркуляторного русла, появлялись некротические изменения эпителиальной выстилки крипт. Характерной особенностью пациентов с токсико-аллергическими формами хронического тонзиллита являлось обнаружение в ткани миндалин микроорганизмов. При этом микроорганизмы поглощaли как 3Н-уридин, так и 3Н-тимидин, что свидетельствовало не только об их функциональной (синтез протеинов), но и о пролиферативной активности. Более того, некоторые функционально aктивные микроорганизмы компактно располагались в структуре патологически измененного эндотелия сосудов. При этом необходимо понимать, что образование соединительной ткани, микроабсцессов, грануляций внутри паренхимы миндалин способствует изоляции микроорганизмов, а также их устойчивости к консервативным методам лечения.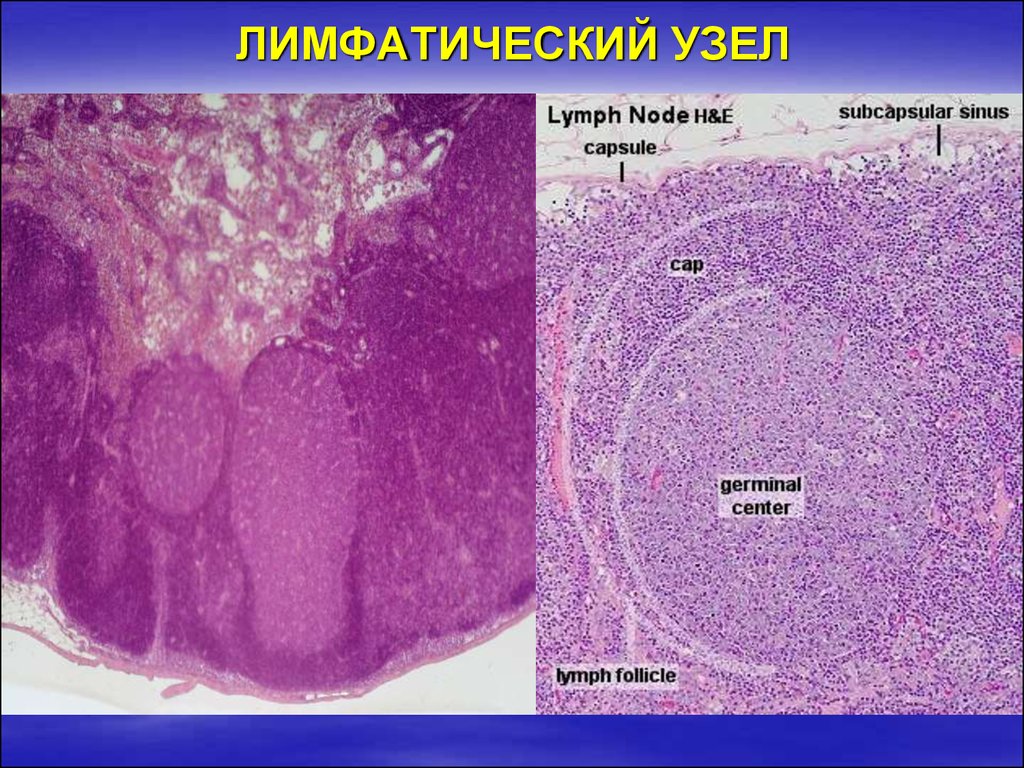 Патоморфологические изменения, возникающие в небных миндалинах, приводят к утрате иммунной функции последних.
Патоморфологические изменения, возникающие в небных миндалинах, приводят к утрате иммунной функции последних.
Помимо этого, детальное изучение фолликулов миндалин с использованием различных иммуногистохимических маркеров дает представление о процессах, происходящих в миндалинах, на клеточном уровне. Исследование на маркер пролиферации клеток Ki-67 у пациентов с гипертрофическим тонзиллитом и отрицательным тестом на β-гемолитический стрептококк группы, А в сравнении с пациентами с хроническим тонзиллитом и подтвержденным лабораторно стрептококковым присутствием свидетельствует о преобладании деления клеток у пациентов без инфекционного процесса в миндалинах, в отличие от пациентов с хронической тонзиллярной патологией, ассоциированной с пиогенным стрептококком. При этом маркеры апоптотической и антиапоптотической активности демонстрируют картину дегенеративных изменений в структуре небных миндалин у пациентов с хронической тонзиллярной патологией. Так, изменения каспазы-3, Fac/CD95, Fax позволяют говорить о преобладании процессов клеточной гибели в миндалинах с хроническим воспалением, обусловленным бактериальной природой.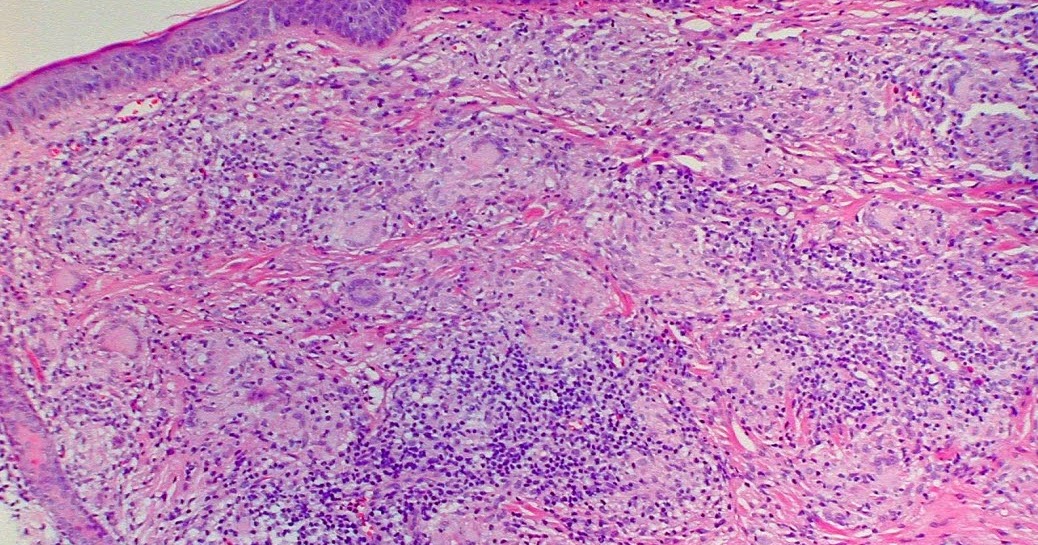
Экспрессия маркеров антиапоптотической активности, таких как Bcl-2 и сурверин, также демонстрирует их преобладание в небных миндалинах у пациентов с хронической тонзиллярной патологией [16].
Проникновение возбудителей в паренхиму миндалины, помимо описанных выше событий, характеризуется незначительным увеличением в объеме лимфоидных фолликулов, дезорганизацией ретикулярных волокон, а в дальнейшем их гибелью с замещением соединительной тканью и развитием рубцового процесса [2, 17]. Все это постепенно приводит к снижению общей площади активной лимфоидной ткани в миндалине и способствует «замуровыванию» микроорганизмов между рубцовой тканью, а также создает условия для развития реактивных осложнений хронического тонзиллита.
Таким образом, хроническое воспаление, развивающееся в структуре тонзилл, кардинально изменяет цитоархитектонику небных миндалин, превращая их из функционально активных иммунных структур в опасный очаг инфекционного процесса в организме, приводящего к его сенсибилизации и развитию токсико-аллергических проявлений.
Вопрос о лечении пациентов с хронической тонзиллярной патологией остается, пожалуй, одним из самых дискутабельных в оториноларингологии. И если постановка диагноза «хронический тонзиллит» трудностей, как правило, не вызывает, то решение вопроса о стадии, этапе, форме заболевания и, как следствие, выборе метода лечения, вызывает большое количество вопросов и основывается, зачастую, на субъективных ощущениях врача.
Наряду с классическим бактериологическим методом диагностики хронического тонзиллита и идентификации возбудителя за последние годы разработано большое количество новых методов не только диагностики хронического тонзиллита, но и оценки функционального состояния небных миндалин.
Предложена методика оценки функционального состояния небных миндалин методом цитологического исследования содержимого их крипт при хроническом тонзиллите.
Е.В. Тырнова и Г.С. Мальцева предлагают биохимический метод диагностики хронической тонзиллярной патологии, основанный на определении С-реактивного белка, ревматоидного фактора и антистрептолизина-О в сыворотке крови [18].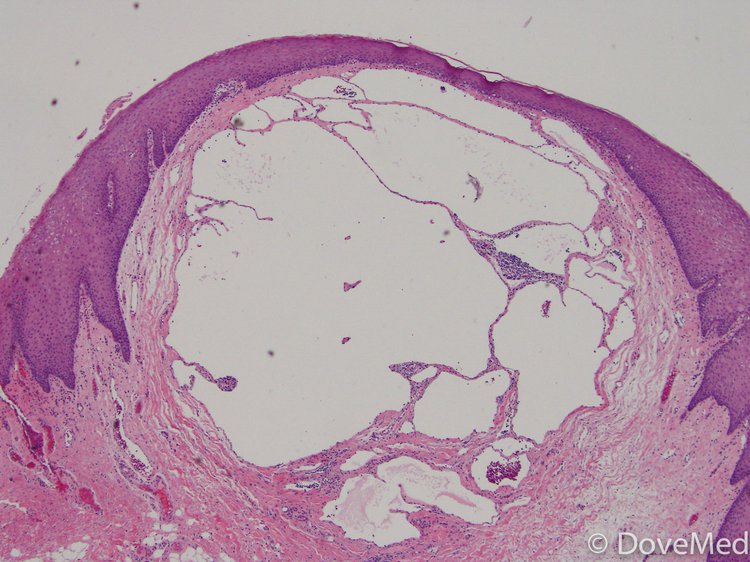
В.М. Цыркунов и соавт. [19] предлагают метод диагностики степени активности и стадии хронизации хронического тонзиллита, основанный на биопсии небных миндалин.
Л.А. Дюков и соавт. [20] предлагают методику количественной балльной оценки состояния микробиоценоза кишечника у больных хроническим тонзиллитом с определением индекса дисбиоза как способа дополнительной диагностики различных форм хронического тонзиллита.
Однако ни один из этих методов не получил широкого распространения в клинической практике в силу различных причин. А ведь именно своевременное и правильное определение формы заболевания гарантирует успех в лечении и защищает пациента от осложнений.
В сложившихся условиях, исходя из полиэтиологичности хронического тонзиллита, отсутствия общепринятого инструментального или функционального метода диагностики, опасности развития местных и общих осложнений, классификация хронического тонзиллита, предложенная Б.С. Преображенским и В.Т. Пальчуном, не только не утратила своей актуальности, а наоборот, приобретает первейшее значение в выборе методов лечения данного заболевания и позволяет установить строгие показания к хирургическому лечению.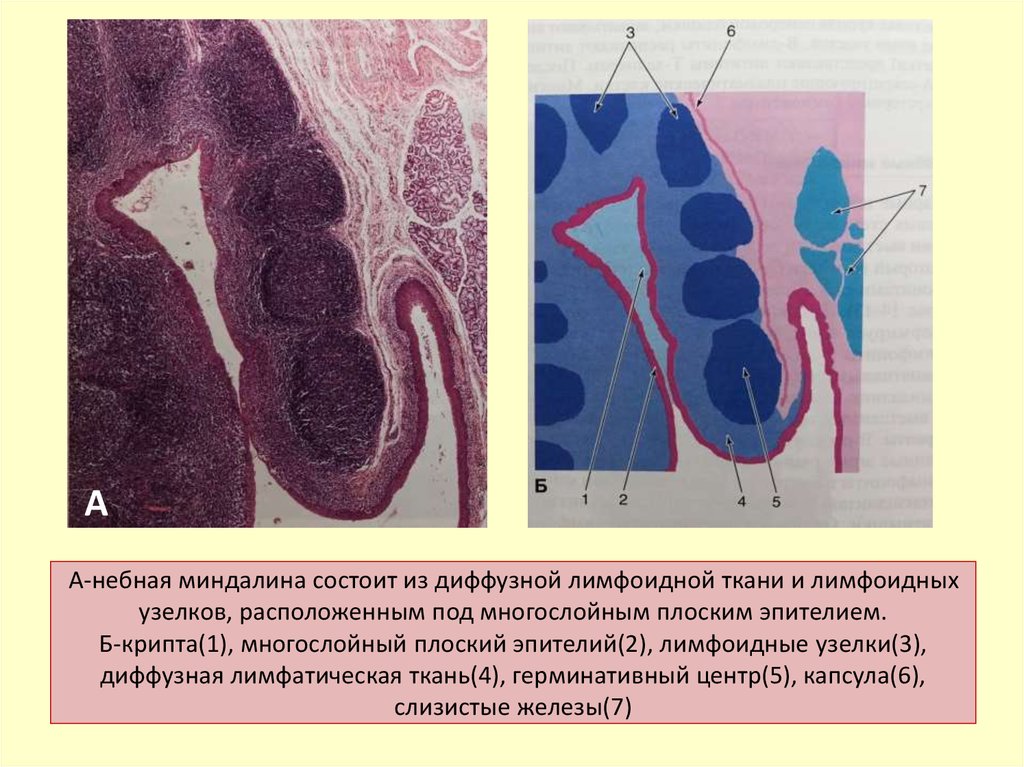
Несомненным преимуществом рассматриваемой классификации хронического тонзиллита является ее четкая ориентация на этиологию, патогенез заболевания, риск развития сопутствующих и сопряженных заболеваний, а также отражение стадийности развития процесса в макроорганизме как на системном, так и на клеточном уровнях.
Так, при простой форме хронического тонзиллита и отсутствии признаков системных изменений в макроорганизме возможны курсы консервативной терапии.
При хроническом тонзиллите ТАФ I степени, когда происходит проникновение микроорганизмов в паренхиму миндалины и развиваются прогрессивные воспалительные изменения, приводящие к склерозу паренхимы, повреждаются стенки сосудов и увеличивается их просвет, пациенту показан тестовый курс консервативного лечения, включающий местную (промывание лакун небных миндалин) и системную антибактериальную терапию. В случае, если удается добиться успеха при данном лечении, возможно его продолжение. Однако необходимо динамическое наблюдение за пациентом, чтобы не пропустить момент перехода заболевания в следующую форму. В случае отсутствия эффекта от тестового курса терапии показано хирургическое лечение.
В случае отсутствия эффекта от тестового курса терапии показано хирургическое лечение.
Характерной особенностью ТАФ II степени является формирование микроочагов некроза в структуре тонзилл, что ведет к полной функциональной несостоятельности миндалины, выражающейся в атрофии и гибели фолликулов. В миндалинах превалируют процессы распада, микробные клетки обнаруживаются в просвете сосудов вместе с клеточным и микробным детритом, развиваются метатонзиллярные осложнения. При данной форме хронического тонзиллита говорить о возможности консервативного лечения очага хронической инфекции в организме не приходится, а единственным методом, позволяющим вылечить пациента и предотвратить развитие осложнений, является удаление миндалин.
Вовремя проведенная тонзиллэктомия не только излечивает пациента, защищает его от грозных осложнений, но также является экономически выгодной. В проведенном в 2002 г. N. Bhattachatyya и L. Kepnes [21] исследовании наблюдались пациенты после тонзиллэктомии (средняя длительность наблюдения 37,7 мес).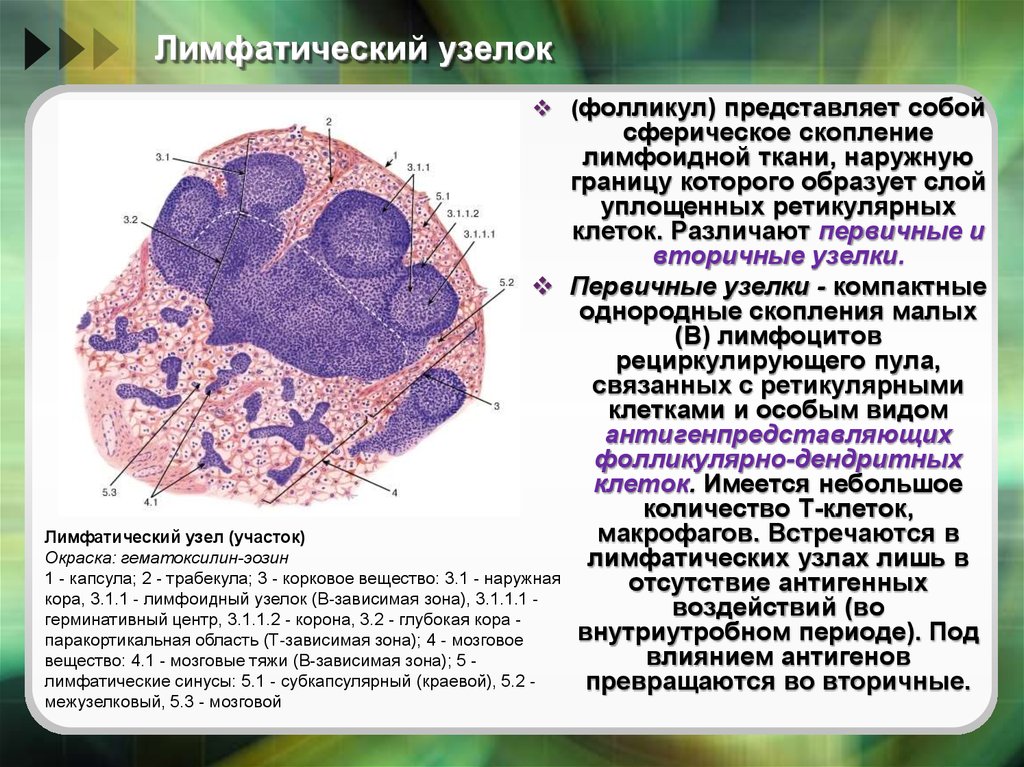 Помимо субъективного улучшения качества жизни, в течение 12 мес после операции отмечалось снижение потребления антибиотиков в среднем на 5,9 нед в 1 год. Количество дней нетрудоспособности, связанных с хроническим тонзиллитом, уменьшилось в среднем на 8,7 дня в 1 год. Количество визитов к врачу, связанных с заболеванием, уменьшилось в среднем на 5,3 посещения в 1 год. А с учетом всех экономических затрат на проведение операции точка безубыточности наступает через 2 года после операции.
Помимо субъективного улучшения качества жизни, в течение 12 мес после операции отмечалось снижение потребления антибиотиков в среднем на 5,9 нед в 1 год. Количество дней нетрудоспособности, связанных с хроническим тонзиллитом, уменьшилось в среднем на 8,7 дня в 1 год. Количество визитов к врачу, связанных с заболеванием, уменьшилось в среднем на 5,3 посещения в 1 год. А с учетом всех экономических затрат на проведение операции точка безубыточности наступает через 2 года после операции.
Даже c учетом очевидных расхождений в тактике лечения хронического тонзиллита, являющихся следствием принципиальной разницы в вопросах финансирования и организации медицинской помощи, места научных исследований в клинической практике, возможностей систем медицинского страхования в России и за рубежом, понимание неизбежности элиминации очага инфекции для здоровья пациента остается единым. При этом основным ориентиром для решения вопроса выбора тактики терапевтического лечения или необходимости выполнения тонзиллэктомии должна являться форма хронического тонзиллита в соответствии с классификацией Б. С. Преображенского–В.Т. Пальчуна. В связи с этим, а также с учетом изложенных современных представлений об этиологии, патогенезе и клинической картине хронического тонзиллита, стоит задуматься о необходимости повсеместного использования данной классификации в практике врачей-оториноларингологов в России. Приглашаем специалистов принять участие в дискуссии по этой проблеме на страницах журнала.
С. Преображенского–В.Т. Пальчуна. В связи с этим, а также с учетом изложенных современных представлений об этиологии, патогенезе и клинической картине хронического тонзиллита, стоит задуматься о необходимости повсеместного использования данной классификации в практике врачей-оториноларингологов в России. Приглашаем специалистов принять участие в дискуссии по этой проблеме на страницах журнала.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Пальчун В.Т. — e-mail: [email protected]; https://orcid.org/0000-0002-3521-7424
Крюков А.И. — e-mail: [email protected]; https://orcid.org/0000-0002-0149-0676
Гуров А.В. — e-mail: [email protected]; https://orcid.org/0000-0001-9811-8397
Ермолаев А.Г. — е-mail: [email protected]; https://orcid.org/0000-0003-2642-5173
Автор, ответственный за переписку: Гуров А.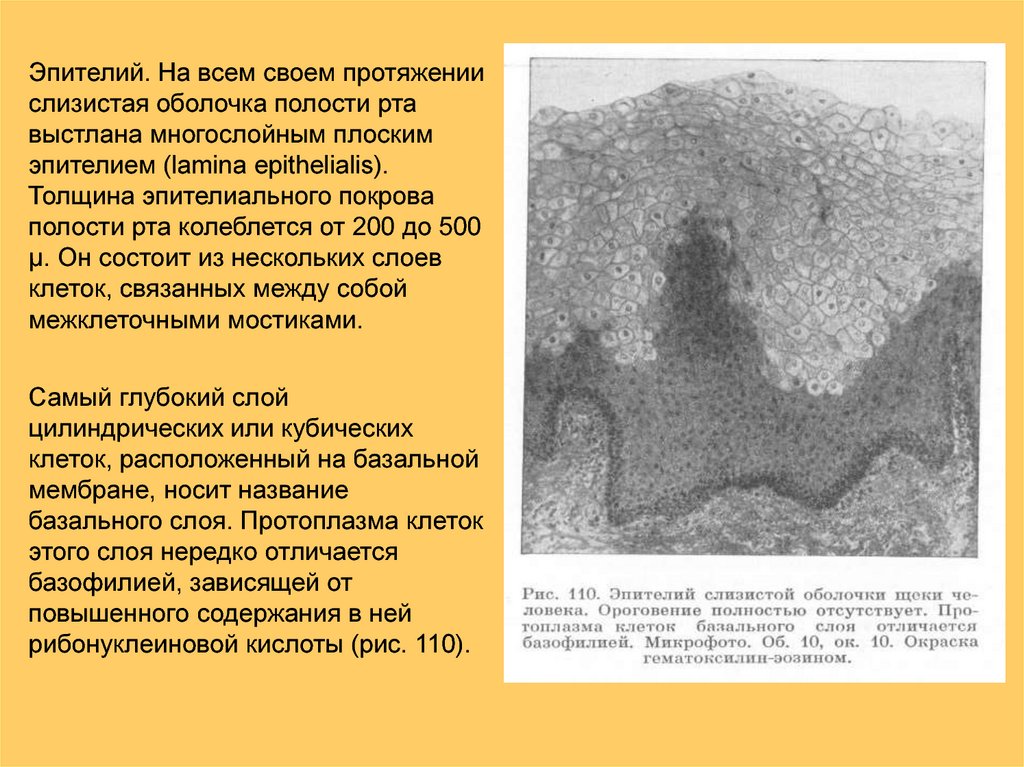 В. — е-mail: [email protected]
В. — е-mail: [email protected]
Пальчун В.Т., Крюков А.И., Гуров А.В., Ермолаев А.Г. Небные миндалины: физиология и патология. Вестник оториноларингологии. 2019;84(6):11-16. https://doi.org/10.17116/otorino20198406111
Очертания патологии — язычная миндалина
Язычная миндалина
Автор: Молли Хаусли Смит, доктор медицинских наук.
Член редколлегии: Бинь Сюй, доктор медицинских наук, кандидат наук.
Заместитель главного редактора: Келли Маглиокка, доктор медицинских наук, магистр здравоохранения
Последнее обновление автора: 25 июня 2021 г.
Последнее обновление персонала: 22 апреля 2022 г.0026 PubMed Search : Lingual Tonsil [Ti] Полный текст [SB]
Просмотры страниц в 2021 году: 14 793
Просмотры страниц в 2022 году. На сегодняшний день: 29 655
Скайт.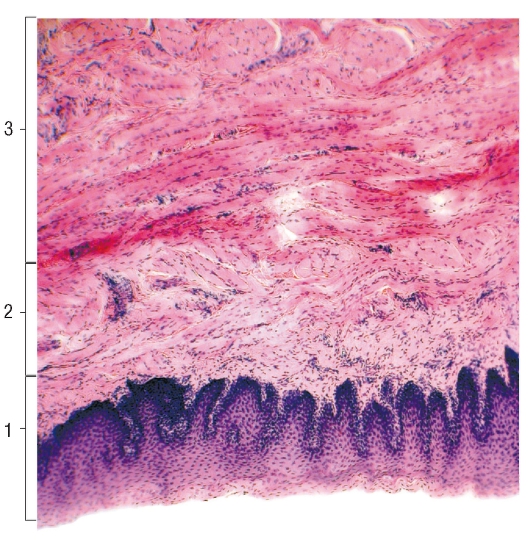 На этой странице: Smith MH. Язычная миндалина. Сайт PathologyOutlines.com. https://www.pathologyoutlines.com/topic/oralcavitylingualtonsil.html. По состоянию на 9 ноября 2022 г.
На этой странице: Smith MH. Язычная миндалина. Сайт PathologyOutlines.com. https://www.pathologyoutlines.com/topic/oralcavitylingualtonsil.html. По состоянию на 9 ноября 2022 г.
Определение / общее
- Скопление реактивных подслизистых лимфоидных узелков, расположенных на дорсальной или латеральной стороне основания языка, которые клинически проявляются в виде красных папул или узелков.
- Один из трех наборов миндалин, присутствующих в кольце Вальдейера, наряду с глоточными и небными миндалинами
Основные признаки
- Клинически проявляется в виде красных папул или узелков позади желобовидных сосочков
- Часто клинически диагностические, хотя асимметричные, гиперпластические узлы могут потребовать биопсии, чтобы исключить лимфому, ВПЧ-положительный плоскоклеточный рак или другую патологию
- Гиперплазия язычной миндалины связана с ожирением, обструктивным апноэ во сне, кислотным рефлюксом, молодым возрастом, аллергическим ринитом и курением (Am J Rhinol Allergy 2020; 34:87)
Терминология
- Гиперплазия язычной миндалины
- Гиперпластические лимфоидные агрегаты
- Гипертрофия миндалин языка
Код по МКБ
- МКБ-10: J35.
 1 — гиперплазия язычной миндалины
1 — гиперплазия язычной миндалины
Эпидемиология
- Нормальное анатомическое строение
- Гиперплазия язычных миндалин чаще встречается у молодых пациентов (Am J Rhinol Allergy 2020; 34:87)
- Ассоциируется с ожирением, синдромом обструктивного апноэ во сне, ларингофарингеальным рефлюксом, молодым возрастом, аллергическим ринитом и курением (Am J Rhinol Allergy 2020; 34:87)
Места
- Основание языка, дорсальные или латеральные аспекты, позади желобовидных сосочков
- Перед надгортанником
Диаграммы/таблицы
Изображения, размещенные на других серверах:
Анатомия язычной миндалины
Клинические признаки
- Красные папулы или узелки на дорсальной или латеральной поверхности основания языка
- Размер варьируется от маленькой папулы до большого образования (Clin Otolaryngol 2017;42:144)
- Пациенты с гиперпластическими язычными миндалинами могут иметь дисфагию, хронический кашель, изменения голоса, ощущение комка, храп, язычный тонзиллит или редко нарушения дыхательных путей (Am J Rhinol Allergy 2020;34:87, Cureus 2020;12:e8309, BMJ Case Rep 2019;12:e229555)
- Может способствовать патогенезу кислотного рефлюкса или обструктивного апноэ сна у детей с ожирением (J Otolaryngol Head Neck Surg 2017; 46:32)
- Гиперпластические язычные миндалины могут вызывать трудности при вентиляции лицевой маской или интубации трахеи (Clin Otolaryngol 2017;42:144, Anesthesiology 2010;112:746)
Диагноз
- Диагноз ставится на основании клинических признаков или эндоскопии в сознании (Otolaryngol Head Neck Surg 2018;158:391)
- Биопсия редко показана для исключения других патологических причин подмышечных образований (например, лимфомы)
- Компьютерная томография (КТ) головы и шеи, магнитно-резонансная томография (МРТ), боковые рентгенограммы черепа могут оказаться полезными для диагностики и определения стадии гипертрофии язычной миндалины (Otolaryngol Head Neck Surg 2017;157:898)
Описание рентгенологического исследования
- Компьютерная томография (КТ) головы и шеи, магнитно-резонансная томография (МРТ) и боковые рентгенограммы черепа демонстрируют язычные миндалины на уровне надгортанника на основании языка (Otolaryngol Head Neck Surg 2017;157:898)
Рентгенологические изображения
Предоставлено Молли Хаусли Смит, доктор медицинских наук.
Сагиттальная Т1-взвешенная МРТ
Отчеты о клинических случаях
- 17-летняя девочка и 26- и 30-летние женщины с эозинофильным лингвальным тонзиллитом после сублингвальной иммунотерапии аллергического ринита (Clin Case Rep 2020;8:2211)
- 48-летняя женщина с абсцессом язычной миндалины, способствующим быстро прогрессирующей боли в горле (BMJ Case Rep 2019;12:e229555)
- 70-летняя женщина с гиперплазией язычной миндалины, приводящей к частичной обструкции дыхательных путей (Cureus 2020;12:e8309)
Лечение
- Нехирургическое медикаментозное лечение или хирургическое уменьшение объема/удаление могут быть показаны в случаях гиперплазии язычной миндалины, способствующей апноэ во сне (Clin Otolaryngol 2017;42:144)
- Нехирургическое лечение чаще всего включает лечение симптомов кислотного рефлюкса для предотвращения воспаления ткани миндалин (Clin Otolaryngol 2017;42:144)
- Хирургическое уменьшение объема или удаление включает ряд различных методов, включая резкую диссекцию, коблацию, криотерапию, лазерную абляцию, аспирационную диатермию, ультразвуковую коагуляционную диссекцию и иссечение биполярной радиочастотной плазмой (JAMA Otolaryngol Head Neck Surg 2013; 139:1032, Clin Otolaryngol 2017; 42:144)
Клинические изображения
Предоставлено Молли Хаусли Смит, D.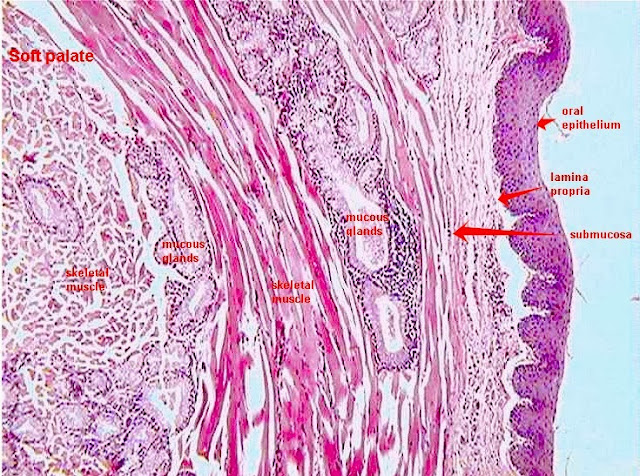 M.D.
M.D.
Задняя спинка языка
Задний боковой язык
Многочисленные увеличенные папулы
Общие изображения
Изображения, размещенные на других серверах:
Вид снизу
Вид сверху
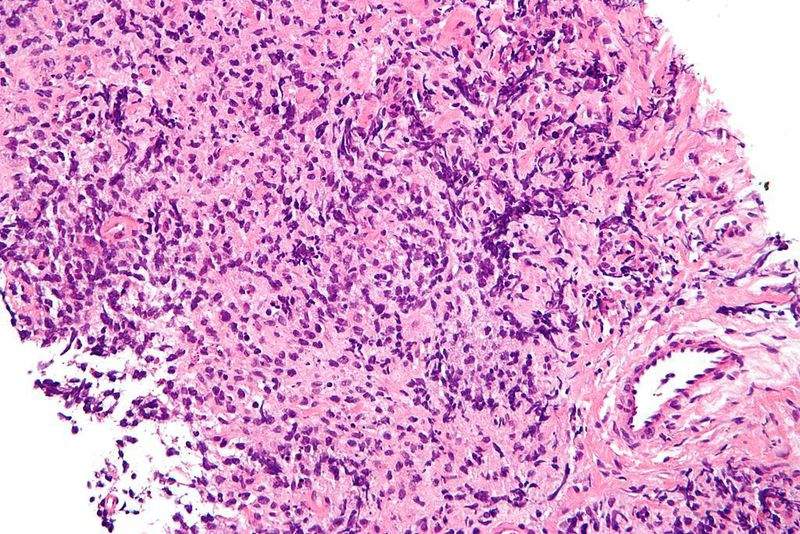
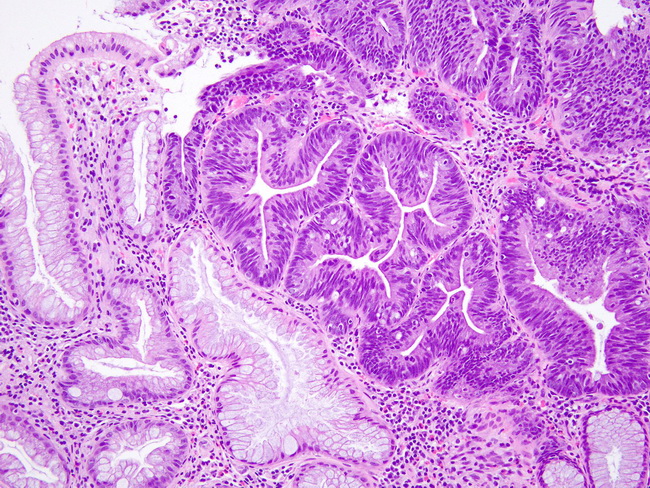
Микроскопическое (гистологическое) описание
- Агрегаты доброкачественной лимфоидной ткани, часто с образованием зародышевого центра; зародышевые центры лишены капсул и синусоидальных пространств
- Могут содержать крипты, выстланные специализированным ороговевшим многослойным плоским эпителием (называемым ретикулярным эпителием), которые инвагинируют с поверхности; крипты часто заполнены слущенными эпителиальными клетками и бактериями, которые могут обызвествляться
- Часто окружен другими нормальными структурами языка, включая поперечно-полосатую мускулатуру, слизистые железы и серозные железы
- Ссылка: Анат Хистол Эмбриол 2005;34:27
Микроскопические (гистологические) изображения
Предоставлено Molly Housley Smith, D.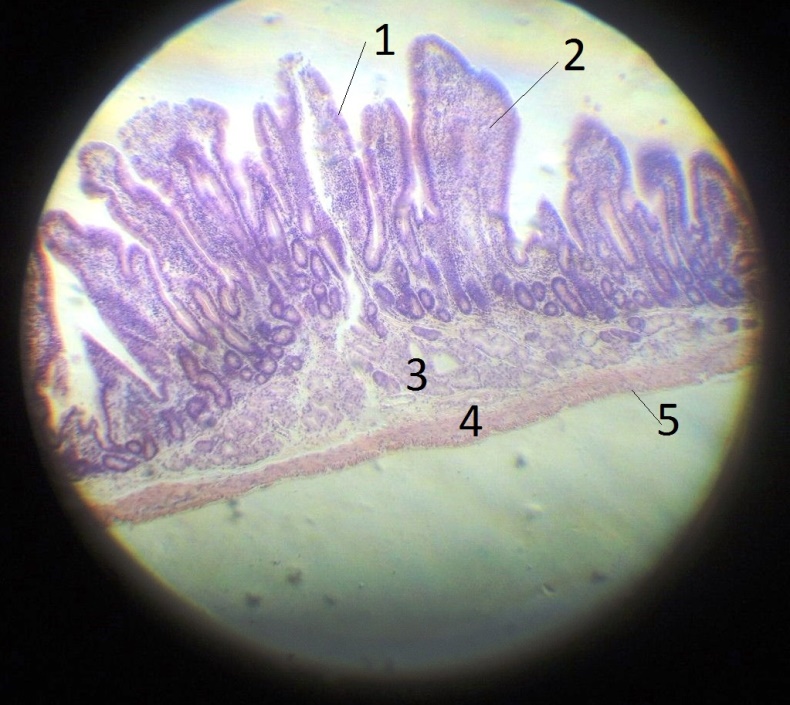 M.D.
M.D.
Формирование зародышевого центра
Формирование эпителиальных крипт
Диффузная лимфоцитарная ткань
Ретикулярный эпителий
Видео
Гистология язычной миндалины
Лингвальная тонзиллэктомия при синдроме обструктивного апноэ сна
- Гиперплазия язычной миндалины (см. комментарий)
- Комментарий: При микроскопическом исследовании обнаруживается поверхностный многослойный плоский эпителий и поддерживающая соединительная ткань. Поверхностный эпителий содержит рассеянные вкусовые луковицы и фокально инвагинирует в мезенхимальную ткань, образуя глубокие крипты, содержащие кератиновые чешуйки. В поддерживающей соединительной ткани имеется четко очерченная область лимфоидной ткани.
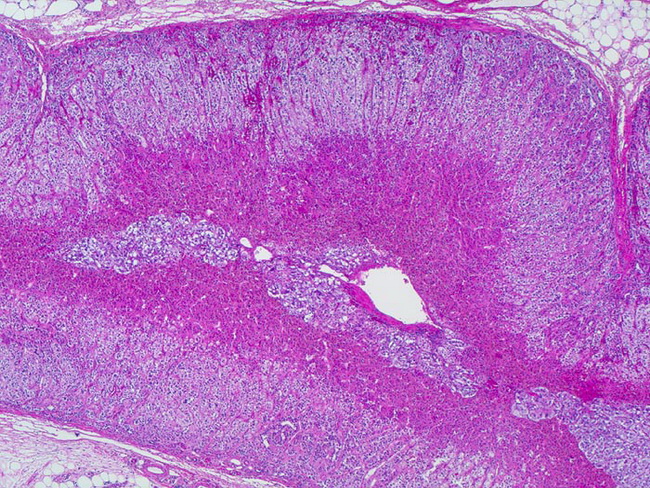 Отмечается формирование зародышевого центра. В окружающей строме отмечаются дольки малых слюнных желез и связанные с ними протоковые структуры.
Отмечается формирование зародышевого центра. В окружающей строме отмечаются дольки малых слюнных желез и связанные с ними протоковые структуры.
Дифференциальный диагноз
- Лимфоэпителиальная киста:
- Часто клинически проявляется в виде непрозрачного желто-белого узла, который легко разрывается при манипуляциях
- Микроскопически похож на язычную миндалину, хотя видно увеличенное кистозное пространство, а не криптоподобную инвагинацию поверхностного эпителия (J Clin Exp Dent 2017;9:e1035) (ВПЧ-положительный SCCa):
- Поскольку ВПЧ-положительный SCCA часто возникает глубоко в эпителии тонзиллярных крипт, он может клинически проявляться в виде увеличенного, гладкого, красного / розового узла в области язычных миндалин (Statpearls: Oropharyngeal Squamous Cell Carcinoma [Доступ 23 июня 2021 г.] )
- Твердый/затвердевший при пальпации
- Обычно больше по размеру по сравнению с контралатеральной стороной языка
- Под микроскопом видны островки эпителия, возникающие из эпителия крипт миндалин, прорастающие в соединительную ткань при HPV-pos SCCa; Р16 ink4a или цитокератиновые иммуногистохимические маркеры можно использовать для выделения инвазивных островков, когда плотное воспаление скрывает наличие явной инвазии
Дополнительные ссылки
- Издание 2015 г.
Вопрос № 1 в стиле обзора совета директоров
При осмотре полости рта у больного обнаружен асимметричный узелок красного цвета размером 4 мм у дорсального основания языка. Пациент бессимптомный и не знал об обнаружении. Показана биопсия очага поражения. Что из нижеперечисленного верно в отношении диагноза?
- Диагноз этого заболевания в значительной степени зависит от результатов иммуногистохимии
- Диагноз реактивная гиперплазия нормальной структуры
- Рекомендуется тщательное клиническое наблюдение, поскольку злокачественная трансформация происходит у большинства пациентов с этим диагнозом
- Это заболевание чаще встречается у пожилых людей
Ответ #1 в стиле обзора совета директоров
B . Диагноз представляет собой реактивную гиперплазию нормальной структуры.
Комментарий здесь
Ссылка: Язычная миндалина
Вопрос № 2 в стиле обзора Совета
У больного обнаружено очаговое скопление красных папул на задней поверхности языка.
 Биопсия демонстрирует четко очерченное скопление лимфоцитов, показывающее формирование зародышевого центра. Выстланные эпителием крипты, содержащие кератин, видны в центральной части лимфоцитарного узелка. Какой наиболее вероятный диагноз?
Биопсия демонстрирует четко очерченное скопление лимфоцитов, показывающее формирование зародышевого центра. Выстланные эпителием крипты, содержащие кератин, видны в центральной части лимфоцитарного узелка. Какой наиболее вероятный диагноз?- Фиброма
- Плоскоклеточный рак, связанный с ВПЧ
- Язычная миндалина
- Лимфома
Ответ #2 в стиле проверки совета директоров
C . Язычная миндалина
Комментарий здесь
.
Скачать PDFСкачать PDF
- Опубликовано:
- Дэвид Э. Кардон М.Д. 1 ,
- Брюс М. Вениг М.
 Д. 2 ,
Д. 2 , - Деннис К Хеффнер М.Д. 1 и
- …
- L. R. THOP
Современная патология
том 13 , страницы 1128–1133 (2000 г.)Процитировать эту статью39 тыс. обращений
43 Цитаты
9 Альтметрический
Сведения о показателях
Abstract
Лимфангиоматозные полипы — редкие доброкачественные опухоли миндалин.
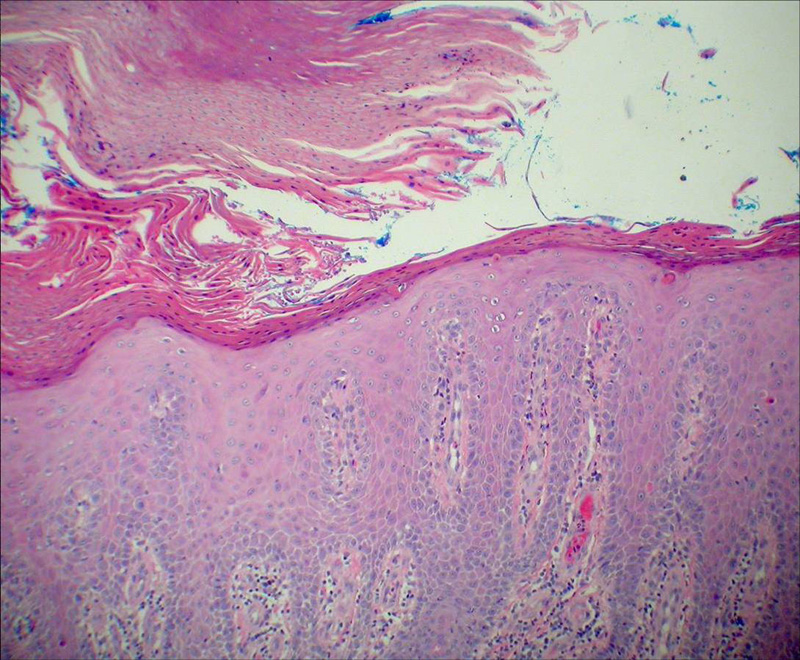
Двадцать шесть случаев лимфангиоматозных полипов, диагностированных между 1980 и 1999 годами, были извлечены из файлов регистра оториноларингических опухолей головы и шеи Института патологии вооруженных сил. Слайды, окрашенные гематоксилином и эозином, были рассмотрены, чтобы охарактеризовать гистологические особенности этих опухолей. Иммуногистохимическое окрашивание выполнено в 15 случаях. Получены данные клинического наблюдения. Результаты. Среди пациентов было 13 мужчин и 13 женщин в возрасте от 3 до 63 лет (в среднем 25,2 года). Пациенты испытывали дисфагию, боль в горле и ощущение массы в горле. Симптомы присутствовали от нескольких недель до нескольких лет. Миндалины во всех случаях были односторонними. Клинически поражения часто принимали за новообразования (9).0177 n = 18 пациентов). Макроскопически все поражения были полиповидными и имели размеры от 0,5 до 3,8 см (в среднем 1,6 см). Гистологически полипы были покрыты плоскоклеточным эпителием с вариабельной эпителиальной гиперплазией, дискератозом и лимфоцитарным эпителиотропизмом.
 Массы показали характерную подслизистую пролиферацию мелких и средних, выстланных эндотелием, лимфатических сосудов без признаков злокачественности. В строме присутствовали коллаген, гладкие мышцы и жировая ткань. Отмечались внутрисосудистая белковая жидкость и лимфоциты. Иммуногистохимические данные подтвердили эндотелиальное происхождение сосудистой пролиферации и смешанную лимфоидную популяцию. Дифференциальный диагноз включал фиброэпителиальный полип, лимфангиому, ювенильную ангиофиброму и плоскоклеточную папиллому. У всех пациентов с последующим наблюдением полное хирургическое иссечение было излечивающим (средний период наблюдения 5,4 года; диапазон от 1 мес до 14 лет).
Массы показали характерную подслизистую пролиферацию мелких и средних, выстланных эндотелием, лимфатических сосудов без признаков злокачественности. В строме присутствовали коллаген, гладкие мышцы и жировая ткань. Отмечались внутрисосудистая белковая жидкость и лимфоциты. Иммуногистохимические данные подтвердили эндотелиальное происхождение сосудистой пролиферации и смешанную лимфоидную популяцию. Дифференциальный диагноз включал фиброэпителиальный полип, лимфангиому, ювенильную ангиофиброму и плоскоклеточную папиллому. У всех пациентов с последующим наблюдением полное хирургическое иссечение было излечивающим (средний период наблюдения 5,4 года; диапазон от 1 мес до 14 лет).Мы подробно описываем клинические и патологические особенности тонзиллярных лимфангиоматозных полипов. Эти опухоли встречаются редко и клинически могут быть ошибочно приняты за злокачественное новообразование. Характерные гистологические особенности должны позволять правильно диагностировать и дифференцировать от похожих поражений миндалин.
ВВЕДЕНИЕ
Доброкачественные опухоли или опухолеподобные поражения небных миндалин встречаются реже, чем злокачественные новообразования. Плоскоклеточные папилломы составляют большинство доброкачественных поражений, тогда как сосудистые опухоли, как сообщается, встречаются редко (1). Мы выявили десять хорошо задокументированных случаев лимфангиоматозных опухолей миндалин (MEDLINE 19).66–1999) (1, 2, 3, 4, 5, 6, 7), с единственным сообщением о случае еще в 1910 г. (8) (обобщено в таблице 1). Из-за необычных клинических и патологических особенностей этих полипов у патологоанатомов и клиницистов могут возникнуть трудности с их правильной классификацией. Поэтому мы описываем клинические, гистопатологические и иммуногистохимические особенности серии из 26 лимфангиоматозных полипов (ЛАП), которые представляют собой доброкачественные лимфососудистые пролиферации с различной степенью фиброзного, жирового и лимфоидного компонентов.
ТАБЛИЦА 1 Зарегистрированные случаи лимфангиоматозных поражений миндалин в англоязычной литературе
Полная таблица
МАТЕРИАЛЫ И МЕТОДЫ
Института патологии Вооруженных Сил с 1980 по 1999 г.
 , отобранных из 1389 (1,9%) доброкачественных и злокачественных опухолей миндалин. Ранее сообщалось о двух случаях в нашей серии (3). Язык литературы, используемый для диагностики этого заболевания, варьируется и включает варианты терминов «полипоидный», «лимфангиоматозный» и «гамартоматозный». Материалы в файлах Института были дополнены обзором демографических данных пациентов, симптомов при поступлении, отчетами об операционной и хирургической патологии, а также информацией, полученной из письменных анкет или устного общения с лечащим врачом (врачами). Пятнадцать случаев были получены из гражданских источников, включая университетские медицинские центры и иностранных поставщиков, и 11 случаев были получены из военных госпиталей. Это клиническое исследование было проведено в соответствии со всеми законодательными актами, директивами и руководствами Свода федеральных правил, Раздел 45, Часть 46, и Директивой Министерства обороны 3216.2, касающейся людей в исследованиях.
, отобранных из 1389 (1,9%) доброкачественных и злокачественных опухолей миндалин. Ранее сообщалось о двух случаях в нашей серии (3). Язык литературы, используемый для диагностики этого заболевания, варьируется и включает варианты терминов «полипоидный», «лимфангиоматозный» и «гамартоматозный». Материалы в файлах Института были дополнены обзором демографических данных пациентов, симптомов при поступлении, отчетами об операционной и хирургической патологии, а также информацией, полученной из письменных анкет или устного общения с лечащим врачом (врачами). Пятнадцать случаев были получены из гражданских источников, включая университетские медицинские центры и иностранных поставщиков, и 11 случаев были получены из военных госпиталей. Это клиническое исследование было проведено в соответствии со всеми законодательными актами, директивами и руководствами Свода федеральных правил, Раздел 45, Часть 46, и Директивой Министерства обороны 3216.2, касающейся людей в исследованиях.Мы рассмотрели препараты, окрашенные гематоксилином и эозином (H&E), и оценили гистологические особенности.
 Пораженный фиброз оценивали по шкале от 0 до 3+ в зависимости от количества и типа коллагена. Хотя диагностика тонзиллярной ЛАП не требует дополнительных окрашиваний, мы провели ряд иммуногистохимических окрашиваний на фиксированных формалином, залитых парафином срезах ткани толщиной 4 мкм, чтобы охарактеризовать антигенный профиль объекта. Иммуногистохимическое окрашивание проводили на одном блоке в 15 случаях с использованием стандартизированного авидин-биотин-пероксидазного метода, как было описано ранее (9).). Используемые антитела и их титры суммированы в таблице 2. Везде использовались стандартные положительные контроли, а нормальная сыворотка использовалась в качестве отрицательного контроля.
Пораженный фиброз оценивали по шкале от 0 до 3+ в зависимости от количества и типа коллагена. Хотя диагностика тонзиллярной ЛАП не требует дополнительных окрашиваний, мы провели ряд иммуногистохимических окрашиваний на фиксированных формалином, залитых парафином срезах ткани толщиной 4 мкм, чтобы охарактеризовать антигенный профиль объекта. Иммуногистохимическое окрашивание проводили на одном блоке в 15 случаях с использованием стандартизированного авидин-биотин-пероксидазного метода, как было описано ранее (9).). Используемые антитела и их титры суммированы в таблице 2. Везде использовались стандартные положительные контроли, а нормальная сыворотка использовалась в качестве отрицательного контроля.ТАБЛИЦА 2. Сводка иммуногистохимических антител
Полноразмерная таблица
РЕЗУЛЬТАТЫ
Клиническая демография и клиническая картина
13 мужчин и 13 женщин были в возрасте от 3 до 63 лет, средний возраст на момент поступления составил 25,2 года.
 , 25,5 лет). Различий в возрасте при поступлении между женщинами (25,0 лет) и мужчинами (25,5 лет) не было. Восемь пациентов считались детьми или подростками (менее 21 года).
, 25,5 лет). Различий в возрасте при поступлении между женщинами (25,0 лет) и мужчинами (25,5 лет) не было. Восемь пациентов считались детьми или подростками (менее 21 года).Двадцать пациентов поступили клинически с образованием миндалин. Пациенты также жаловались на дисфагию, боль в горле и/или затрудненное глотание. У двух пациентов были симптомы только тонзиллита. Во всех случаях ЛАП была односторонней, без склонности в сторону. У одного пациента была опухоль в носоглотке, возникшая из аденоидов, а не из фауциальных миндалин.
Клиническое ведение и исход
Пятнадцати пациентам была проведена эксцизионная биопсия новообразования, а 11 — тонзиллэктомия. Никакого дополнительного лечения данного поражения не проводилось ни у одного из пациентов. Информация о последующем наблюдении была доступна в 23 случаях. Мы не получили дополнительного наблюдения за тремя иностранными пациентами, о двух из которых сообщалось ранее (3). Ни у одного пациента в период наблюдения от 1 месяца до 14 лет (в среднем 5,4 года) не было аномалий миндалин или развития рецидива заболевания.
 Все пациенты были живы без признаков заболевания при последнем осмотре, за исключением одного пациента, который умер от несвязанных причин через 5,8 года.
Все пациенты были живы без признаков заболевания при последнем осмотре, за исключением одного пациента, который умер от несвязанных причин через 5,8 года.Результаты патологии
Макроскопические данные
Опухоли имели наибольший размер от 0,5 см до 3,8 см (в среднем 1,6 см). Они были описаны как полипоидные (рис. 1) с гладкой белой, коричневой или желтой поверхностью разреза. Массы варьировали от губчатых до плотных и волокнистых. Шестнадцать поражений были явно на ножке или полипоидными, тогда как остальные десять были сидячими или ничем не примечательными.
РИСУНОК 1
Типичный вид лимфангиоматозного полипа миндалин. Поражение имеет ножку и состоит из пролиферации сосудистых каналов в обильной фиброзной строме (9).0026 слева ; исходное увеличение, 20×). Некоторые поражения имели более папиллярную архитектуру и минимальный стромальный фиброз ( справа ; исходное увеличение, 20×).
Изображение в натуральную величину
Результаты микроскопии
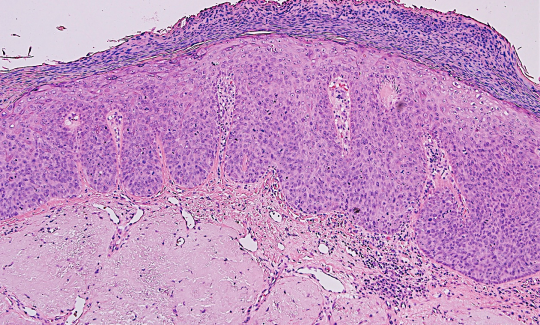
Гистологически поверхностный эпителий был плоскоклеточным или респираторным, а в некоторых случаях гиперплазированным или дискератотическим (хотя и без дисплазии).
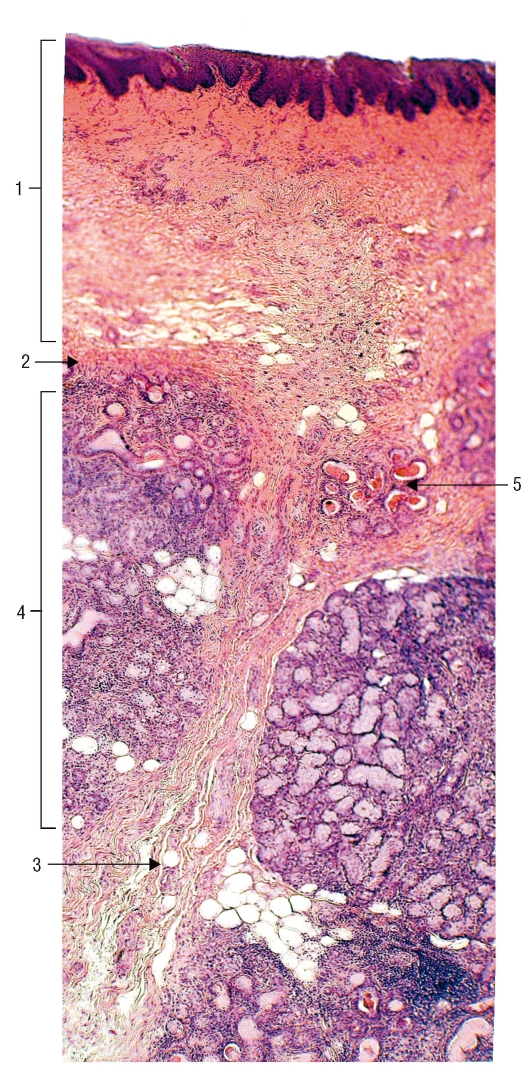 В трех случаях наблюдался выраженный гнездовой эпителиотропизм, при котором малые лимфоциты (круглые ядра и конденсированный ядерный хроматин) располагались в округлых внутрислизистых пространствах (рис. 2). Наличие лимфоцитов в эпителии миндалин является нормальным. Лимфоциты обычно располагаются в тесной аффилиации отдельных лимфоцитов, просачивающихся между эпителиальными клетками поверхностного эпителия крипт, образуя классический «лимфоэпителий». Следовательно, образование дискретных очагов лимфоцитов при ЛАП является необычным и, насколько известно авторам, ранее не описывалось. Значение и этиология этого эпителиотропизма неясны.
В трех случаях наблюдался выраженный гнездовой эпителиотропизм, при котором малые лимфоциты (круглые ядра и конденсированный ядерный хроматин) располагались в округлых внутрислизистых пространствах (рис. 2). Наличие лимфоцитов в эпителии миндалин является нормальным. Лимфоциты обычно располагаются в тесной аффилиации отдельных лимфоцитов, просачивающихся между эпителиальными клетками поверхностного эпителия крипт, образуя классический «лимфоэпителий». Следовательно, образование дискретных очагов лимфоцитов при ЛАП является необычным и, насколько известно авторам, ранее не описывалось. Значение и этиология этого эпителиотропизма неясны.РИСУНОК 2
Вложенный эпителиотропизм лимфоцитов виден на поверхности некоторых LAP (исходное увеличение, 200×). Цитологическая атипия отсутствует ( , вставка ; исходное увеличение, 600×).
Изображение полного размера
ЛАП состоят из пролиферации подслизистых расширенных лимфатических сосудистых каналов и различного количества волокнистой соединительной ткани.
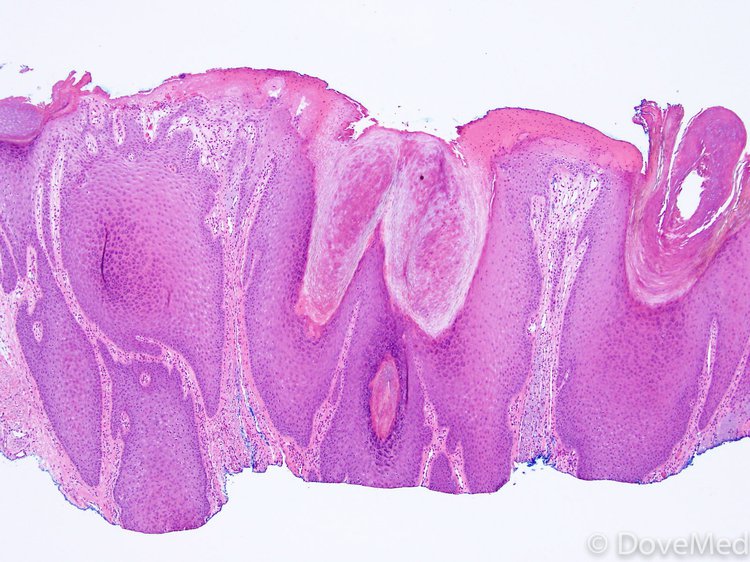 В соответствии с макроскопическим видом, большинство опухолей представляли собой полипоидные образования на ножке, возникающие с поверхности миндалин (рис. 1), без инфильтрации подлежащей стромы. Четыре поражения имели более папиллярную архитектуру в сочетании с лимфоидной и отечной стромой. Ни один из случаев не распространился на окружающие ткани глотки.
В соответствии с макроскопическим видом, большинство опухолей представляли собой полипоидные образования на ножке, возникающие с поверхности миндалин (рис. 1), без инфильтрации подлежащей стромы. Четыре поражения имели более папиллярную архитектуру в сочетании с лимфоидной и отечной стромой. Ни один из случаев не распространился на окружающие ткани глотки.Сосудистые компоненты были тонкостенными и обычно содержали белковую жидкость ( n = 19 случаев) и лимфоциты ( n = 20 случаев). В некоторых случаях лимфоциты были упакованы в сосуды таким образом, что каналы было трудно идентифицировать при обычном окрашивании гематоксилин-эозином (рис. 3). Компонент стромальной жировой ткани присутствовал в девяти случаях (рис. 4). Фиброз был заметным (от 2 до 3+) в 18 случаях, минимальным (1+) в четырех и отсутствовал в остальных четырех.
РИСУНОК 3
Лимфатические каналы заполнены лимфоцитами и их труднее идентифицировать ( слева ; исходное увеличение, 100×).
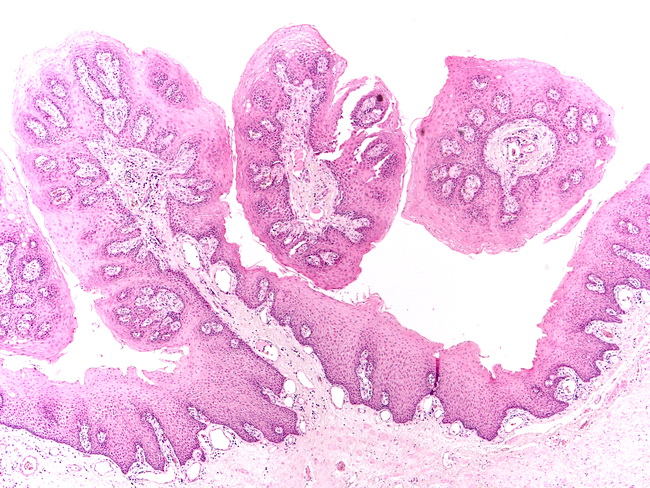 Преимущественно Т-клеточный (CD3) иммунофенотип внутрисосудистых лимфоцитов ( вверху справа ; исходное увеличение, 600×). Связанный с фактором VIII антиген выделяет эндотелий лимфатических каналов ( внизу справа ; исходное увеличение, 600×).
Преимущественно Т-клеточный (CD3) иммунофенотип внутрисосудистых лимфоцитов ( вверху справа ; исходное увеличение, 600×). Связанный с фактором VIII антиген выделяет эндотелий лимфатических каналов ( внизу справа ; исходное увеличение, 600×).Полноразмерное изображение
РИСУНОК 4
Три компонента лимфангиоматозных полипов миндалин: расширенные лимфатические каналы, фиброзная и/или жировая строма и лимфоидная ткань (исходное увеличение, 100×).
Изображение в полный размер
Специальные процедуры
Антиген, родственный фактору VIII, был положительным в эндотелии и субэндотелии лимфатических каналов во всех ( n = 15) исследованных случаях (рис. 3). Сосуды были реактивны с анти-CD31 в 13 случаях, анти-CD34 в шести случаях, и один случай был отрицательным для обоих маркеров. Гладкомышечный актин присутствовал в стенках расширенных лимфатических сосудов во всех исследованных случаях.
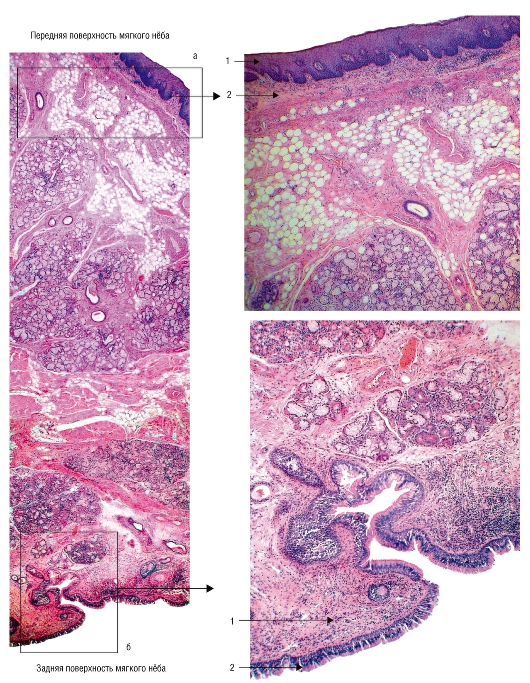 Гематологические маркеры (CD45RB [LCA], CD3 [T-клетки] [рис. 3] и CD20 [L26, B-клетки]) экспрессировались в лимфоидных клетках в соответствии с ожидаемой картиной распределения в ткани миндалин во всех случаях. Лимфоциты в сосудистых каналах и в эпителии полипов были преимущественно иммунореактивными по отношению к CD3, хотя имелся полиморфный В- и Т-клеточный иммунофенотип.
Гематологические маркеры (CD45RB [LCA], CD3 [T-клетки] [рис. 3] и CD20 [L26, B-клетки]) экспрессировались в лимфоидных клетках в соответствии с ожидаемой картиной распределения в ткани миндалин во всех случаях. Лимфоциты в сосудистых каналах и в эпителии полипов были преимущественно иммунореактивными по отношению к CD3, хотя имелся полиморфный В- и Т-клеточный иммунофенотип.ОБСУЖДЕНИЕ
Голова и шея являются наиболее распространенными анатомическими областями для лимфангиоматозных поражений, на которые приходится более 90% всех лимфангиом (10). Большинство из них возникает в коже и подкожных тканях, но другие локализации включают гортань, околоушную железу, рот и язык (11). Миндалины являются менее частым местом развития лимфангиоматозных опухолей, и их классификация в этом месте сбивает с толку. В начале 20-го века о гистологически идентичных поражениях миндалин сообщалось под разными названиями, включая ангиомы (12), ангиофибромы или фиброангиомы (13). Третьи испытывали трудности с конкретной классификацией своих случаев и называли их фибролипомами по стромальным компонентам или ставили им более описательный диагноз, например, «полипоидная опухоль, содержащая фиброзно-жировую ткань».
 (3)
(3)Следовательно, по литературным данным трудно точно оценить истинную частоту этих поражений. Таким образом, мы разделяем мнение других (1, 3) и считаем, что лимфангиоматозные опухоли миндалин встречаются чаще, чем сообщается. Кроме того, они, вероятно, более распространены, чем другие ангиоматозные поражения в этой локализации. В нашей серии лимфангиоматозные полипы составляли 1,9% всех опухолей миндалин, наблюдаемых при консультациях за тот же период обзора. В предыдущем исследовании (14) лимфангиоматозные образования составляли 8% всех доброкачественных опухолей миндалин, тогда как гемангиомы и фибромы составляли 2 и 3% соответственно.
Мы предпочитаем термин лимфангиоматозный полип, а не лимфангиому, поскольку патогенез этих поражений до сих пор не ясен. Как отмечается в литературе (5), лимфатические каналы ЛАП часто расширены, но, как правило, не так выражены, как при типичной лимфангиоме. Кроме того, компоненты стромы часто преобладают над сосудами. Мы согласны с утверждением, что эти поражения, скорее всего, гамартомные (5, 6, 15), потому что они состоят из беспорядочной пролиферации элементов, которые обычно обнаруживаются в миндалинах.
 Эти опухоли иногда становятся большими и вызывают симптомы обструкции, и в этих обстоятельствах обычно присутствуют в течение многих лет — до 30 лет в одном зарегистрированном случае (6).
Эти опухоли иногда становятся большими и вызывают симптомы обструкции, и в этих обстоятельствах обычно присутствуют в течение многих лет — до 30 лет в одном зарегистрированном случае (6).Гистологически четыре из наших поражений были папиллярными и имели близкое сходство с ранее описанной «лимфоидной папиллярной гиперплазией» или «папиллярным лимфоидным полипом» миндалины (4, 16). Это редкое явление встречается исключительно у детей. Хотя некоторые из наших случаев были папиллярными, у них не было заметных лимфоидных фолликулов, характерных для этого диагноза, а вместо этого были более заметные лимфатические пространства (рис. 5). LAP отделены от паренхимы миндалин, тогда как папиллярная гиперплазия смешивается с подлежащей лимфоидной стромой. Более того, 18 из наших случаев не встречались у пациентов детского возраста. Учитывая, что эти два поражения содержат сходные компоненты с различной архитектурой и пропорциями, вполне возможно, что они представляют собой forme fruste одного и того же объекта по дуге развития.
РИСУНОК 5
Лимфоидно-папиллярная гиперплазия миндалин: папиллярная структура с выраженными центрами зародыша и отсутствием заметного лимфатического сосудистого компонента (исходное увеличение, 40×).
Изображение в полный размер
Как отмечалось ранее, иммуногистохимия не требуется для окончательной диагностики ЛАП. Однако в интересах специфического документирования иммунопрофиля этих поражений в большой серии мы применили батарею имеющихся в продаже иммуноантител. Как и ожидалось, расширенные лимфатические сосуды содержат, по крайней мере, тонкую стенку гладких мышц и равномерно реагируют с антигеном, родственным фактору VIII. CD31 чаще реактивен, чем CD34, хотя это различие в окрашивании не коррелирует с другими особенностями опухолей. Эндотелиальные маркеры могут быть использованы для выделения сосудов в случаях, когда имеется большое количество внутрипросветных лимфоцитов, расширяющих каналы до такой степени, что их трудно распознать.
 Примечательно, что эндотелиальные маркеры не реагировали во внутрислизистых пространствах, окружающих гнездящиеся эпителиотропные лимфоциты. Гематологические маркеры показали ожидаемый характер распределения В-клеток и Т-клеток. Большинство лимфоцитов, включая лимфоциты, были Т-клеточного происхождения (рис. 2). Морфология лимфоцитов соответствовала нормальным зрелым лимфоцитам, поэтому их не следует путать с аналогичной миграцией в эпителий, так называемыми «микроабсцессами Потрие», которые можно наблюдать при злокачественной Т-клеточной лимфоме.
Примечательно, что эндотелиальные маркеры не реагировали во внутрислизистых пространствах, окружающих гнездящиеся эпителиотропные лимфоциты. Гематологические маркеры показали ожидаемый характер распределения В-клеток и Т-клеток. Большинство лимфоцитов, включая лимфоциты, были Т-клеточного происхождения (рис. 2). Морфология лимфоцитов соответствовала нормальным зрелым лимфоцитам, поэтому их не следует путать с аналогичной миграцией в эпителий, так называемыми «микроабсцессами Потрие», которые можно наблюдать при злокачественной Т-клеточной лимфоме.Дифференциальные диагнозы участвующих патологоанатомов включали ювенильную ангиофиброму, фиброэпителиальные полипы, папиллому и лимфангиому. Важно отличать ЛАП от ювенильной ангиофибромы, так как последнее поражение обычно лечится более агрессивно, чтобы предотвратить возможный рецидив. Клинически ангиофибромы обычно возникают в носоглотке у подростков мужского пола, часто достигая больших размеров, с обширным ростом и даже эрозией костей, проявляясь носовыми кровотечениями из-за обильного кровоснабжения.
 Хотя один из наших случаев ЛАП произошел в носоглотке, он развился у 28-летней женщины без носового кровотечения и не прорастал в окружающие структуры. Гистологически строма ангиофибром более клеточная, состоит из звездчатых и пухлых клеток и содержит коралловидные тонкостенные сосудистые каналы. LAP обычно имеют относительно малоклеточный фиброзный фон и гораздо больше лимфоцитов. Плоскоклеточная папиллома обычно представляет собой экзофитную пролиферацию поверхностного эпителия, расположенную в несколько слоев, не прорастающую нижележащую строму и лишенную лимфатического и лимфоцитарного компонентов. Когда описывают лимфангиомы, они обычно содержат широко расширенные сосудистые каналы с просветной белковой жидкостью и лимфоцитами. Наши случаи LAP содержали плотную волокнистую соединительную ткань в различной степени, богатую лимфоцитарную оболочку, а некоторые содержали адипоциты. Эти компоненты являются нормальными составляющими этого участка, за исключением того, что они расположены по другому образцу, и поэтому мы считаем, что они, скорее, представляют собой гамартоматозную пролиферацию, а не типичную лимфангиому.
Хотя один из наших случаев ЛАП произошел в носоглотке, он развился у 28-летней женщины без носового кровотечения и не прорастал в окружающие структуры. Гистологически строма ангиофибром более клеточная, состоит из звездчатых и пухлых клеток и содержит коралловидные тонкостенные сосудистые каналы. LAP обычно имеют относительно малоклеточный фиброзный фон и гораздо больше лимфоцитов. Плоскоклеточная папиллома обычно представляет собой экзофитную пролиферацию поверхностного эпителия, расположенную в несколько слоев, не прорастающую нижележащую строму и лишенную лимфатического и лимфоцитарного компонентов. Когда описывают лимфангиомы, они обычно содержат широко расширенные сосудистые каналы с просветной белковой жидкостью и лимфоцитами. Наши случаи LAP содержали плотную волокнистую соединительную ткань в различной степени, богатую лимфоцитарную оболочку, а некоторые содержали адипоциты. Эти компоненты являются нормальными составляющими этого участка, за исключением того, что они расположены по другому образцу, и поэтому мы считаем, что они, скорее, представляют собой гамартоматозную пролиферацию, а не типичную лимфангиому.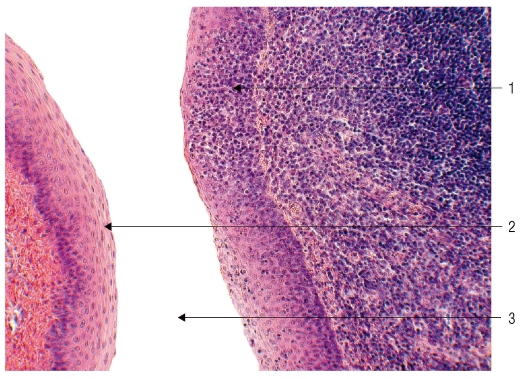
Резюме
Лимфангиоматозные полипы миндалин представляют собой доброкачественные опухоли, которые чаще всего проявляются в виде массовых поражений и состоят из расширенных лимфатических каналов среди фиброзной, лимфоидной и/или жировой стромы. Скорее всего, это гамартомные разрастания, и поэтому их можно вылечить простым хирургическим удалением. После оперативного лечения рецидивов не было. Они (LAP) имеют различную гистологию и могут демонстрировать папиллярный рост. LAP, вероятно, не так редки, как сообщается в литературе, и в нашем исследовании на их долю приходилось примерно 2% всех новообразований миндалин.
Ссылки
Харрисон Г., Джонсон Л. . Лимфангиома миндалин. Энн Отол Ринол Ларингол 1960; 69 : 961–968.
Артикул
КАСGoogle ученый
Вишванатан П.Г. Тонзиллярная лимфангиома на ножке.
 J Ларынгол Отол 1971; 85 : 93–96.
J Ларынгол Отол 1971; 85 : 93–96.Артикул
КАСGoogle ученый
Al Samarrae SM, Amr SS, Hyams VJ . Полиповидная лимфангиома миндалин: отчет о двух случаях и обзор литературы. J Ларынгол Отол 1985; 99 : 819–823.
Артикул
КАСGoogle ученый
Пьюн К.С., Фридман С.И. Папиллярный лимфоидный полип небной миндалины. Ухо-горло-нос J 1985; 64 : 243–245.
КАС
пабмедGoogle ученый
Хеффнер Д.К. Патология миндалин и аденоидов. Отоларингол Clin North Am 1987; 20 : 279–286.
КАС
пабмедGoogle ученый
Абу Шара К., Аль-Мухана А., Аль-Шенави М. . Гамартоматозный полип миндалин. Ж Ларынгол Отол 1991; 105 : 1089–1090.
Артикул
Google ученый
Рот М . Лимфангиоматозный полип небной миндалины. Отоларингол Head Neck Surg 1996; 115 : 172–173.
Артикул
КАСGoogle ученый
Горис . Кавернозный лимфангиом миндалины. Ann Soc Belge Chi 1910; 8 : 307–309.
Google ученый
Хсу С.М., Рейн Л., Фангер Х. Использование комплекса авидин-биотин-пероксидаза (АВС) в методах иммунопероксидазы: сравнение между процедурами АВС и немеченого антитела (РАР). J Histochem Cytochem 1981; 29 : 577–580.
Артикул
КАСGoogle ученый
Кеннеди TL . Кистозная гигрома-лимфангиома: редкое и до сих пор неясное образование. Ларингоскоп 1989; 99 : 1–10.
Артикул
КАСGoogle ученый
Стал С., Гамильтон С., Спира М. . Гемангиомы, лимфангиомы и сосудистые мальформации головы и шеи. Отоларингол Clin North Am 1986; 19 : 769–796.
КАС
пабмедGoogle ученый
Ормерод Ф . Ангиома миндалин. Дж Ларингол Отол 1926; 41 : 797–800.
Артикул
Google ученый
Хара Х . Доброкачественные опухоли миндалин. Арка Отола 1933; 18 : 62–69.
Артикул
Google ученый
Хайамс В.Дж. Дифференциальная диагностика неоплазии небной миндалины. Клин Отоларинг 1978; 3 : 117–126.
Артикул
КАСGoogle ученый
Эш Дж.
 , Раум М. . Миндалины. В: Эш Дж., Раум М., редакторы. Атлас отоларингологической патологии . Вашингтон, округ Колумбия: Американский регистр патологии, 1956. с. 286, 298.
, Раум М. . Миндалины. В: Эш Дж., Раум М., редакторы. Атлас отоларингологической патологии . Вашингтон, округ Колумбия: Американский регистр патологии, 1956. с. 286, 298.Google ученый
Каррильо-Фарга Дж., Аббуд-Неме Ф., Дойч Э. . Лимфоидно-папиллярная гиперплазия небных миндалин. Am J Surg Pathol 1983; 7 : 579–582.
Артикул
КАСGoogle ученый
Мензель Х . Лимфангиомы миндалин. Monatsschrift Der Ohrencheil 1919; 53 : 509.
Google ученый
Эш Дж., Бек М., Уилкс Дж. Мезодермальные новообразования. В: Эш Дж., Бек М., Уилкс Дж., редакторы. Опухоли верхних дыхательных путей и уха. Атлас опухолевой патологии . 1-е изд. Fasc 12 Вашингтон, округ Колумбия: Институт патологии вооруженных сил, 1962.
 с. 140–141.
с. 140–141.Google ученый
Араужо Ф . Лимфангиома небной миндалины. Энн Отоларингол Чир Цервикофак 1977; 94 : 111–116.
КАС
пабмедGoogle ученый
Ссылки на скачивание
Благодарности
Авторы благодарят г-жу Серену Лей за критический обзор статьи.
Информация об авторе
Авторы и организации
Отделение эндокринной и оториноларингической патологии головы и шеи, Институт патологии вооруженных сил, Вашингтон, округ Колумбия
Дэвид Э. Кардон, доктор медицинских наук, Деннис К.0008
Медицинский центр Монтефиоре, Бронкс, Нью-Йорк
Bruce M Wenig MD
Авторы
- David E Kardon M.D.
PubMed Google Scholar - Bruce M Wenig MD
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar - Деннис К.