Лямблии в грудном молоке: как вылечить лямблий во время ГВ — 5 ответов на Babyblog
Лямблиоз. Симптомы, профилактика, лечение — Доказательная медицина для всех
Лямблиоз (жиардиаз) — заболевание, вызываемое простейшими — лямблиями, паразитирующими в двенадцатиперстной и начальном отделе тонкого кишечника. Вопреки распространенному мнению, лямблии не поражают желчные пути и желчный пузырь – желчь для них губительна. Впервые роль лямблий как возбудителя заболевания описал в 1859 г. врач Д.Ф.Лямбль.
Ежегодно в России заражается лямблиозом более 130 тысяч человек. Человек заражается при проглатывании цист лямблий.
Пути передачи лямблий
Три основных способа попадания в организм человека:
- При употреблении воды из загрязненного источника. Это наиболее частый вариант заражения. Опасны не только непосредственное употребление воды, но и использование ее для мытья продуктов питания, приготовления напитков и т.д. Опасны не только открытые источники, но и водопроводная вода в регионах с несоблюдением стандартов очистки воды.
 Один из распространенных вариантов заражения лямблиозом – плавательные бассейны. Хлорирование не уничтожает цисты лямблий.
Один из распространенных вариантов заражения лямблиозом – плавательные бассейны. Хлорирование не уничтожает цисты лямблий. - Возможно заражения при употреблении плохо промытых фруктов, ягод и овощей. С учетом бытующей в России традиции вносить в компост, которым удобряют грядки, человеческие фекалии, этот путь весьма вероятен. Необходимо уделять внимание правилам пищевой безопасности.
- От человека к человеку. Данный вид заражения возможен при несоблюдении правил личной гигиены, или при незащищенном анальном сексе. Если вы и ваша семья моете руки после туалета, передача заражения от членов семьи не происходит.
Симптомы лямблиоза
Нередко лямблиоз протекает без симптомов, но могут развиться и следующие его проявления:
- Диарея или послабления стула, сменяющиеся запорами. Диарея при лямблиозе протекает мягко, стул бывает 3-5 раз в день, без большого количества слизи, состояние больного в целом не страдает.
 Температура повышается очень редко.
Температура повышается очень редко. - Боли в животе, особенно утренние «тощаковые». Для лямблиоза характерно снижение болевого синдрома после еды.
- Спазмы в животе, газы, вздутие живота
- Тошнота или рвота (редко)
- Потеря в весе
Обычно заболевание длится от двух до четырех недель, но возможен переход в хроническую форму, когда заболевание с менее выраженными симптомами длится 3-4 месяца, затем происходит самопроизвольное выздоровление. Длительное нахождение лямблий в желудочно-кишечном тракте человека может приводить к ухудшения всасывания полезных веществ из пищи. Например, в 40% случаев поражения лямблиями сопровождается нарушением всасывания лактозы – молочного сахара. Одно из возможных следствий частых повторных лямблиозов – развитие железодефицитной анемии.
Диагностика лямблиоза
Основным методом диагностики заболевания является выявление цист лямблий в стуле.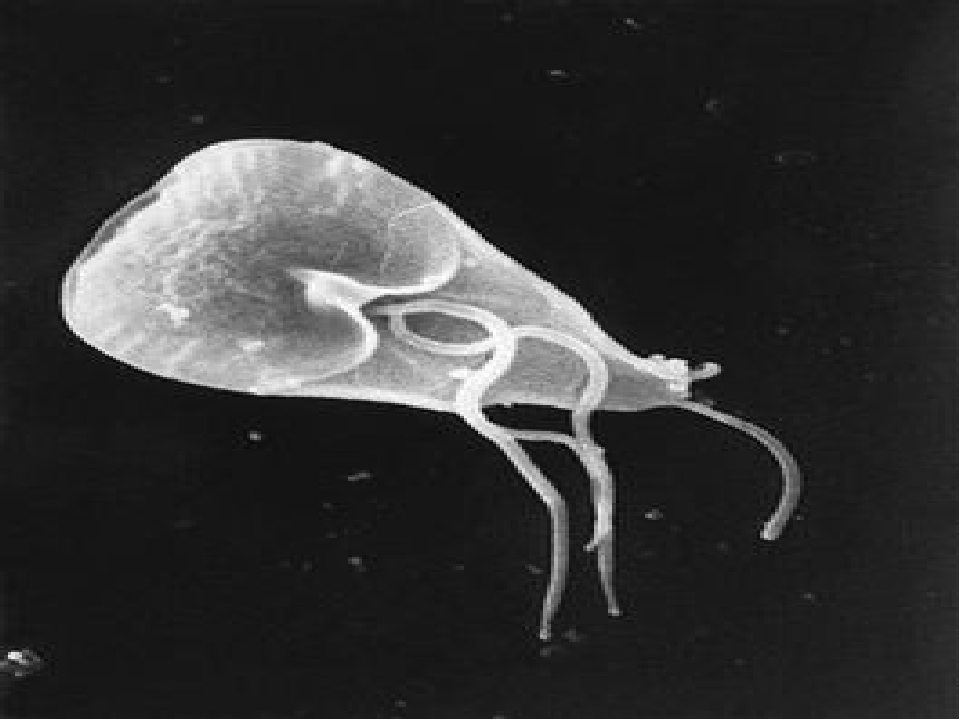 Исследования называется «кал на яйца глист». В последние годы во многих лабораториях стали выполнять анализ кала в консерванте, такой анализ выявляет как цисты, так и вегетативные формы лямблий. Для лямблий характерен прерывистый цистогенез, «слепые» промежутки могут длиться до 2-х недель, поэтому при отрицательном результате анализ необходимо сдать трижды. Промежутки между анализами произвольные.
Исследования называется «кал на яйца глист». В последние годы во многих лабораториях стали выполнять анализ кала в консерванте, такой анализ выявляет как цисты, так и вегетативные формы лямблий. Для лямблий характерен прерывистый цистогенез, «слепые» промежутки могут длиться до 2-х недель, поэтому при отрицательном результате анализ необходимо сдать трижды. Промежутки между анализами произвольные.
Лечение лямблиоза
Лечение проводится препаратами с известной активностью против лямблий. Чаще всего при лечении используются следующие препараты:
- Метронидазол
- Альбендазол
- Фуразолидон
- Макмирор
- Орнидазол
- Тинидазол
Обычно лечение быстрое и эффективное. Если контрольные исследования продемонстрировали неэффективность лечения, врач порекомендует сменить препарат, изменить его дозу или длительность приема.
Течение болезни без симптомов у детей и взрослых в лечении не нуждается, это носительство, которое излечивается самопроизвольно.
Во время лечения рекомендуется диета с максимальным ограничением коротких углеводов (сладкое, мучное) и увеличением доли белков в пище. Также рекомендуется ограничение молочных продуктов для уменьшения симптоматики.
При выраженных симптомах у ребенка (длительная и частая диарея) лямблиоз может сопровождаться потерей электролитов. В этом случае необходимо связаться с врачом и обсудить необходимость применения солевых растворов.
Лечение и грудное вскармливание: если вы кормите грудью, поставьте в известность своего врача, для подбора препаратов безопасных для кормящих матерей.
Лямблиоз при грудном вскармливании: в Вашем грудном молоке находятся вещества защищающие Вашего ребенка. У детей находящихся на грудном вскармливании риск заражения значительно ниже, а проявления заболевания существенно мягче.
Профилактика заболеваемости
- Мойте руки с мылом перед едой и после посещения туалета
- Мойте руки водой с мылом после смены подгузников или пеленок
- Следите, что бы при смене подгузников или пеленок каловые массы не запачкали Вашу одежду и окружающие предметы.

- Старайтесь не глотать воду во время купания.
- Обеззараживайте воду кипячением во время путешествий и на природе. Использование бутилированной не гарантирует не заражение лямблиями.
- Кипятите воду не менее 10 минут.
- Если не возможно вскипятить, добавьте пять капель настойки йода на один литр, и подождите 30 минут.
- Тщательно промывайте зелень, овощи и фрукты с последующим ополаскиванием в кипяченой воде.
симптомы, причины, лечение, профилактика, осложнения
Причины
От чего может быть лямблиоз в период грудного вскармливания, и как проявляется заболевание на данном этапе? В случае лямблиоза, провоцирующим фактором являются микроскопические паразиты, известные, как лямблии. После попадания в организм будущей мамы, микроорганизмы локализуются в тонком кишечнике и развиваются там в активной форме или оставаясь неактивными.
Заражение происходит фекально-оральным путем. Так, цисты – под таким названием известны неактивные лямблии, – попадают в среду вместе с каловыми массами, принадлежащими человеку или животному. Здесь местом «обитания» лямблий являются сточные воды, естественные и искусственные водоемы с застоялой водой. Находясь в водоеме, лямблии остаются жизнеспособными на протяжении месяцев, с легкостью выдерживая заморозки и высокие температуры, вплоть до показателей в 50 градусов. Гибель лямблий происходит только при кипячении.
Заражение может вызвать контакт с фекалиями носителя заболевания – человека или домашнего животного, – употребление некипячёной воды, грязных фруктов и овощей. Случаи контактно-бытового заражения встречаются намного реже.
Симптомы
Как правило, после родов, когда организм кормящей мамы еще ослаблен, заболевание проявляется не тогда, когда начинается активность микроорганизмов, а позже. В некоторых случаях признаки могут отсутствовать полностью или быть слабо выраженными и не вызывать подозрений у пациентки. Аналогичным образом встречаются ситуации, когда болезнь проходила без вмешательства специалистов в течение нескольких недель или месяцев.
В некоторых случаях признаки могут отсутствовать полностью или быть слабо выраженными и не вызывать подозрений у пациентки. Аналогичным образом встречаются ситуации, когда болезнь проходила без вмешательства специалистов в течение нескольких недель или месяцев.
Данные истории являются скорее исключением, чем правилом, и не говорят о возможности пренебрежения обращением к врачам. Есть вероятность того, что болезнь будет проявляться продолжительным и серьезным нарушением функционирования желудочно-кишечного тракта, а также органов пищеварительной системы.
В большинстве случаев первые признаки лямблиоза можно распознать в первую-вторую неделю после инфицирования. На этом этапе глистные организмы уже успевают размножиться и активизироваться, воздействуя на кишечник. Определить лямблиоз и его тип можно, обратив внимание на следующие симптомы:
- Тошноту и рвотные позывы, плохой аппетит, потерю массы тела, боли в области расположения пупка, запоры и метеоризм. Данные признаки указывают на кишечный лямблиоз.

- Дискинезию желчевыводящих путей, чувство тяжести в правой стороне тела, болям с локализацией, типичной для панкреатита и схожих заболеваний. Это – характерная симптоматика для гепатобилиарного лямблиоза.
- Головные боли, нервные срывы, утомляемость, нарушения сна, вегетососудистую дистонию. Наличие этих симптомов указывает на астено-невротический лямблиоз.
- Атопический дерматит или высыпания других видов на кожных покровах, зуд, крапивница, отеки Квинке, остальные аллергические симптомы. Такими проявлениями сопровождается токсико-аллергический лямблиоз.
Диагностика лямблиоза у кормящих мам
Диагностировать заболевание можно, изучив результаты лабораторных анализов крови и кала. Постановка диагноза на основании этих данных гарантирует точность до 70-ти процентов. В целях повышения этих показателей, лабораторные исследования биологических составов выполняются несколько раз с периодичностью – 1 раз в 3-4 дня. Дополнительно осуществляется проверка кала на антигены.
Осложнения
Чем опасен лямблиоз, когда речь идет о периоде грудного вскармливания? Опасными являются прежде всего симптомы этого заболевания, а именно – истощение, понос, нарушения сна и др. Они могут вызвать преждевременное прекращение лактации. Кроме того, негативные последствия возникают при самостоятельном увеличении дозировки противопаразитарных препаратов и отсутствия поддерживающей витаминной терапии.
Лечение
Вылечить лямблиоз достаточно легко, если симптомы заболевания были обнаружены на ранних сроках, а кормящая мама вовремя обратилась к врачу за квалифицированной помощи. В период кормления грудью могут применяться все методы, с которыми традиционно работают специалисты. Так, решая, что делать с лямблиозом у женщины во время грудного кормления, врач может использовать лечение противопаразитарными, антибиотическими препаратами. Аналогично важно назначение правильной диеты без жирных и жареных продуктов. В рамках диеты при лямблиозе, источником углеводов являются преимущественно бананы. В остальном, рацион кормящей мамы состоит из рисового отвара, тостов, фруктового пюре и обильного питья.
Аналогично важно назначение правильной диеты без жирных и жареных продуктов. В рамках диеты при лямблиозе, источником углеводов являются преимущественно бананы. В остальном, рацион кормящей мамы состоит из рисового отвара, тостов, фруктового пюре и обильного питья.
Что можете сделать вы
Для того чтобы не только вылечить лямблиоз, но и исключить вероятности заражения окружающих или повторного инфицирования самой беременной женщины, нужно:
- избавиться от длинных ногтей,
- мыть руки после каждого контакта с носителем заболевания,
- использовать отдельную посуду на период лечения,
- строго соблюдать все рекомендации врача.
Что делает врач
Начиная лечить лямблиоз, врач назначает женщине симптоматическую терапию. Первая помощь заключается в устранении поноса и нормализации пищеварительных функций. Это достигается за счет использования противопаразитарных препаратов и антибиотиков. В процессе лечения врач осуществляет динамическое наблюдение за пациенткой до тех пор, пока не убедится в отсутствии инфекции.
Профилактика
Наиболее эффективный способ предотвратить лямблиоз – это соблюдение правил личной гигиены и термической обработки продуктов перед употреблением. Обязательна тщательная очистка всех продуктов, предварительное кипячёние воды для питья.
Оцените материал:
спасибо, ваш голос принят
Статьи на тему
Показать всё
Пользователи пишут на эту тему:
Показать всё
Вооружайтесь знаниями и читайте полезную информативную статью о заболевании лямблиоз у кормящих мам. Ведь быть родителями – значит, изучать всё то, что поможет сохранять градус здоровья в семье на отметке «36,6».
Узнайте, что может вызвать недуг лямблиоз у кормящих мам, как его своевременно распознать. Найдите информацию о том, каковы признаки, по которым можно определить недомогание. И какие анализы помогут выявить болезнь и поставить верный диагноз.
В статье вы прочтёте всё о методах лечения такого заболевания, как лямблиоз у кормящих мам. Уточните, какой должна быть эффективная первая помощь. Чем лечить: выбрать лекарственные препараты или народные методы?
Также вы узнаете, чем может быть опасно несвоевременное лечение недуга лямблиоз у кормящих мам, и почему так важно избежать последствий. Всё о том, как предупредить лямблиоз у кормящих мам и не допустить осложнений. Будьте здоровы!
Вопрос от: алена — Клиника Здоровье 365 г. Екатеринбург
Вопрос Иммунологу
Вопрос от алена
Вопрос: . мне 36 лет, после рождения третьего ребенка(1г 2 м назад)у меня сильно снизился иммунитет.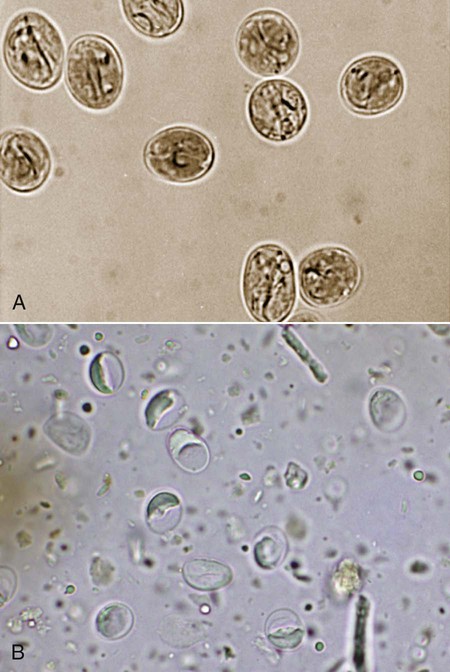 начался фурункулез ,лечилась ,но безуспешно, последнний раз 3 дня назад сдали со старшим сыном анализ в СЭС на лямблии, лямблии были обнаружены у обоих(у сына та же проблема с фурункулезом .боли в суставах и еще месяц как обнаружился стафилококк золотистый)
начался фурункулез ,лечилась ,но безуспешно, последнний раз 3 дня назад сдали со старшим сыном анализ в СЭС на лямблии, лямблии были обнаружены у обоих(у сына та же проблема с фурункулезом .боли в суставах и еще месяц как обнаружился стафилококк золотистый)
Иммунолог назначила мне и мужу лечение от лямблей
1 немозол(400)по 1 т -5дн
Аллахол по 2т 3 р-5 дн
2 этап-хилак по 40 кап 3 р-10дн
Одновременнобактисуптил 1 кап 3р-10 дн
3 этап только мне эрсифурил 200 по 1 т 4 р -7 дн
Т-активин
Сыну(14 лет .70 кг)-эрсифурил200.4р+холензим2 др*3р-7дн
2 эт-хилак и бактисупт
3 эт-тинидазол 4 т однокр.
Маленьким сыновьям 3г 4 м(15кг) и 1г2м(10кг)-Фурозолидон и аллахол
Младший сын находиться на грудном вскармливании ,но иммунолог все равно назначила немозол(на всякий случай еще от глистов )насколько я знаю немозол токсичен и при лактации применять нельзя. Иммунолог довольно в резкой форме сказала,что кормить надо было бросать когда ребенку было месяцев 8. Резко оторвать от груди или на время не представляется возможным(хотя в ближайшее время планирую отлучать) ,а лечиться(и всех лечить одновременно) планирую начать через несколько дней И в связи с этим у меня вопрос:
Резко оторвать от груди или на время не представляется возможным(хотя в ближайшее время планирую отлучать) ,а лечиться(и всех лечить одновременно) планирую начать через несколько дней И в связи с этим у меня вопрос:
1. Адекватно ли назначенное лечение?
2.Не могли бы вы посоветовать что нибудь вместо немозола(от глистов отдельно пролечиться) чтобы во время лактакции.
3.какую диету нужно соблюдать?неужели ни грамма сахара,маленьких ведь не заставишь к примеру творог без сахара есть,чем можно кормить.?
Ответ:
Здравствуйте, Алена.
Спасибо за вопрос. Отвечаю по порядку на Ваши вопросы:
1.Лечения лямблиоза лучше проводить под контролем врача — паразитолога, в том числе детского.
2. Немозол — антигельминтное средство. Препараты этой группы противопоказаны при лактации.
3. Важную роль в подготовке и лечении лямблиоза играют диетические мероприятия, ограничение поступления простых углеводов в пищу. При этом из рациона исключается:
-
цельное коровье молоко или производят его замену соевыми, низколактозными смесями, гидролизатами коровьего молока;
-
резко ограничивают или исключают продукты, содержащие глютен, — это хлебобулочные и макаронные изделия, паштеты, колбасы, все крупы, кроме рисовой, гречневой и кукурузной; вместо хлеба можно использовать оладьи на кефире из рисовой, гречневой или кукурузной муки или использовать хлеб на основе отрубей.
Вместо мучных продуктов, привычных для детей, к которым относится печенье, сдоба, можно использовать в пищу рисовые шарики, хлебцы (рисовые и кукурузные), не имеющие в своем составе пшеничной муки.
Кроме того, исключить: сладости, пищу с консервантами и вкусовыми добавками. Рекомендуется кислое питье в виде клюквенных, брусничных морсов (при их переносимости), нежирный кефир, компоты из сухофруктов. Мясо отварное нежирное и овощные гарниры.
С уважением,
аллерголог — иммунолог, к.м.н., Каракина М. Л.
Назад
Подробно о непереносимости лактозы – Аллергии нет
Непереносимость лактозы плохо изучена в австралийском обществе. Есть много мифов и недоразумений об этом, особенно когда проблема касается детей.
Вопреки тому, что Ты можешь услышать:
- В грудном молоке не будет меньше лактозы, если мать перестанет принимать молочные продукты.
- Нет никакой связи между непереносимостью лактозы у взрослых членов семьи, в том числе у матери, и у детей.
 Это разные виды непереносимости лактозы.
Это разные виды непереносимости лактозы. - Ребёнку с симптомами непереносимости лактозы нельзя отменить грудное вскармливание и перевести на молочные смеси на основе сои или специальной лактозы.
- Непереносимость лактозы чётко отличается от пищевой непереносимости или аллергии на белок коровьего молока.
Лактоза является сахаром молока всех млекопитающих. Она вырабатывается в груди. Количество лактозы в грудном молоке не зависит от потребления матерью лактозы и практически не меняется. Молоко, которое ребёнок получает, когда он впервые начинает самостоятельно кормиться, содержит столько же лактозы, сколько и в материнском молоке в период завершения грудного вскармливания. Но последнее содержит больше жира.
Лактаза – это фермент, необходимый для переваривания лактозы. Непереносимость лактозы возникает, когда организм не производит этого фермента или не вырабатывает его в достаточном количестве, и поэтому он не способен переваривать лактозу. Если лактоза не переваривается и не расщепляется, она не может быть поглощена. Если это произойдёт, лактоза будет проходить в непереваренном виде в пищеварительном тракте, пока не достигнет толстой кишки. Именно здесь бактерии разлагают её, образуя кислоты и газы.
Если лактоза не переваривается и не расщепляется, она не может быть поглощена. Если это произойдёт, лактоза будет проходить в непереваренном виде в пищеварительном тракте, пока не достигнет толстой кишки. Именно здесь бактерии разлагают её, образуя кислоты и газы.
Симптомами непереносимости лактозы являются жидкий, иногда зелёный, пенистый стул и раздражительный ребёнок. Если ребёнок не переносит лактозу, можно ожидать, что медицинские тесты (водородный дыхательный тест и анализ содержания сахара в кале) будут положительными. Однако они также бывают положительны у большинства нормальных детей на грудном вскармливании в возрасте до 3-х месяцев. Поэтому применение этих анализов для диагностики непереносимости лактозы у маленьких детей остаётся под вопросом.
Непереносимость лактозы у детей
- Первичная (или истинная) непереносимость лактозы
Это крайне редкое генетическое заболевание несовместимое с жизнью при отсутствии медицинского вмешательства. Ребёнок с истинной непереносимостью лактозы плохо развивается с рождения (то есть даже не начнает набирать вес). У него появляются явные симптомы мальабсорбции и обезвоживания. Это состояние требует неотложной медицинской помощи, и ребёнку потребуется специальная диета сразу после рождения.
Ребёнок с истинной непереносимостью лактозы плохо развивается с рождения (то есть даже не начнает набирать вес). У него появляются явные симптомы мальабсорбции и обезвоживания. Это состояние требует неотложной медицинской помощи, и ребёнку потребуется специальная диета сразу после рождения.
- Вторичная непереносимость лактозы
Поскольку фермент лактаза вырабатывается энтероцитами в ворсинках микроскопических складок тонкой кишки, то любое повреждение слизистой оболочки тонкой кишки может вызвать вторичную непереносимость лактозы. Даже незначительные повреждения тонкой кишки могут разрушить эти ворсинки и снизить выработку этого фермента. Примеры:
- Гастроэнтериты.
- Пищевая непереносимость или аллергия. У детей, находящихся на грудном вскармливании, это может быть связано с пищевыми белками такими, как коровье молоко, пшеница, соя или яйца, а также с другими пищевыми веществами, которые попадают в грудное молоко из рациона матери, а также из пищи, которую принял ребёнок.
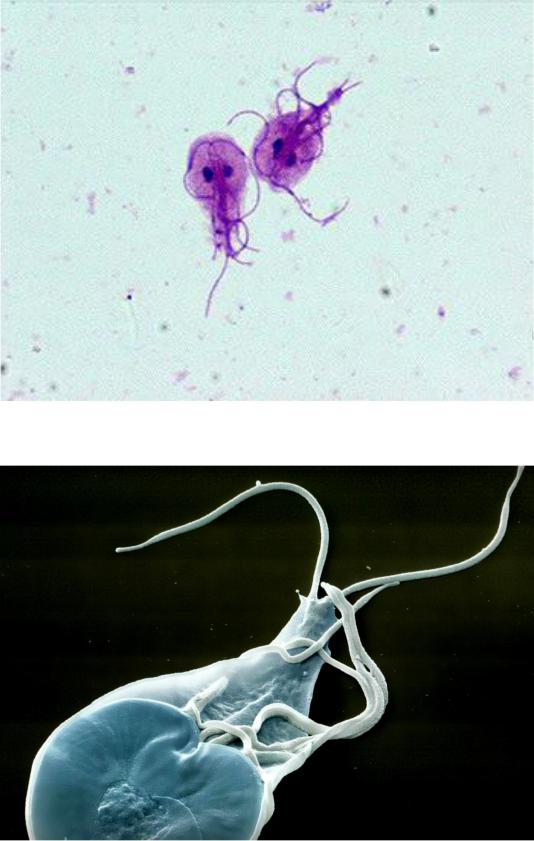
- Паразитарная инфекция, такая как лямблиоз или криптоспоридиоз.
- Целиакия (непереносимость глютена в пшенице и некоторых других зерновых продуктах).
- Хирургические операции на кишечнике.
Пищевая аллергия и пищевая непереносимость могут вызвать беспокойство ребёнка. Продукты, на которые у ребёнка имеется аллергия или непереносимость, могут проходить через грудное молоко матери. В некоторых случаях может помочь исключение из рациона матери продуктов, на которые у ребёнка аллергия или непереносимость, например, продукты из коровьего молока. Если Ты хочешь исключить из своего рациона определённые продукты потому, что подозреваешь их роль в появлении аллергии или пищевой непереносимости у ребёнка, проконсультируйся с диетологом.
Аллергию и пищевую непереносимость коровьего молока часто путают с непереносимостью лактозы, и многие люди думают, что это одно и то же. Путаница, вероятно, возникает из-за того, что белок коровьего молока и лактоза содержатся в одном и том же продукте, а именно в молоке. Поскольку аллергия или непереносимость пищевого белка могут вызывать вторичную непереносимость лактозы, то эти оба состояния могут присутствовать одновременно, что ещё больше усугубляет эту путаницу.
Поскольку аллергия или непереносимость пищевого белка могут вызывать вторичную непереносимость лактозы, то эти оба состояния могут присутствовать одновременно, что ещё больше усугубляет эту путаницу.
Вторичная непереносимость лактозы является временной, и она присутствует до сих пор пока не восстановится целостность тонкого кишечника. Если Твой врач поставит диагноз «непереносимость лактозы», продолжение грудного вскармливания не нанесёт вреда ребёнку, если он здоров и нормально растёт.
Когда у ребёнка наблюдаются симптомы непереносимости лактозы, иногда предлагается матери поочередно кормить ребёнка грудью и безлактозной смесью или даже полностью отлучить ребёнка от груди. Рекомендуется применять безлактозные смеси только в том случае, если ребёнок, который находится на искусственном вскармливании, не доедает и/или теряет вес. Грудное молоко остаётся лучшей пищей. Оно способствует быстрому восстановлению кишечника. Кроме того, чувствительность ребёнка к чужеродному белку (коровье или соевое) следует обследовать до введения какой-либо смеси, так как обычные смеси, в том числе безлактозные, могут усугубить эту проблему. Тебе следует обратиться за профессиональной консультацией по поводу необходимости гипоаллергенной формулы. Врач должен смотреть любого ребёнка с упорными симптомами и с плохим темпом развития.
Тебе следует обратиться за профессиональной консультацией по поводу необходимости гипоаллергенной формулы. Врач должен смотреть любого ребёнка с упорными симптомами и с плохим темпом развития.
Прежде чем отнять ребёнка от груди (даже частично) на короткое время, следует подумать о других вопросах, связанных с грудным вскармливанием. Вопросы, которые Ты должен себе задать:
- Как может повлиять на моего ребёнка альтернативные способы вскармливания?
- Сможет ли вскармливание ребёнка из бутылочки искусственными молочными продуктами позже привести к отказу от груди?
- Смогу ли я на продолжительное время сцеживать молоко, чтобы поддерживать запасы молока?
Средняя продолжительность восстановления кишечника у ребёнка с тяжёлым гастроэнтеритом составляет 4 недели, но может быть и до 8 недель для ребёнка младше 3-х месяцев. Для детей старшего возраста (около 18 месяцев) выздоровление может занимать всего одну неделю. Если врач назначает искусственное вскармливание ребёнка, то мать должна помнить, что её грудное молоко всё ещё является нормальным и пригодной пищей для ребёнка в перспективе.
Возможно Ты слышал о каплях, содержащих фермент лактазу для детей с симптомами непереносимости лактозы. Существует мало доказательств того, что они имеют большую ценность при использовании, хотя есть отдельные сообщения о том, что в некоторых случаях могут помочь только в больших дозах. Лактазные препараты в основном предназначены для добавления в сцеженное грудное молоко (или молочную смесь). Их оставляют на ночь для ферментизации. На практике они иногда полезны для детей. Хотя эти продукты могут помочь уменьшить симптомы, они не решают основную проблему, связанную с повреждением кишечника.
Непереносимость лактозы у взрослых
Количество фермента лактазы обычно меняется в течение жизни человека. Оно быстро растёт в первую неделю после рождения, начинает падать примерно с 3-5 лет, и затем начинает резко снижаться в период школьного возраста. Низкие уровни лактозы в молозиве соответствуют низкому уровню лактазы, присутствующего на первой неделе жизни.
В некоторых народах коровье молоко обычно употребляют взрослые, это в основном люди североевропейского происхождения. Приблизительно у 70% людей в мире, и в значительном числе австралийцев, уровень этого фермента в зрелом возрасте падает настолько низко, что они становятся непереносимыми к лактозе. Тенденция к непереносимости лактозы у взрослых определяется генетически. Люди с азиатским, африканским, австралийским аборигеном и латиноамериканским происхождением более склонны к непереносимости лактозы. Взрослые кавказцы с большей вероятностью смогут употреблять молоко потому что, они, как правило, продолжают вырабатывать фермент лактазу на протяжении всей жизни. Взрослые с низким уровнем лактазы обычно могут переносить лактозу так, как нормальные бактерии, живущие в кишечнике, обладают ограниченной способностью расщеплять его. Однако они могут иметь жидкий стул и накопление газов в кишечнике.
Дети любого происхождения могут переносить лактозу. На самом деле, в грудном молоке содержится очень высокая концентрация лактозы, если сравнить с коровьим молоком и молоком других млекопитающих. Считается, что это связано с быстрым ростом мозга ребёнка в младенчестве по сравнению с другими млекопитающими. Исключение лактозы из рациона любого ребёнка на продолжительный срок не следует с легкостью делать, а только под наблюдением врача.
Считается, что это связано с быстрым ростом мозга ребёнка в младенчестве по сравнению с другими млекопитающими. Исключение лактозы из рациона любого ребёнка на продолжительный срок не следует с легкостью делать, а только под наблюдением врача.
Перегрузка лактозой у детей
Признаки перегрузки лактозой могут напоминать непереносимость лактозы и часто ошибочно принимается за неё.
Перегрузка лактозой часто наблюдается у детей, потребляющих большое количество грудного молока, то есть, когда у матерей имеется его избыток. Это обычно происходит у детей в возрасте до 3 месяцев и может быть легко исправлено. Большой объём обезжиренного молока проходит так быстро, что не вся лактоза усваивается. Лактоза, попадающая в нижнюю часть кишечника, втягивает в кишечник дополнительную воду и ферментируется там бактериями, образуя кислый стул с большим количеством газов. Кислый стул часто вызывает опрелости кожи. Образование газов и жидкости вызывает боль в животе, и ребёнок «ведёт себя голодно» (хочет сосать, встревожен, поднимает ножки, кричит). Сосание – это лучший комфорт, который он знает. Оно также помогает перемещать газ по кишечнику и временно ослабляет боль. Поскольку ребёнок выглядит так, будто хочет сосать грудь, его мать снова кормит его.
Сосание – это лучший комфорт, который он знает. Оно также помогает перемещать газ по кишечнику и временно ослабляет боль. Поскольку ребёнок выглядит так, будто хочет сосать грудь, его мать снова кормит его.
У таких детей наблюдается быстрое нарастание массы тела, беспокойство, большой объём мочи (больше 10 раз в сутки), зелёный, пенистый стул и частый метеоризм.
Что делать маме?
Цель состоит в том, чтобы уменьшить скорость, с которой молоко проходит по пищеварительному тракту ребёнка путём вскармливания только одной грудью за каждое кормление. Нужно зафиксировать время вскармливания и установить 4-часовой перерыв. Затем надо использовать вторую грудь и т. д. Каждый раз, когда Твой ребёнок возвращается к уже использованной груди, он получает корм с меньшим объёмом и большим количеством жира, который помогает замедлить процесс пищеварения.
Вывод
Как объяснено выше, существует несколько типов непереносимости лактозы, но это не является поводом для прекращения грудного вскармливания. За исключением крайне редких случаев первичной непереносимости лактозы, существуют другие причины непереносимости лактозы у детей. Выяснение этой причины и её устранение является ключом к лечению ребёнка.
За исключением крайне редких случаев первичной непереносимости лактозы, существуют другие причины непереносимости лактозы у детей. Выяснение этой причины и её устранение является ключом к лечению ребёнка.
Перевод: доктор ХАЛИД
https://www.breastfeeding.asn.au/bf-info/lactose
Лямблиоз: симптомы и лечение
Все сегодня обеспокоены ситуацией с коронавирусом, и это понятно и правильно. Но не стоит забывать и о других инфекциях — кишечных. Расскажем об одной из них — лямблиозе. Каждый год в России регистрируется более 140 тысяч случаев этого заболевания. Начинают фиксировать весной, в апреле и мае, а пик болезни приходится на лето. Лямблиоз опасен в первую очередь тем, что имеет бессимптомное течение, а клинические признаки не являются специфичными. Часто это заболевание скрывается под маской дискинезии желчных путей, под хроническим энтеритом и иными патологиями органов ЖКТ.
КАК ЗАРАЖАЮТСЯ
Лямблиоз — это распространённое инфекционное заболевание организма человека, вызванное кишечным одноклеточным паразитом лямблией.
Основной способ заражения — фекально-оральный. Цисты с фекалиями больного человека или животного попадают во внешнюю среду, прежде всего в воду. Здоровый человек заражается, когда пьёт такую воду или ест загрязнённые цистами продукты. В летний период можно заразиться, покупавшись в водоёме, заражённом цистами лямблий.
Животные наряду с человеком подвержены лямблиозу. Эта паразитарная инвазия обнаруживается у кроликов, собак, кошек, грызунов, крупного рогатого скота и у иных млекопитающих. Человек чаще всего заражается от другого человека, однако не исключена возможность заражения от животных и от мух и тараканов, которые переносят цисты лямблий.
Когда циста лямблии с водой или пищей попадает в желудок человека, то её защитная оболочка растворяется. В результате из цисты “вылупляется” вегетативная форма паразита. Чтобы у человека развился лямблиоз, достаточно всего десяти цист.
НА ЧТО ВЛИЯЮТ ЛЯМБЛИИ
Эти паразиты выделяют в организме человека множество токсинов, что отравляет его изнутри. Активность лямблий и скорость их размножения напрямую зависит от состояния органов пищеварения человека. Резко снижается количество особей во время голодания и при употреблении больным достаточного количества белковой пищи. При поступлении в организм углеводной пищи, напротив, стимулируется рост и размножение паразитов.
Активность лямблий и скорость их размножения напрямую зависит от состояния органов пищеварения человека. Резко снижается количество особей во время голодания и при употреблении больным достаточного количества белковой пищи. При поступлении в организм углеводной пищи, напротив, стимулируется рост и размножение паразитов.
ФОРМЫ ЛЯМБЛИОЗА
Существует три формы заболевания.
1. Лямблионосительство, или бессимптомный лямблиоз, — признаков болезни нет, но при этом человек выделяет лямблии в окружающую среду. Бессимптомное течение заболевания наблюдается у 60 процентов пациентов.
2. Кишечная форма — признаки нарушения функций кишечника. Основные проявления: постоянные ноющие боли в области правого подреберья, болезненность в районе пупка, часто связанная с приёмами пищи; приступообразные боли с тошнотой и рвотой; чувство переполненного желудка, сопровождающееся вздутием живота; ухудшение аппетита; тошнота, отрыжка; стеаторея — большое количество жиров в кале; изжога; проблемы со стулом: диарея может сменяться запорами.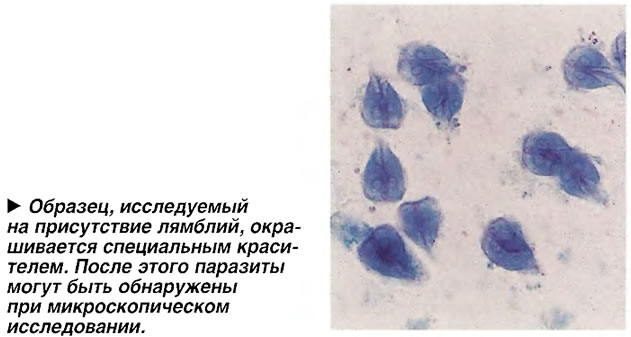
3. Гепатобилиарная форма — нарушение функций печени, желчевыводящих путей. Основные симптомы: боль в правом подреберье; ощущение горечи во рту; отрыжка с горьким привкусом; болезненность при дотрагивании до живота в области желчного пузыря; кожные проявления ограничиваются небольшой желтухой и зудом.
Характерны также общие симптомы: бледность кожи даже при нормальной концентрации гемоглобина в крови, слабость, раздражительность, синяки под глазами, заеды вокруг рта, аллергические проявления, повышенная утомляемость, головные боли.
Длительность острой фазы не дольше семи дней, после чего наступает либо выздоровление, либо течение болезни становится подострым или хроническим.
Признаки лямблиоза при хроническом течении:
— нарушение работы органов пищеварения. Стул больного становится неустойчивым, частые запоры сменяются такими же частыми диареями. Снижается аппетит, беспокоит вздутие и урчание в кишечнике
— часто беспокоят головные боли, появляется чрезмерная сонливость и раздражительность
— ухудшается цвет кожи, возможно развитие слабой желтухи
— кожные высыпания начинают беспокоить больного всё чаще, даже если раньше человек аллергией не страдал. Возможны проявления дерматита или крапивницы
Возможны проявления дерматита или крапивницы
— характерен фолликулярный кератоз с появлением на коже точечных припухлостей. Преимущественно страдает кожа плеч. Она покрывается шершавой коркой или белыми округлыми бляшками, склонными к повышенному шелушению
— страдает слизистая оболочка ротовой полости: часто возникает афтозный стоматит, в уголках рта появляются заеды, кайма губ воспаляется
Если лямблии паразитируют на протяжении длительного времени, то будут наблюдаться признаки угнетения иммунитета и симптомы интоксикации.
Ещё одним косвенным признаком лямблиоза у взрослых является непереносимость цельного коровьего молока.
Поставить диагноз лямблиоза невозможно без лабораторного подтверждения. Базовым методом диагностики является микроскопическое исследование кала. Его необходимо проводить не менее трёх раз. Желательно исследовать дуоденальное содержимое: цисты обнаруживают в просвете двенадциперстной кишки. Также проводится серологическая диагностика лямблиоза, когда специфические антитела обнаруживаются в крови через 2—4 недели после заражения.
КАК ЛЕЧАТ ЛЯМБЛИОЗ
Лечение лямблиоза должно проводиться только врачом — инфекционистом или гастроэнтерологом. Лечение довольно длительное. Для того чтобы уничтожить все лямблии, количество которых у взрослого человека может достигать нескольких миллионов, требуется несколько курсов противопаразитарных препаратов. Также необходимо восстановить микрофлору кишечника, провести детоксикацию. Лечение проводится поэтапно.
1. Подготовительный этап. Необходимо попытаться механическим путём убрать из кишечника максимальное количество лямблий, а также снять интоксикацию с организма.
Для этого больной должен полностью исключить из меню сладкое и углеводы, которые быстро усваиваются; употреблять продукты питания, богатые клетчаткой, и белковые продукты; отказаться от цельного молока, ограничить поступление жиров; перейти на дробное питание: 5-6 раз в день; пить больше жидкости, отдавая предпочтение кислым морсам и желчегонным отварам.
Дополнением диеты становится приём энтеросорбентов, желчегонных препаратов, антигистаминных средств и пищеварительных ферментов.
2. Применение антипаразитарных средств. Второй этап занимает 5—10 дней. Все лекарственные средства назначаются лечащим врачом. Одновременно с приёмом антипаразитарных препаратов больные принимают курс антигистаминных средств, ферментов и сорбентов.
3. Восстановление организма после лечения. Заключительный этап лечения направлен на повышение иммунитета пациента, нормализацию микрофлоры кишечника. Для этого ему назначают витаминно-минеральные комплексы, кишечные бактерии, ферментные препараты.
От лямблиоза нет вакцины, а иммунитет, который вырабатывается после перенесённой болезни, весьма нестойкий. Поэтому риск повторного заражения сохраняется на высоком уровне. Гораздо проще предотвратить инвазию, чем осуществлять последующее лечение лямблиоза.
Справка
Лямблии — одноклеточные микроскопические жгутиковые паразиты. Они существует в двух формах: в форме вегетаций — обычных клеток и цист. Вне человеческого тела вегетативные формы не способны к длительному существованию. Весь цикл жизнедеятельности паразита проходит в кишечнике человека или животного. Проникая в тонкий кишечник, лямблии прикрепляются к ворсинкам и начинают всасывать питательные вещества, образуя новые вегетации. Те вегетативные формы лямблий, которые не прикрепились к ворсинкам, опускаются в толстый кишечник, где становятся цистами, покрываясь защитной оболочкой. Из организма выходят вместе с каловыми массами больного. Цисты сохраняют свою жизнеспособность вне тела человека на протяжении 18 суток и более, если находятся в воде. А без достаточного увлажнения они погибают за несколько часов. При кипячении тоже гибнут. На продукты питания цисты попадают с водой: на фруктах и овощах цисты паразита способны сохранять жизнеспособность на протяжении шести часов, в молочных продуктах — до 12 суток.
Долгое время считалось, что лямблии способны паразитировать в желчевыводящих путях. Однако доказано, что желчь в высоких концентрациях для этих паразитов губительна.
Профилактика
Предупреждение инвазии лямблиями включает комплекс стандартных мер:
— не пить сырую (некипячёную или не очищенную иным способом) воду
— не глотать воду во время купания в открытых водоёмах
— тщательно мыть все подаваемые на стол фрукты и овощи, а также руки перед приёмом пищи
— не позволять домашним животным, кошкам, собакам, облизывать лицо и руки
Лямблии у детей — симптомы, диагностика, лечение
Лямблии – это простейшие жгутиковые паразиты, которые вызывают лямблиоз. Лямблии встречаются у детей разных возрастов. 10% людей на Земле заражены этими паразитами и даже не догадываются об этом. Лямблии имеют 2 степени развития в организме: цистную и вегетативную.
Лямблии встречаются у детей разных возрастов. 10% людей на Земле заражены этими паразитами и даже не догадываются об этом. Лямблии имеют 2 степени развития в организме: цистную и вегетативную.
Паразиты вегетативной стадии подвижны, имеют грушевидную форму и присасывательный диск. В течение 10-12 часов они удваиваются за счет деления. Цисты неподвижны, имеют овальную форму, и при этом очень живучие (не разрушаются в желудке). Чем страшен лямблиоз у детей, как вывести паразитов, расскажем далее.
Источники заражения детей цистами лямблий: как простейшие попадают в организм и чем они опасны?
Пути заражения лямблиями:
- Переносчиками этого заболевания являются домашние животные (коты, собаки, свинки), а также сам человек.
- Лямблиоз передается контактно-бытовым способом, а также через воду и пищу. Заражение произойдет, если в организм попадет 10 цист лямблий. Цисты могут находиться на игрушках, в песке, на немытых фруктах, овощах.
- Немытые руки после улицы – прямой проводник паразитов.
- Ребенок может заразиться через грудное молоко, если в организме матери есть лямблии.
Лямблиоз опасен для детей и взрослых, так как паразиты инфицируют кишечник и печень, вызывая острое воспаление. Приблизительно 1 млн. паразитов располагается в 1 см кишечника. Лямблиоз влечет за собой массу негативных последствий.
Последствия лямблиоза:
Симптомы заражения лямблиями детей до 1 года и старше
Пораженный лямблиями малыш достаточно тяжело переносит это заболевание. Как проявляется этот недуг у детей до года и ребят постарше? В таблице ниже приведены признаки лямблиоза у детей до года и ребят постарше.
Таблица №1. Как определить лямблии у детей?
| Возраст | Признаки лямблиоза у малышей |
| Дети до 1 года (груднички) | У грудничков болезнь обычно сопровождается повышением температуры, которую трудно сбить, поносом, дисбактериозом. Малыш становится капризный, верченый, может полностью отказаться от еды. |
| Дети старше 1 года | У деток постарше наблюдается лихорадка и понос, но еще сопровождается болезнь кожной сыпью в виде крапивницы. У ребенка может присутствовать отдышка. Иногда родители могут спутать этот симптом с астмой. Дети становятся малоподвижными, отчетливо видно темные или синие круги под глазами. В целом ребенок выглядит болезненным. Нередко ребенка тошнит, и он может рвать. Это уже запущенная форма лямблиоза. Обычно родители на первых стадиях ведут малыша на диагностику. У подростков лямблиоз может вызвать головокружение, перепады с давлением, укачивание в транспорте. |
Как у ребенка выявить лямблии: анализы и обследования
Таблица №2. Какие медицинские обследования помогут выявить лямблии у детей?
| Вид исследования на лямблии | Как проводиться? | Плюсы/минусы |
| Копрологическое исследование | Для этого исследования сдается кал ребенка, который проверяется на цист.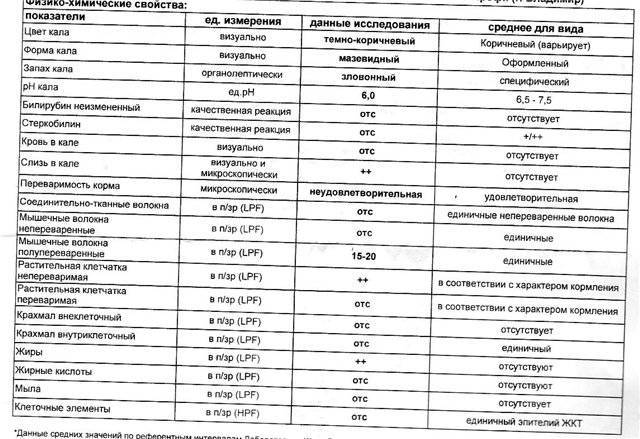 | Процедура безвредная, но минус в том, что цисты могут и не выходить вместе с калом. Недостоверный анализ, который не гарантирует 100% диагностику. |
| Серологическая диагностика | Это исследование проводится посредством сдачи анализа крови. | Процедура доступна даже для грудничков. Минус исследования заключается в том, что оно актуально только в первые 3 недели после заражения паразитами. После анализ крови может ничего не выдать. |
| Дуоденальное исследование | Это способ позволяет посредством зондирования исследовать желчь, в которой зачастую находятся лямблии. | Процедура эффективная со 100% результатом, но ее можно применять на детях от 10 лет. Малышам зондирование противопоказано. |
Как правильно сдать анализ кала на лямблии?
- Кал желательно собрать утром, имея при себе предназначенный для этого контейнер с консервантом.
 Для этого анализа нужно заранее взять сосуд в лаборатории.
Для этого анализа нужно заранее взять сосуд в лаборатории. - Если такого герметичного сосуда нет, тогда после забора кала нужно как можно быстрее привезти на обследование. Конечно, посуда должна быть чистая и стерильная.
- Если вы знаете особенность своего ребенка, что он не ходит утром в туалет, тогда можете собрать кал вечером и поставить его в холодильник, но достоверность исследования снизится в разы.
Точность одного исследования составляет 50-80%. Поэтому желательно сдать анализ кала несколько раз.
Как избавиться от лямблий на 100% — лечение лямблиоза у детей
Лямблиоз считается трудно излечимым недугом. Но, врачи нашли способ успешно справляться с этим заболеванием.
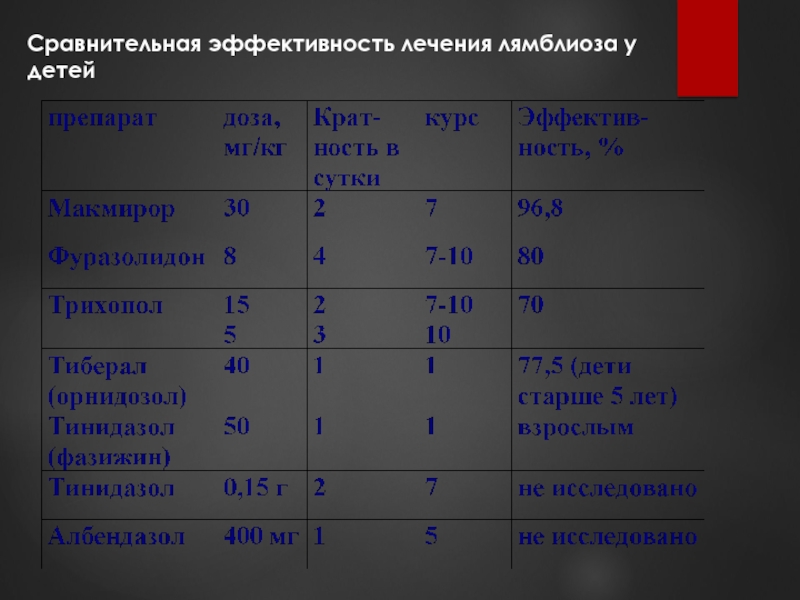
Эффективными препаратами для выведения лямблий из организма на сегодняшний день являются:
- Метронидазол.
- Фуразолидон.
- Албендазол.
- Макмирор.
- Тинидазол.
Важно!
Дозировка препаратов определяется только врачом. Она зависит от возраста, веса и типа заболевания. Самодеятельность в решении этого вопроса родителями должна быть исключена, так как представленные средства при передозировке могут нанести вред малышу.
Как меняется самочувствие больного во время лечения от лямблий?
- После начала лечения родители на 2-3 день могут увидеть значительные улучшения внешнего вида малыша.
- Если вдруг на 5-6 день лечения картина измениться в худшую сторону, бояться не следует, так как под воздействием лекарственных средств происходит окончательная гибель паразитов и их распад в кишечнике малыша. Токсичные вещества всасываются в кровь, чем и ухудшают состояние самого крохи. Для облегчения оздоровительного процесса доктор может приписать антигистаминные препараты, которые будут бороться с аллергической реакцией и токсинами. Лечение лямблиоза должно проходить в комплексе, иначе результат может затянуться на длительный срок.
- Обычно при комплексном подходе дети на 9-10 сутки чувствует облегчение и бодрость. Спадает сыпь на кожных покровах, улучшается взгляд, ребенку хочется кушать и даже играть. Но нужно понимать, что после окончания периода лечения стоит повторно обследовать малыша на остатки паразитов в организме.
Эффективные народные средства от лямблий для детей
Сразу стоит отметить, что вылечить ребенка только народными средствами от лямбиоза невозможно. Народный метод может выступать в роли дополнительного лечения, а не основного. Более того, лучше проконсультироваться с врачом о том или ином прочитанном вами способе народного лечения. Тем не менее, в народе все-таки существуют эффективные методы борьбы с этим недугом.
Топ-5 лучших народных рецептов от лямблиоза
Огуречный напиток
Свежие зеленые огурцы порезать на части и залить кипятком. Оставить отстаиваться пару часов. После сцедить жидкость и давать напиток малышу в течение дня не менее 0,5 л в сутки.
Настойка осины
Взять листья, можно почки и даже кору, залить кипятком и проварить 30 минут на среднем газу. После дать настояться и давать малышу 2 раза в день по полчашки. Курс длится 14 дней.
Коктейль из корней одуванчика
Мелко нарезанные корешки варят 15 минут на тихом огне, после процеживания дают раствор малышу 2 раза в день. Расчет напитка – 1 ч. л. на 10 кг веса ребенка. Кстати, такой отвар может хранится в холодильнике 2-е суток.
Бергамотовое масло
Одну капельку масла капают на сахар-рафинад и натощак дают его малышу. Курс лечения 7 дней максимум.
Настойка чистотела
Траву измельчают и заливают кипятком в термосе. Отвар настаивают два часа. После по 1 ст. л. дают малышу два раза в день. Курс длиться 5 дней. После 2-х дневного перерыва курс можно снова повторить, но не более 3 раз.
Врачи советуют после окончания периода лечения использовать лекарственные травы, которые способствуют налаживанию ЖКТ. После перенесения болезни ребенок должен обследоваться повторно, и может быть назначена противорецедивная терапия.
Мнения врачей о лечении лямблиоза
Лямблиоз достаточно труднопреодолимое заболевание, но вылечить этот недуг сегодня можно, хоть этот процесс длительный и может продолжаться от 10 до 17 дней. О методах исследования этого заболевания всегда ведутся споры, ведь диагностических процедур масса, а обнаружить лямблии по факту не так просто.
Доктор Комаровский о лямблиозе:
Самый эффективный метод диагностики лямблий и цист – это кал. Исследование крови не выявляет со 100% достоверностью наличие простейших в организме ребенка. Также нужно отметить, что современные безмедикаментозные методы борьбы с паразитами невозможны. Никакой ультразвук не убивает простейших в организме человека.
Доктор Комаровский о профилактике лямблиоза:
Никто не застрахован от того, что после лечения антибиотиками через 2 часа лямблии опять не попадут в организм и не начнут размножаться. Следовательно, нужно соблюдать культуру общения, гигиену и обезопасить себя и близких от внешних атак, а не жить в постоянной борьбе с цистами. Поэтому лямблиоз, в первую очередь – это уровень соблюдения гигиенических норм, а не эпидемия.
Также доктор Комаровский отвечает на самый животрепещущий вопрос людей о лямблиях:
А стоит ли лечить лямблиоз, когда имеет место носительства цистов? Одни говорят, что неразумно лечить человека при отсутствии жалоб (т.е. фактически лечить анализы), другие считают, что с лямблиями связано множество болезней, поэтому лечить надо обязательно. Кстати, одна из гипотез предполагает, что наличие лямблий способствует развитию и тяжелому течению аллергического дерматита (того самого, который наш народ называет диатезом), поэтому, ежели есть признаки дерматита, обследование на наличие лямблий (ну и лечение при обнаружении) – обязательны (это не я утверждаю, а авторы гипотезы). Лечение лямблиоза несложное, поскольку есть множество эффективных лекарств.
Кандидат медицинских наук Т. Ю. Бандурин:
Обследование на лямблиоз показано при следующих состояниях: наличие заболеваний пищеварительного тракта, тенденция к их хроническому течению с частыми, но умеренно выраженными обострениями; нейроциркуляторная дисфункция, особенно в сочетании с желудочно-кишечными нарушениями; стойкая эозинофилия крови; аллергические проявления.
Существует одно «естественное» препятствие, затрудняющее диагностику лямблиоза, — «феномен прерывистого цистовыделения». Ребенок, зараженный лямблиозом, выделяет цисты не каждый день — интервал в выделении цист составляет 8–14 дней, для лабораторного подтверждения диагноза следует проявить определенную настойчивость. Рекомендуется повторная многократная микроскопия фекалий.
Известно, что создание неблагоприятных условий способствует цистированию и выделению цист. Было отмечено, что при назначении желчегонных и противолямблиозных препаратов цисты обнаруживаются значительно чаще.
В качестве средств «провокации» используются различные препараты с учетом возраста ребенка, выраженности клинических проявлений и наличия сопутствующих показаний: настой кукурузных рыльцев, гомеопатический препарат холевит, макмирор, фуразолидон, метронидазол. При однократном обследовании цисты лямблий были обнаружены у 92,5% детей, у которых клинически был заподозрен лямблиоз. Таким образом, выполнение простых правил позволяет улучшить диагностику лямблиоза.
Как предупредить заражение лямблиями: профилактика лямблиоза у детей
Чем длительный период видеть, как малыш мучается и страдает от лямблиоза, лучше предупредить эту болезнь. Очевидно, что ограничить кроху от внешнего мира невозможно, как и защитить его от попадания цистов в организм на 100%. Но, предусмотрительность не помешает.
Снизить риск попадания лямблий в организм малыша поможет соблюдение следующих правил:
- Перед едой мыть овощи и фрукты.
- Грудничкам давать только кипяченую воду.
- Любое мясо, рыбу поддавать термической обработке.
- Но, самое главное – это приучать с маленького возраста малыша к гигиене. До трех лет вся ответственность ложится на плечи родителей, ведь они должны тщательно следить за малышом (что он есть, берет в рот, мыть руки после улицы, котов и собак). Но уже с трех лет вы можете активно внедрять в кроху понимание о чистоте, ведь вас он уже прекрасно понимает. Не позволяйте глотать воду в речке, водоемах и т.д. Учите его вести себя осторожно.
Лямблиоз сегодня лечится эффективно, но лучше не пичкать малыша противопаразитарными средствами, а прививать ему правила гигиены.
Поделитесь с друзьями:
Дисбактериоз у грудного ребенка или гадание по содержимому подгузников
Наталия Гербеда-Вильсон
Лидер Ла Лече Лиги
Август 2008г.
Очень часто родители грудничков в России сталкиваются с необходимостью сдать анализы на дисбактериоз, а потом и лечить его. Ситуация обычно развивается по следующему сценарию: у ребенка наблюдается жидкий по сравнению с детьми на искусственных заменителях грудного молока и взрослыми стул, или зеленоватый стул, или пенистый стул, и врач рекомендует сдать анализы на дисбактериоз. Назначенное лечение, как правило, включает в себя прием препаратов, содержащих полезные бактерии-пробиотики и дрожжи. В худшем случае, грешат на грудное молоко и рекомендуют перевести ребенка на иные виды вскармливания.
Что же такое дисбактериоз? Бывает ли он у грудных детей? Что делать, если ребенку ставят такой диагноз? Нужно ли волноваться? (Прим. автора. Тут я немного забегу вперед, чтобы успокоить всех мам. Дисбактериоз у грудных детей – неслыханная вещь!) Давайте шаг за шагом разберемся с вопросом, который поглощает умы всех мам во всех уголках планеты – содержимое подгузников ребенка и что это значит.
Содержимое кишечника и подгузников здорового грудничка
В период внутриутробного развития желудочно-кишечный тракт (ЖКТ) плода стерилен. Там нет никаких бактерий и других микроорганизмов. Когда ребенок рождается, ЖКТ заселяется, или колонизируется, бактериями, которые попадают ему в рот во время прохождения через родовые пути матери. Бактерии могут также попасть ребенку из материнского стула во время родов. Именно так создается нормальная и здоровая микрофлора кишечника. После рождения ЖКТ ребенка заселяется бактериями, которые находятся в окружающей среде, во рту и на коже матери. Это происходит во время кормления грудью, при поцелуях и прикосновениях к ребенку.
В грудном молоке содержится бифидус-фактор, вещество, которое способствует росту бифидобактерий. Неудивительно, что бифидобактерии составляют 95-99% флоры кишечника детей на грудном вскармливании. Бифидобактерии, которые иногда называют еще пробиотиками, являются частью здоровой флоры кишечника. Да-да, это те самые пробиотики, которые обычно прописывают как лечение от дисбактериоза. Эти добрые «рыцари» способствуют пищеварению, нормальной работе иммунной системы, а также не дают разростаться потенциально патогенным бактериям, которые приводят к заболеваниям. Бифидобактерии преобладают в кишечнике у грудного ребенка до тех пор, пока грудное молоко составляет бо́льшую часть питания ребенка. Помимо этого, в кишечнике грудничка в небольших количествах могут обитать стрептококки, бактероиды, клостридии, микрококки, энтерококки и кишечная палочка (E.Coli). Все эти микроорганизмы являются нормальной флорой пищеварительного тракта ребенка на грудном вскармливании.
Сразу же после рождения ребенок начинает сосать грудь и получает молозиво, которое обладает слабительным эффектом. Это помогает быстро избавиться от первого стула новорожденного – мекония. Меконий – черный, липкий, похожий на смолу стул, без запаха. При частых прикладываниях в первые сутки, меконий выходит за первые 48 часов.
По мере прихода молока, стул новорожденного меняется с темного на более светлый. Переходный стул обычно зеленоватого цвета и жиже, чем меконий. К пятому дню жизни ребенка его стул становится желтым, похожим на горчицу или густой гороховый суп, часто зернистым, с вкраплениями, похожими на кусочки творога. Цвет стула грудного ребенка может варьироваться от желтого до желто-зеленого или желто-коричневого. Изредка стул может быть зеленым или пенистым. У стула грудных детей нет запаха или же запах неотталкивающий и слабый сладковатый или творожистый запах (что невероятно помогает менять грязные подгузники!)
В первые три дня после рождения число опорожнений кишечника должно соответствовать возрасту ребенка – в первые сутки ребенок должен опорожнить кишечник один раз, на вторые сутки – два, на третьи – три. После прихода молока грудной ребенок опорожняет кишечник минимум 3-4 раза в сутки, и количество стула довольно значительное. Большинство грудных детей опорожняют кишечник намного чаще, нередко после каждого кормления. Даже неопытная мама без труда распознает радостный залп похода в туалет у грудничка – его невозможно не услышать и пропустить.
По мере взросления, в районе 6 недель от рождения или чуть раньше, многие грудные дети переходят на более редкий режим дефекации – от раза в несколько дней до раза в неделю или даже реже. При этом отсутствуют признаки запора (сухой, твердый стул) – стул ребенка попрежнему неоформленный, пюреобразный.
Введение любой другой пищи помимо грудного молока приведет к изменению консистенции, цвета и запаха стула у грудного ребенка. Если вы начали вводить прикорм, в стуле можно будет заметить кусочки пищи, которую вы даете ребенку.
Как мы видим, нормы дефекации и стула грудных детей значительно отличаются от нормы взрослых. То, что стало бы признаком беспокойства и поводом обратиться к врачу у взрослых, является нормой у грудничков. Для сравнения, нормы детей на грудном вскармливании значительно отличаются от показателей и детей на смешанном и искусственном вскармливании. Например, флора кишечника младенца на искусственном вскармливании уже в 2 недели почти не отличается от взрослого человека. У детей на искусственном вскрамливании более редкая дефекация, а также более оформленный стул с заметным типичным запахом.
Содержимое подгузника грудничка, на которое следует обратить внимание
Отклонения от нормы частоты и внешнего вида стула не всегда означает, что ребенок обязательно чем-то болен. Однако, стул ребенка может быть полезным признаком достаточности питания или симптомом аллергии. В таких случаях изменение способа кормления или устранения аллергена – все что требуется для решения проблемы.
Частый, водянистый, зеленый и/или пенистый стул может быть признаком недоедания. Нередко такой стул бывает в сочетании с медленным набором веса. Иногда такое состояние называют дисбаланс переднего и заднего молока. Ребенок высасывает много переднего молока с низким содержанием жира, которое проходит через пищеварительную систему слишком быстро и вызывает вышеуказанные симптомы. Обычно это легко разрешается изменением поведения во время кормлений, а именно увеличение продолжительности сосания у одной груди. Это позволяет малышу дососаться до жирного заднего молока, которое переваривается медленнее. Об этой проблеме можно узнать больше в статье Значение учета частоты стула новорожденного.
Если у малыша постоянно зеленый и водянистый стул, это может быть признаком аллергии. Помимо этого у ребенка может быть рвота, слизь или кровь в стуле, а также раздражительность, высыпания на коже. В этом случае особенно важно продолжать кормить грудью, т.к. отлучение от груди сопряжено с повышением риска аллергий. О том как справляться с аллергией у грудного ребенка можно узнать в статье Аллергии и семья грудного ребенка.
Если ваш малыш пачкает более 12-16 подгузников в сутки, и стул плохо пахнет и водянистый — это понос. Обычно понос у грудных детей быстро проходит сам по себе и без всяких осложнений. Причной поноса может стать инфекция, лечение антибиотиками, введение прикорма, чрезмерное потребление фруктовых соков. В случае острого поноса или поноса при приеме антибиотиков ребенка обязательно нужно как можно больше кормить грудью. В грудном молоке содержится все необходимое для предотвращения обезвоживания, а также антитела, которые помогают ребенку справится с инфекцией, и также факторы, которые позволяют восстановить нормальную флору кишечника. Американская ассоциация педиатрии рекомендует обязательно продолжать кормить ребенка грудью во время острого поноса. Исследования показывают, что прекращение кормления во время поноса увеличивает продолжительность и серьезность заболевания, а также вдвое увеличивает риск смертности. Если же причиной поноса стало введение прикорма или соки, возможно нужно отложить введение прикорма на некоторое время. Подробнее о введении прикорма написано в статье Когда вводить прикорм?
Что такое дисбактериоз
Дисбактериоз (от гр. dys- «нарушение, расстройство», bacterio- «бактерии» и –sis «состояние») или дисбиоз – нарушение качественного или количественного баланса микроорганизмов в организме, в данном случае, в кишечнике. Это значит, что изменилась пропорция бактерий в кишечнике или там появились необычные для нормальной флоры микроорганизмы. Дисбактериоз часто связывают с кишечными инфекциями и лечением антибиотиками.
Диагностирование дисбактериоза проводится по симптомам или же анализом кала на дисбактериоз. Обозначить симптомы дисбактериоза трудно, так как это состояние не является заболеванием согласно «Международной статистической классификации болезней и проблем, связанных со здоровьем» Десятого пересмотра (МКБ-10) — документу Всемирной организации здравоохранения, который является общепринятой международной диагностической классификацией в здравоохранении.
Обычно, показанием к анализу на дисбактериоз является непроходящий в течение двух или трех суток понос. У взрослых людей и детей на искусственном вскармливании понос определяется как частый и жидкий стул. Как уже было сказано выше, для грудных детей частый, неоформленный жидкий стул является нормой, поэтому не может являться показанием для анализов. Среди других симптомов, которые служат поводом для лабораторных исследований на дисбактериоз могут быть зеленоватый стул, стул со слизью, запор (редкий стул у грудных детей часто ошибочно принимают за запор), пенистый стул, частички непереваренной пищи. Все эти симптомы не у грудных детей действительно сопровождают поносы, которые часто вызваны патогенными бактериями и требуют лечения антибиотиками. У грудных детей каждый из перечисленных признаков может являться разновидностью нормы.
Насколько показательны анализы на дисбактериоз у здоровых грудных детей?
Изучение состава кишечной флоры у здорового грудного ребенка, то есть ребенка без видимых симптомов заболевания, в данном случае поноса, представляет интерес для ученых, но не для родителей или практикующих врачей. Многочисленные исследования показали, что грудное молоко защищает детей от заболеваний, даже если кишечник колонизирован патогенными микроорганизмами. Например, в грудном молоке содержатся антитела и факторы против кишечной палочки, холерного вибриона, сальмонеллы, шигеллы, ротавируса и лямблии. Это значит, что в стуле может высеваться патологический микроорганизм, но ребенок при этом не проявляет никаких симптомов заболевания.
Когда нужно обратится к врачу?
В крайне редких случаях грудному ребенку может понадобиться медицинская помощь.
Обратитесь к врачу, если у ребенка в первые недели жизни наблюдается
- понос (более 12 дефекаций в сутки, водянистый стул)
- рвота
- темпаратура
- летаргия
- низкий набор веса
- потеря в весе
Обратитесь к врачу с грудным ребенком любого возраста, если у ребенка появились признаки обезвоживания
- слабость
- сонливость или летаргия
- слабый плач
- кожа не разглаживается быстро, если ее ущипнуть
- отсутствие слез
- сухой рот, во рту мало или отсуствует слюна
- менее двух мокрых подгузников в сутки
- моча темная, с сильным запахом
- запавший родничок
- температура
Что нужно знать и помнить кормящей маме?
Кормление грудью является самой настоящей страховкой здоровья желудочно-кишечного тракта ребенка в течение первых лет жизни. Грудное молоко способствует росту бифидобактерий, которые препятствуют колонизации кишечника болезнетворными бактериями, а также содержит антитела и факторы, которые защищают ребенка от болезни, даже если патогенным бактериям удалось прижиться в кишечнике. Кормление грудью помогает восстановить баланс микрофлоры кишечника ребенка после лечения антибиотиками. Попросту говоря, грудным детям дисбактериоз не страшен.
Библиография
Lawrence, R. A. and Lawrence R.M. Breastfeeding: A Guide for the Medical Profession, 6th ed. St. Louis: Mosby, 2005.
Mohrbacher N., Stock J. Breastfeeding Answer Book, Third Revised Edition, January 2003, La Leche League International.
Mosby’s Dictionary of Medicine, Nursing & Health Professions. 7th ed. St. Louis: Mosby, 2005.
Riordan, J. and Auerbach, K. Breastfeeding and Human Lactation, 3rd ed. Boston: Jones and Barlett, 2005.
World Health Organization. International Statistical Classification of Diseases and Related Health Problems.10th revision, version 2007. Доступ 6 августа 2008, http://www.who.int/classifications/icd/en/
Смагин А.Ю. «Пробиотики и пребиотики у новорожденных и детей грудного возраста (обзор литературы)». Журнал интенсивная терапия 2007. Доступ 6 августа 2008, http://www.icj.ru/2007-02-03.html
Лямблиоз: проблемы при беременности и кормлении грудью
Примечание : Веб-сайт Pregistry содержит отчеты экспертов по более чем 2000 лекарствам, 300 заболеваниям и 150 распространенным воздействиям во время беременности и кормления грудью. По теме Лямблиоз при беременности перейдите сюда. Эти экспертные отчеты предоставляются бесплатно, их можно сохранять и передавать.
Лямблиоз — паразитарная инфекция желудочно-кишечного тракта, вызываемая простейшими паразитами.Это организм, состоящий из одной клетки, называемой Giardia , обычно это особый вид Giardia , называемый Giardia lamblia , который также называется Giardia duodenalis или Giardia Кишечник . Лямблиоз развивается примерно у 2% взрослых в развитых странах. Это наиболее распространенное паразитарное заболевание в Соединенных Штатах, поражающее людей. В развивающихся странах почти 33 процента людей в какой-то момент жизни страдают лямблиозом.Факторы риска, которые подвергают риску беременных женщин: путешествия в страну, где лямблиоз распространен, уход за детьми, контакт с кем-то, кто болел лямблиозом, контакт с инфицированными животными, такими как собака или кошка (даже если они обычно заражены другими видами Giardia , чем обычно заражают людей), и питьевая вода, зараженная паразитами Giardia или яйцами Giardia . Часто зараженная вода — это неочищенная вода из озер или рек, которую люди пьют во время походов или кемпинга.
Если у вас разовьется лямблиоз, симптомы будут включать диарею, характеризующуюся жидким, неприятным запахом и жирным стулом. Другие симптомы, которые могут возникнуть, включают метеоризм (газы), спазмы в животе, тошноту, вздутие живота, усталость, анорексию (отсутствие аппетита) и потерю веса. Все это также может привести к обезвоживанию. Инфекция лямблиоза может быть острой и проявляться симптомами, которые проявляются через 7–14 дней после заражения и продолжаются примерно от 7 до 14 дней. С другой стороны, у вас может быть хронический лямблиоз; это означает, что заболевание сохраняется через несколько месяцев после заражения, а симптомы появляются и исчезают.
Что касается диагностики лямблиозной инфекции, это предполагает, что клинический патолог с помощью микроскопа исследует образец вашего стула после того, как ваш врач назначит «O и P» (яйцеклетки и паразиты) для образца стула, который вам необходимо предоставить. Если патологоанатом или другой исследователь обнаружит зрелые клетки паразитов и яйца Giardia , этого достаточно для постановки диагноза. В некоторых случаях также проводятся тесты с использованием антител для выявления Giardia . Когда анализы повторных проб стула оказываются отрицательными, но все еще есть сильное подозрение, что у вас лямблиоз, следующим шагом будет взятие пробы из двенадцатиперстной кишки, первой части тонкой кишки, потому что именно там концентрируются паразиты. будет самым высоким у инфицированного человека.Образец можно получить с помощью неинвазивного метода, называемого «сильным тестом», при котором вы проглатываете желатиновую капсулу, прикрепленную к веревке. По мере растворения желатина конец нити в виде капсулы продвигается через желудок в двенадцатиперстную кишку. Затем струна вытягивается через рот вместе с содержимым двенадцатиперстной кишки, которое прикрепилось к струне. Это содержимое может быть исследовано на наличие клеток и яиц Giardia, . Также существует более сложная процедура, называемая эндоскопией, которая может быть выполнена для получения лучших образцов двенадцатиперстной кишки, если более простые тесты окажутся отрицательными.
Хотя эта паразитарная инфекция не наносит прямого вреда ребенку, если вы действительно станете обезвоженным, это может уменьшить объем околоплодных вод, замедлить рост плода и, возможно, спровоцировать преждевременные роды и роды. К счастью, есть лекарства для лечения лямблиоза. Основным лекарством является метронидазол, который при необходимости можно принимать во втором и третьем триместрах. Однако следует избегать приема метронидазола в течение первого триместра, поскольку он может нанести вред эмбриону и раннему плоду.С другой стороны, лекарство под названием паромомицин одновременно эффективно против Giardia и безопасно на протяжении всей беременности, поскольку не всасывается через желудочно-кишечный тракт. Поскольку он не попадает в кровь матери, он также не попадает в грудное молоко, поэтому он также безопасен, если вы кормите грудью. Сообщалось о штаммах Giardia , устойчивых к метронидазолу и паромомицину. Препараты хинакрин и фуразолидон эффективны против таких штаммов, но хинакрин и фуразолидон недоступны в США.Если вы беременны с легкими симптомами лямблиоза, вам могут не понадобиться никакие лекарства. Помимо лекарств, очень важным компонентом лечения является регулирование жидкости и электролитов (с помощью жидкости и соответствующих химических веществ внутривенно). Вам необходимо пить жидкость, а в некоторых случаях может потребоваться внутривенное введение жидкости.
Доктор Дэвид Вармфлэш — научный коммуникатор и врач с исследовательским опытом в области астробиологии и космической медицины. Он прошел исследовательскую стажировку в Космическом центре НАСА имени Джонсона, Университете Пенсильвании и Университете Брандейса.С 2002 года он сотрудничал с Планетарным обществом в проведении экспериментов, помогающих нам понять влияние излучения дальнего космоса на формы жизни, а с 2011 года почти полный рабочий день работал в области медицинских работ и научной журналистики. Его основная сфера деятельности — появление новых биотехнологий и их влияние на биомедицину, общественное здоровье и общество.
(PDF) Влияние грудного вскармливания на инфекции Giardia lamblia в Бильбейсе, Египет
260
МАХМУД И ДРУГИЕ
3.Заки А.М., DuPont HL, эль-Алами М.А., Арафат Р.Р., Амин К.,
Авад М.М., Бассиуни Л., Имам И.З., эль-Малих Г.С., эль-Марсафи
А, Мохилдин М.С., Нагиб Т., Ракха М.А., Сидарос М., Вазеф N,
Wright CE, Wyatt RG, 1986. Выявление энтеропатогенов
при острой диарее у семейной когорты населения в сельских районах Египта.
Am J Trop Med Hyg 35: 1013–1022.
4. Линдо Дж. Ф., Леви В. А., Баум М. К., Палмер С. Дж., 1998. Эпидемиология
лямблиоза и криптоспоридиоза на Ямайке.Am J Trop Med
Hyg 59: 717–721.
5. Ish-Horowitz M, Korman SH, Shapiro M, Har-Even V, Tamir I,
Strauss N, Deckelbaum RJ, 1989. Бессимптомный лямблиоз у
детей. Pediatr Infect Dis J 8: 773–779.
6. Фрейзер Д., Даган Р., Нагган Л., Грин В., Эль-Он Дж., Абу-Рбиа
Y, Декельбаум Р.Дж., 1997. Естественная история инфекций Giardia lamblia
и Cryptosporidium в когорте израильских бедуинов
младенцев: исследование населения с переходной экономикой.Am J Trop Med
Hyg 57: 544–549.
7. Махмуд М.А., Чаппелл С., Хоссейн М.М., Хабиб М., DuPont HL,
1995. Факторы риска развития первой симптоматической инфекции среди младенцев из когорты новорожденных в сельских районах Египта. Am J Trop
Med Hyg 53: 84–88.
8. Гранот Э., Спира Д.Т., Фрейзер Д., Деккельбаум Р.Дж., 1998. Immu-
Нологический ответ на инфекцию Giardia lamblia у детей:
влияние различных клинических условий. J Trop Pediatr 44: 241–
246.
9. Раух А.М., Ван Р., Бартлетт А.В., Пикеринг Л.К., 1990. Longitu-
Динальное исследование инфекции Giardia lamblia в центре дневного ухода
населения. Pediatr Infect Dis J 9: 186–189.
10. Фичем Р.Г., Коблинский М.А., 1984. Вмешательства по борьбе с
диарейных заболеваний у детей раннего возраста: популяризация грудного вскармливания. Bull World Health Organ 62: 271–291.
11. Салливан П.С., Дюпон Х.Л., Арафат Р.Р., Торнтон С.А., Селвин Б.Дж.,
Эль-Алами М.А., Заки А.М., 1988.Болезнь и резервуары, связанные с инфекцией Giardia lamblia
в сельских районах Египта: случай
против лечения в развивающихся странах с высокой эндемичностью
. Am J Epidemiol 127: 1272–1281.
12. Хосайн М.М., Радван М.М., Арафа С.А., Хабиб М., Дюпон Х.Л.,
1992. Практика кормления грудных младенцев в предлактеальном периоде в сельских районах Египта. J Trop
Pediatr 38: 317–322.
13. Ungar BL, Yolken RH, Nash TE, Quinn TC, 1984. Иммуноферментный анализ, связанный с ферментом
, для обнаружения Giardia lam-
blia в образцах фекалий.J Infect Dis 149: 94–97.
14. Morrow Al, Reves RR, West MS, Guerrero ML, 1992. Защита от заражения Giardia lamblia грудным вскармливанием
в когорте мексиканских младенцев. J Pediatr 121: 363–370.
15. Кокс Д. Р., Оукс Д., 1984. Анализ данных о выживаемости. Нью-Йорк:
Чепмен и Холл.
16. Пикеринг Л.К., Woodward WE, DuPont HL, Sullivan P, 1984.
Возникновение Giardia lamblia у детей в детских садах.
J Pediatr 104: 522–526.
17. Гласс Р.И., Столл Б.Дж., 1989. Защитное действие грудного молока
против диареи. Acta Paediatr Scand Suppl 351: 131–136.
18. Ислам А., Столл Дж. Б., Люнгстрем И., Бисвас Дж., Назрул Х, Хульдт Г.,
1983. Инфекции лямблий в когорте Бангладеш
матери и ребенка наблюдались в течение одного года. J Pediatr 103: 996–
100.
19. Hernell O, Ward H, Blackberg L, Pereira ME, 1986. Убийство
Giardia lamblia липазами грудного молока: эффект, опосредованный липолизом липидов молока
.J Infect Dis 153: 715–720.
20. Гиллин Ф.Д., Райнер Д.С., Ван С.С., 1983. Грудное молоко убивает par-
простейших асит кишечного тракта. Наука 221: 1290–1292.
21. Эндрю Дж. С., Hewlett EL, 1981. Защита от заражения
Giardia muris с помощью молока, содержащего антитела к лямблии. J Infect
Dis 143: 242–246.
22. Миотти П.Г., Гилман Р.Х., Сантошам М., Райдер Р.В., Йолкен Р.Х.,
1986. Возрастная зависимость серопозитивности антител к лямблиям
в четырех различных популяциях.J Clin Microbiol 24: 972–
975.
23. Nayak N, Ganguly NK, Walia BN, Wahi V, Kanwar SS, Ma-
hajan RC, 1987. Специфический секреторный IgA в молоке Giardia
lamblia –Инфицированные и неинфицированные женщины. J Infect Dis 155:
724–727.
24. Миотти П.Г., Гилман Р.Х., Пикеринг Л.К., Руис-Паласиос Дж., Парк
HS, Йолкен Р.Х., 1985. Распространенность сывороточных и молочных антител —
лет в лямблии в различных популяциях кормящих
женщин.Журнал Infect Dis 152: 1025–1031.
25. Ruiz-Palacios GM, Calva JJ, Pickering LK, Lopez-Vidal Y, Vol-
kow P, Pezzarossi H, West MS, 1990. Защита грудных детей
от диареи Campylobacter с помощью антител человека
молоко. J Pediatr 116: 707–713.
26. Гласс Р.И., Свеннерхольм А., Столл Б.Дж., Хан М.Р., Хоссейн К.М.Б.,
Хук I, Холмгрен Дж., 1983. Защита от холеры в груди —
детей, вскармливаемых грудью, с помощью антител в молоке. N Engl J Med 308: 1389–
1392.
27. Клеменс Д.Д., Стэнтон Б., Столл Б., Шайд Н.С., Бану Х., Чоудхури
AM, 1986. Грудное вскармливание как фактор тяжести эллеза Шиг-
: доказательства защиты в течение первых трех лет
жизни в бангладешских детях. Am J Epidemiol 123: 710–720.
Как предотвратить лямблиоз?
Автор
Хишам Назер, MBBCh, FRCP, DTM & H Профессор педиатрии, консультант по детской гастроэнтерологии, гепатологии и клиническому питанию, Медицинский факультет Университета Иордании, Иордания
Хишам Назер, MBBCh, FRCP, DTM & H является членом следующих медицинских общества: Американская ассоциация врачей-лидеров, Королевский колледж педиатрии и здоровья детей, Королевский колледж хирургов в Ирландии, Королевское общество тропической медицины и гигиены, Королевский колледж врачей и хирургов Соединенного Королевства
Раскрытие информации: не раскрывать.
Главный редактор
Берт Кагир, доктор медицины, FACS Клинический профессор хирургии Медицинской школы Содружества Гейзингер; Директор программы ординатуры по общей хирургии, больница Гатри Роберт Пакер; Лечащий хирург, Госпиталь Гатри Роберт Пакер и Госпиталь Корнинг
Берт Кагир, доктор медицины, FACS является членом следующих медицинских обществ: Американского колледжа хирургов, Ассоциации директоров программ по хирургии, Общества хирургии пищеварительного тракта
Раскрытие: Нечего раскрывать.
Благодарности
Мануп С. Бутани, доктор медицины Профессор, содиректор Центра эндоскопических исследований, обучения и инноваций (CERTAIN), директор Центра эндоскопического ультразвука, Департамент медицины, Отделение гастроэнтерологии, Медицинское отделение Техасского университета; Директор отдела эндоскопических исследований и разработок, Онкологический центр Андерсона Техасского университета
Мануп С. Бутани, доктор медицинских наук, является членом следующих медицинских обществ: Американской ассоциации развития науки, Американского колледжа гастроэнтерологии, Американского колледжа врачей, Американской гастроэнтерологической ассоциации, Американского института ультразвука в медицине и Американского общества гастроэнтерологической эндоскопии.
Раскрытие: Ничего не нужно раскрывать.
Брукс Д. Кэш, доктор медицины, FACP Директор клинических исследований, доцент медицины, отделение гастроэнтерологии, Национальный военно-морской медицинский центр
Брукс Д. Кэш, доктор медицины, FACP является членом следующих медицинских обществ: Alpha Omega Alpha, Американского колледжа гастроэнтерологии, Американской гастроэнтерологической ассоциации и Американского общества гастроэнтерологической эндоскопии
Раскрытие: Ничего не нужно раскрывать.
Стивен К. Дронен, доктор медицины, FAAEM Председатель, отделение неотложной медицины, Медицинский центр ЛеКонт
Стивен Дронен, доктор медицины, FAAEM является членом следующих медицинских обществ: Американской академии неотложной медицины и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Мишель Эрвин, доктор медицины , председатель отделения неотложной медицины, больница Ховардского университета
Мишель Эрвин, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации, Национальной медицинской ассоциации и Общества академической неотложной медицины
Раскрытие: Ничего не нужно раскрывать.
Гленн Феннелли, доктор медицины, магистр здравоохранения Директор отдела инфекционных заболеваний, отделение педиатрии им. Льюиса М. Фрада, Медицинский центр Якоби; Клинический доцент педиатрии, Медицинский колледж Альберта Эйнштейна
Гленн Феннелли, доктор медицины, магистр здравоохранения является членом следующих медицинских обществ: Общество педиатрических инфекционных болезней
Раскрытие: Ничего не нужно раскрывать.
Мурат Хёкелек, MD, PhD Технический консультант лаборатории паразитологии, профессор кафедры клинической микробиологии, Медицинская школа Университета Ондокуз Майис, Турция
Мурат Хёкелек, доктор медицины, доктор философии является членом следующих медицинских обществ: Турецкое общество паразитологов
Раскрытие: Ничего не нужно раскрывать.
Марк Х. Джонстон, доктор медицины Адъюнкт-профессор медицины Университета медико-санитарных служб и служб униформы; Консультант, Lancaster Gastroenterology Inc
Марк Х. Джонстон, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа гастроэнтерологии, Американского колледжа врачей, Американской гастроэнтерологической ассоциации и Христианского медицинского и стоматологического общества
Раскрытие: Ничего не нужно раскрывать.
Сандип Мукерджи, MB, BCh, MPH, FRCPC Доцент, Отделение внутренней медицины, Отделение гастроэнтерологии и гепатологии, Медицинский центр Университета Небраски; Консультанты отделения гастроэнтерологии и гепатологии Медицинского центра по делам ветеранов
Сандип Мукерджи, MB, BCh, MPH, FRCPC является членом следующих медицинских обществ: Королевский колледж врачей и хирургов Канады
Раскрытие информации: Merck Honoraria Выступление и обучение; Членство в Правлении гонорара Ikaria Pharmaceuticals
Майкл Д. Ниссен, MBBS, FRACP, FRCPA Доцент кафедры биомолекулярных, биомедицинских наук и здравоохранения, Университет Гриффита; Директор инфекционных болезней и заведующий отделением детской инфекционной лаборатории Квинсленда, Центр вирусных исследований сэра Альберта Сакжевски, Королевская детская больница
Майкл Д. Ниссен, MBBS, FRACP, FRCPA является членом следующих медицинских обществ: Американской академии педиатрии, Американского общества микробиологии, Общества педиатрических инфекционных болезней, Королевского австралазийского колледжа врачей и Королевского колледжа патологов Австралии
Раскрытие: Ничего не нужно раскрывать.
Андре Пеннардт, доктор медицины, FACEP, FAAEM, FAWM , доцент кафедры неотложной медицинской помощи, Медицинский колледж Джорджии; Доцент кафедры военной и неотложной медицины Университета медицинских наук военнослужащих; Консультанты, отделения неотложной медицины, авиационной медицины и подводной медицины, Медицинский центр армии Вомак
Андре Пеннардт, доктор медицины, FACEP, FAAEM, FAWM является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Ассоциации военных хирургов США, Международного общества горной медицины, Национальной ассоциации скорой медицинской помощи. Врачи, Медицинская ассоциация специальных операций и Медицинское общество дикой природы
Раскрытие: Ничего не нужно раскрывать.
Барри Дж. Шеридан, DO Главный воин в переходных службах, Армейский медицинский центр Брук
Barry J Sheridan, DO является членом следующих медицинских обществ: American Academy of Emergency Medicine
.
Раскрытие: Ничего не нужно раскрывать.
Russell W. Steele, MD Руководитель отделения детских инфекционных болезней Детского оздоровительного центра Ochsner; Клинический профессор кафедры педиатрии медицинского факультета Тулейнского университета
Рассел Стил, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии педиатрии, Американской ассоциации иммунологов, Американского педиатрического общества, Американского общества микробиологов, Американского общества инфекционных заболеваний, Медицинского общества штата Луизиана, Общества педиатрических инфекционных болезней, Общество педиатрических исследований и Южная медицинская ассоциация
Раскрытие: Ничего не нужно раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Влияние антител в материнском молоке на антигенную изменчивость Giardia lamblia в модели заражения потомства мышей
РЕФЕРАТ
В настоящем исследовании новорожденные мыши ZU.ICR и их матери были инфицированы трофозоитами Giardia lamblia . GS / M-83-H7, экспрессирующий вариантный поверхностный белок (VSP) H7.Эксперименты по заражению включали подробный анализ специфичности антител к иммуноглобулину A (IgA) против Giardia в материнском молоке и определение эффектов молочных антител как на рост паразита во время культивирования in vitro, так и на колонизацию паразита. паразит в кишечнике грудного потомства. Эти исследования показали, что временно возникающие молочные IgA-антитела против вариантно-специфической 314-аминокислотной N-концевой области VSP H7 проявляют сильный паразитицидный эффект на трофозоиты типа VSP H7 как in vitro, так и in vivo.Эти данные показали, что паразитарные эффекты местных антител IgA против N-концевой части VSP H7 приводят к появлению новых типов вариантов в популяции кишечных паразитов мышей-сосунков. Селективное влияние таких антител способствует антигенной изменчивости in vivo клона GS / M-83-H7 G. lamblia и модулирует раннее течение паразитарной инфекции у этих животных.
Простейшие паразиты Giardia lamblia — кишечные паразиты человека и различных животных.Проявления болезни варьируются от бессимптомного носительства до тяжелой диареи и мальабсорбции. Считается, что на развитие заболевания существенное влияние оказывает иммунная система инфицированного хозяина, но соответствующие иммунологические механизмы борьбы с паразитарной инфекцией до сих пор полностью не изучены (3, 4). В последнее десятилетие иммунобиология G. lamblia была особенно изучена с точки зрения способности паразита претерпевать антигенные изменения. В г.lamblia , антигенная изменчивость опосредуется уникальным семейством богатых цистеином белков, вариантных поверхностных белков (VSP), и было продемонстрировано, что они связаны с диверсификацией популяции кишечных паразитов в сложную смесь различных типов вариантных антигенов (10). . Исследования in vitro показали, что антигенная изменчивость может происходить спонтанно (11) и что иммунологические (11) или физиологические (12) факторы могут способствовать или противостоять различным типам VSP. Как продемонстрировано в экспериментальных инфекциях иммунокомпетентных взрослых мышей с дефицитом В-клеток (и антител), антигенная вариация in vivo G.lamblia стимулируется кишечным ответом антител против VSP иммуноглобулина A (IgA) (14).
В одном из наших недавних исследований новорожденных мышей инфицировали трофозоитами клона G. lamblia GS / M-83-H7 (человеческий изолят), а затем исследовали их сывороточный ответ антител, направленный против основного поверхностного антигена (VSP). H7) паразита (9). Рекомбинантные полипептиды, представляющие перекрывающиеся сегменты VSP H7 и нативных белков Giardia , использовали в качестве антигенных реагентов для исследования антигенной субструктуры VSP H7 и степени антигенной изменчивости in vivo.Данные указывают на то, что VSP H7 состоит из двух антигенно различных частей: (i) уникальной, специфичной к варианту 314-аминокислотной (аа) N-концевой области, которая вызывает слабый ответ антител, который предпочтительно выявляется на ранней фазе инфекции, и (ii) С-концевую область из 171 аминокислот, содержащую относительно консервативные эпитопы, которые вызывают ответ антител высокого уровня во время более поздней и регрессивной фазы инфекции. Дальнейшие исследования показали, что антигенная изменчивость популяции кишечных паразитов была связана с диверсификацией по крайней мере от шести до девяти новых типов вариантных антигенов.Ни один из этих белков не имеет общих антигенных эпитопов с N-концевой частью, но некоторые из них перекрестно реагируют с антителами, специфичными к C-концевой части VSP H7. Эти результаты показали следующее. (i) Из-за своей высокой вариабельности N-концевая часть VSP стимулирует только временный и, следовательно, низкий уровень антител. (ii) Полуконсервативные эпитопы С-концевой части стимулируют стойкий и, следовательно, высокий уровень антител во время паразитарной инфекции.Сывороточные антитела мышей на ранней стадии инфекции, направленные против вариабельных эпитопов N-концевой области, вызывали отслоение и агрегацию трофозоитов и проявляли независимый от комплемента цитотоксический эффект по отношению к паразиту (15). Напротив, сывороточные антитела поздней фазы инфекции, направленные против полуконсервированных эпитопов С-концевой области, не обладали цитотоксическим действием и вызывали только временное отрывание и агрегацию паразита.
Чтобы выяснить, генерирует ли местный ответ против Giardia гетерогенный репертуар антител против VSP H7, напоминающий системный ответ антител, мы выполнили дополнительную серию экспериментальных G.lamblia (клон GS / M-83-H7) с использованием комбинированной модели мышей-потомков. Эти эксперименты включали исследование выработки материнскими секреторными анти-VSP H7 IgA в молоке и характеристику влияния этих антител на рост паразитов у сосущих мышей. Анализы показали, что прием потомством временно возникающих молочных IgA-антител против вариабельной N-концевой части VSP H7 вызывает прямой паразитицидный эффект на трофозоиты исходного инокулята.Путем отбора новых вариантных типов антигенов в популяции кишечных паразитов этот опосредованный антителами паразитицидный механизм, по-видимому, запускает процесс антигенной диверсификации популяций клона GS / M-83-H7 G. lamblia в кишечнике мыши-хозяина.
МАТЕРИАЛЫ И МЕТОДЫ
Животные. Беспородных мышей Gravid в возрасте от 10 до 12 недель были получены из Institut für Labortierkunde, Университет Цюриха, Цюрих, Швейцария. Животных содержали в соответствии со швейцарскими правилами проведения экспериментов на животных со свободным доступом к стерильной воде и стерильной воде.
Паразит. Происхождение, аксенизация и клонирование клона GS / M-83-H7 G. lamblia были описаны Аггарвалом с соавторами (1). Этот клон экспрессирует на своей поверхности основной антиген массой 72 кДа (VSP H7), который распознается моноклональным антителом (MAb) G10 / 4. G. lamblia трофозоитов культивировали в среде TYI-S-33 с антибиотиками, как описано ранее (8).
Экспериментальная паразитарная инфекция и сбор образцов. Группа из восьми беременных мышей ZU.ICR (обозначенных как предварительно инфицированные матери) была инфицирована 3 раза (на 5, 10 и 15 дни после оплодотворения животных) G.lamblia клон GS / M-83-H7 с помощью иглы с тупым концом для пероральной инокуляции 200 мкл суспензии паразитов, содержащей 10 6 трофозоитов. Инокулят паразита получали путем двукратной промывки культивированных in vitro трофозоитов стерильным фосфатно-солевым буфером (PBS) и последующего ресуспендирования клеток в 0,3 М буфере NaHCO 3 . Параллельно группе из восьми беременных мышей ZU.ICR (обозначенных как непреинфицированные матери) инокулировали 200 мкл 0,3 М буфера NaHCO 3 .Животных из пометов (от 8 до 12 мышей в помете) предварительно инфицированных и непреинфицированных матерей инфицировали в послеродовом периоде путем внутрижелудочной инокуляции 5 × 10 4 трофозоитов G. lamblia (клон GS / M-83-H7), как описано ранее (6 ).
Молоко из молочной железы собирали по методу Парра и соавторов (13) после эвтаназии (с CO 2 ) матерей. Молоко, проглоченное потомством, получали путем выделения содержимого желудка (примерно от 200 до 500 мкл на мышь) с последующим добавлением того же объема PBS и окончательной гомогенизацией образцов путем встряхивания в течение 2 мин.Образцы молока собирали и хранили при -20 ° C. После оттаивания образцов нерастворимые компоненты удаляли центрифугированием в течение 10 минут при 10,000 × g , а затем надосадочные жидкости молока использовали для дальнейших исследований (см. Ниже).
Течение инфекции G. lamblia у матерей и потомков было определено путем количественной оценки паразитарной нагрузки посредством микроскопического исследования прилипших трофозоитов из смывов кишечника и дополнительного подтверждения присутствия жизнеспособных кишечных паразитов посредством 6-дневного размножения таких паразитов. адгезивные трофозоиты в культуральной среде TYI-S-33, содержащей антибиотики (8).В частности, продольно разрезали срезы примерно 0,5 (разрез 1) и 1 (разрез 2) см от верхней части двенадцатиперстной кишки. Раздел 1 помещали в чашку Петри, добавляли 2 капли PBS и исследовали под микроскопом на наличие трофозоитов. Если на участке 1 был обнаружен высокий уровень заражения паразитом (т. Е. От нескольких сотен до нескольких тысяч паразитов на одно микроскопическое поле при 100-кратном увеличении), участок 2 был дополнительно исследован, сначала инкубируя срез в течение 20 минут в 1 мл PBS. на льду для отделения трофозоитов от поверхности кишечника, а затем с помощью гемоцитометра для определения количества отделившихся трофозоитов в супернатанте PBS.В тех случаях, когда на участке 1 был отмечен низкий уровень инфекции (менее 10 трофозоитов на микроскопическое поле), со вторым участком обрабатывали так же, как описано выше, но отделенные трофозоиты впоследствии повторно переносили на дно лунки из 24-луночной культуры ткани пластины (Sarstedt, Newton, NC) в течение 30 мин инкубации суспензии трофозоитов при 37 ° C. Перечитанные трофозоиты подсчитывали под микроскопом (при 100-кратном увеличении) с использованием прозрачной сетки размером 1 мм 2 для лучшей ориентации.Кумулятивное количество трофозоитов в 10 отдельных микроскопических полях (размер ≈3 мм 2 ) было взято для экстраполяции общего количества прикрепившихся клеток на лунку (размер дна, ≈200 мм 2 ).
Иммунофлуоресцентные анализы. Кинетику экспрессии основного поверхностного антигена на трофозоитах, выделенных из двенадцатиперстной или подвздошной кишки, оценивали с использованием MAb G10 / 4 для иммунофлуоресцентного анализа, как описано в другом месте (6). Для определения иммунореактивности антитела с поверхностным антигеном использовали козий антимышиный IgG (IgG Fab ‘специфический; Sigma, St.Louis, Mo.), конъюгированный с TRITC, использовали в разведении 1:50. Для двойной маркировки для одновременного обнаружения IgA-несущих трофозоитов, происходящих из срезов кишечника (выделенных от трех животных в экспериментальной группе), использовали козий антимышиный IgA (специфичный для α-цепи; Sigma), конъюгированный с флуоресцеинизотиоцианатом (FITC) в том же разведении. . Изотипическая специфичность двух конъюгатов антител была ранее подтверждена в контрольных экспериментах путем доказательства отсутствия реактивности при инкубации (i) IgA-несущих трофозоитов (выделенных от потомков непреинфицированных матерей на 8-й и 9-й дни p.i., см. Результаты и рис. 1) с конъюгатом антимышиных IgG-TRITC и (ii) трофозоитами, меченными MAb G10 / 4 и не содержащими IgA (выделенными из потомства непреинфицированных матерей на 5 день после инфицирования; см. Результаты и Фиг.1) с конъюгатом антимышиных IgA-FITC. Количество трофозоитов типа VSP H7 (меченных TRITC) и / или IgA-несущих (меченных FITC) определяли путем исследования четырех случайно выбранных микроскопических полей (при 100-кратном увеличении).
Анализ цитотоксичности. Анализы цитотоксичности проводили в трех экземплярах, как описано ранее (1, 15), с использованием 96-луночных микротитровальных планшетов для инкубации 4 × 10 4 трофозоитов Giardia на 100 мкл культуральной среды в присутствии или в отсутствие аликвот надосадочной жидкости молока по 1 мкл (см. выше).Во время инкубации трофозоиты поддерживались и размножались в среде TYI-S-33 (8) в анаэробных условиях. Отделение и агрегацию трофозоитов исследовали сразу после добавления реагента, а также через 5 мин, 15 мин, 1 ч, 6 ч и 24 ч. Цитотоксичность определяли через 24 часа, оценивая количество прикрепившихся жизнеспособных паразитов с помощью микроскопического исследования. Тестовые культуры, содержащие заранее определенное количество прикрепленных клеток, менее примерно 10% от количества прикрепленных клеток, видимых в параллельной контрольной культуре, были признаны положительными в отношении цитотоксичности.Тестовые культуры, содержащие количество прилипших клеток, визуально неотличимых от количества в параллельной контрольной культуре, получили отрицательный результат. Все анализы цитотоксичности воспроизводили в двух отдельных экспериментах. В каждом эксперименте все супернатанты молока анализировали параллельно с использованием трофозоитов только из одной культуры in vitro для индивидуальных тестов.
Бактериальная экспрессия и очистка рекомбинантного VSP H7. Сегмент гена, кодирующий 314-аминокислотную N-концевую или 171-аминокислотную С-концевую область VSP H7, клонировали в вектор экспрессии pMalc2 Escherichia coli (New England Biolabs , Беверли, Массачусетс.), и соответствующие рекомбинантные белки (полученные как C-концевые слияния с N-концевой частью мальтозосвязывающего белка E. coli [MBP]) были очищены, как описано в другом месте (9).
ELISA и вестерн-блоттинг. Для анализа антител IgA молока против различных пептидных фрагментов VSP H7 был проведен следующий иммуноферментный анализ с захватом IgA (ELISA). Козье антитело против IgA мыши (специфическое для α-цепи; Sigma) использовали в разведении 1: 100 (в 0,1 М NaHCO 3 , pH 8.2) для покрытия планшетов microELISA (Maxisorp F 96 Immunoplates; Nunc, Роскилле, Дания). Лунки, покрытые анти-IgA, инкубировали в течение 4 ч при комнатной температуре с аликвотами по 100 мкл супернатанта молока (см. Выше), разведенного 1: 5 (супернатанты молока из содержимого желудка) или 1:50 (супернатанты молока из молочной железы) для блокирования. раствор (PBS, содержащий 0,3% Tween 20, 10% среду TYI-S-33 и 0,5% обезжиренное молоко). Затем лунки инкубировали в течение 2 ч при комнатной температуре со 100 мкл раствора антигена (1 мкг антигена на мл блокирующего раствора), содержащего очищенный MBP’-VSP H7 (314-аа N-концевую область), MBP’-VSP H7. (С-концевой участок из 171 аминокислот) или контрольный антиген MBP ‘соответственно.Комплексы антиген-антитело детектировали путем последовательной инкубации (2 ч при комнатной температуре) с кроличьими антителами против МВР IgG (New England Biolabs) и козьими антикроличьими антителами (специфичными для Fcγ; Promega, Мэдисон, Висконсин), конъюгированными с щелочная фосфатаза в разведении 1: 10 000 и 1: 500 соответственно. Результаты испытаний были подтверждены только тогда, когда обе вариабельность в трех определениях были менее 15% и значения A 405 (поглощение при 405 нм), полученные для всех MBP-специфичных контрольных реакций, были ниже 0.05. Индивидуальные значения, специфичные для VSP H7, рассчитывали путем вычитания среднего значения (плюс 2 стандартных отклонения) для трехкратного определения контрольных реакций MBP из среднего значения для соответствующих MBP’-VSP H7-специфических реакций.
Вестерн-блот-анализ растворимых антигенов GS / M-83-H7 клона G. lamblia проводили, как описано Gottstein и соавторами (6). Супернатанты молока (супернатанты молока из молочной железы; см. Выше), MAb G10 / 4 и конъюгированные с щелочной фосфатазой козьи антимышиные IgA (специфичные для α-цепи; Promega) разбавляли 1:50, 1: 200 и 1: 500. соответственно.
Статистические методы. Достоверность различий между контрольной и экспериментальной группами определяли по критерию Стьюдента t с использованием программы Microsoft Excel. P Значения <0,05 считались статистически значимыми.
РЕЗУЛЬТАТЫ
Течение инфекции G. lamblia и антигенная изменчивость паразита. Для изучения иммунологических и инфекционных параметров, связанных с процессом антигенной изменчивости, беременная ЗУ.Мыши ICR либо содержались неинфицированными (непреинфицированные матери), либо были перорально инфицированы трижды трофозоитами G. lamblia (предварительно инфицированные матери). Трехдневное послеродовое потомство от этих животных было инфицировано внутрижелудочной инъекцией того же типа трофозоитов. В разные моменты времени во время фазы лактации шесть потомков от разных матерей были умерщвлены посредством эвтаназии CO 2 . Микроскопическое определение количества кишечных паразитов (выделенных из двенадцатиперстной кишки) у грудного потомства показало, что течение инфекции было связано с колебаниями количества паразитов (рис.1б). У потомков от предварительно инфицированных матерей три волны инфекции высокой степени были очевидны на 5-7 день (первая волна), на 9 день (вторая волна) и на 11-13 дни (третья волна) постинфекции (p.i.). В течении инфекции у потомков от непреинфицированных матерей первая волна проявлялась между 3 и 7 днями, а вторая волна возникала на 9 день и продолжалась после фазы лактации. В экспериментах по заражению передачу паразитарной инфекции от матери к потомству можно было исключить, продемонстрировав отсутствие паразитов в биопсийном материале кишечника экспериментально незараженного потомства, полученного от предварительно инфицированных матерей (данные не показаны).Все данные, описанные в этом параграфе, были успешно воспроизведены во втором эксперименте, который включал эквивалентное последующее исследование паразитарной нагрузки у потомков от непреинфицированных и предварительно инфицированных матерей (данные не показаны).
Рис. 1.
Последующий анализ потомков, инфицированных G. lamblia (клон GS / M-83-H7) от экспериментально предварительно инфицированных (A) и непреинфицированных (B) матерей, с точки зрения бремени кишечных паразитов (дано в виде логарифма числа паразитов, обнаруживаемых в срезе двенадцатиперстной кишки длиной 1 см) (b) и включение IgA материнского молока против очищенного рекомбинантного MBP, слитого с 314-аминокислотным N-концом (c) и 171-аминокислотным C-концом (d ) части ВСП Н7.Анализировали паразитарную нагрузку и молочный IgA к VSP H7 от шести мышей на временную точку (указанную в днях рождения потомства). Показаны средние значения оптической плотности при 405 нм ( A 405 ) для реакций, специфичных для VSP H7, а также диапазоны. Средние значения <0,01 (включая отрицательные значения) обозначены пустой позицией. Существенные различия между значениями определяли с помощью критерия Стьюдента t (*, P <0,05). (a) Цифры указывают процент кишечных паразитов с типом антигена Mab G10 / 4 (VSP H7) -позитивного варианта.#, числа представляют собой процентное содержание MAb G10 / 4-положительных паразитов в исходном посевном материале.
Иммунофлуоресцентный анализ антигенной изменчивости паразита у потомков от предварительно инфицированных матерей показал, что трофозоиты первой волны уже претерпели диверсификацию от положительных типов MAb G10 / 4 к отрицательным (рис. 1а). Напротив, антигенная диверсификация паразитов у потомства от непреинфицированных матерей по существу происходила между 8 и 10 днями p.i. одновременно со второй волной инфекции высокой степени.
В совокупности эти наблюдения показали, что преинфекция матерей клоном GS / M-83-H7 G. lamblia оказала влияние как на течение инфекции у потомства, так и на антигенную изменчивость популяции кишечных паразитов в этих животные.
Производство IgA к VSP H7 в молоке. Использование рекомбинантных пептидных фрагментов как из вариантно-специфической 314-аминокислотной N-концевой части, так и из 171-аминокислотной С-концевой части VSP H7 в качестве антигенных реагентов, иммунный ответ материнского молока против паразита Инфекцию исследовали с помощью ИФА (рис.1c и d). Образцы молока брали из желудка мышей-сосунков в разное время. ELISA выявил, что во время инокуляции потомства (день 0) предварительно инфицированные матери преимущественно синтезировали молочный IgA против С-концевой части VSP H7 (фиг. 1Ad). Во время ранней фазы инфицирования потомства (дни с 1 по 5 p.i.) молочный IgA от предварительно инфицированных матерей был направлен как против N-концевых (фиг. 1Ac), так и C-концевых (фиг. 1Ad) областей VSP H7. С 6 дня p.i. антитела против N-концевой части исчезли, тогда как антитела против C-концевой части присутствовали на протяжении всего периода лактации.У непреинфицированных матерей выработка молочного IgA против обеих частей VSP H7 (между 8 и 12 днями p.i.) (рис. 1Bc и d) совпадала с первоначальным появлением антигенных вариантов среди популяции кишечных паразитов у потомства. На этот раз корреляция предполагает избирательную функцию этих специфичностей антител в процессе антигенной изменчивости паразита. Избирательная функция антител IgM и IgG к VSP H7 в этом процессе была исключена путем демонстрации отсутствия таких антител в любом из образцов молока любой исследуемой экспериментальной группы животных (данные не показаны).
ELISA, результаты которого показаны на фиг. 1, также показал, что как экспериментально предварительно инфицированные, так и непреинфицированные матери продуцировали молочные анти-VSP H7 IgA-антитела только в течение относительно короткого периода времени после инфицирования потомства (1 день после инфицирования, предварительно инфицированные матери; день 8 пи, непреинфицированные матери). Это указывало на то, что матери из обеих экспериментальных групп получили иммунологический стимул в результате попадания паразитарных загрязнений на потомство (скорее всего, в результате утечки трофозоитов во время внутрижелудочной инъекции инокулята).Возникновение такой экспериментально неконтролируемой инфекции было подтверждено демонстрацией присутствия трофозоитов в кишечнике экспериментально непреинфицированных материнских животных (данные не показаны). С другой стороны, заражение матерей кистами паразита, фекально выделяемыми потомством, было исключено из-за преждевременной беременности, а также исключено копрологическими исследованиями.
Тест на цитотоксичность молочных антител и характеристика специфичности паразитарных антител. Предыдущие исследования показали, что сывороточные антитела против 314-аминокислотной N-концевой области VSP H7 проявляют прямое цитотоксическое и агглютинирующее действие на культивируемых in vitro трофозоитов с массой G.lamblia клон GS / M-83-H7 (15). Чтобы проверить способность антител IgA к молоку опосредовать цитотоксичность, культивируемые in vitro трофозоиты из клона GS / M-83-H7 инкубировали в присутствии супернатантов молока из молочных желез предварительно инфицированных и непреинфицированных матерей, взятых на пробы при 0, 2. , и 8 дней пи (Рис. 2а). Этот анализ показал, что супернатанты молока с детектируемыми антителами против 314-аминокислотной N-концевой части VSP H7 (день 2 p.i., предварительно инфицированные матери; день 8 p.i., непреинфицированные матери) (рис.2b) были цитотоксичными и оказывали сильное и немедленное агглютинирующее действие на трофозоиты, видимое примерно через 5 мин. Напротив, молочные супернатанты, содержащие только IgA против 171-аминокислотной С-концевой части VSP H7 (дни 0 и 8, инфицированные матери) (рис. 2c), не были цитотоксичными и вызывали только слабую и временную агглютинацию трофозоитов, видимую примерно через 1 час и исчезает в течение следующих 24 часов инкубации в культуральной среде. Супернатанты молока, вообще не содержащие антител IgA к VSP H7 (дни 0 и 2, с.i., непреинфицированные матери) (рис. 2b и c) не проявляли ни одного из этих цитологических эффектов, даже после продолжительного инкубационного периода, составляющего около 24 часов. Кроме того, аналогичное тестирование всего набора надосадочных жидкостей молока с трофозоитами не-VSP H7-типа, выделенными на 12 день p.i. от потомства непреинфицированных матерей не оказали значительного эффекта (данные не показаны). Все тесты на цитотоксичность, описанные выше, проводили в условиях, в которых супернатанты предварительно инкубировали в течение 40 мин при 56 ° C для инактивации компонентов комплемента.Результат этих экспериментов был по существу таким же, как и описанный для анализов с необработанными надосадочными жидкостями молока.
Рис. 2.
Определение на основе ELISA молочного IgA против очищенного рекомбинантного MBP, слитого с 314-аминокислотной N-концевой (b) и 171-аминокислотной С-концевой (c) частями VSP H7. Молоко получали в разные моменты времени (в днях на день рождения потомства) из молочной железы G. lamblia (клон GS / M-83-H7) -преинфицированных (A) и непреинфицированных (B) матерей. Указаны средние значения поглощения при 405 нм ( A 405 ) для реакций, специфичных для VSP H7, а также диапазоны.Существенные различия между значениями определяли с помощью критерия Стьюдента t (*, P <0,05). (а) Показаны надосадки молока с (+) и без (-) цитотоксическим действием в отношении трофозоитов GS / M-83-H7 клона G. lamblia .
Чтобы дополнительно охарактеризовать специфичность антител IgA к Giardia , был проведен вестерн-блоттинг с использованием сырых экстрактов трофозоитов в качестве антигенных реагентов и тех же супернатантов молока, которые использовались выше (рис.3А и В). Этот эксперимент показал, что IgA из цитотоксических супернатантов молока (день 2 p.i., предварительно инфицированные матери; день 8 p.i., непреинфицированные матери) был по существу направлен против VSP H7. С другой стороны, нецитотоксические супернатанты молока, реагирующие с VSP H7, полученные от предварительно инфицированных матерей на 8 день p.i. проявляли дополнительную специфичность IgA к антигенам паразита, не относящимся к VSP H7. В этом Вестерн-блот-анализе полоса VSP H7 была идентифицирована по ее иммунореактивности с MAb G10 / 4 (фиг. 3C).
Рис. 3.
Вестерн-блот-анализ продукции паразитоспецифического молочного IgA у матерей, преинфицированных (A) и непреинфицированных (B) G. lamblia (клон GS / M-83-H7). Додецилсульфат-10% полиакриламид фракционировали и блотировали общий белок из клона G. lamblia GS / M-83-H7 инкубировали с супернатантами молока, взятыми у матерей в дни 0 (дорожки 1), 2 (дорожки 2), и 8 (дорожки 3) после заражения потомства. (C) Показаны контрольные блоты, инкубированные с VSP H7-реактивным MAb G10 / 4 (дорожка 1) и отрицательным контролем, MAb 6E7 (дорожка 2).Слева размеры белковых маркеров указаны в килодальтонах.
Определение относительных количеств трофозоитов типа VSP H7 из разных участков кишечника. Как продемонстрировано иммунофлуоресцентным анализом (рис. 1), потомство от непреинфицированных матерей на 8 день р.и. укрывали популяцию трофозоитов, которые были гетерогенными по составу вариантного антигена. Популяция паразитов в двенадцатиперстной кишке этих животных претерпела частичную антигенную диверсификацию и состояла только из 60-70% MAb G10 / 4-положительных трофозоитов.В следующем эксперименте дополнительное окрашивание трофозоитов двенадцатиперстной кишки вторым антителом, специфичным к мышиному IgA, показало, что, в отличие от MAb G10 / 4-отрицательных клеток, подавляющее большинство (> 90%) положительных клеток было покрыто кишечными клетками. Антитела IgA (таблица 1). Аналогичное исследование трофозоитов, выделенных из подвздошной кишки тех же животных, показало, что относительное количество MAb G10 / 4-положительных клеток было намного выше (> 95%), и эти паразиты по существу также были покрыты IgA (> 95%).По оценке краткосрочного (2-дневного) культивирования in vitro и последующего иммунофлуоресцентного окрашивания, пролиферативная (жизнеспособная) группа дуоденальных трофозоитов состояла из MAb G10 / 4-отрицательных клеток. Напротив, MAb G10 / 4-положительные трофозоиты из подвздошной кишки (> 95% паразитов) частично появлялись как агрегаты клеток и не могли быть впоследствии выращены in vitro.
Таблица 1.
Определение MAb G10 / 4-позитивных и IgA-несущих паразитов в двенадцатиперстной и подвздошной кишке G. lamblia клон GS / M-83-H7-инфицированных мышей a
В качестве контроля кишечные Популяции паразитов, взятые от потомков непреинфицированных матерей, исследовали на 5-е сутки.i., когда первоначальная антигенная диверсификация еще не произошла. В этом случае более 95% трофозоитов были положительными на MAb G10 / 4 и не содержали определяемых количеств IgA. При отдельных исследованиях адгезивные и пролиферативные паразиты были обнаружены в двенадцатиперстной кишке, тогда как паразитов в подвздошной кишке не было обнаружено ни под микроскопом, ни в долгосрочных (6-дневных) культурах in vitro. После кратковременного культивирования in vitro паразитов из двенадцатиперстной кишки большинство (> 95%) клеток сохраняли тип антигена Mab G10 / 4-позитивного варианта.
Результаты, описанные выше, были получены в трех параллельных экспериментах, представляющих собой исследования трофозоитов двенадцатиперстной и подвздошной кишки от трех животных в каждой экспериментальной группе. Взятые вместе, эти исследования показали, что популяция жизнеспособных трофозоитов G. lamblia располагалась в основном в двенадцатиперстной кишке. Принимая во внимание иммунофлуоресцентные анализы и тесты культивирования in vitro различных изолятов кишечных паразитов, наши данные также позволяют предположить, что те трофозоиты, которые были опсонизированы IgA, представляют собой популяцию нежизнеспособных паразитов, преимущественно локализованных в подвздошной кишке (см. Также Обсуждение).
ОБСУЖДЕНИЕ
Мы провели серию экспериментальных инфекций G. lamblia (клон GS / M-83-H7) новорожденных мышей и их матерей, чтобы изучить функцию местных антител IgA к VSP H7 в процессе антигенного воздействия. разновидность паразита. Наше исследование включало анализ IgA молока как от изначально неинфицированных матерей, так и от матерей, которые ранее получали сильный иммунологический стимул в результате повторяющейся пероральной инфекции паразитом. Используя комбинированную модель матери и потомства, мы смогли обойти две проблемы, которые мешают патогенным и иммунологическим исследованиям G.lamblia в обычной мышиной системе. Во-первых, инокуляция трофозоитов G. lamblia взрослым мышам, как было показано, приводит к сильному иммунному ответу против Giardia , но с относительно низкой степенью инфицирования (2), что затрудняет анализ соответствующих популяций паразитов в терминах. их вариантно-антигенотипного состава. Во-вторых, у новорожденных мышей обычно развивается инфекция высокой степени (7), но они обладают незрелой иммунной системой, которая не реагирует на раннюю фазу инфекции.Поэтому мы разработали настоящую стратегию для проверки влияния молочных антител IgA против VSP H7 от инфицированных матерей на популяцию G. lamblia у инфицированного потомства. В этом контексте разработка высокочувствительного ИФА с захватом IgA (см. «Материалы и методы») была важной предпосылкой для надежного и воспроизводимого мониторинга продукции анти-VSP H7 IgA в молоке у инфицированных животных. Стандартный ELISA (данные не показаны) ранее демонстрировал как более высокий уровень неспецифических фоновых реакций, так и большую вариабельность в пределах отдельных трех значений A 405 (см. Также материалы и методы).
Наши исследования показали, что антитела IgA против относительно консервативных эпитопов 171-аминокислотной С-концевой области VSP H7 проявляют слабые трофозоит-агглютинирующие эффекты, которые, по-видимому, существенно не препятствуют росту паразита in vitro. Напротив, IgA-антитела материнского молока против вариантно-специфической 314-аа N-концевой части VSP H7 вызывали немедленную агрегацию и прямую цитотоксичность в отношении культивируемых in vitro трофозоитов типа VSP H7. Актуальность этих паразитарных эффектов, опосредованных антителами in vivo, была подтверждена исследованием, которое определило относительное количество трофозоитов типа VSP H7 как в двенадцатиперстной, так и в подвздошной кишке у G.lamblia — зараженное потомство. Когда варианты типов антигенов в этих конкретных участках кишечника были уточнены на начальной стадии антигенной изменчивости, соотношение трофозоитов типа VSP H7 по сравнению с трофозоитами не-VSP H7 типа оказалось намного выше в подвздошной кишке, чем в двенадцатиперстной кишке. потомство. Дальнейшие анализы показали, что трофозоиты, положительные по MAb G10 / 4 (тип VSP H7), были специфически покрыты антителами IgA, а также представляли собой коллекции нежизнеспособных клеток, которые не пролиферировали in vitro.В соответствии с результатами наших предыдущих исследований (9, 14, 15), результаты, описанные выше, позволяют предположить, что опосредованный антителами и селективный механизм роста участвует в процессе антигенной диверсификации в пределах G. lamblia (клон GS / M-83-H7) у грудных мышей. Предлагается следующий механизм действия. Антитела IgA к молоку против 314-аминокислотной N-концевой части VSP H7 специфически взаимодействуют с трофозоитами типа VSP H7 в двенадцатиперстной кишке и вызывают прямые паразитарные эффекты в отношении них.В то время как трофозоиты, не относящиеся к типу VSP H7, остаются незатронутыми и находятся в виде прикрепленных жизнеспособных клеток в двенадцатиперстной кишке, нежизнеспособные и неприлипающие трофозоиты типа VSP H7 захватываются слизью и впоследствии транспортируются через перистальтику кишечника в подвздошную кишку. В этом дистальном отделе кишечника мышей такие трофозоиты появляются как неприлипающие клеточные агрегаты, состоящие исключительно из нежизнеспособных паразитов типа VSP H7.
Течение инфекции G. lamblia у грудных мышей было связано с колебаниями количества паразитов.Интересно, что разрастание трофозоитов во время прогрессирующей фазы второй и третьей волны высокоинтенсивной инфекции привело к темпам роста, которые были по крайней мере в три раза выше, чем наблюдаемые in vitro. Квазиэлиминация трофозоитов типа VSP H7, которые составили первую волну высокоинтенсивной инфекции у потомков от непреинфицированных матерей, совпала как с антигенной диверсификацией от популяции по существу MAb G10 / 4 к отрицательной популяции паразитов, так и с образованием паразитов. -агглютинирующие и цитотоксические молочные антитела, направленные против вариантно-специфической 314-аминокислотной N-концевой части VSP H7.Эти данные снова предоставили убедительные доказательства того, что in vivo рост таких отдельных популяций различных типов антигенов контролировался селективным давлением через паразитицидную активность вариантно-специфичных антител IgA.
Дальнейшие исследования модельной системы мыши G. lamblia GS / M-83-H7 будут направлены на ответы на следующие вопросы. (i) Представляют ли отдельные волны колеблющейся инфекции отдельные и последовательно возникающие популяции различных типов антигенов? (ii) Состоит ли индивидуальная волна из одного или нескольких типов вариантных антигенов? (iii) Объясняет ли последовательное и временное производство цитотоксических антител IgA против VSP последовательно появляющихся вариантных типов антигенов колеблющееся течение инфекции? (iv) Происходит ли антигенная вариация in vivo случайным образом или «запрограммированным» образом, что приводит к одной и той же последовательности G.lamblia различных типов антигена у разных хозяев? Из этих исследований мы надеемся получить дальнейшее понимание как стратегии антигенной изменчивости, применяемой паразитом для борьбы с иммунной системой, так и иммунологических эффекторных механизмов, генерируемых мышиной-хозяином для устранения различных вариантов антигенных типов паразита из организма. их кишечная среда обитания.
БЛАГОДАРНОСТИ
Мы благодарим В. Циммерманна за отличную техническую помощь, А.Хемфиллу за плодотворное обсуждение, Б. Коннолли за внимательное чтение рукописи и Т.Е. Нэша (NIH, Бетесда, Мэриленд) за дар MAb, фрагмента кДНК vspH7 и клона G. lamblia GS / M-83. -H7.
Работа поддержана грантами Швейцарского национального научного фонда (№ 31-37607.93 и 31-49439.96).
СНОСКИ
- Получено 26 августа 1997 г.
- Возвращено на доработку 1 октября 1997 г.
- Принято 11 января 1998 г.
- Copyright © 1998 Американское общество микробиологии
Действие человеческого молозива против инфекции Giardia lamblia под влиянием гормонов и пожилого возраста матери
Биленко Н., Гош Р., Леви А., Декельбаум Р. Дж., Фрейзер Д. (2008) Частично грудное вскармливание защищает младенцев-бедуинов от инфекций и заболеваемости: проспективное когортное исследование. Asia Pac J Clin Nutr 17: 243–249
PubMed
Google Scholar
Brandtzaeg P (2010) Иммунная система слизистой оболочки и ее интеграция с молочными железами.J Pediatr 156: 8–15
Статья
Google Scholar
Caetano MR, Couto E, Passini Junior R, Simoni RZ, Barini R (2006) Гестационные прогностические факторы у женщин с повторным самопроизвольным абортом. São Paulo Med J 124: 181–185
Статья
PubMed
Google Scholar
Caspari GR (1993) Влияние лейкоцитов молозива на экспериментальную инфекцию Escherichia coli и сывороточные антитела новорожденных телят.Vet Immunol Immunopathol 35: 275–288
Статья
Google Scholar
Cecatti JG, De Aquino MMA (1998) Причины и факторы, связанные со смертью плода. Rev Ciênc Méd 7: 43–48
Google Scholar
Cohen WR (2014) Влияет ли возраст матери на исход беременности? BJOG 121: 252–254
Статья
PubMed
Google Scholar
Fagundes DLG, França EL, Hara CCP, Honorio-França AC (2012) Иммуномодулирующие эффекты микросфер полиэтиленгликоля, адсорбированных кортизолом, на активность фагоцитов молозива.Int J Pharmacol 8: 510–518
CAS
Статья
Google Scholar
Fagundes DLG, França EL, Morceli G, Rudge MVC, Calderon IPM, Honorio-França AC (2013) Роль цитокинов в функциональной активности фагоцитов в крови и молозиве матерей с диабетом. Clin Dev Immunol 2013: 5
: 1–8
Статья
Google Scholar
Fagundes DLG, França EL, Fernandes RTS, Hara CCP, Morceli G, Honorio-França AC, Calderon IMP (2016) Изменения фенотипа Т-клеток и профиля цитокинов в материнской крови, пуповинной крови и молозиве матерей с диабетом.J Matern Fetal Neonatal Med 29: 998–1004
CAS
Статья
Google Scholar
Foligne B, Aissaoui F, Senegal-Balas F, Cayuela C, Bernard P, Antoine JM (2001) Изменения клеточной пролиферации и дифференцировки эпителия тонкой кишки взрослых крыс после адреналэктомии. Dig Dis Sci 46: 1236–1246
CAS
Статья
PubMed
Google Scholar
França EL, Nicomedes TR, Calderon IMP, Honorio-França AC (2010) Зависящие от времени изменения растворимых и клеточных компонентов в материнском молоке.Biol Rhythm Res 41: 333–347
Статья
Google Scholar
França EL, Bitencourt RV, Fujimori M, Moraes TC, Calderon IMP, Honorio-França AC (2011a) Колостральные фагоциты человека устраняют энтеротоксигенные Escherichia coli , опсонизированные супернатантом молозива. J Microbiol Immunol Infect 44: 1–7
Статья
PubMed
Google Scholar
França EL, Morceli G, Fagundes DLG, Calderon IMP, Honorio-França AC (2011b) Взаимодействие секреторных IgA-Fc альфа-рецепторов, модулирующее фагоцитоз и микробицидную активность фагоцитов в человеческом молозиве диабетиков.APMIS 119: 710–719
Статья
PubMed
Google Scholar
Franca EL, Calderon IMP, Vieira EL, Morceli G, Honorio-França AC (2012) Передача материнского иммунитета новорожденным от матерей с диабетом. Clin Dev Immunol 2012: 928187: 1–7
Статья
Google Scholar
França-Botelho AC, Honorio-França AC, França EL, Gomes MA, Costa-Cruz JM (2006) Фагоцитоз Giardia lamblia трофозоитов колостральными лейкоцитами человека.Acta Paediatr 95: 438–443
Статья
PubMed
Google Scholar
França-Botelho ACF, França JL, Oliveira FC, França EL, Honorio-França AC, Caliari MV, Gomes MA (2011) Мелатонин снижает тяжесть экспериментального амебиаза. Parasit Vectors 4: 62–67
Статья
PubMed
PubMed Central
Google Scholar
Fujimori M, França EL, Moraes TC, Fiori V, Abreu LC, Honorio-Franca AC (2017) Цитокин и адипокин — биофакторы, которые могут действовать в крови и молозиве матерей с ожирением.Биофакторы 23: 45–51
Google Scholar
Garofalo R (2010) Цитокины в материнском молоке. J Pediatr 156: S36 – S40
CAS
Статья
PubMed
Google Scholar
Gravena AAF, Sass A, Marcon SS, Pelloso SM (2012) Исходы беременностей в позднем возрасте. Ред. Esc Enferm USP 46: 15–21
Статья
PubMed
Google Scholar
Hara CCP, Honorio-França AC, Fagundes DLG, Guimarães PCL, França EL (2013) Наночастицы мелатонина, адсорбированные на микросферах полиэтиленгликоля, как активаторы макрофагов молозива человека.J Nanomater 2: 1–8
Статья
Google Scholar
Hernandes MRG, Moraes LCA, Ribeiro EB, Fagundes DLG, Honorio-França AC, França EL (2017) Иммуномодулирующие эффекты in vitro микроэмульсий с системами доставки левамизола на фагоциты крови, взаимодействующие с Giardia lamblia . Parasitol Int 66: 299–304
CAS
Статья
PubMed
Google Scholar
Hill DR, Pearson RD (1987) Проглатывание трофозоитов Giardia lamblia мононуклеарными фагоцитами человека.Infect Immun 55: 3155–3161
CAS
PubMed
PubMed Central
Google Scholar
Honorio-França AC, Carvalho MP, Isaac L, Trabulsi LR, Carneiro-Sampaio MMS (1997) Колостральные мононуклеарные фагоциты способны убивать энтеропатогенные Escherichia coli , опсонизированные колостральным IgA. Scand J Immunol 46: 59–66
Артикул
PubMed
Google Scholar
Honorio-França AC, Launay P, Carneiro-Sampaio MM, Monteiro RC (2001) Колостральные нейтрофилы экспрессируют рецепторы Fc-альфа (CD89), лишенные ассоциации с гамма-цепью, и опосредуют невоспалительные свойства секреторного IgA.J Leukoc Biol 69: 289–296
PubMed
Google Scholar
Honorio-França AC, Hara CCP, Ormonde JVS, Nunes GT, França EL (2013) Мелатонин человеческого молозива изменяется день-ночь и модулирует активность фагоцитов молозива. J Appl Biomed 11: 153–162
Статья
Google Scholar
Hugaes A, Brock JH, Parrott DMV, Cockburn F (1988) Взаимодействие детской смеси с макрофагами: влияние на фагоцитарную активность, связь с экспрессией антигена MHC класса II и выживаемость перорально вводимых макрофагов в кишечнике новорожденных.Иммунология 64: 213–218
Google Scholar
Ignatius R, Gahutu JG, Klotz C, Steininger C, Shyirambere C, Lyng M, Musemakweri A, Aebischer T, Martus P, Harms G, Mockenhaup FP (2012) Высокая распространенность инфекции Giardia duodenalis и Assemblage связь с недостаточным весом у руандийских детей. PLoS Negl Trop Dis 6: e1677
Jouana PN, Pouliotb Y, Gauthiera SF, Laforest JP (2006) Гормоны в коровьем молоке и молочных продуктах.Int Dairy J 16: 1408–1414
Артикул
Google Scholar
Keister DB (1983) Аксеническая культура Giardia lamblia в среде TYI-S-33 с добавлением желчи. Trans R Soc Trop Med Hyg 77: 487–488
CAS
Статья
PubMed
Google Scholar
Kohut ML, Martin AE, Senchina DS, Lee W (2005) Глюкокортикоиды, вырабатываемые во время упражнений, могут быть необходимы для оптимального вирус-индуцированного IL-2 и пролиферации клеток, тогда как катехоламины и глюкокортикоиды могут потребоваться для адекватной иммунной защиты от вирусов. инфекционное заболевание.Brain Behav Immun 19: 423–435
CAS
Статья
PubMed
Google Scholar
Кройтнер А.К., Дель Бене В.Е., Амстей М.С. (1981) Лямблиоз во время беременности. Am J Obstet Gynecol 140: 895–901
CAS
Статья
PubMed
Google Scholar
Kunz-Ebrecht SR, Mohamed-Ali V, Feldman PJ, Kirschbaum C, Steptoe A (2003) Реакция кортизола на легкий психологический стресс обратно пропорциональна провоспалительным цитокинам.Brain Behav Immun 17: 373–383
CAS
Статья
PubMed
Google Scholar
Lim HY, Muller N, Herold MJ, Van Den Brandt J, Reichardt HM (2007) Глюкокортикоиды оказывают противоположное влияние на функцию макрофагов в зависимости от их концентрации. Иммунология 122: 47–53
CAS
Статья
PubMed
PubMed Central
Google Scholar
Maestroni GS (2001) Иммунотерапевтический потенциал мелатонина.Мнение эксперта по исследованию наркотиков 10: 467–476
CAS
Статья
PubMed
Google Scholar
Mahmud MA, Chappell CL, Hossain MM, Chappell M, Hossain M, Huang DB, Habib M, Dupont HL (2001) Влияние грудного вскармливания на Giardia lamblia инфекций в Bilbeis. Египет. Am J Trop Med Hyg 65: 257–260
CAS
Статья
PubMed
Google Scholar
Medeiros SF, Maitelli A, Nince APB (2007) Влияние гормональной терапии менопаузы на иммунную систему.Rev Bras Ginecol Obstet 29: 593–601
Google Scholar
Moraes LCA, França EL, Pessoa RS, Fagundes DL, Gomes MA, Honorio-França AC (2015) Влияние IFN-γ и TGF-β на функциональную активность мононуклеарных клеток в присутствии Entamoeba histolytica . Parasit Vectors 8: 413
Статья
PubMed
PubMed Central
Google Scholar
Morceli G, França EL, Magalhães VB, Damasceno DC, Calderon IMP, Honorio França A (2011) Диабет вызвал иммунологические и биохимические изменения в молозиве человека.Acta Paediatr 100: 550–556
CAS
Статья
PubMed
Google Scholar
Morceli G, Honorio-França AC, Fagundes DLG, Calderon IMP, Franca EL (2013) Антиоксидантный эффект мелатонина на функциональную активность фагоцитов молозива у женщин с диабетом. PLoS One 8: 569–571
Статья
Google Scholar
Pandi-Perumal SR, Trakht I, Srinivasan V, Spence DW, Maestroni GJ, Zisapel N, Cardinali DP (2008) Физиологические эффекты мелатонина: роль рецепторов мелатонина и пути передачи сигнала.Прог Нейробиол 85: 335–353
CAS
Статья
PubMed
Google Scholar
Pick E, Mizel D (1981) Быстрые микроанализы для измерения продукции супероксида и пероксида водорода макрофагами в культуре с использованием автоматического считывающего устройства для иммуноферментного анализа. J Immunol Methods 46: 211–226
CAS
Статья
PubMed
Google Scholar
Quihui L, Morales GG, Mendez RO, Leyva JG, Romero JE, Valencia ME (2010) Может ли лямблиоз быть фактором риска низкого статуса цинка у школьников из северо-западной Мексики? Поперечное исследование с продолжительным наблюдением.BMC Public Health 10: 85–91
Статья
PubMed
PubMed Central
Google Scholar
Рэди М.Ю., Джонсон Д.Д., Патель Б., Ларсон Дж., Хелмерс Р. (2005) Уровни кортизола и введение кортикостероидов не могут предсказать смертность при критическом заболевании: смешанные эффекты дисфункции органов и пола. Arch Surg 140: 661–668
Артикул
PubMed
Google Scholar
Reiner DS, Wang CS, Gillin FD (1986) Грудное молоко убивает Giardia lamblia путем образования токсичных липолитических продуктов.J Infect Dis 154: 825–832
CAS
Статья
PubMed
Google Scholar
Робертсон Л.К., Ханевик А.А., Эскобедо К., Мёрч Н. (2010) Лангеланд, лямблиоз — почему симптомы иногда никогда не прекращаются? Trends Parasitol 26: 75–82
Статья
PubMed
Google Scholar
Sadeghi H, Borji H (2015) Исследование кишечных паразитов в популяции в Казвине, к северу от Ирана.Asian Pac J Trop Dis 5: 231–233
Статья
Google Scholar
Salazar-Molina A, Klijn TP, Delgado JB (2015) Сексуальное удовлетворение в парах на мужской и женской климактерической стадии. Satisfacción sex en parejas durante el climaterio femenino y masculino Satisfação sex nos casais durantemin o climatériino femen. Cad Saude Publica 31: 311–320
Статья
PubMed
Google Scholar
Судникович Е.Ю., Мсксимчик Ю.З., Забродская С.В., Кубышин В.Л., Лапшина Е.А., Брыжевская М., Рейтер Р.Дж., Заводник И.Б. (2007) Мелатонин ослабляет метаболические нарушения у крыс, вызванные стрептозотоцином.Eur J Pharmacol 569: 180–187
CAS
Статья
PubMed
Google Scholar
Вальтерспиль Дж. Н., Морроу А. Л., Герреро Л., Руис-Паласиос Г. М., Пикеринг Л. К. (1994) Секреторные антитела против лямблии в материнском молоке: защитный эффект против диареи. Педиатрия 93: 28–31
CAS
PubMed
Google Scholar
Изменения иммуномодулирующих компонентов грудного молока в ответ на активную инфекцию у грудного ребенка
Человеческое грудное молоко обеспечивает важную систему иммунологической поддержки для младенца в течение первых месяцев жизни.В нашем исследовании мы обнаружили, что среднее количество лейкоцитов (CD45 + ) в материнском молоке значительно снизилось между фазами активной инфекции и выздоровления их грудных детей, причем наиболее значительным и выраженным падением было количество макрофагов. . Также уменьшилось количество лимфоцитов и нейтрофилов. Это снижение было более значительным в молоке матерей младенцев с доказанной локализованной инфекцией. В контрольной группе подобных изменений не наблюдалось.
Уровни TNFα достоверно снизились в молоке матерей исследуемой группы между периодами острой инфекции и выздоровлением. Уровни лактоферрина также имели тенденцию к снижению, но это имело лишь пограничную статистическую значимость. Хотя уровни ИЛ-10 значительно снизились, этот результат следует интерпретировать с осторожностью, поскольку аналогичное снижение было отмечено и в контрольной группе.
Состав грудного молока у кормящих женщин сильно различается по количеству различных питательных веществ, а также по клеточным компонентам, олигосахаридам и уровням цитокинов.Эта изменчивость, которая может быть суточной и даже возникать в течение одного грудного вскармливания, также контролируется генетически и может зависеть от атопического статуса матери (26,27,28,29). Чтобы справиться с этой значительной биологической вариабельностью, мы взяли по две пробы от каждой кормящей матери в исследуемой и контрольной группах, чтобы каждая мать стала для себя контролем. Первый образец, взятый у исследуемых матерей, отражал состав молока во время активной инфекции, а второй образец отражал изменения в его составе во время выздоровления.Отсутствие аналогичных изменений между двумя образцами молока в контрольной группе сформировало прочную основу для определения изменений между образцами молока в исследуемой группе как истинного доказательства иммунологических изменений в составе материнского молока в ответ на инфекцию.
Известно, что лейкоциты материнской крови, находящиеся в молочной железе, проходят через стыки эпителиальных клеток и секретируются в грудное молоко. Напротив, моноциты крови, достигающие молочной железы, активируются локально, превращаясь в макрофаги, а затем секретируются в грудное молоко.
Наш главный результат — увеличение общего количества лейкоцитов в материнском молоке по сравнению с активной инфекцией у их грудных младенцев. Механизм, объясняющий это явление, не ясен и не исследовался в данном исследовании. Разумно предположить, что инфекции дыхательных путей или желудочно-кишечного тракта у младенца на самом деле заражают и мать, что приводит к воспалительной реакции в ее организме, которая вызывает повышенную секрецию лейкоцитов и цитокинов в молоко, которое она производит.Можно предположить, что воспалительный ответ может увеличить лейкоциты в ее крови или привлечь больше клеток к молочной железе, или изменить движение клеток внутри молочной железы, что приведет к увеличению секретируемых клеток в грудном молоке. Наши данные подтверждают эту гипотезу тем, что 35% матерей и 65% братьев и сестер младенцев, участвовавших в исследовании, имели сопутствующую лихорадку. Этот механизм выглядит менее вероятным в случае бактериальных или локализованных инфекций, таких как инфекции мочевыводящих путей или менингит.Однако, когда мы специально исследовали компоненты клеток грудного молока только у здоровых матерей, мы все же обнаружили, что во время инфицирования младенца по сравнению с выздоровлением они секретировали статистически значимое увеличение количества лейкоцитов и макрофагов.
В нашем исследовании мы также продемонстрировали, что концентрации TNFα в грудном молоке матерей исследуемой группы были относительно высокими в первых образцах во время инфекции, а затем значительно снизились во время выздоровления их младенцев. Основным источником TNFα является секреция макрофагов, хотя другие клетки, такие как нейтрофилы, Т- и B-лимфоциты, а также естественные клетки-киллеры, также могут секретировать TNFα, особенно после антигенной стимуляции бактериального происхождения.Обнаружение увеличения воспалительных клеток, особенно макрофагов и нейтрофилов, в грудном молоке, взятом от матерей больных младенцев, может объяснить повышенные уровни TNFα. Это объяснение подтверждается обнаруженной нами положительной корреляцией между общим количеством лейкоцитов CD45 + , особенно количеством макрофагов, и уровнями TNFα (
Рисунок 1
).
Лактоферрин секретируется эпителиальными клетками ткани молочной железы и активированными лейкоцитами.В нашем исследовании мы продемонстрировали более высокий уровень лактоферрина в молоке матерей, кормящих больных младенцев. Хотя эта разница не достигла необходимого уровня статистической значимости, она показала погранично значимую тенденцию, которая не наблюдалась в контрольной группе. Это можно объяснить тем фактом, что обнаруженное нами увеличение количества активированных нейтрофилов, которые секретируют часть лактоферрина с грудным молоком во время инфекции, также было на уровне пограничного значения.
sIgA секретируется лимфоидными клетками молочной железы, которые, вероятно, происходят из B-лимфоцитов, мигрирующих из желудочно-кишечного тракта в молочную железу (4). Лишь небольшая часть sIgA секретируется макрофагами, содержащими это антитело. Из наших результатов кажется, что секреция этого иммуноглобулинового антитела недостаточно подвержена влиянию инфекционного заболевания у грудного ребенка, чтобы вызвать статистически значимое повышение.
Иммунологический смысл нашего открытия не ясен.Можно предположить, что повышенное количество клеток, а также более высокие уровни TNFα и, в меньшей степени, лактоферрина в грудном молоке могут помочь кормящемуся ребенку справиться с инфекцией. Это подтверждается доказанной способностью макрофагов и лейкоцитов грудного молока убивать энтеропатогенные Escherichia coli, Giardia lamblia, Staphylococcus aureus и Candida albicans (30, 31, 32).
Хотя это предполагало динамическое взаимодействие между больными младенцами и их матерями, которое изменяет молоко, чтобы помочь защитить младенцев, кажется очень правдоподобным, возможно, что некоторые из результатов в первых пробах молока от матерей больных младенцев (например,g., больше клеток CD45 и более высокие уровни TNFα, особенно по сравнению с теми, которые были обнаружены в контроле,
Таблица 2
) фактически отражают неспецифическую стрессовую реакцию матерей, чьи младенцы были госпитализированы.
Таким образом, в этом исследовании мы обнаружили, что во время активной инфекции у грудного ребенка общее количество лейкоцитов, в частности количество макрофагов и уровни TNFα, увеличиваются. Наши результаты подтверждают динамическую иммунологическую связь между кормящими матерями и их грудными младенцами, особенно во время активной инфекции, что еще больше способствует грудному вскармливанию.Наше исследование дает лишь представление о богатой природе иммунологической защиты, обеспечиваемой грудным молоком. Необходимы дальнейшие исследования, чтобы выяснить иммунологические механизмы, лежащие в основе этих реакций, а также их клиническое значение.
Защищает ли грудное вскармливание ребенка от инфекции Giardia lamblia?
Актуальность проблемы: Giardia lamblia — одна из наиболее распространенных простейших инфекций тонкой кишки человека.Хотя лямблиозом может заразиться любой человек, женщины и дети более восприимчивы к нему. Инфекция лямблий может вызвать недоедание, диарею и несварение жира. В этом исследовании изучается влияние грудного вскармливания на распространенность лямблий среди детей. Методы. Всего в опросе приняли участие 482 ребенка в возрасте от 6 до 24 месяцев из городских районов Семнан, Дамган и Гармсар в Иране. Каждая мать прошла собеседование и заполнила анкету, в которой были указаны возраст матери, размер семьи, порядок рождения ребенка, возраст и пол ребенка и тип потребляемого молока, среди других переменных.Затем каждой матери дали контейнер для образцов с 30 см3 фенол-спирта и формальдегида (PAF) и аппликатор для отбора образцов стула ее ребенка. Каждую мать учили последовательно брать образцы стула своего ребенка в течение трех дней, помещать стул в предоставленный контейнер с помощью аппликатора и встряхивать его до тех пор, пока образец и жидкость не станут однородными. Образец исследовали прямым методом с использованием простого формалина и тионина. Данные были проанализированы с использованием теста ‡ 2 и логистической регрессии с использованием SPSS версии 11.5. Результаты. Средний возраст детей составлял 13,6 (± 5,6) месяцев. Из этих детей 45,6% составляли девочки. Распространенность инфекции G. lamblia составила 8,5%. Существовала значимая взаимосвязь между лямблиями и возрастом ребенка, уровнем образования матери и типом молока, потребляемого ребенком (p & lt; 0,05), так что дети, которые не употребляли материнское молоко, имели более высокую вероятность заражения по сравнению с тем, кто кормил грудью (OR = 2,38, 95% ДИ: 1,13–5,03, P = 0,023). Выводы. Результаты показывают, что грудное вскармливание является более безопасным методом кормления в отношении инфекции лямблий.Поэтому матерей следует научить кормить своих детей грудью и не использовать другие виды молока или заменители молока. Этот важный вопрос должен быть рассмотрен политиками в отношении программ образования и субсидий. © 2008, Тегеранский университет медицинских наук.
