Энтероколит у грудничка симптомы: Энтероколит у детей. Что такое Энтероколит у детей?
Энтероколит у детей. Что такое Энтероколит у детей?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Энтероколит у детей — это сочетанное воспаление тонкого и толстого кишечника. Возникает при инфицировании патогенными бактериями, вирусами или простейшими, под действием аллергических, механических или токсических провоцирующих факторов. Заболевание проявляется разнообразными болями в животе, запорами или диареей, интоксикационным синдромом. План диагностики включает ультразвуковые, эндоскопические и рентгенологические методы, серологические и бактериологические анализы. Лечение энтероколита у детей состоит из диетотерапии, фармакотерапии (энтеросорбенты, пробиотики, антибиотики и антипротозойные препараты).
МКБ-10
K52 A09
- Причины
- Патогенез
- Симптомы энтероколита у детей
- Осложнения
- Диагностика
- Лечение энтероколита у детей
- Диетотерапия
- Консервативная терапия
- Хирургическое лечение
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Энтероколит — синдром, который встречается при разных инфекционных и неинфекционных заболеваниях ЖКТ. Это самый распространенный тип поражения желудочно-кишечного тракта у детей, но его точную частоту установить затруднительно в связи с большим разнообразием клинических диагнозов, протекающих с кишечным воспалением. В самостоятельную нозологическую единицу выделяют некротический энтероколит новорожденных, определяемый у 5% младенцев, которые поступают в отделение интенсивной терапии.
Энтероколит у детей
Причины
Этиологические факторы энтероколита подразделяют на инфекционные и неинфекционные. В педиатрической практике чаще диагностируется первый вариант, поскольку кишечные инфекции — вторая по частоте после ОРВИ группа заболеваний детского возраста. Кишечное воспаление вызывают бактериальные (сальмонелла, эшерихия, иерсиния и шигелла), вирусные (ротавирус, норовирус) и паразитарные инвазии (амебиаз, балантидиаз, лямблиоз).
В педиатрической практике чаще диагностируется первый вариант, поскольку кишечные инфекции — вторая по частоте после ОРВИ группа заболеваний детского возраста. Кишечное воспаление вызывают бактериальные (сальмонелла, эшерихия, иерсиния и шигелла), вирусные (ротавирус, норовирус) и паразитарные инвазии (амебиаз, балантидиаз, лямблиоз).
Инфекционные причины энтероколита более характерны для пациентов раннего возраста и дошкольников. Исключение составляет псевдомембранозный колит, который обусловлен размножением условно-патогенных клостридий на фоне приема антибиотиков и выявляется у детей любого возраста. Помимо инфекционных агентов, развитие энтероколита провоцируют:
- Реакции гиперчувствительности. Симптомы воспаления кишечника наблюдаются у детей с экссудативным диатезом, которые имеют склонность к пищевой аллергии и «аллергическому маршу». Расстройство вызвано повреждающим действием иммунных молекул, образующихся в ответ на чужеродные белки.
- Токсины.
 Прямое повреждающее действие на слизистую тонкой и толстой кишки оказывают химические вещества, пестициды, некоторые лекарства. Острый энтероколит возникает, если ребенок по ошибке выпьет средство бытовой химии или другие опасные вещества, а хроническая форма развивается при длительной медикаментозной терапии.
Прямое повреждающее действие на слизистую тонкой и толстой кишки оказывают химические вещества, пестициды, некоторые лекарства. Острый энтероколит возникает, если ребенок по ошибке выпьет средство бытовой химии или другие опасные вещества, а хроническая форма развивается при длительной медикаментозной терапии. - Механическое повреждение. Патология связана со сдавлением кишечной стенки и раздражением ее твердыми частицами кала, что зачастую случается при хронических запорах. У детей расстройство преимущественно осложняет врожденные аномалии пищеварительного тракта, как, например, в случае с гиршпрунг-ассоциированным энтероколитом.
- Ишемия кишечника. Сосудистые нарушения лежат в основе некротического энтероколита, поражающего новорожденных с антенатальными или перинатальными факторами риска. Недостаток кровоснабжения сочетается с тромбозом сосудов, участками омертвения кишечной стенки.
Патогенез
Механизм развития заболевания основан на повреждении слизистой с последующим распространением патологического процесса на все слои кишечной стенки. Как следствие нарушаются функции ЖКТ: полостное и пристеночное пищеварение, всасывание питательных веществ, секреция воды и солей в просвет кишки. Воспаление сопровождается изменением перистальтики в сторону ускорения или замедления, снижением местного иммунного ответа и нарушением микрофлоры.
Как следствие нарушаются функции ЖКТ: полостное и пристеночное пищеварение, всасывание питательных веществ, секреция воды и солей в просвет кишки. Воспаление сопровождается изменением перистальтики в сторону ускорения или замедления, снижением местного иммунного ответа и нарушением микрофлоры.
Симптомы энтероколита у детей
Клиническая картина энтероколита у детей во многом определяется его причинами, степенью повреждения кишечника. Основные симптомы — нарушения стула, боли в полости живота. Для острого течения типичны спазмы и рези, которые не имеют четкой локализации. Появление болезненности в левой подвздошной области и тенезмов указывает на поражение дистальных отделов ЖКТ. При хроническом варианте беспокоят дискомфорт, тяжесть и покалывание в животе.
Расстройства стула при энтероколитах имеют различный характер: запоры, диарея, чередование этих двух форм либо фракционированная дефекация. При остром процессе, чаще инфекционной этиологии, у детей отмечается учащение стула до 10-20 раз в сутки. Испражнения жидкие, с обильными примесями слизи, иногда в кале есть кровь или гной. Симптомы дополняются тошнотой и рвотой. При хроническом заболевании 2-5-дневные запоры сменяются несколькими днями диареи и т. д.
Испражнения жидкие, с обильными примесями слизи, иногда в кале есть кровь или гной. Симптомы дополняются тошнотой и рвотой. При хроническом заболевании 2-5-дневные запоры сменяются несколькими днями диареи и т. д.
Общие симптомы энтероколита у детей включают повышенную утомляемость, слабость и сонливость, отказ от еды. Кишечные инфекции проявляются признаками общей интоксикации: лихорадкой, головными болями, ломотой в теле. Если ребенку не проводится лечение хронической патологии, прогрессирующе ухудшается пищеварительная функция, из-за чего у ребенка появляются симптомы нутритивной недостаточности и гиповитаминоза.
Осложнения
При остром энтероколите диарея сопровождается обезвоживанием, которое особенно опасно для детей до 5 лет. Развитие эксикоза тяжелой степени проявляется спутанностью сознания, нарушениями гемодинамики, снижением тургора кожи. Тяжелые формы кишечных инфекций, помимо дегидратации, могут осложняться панкреатитом (13%), гепатитом (11%), поражением чашечно-лоханочной системы почек (9%).
Воспалительный процесс, распространяющийся за пределы слизистого слоя кишки, приводит к изъязвлениям, перфорации и пенетрации стенки. При ускоренной перистальтике возможны острые хирургические состояния: завороты кишечника, инвагинации, которые чаще встречаются в раннем возрасте. Прием некоторых лекарств или попадание токсинов может способствовать формированию мегаколона.
Диагностика
Обнаруженные симптомы энтероколита — основание для постановки педиатром синдромального (топического) диагноза. Дальнейшее обследование с привлечением детского гастроэнтеролога, инфекциониста, иммунолога-аллерголога необходимо для установления причин патологического состояния и постановки клинического диагноза. Ребенку обычно назначаются:
- УЗИ брюшной полости. Ультразвуковая диагностика — простой и неинвазивный метод, который выявляет сонографические симптомы воспаления, структурные и функциональные нарушения ЖКТ. Исследование проводится в качестве скрининга для исключения острых хирургических патологий.

- Рентгенография брюшной полости. Обзорная рентгенограмма информативна в диагностике кишечной непроходимости, инородных тел. Для детальной визуализации структуры слизистой оболочки ЖКТ и оценки моторной функции необходимы рентгенологический снимок с пероральным контрастированием, ирригография.
- Эндоскопические исследования. В практической детской гастроэнтерологии колоноскопию используют при подозрении на кишечный полипоз, неспецифический язвенный колит или болезнь Крона. Современный и безболезненный способ визуализации ЖКТ — видеокапсульная эндоскопия, которая без введения зонда показывает состояние толстой и тонкой кишки на всем их протяжении.
- Анализы кала. В копрограмме при энтероколитах определяются непереваренная клетчатка, капли нейтрального жира, исчерченные мышечные волокна. На симптомы воспаления указывают лейкоциты и слизь. Для подтверждения инфекционного характера болезни делают бактериологическое исследование испражнений.
- Серологические реакции.
 При возможном вирусном происхождении энтероколита и для ускоренного выявления бактериальной инфекции применяют РПГА крови со специфическими диагностикумами. Положительный результат устанавливают при нарастании титров антител в 4 и более раз. Для обнаружения ДНК патогенных микроорганизмов рекомендована ПЦР.
При возможном вирусном происхождении энтероколита и для ускоренного выявления бактериальной инфекции применяют РПГА крови со специфическими диагностикумами. Положительный результат устанавливают при нарастании титров антител в 4 и более раз. Для обнаружения ДНК патогенных микроорганизмов рекомендована ПЦР.
Лечение энтероколита у детей
Диетотерапия
Лечение энтероколита начинается с соответствующей диетотерапии. При остром течении назначается лечебное голодание, слизистые каши и супы, а по мере устранения симптоматики рацион расширяют. Хроническая патология требует щадящей диеты с ограничением экстрактивных веществ, грубой и волокнистой пищи, жирных и высокоуглеводных блюд. Для младенцев до 1 года оставляют привычное грудное вскармливание или питание искусственными смесями.
Консервативная терапия
Если энтероколиту сопутствуют диарея и обезвоживание, необходима адекватная регидратация. При эксикозе легкой степени ребенку дают жидкость через рот каждые 10-15 минут в объеме, который рассчитывается с учетом массы тела. Средняя и тяжелая степень дегидратации, когда пациент отказывается пить самостоятельно, требует внутривенных вливаний солевых растворов. Лекарственное лечение энтероколита подбирается в соответствии с причинами болезни и включает:
Средняя и тяжелая степень дегидратации, когда пациент отказывается пить самостоятельно, требует внутривенных вливаний солевых растворов. Лекарственное лечение энтероколита подбирается в соответствии с причинами болезни и включает:
- Антибактериальные препараты. Используются кишечные антисептики, сульфаниламиды или противопротозойные лекарства. Они подбираются после получения результатов бактериологического исследования и установления возбудителя. Легкие формы инфекционных энтероколитов не требуют назначения антибиотиков.
- Средства для нормализации стула. Хронические запоры являются показанием к введению слабительных свечей или приему системных препаратов, которые размягчают каловые массы, улучшают моторику и облегчают дефекацию. Если медикаментозное лечение неэффективно, ставят клизмы. При жидком стуле рекомендованы противодиарейные лекарства.
- Энтеросорбенты. Лекарства выполняют несколько задач: связывают и выводят из организма токсины и бактерии, ликвидируют газообразование и кишечные колики, уменьшают интенсивность диареи.
 Они применяются независимо от этиологических факторов, когда обнаружены первые диспепсические симптомы.
Они применяются независимо от этиологических факторов, когда обнаружены первые диспепсические симптомы. - Пробиотики. Дисбактериоз может быть причиной или следствием энтероколита, но в любом случае он подлежит медикаментозной коррекции. Лечение включает препараты бифидо- и лактобактерий, которые дополняют пребиотиками для быстрого восстановления кишечной микрофлоры.
- Ферменты. При хроническом энтероколите назначаются панкреатические энзимы, которые улучшают процессы пищеварения в тонкой кишке, нормализуют частоту стула и консистенцию каловых масс. При сопутствующей билиарной патологии эффективны холеретики и холекинетики, минеральные воды.
Хирургическое лечение
Помощь детских хирургов требуется при энтероколите, осложненном перфорацией кишки, перитонитом, кровотечением. Оперативное вмешательство предполагает иссечение дефекта кишечной стенки или удаление части кишки при ее тотальном повреждении, санацию и дренирование брюшной полости, окончательную остановку кровотечения.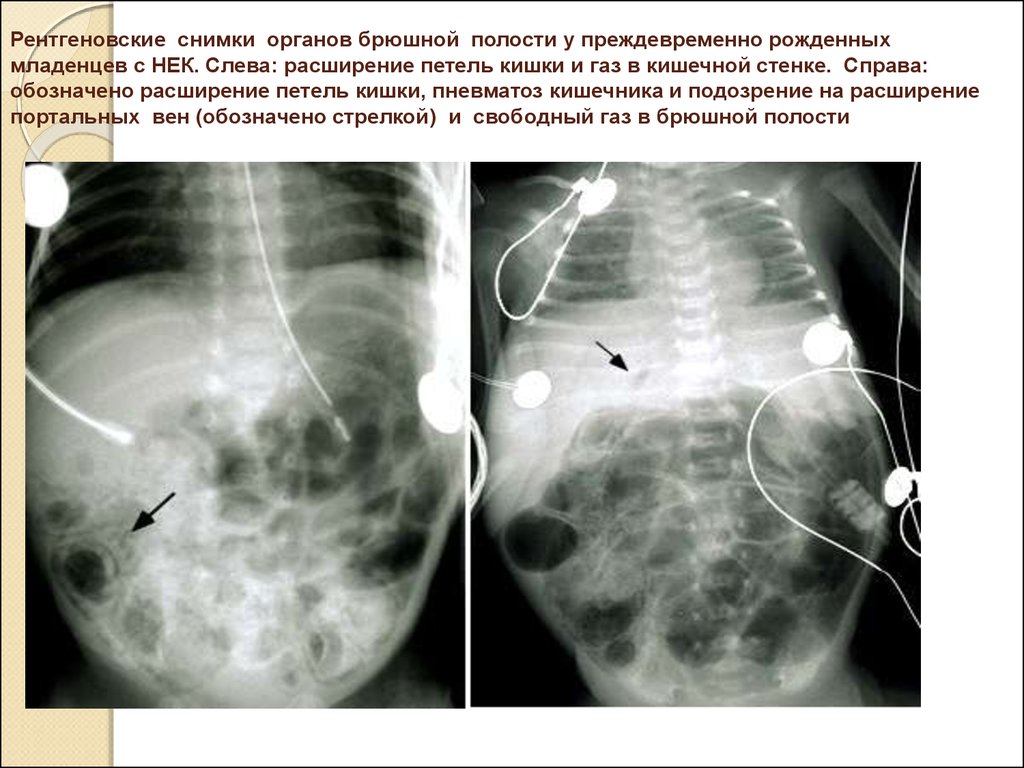 Объем и метод операции подбирается индивидуально соответственно характеру и тяжести состояния.
Объем и метод операции подбирается индивидуально соответственно характеру и тяжести состояния.
Прогноз и профилактика
Адекватное лечение быстро купирует вовремя диагностированный острый инфекционный энтероколит, поэтому он проходит за несколько недель и не оставляет негативных последствий. Хроническое воспаление кишечника чаще встречается у детей, страдающих врожденными аномалиями или сопутствующей патологией. Прогноз зависит от тяжести основного заболевания, степени белково-энергетической недостаточности. При комплексной терапии удается достичь стойкой ремиссии.
Превентивные мероприятия включают привитие ребенку правил личной гигиены и гигиены питания, сбалансированный рацион без вредных продуктов и фастфуда. Недопустимо применение лекарственных средств без назначения и контроля педиатра. Меры вторичной профилактики: своевременное лечение кишечных инфекций и острых состояний, чтобы они не перешли в хроническую форму.
Вы можете поделиться своей историей болезни, что Вам помогло при лечении энтероколита у детей.
Источники
- Гиршпрунг-ассоциированый энтероколит у детей/ Д.А. Морозов, Е.С. Пименова, Г.А. Королев// Вопросы практической педиатрии. – 2019.
- Рациональная профилактика осложнений острых кишечных инфекций в практике педиатра/ Т.А. Руженцова, Н.А. Мешкова// Лечащий врач. – 2019.
- Детские болезни/ Н.П. Шабалов. – 2017.
- Этиопатогенетическая терапия острых кишечных инфекций у детей на современном этапе/ А.А. Новокшонов, В.Ф. Учайкин, Н.В. Соколова // Лечащий врач. – 2010.
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Эозинофильный энтероколит: клиническое наблюдение
БК — болезнь Крона
ВЗК — воспалительные заболевания кишечника
ЖКТ — желудочно-кишечный тракт
МСКТ — мультиспиральная компьютерная томография
ЭК — эозинофильный колит
ЭЭК — эозинофильный энтероколит
IgE — иммуноглобулин Е
Первичные эозинофильные заболевания желудочно-кишечного тракта (ЖКТ) представляют собой редкую патологию пищевода, желудка, тонкой и толстой кишки, характеризующуюся эозинофилией периферической крови и эозинофильными инфильтратами в стенке пищеварительной трубки [1]. Болезнь может поражать один или несколько отделов ЖКТ. Клинические проявления данной патологии зависят от уровня поражения ЖКТ и могут проявляться тошнотой, рвотой, болями в животе, диареей, непроходимостью кишечника, синдромом мальабсорбции, асцитом, снижением массы тела. Выделяют первичный эозинофильный эзофагит, первичный эозинофильный гастрит, первичный эозинофильный энтероколит (ЭЭК)/колит [2]. Впервые данную патологию описал в 1937 г. R. Kaijer. Истинные причины первичного эозинофильного поражения ЖКТ неизвестны, при верификации заболевания необходимо исключить вторичные эозинофилии, которые могут сопровождать паразитарные инвазии, пищевую аллергию на белки (коровье молоко, яйца, соя) [3], гиперэозинофильный синдром, системные заболевания (целиакия, воспалительные заболевания кишечника — ВЗК и др.), прием лекарственных препаратов (нестероидные противовоспалительные препараты, препараты золота, рифампицин, клозапин, сульфасалазин) [4, 5]. Реже причиной эозинофилии могут быть заболевания кожи, тяжелые инфекции, онкогематологическая патология.
Болезнь может поражать один или несколько отделов ЖКТ. Клинические проявления данной патологии зависят от уровня поражения ЖКТ и могут проявляться тошнотой, рвотой, болями в животе, диареей, непроходимостью кишечника, синдромом мальабсорбции, асцитом, снижением массы тела. Выделяют первичный эозинофильный эзофагит, первичный эозинофильный гастрит, первичный эозинофильный энтероколит (ЭЭК)/колит [2]. Впервые данную патологию описал в 1937 г. R. Kaijer. Истинные причины первичного эозинофильного поражения ЖКТ неизвестны, при верификации заболевания необходимо исключить вторичные эозинофилии, которые могут сопровождать паразитарные инвазии, пищевую аллергию на белки (коровье молоко, яйца, соя) [3], гиперэозинофильный синдром, системные заболевания (целиакия, воспалительные заболевания кишечника — ВЗК и др.), прием лекарственных препаратов (нестероидные противовоспалительные препараты, препараты золота, рифампицин, клозапин, сульфасалазин) [4, 5]. Реже причиной эозинофилии могут быть заболевания кожи, тяжелые инфекции, онкогематологическая патология.
Патогенез эозинофильного поражения ЖКТ недостаточно изучен. Дискутируется вопрос о том, являются ли эозинофильные поражения ЖКТ опосредованными иммуноглобулином Е (IgE) заболеваниями. Специфические эозинофильные хемоаттрактанты, такие как интерлейкин-5 и эотоксин, также могут играть роль в их возникновении [6, 7].
Диагностическими критериями эозинофильного поражения ЖКТ служат персистирующая эозинофилия в периферической крови (5—35%), при морфологическом исследовании эозинофильная инфильтрация стенки какого-либо отдела пищеварительной трубки, в кишечнике возможны крипт-абсцессы и лимфонодулярная гиперплазия [8]. Для исключения вторичных эозинофилий проводится анализ кала для выявления гельминтов, серологическая диагностика гельминтозов, проведение кожных проб, элиминационных тестов, определение уровня IgE.
В лечении предлагается использование глюкокортикостероидов [9], антигистаминных препаратов, месалазина [10], ингибиторов лейкотриенов, азатиоприна и биологических методов лечения [5]. Критерием эффективной терапии является уменьшение плотности эозинофильной инфильтрации при морфологическом исследовании биоптатов пораженного участка ЖКТ. Исследователями подчеркивается важность подсчета количества эозинофилов в поле зрения [1, 11].
Критерием эффективной терапии является уменьшение плотности эозинофильной инфильтрации при морфологическом исследовании биоптатов пораженного участка ЖКТ. Исследователями подчеркивается важность подсчета количества эозинофилов в поле зрения [1, 11].
Эозинофильный колит (ЭК) — самая редкая среди эозинофильных заболеваний ЖКТ патология, может встречаться как у детей, так и у взрослых [5]. Наиболее частая причина ЭК у детей — пищевая аллергия на белки, содержащиеся в коровьем молоке, яйцах, сое. Соблюдение диеты приводит к регрессу симптомов в течение нескольких дней. С возрастом симптомы заболевания у детей купируются [12].
Клинические проявления ЭК зависят от глубины инфильтрации эозинофилами стенки пищеварительной трубки. Впервые в 1970 г. N. Klein описал 3 основных типа инфильтрации эозинофилами стенки ЖКТ [13]:
— эозинофильная инфильтрация слизистой оболочки приводит к развитию синдрома мальабсорбции, что может быть причиной железодефицитной анемии, гипоальбуминемии, стеатореи;
— инфильтрация эозинофилами подслизистой основы и мышечной оболочки приводит к полной или частичной непроходимости кишечника;
— инфильтрация эозинофилами серозной оболочки кишечника проявляется асцитом.
Вовлеченность в процесс различных тканей дает возможность понять, что многочисленные клинические формы болезни могут протекать либо с асцитом, либо с непроходимостью кишечника [14].
В связи с небольшим количеством случаев ЭК проспективные рандомизированные контролируемые исследования в отношении данной патологии не проводились, диагностические и терапевтические подходы основаны на клинических наблюдениях. Современная медицина накапливает информацию о данной патологии. В 1985 г. R. Naylor и J. Pollet [15] описали 22 случая ЭК, в которых не выделен общий этиологический фактор, но у некоторых больных имелись указания на пищевую аллергию, реакцию на лекарственные препараты, паразитарною инвазию. Описаны случаи ЭК в пожилом возрасте (женщины 72, 78 и 83 лет). Половые различия не выявляются. Известны случаи ассоциации ЭК со склеродермией, синдромом Черджа—Стросса, гиперэозинофильным синдромом. Описаны наблюдения ЭК у пациентов с ВЗК [16]. Имеется наблюдение ЭК у 29-летней женщины с аллогенной трансплантацией костного мозга, описаны наблюдения ЭК у детей после трансплантации печени, получающих циклоспорин [17, 18]. Обсуждается вопрос о сочетании ЭК с эозинофильной инфильтрацией ЖКТ другой локализации. В клинических наблюдениях описывают случаи изолированного эозинофильного эзофагита, изолированного ЭК, но нет наблюдений сочетаний инфильтрации эозинофилами и пищевода, и толстой кишки у одного пациента. В то же время о сочетании эозинофильной инфильтрации толстой кишки и терминального отдела тонкой кишки известно [19]. Данный факт заслуживает дальнейшего наблюдения.
Обсуждается вопрос о сочетании ЭК с эозинофильной инфильтрацией ЖКТ другой локализации. В клинических наблюдениях описывают случаи изолированного эозинофильного эзофагита, изолированного ЭК, но нет наблюдений сочетаний инфильтрации эозинофилами и пищевода, и толстой кишки у одного пациента. В то же время о сочетании эозинофильной инфильтрации толстой кишки и терминального отдела тонкой кишки известно [19]. Данный факт заслуживает дальнейшего наблюдения.
В Омской областной клинической больнице наблюдали один случай первичного Э.К. Предоставляем его описание.
Больная Ф., 41 год. С 17-летнего возраста отмечает приступы схваткообразной боли в животе, сопровождающейся тошнотой, рвотой, жидким стулом до 5 раз в сутки со слизью. Связи с употреблением определенных продуктов питания, приемом лекарственных препаратов, стрессовыми ситуациями не отмечает. Указанные симптомы появлялись редко, за медицинской помощью не обращалась. В возрасте 25 лет спустя 6 мес после родов (беременность и роды протекали без осложнений) возникли приступ боли в животе, тошнота, многократная обильная рвота, жидкий стул до 5—6 раз в день. При этом стала отмечать увеличение живота в размере. При обследовании выявлен асцит, проведен лапароцентез, эвакуировано 4 л светлой прозрачной жидкости. В общем анализе крови эозинофилия 6—11%, при неоднократных дуоденальных зондированиях и анализах кала паразитарной инвазии не выявлено. При фиброколоноскопии на границе слепой кишки и восходящего отдела ободочной кишки обнаружено полиповидное образование до 15 мм высотой 5 мм с гладкой поверхностью. Биопсия по техническим причинам не проведена.
При этом стала отмечать увеличение живота в размере. При обследовании выявлен асцит, проведен лапароцентез, эвакуировано 4 л светлой прозрачной жидкости. В общем анализе крови эозинофилия 6—11%, при неоднократных дуоденальных зондированиях и анализах кала паразитарной инвазии не выявлено. При фиброколоноскопии на границе слепой кишки и восходящего отдела ободочной кишки обнаружено полиповидное образование до 15 мм высотой 5 мм с гладкой поверхностью. Биопсия по техническим причинам не проведена.
В течение года после лапароцентеза при ультразвуковом контроле в брюшной полости определялась свободная жидкость в небольшом количестве. При диагностической лапароскопии патологии не выявлено. В гемограмме сохранялась эозинофилия до 18%. Пациентка чувствовала себя удовлетворительно. В течение последних 7 лет боль и диспепсические явления не возобновлялись.
В конце сентября 2013 г. вновь появилась приступообразная боль в эпигастрии, правом и левом подреберьях, многократная рвота пищей, жидкий стул до 5—6 раз в сутки. Госпитализирована в ОКБ 25.09.13 для уточнения диагноза, лечения.
Госпитализирована в ОКБ 25.09.13 для уточнения диагноза, лечения.
При расспросе дополнительных жалоб не предъявляла.
Особенности анамнеза жизни: у матери рак прямой кишки, эпидемиологический анамнез: употребляет в пищу рыбу Обь-Иртышского бассейна.
При объективном исследовании индекс массы тела 34. Кожа и слизистые оболочки обычной окраски. Лимфатические узлы, щитовидная железа не изменены. Периферических отеков нет. Над легкими при перкуссии звук легочной. Дыхание везикулярное, хрипов нет. Границы сердца в пределах нормы. Тоны сердца ритмичные, приглушены. Пульс ритмичный, с частотой 70 уд/мин. Артериальное давление 120/80 мм рт.ст. Язык влажный. Живот мягкий, болезненный в проекции толстой кишки (в подвздошных областях) и в эпигастральной области. Печень, селезенка, почки не увеличены.
В ходе обследования выявлены повышение уровня эозинофилов до 18—27%, небольшое увеличение активности панкреатической амилазы. Функциональные пробы печени, общий анализ мочи без изменений. Общий белок крови незначительно снижен, уровень альбуминов в пределах нормы. Результаты иммуноферментного анализа на ВИЧ и маркеры вирусных гепатитов В и С отрицательные.
Общий белок крови незначительно снижен, уровень альбуминов в пределах нормы. Результаты иммуноферментного анализа на ВИЧ и маркеры вирусных гепатитов В и С отрицательные.
При ирригоскопии (рис. 1) получены данные, свидетельствующие об объемном образовании илеоцекального угла: тугое наполнение с контрастированием просвета червеобразного отростка, циркулярное сужение в области слепой кишки на уровне баугиниевой заслонки.
Рис. 1. Результаты ирригоскопии.
По данным ультразвукового исследования органов брюшной полости обнаружены асцит, диффузные изменения в поджелудочной железе.
При мультиспиральной компьютерной томографии (МСКТ) органов брюшной полости (рис. 2) выявлено неоднородное образование в правой подвздошной области, муфтообразно охватывающее подвздошную кишку.
Рис. 2. Данные МСКТ с внутривенным болюсным контрастированием, венозная фаза. Аксиальные срезы. а — инфильтрат в области слепой кишки на уровне илиоцекального перехода, стенки кишки неравномерно утолщены с умеренным неоднородным накоплением контрастного препарата; б — периколитическое скопление жидкости выше по ходу восходящей толстой кишки, асцит.
При фиброколоноскопии в области слепой и восходящей ободочной кишки определяется ярко-красная циркулярная инфильтрация в виде валика. При гистологическом исследовании биоптата, взятого из участка инфильтрации, — признаки неспецифического воспаления (слабая лимфо- и плазмоцитарная инфильтрация с примесью единичных полиморфно-ядерных лейкоцитов).
В связи с наблюдающимися эпизодами абдоминальной боли с симптомами непроходимости кишечника выполнен обзорный снимок органов брюшной полости (рис. 3). Выявлены множественные куполообразные просветления (чаши Клойбера).
Рис. 3. Обзорный снимок органов брюшной полости. Множественные куполообразные просветления (чаши Клойбера).
С учетом полученных данных дифференциальный диагноз проводили между болезнью Крона (БК) и злокачественным образованием кишечника. Основанием для предположения БК послужили илеоцекальная локализация процесса, наличие инфильтрата, стриктур, признаков непроходимости кишечника.
Предпринята лапаротомия 17. 10.13: эвакуировано 1500 мл асцитической жидкости; при ревизии выявлены утолщение, инфильтрация стенки тонкой кишки, отек висцеральной брюшины (рис. 4). На расстоянии 10, 20 и 35 см от илеоцекального угла обнаружены три формирующиеся стриктуры, в просвете слепой кишки — инфильтрированная, увеличенная до 5 см баугиниевая заслонка. Выполнена резекция тонкой кишки на расстоянии 50 см от илеоцекального угла и средней трети восходящей кишки, наложен илеоасцендоанастомоз бок в бок.
10.13: эвакуировано 1500 мл асцитической жидкости; при ревизии выявлены утолщение, инфильтрация стенки тонкой кишки, отек висцеральной брюшины (рис. 4). На расстоянии 10, 20 и 35 см от илеоцекального угла обнаружены три формирующиеся стриктуры, в просвете слепой кишки — инфильтрированная, увеличенная до 5 см баугиниевая заслонка. Выполнена резекция тонкой кишки на расстоянии 50 см от илеоцекального угла и средней трети восходящей кишки, наложен илеоасцендоанастомоз бок в бок.
Рис. 4. Макропрепарат резецированной части подвздошной кишки. Утолщение стенки тонкой кишки до 8 мм. Серозная оболочка шероховатая, с инъецированными сосудами.
При гистологическом исследовании в стенке резецированной части кишки (рис. 5) — клеточная инфильтрация с большим количеством эозинофильных лейкоцитов.
Рис. 5. Микропрепараты стенки резецированной части кишки. Окраска гемотоксилином и эозином. а — слизистая оболочка толстой кишки: в собственной пластинке между двух крипт обычное количество клеточных элементов с увеличением количества эозинофильных лейкоцитов (12%), ув. 400; б — мышечная оболочка тонкой и толстой кишки с густым инфильтратом, состоящим сплошь из эозинофильных лейкоцитов, ув. 100; в — подслизистая основа толстой кишки (эозинофильные лейкоциты 91,4%), ув. 400.
400; б — мышечная оболочка тонкой и толстой кишки с густым инфильтратом, состоящим сплошь из эозинофильных лейкоцитов, ув. 100; в — подслизистая основа толстой кишки (эозинофильные лейкоциты 91,4%), ув. 400.
На основании персистирующей эозинофилии в периферической крови в течение длительного периода, а также инфильтрации стенок подвздошной и слепой кишки эозинофилами установлен диагноз: ЭЭК с формированием стриктур в подвздошной кишке, асцит. Операция 17.10.13: резекция подвздошной кишки и илеоцекального угла, илеоасцендоанастомоз бок в бок. Сопутствующая патология органов пищеварения: хронический токсико-метаболический панкреатит, обострение.
Послеоперационный период протекал благополучно, проводилась терапия антисекреторными препаратами (рабепразол, омепразол), ферментами (панкреатин), спазмолитиками, антибактериальными препаратами, в последующем антигистаминными препаратами и преднизолоном.
Во время последней госпитализации (январь 2014 г.) проведено дополнительное обследование с целью исключения паразитарных инвазий и аллергических заболеваний. Аллергологический анализ крови показал повышение общего уровня IgЕ (137,25 МЕ/мл при норме <130 МЕ/мл). Инфекционно-иммунологический анализ крови позволил выявить повышенный титр IgG к аспергиллам 1/200. При этом антитела IgG к аскаридам, трихинеллам, описторхам и лямблиям не обнаружены. Уровень кальпротектина в кале соответствовал норме (24,15 мг/кг при норме <50 мг/кг). Поводилось исследование кала сверхчувствительным комплексным методом на яйца гельминтов следующих видов: Strongiloideus stercoralis, Hymenolepis nana, Opistorchis filineus, Trichocepalus triciurus, Askaris lumbrikoides, Clonorchis sinensis, Methagonimus jokogowai, Nanophyetus salmincoli, Dipylioobotrium latum, Dicrocoelium lanceatum, Fasciola hepatica, а также на цисты Lamblia intestinalis, Entamoeba histolitica, Blastocystis hominis, онкосферы тениид. Результаты всех исследований отрицательные. Подтверждением правильно установленного диагноза и правильной стратегии медикаментозной терапии является постоянный уровень эозинофилов в периферической крови, не превышающий 1—2%.
Аллергологический анализ крови показал повышение общего уровня IgЕ (137,25 МЕ/мл при норме <130 МЕ/мл). Инфекционно-иммунологический анализ крови позволил выявить повышенный титр IgG к аспергиллам 1/200. При этом антитела IgG к аскаридам, трихинеллам, описторхам и лямблиям не обнаружены. Уровень кальпротектина в кале соответствовал норме (24,15 мг/кг при норме <50 мг/кг). Поводилось исследование кала сверхчувствительным комплексным методом на яйца гельминтов следующих видов: Strongiloideus stercoralis, Hymenolepis nana, Opistorchis filineus, Trichocepalus triciurus, Askaris lumbrikoides, Clonorchis sinensis, Methagonimus jokogowai, Nanophyetus salmincoli, Dipylioobotrium latum, Dicrocoelium lanceatum, Fasciola hepatica, а также на цисты Lamblia intestinalis, Entamoeba histolitica, Blastocystis hominis, онкосферы тениид. Результаты всех исследований отрицательные. Подтверждением правильно установленного диагноза и правильной стратегии медикаментозной терапии является постоянный уровень эозинофилов в периферической крови, не превышающий 1—2%.
В последующем продолжено лечение месалазином, преднизолоном, кетотифеном, ферментными препаратами. Наблюдается амбулаторно, состояние удовлетворительное.
Проявления заболевания у пациентки укладываются в клиническую картину первичного ЭЭК, описанную в литературе. Рассматривается случай, когда в воспалительный процесс вовлечена брюшина, что и явилось причиной асцита. Распространение инфильтрации в подслизистую основу и мышечный слой привело к формированию стриктур подвздошной кишки. Локализация патологического процесса — терминальный отдел подвздошной кишки и слепая кишка, образование стриктур, наличие инфильтрата слепой кишки характерны и для Б.К. Однако отсутствие изменений слизистой в виде глубоких язв, рубцовой деформации и результаты гистологического исследования позволили исключить Б.К. Вторичные эозинофилии в процессе обследования не получили подтверждения.
Наше наблюдение дополняет немногочисленные описания случаев ЭЭК. При проведении дифференциальной диагностики заболеваний кишечника врач не должен забывать и о такой редкой патологии, как ЭЭК.
Некротизирующий энтероколит (НЭК) – проблемы со здоровьем у детей
By
William J. Cochran
, доктор медицины, клиника Geisinger
Полный обзор/редакция, август 2021 г. | Изменено в сентябре 2022 г.
ПОСМОТРЕТЬ ПРОФЕССИОНАЛЬНУЮ ВЕРСИЮ
ПОЛУЧИТЕ БЫСТРЫЕ ФАКТЫ
Некротизирующий энтероколит — поражение внутренней поверхности кишечника. Это расстройство чаще всего встречается у недоношенных и/или тяжелобольных новорожденных.
Живот может быть вздут, стул может быть с примесью крови, а новорожденный может срыгивать жидкостью зеленоватого, желтого или цвета ржавчины и казаться очень больным и вялым.
Диагноз подтверждается рентгенографией брюшной полости.
Около 70–80% новорожденных с этим заболеванием выживают.
Лечение включает прекращение кормления, введение в желудок аспирационной трубки для удаления содержимого желудка и снижения давления, а также внутривенное введение антибиотиков и жидкостей.
В тяжелых случаях требуется операция по удалению поврежденного кишечника.
Более 90% случаев некротизирующего энтероколита приходится на недоношенных новорожденных Недоношенные (недоношенные) новорожденные Недоношенным новорожденным считается ребенок, родившийся до 37 недель гестации. В зависимости от того, когда они родились, недоношенные новорожденные имеют недоразвитые органы, которые могут быть не готовы функционировать за пределами… Common.TooltipReadMore. Некротизирующий энтероколит может возникать кластерами или в виде вспышек в отделениях интенсивной терапии новорожденных (ОИТН). Иногда эти вспышки могут быть связаны с конкретными бактериями (такими как кишечная палочка 9). 0042 Escherichia coli Инфекции Escherichia coli ( E. coli ) представляет собой группу грамотрицательных бактерий, которые обычно обитают в кишечнике здоровых людей, но некоторые штаммы могут вызывать инфекции в пищеварительном тракте… Common.TooltipReadMore ) , но часто причина неизвестна.
0042 Escherichia coli Инфекции Escherichia coli ( E. coli ) представляет собой группу грамотрицательных бактерий, которые обычно обитают в кишечнике здоровых людей, но некоторые штаммы могут вызывать инфекции в пищеварительном тракте… Common.TooltipReadMore ) , но часто причина неизвестна.
Причина некротизирующего энтероколита до конца не выяснена, но частично она связана с незрелостью кишечника наряду с низким уровнем кислорода в крови и/или уменьшением притока крови к кишечнику. Снижение притока крови к кишечнику у больного недоношенного новорожденного может привести к повреждению внутренней поверхности кишечника. Травма позволяет бактериям, которые обычно существуют в кишечнике, вторгаться в поврежденную стенку кишечника, а затем попадать в кровоток новорожденного, вызывая инфекцию (сепсис Сепсис у новорожденных Сепсис — это серьезная общечеловеческая реакция на инфекцию, распространяющуюся через кровь. Новорожденные с сепсисом обычно выглядят больными— они вялые, плохо питаются, часто имеют серую окраску и могут иметь. .. Common.TooltipReadMore ), а иногда и смерть. При прогрессировании травмы на всю толщину стенки кишечника и разрывах стенки кишечника (перфорациях) Перфорации пищеварительного тракта Любой из полых органов пищеварения может стать перфорированным (проколотым), что вызывает выход желудочно-кишечного содержимого и может привести к сепсису (опасная для жизни инфекция кровотока)… Common.TooltipReadMore, кишечное содержимое просачивается в брюшную полость и вызывает воспаление и, как правило, инфицирование брюшной полости и ее слизистой оболочки (перитонит Перитонит Боль в животе распространена и часто незначительна. Тяжелая абдоминальная Однако быстро возникающая боль почти всегда указывает на серьезную проблему. Боль может быть единственным признаком необходимости операции… Common.TooltipReadMore ).
.. Common.TooltipReadMore ), а иногда и смерть. При прогрессировании травмы на всю толщину стенки кишечника и разрывах стенки кишечника (перфорациях) Перфорации пищеварительного тракта Любой из полых органов пищеварения может стать перфорированным (проколотым), что вызывает выход желудочно-кишечного содержимого и может привести к сепсису (опасная для жизни инфекция кровотока)… Common.TooltipReadMore, кишечное содержимое просачивается в брюшную полость и вызывает воспаление и, как правило, инфицирование брюшной полости и ее слизистой оболочки (перитонит Перитонит Боль в животе распространена и часто незначительна. Тяжелая абдоминальная Однако быстро возникающая боль почти всегда указывает на серьезную проблему. Боль может быть единственным признаком необходимости операции… Common.TooltipReadMore ).
В дополнение к недоношенным (недоношенным) новорожденным Недоношенным новорожденным считается ребенок, родившийся до 37 недель беременности. В зависимости от того, когда они рождаются, недоношенные новорожденные имеют недоразвитые органы, которые могут быть не готовы функционировать за пределами. .. Common.TooltipReadMore, другие факторы риска включают
.. Common.TooltipReadMore, другие факторы риска включают
Предродовой разрыв плодных оболочек Предродовой разрыв плодных оболочек (PROM) Предродовой разрыв плодных оболочек – это подтекание амниотической жидкости вокруг плода в любое время до начала родов. После разрыва плодных оболочек часто вскоре следуют роды. Если роды продолжаются… Common.TooltipReadMore (воды у матери отходят более чем за 12 часов до начала родов): подтекание амниотической жидкости может привести к инфицированию плода.
Поражение бактерий, живущих в пищеварительной системе: Лечение антибиотиками или кислотоподавляющими препаратами может стимулировать рост потенциально вредных бактерий, которые могут проникнуть в кишечник.
Перинатальная асфиксия Перинатальная асфиксия Родовая травма – это повреждение, возникающее в результате физического давления в процессе родов, обычно при прохождении через родовые пути. Многие новорожденные получают незначительные травмы во время родов.
 .. Общее.ПодсказкаПодробнее: Это расстройство связано с уменьшением притока крови к тканям новорожденного или уменьшением содержания кислорода в крови новорожденного до, во время или сразу после родов.
.. Общее.ПодсказкаПодробнее: Это расстройство связано с уменьшением притока крови к тканям новорожденного или уменьшением содержания кислорода в крови новорожденного до, во время или сразу после родов.Заболевание сердца, присутствующее при рождении Обзор пороков сердца Примерно один из 100 детей рождается с пороком сердца. Некоторые из них серьезны, но многие нет. Дефекты могут включать аномальное формирование стенок или клапанов сердца или кровеносных сосудов, которые впадают в… Common.TooltipПодробнее (врожденный порок сердца): врожденные дефекты сердца могут влиять на то, как течет кровь, или влиять на уровень кислорода в крови. .
Анемия Анемия у новорожденных Анемия — это заболевание, при котором в крови содержится слишком мало эритроцитов. Анемия может возникнуть, когда эритроциты разрушаются слишком быстро, теряется слишком много крови или костный мозг… Common.TooltipReadMore (низкое количество эритроцитов): при анемии кровь новорожденного может быть затруднена.
2007/96/3_23b.png) иметь достаточный запас кислорода.
иметь достаточный запас кислорода.Обменные переливания Обменные переливания Желтуха — это пожелтение кожи и/или глаз, вызванное повышением уровня билирубина в кровотоке. Билирубин представляет собой желтое вещество, образующееся, когда гемоглобин (часть красных кровяных возраст Малый вес для гестационного возраста (SGA) Новорожденные Новорожденный с массой тела менее 9 г.0% новорожденных того же гестационного возраста при рождении (ниже 10-го процентиля) считаются маленькими для гестационного возраста. Новорожденные могут быть маленькими, потому что их родители… Common.TooltipReadMore (SGA)
Кормление смесью: Грудное молоко содержит вещества, помогающие защитить стенки пищеварительного тракта, которых нет в смесях.
У новорожденных с некротизирующим энтероколитом может развиться вздутие живота и трудности с кормлением. У них может быть рвота с примесью крови, жидкостью с зеленым или желтым оттенком, а в стуле может быть видна кровь. Эти новорожденные вскоре кажутся очень больными и вялыми (вялыми), у них низкая температура тела и повторяющиеся паузы дыхания (апноэ).
Эти новорожденные вскоре кажутся очень больными и вялыми (вялыми), у них низкая температура тела и повторяющиеся паузы дыхания (апноэ).
Диагноз некротизирующего энтероколита подтверждается рентгенографией брюшной полости Простые рентгеновские лучи Рентгеновские лучи представляют собой высокоэнергетические волны излучения, которые могут проникать в большинство веществ (в разной степени). В очень малых дозах рентгеновские лучи используются для получения изображений, которые помогают врачам диагностировать заболевание. При высоком… Common.TooltipReadMore, которые показывают газ в стенке кишечника (так называемый пневматоз кишечника) или наличие свободного воздуха в брюшной полости, если стенка кишечника перфорирована. Врачи также могут провести УЗИ брюшной полости, чтобы оценить толщину стенки кишечника, пневматоз кишечника и кровоток.
Образцы крови берутся для выявления бактерий и других аномалий (например, повышенное количество лейкоцитов).
Современные медикаментозные и хирургические методы лечения улучшили прогноз для новорожденных с некротизирующим энтероколитом. Около 70–80% пораженных новорожденных выживают.
Около 70–80% пораженных новорожденных выживают.
Сужение кишечника (кишечная стриктура) является наиболее частым долговременным осложнением. Стриктуры возникают у 10–36% новорожденных, переживших начальный эпизод некротизирующего энтероколита. Стриктуры обычно вызывают симптомы через 2–3 месяца после эпизода некротизирующего энтероколита. Иногда стриктуры необходимо исправлять хирургическим путем.
Кормление недоношенных новорожденных грудным молоком матери Грудное вскармливание Грудное молоко является идеальной пищей для новорожденных. Хотя младенцев можно кормить грудным молоком или смесью, Всемирная организация здравоохранения (ВОЗ) и Американская академия педиатрии (AAP) рекомендуют исключительно… Common.TooltipReadMore, а не смесь, по-видимому, обеспечивает некоторую защиту от некротизирующего энтероколита. Кроме того, персонал больницы избегает давать младенцу высококонцентрированную смесь и принимает меры для предотвращения низкого уровня кислорода в крови младенца. По возможности также следует избегать антибиотиков и кислотоподавляющих препаратов.
По возможности также следует избегать антибиотиков и кислотоподавляющих препаратов.
Есть некоторые доказательства того, что пробиотики (хорошие бактерии) могут быть полезны для профилактики, но эта терапия все еще находится в экспериментальной стадии.
Беременным женщинам с риском преждевременных родов могут быть назначены кортикостероиды для предотвращения некротизирующего энтероколита.
Новорожденные с некротизирующим энтероколитом остаются в стационаре и лечатся в отделении интенсивной терапии новорожденных (ОИТН) Отделение интенсивной терапии новорожденных (ОИТН) Проблемы у новорожденных могут развиться До рождения, пока плод растет Во время родов После родов Около 9% новорожденных нуждаются в особом уходе после рождения из-за недоношенности, проблем… Common.TooltipReadMore .
Кормление прекращают у новорожденных с некротизирующим энтероколитом. В желудок новорожденного вводят отсасывающую трубку для удаления его содержимого, что снижает давление и помогает предотвратить рвоту.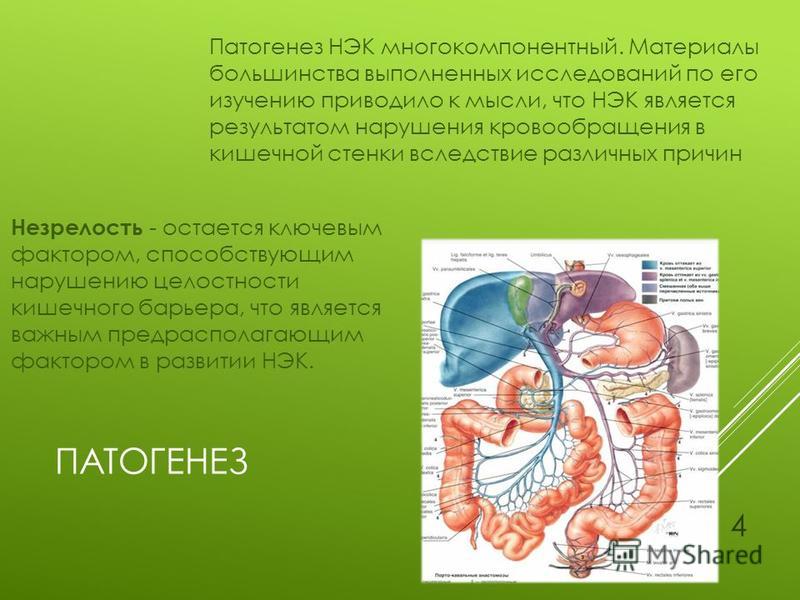 Питание и жидкости вводятся внутривенно для поддержания гидратации и питания, а также для заживления кишечника. Антибиотики вводят внутривенно для лечения инфекции.
Питание и жидкости вводятся внутривенно для поддержания гидратации и питания, а также для заживления кишечника. Антибиотики вводят внутривенно для лечения инфекции.
Более 75% новорожденных с некротизирующим энтероколитом не нуждаются в хирургическом вмешательстве. Тем не менее, операция необходима, если есть перфорация кишечника или сильно поражена часть кишечника. Операция включает удаление части кишечника, в которую не поступает достаточно крови. Концы здоровой кишки выводят на поверхность кожи, чтобы создать временное отверстие для дренирования кишечника (остомия). Позже, когда ребенок здоров, концы кишечника пришивают и кишку возвращают в брюшную полость.
Очень маленьким (около 1 фунта или менее или менее 600 г) или тяжелобольным младенцам, которые могут не пережить более обширную операцию, врачи могут установить перитонеальные дренажи в брюшную полость. Перитонеальные дренажи позволяют инфицированному материалу в брюшной полости вытекать из организма и могут уменьшить симптомы. Процедура помогает стабилизировать этих младенцев, чтобы операцию можно было провести в более позднее время, когда они будут в менее критическом состоянии. В некоторых случаях младенцы выздоравливают без дополнительной операции.
Процедура помогает стабилизировать этих младенцев, чтобы операцию можно было провести в более позднее время, когда они будут в менее критическом состоянии. В некоторых случаях младенцы выздоравливают без дополнительной операции.
ПРИМЕЧАНИЕ:
Это потребительская версия.
ВРАЧИ:
ПОСМОТРЕТЬ ПРОФЕССИОНАЛЬНУЮ ВЕРСИЮ
ПОСМОТРЕТЬ ПРОФЕССИОНАЛЬНУЮ ВЕРСИЮ
Авторские права © 2023 Merck & Co., Inc., Рэуэй, Нью-Джерси, США и ее филиалы. Все права защищены.
Проверьте свои знания
Пройди тест!
Некротический энтероколит — familydoctor.org
Что такое некротический энтероколит?
Некротизирующий энтероколит (НЭК) — кишечное заболевание. Кишечная ткань воспаляется, а затем отмирает. Встречается в основном у недоношенных и больных новорожденных. Это часто начинается в течение 2 недель после рождения, когда ребенок все еще находится в больнице.
Это часто начинается в течение 2 недель после рождения, когда ребенок все еще находится в больнице.
Симптомы некротического энтероколита
Симптомы НЭК могут появиться внезапно или со временем. Общие симптомы включают:
- Вздутие живота
- Боль в животе
- Кровавый стул
- Изменение количества или времени стула
- Диарея
- Рвота
- Проблемы с подачей
- Пониженная энергия
- Изменение температуры тела
- Неравномерное дыхание, частота сердечных сокращений или кровяное давление
Что вызывает некротический энтероколит?
Точной причины НЭК нет. Основным источником являются кишечные бактерии. Если ваш ребенок недоношен, его иммунная система и пищеварительная система слабее. Другим триггером может быть снижение поступления крови или кислорода в кишечник. Это может повредить ткани и привести к НЭК. Доношенные дети с врожденным пороком сердца также могут заболеть НЭК.
Как диагностируется некротизирующий энтероколит?
Ваш врач может диагностировать НЭК. Они проведут медицинский осмотр, чтобы проверить наличие симптомов. Скорее всего, они сделают рентген желудка, чтобы проверить наличие воспаления или воздуха в кишечнике вашего ребенка. Лабораторные анализы, такие как кровь, моча и кал, также вероятны. Эти тесты могут определить тяжесть состояния.
Можно ли предотвратить или избежать некротического энтероколита?
Трудно предотвратить или избежать НЭК. Однако существуют факторы, которые могут увеличить риск НЭК у вашего ребенка, в том числе:
- Преждевременные роды
- Болезнь
- Переливание крови
- Смесь вместо грудного молока
- Воздействие вспышки
- Длительное воздействие антибиотиков
Лечение некротического энтероколита
Доступен ряд вариантов лечения НЭК. Для начала ваш врач захочет дать кишечнику вашего ребенка отдохнуть. Вместо обычного кормления они будут получать питание через внутривенную трубку. Вашему врачу может потребоваться уменьшить газообразование в кишечнике вашего ребенка. Это делается путем введения трубки в желудок. Антибиотики лечат инфекцию. Вашему ребенку, возможно, потребуется использовать дыхательный аппарат, если дыхание станет затрудненным. В тяжелых случаях НЭК может потребоваться экстренное хирургическое вмешательство. Это если ослабленная инфицированная ткань создает отверстие в кишечнике. Хирург удалит мертвую ткань и восстановит кишечник и кишечник.
Вместо обычного кормления они будут получать питание через внутривенную трубку. Вашему врачу может потребоваться уменьшить газообразование в кишечнике вашего ребенка. Это делается путем введения трубки в желудок. Антибиотики лечат инфекцию. Вашему ребенку, возможно, потребуется использовать дыхательный аппарат, если дыхание станет затрудненным. В тяжелых случаях НЭК может потребоваться экстренное хирургическое вмешательство. Это если ослабленная инфицированная ткань создает отверстие в кишечнике. Хирург удалит мертвую ткань и восстановит кишечник и кишечник.
Жизнь с некротизирующим энтероколитом
Младенцы с НЭК нуждаются в лечении и постоянном наблюдении. NEC можно вылечить, и он практически не имеет длительного эффекта. У некоторых детей могут быть проблемы в будущем. Это включает кишечник или пищеварительный тракт. У них может быть закупорка, вызванная аномальной кишечной тканью или рубцовой тканью. Другая проблема называется синдромом короткой кишки или короткой кишки.
