Аг при беременности: Беременность и артериальная гипертензия
Принципы лечения артериальной гипертонии при беременности | Кирсанова Т.В., Михайлова О.И.
Артериальная гипертония (АГ) у беременных в настоящее время является одной из наиболее распространенных форм патологии во время гестации и во многих экономически развитых странах по–прежнему остается основной причиной как материнской, так и перинатальной заболеваемости и летальности, а также ряда акушерских осложнений. В России АГ встречается у 5–30% беременных, и на протяжении последних десятилетий отмечается тенденция к увеличению этого показателя. По данным ВОЗ, в структуре материнской смертности доля гипертензивного синдрома составляет 20–30%, ежегодно во всем мире более 50 тыс. женщин погибают в период беременности из–за осложнений, связанных с АГ [1,4,6].
АГ увеличивает риск отслойки нормально расположенной плаценты, массивных коагулопатических кровотечений в результате отслойки плаценты, а также может быть причиной эклампсии, нарушения мозгового кровообращения, отслойки сетчатки [1,12].
В последнее время отмечено увеличение распространенности АГ во время беременности за счет ее хронических форм на фоне роста числа пациенток с ожирением, сахарным диабетом и в связи с увеличением возраста беременных. И наоборот – женщины, у которых развиваются гипертензивные расстройства в период беременности, в дальнейшем относятся к группе риска по развитию ожирения, сахарного диабета, сердечно–сосудистых заболеваний. Дети этих женщин имеют повышенный риск развития различных метаболических и гормональных нарушений, сердечно–сосудистой патологии [1,4].
Критериями для диагностики АГ при беременности, по данным ВОЗ, являются уровень систолического АД (САД) 140 мм рт.ст. и более или диастолического АД (ДАД) 90 мм рт.ст. и более либо увеличение САД на 25 мм рт.ст. и более или ДАД на 15 мм рт. ст. по сравнению с уровнями АД до беременности или в I триместре беременности. Следует отметить, что при физиологически протекающей беременности в I и II триместрах возникает физиологическое снижение АД, обусловленное гормональной вазодилатацией, в III триместре АД возвращается к обычному индивидуальному уровню или может немного превышать его [1,6,8].
Выделяют следующие 4 формы АГ у беременных.
• Хроническая АГ (это гипертоническая болезнь или вторичная (симптоматическая) гипертония, диагностированная до наступления беременности или до 20 нед.).
• Гестационная АГ (повышение уровня АД, впервые зафиксированное после 20 нед. беременности и не сопровождающееся протеинурией). В большинстве рекомендаций для уточнения формы АГ и представления о дальнейшем прогнозе предлагается наблюдение как минимум в течение 12 нед. после родов.
• Преэклампсия/эклампсия (ПЭ) (специфичный для беременности синдром, который возникает после 20–й нед. беременности, определяется по наличию АГ и протеинурии (более 300 мг белка в суточной моче). При этом наличие отеков не является диагностическим критерием ПЭ, т.к. при физиологически протекающей беременности их частота достигает 60%.
Эклампсию диагностируют в случае возникновения у женщин с ПЭ судорог, которые не могут быть объяснены другими причинами.
• Преэклампсия/эклампсия на фоне хронической АГ:
а) появление после 20 нед. беременности протеинурии впервые (0,3 г белка и более в суточной моче) или заметное увеличение ранее имевшейся протеинурии;
беременности протеинурии впервые (0,3 г белка и более в суточной моче) или заметное увеличение ранее имевшейся протеинурии;
б) прогрессирование АГ у тех женщин, у которых до 20 нед. беременности АД легко контролировалось;
в) появление после 20 нед. признаков полиорганной недостаточности.
По степени повышения уровня АД у беременных различают умеренную АГ (при САД 140–159 мм рт.ст. и/или ДАД 90–109 мм рт.ст.) и тяжелую АГ (при САД >160 и/или ДАД>110 мм рт.ст.). Выделение двух степеней АГ при беременности имеет принципиальное значение для оценки прогноза и выбора тактики ведения пациенток. Тяжелая АГ беременных ассоциируется с высоким риском развития инсульта. Инсульты у женщин одинаково часто развиваются как во время родов, так и в раннем послеродовом периоде и в 90% случаев являются геморрагическими, ишемические инсульты встречаются крайне редко. Повышение САД имеет большее по сравнению с ДАД значение в развитии инсульта. Отмечено, что у тех женщин, у которых в период беременности, родов или вскоре после родоразрешения развился инсульт, в 100% случаев значения САД составляли 155 мм рт. ст. и выше, в 95,8% случаев – 160 мм рт.ст. и выше. Повышение ДАД до 110 мм рт.ст. и выше наблюдалось только у 12,5% пациенток, перенесших инсульт [4,8,9].
ст. и выше, в 95,8% случаев – 160 мм рт.ст. и выше. Повышение ДАД до 110 мм рт.ст. и выше наблюдалось только у 12,5% пациенток, перенесших инсульт [4,8,9].
Оптимальным уровнем АД являются цифры ниже 150/95 мм рт.ст. В послеродовом периоде пациентка нуждается в дополнительном обследовании с целью выявления этиологии АГ и оценки состояния органов–мишеней. По истечении 12 нед. после родов диагноз гестационной АГ при сохраняющейся АГ должен быть изменен на «гипертоническая болезнь» или один из возможных вариантов диагноза вторичной (симптоматической) АГ. В случаях самопроизвольной нормализации уровня АД в срок до 12 нед. после родов ретроспективно устанавливается диагноз транзиторной АГ. Существуют данные о том, что восстановительный период после родов у большинства женщин, перенесших гестационную АГ и ПЭ, независимо от тяжести АГ, протекает достаточно длительно. Через 1 мес. после родов только 43% из числа этих пациенток имеют нормальный уровень АД, и даже через 6 мес. у половины женщин уровень АД остается повышенным. Через 3 мес. (12 нед.) наблюдения после родов 25% женщин, перенесших ПЭ, еще имеют АГ, через 2 года у 40% пациенток из их числа отмечается нормализация уровня АД [1,4,9].
Через 3 мес. (12 нед.) наблюдения после родов 25% женщин, перенесших ПЭ, еще имеют АГ, через 2 года у 40% пациенток из их числа отмечается нормализация уровня АД [1,4,9].
После выявления АГ у беременной следует обследовать пациентку с целью уточнения происхождения гипертензивного синдрома, определения тяжести АГ, выявления сопутствующих органных нарушений, включая состояние органов–мишеней, плаценты и плода.
В план обследования при АГ входят:
– консультации: терапевта (кардиолога), невролога, офтальмолога, эндокринолога;
– инструментальные исследования: электрокардиография, эхокардиография, суточное мониторирование АД, ультразвуковое исследование почек, ультразвуковая допплерометрия сосудов почек;
– лабораторные исследования: общий анализ крови, общий анализ мочи, биохимический анализ крови (с липидным спектром), микроальбуминурия (МАУ).
Если диагноз не был уточнен на этапе планирования беременности, необходимо проведение дополнительных обследований с целью исключения вторичного характера АГ. Если полученные данные достаточны для уточнения диагноза, исключения вторичных АГ, и на их основании возможно четко определить группу риска пациентки в соответствии с критериями стратификации, применяемыми при хронической АГ, а следовательно, и тактику ведения беременной, то на этом обследование может быть закончено.
Если полученные данные достаточны для уточнения диагноза, исключения вторичных АГ, и на их основании возможно четко определить группу риска пациентки в соответствии с критериями стратификации, применяемыми при хронической АГ, а следовательно, и тактику ведения беременной, то на этом обследование может быть закончено.
Второй этап предполагает использование дополнительных методов обследования для уточнения формы вторичной АГ при наличии таковой либо для выявления возможных сопутствующих заболеваний [6,8].
Одной из наиболее сложных задач при терапии АГ является выбор фармакологического препарата. При лечении АГ у беременных часто рассматриваются антигипертензивные средства, практически утратившие свое клиническое значение у других категорий пациентов с АГ. По этическим причинам проведение рандомизированных клинических исследований лекарственных средств у беременных ограничено, сведения об эффективности и безопасности большинства новых препаратов для лечения АГ практически отсутствуют. Основными лекарственными средствами, оправдавшими свое использование для лечения АГ в период беременности, являются центральные α2–агонисты, β–адреноблокаторы (β–АБ), α–β–адреноблокатор лабеталол, антагонисты кальция (АК) и некоторые вазодилататоры миотропного действия [3,5,7,11].
Основными лекарственными средствами, оправдавшими свое использование для лечения АГ в период беременности, являются центральные α2–агонисты, β–адреноблокаторы (β–АБ), α–β–адреноблокатор лабеталол, антагонисты кальция (АК) и некоторые вазодилататоры миотропного действия [3,5,7,11].
Ингибиторы ангиотензинпревращающего фермента (АПФ) и антагонисты рецепторов к ангиотензину II противопоказаны при беременности в связи с высоким риском развития задержки внутриутробного развития плода, костных дисплазий с нарушением оссификации свода черепа, укорочением конечностей, олигогидрамниона, неонатальной почечной несостоятельности (дисгенезия почек, острая почечная недостаточность у плода или новорожденного), возможна гибель плода [11,14].
Большинство международных и отечественных рекомендаций признают препаратом первой линии метилдопа, который успешно доказал свою эффективность и безопасность для матери и плода, его применяют в дозе 500–2000 мг/сут. в 2–3 приема. Несмотря на проникновение через плацентарный барьер, в многочисленных исследованиях было подтверждено отсутствие серьезных нежелательных эффектов у детей. В ходе лечения препаратом остаются стабильными маточно–плацентарный кровоток и гемодинамика плода, снижается перинатальная смертность. Отмечено, что метилдопа не влияет на величину сердечного выброса и кровоснабжение почек у матери.
В ходе лечения препаратом остаются стабильными маточно–плацентарный кровоток и гемодинамика плода, снижается перинатальная смертность. Отмечено, что метилдопа не влияет на величину сердечного выброса и кровоснабжение почек у матери.
Однако метилдопа имеет ряд существенных недостатков, связанных в основном с его относительной «несовременностью» – по сравнению с современными антигипертензивными средствами он имеет гораздо меньшую эффективность, короткий период действия, достаточно большое число побочных реакций при длительном применении (депрессия, сонливость, сухость во рту и ортостатическая гипотензия), для него характерно отсутствие органопротективного действия. Метилдопа может усугублять диспропорциональную задержку жидкости в организме, и без того свойственную беременности. Кроме того, метилдопа может вызывать анемию из–за токсического влияния на красный костный мозг или на сами эритроциты, следствием чего является гемолиз. При приеме метилдопа антитела к эритроцитам обнаруживаются примерно у 20% больных АГ, клинически гемолитическая анемия развивается у 2% пациентов, включая детей, внутриутробно подвергшихся воздействию препарата. Кроме того, у детей, рожденных от матерей, принимавших метилдопа, в первые сутки жизни возможно развитие гипотонии [10,13,15].
Кроме того, у детей, рожденных от матерей, принимавших метилдопа, в первые сутки жизни возможно развитие гипотонии [10,13,15].
Другим препаратом первого ряда при лечении АГ у беременных в большинстве зарубежных руководств считается неселективный β– и α–адреноблокатор лабеталол, однако в РФ лабеталол не зарегистрирован, поэтому опыт его применения в нашей стране отсутствует. По данным многочисленных исследований, он рекомендован для лечения АГ разной степени тяжести, представляется достаточно безопасным для матери и плода [9,11].
По поводу применения АК существует настороженность из–за потенциального риска развития тератогенных эффектов, т.к. кальций активно участвует в процессах органогенеза. Наиболее изученным препаратом группы АК является представитель дигидропиридиновой группы – нифедипин. Короткодействующий нифедипин рекомендован в качестве средства для быстрого снижения АД. Таблетки пролонгированного действия, а также таблетки с контролируемым высвобождением используются для продолжительной плановой базисной терапии АГ в период гестации. Гипотензивный эффект нифедипина достаточно устойчив, в клинических исследованиях не отмечено серьезных нежелательных явлений, в частности развития тяжелой гипотензии у матери [9,11].
Гипотензивный эффект нифедипина достаточно устойчив, в клинических исследованиях не отмечено серьезных нежелательных явлений, в частности развития тяжелой гипотензии у матери [9,11].
Нифедипин короткого действия при сублингвальном использовании в ряде случаев может провоцировать резкое неконтролируемое падение уровня АД, что приводит к снижению плацентарного кровотока. В связи с этим даже при оказании неотложной помощи препарат не стоит принимать внутрь. Пролонгированные формы нифедипина не вызывают патологического снижения уровня АД, рефлекторной активации симпатической нервной системы, обеспечивают эффективный контроль за уровнем АД на протяжении суток без значимого повышения его вариабельности. Кроме того, АК моделируют гемодинамику, свойственную физиологически протекающей беременности [3,11].
В качестве препаратов второго ряда используются β–адреноблокаторы. Их применение в период беременности изучено хуже, чем применение лабеталола. Однако большинство из них по классификации безопасности применения во время беременности FDA относятся, так же, как лабеталол, к категории С («риск нельзя исключить»). Одно из самых значимых преимуществ препаратов этой группы – это высокая гипотензивная эффективность, которая была подтверждена даже при сравнении их с лабеталолом. Так, атенолол в сравнительном исследовании с лабеталолом вызывал сопоставимый гипотензивный эффект и не вызывал тератогенных эффектов, бронхоспазма или брадикардии. Однако у детей, рожденных от матерей, принимавших атенолол, была более низкая масса тела (2750±630 г) по сравнению с группой детей, матери которых получали лабеталол (3280±555 г). Позднее в ряде других исследований было показано, что антенатальное применение атенолола ассоциировалось с замедлением внутриутробного роста и более низкой массой при рождении. Следует отметить, что имеются данные о снижении частоты развития ПЭ у пациенток, принимавших атенолол. В исследовании 56 беременных было показано, что атенолол может снижать частоту развития ПЭ у женщин с высоким сердечным выбросом (более 7,4 л/мин. до 24 нед. гестации) c 18 до 3,8%. В 2009 г. было выявлено, что у этих женщин снижается концентрация fms–подобной тирозинкиназы 1 типа (sFlt–1) – признанного ведущим этиологического фактора ПЭ [2,7].
Одно из самых значимых преимуществ препаратов этой группы – это высокая гипотензивная эффективность, которая была подтверждена даже при сравнении их с лабеталолом. Так, атенолол в сравнительном исследовании с лабеталолом вызывал сопоставимый гипотензивный эффект и не вызывал тератогенных эффектов, бронхоспазма или брадикардии. Однако у детей, рожденных от матерей, принимавших атенолол, была более низкая масса тела (2750±630 г) по сравнению с группой детей, матери которых получали лабеталол (3280±555 г). Позднее в ряде других исследований было показано, что антенатальное применение атенолола ассоциировалось с замедлением внутриутробного роста и более низкой массой при рождении. Следует отметить, что имеются данные о снижении частоты развития ПЭ у пациенток, принимавших атенолол. В исследовании 56 беременных было показано, что атенолол может снижать частоту развития ПЭ у женщин с высоким сердечным выбросом (более 7,4 л/мин. до 24 нед. гестации) c 18 до 3,8%. В 2009 г. было выявлено, что у этих женщин снижается концентрация fms–подобной тирозинкиназы 1 типа (sFlt–1) – признанного ведущим этиологического фактора ПЭ [2,7].
При применении пропранолола во время беременности описаны множественные нежелательные эффекты у плода и новорожденного (внутриутробная задержка роста, гипогликемия, брадикардия, угнетение дыхания, полицитемия, гипербилирубинемия и др.), поэтому препарат не рекомендован для использования во время беременности.
Во многих национальных рекомендациях метопролол рассматривается в качестве препарата выбора среди β–адреноблокаторов у беременных, т.к. он доказал свою высокую эффективность, отсутствие влияния на вес плода и имеет минимальное количество нежелательных эффектов. Несмотря на это, данные литературы позволяют обсуждать возможность применения в качестве препаратов выбора β–блокаторов с вазодилатирующими свойствами [1,9].
Данные нескольких рандомизированных клинических исследований в целом свидетельствуют, что β–адреноблокаторы (β–АБ) эффективны и безопасны в качестве антигипертензивной терапии у беременных. Существует мнение, что назначенные на ранних сроках беременности β–АБ, в особенности атенолол и пропранолол, могут вызывать задержку развития плода в связи с повышением общего сосудистого сопротивления. В то же время в плацебо–контролируемом исследовании с применением метопролола не получено данных, указывающих на отрицательное влияние препарата на развитие плода. Р. von Dadelszen в 2002 г. [16] провел метаанализ клинических исследований по β–блокаторам и сделал вывод, что задержка развития плода обусловлена не эффектом β–блокаторов, а снижением АД в результате гипотензивной терапии любым препаратом, при этом все гипотензивные препараты одинаково снижали риск развития тяжелой гипертензии в 2 раза по сравнению с плацебо. При сравнении различных гипотензивных средств между собой каких–либо преимуществ, касающихся влияния на конечные точки (развитие тяжелой АГ, материнская и перинатальная летальность), не было выявлено.
В то же время в плацебо–контролируемом исследовании с применением метопролола не получено данных, указывающих на отрицательное влияние препарата на развитие плода. Р. von Dadelszen в 2002 г. [16] провел метаанализ клинических исследований по β–блокаторам и сделал вывод, что задержка развития плода обусловлена не эффектом β–блокаторов, а снижением АД в результате гипотензивной терапии любым препаратом, при этом все гипотензивные препараты одинаково снижали риск развития тяжелой гипертензии в 2 раза по сравнению с плацебо. При сравнении различных гипотензивных средств между собой каких–либо преимуществ, касающихся влияния на конечные точки (развитие тяжелой АГ, материнская и перинатальная летальность), не было выявлено.
В связи с указанным выше с целью минимизации побочных эффектов в период гестации предпочтение целесообразно отдавать кардиоселективным β–АБ с вазодилатирующими свойствами, т.к. это в первую очередь позволяет избежать повышения общего периферического сосудистого сопротивления и тонуса миометрия. Наиболее перспективным для успешного использования в терапии АГ беременных является высокоселективный β1–АБ с вазодилатирующими и вазопротективными свойствами – бисопролол (Бисогамма). Блокируя β1–адренорецепторы сердца, уменьшая стимулированное катехоламинами образование цАМФ из АТФ, бисопролол снижает внутриклеточный ток ионов кальция, урежает частоту сердечных сокращений, угнетает проводимость, снижает сократимость миокарда. При увеличении дозы оказывает β2–адреноблокирующее действие. В первые 24 ч после назначения уменьшает сердечный выброс, повышает общее периферическое сосудистое сопротивление, которое максимум через 3 сут. возвращается к исходному уровню.
Наиболее перспективным для успешного использования в терапии АГ беременных является высокоселективный β1–АБ с вазодилатирующими и вазопротективными свойствами – бисопролол (Бисогамма). Блокируя β1–адренорецепторы сердца, уменьшая стимулированное катехоламинами образование цАМФ из АТФ, бисопролол снижает внутриклеточный ток ионов кальция, урежает частоту сердечных сокращений, угнетает проводимость, снижает сократимость миокарда. При увеличении дозы оказывает β2–адреноблокирующее действие. В первые 24 ч после назначения уменьшает сердечный выброс, повышает общее периферическое сосудистое сопротивление, которое максимум через 3 сут. возвращается к исходному уровню.
Гипотензивный эффект связан с уменьшением минутного объема крови, симпатической стимуляцией периферических сосудов, восстановлением чувствительности в ответ на снижение артериального давления и влиянием на центральную нервную систему. Кроме того, гипотензивное действие обусловлено уменьшением активности ренин–ангиотензиновой системы. В терапевтических дозах применение Бисогаммы не оказывает кардиодепрессивного действия, не влияет на обмен глюкозы и не вызывает задержки ионов натрия в организме. Бисогамма не оказывает прямого цитотоксического, мутагенного и тератогенного действия. Ее преимуществами при лечении АГ в период беременности являются: постепенное начало гипотензивного действия, отсутствие влияния на объем циркулирующей крови, отсутствие ортостатической гипотензии, уменьшение частоты развития респираторного дистресс– синдрома у новорожденного. Данный препарат имеет устойчивую антигипертензивную активность, оказывает мягкое хронотропное влияние.
В терапевтических дозах применение Бисогаммы не оказывает кардиодепрессивного действия, не влияет на обмен глюкозы и не вызывает задержки ионов натрия в организме. Бисогамма не оказывает прямого цитотоксического, мутагенного и тератогенного действия. Ее преимуществами при лечении АГ в период беременности являются: постепенное начало гипотензивного действия, отсутствие влияния на объем циркулирующей крови, отсутствие ортостатической гипотензии, уменьшение частоты развития респираторного дистресс– синдрома у новорожденного. Данный препарат имеет устойчивую антигипертензивную активность, оказывает мягкое хронотропное влияние.
Бисопролол (Бисогамма) характеризуется высокой биодоступностью, низкой индивидуальной вариабельностью концентрации в плазме, умеренной липофильностью и стереоспецифической структурой, продолжительным периодом полувыведения, что в совокупности дает возможность его длительного применения. Препарат отличается низкой частотой прекращения приема, отсутствием побочных эффектов со стороны биохимических, метаболических, почечных и гематологических показателей во время долгосрочных наблюдений.
Важными преимуществами этого препарата, особенно если говорить об АГ беременных, являются высокая эффективность в коррекции дисфункции эндотелия и нефропротективное действие. Не отмечено неблагоприятных влияний бисопролола (Бисогамма) на плод, а также на состояние здоровья, рост и развитие детей в течение их первых 18 мес. жизни. К побочным эффектам β–АБ относятся брадикардия, бронхоспазм, слабость, сонливость, головокружение, редко – депрессия, тревога, кроме того следует помнить о возможности развития «синдрома отмены» [1,2].
Данные обсервационных исследований бисопролола (Бисогамма) позволяют предположить эффективность и достаточную безопасность при применении во II–III триместрах беременности. В российской литературе есть данные об эффективности и отсутствии побочных эффектов применения бисопролола, в том числе в составе низкодозовой комбинированной терапии, для лечения АГ и нарушений сердечного ритма у беременных. Неблагоприятного влияния на плод не отмечено [3].
С целью оценки влияния бисопролола (Бисогамма) на уровень суточного АД, частоту развития ПЭ мы обследовали 25 женщин в возрасте 21–40 лет со сроком беременности 20–30 нед. и гестационной АГ. В качестве гипотензивных препаратов использовали бисопролол (Бисогамма) в дозировке 2,5–5 мг/сут. (13 женщин) – группа 1 или атенолол в дозировке 25–50 мг/сут. (12 женщин) – группа 2. До и после 4–недельного курса гипотензивной терапии выполняли стандартное клиническое и лабораторно–диагностическое обследование матери и плода, суточное АД–мониторирование.
Гипотензивные эффекты атенолола и бисопролола (Бисогамма) были сопоставимы. Среднее САД при приеме атенолола уменьшилось с 158 до 121 мм рт.ст., ДАД – с 102 до 80 мм рт.ст. Под влиянием бисопролола (Бисогамма) среднее САД уменьшилось со 159 до 120 мм рт.ст. (р<0,01), ДАД – со 121 до 78 мм рт.ст (р>0,01). ПЭ в III триместре развилась у 5 женщин группы 2 и только у 1 пациентки группы 1. В результате проведенного исследования был сделан вывод, что бисопролол (Бисогамма) при гестационной АГ эффективно снижает АД и предупреждает развитие ПЭ.
Таким образом, проблема АГ у беременных еще далека от разрешения и требует объединения усилий акушеров и терапевтов для подбора оптимального метода лечения.
Литература
1. Верткин А.Л., Ткачева О.Н., Мурашко Л.Е. и др. Артериальная гипертония беременных: диагностика, тактика ведения и подходы к лечению. // Лечащий врач. – 2006. – № 3. – С. 25–8.
2. Осадчий К.К. βАдреноблокаторы при артериальной гипертензии: фокус на бисопролол // Кардиология. – 2010. – №1. – С 84–89.
3. Стрюк Р.И., Брыткова Я.В., Бухонкина Ю.М. и др. Клиническая эффективность антигипертензивной терапии пролонгированным нифедипином и бисопрололом беременных с артериальной гипертонией // Кардиология. – 2008. – № 4. – С. 29–33.
4. Манухин И.Б., Маркова Е.В., Маркова Л.И., Стрюк Р.И. Комбинированная низкодозовая антигипертензивная терапия у беременных с артериальной гипертонией и гестозом // Кардиология. – 2012. – № 1. – С.32–38.
5. Cifkova R. Why is the treatment of hypertension in pregnancy still so difficult? // Expert Rev. Cardiovasc. Ther. 2011. Vol. 9 (6). P. 647–649.
Cardiovasc. Ther. 2011. Vol. 9 (6). P. 647–649.
6. Clivaz Mariotti L., Saudan P., Landau Cahana R., Pechere–Bertschi A. Hypertension in pregnancy // Rev. Med. Suisse. 2007. Vol. 3(124). P. 2015–2016.
7. Hebert M.F., Carr D.B., Anderson G.D. et al. Pharmacokinetics and pharmacodynamics of atenolol during pregnancy and postpartum // J. Clin. Pharmacol. 2005. Vol. 45(1). P. 25–33.
8. Leeman M. Arterial hypertension in pregnancy // Rev. Med. Brux. 2008. Vol. 29 (4). P. 340–345.
9. Lindheimer M.D., Taler S.J., Cunningham F.G. American Society of Hypertension. ASH position paper: hypertension in pregnancy // J. Clin. Hypertens. 2009. Vol. 11 (4). P. 214–225.
10. Mahmud H., Foller M., Lang F. Stimulation of erythrocyte cell membrane scrambling by methyldopa // Kidney Blood Press Res. 2008. Vol. 31 (5). P. 299–306.
11. Montan S. Drugs used in hypertensive diseases in pregnancy // Curr. Opin. Obstet. Gynecol. 2004. Vol. 16 (2). P. 111–115.
12. Mustafa R., Ahmed S., Gupta A., Venuto R.C. A comprehensive review of hypertension in pregnancy // J. Pregnancy. 2012. Vol. 5 (3). P. 534–538.
13. Ozdemir O.M., Ergin H., Ince T. A newborn with positive antiglobulin test whose mother took methyldopa in pregnancy // Turk. J. Pediatr. 2008. Vol. 50 (6). P. 592–594.
14. Podymow T., August P. Update on the use of antihypertensive drugs in pregnancy // Hypertension. 2008. Vol. 51 (4). P. 960–969.
15. Seremak–Mrozikiewicz A., Drews K. Methyldopa in therapy of hypertension in pregnant women // Ginekol. Pol. 2004. Vol. 75 (2). P. 160–165.
16. von Dadelszen P., Magee L.A. Fall in mean arterial pressure and fetal growth restriction in pregnancy hypertension: an updated metaregression analysis // J. Obstet. Gynaecol. Can. 2002. Vol. 24 (12). P. 941–945.
Артериальная гипертензия у беременных. Что, зачем и чем лечим?
Под артериальной гипертензией (АГ) у беременных определяют состояние, при котором в результате повторных измерений артериального давления (АД) цифры систолического АД составляют 140 мм рт. ст. и более и/или диастолическое АД равно 90 мм рт.ст. или более [1].
ст. и более и/или диастолическое АД равно 90 мм рт.ст. или более [1].
АГ отмечается у 10% беременных и является важным фактором материнской и неонатальной заболеваемости и смертности [2]. Около 15—18% случаев материнской смертности в мире связаны с развитием АГ, что составляет 62 000—77 000 смертей в год [3—7]. Частота А.Г. в последние годы увеличивается в связи с ростом числа беременных женщин старшего возраста и «эпидемией» ожирения [5]. Диагноз данного заболевания необходимо подтвердить определением повышенного АД, как минимум, при двух измерениях и в течение не менее 4 ч.
Гипертензивные состояния при беременности представлены группой заболеваний, существующих до беременности или развившихся непосредственно в связи с беременностью. Выделяют четыре основные формы АГ: артериальная гипертензия, имевшаяся до беременности (гипертоническая болезнь или симптоматическая АГ), гестационная артериальная гипертензия; артериальная гипертензия, имевшаяся до беременности и сочетающаяся с гестационной гипертензией и протеинурией, а также неклассифицируемая артериальная гипертония [8, 9].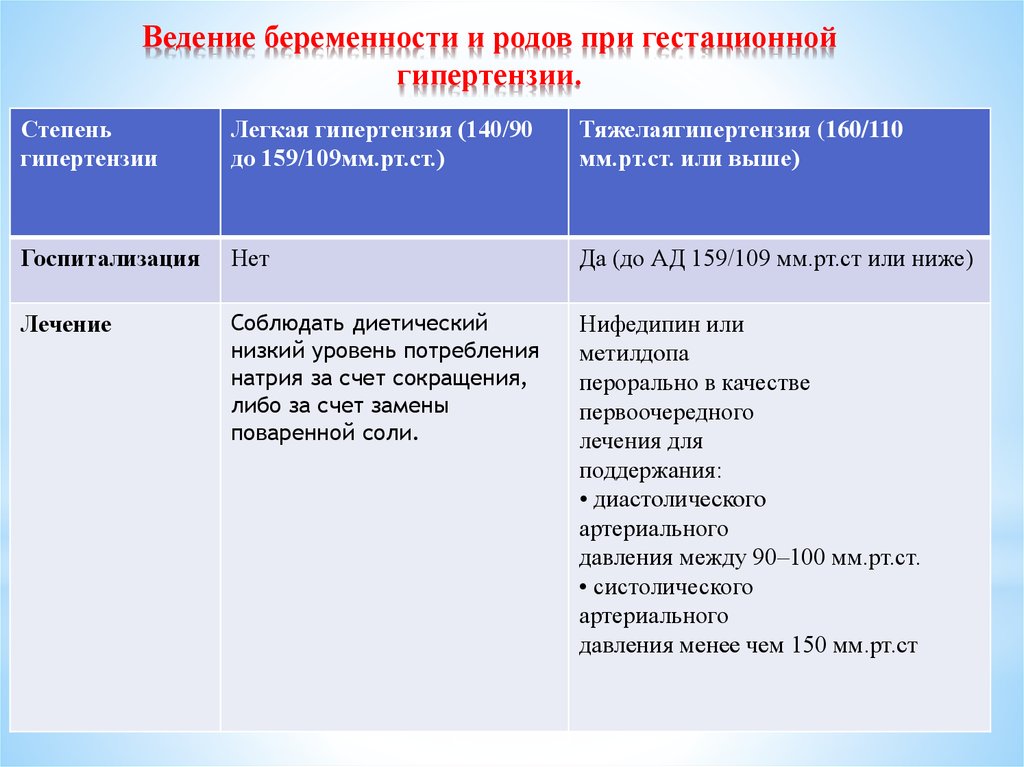
Существуют следующие цели антигипертензивной терапии у беременных, которые чаще всего сразу все бывают недостижимы:
1. Предотвращение серьезных материнских осложнений, таких как кровоизлияние в мозг.
2. Предотвращение перехода заболевания в преэклампсию.
3. Улучшение перинатальных исходов.
4. Улучшение отдаленных результатов у детей, рожденных матерями с АГ.
5. Снижение риска развития сердечно-сосудистых осложнений у женщин с АГ во время беременности.
К сожалению, лечение беременных с АГ не предотвращает развитие преэклампсии. Так, данные электронной базы Кокрановской библиотеки (19 рандомизированных исследований, включавших 2409 женщин и изучавших роль антигипертензивной терапии при мягкой — легкая АГ, или АГ I стадии или умеренно выраженной АГ), свидетельствуют об отсутствии разницы в частоте развития протеинурии или преэклампсии между леченными пациентками и получавшими плацебо.
Определенные опасения вызывает то, что жесткий контроль за уровнем АД способен ухудшить перинатальные исходы из-за снижения маточно-плацентарной перфузии и ухудшения условий для роста плода. Проводимое в настоящее время многоцентровое рандомизированное контролируемое исследование должно помочь ответить на вопрос: увеличивает или уменьшает вероятность потери беременности и влияет ли на перинатальный исход в ближайшие 48 ч после родов «жесткость» контроля АД (диастолическое АД 100 или 85 мм рт.ст.) [10].
Проводимое в настоящее время многоцентровое рандомизированное контролируемое исследование должно помочь ответить на вопрос: увеличивает или уменьшает вероятность потери беременности и влияет ли на перинатальный исход в ближайшие 48 ч после родов «жесткость» контроля АД (диастолическое АД 100 или 85 мм рт.ст.) [10].
В соответствии с рекомендациями Всероссийского научного общества кардиологов (2010), Рабочей группы по лечению А.Г. Европейского общества кардиологов (2007), а также рекомендациями Европейского общества кардиологов по лечению сердечно-сосудистых заболеваний у беременных (2011, 2018) в настоящее время для лечения АГ в период беременности используют три группы препаратов, отвечающих критериям фармакотерапии в период беременности: препараты центрального действия (метилдопа, допегит), антагонисты кальция (АК) дигидропиридинового ряда (нифедипины короткого и длительного действия), кардиоселективные β-адреноблокаторы — β-АБ (метопролол сукцинат, бисопролол), а также препарат, оказывающий смешанное α- и β-блокирующее действие (лабеталол). Комбинированная терапия проводится в случае неэффективности монотерапии в максимальной дозе. Рациональной комбинацией является сочетание нифедипина длительного действия и β-АБ, при неэффективности такой комбинации возможно присоединение гидрохлортиазида в малых дозах (6,5—25,0 мг/сут).
Комбинированная терапия проводится в случае неэффективности монотерапии в максимальной дозе. Рациональной комбинацией является сочетание нифедипина длительного действия и β-АБ, при неэффективности такой комбинации возможно присоединение гидрохлортиазида в малых дозах (6,5—25,0 мг/сут).
Препаратом выбора для лечения АГ у беременных в настоящее время является метилдопа (М) (отечественный аналог — допегит). Препарат начал использоваться с 50-х годов прошлого столетия и представляет собой аминокислоту, способную блокировать действие фермента допа-декарбоксилазы и, таким образом, предотвращать образование норадреналина. Другой механизм действия основан на образовании метаболита α-метилового норэпинефрина, действующего как «ложный нейромедиатор». Путем конкурентного блокирования симпатического действии норадреналина, М снижает системное артериальное давление, а также уменьшает активность ренина плазмы.
Кроме того, в последние годы показано, что М, гидралазин и клонидин способны улучшить клеточное взаимодействие между трофобластом и эндотелиальными клетками путем снижения концентрации fms-подобной тирозинкиназы-1 (sFlt-1) [11]. Выявлено, что наиболее чувствительными и специфичными прогностическими показателями преэклампсии являются маркеры ангиогенеза — плацентарный фактор роста и fms-подобная тирозинкиназа-1, представляющая собой антиангиогенный протеин, который выполняет роль мощного ингибитора фактора роста эндотелия сосудов и плацентарного фактора роста. Чувствительность тестов определения fms-подобной тирозинкиназы-1 в отношении прогнозирования ПЭ достигает 89%, а специфичность — 97% [12—14].
Выявлено, что наиболее чувствительными и специфичными прогностическими показателями преэклампсии являются маркеры ангиогенеза — плацентарный фактор роста и fms-подобная тирозинкиназа-1, представляющая собой антиангиогенный протеин, который выполняет роль мощного ингибитора фактора роста эндотелия сосудов и плацентарного фактора роста. Чувствительность тестов определения fms-подобной тирозинкиназы-1 в отношении прогнозирования ПЭ достигает 89%, а специфичность — 97% [12—14].
Исторически сложилось, что метилдопа является наиболее широко используемым антигипертензивным препаратом у беременных.
Тем не менее широко принятое мнение о безопасности данного препарата является явно преувеличенным. Прием препарата часто (до 20% наблюдений) приходится прекращать из-за поражения центральной нервной системы и появления таких сипмтомов, как депрессия и слабость.
Другим тяжелым, однако нечастым (2,5—10%) осложнением лечения М является непрямое поражение печени по типу гепатита, развивающееся обычно через 3 мес от начала лечения. О гепатотоксичности препарата впервые было сообщено S. Elkington в 1969 г., а позже это мнение нашло свое подтверждение в работах других авторов [15—17]. Предполагается, что гепатотоксичность обусловлена аномальным метаболизмом М, проходящим через цитохром Р450, с последующим развитием иммунной реакции на эти метаболиты.
О гепатотоксичности препарата впервые было сообщено S. Elkington в 1969 г., а позже это мнение нашло свое подтверждение в работах других авторов [15—17]. Предполагается, что гепатотоксичность обусловлена аномальным метаболизмом М, проходящим через цитохром Р450, с последующим развитием иммунной реакции на эти метаболиты.
Малоизвестным осложнением терапии М является аутоиммунная гемолитическая анемия, развивающаяся обычно, как и гепатит, также через 3 мес от начала использования препарата, что во многом объединяет патогенез этих страданий. Выяснено, что у 15% больных, получающих М, отмечается появление в крови аутоантител против эритроцитов, а еще у 0,5—1% развивается гемолитическая анемия [18]. Заболевание не имеет характерных особенностей, а тяжесть симптомов колеблется от незначительной слабости до одышки и дыхательной недостаточности, а в отсутствие лечения — смерти [19—21]. Возможно появление гипербилирубинемии у плода за счет непрямой фракции [22]. Кроме того, длительный прием М матерью в высокой дозе 1500 мг/сут и невысокий клиренс препарата у новорожденного способны привести к накоплению препарата в его тканях, а затем — к синдрому отмены с развитием тахикардии, повышения АД и сердечной недостаточности у новорожденного [23].
Обзор электронной базы Кохрановской библиотеки, касающийся 12 рандомизированных контролируемых исследований по вопросам лечения первичной АГ, выявил эффективность М в отношении снижения А.Д. Однако ни в одном из этих исследований не продемонстрировано снижение числа осложнений, например, инсультов, на фоне лечения М по сравнению с плацебо [24]. Обзор электронной базы Кохрановской библиотеки, касающийся лечения мягкой или умеренно выраженной АГ у беременных, выявил, что для предотвращения перехода в выраженную АГ β-АБ являются более эффективными препаратами, чем М [25]. Кроме того, не было установлено различий по частоте развития преэклампсии, случаев смерти и преждевременных родов между пациентками, получающими М или другой антигипертензивный препарат. Однако после рандомизации пациенток, получавших М или лабетолол, выявлено преимущество первого в отношении предотвращения развития выраженной АГ, преэклампсии и преждевременных родов [26].
Все изложенное позволило Обществу акушеров и гинекологов Канады, а также Великобритании не рассматривать М в качестве препарата первого ряда [10, 27, 28].
Возможно использование блокаторов кальциевых каналов: нифедипина короткого (в дозе 30—60 мг/сут на 1 прием) или продленного (амлодипин, норваск) действия (в дозе до 10 мг/сут на 2 приема). Нифедипин, который является наиболее изученным препаратом этой группы, применяемым при беременности, считается достаточно безопасным и эффективным, поэтому может быть с успехом использован, особенно в тех случаях, когда АГ рефрактерна к лечению М или β-АБ, либо имеются противопоказания к названным препаратам. Использование нифедипина (а также его пролонгированных форм) позволяет эффективно снижать АД, однако это не оказывает влияние на частоту госпитализаций беременных и перинатальные исходы [29]. Безопасно у беременных может использоваться верапамил. В настоящее время дилтиазем пока не рассматривается в качестве антигипертензивного препарата у беременных [9], а в инструкции, прилагаемой к препарату, прямо указано, что он противопоказан при беременности и лактации. Однако в «Заявлении Американской ассоциации сердца» — AHA (2017) отмечено, что препарат может применяться, если потенциальная польза выше потенциального риска для плода [30].
β-АБ, в основном — кардиоселективные, также широко применяются при беременности и считаются в целом безопасными и эффективными, что с 80-х годов прошлого столетия подтверждено целым рядом рандомизированных исследований [31—34]. Существует мнение, что β-АБ, назначенные в ранние сроки беременности, в особенности атенолол, могут вызывать брадикардию у плода, задержку его роста и снижение маточно-плацентарного кровотока [35—37], в то время, как, например, карведилол не оказывает такого негативного воздействия [38]. Однако действие атенолола на задержку роста плода прослеживается только при назначении препарата в I триместре беременности, что было подтверждено сравнительными исследованиями [39]. В то же время эффективность атенолола в плане снижения АД является наиболее высокой [40].
P. von Dadelszen и соавт. [41] в 2000 г. провели метаанализ клинических исследований и сделали следующие выводы. Задержка внутриутробного развития плода обусловлена не эффектом β-АБ, а снижением АД в результате антигипертензивной терапии любым препаратом (β-АБ, М, антагонисты кальция). Так, снижение АД на 10 мм рт.ст. приводило к уменьшению массы тела новорожденного на 145 г. Все антигипертензивные препараты в сравнении с плацебо одинаково снижали риск развития тяжелой гипертензии в 2 раза. При сравнении различных антигипертензивных средств между собой каких-либо преимуществ по влиянию на конечные точки (развитие тяжелой АГ, материнская и перинатальная летальность) не выявлено [41]. Использование β-АБ не сопровождается усилением сократимости матки, увеличением частоты преждевременных родов. Ряд авторов считают, что прохождение этих препаратов через кровоток плода не вызывает у него брадикардии, респираторного дистресс-синдрома или гипогликемии [42].
Так, снижение АД на 10 мм рт.ст. приводило к уменьшению массы тела новорожденного на 145 г. Все антигипертензивные препараты в сравнении с плацебо одинаково снижали риск развития тяжелой гипертензии в 2 раза. При сравнении различных антигипертензивных средств между собой каких-либо преимуществ по влиянию на конечные точки (развитие тяжелой АГ, материнская и перинатальная летальность) не выявлено [41]. Использование β-АБ не сопровождается усилением сократимости матки, увеличением частоты преждевременных родов. Ряд авторов считают, что прохождение этих препаратов через кровоток плода не вызывает у него брадикардии, респираторного дистресс-синдрома или гипогликемии [42].
H. Orbach и соавт. [43] считают, что, наоборот, сама АГ является значительным и независимым фактором риска развития таких тяжелых осложнений, как синдром задержки роста плода и преждевременные роды.
Для лечения АГ у беременных могут быть использованы многие β-АБ (метопролол сукцинат, пропранолол, атенолол, оксипренолол относятся к группе C, как и другие препараты, кроме М), однако считается, что их применение не имеет широкой доказательной базы. В Рекомендациях Российского общества кардиологов (2018) отмечена возможность использования только кардиоселективных β-АБ метопролола сукцината и бисопролола [9].
В Рекомендациях Российского общества кардиологов (2018) отмечена возможность использования только кардиоселективных β-АБ метопролола сукцината и бисопролола [9].
С 70-х годов прошлого столетия в лечении больных с АГ применяется комбинированный α- и β-АБ лабеталол, обладающий способностью снижать АД, сердечный выброс (β-блокирующее действие) и общее периферическое сопротивление (α-блокирующее действие) [44]. В некоторых странах он является препаратом первого ряда при лечении АГ у беременных [28, 45], однако в рекомендации Российского общества кардиологов по лечению АГ у беременных в 2013 и 2018 г. он включен не был [8, 9]. В инструкции, прилагаемой к препарату, сказано, что он может использоваться при беременности и лактации, если его польза для матери превышает вероятность нанесения вреда здоровью плода.
В отдельных работах показано, что у беременных могут также безопасно применяться «чистые» α-адреноблокаторы (празозин, доксазозин) [46, 47], которые широко используются у пациенток с симптоматической АГ (феохромоцитома) [48, 49]. В нашей стране согласно инструкциям Фармацевтического комитета РФ при АГ у беременных α-блокаторы не применяются.
В нашей стране согласно инструкциям Фармацевтического комитета РФ при АГ у беременных α-блокаторы не применяются.
Таким образом, во-первых, до настоящего времени для начала антигипертензивной терапии у беременных четко не определены уровни АД. В большинстве национальных рекомендаций стран Европы, Австралии и Новой Зеландии указаны таковыми 140/90 или даже 150/100 мм рт.ст., а также случаи хронической АГ, особенно протекающей с поражением органов-мишеней [8, 9]. Показано, что антигипертензивная терапия с использованием М или лабеталола при мягкой или умеренной гестационной АГ позволяет снизить риск неблагоприятных материнских и перинатальных исходов [50].
Собственный многолетний опыт авторов свидетельствует о том, что отечественные практикующие врачи, опасаясь подчас мер административного (а то и уголовного!) воздействия, часто назначают антигипертензивные препараты у беременных при нормально высоких цифрах АД (АД до 140/90 мм рт.ст.), хотя остается недоказанным положительное прогностическое значение этих мероприятий в отношении матери и плода, и вызывает вопросы сохранность при таком лечении маточно-плацентарного кровотока.
Во-вторых, на наш взгляд, до сих пор необоснованно широко назначается препарат метилдопа (допегит). Этому способствует как мнение о его безопасности (препарат «первой линии»), так и распространяемые сведения о побочных эффектах других антигипертензивных средств. Более того, М продолжает назначаться даже в случаях умеренной и выраженной АГ в отсутствие положительного эффекта от лечения, что резко снижает эффективность коррекции терапии в последующем, приводит к необратимым нарушениям маточно-плацентарного кровотока и фетоплацентарной недостаточности.
В-третьих, обоснованным в зависимости от характера гемодинамических изменений является использование (особенно — во II и III триместрах) не только антагонистов кальция, но и β-, а также α-адреноблокаторов. Актуальной выглядит у беременных и комбинированная антигипертензивная терапия с использованием этих препаратов. Собственный опыт свидетельствует о том, что такие подходы к терапии позволяют эффективно снижать АД у беременных при умеренной, а в ряде случаев — и при выраженной АГ, создавая условия для дальнейшего пролонгирования беременности.
1. Выделение препаратов «первой линии» у беременных является нецелесообразным, так как ориентирует практикующих врачей исключительно на использование таковых, даже в условиях их неэффективности или развития осложнений АГ.
2. Метилдопа (допегит) должен использоваться только при мягкой АГ и наличии адекватного эффекта от лечения (нормализация или снижение АД).
3. Необходимо менять парадигму подхода к использованию антигипертензивных препаратов у беременных, пересмотрев Рекомендации Всероссийского общества кардиологов. При умеренной и выраженной АГ и в случаях неэффективного лечения М незамедлительно должны назначаться антагонисты кальция, β-, и, возможно, α-адреноблокаторы в виде моно- или комбинированной терапии.
Сведения об авторах
Мравян С.Р. — д.м.н., проф.; e-mail: [email protected]; https://orcid.org/0000-0002-9591-8433
Петрухин В.А. — д.м.н., проф.; e-mail: [email protected]; https://orcid.org/0000-0003-0460-3047
*e-mail: sergeymrav@list. ru; https://orcid.org/0000-0002-9591-8433
ru; https://orcid.org/0000-0002-9591-8433
Отчетность о статусе беременности для ВГВ-позитивных женщин
- Роль лабораторий
- * Определение статуса беременности
- * Обучение клиентов
- * Отчетность и тестирование
- Роль клиницистов и медицинских отделов
- *
- * Департаменты здравоохранения
- Справочная информация
- Ресурсы CDC:
- Дополнительные ресурсы:
Как я могу помочь остановить передачу вируса гепатита В от матери к ребенку?
Проблема: Хотя примерно 95% беременных женщин проходят пренатальное тестирование на поверхностный антиген гепатита В (HBsAg), выявляется менее половины ожидаемых родов у HBsAg-положительных женщин. Лабораторные отчеты должны включать пол и возраст/дату рождения, но статус беременности обычно не сообщается в отделы здравоохранения.
Решение: Следует призвать все лаборатории, предоставляющие услуги по тестированию на HBsAg, фиксировать статус беременности у женщин, прошедших тестирование на HBsAg, чтобы помочь в выявлении инфицированных ВГВ беременных женщин.
Роль лабораторий
Лаборатории, заинтересованные в присоединении к этим усилиям, могут предпринять следующие шаги:
- Определение статуса беременности
- Четко указывайте статус беременности, если таковой имеется во всех положительных результатах теста на HBsAg, сообщаемых в отделы здравоохранения и врачам, назначающим лечение. Эти результаты испытаний включают, но не ограничиваются следующим:
- Заказы, исходящие от акушерских («акушерских») групп или панелей пренатального скрининга, которые включают тестирование на HBsAg в качестве компонента
- Индивидуальные заказы на тестирование на HBsAg, исходящие от акушерской или пренатальной панели, выполненной в другом месте (HBsAg передан на аутсорсинг в референс-лабораторию)
- Заказы на индивидуальный пренатальный тест на HBsAg
- Заказы на отдельный тест на HBsAg, который не является частью акушерства или пренатальной панели, но где статус беременности указан в другом месте заказа (например, в виде кода диагноза, связанного с беременностью, по МКБ-10; примеры можно найти здесь)
- Четко указывайте статус беременности, если таковой имеется во всех положительных результатах теста на HBsAg, сообщаемых в отделы здравоохранения и врачам, назначающим лечение. Эти результаты испытаний включают, но не ограничиваются следующим:
РЕКОМЕНДУЕМЫЙ МЕТОД ИДЕНТИФИКАЦИИ : Вставьте слово «ПРЕНАТАЛЬНЫЙ» в сообщаемые результаты теста либо рядом с названием теста в результатах, отправленных на бумаге/факсе, либо в поле OBR-13 результатов, отправленных ELR.
- Обучение клиентов
- Обучить клиницистов возможностям лабораторного тестирования для выбора акушерской или пренатальной панели при скрининге беременных женщин на HBsAg.
- Рекомендовать клиницистам выявлять беременных женщин при заказе тестов на HBsAg в качестве отдельного теста или в составе неакушерской/непренатальной панели. Например, попросите клиницистов предоставить диагностические коды МКБ-10, указывающие на беременность, и включить эти коды в положительные отчеты, отправляемые в департаменты здравоохранения.
- Отчетность и тестирование
- Своевременно предоставлять отчеты обо всех положительных результатах анализов на HBsAg в соответствующие отделы здравоохранения. Лабораториям также рекомендуется предоставлять положительные результаты анализов известных беременных женщин непосредственно в местные программы профилактики перинатального гепатита B, насколько это возможно.

- Выполнение лицензированного нейтрализующего подтверждающего тестирования для всех тестов на HBsAg, включенных в акушерские и пренатальные панели, или когда диагностический код МКБ-10 указывает на беременность.
- Включите подтверждение подтвержденных HBsAg-положительных результатов в окончательный лабораторный отчет, если анализ проводится на беременной женщине.
- Своевременно предоставлять отчеты обо всех положительных результатах анализов на HBsAg в соответствующие отделы здравоохранения. Лабораториям также рекомендуется предоставлять положительные результаты анализов известных беременных женщин непосредственно в местные программы профилактики перинатального гепатита B, насколько это возможно.
Для получения помощи в установлении метода выявления HBsAg-позитивных беременных женщин или для любых дополнительных вопросов : Пожалуйста, обращайтесь по адресу [email protected].
Роль клиницистов и отделов здравоохранения
Клиницисты и отделы здравоохранения также играют важную роль в лабораторных отчетах о статусе беременности для женщин с положительным гепатитом В.
Клиницисты:
- При заказе скринингового теста на HBsAg для беременной женщины выберите тест, обозначенный как «пренатальный», или из пренатальной/акушерской панели, чтобы обеспечить проведение подтверждающего тестирования при всех положительных результатах скрининга на HBsAg.

- Сообщите выбранной лаборатории о статусе беременности женщины, чтобы обеспечить проведение подтверждающего тестирования для всех положительных результатов скрининга на HBsAg.
- При заказе тестов на HBsAg укажите все без исключения диагностические коды МКБ-10, указывающие на текущую или недавнюю беременность.
Алгоритм скрининга и направления к специалистам для выявления вируса гепатита В (HBV) среди беременных женщин
Это клинический алгоритм скрининга и направления к специалистам беременных женщин с положительным HBsAg. Инструмент pdf icon[PDF – 1 страница]
Департаменты здравоохранения:
- Будьте в курсе того, как лаборатории, подотчетные вашей юрисдикции, сообщают информацию о беременности (например, включая слово «пренатальный», предоставляя коды МКБ-10).
- Извлеките эти пренатальные индикаторы как из бумажных, так и из электронных лабораторных отчетов (ELR).
- Убедитесь, что пренатальные индикаторы предоставлены вашим координаторам программы профилактики перинатального гепатита В.

Пожалуйста, обращайтесь по адресу [email protected] для получения информации о пренатальных индикаторах для ARUP Laboratories, LabCorp, Mayo Medical Laboratories и Quest Diagnostics.
История вопроса
Младенцы, рожденные от женщин с положительной реакцией на поверхностный антиген гепатита В (HBsAg), подвергаются высокому риску заражения вирусом гепатита В (ВГВ). При отсутствии лечения у младенцев, инфицированных ВГВ,Риск прогрессирования в хронический гепатит В составляет 0%, и до 25% младенцев, заразившихся хронической инфекцией ВГВ, преждевременно умрут от связанной с ВГВ гепатоцеллюлярной карциномы или цирроза печени. В 1988 году Консультативный комитет по практике иммунизации (ACIP) рекомендовал, чтобы все беременные женщины проходили скрининг на HBsAg при каждой беременности, чтобы гарантировать, что младенцы, рожденные от HBsAg-положительных женщин, получают постконтактную профилактику, эффективность которой составляет до 95 %. перинатальная ВГВ-инфекция.
Совет эпидемиологов штатов и территорий (CSTE) рекомендует, чтобы обо всех HBsAg-положительных тестах сообщалось в отделы здравоохранения во всех штатах, чтобы координаторы перинатальной профилактики гепатита B могли отслеживать их и обеспечивать надлежащее ведение младенцев. Хотя некоторые скрининговые исследования показали, что около 95% беременных женщин проходят пренатальное тестирование на HBsAg, выявляется менее половины ожидаемых родов у HBsAg-положительных женщин, что указывает на то, что не все HBsAg-положительные беременные женщины сообщаются и выявляются координаторами по перинатальному гепатиту B в департаментах здравоохранения.
Причины пропуска HBsAg-позитивных беременных женщин отделами здравоохранения включают занижение данных, неправильный заказ поставщиками медицинских услуг, неправильное толкование результатов анализов и, что важно, предоставление результатов анализов без информации для идентификации анализов беременных женщин.
В соответствии с Поправкой к поправке на улучшение клинических лабораторий (CLIA) в лабораторных отчетах должны быть указаны только пол и возраст/дата рождения, поэтому о статусе беременности обычно не сообщается в отделы здравоохранения. Чтобы помочь улучшить выявление HBsAg-положительных беременных женщин, CDC и партнеры из департаментов здравоохранения, коммерческих лабораторий, Американского колледжа акушеров-гинекологов (ACOG) и других профессиональных организаций работали вместе, чтобы включить статус беременности в отчеты о лабораторных тестах, отправляемые в департаменты здравоохранения. . Эти усилия руководствовались рекомендациями CSTE по улучшению выявления HBsAg-позитивных беременных женщин.
Чтобы помочь улучшить выявление HBsAg-положительных беременных женщин, CDC и партнеры из департаментов здравоохранения, коммерческих лабораторий, Американского колледжа акушеров-гинекологов (ACOG) и других профессиональных организаций работали вместе, чтобы включить статус беременности в отчеты о лабораторных тестах, отправляемые в департаменты здравоохранения. . Эти усилия руководствовались рекомендациями CSTE по улучшению выявления HBsAg-позитивных беременных женщин.
В этой работе активно участвуют четыре крупные коммерческие лаборатории: ARUP Laboratories, LabCorp, Mayo Medical Laboratories и Quest Diagnostics. Каждая лаборатория теперь предлагает специализированные тесты на HBsAg для беременных женщин в качестве отдельного анализа и/или в составе пренатальной/акушерской панели, чтобы упростить регистрацию HBsAg-позитивных женщин в департаментах здравоохранения. Если в лаборатории заказан назначенный пренатальный тест на HBsAg и получен положительный результат, специальный лабораторный отчет (SLR) с указанием статуса беременности автоматически отправляется в соответствующий отдел здравоохранения.
В настоящее время предпринимаются усилия по расширению этой отчетности о статусе беременности и вовлечению всех лабораторий, предоставляющих услуги тестирования на HBsAg, в эту инициативу общественного здравоохранения.
Ресурсы CDC:
- Профилактика вирусной инфекции гепатита В в США: рекомендации Консультативного комитета по практике иммунизации MMWR 2018;67(№ RR-1).
- Центры по контролю и профилактике заболеваний (CDC). Рекомендации по выявлению и ведению общественного здравоохранения лиц с хронической инфекцией вируса гепатита В pdf icon[PDF – 28 страниц]. MMWR 2008; 57 (RR-08).
- Центры по контролю и профилактике заболеваний (CDC). Комплексная стратегия иммунизации для ликвидации передачи вируса гепатита В в Соединенных Штатах. Рекомендации Консультативного комитета по практике иммунизации (ACIP), часть 1: иммунизация младенцев, детей и подростков pdf icon[PDF – 39 страниц]. MMWR 2005; 54 (RR-16).
- Веб-сайт CDC по профилактике перинатального гепатита В
- CDC/ACOG Prenatal HBsAg Test Guide and Referral Algorithm pdf icon[PDF – 2 страницы]
Дополнительные ресурсы:
- Американский колледж акушеров и гинекологов – Иммунизация для женщин: о гепатите Bexternal icon
- Американский конгресс акушеров и гинекологовВнешний значок
- Целевая группа профилактических услуг США (USPSTF).
 Скрининг на вирусную инфекцию гепатита В во время беременности: Заявление рабочей группы профилактических служб США о подтверждении рекомендаций Внешний значок. Энн Интерн Мед 2009;150;869-873.
Скрининг на вирусную инфекцию гепатита В во время беременности: Заявление рабочей группы профилактических служб США о подтверждении рекомендаций Внешний значок. Энн Интерн Мед 2009;150;869-873. - Поправка к поправке на улучшение клинических лабораторий (CLIA) внешний значок, 42 CFR § 493.1241
Лечение гепатита В у беременных: обновленная информация
1. Лечение коинфекции гепатита В и ВИЧ. Доступно по адресу: http://www.euro.who.int/_data/assets/pdf_file/0011/152012/e95792.pdf.
2. Гроссблатт Н. Гепатит и рак печени: Национальная стратегия профилактики и борьбы с гепатитами В и С. Комитет Института медицины (США) по профилактике и борьбе с инфекциями вирусного гепатита. Вашингтон, округ Колумбия: Издательство национальных академий; 2010. [Google Академия]
3. Wasley A, Kruszon-Moran D, Kuhnert W, Simard EP, Finelli L, McQuillan G, et al. Распространенность вирусной инфекции гепатита В в США в эпоху вакцинации. J заразить дис. 2010; 202:192–201. дои: 10.1086/653622. [PubMed] [Google Scholar]
дои: 10.1086/653622. [PubMed] [Google Scholar]
4. Kowdley KV, Wang CC, Welch S, Roberts H, Brosgart CL. Распространенность хронического гепатита В среди лиц иностранного происхождения, проживающих в США, по стране происхождения. Гепатология. 2012;56:422–433. doi: 10.1002/hep.24804. [PubMed] [Академия Google]
5. Terrault NA, Bzowej NH, Chang KM, Hwang JP, Jonas MM, Murad MH, et al. Рекомендации AASLD по лечению хронического гепатита В. Гепатология. 2016; 63: 261–283. doi: 10.1002/hep.28156. [Бесплатная статья PMC] [PubMed] [Google Scholar]
6. Tran TT. Гепатит В при беременности. Клин Инфекция Дис. 2016; 62 (Приложение 4): S314–S317. doi:10.1093/cid/ciw092. [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Gish RG, Gadano AC. Хронический гепатит B: текущая эпидемиология в Америке и последствия для лечения. J Вирусная гепатит. 2006; 13: 787–79.8. doi:10.1111/j.1365-2893.2006.00787.x. [PubMed] [Google Scholar]
8. Смит Э.А., Жак-Кэрролл Л., Уокер Т. И., Сироткин Б., Мерфи Т.В. Национальная программа перинатальной профилактики гепатита В, 1994–2008 гг. Педиатрия. 2012; 129: 609–616. doi:10.1542/пед.2011-2866. [PubMed] [Google Scholar]
И., Сироткин Б., Мерфи Т.В. Национальная программа перинатальной профилактики гепатита В, 1994–2008 гг. Педиатрия. 2012; 129: 609–616. doi:10.1542/пед.2011-2866. [PubMed] [Google Scholar]
9. Singh AE, Plitt SS, Osiowy C, Surynicz K, Kouadjo E, Preiksaitis J, et al. Факторы, связанные с неэффективностью вакцинации и вертикальной передачей гепатита В среди канадских матерей и младенцев. J Вирусная гепатит. 2011; 18: 468–473. дои: 10.1111/j.1365-2893.2010.01333.х. [PubMed] [Google Scholar]
10. Burk RD, Hwang LY, Ho GY, Shafritz DA, Beasley RP. Исход перинатального воздействия вируса гепатита В зависит от вирусной нагрузки матери. J заразить дис. 1994; 170:1418–1423. doi: 10.1093/infdis/170.6.1418. [PubMed] [Google Scholar]
11. Европейская ассоциация по изучению печени. Руководящие принципы клинической практики EASL: Ведение хронической вирусной инфекции гепатита В. J Гепатол. 2012; 57: 167–185. doi:10.1016/j.jhep.2012.02.010. [PubMed] [Академия Google]
12. Альтер MJ. Эпидемиология гепатита В в Европе и мире. J Гепатол. 2003; 39:S64–S69. doi: 10.1016/S0168-8278(03)00141-7. [PubMed] [Google Scholar]
Альтер MJ. Эпидемиология гепатита В в Европе и мире. J Гепатол. 2003; 39:S64–S69. doi: 10.1016/S0168-8278(03)00141-7. [PubMed] [Google Scholar]
13. Publicover J, Gaggar A, Nishimura S, Van Horn CM, Goodsell A, Muench MO, et al. Зависимая от возраста печеночная лимфоидная организация направляет успешный иммунитет к гепатиту B. J Clin Invest. 2013; 123:3728–3739. дои: 10.1172/JCI68182. [Бесплатная статья PMC] [PubMed] [Google Scholar]
14. Carey I, D’Antiga L, Bansal S, Longhi MS, Ma Y, Mesa IR, et al. Иммунный и вирусный профиль от толерантности до клиренса поверхностного антигена гепатита В: продольное исследование вертикально инфицированных вирусом гепатита В детей, получающих комбинированную терапию. Дж Вирол. 2011;85:2416–2428. дои: 10.1128/ОВИ.01449-10. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Lin HH, Lee TY, Chen DS, Sung JL, Ohto H, Etoh T, et al. Трансплацентарная утечка HBeAg-положительной материнской крови как наиболее вероятный путь внутриутробного инфицирования вирусом гепатита В. J Педиатр. 1987; 111: 877–881. [PubMed] [Google Scholar]
J Педиатр. 1987; 111: 877–881. [PubMed] [Google Scholar]
16. Lazizi Y, Badur S, Perk Y, Ilter O, Pillot J. Избирательная невосприимчивость к вакцине HBsAg у новорожденных, связанная с внутриутробным переносом ДНК вируса гепатита B. вакцина. 1997;15:1095–1100. [PubMed] [Google Scholar]
17. Kim GA, Lee HC, Kim MJ, Ha Y, Park EJ, An J и др. Заболеваемость гепатоцеллюлярной карциномой после серологического клиренса HBsAg у пациентов с хроническим гепатитом В: необходимость наблюдения. J Гепатол. 2015;62:1092–1099. doi:10.1016/j.jhep.2014.11.031. [PubMed] [Google Scholar]
18. Cohen E, Tran TT. Гепатит В у женского населения. Гастроэнтерол Клин Норт Ам. 2016;45:359–370. doi: 10.1016/j.gtc.2016.02.011. [PubMed] [Академия Google]
19. Фонтана Р.Дж. Побочные эффекты длительной пероральной противовирусной терапии гепатита В. Гепатология. 2009; 49: С185–С195. doi: 10.1002/hep.22885. [PubMed] [Google Scholar]
20. Chu CM, Lin CC, Chen YC, Jeng WJ, Lin SM, Liaw YF. Мутация базального основного промотора связана с прогрессированием цирроза, а не гепатоцеллюлярной карциномы при хронической инфекции вируса гепатита В. Бр Дж Рак. 2012;107:2010–2015. doi: 10.1038/bjc.2012.474. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Мутация базального основного промотора связана с прогрессированием цирроза, а не гепатоцеллюлярной карциномы при хронической инфекции вируса гепатита В. Бр Дж Рак. 2012;107:2010–2015. doi: 10.1038/bjc.2012.474. [Бесплатная статья PMC] [PubMed] [Google Scholar]
21. Брунетто М.Р., Оливери Ф., Коломбатто П., Морикони Ф., Чиккоросси П., Коко Б. и соавт. Уровни поверхностного антигена гепатита В в сыворотке крови помогают отличить активных носителей вируса гепатита В генотипа D от неактивных. Гастроэнтерология. 2010; 139: 483–490. doi:10.1053/j.gastro.2010.04.052. [PubMed] [Google Scholar]
22. Lau GK, Piratvisuth T, Luo KX, Marcellin P, Thongsawat S, Cooksley G, et al. Пегинтерферон альфа-2а, ламивудин и их комбинация при HBeAg-положительном хроническом гепатите В. N Engl J Med. 2005; 352: 2682–269.5. doi:10.1056/NEJMoa043470. [PubMed] [Google Scholar]
23. Shaheen AA, Myers RP. Исходы беременности у больных циррозом печени: популяционное исследование. Печень инт. 2010;30:275–283. doi:10.1111/j.1478-3231.2009.02153.x. [PubMed] [Google Scholar]
doi:10.1111/j.1478-3231.2009.02153.x. [PubMed] [Google Scholar]
24. Kim HY, Choi JY, Park CH, Jang JW, Kim CW, Bae SH и др. Исход после прекращения приема противовирусных препаратов во время беременности у женщин, инфицированных вирусом гепатита В. Джей Клин Вирол. 2013; 56: 299–305. doi:10.1016/j.jcv.2012.11.019. [PubMed] [Google Scholar]
25. Pan CQ, Duan ZP, Bhamidimarri KR, Zou HB, Liang XF, Li J, et al. Алгоритм оценки риска и вмешательства передачи вируса гепатита В от матери ребенку. Клин Гастроэнтерол Гепатол. 2012; 10: 452–459. doi:10.1016/j.cgh.2011.10.041. [PubMed] [Google Scholar]
26. Tse KY, Ho LF, Lao T. Влияние материнского статуса носительства HBsAg на исходы беременности: исследование случай-контроль. J Гепатол. 2005; 43: 771–775. doi:10.1016/j.jhep.2005.05.023. [PubMed] [Академия Google]
27. Лао Т.Т., Чан Б.К., Леунг В.К., Хо Л.Ф., Це К.Ю. Инфицирование матери гепатитом В и гестационный сахарный диабет. J Гепатол. 2007; 47:46–50. doi:10.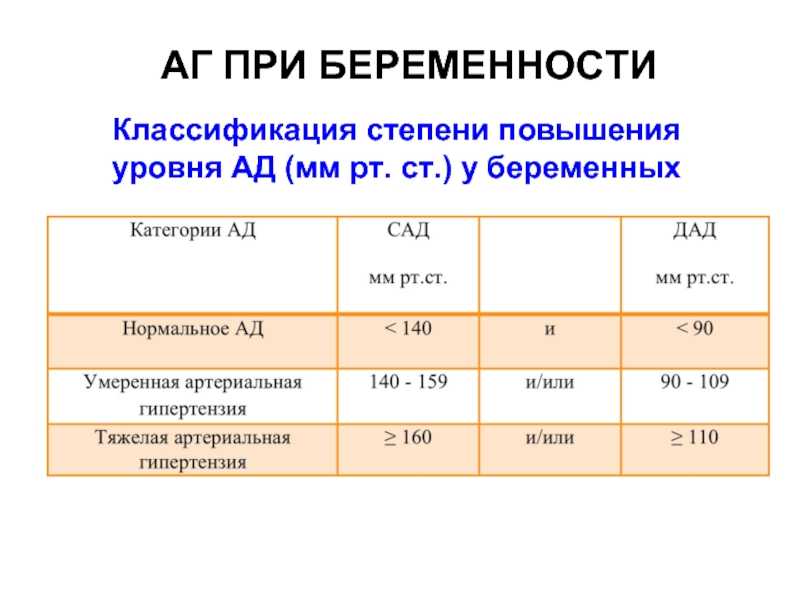 1016/j.jhep.2007.02.014. [PubMed] [Google Scholar]
1016/j.jhep.2007.02.014. [PubMed] [Google Scholar]
28. Американский колледж акушеров и гинекологов. Практический бюллетень ACOG № 86: Вирусный гепатит у беременных. Акушерство Гинекол. 2007; 110:941–956. doi: 10.1097/01.AOG.0000263930.28382.2a. [PubMed] [Google Scholar]
29. Нгуен Г., Гарсия Р.Т., Нгуен Н., Трин Х., Киффе Э.Б., Нгуен М.Х. Клиническое течение инфекции вирусом гепатита В во время беременности. Алимент Фармакол Тер. 2009 г.;29:755–764. doi:10.1111/j.1365-2036.2009.03932.x. [PubMed] [Google Scholar]
30. Zou H, Chen Y, Duan Z, Zhang H, Pan C. Вирусологические факторы, связанные с неэффективностью пассивно-активной иммунопрофилактики у детей, рожденных от HBsAg-положительных матерей. J Вирусная гепатит. 2012;19:e18–e25. doi:10.1111/j.1365-2893.2011.01492.x. [PubMed] [Google Scholar]
31. Bai H, Zhang L, Ma L, Dou XG, Feng GH, Zhao GZ. Взаимосвязь инфицирования вирусом гепатита В плацентарного барьера и механизма внутриутробной передачи вируса гепатита В. Мир J Гастроэнтерол. 2007; 13:3625–3630. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Мир J Гастроэнтерол. 2007; 13:3625–3630. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32. Кар П., Мишра С. Лечение гепатита В во время беременности. Эксперт Опин Фармаколог. 2016;17:301–310. дои: 10.1517/14656566.2016.1118051. [PubMed] [Google Scholar]
33. Han GR, Cao MK, Zhao W, Jiang HX, Wang CM, Bai SF, et al. Проспективное открытое исследование эффективности и безопасности телбивудина при беременности для профилактики перинатальной передачи инфекции, вызванной вирусом гепатита В. J Гепатол. 2011;55:1215–1221. doi:10.1016/j.jhep.2011.02.032. [PubMed] [Академия Google]
34. Pan CQ, Han GR, Jiang HX, Zhao W, Cao MK, Wang CM, et al. Телбивудин предотвращает вертикальную передачу от HBeAg-позитивных женщин с хроническим гепатитом В. Клин Гастроэнтерол Гепатол. 2012;10:520–526. doi:10.1016/j.cgh.2012.01.019. [PubMed] [Google Scholar]
35. Chen HL, Lee CN, Chang CH, Ni YH, Shyu MK, Chen SM, et al. Эффективность материнского тенофовира дизопроксила фумарата в прерывании передачи вируса гепатита В от матери ребенку. Гепатология. 2015;62:375–386. doi: 10.1002/hep.27837. [PubMed] [Академия Google]
Гепатология. 2015;62:375–386. doi: 10.1002/hep.27837. [PubMed] [Академия Google]
36. Han GR, Jiang HX, Zhao W, Ge CY, Xu CL, Pan C. Использование ламивудина во 2-м или 3-м триместре беременности имеет аналогичную эффективность в предотвращении вертикальной передачи (VT) хронического гепатита B (CHB) у матери с высокой виремией. Гепатология. 2011;54:479А. [Google Scholar]
37. Xu WM, Cui YT, Wang L, Yang H, Liang ZQ, Li XM, et al. Ламивудин на поздних сроках беременности для предотвращения перинатальной передачи инфекции, вызванной вирусом гепатита В: многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование. J Вирусная гепатит. 2009 г.;16:94–103. doi:10.1111/j.1365-2893.2008.01056.x. [PubMed] [Google Scholar]
38. Ayres A, Yuen L, Jackson KM, Manoharan S, Glass A, Maley M, et al. Кратковременный прием ламивудина для профилактики передачи вируса гепатита В во время беременности: отсутствие эффективности и выбор резистентных мутаций. J Вирусная гепатит. 2014;21:809–817. дои: 10.1111/jvh.12212. [PubMed] [Google Scholar]
2014;21:809–817. дои: 10.1111/jvh.12212. [PubMed] [Google Scholar]
39. Уиттакер Г., Эррера Дж.Л. Гепатит В при беременности. South Med J. 2014; 107: 195–200. Дои: 10.1097/SMJ.0000000000000077. [PubMed] [Google Scholar]
40. Lamberth JR, Reddy SC, Pan JJ, Dasher KJ. Хронический гепатит В во время беременности. Мир J Гепатол. 2015;7:1233–1237. дои: 10.4254/wjh.v7.i9.1233. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Lee SD, Lo KJ, Tsai YT, Wu JC, Wu TC, Yang ZL, et al. Роль кесарева сечения в профилактике передачи вируса гепатита В от матери ребенку. Ланцет. 1988; 2: 833–834. doi: 10.1016/S0140-6736(88)92792-4. [PubMed] [Академия Google]
42. Hu Y, Chen J, Wen J, Xu C, Zhang S, Xu B, et al. Влияние планового кесарева сечения на риск передачи вируса гепатита В от матери ребенку. BMC Беременность Роды. 2013;13:119. дои: 10.1186/1471-2393-13-119. [Бесплатная статья PMC] [PubMed] [Google Scholar]
43. Общество медицины матери и плода (SMFM) Dionne-Odom J, Tita AT, Silverman NS.
