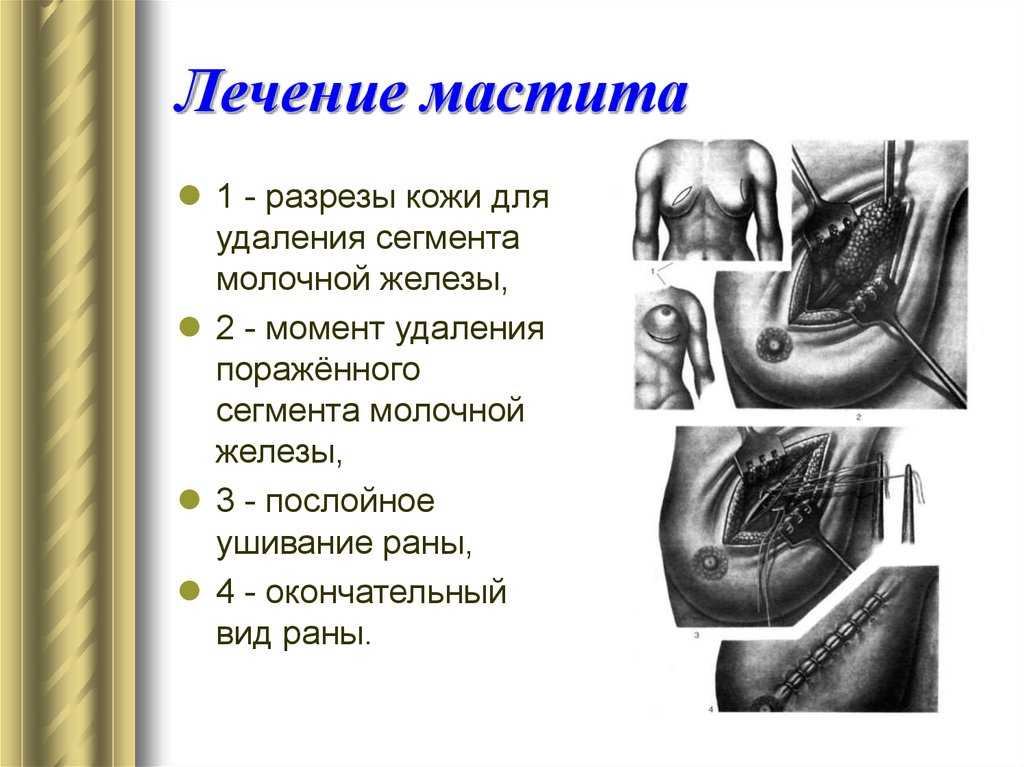
Серозного мастита лечение: Серозный мастит: симптомы, причины и лечение
патогенез, признаки и симптомы, лечение
Содержимое
- 1 Что такое серозный мастит
- 2 Этиология и патогенез серозного мастита у коров
- 3 Клинические признаки серозного мастита у коров
- 4 Как лечить серозный мастит у коровы
- 4.1 Народные средства лечения серозного мастита
- 5 Профилактические мероприятия
- 6 Заключение
Серозный мастит у коров доставляет немало хлопот заводчику. Снижаются удои и качество молока, в запущенных случаях лактация полностью прекращается. Без вмешательства ветеринара вылечить животное сложно.
Что такое серозный мастит
Серозный мастит – серьезное и часто встречающееся заболевание у коров в послеродовом периоде. Молочные железы воспаляются, наполняются жидкостью. Подобного рода отклонения случаются по разным причинам, но чаще всего из-за бактериальных инфекций. Они попадают в организм и поражают треть молочной железы или вымя целиком.
Болезнетворные бактерии попадают через трещины в сосках и мигрируют к другим внутренним органам. Протоки молочной железы сдавливаются, перестают нормально работать, в результате чего происходит воспаление. Молоко полностью меняет свой состав.
Протоки молочной железы сдавливаются, перестают нормально работать, в результате чего происходит воспаление. Молоко полностью меняет свой состав.
Важно! Молочные продукты от больной коровы непригодны в пищу.
Этиология и патогенез серозного мастита у коров
Серозный мастит развивается стремительно и поражает треть стада после отела. Именно поэтому важно знать основные причины его возникновения, правила лечения и профилактики.
История болезни начинается с микробов, которые проникают в кровь и лимфу коровы. Из-за серозного мастита прекращается выработка гормона окситоцина, который отвечает за количество молока. Обмен веществ в тканях вымени нарушается. Начинается воспалительный процесс с более или менее выраженными симптомами мастита. К ним присоединяется болезненность вымени.
Без достаточного опыта определить серозный мастит сложно
Если вовремя не придать значения и не лечить серозный мастит, то он переходит на молочные протоки, начинается более серьезная стадия заболевания.
Основной причиной развития серозного мастита является снижение иммунитета после отела, но есть и другие факторы:
- послеродовые осложнения;
- повреждение вымени;
- заболевание ЖКТ;
- антисанитарные условия содержания;
- неправильное и неполное доение коровы.
Послеродовые осложнения часто наблюдаются у первотелок, когда развивается эндометриоз или не полностью выходит послед. К серозному маститу приводят механические повреждения вымени, различные заболевания, вызванные неправильным кормлением и антисанитарные условия в помещении для коров. Очень часто причиной серозного мастита может стать некачественная дойка. Остатки молока постепенно скапливаются в вымени, что приводит к появлению воспалительного процесса.
Клинические признаки серозного мастита у коров
Воспаление начинается внезапно и протекает быстро, уже в первые сутки можно заметить, что животное ведет себя подозрительно. Самые первые симптомы мастита, по которым можно заподозрить неладное – вялость и отсутствие аппетита. В дальнейшем к ним присоединяются характерные для серозного мастита проявления:
В дальнейшем к ним присоединяются характерные для серозного мастита проявления:
- вымя становится твердым, отекает, появляется болезненность при пальпации;
- корова проявляет раздражительность, испытывает страх;
- ткани вымени меняют оттенок, краснеют;
- температура тела животного повышается, вымя становится горячим;
- молоко приобретает нехарактерный синюшный оттенок, в нем появляются хлопья;
- количество молока резко снижается.
Первоначальные симптомы серозного мастита очень похожи на обычный застой, но постепенно картина проясняется. Существуют характерные различия, о которых нужно помнить. При застое вымя остается мягким, на ощупь как тесто, а при серозном мастите оно сразу затвердевает.
Предупреждение! При первых же признаках мастита нужно сразу обратиться к ветеринару, чтобы вовремя остановить процесс.
Как лечить серозный мастит у коровы
Прогнозы при лечении серозного мастита благоприятные. Если при первых же симптомах обратиться к ветеринару, то через 10 дней корова будет здорова. Однако если микробы проникли в альвеолярную часть молочной железы, то заболевание может приобрести хронический характер. В самом запущенном случае возникают осложнения в виде некроза тканей, что может привести к летальному исходу.
Однако если микробы проникли в альвеолярную часть молочной железы, то заболевание может приобрести хронический характер. В самом запущенном случае возникают осложнения в виде некроза тканей, что может привести к летальному исходу.
Чтобы лечение мастита было успешным, оно должно быть комплексным и включать в себя ряд мероприятий. Для начала больную корову отсаживают от других особей, переводят на стойловое содержание. В ее рационе должны присутствовать преимущественно сухие корма, водопой временно ограничивают. После этого делают массаж и сцеживают содержимое вымени. Дойку проводят 4-5 раз в день, исключая ночное время.
Чтобы не занести инфекцию, при работе нужно соблюдать стерильность
При сильном поражении вымени делают инъекции окситоцина, чтобы экссудат легче отходил. Также для очистки протоков выполняют промывание раствором гидрокарбоната натрия. Для обеззараживания применяют антибактериальную терапию, кроме того, накладывают мази и согревающие повязки. Курс антибиотиков составляет не менее пяти дней.
Согревающие мази и гели направлены на рассасывание сгустков в вымени. Их накладывают тонким слоем. Подходят мази Вишневского, ихтиоловая и гепариновая. Во время лечения серозного мастита корову нужно изолировать от сквозняков. Помещение должно быть теплым, но хорошо проветриваемым. Это способствует скорейшему рассасыванию сгустков.
Внимание! Мази и согревающие повязки при мастите разрешается накладывать только на 3-4 сутки после того, как воспаление немного утихнет.
Из лекарственных препаратов, которые прошли сертификацию и показали лучшие результаты при лечении серозного мастита, можно выделить следующие:
- «Мастисан-А». Лекарство на основе стрептомицина и сульфадимезина, которые дают стойкий антибактериальный эффект. Выпускается в виде жидкости для инъекций по 5 и 20 мл. На начальных стадиях болезни достаточно одного укола. В запущенных случаях раствор вводят каждые сутки до полного выздоровления. Молоко используют в пищу через трое суток.
- «Мастомицин».
 Гель на основе гентамицина и лидокаина. Он дает хороший обезболивающий эффект, кроме того, борется с различной бактериальной микрофлорой. Препарат полностью готов к использованию. На начальной стадии делают две инъекции через каждые 12 ч. В тяжелых случаях допускается до шести уколов с тем же промежутком.
Гель на основе гентамицина и лидокаина. Он дает хороший обезболивающий эффект, кроме того, борется с различной бактериальной микрофлорой. Препарат полностью готов к использованию. На начальной стадии делают две инъекции через каждые 12 ч. В тяжелых случаях допускается до шести уколов с тем же промежутком. - «Масти Вейксим». Немецкий препарат, который оказывает положительное влияние на состояние животного. Для выздоровления достаточно двух инъекций.
Можно использовать и другие антибактериальные препараты, которые вводят через сосок в вымя. Однако нужно строго соблюдать дозировку и точность введения. Неправильная процедура добавит проблем в лечении мастита и вызовет дополнительное инфицирование. Это чревато осложнениями.
Народные средства лечения серозного мастита
Некоторые животноводы прибегают к народным средствам лечения серозного мастита. Для этого активно применяют обычное хозяйственное мыло. Все пораженные участки хорошо им натирают, оставляют на 30 мин. , после чего смывают теплой водой и протирают насухо. Процедуру повторяют до полного выздоровления.
, после чего смывают теплой водой и протирают насухо. Процедуру повторяют до полного выздоровления.
Также против отеков и инфекций при серозном мастите хорошо помогает глиняная болтушка.
Компрессы ставят на 20-30 мин.
На начальных стадиях мастита в питье больным коровам добавляют настои трав. Подходят отвары ромашки и крапивы. Их же можно использовать для компрессов и примочек.
Профилактические мероприятия
Чтобы избежать такого неприятного заболевания у коров как серозный мастит, нужно позаботиться о профилактике. Большое значение имеют условия содержания животного и качественный уход, а также хорошее кормление. Питание телки должно быть сбалансированным, содержать все необходимые витамины и минералы. Кроме того, для профилактики серозного мастита не нужно пренебрегать плановыми профилактическими осмотрами.
Во время доения следует соблюдать стерильность. Все оборудование и инвентарь должны быть чистыми. Вымя телки нужно тщательно мыть и протирать обеззараживающими растворами. Особое внимание в уходе уделяют беременным и недавно отелившимся коровам.
Особое внимание в уходе уделяют беременным и недавно отелившимся коровам.
Заключение
Серозный мастит у коров можно полностью вылечить, если вовремя обратиться за квалифицированной помощью. Однако в любом случае придется прибегнуть к антибактериальной терапии, чтобы избежать повторного инфицирования. Помимо этого, для восстановления иммунитета и поддержки организма нужно активно давать корове витаминные комплексы. Кроме того, особое внимание уделяют профилактике.
признаки, симптомы, причины, диагностика и способы лечения заболевания
Мастит – это воспалительное поражение молочной железы, протекающее в острой или хронической форме. Возникает при инфицировании тканей патогенной микрофлорой и имеет тенденцию к распространению.
Выделяют несколько путей попадания патогенной микрофлоры в ткани молочной железы:
- попадание микробного агента через расширенные молочные ходы в послеродовой период;
- занесение микроба в результате травмы молочной железы или через трещины на сосках;
- распространение возбудителя из близлежащих пораженных очагов.

Таким образом в соответствии с механизмом инфицирования различают:
- лактационный мастит;
- нелактационный мастит.
Принято считать, что основным возбудителем данного заболевания является золотистый стафилококк. Именно он в своем большинстве провоцирует развитие гнойно-воспалительных процессов у человека. Однако для его проникновения необходимо наличие благоприятных условий. К ним относятся:
- заболевание мастопатией;
- послеоперационные изменения тканей;
- врожденные аномалии развития молочной железы;
- тяжело протекающая беременность, роды;
- наличие сопутствующих заболеваний;
- перенесенные острые вирусные, бактериальные инфекции.
СИМПТОМЫ
В клинической картине мастита принято выделять несколько форм переходящих одна в другую соответственно:
- серозная форма – наличие тяжести и болезненных ощущений в груди, при пальпации прощупывается небольшое образование с четкими границами.
 Возможно повышение температуры и ухудшение общего состояния;
Возможно повышение температуры и ухудшение общего состояния; - инфильтративная форма – границы образования в молочной железе становятся нечеткими, нарастает болезненность. Молочная железа увеличивается в размерах. Общее состояние ухудшается, температура поднимается до более высоких цифр;
- деструктивная форма – в этой стадии происходит массивный выброс токсинов в кровь, что обуславливает высокую температуру, значительную слабость у пациентки. Молочная железа воспалена, остро болезненна, отечна. Кожа в этой зоне краснеет, а подмышечные лимфоузлы начинают отдавать болью.
Диагностика мастита
Очаг воспаления в молочной железе определяется пальпаторно. Также отмечается увеличение (иногда умеренная болезненность при пальпации) подмышечных лимфоузлов со стороны пораженной груди. Нагноение характеризуется определением симптома флюктуации.
При проведении УЗИ молочных желез обнаруживается типичная картина воспаления молочной железы. Серозный мастит характеризуется сглаживанием эхографической картины дифференцированных структур железы, расширением млечных протоков, утолщением кожи и подкожной клетчатки. Инфильтрат в молочной железе выглядит как хорошо очерченная ограниченная зона сниженной эхогенности, при прогрессировании возникает картина «пчелиных сот». Хорошо визуализируется при УЗИ формирование абсцессов, и выявляются зоны некроза. Специфичность и достоверность методики достигает 90%.
Серозный мастит характеризуется сглаживанием эхографической картины дифференцированных структур железы, расширением млечных протоков, утолщением кожи и подкожной клетчатки. Инфильтрат в молочной железе выглядит как хорошо очерченная ограниченная зона сниженной эхогенности, при прогрессировании возникает картина «пчелиных сот». Хорошо визуализируется при УЗИ формирование абсцессов, и выявляются зоны некроза. Специфичность и достоверность методики достигает 90%.
Поскольку диагностика мастита, как правило, не вызывает сложностей, маммографию обычно не проводят. При сомнительной ультразвуковой картине для гистологического исследования берут аспират (тонкоигольная аспирационная биопсия молочной железы под контролем УЗИ). Для бактериологического исследования можно взять молоко из пораженной железы.
В случае вялого течения воспаления и в результате формирования вокруг него валика фиброзной ткани (сумкования очага) говорят о развитии хронического мастита. При этом клинические проявления обычно слабо выражены, но при пальпации определяется плотный малоподвижный, спаянный с кожей очаг.
Лечение мастита
При малейшем подозрении на развитие воспаления в молочной железе необходимо срочно обратиться к врачу маммологу, поскольку в лечении этого заболевания очень важно своевременное выявление и незамедлительное принятие мер к устранению причины мастита и подавлению инфекционного процесса. Самолечение или затягивание с обращением к специалисту недопустимо, поскольку воспаление молочной железы склонно к прогрессированию, формированию нагноения и абсцедированию. В случае развития гнойного мастита необходимо оперативное лечение.
При выявлении мастита на стадии серозного воспаления или инфильтрата проводят консервативное лечение мастита. Назначается антибиотикотерапия с применением сильно действующих средств широкого спектра действия. Серозный мастит при этом, как правило, проходит через 2-3 дня, для рассасывания инфильтрата может потребоваться до 7 дней. Если воспалению сопутствует выраженная общая интоксикация, проводят дезинтоксикационные мероприятия (инфузия растворов электролитов, глюкозы). При выраженной избыточной лактации назначают средства для ее подавления.
При выраженной избыточной лактации назначают средства для ее подавления.
Гнойные формы мастита, как правило, требуют хирургического вмешательства. Развившийся абсцесс молочной железы является показанием к экстренной хирургической санации: вскрытию мастита и дренированию гнойного очага.
Прогрессирующий мастит вне зависимости от его стадии является противопоказанием к дальнейшему вскармливанию (в том числе и здоровой грудью), поскольку грудное молоко, как правило, инфицировано и содержит токсические продукты распада тканей. Для ребенка патологически измененное грудное молоко может стать причиной развития дисбактериоза и расстройства функционального состояния пищеварительной системы. Поскольку терапия мастита включает антибиотики, кормление в этот период так же небезопасно для младенца. Антибиотики могут заметно повредить нормальному развитию и росу органов и тканей. Во время лечения мастита можно сцеживать молоко, пастеризовать и только после этого давать ребенку.
Показания к подавлению лактации: отсутствие динамики при серозном и инфильтративном мастите не протяжении трех суток антибиотикотерапии, развитие гнойной формы, сосредоточение воспалительного очага непосредственно под соском, имеющийся гнойный мастит в анамнезе матери, сопутствующие патологии органов и систем, значительно ухудшающие общее самочувствие матери.
причины, симптомы, диагностика, лечение и профилактика
Согласно статистике, в 85% случаев мастит развивается у первородящих женщин, что может быть связано с нарушением проходимости молочных протоков из-за неправильного сцеживания молока. Течение мастита грудной железы острое, но иногда оно бывает и хроническим.
Различают послеродовой или острый лактационный мастит, наблюдающийся у кормящих матерей, а также фиброзно-кистозный мастит, который не связан с грудным вскармливанием.
С учетом особенностей протекания воспалительного процесса острый мастит подразделяется на:
- серозный,
- инфильтративный,
- гнойный.
Причины развития мастита
Основной причиной развития мастита является инфицирование тканей молочной железы через трещины в сосках, ведь любые дефекты кожи являются воротами для падания туда бактерий. После родов женский организм ослаблен и во многих случаях плохо борется с инфекцией, поступившей извне. Лактостаз (застой молока в протоках молочных желез), хронические тонзиллит, пиелонефрит, нарушение нормального гормонального баланса, стрессы, простудные заболевания, наследственная предрасположенность и снижение иммунитета также могут спровоцировать развитие мастита. Опасным для здоровья может оказаться даже ношение тесного белья, которое сдавливает протоки, тем самым провоцируя нарушение прохождения молока.
Лактостаз (застой молока в протоках молочных желез), хронические тонзиллит, пиелонефрит, нарушение нормального гормонального баланса, стрессы, простудные заболевания, наследственная предрасположенность и снижение иммунитета также могут спровоцировать развитие мастита. Опасным для здоровья может оказаться даже ношение тесного белья, которое сдавливает протоки, тем самым провоцируя нарушение прохождения молока.
Нелактационный мастит чаще всего проявляется вследствие попадания инфекции во внутренние ткани груди из-за травм груди и пирсинга (прокола с целью носить украшения) сосков.
Симптомы мастита
Серозный мастит является самым ранним этапом заболевания, который характеризуется незначительным повышением температуры тела, увеличением молочной железы в объеме, а также общей болезненностью при ощупывании груди. Первые симптомы этого заболевания могут проявиться достаточно быстро, в течение одного-двух часов. Инфильтративный мастит проявляется в случае отсутствия лечения первой стадии мастита и проявляется лихорадкой и появлением в груди локальных болезненных зон. Становится затруднительно кормить ребенка, наблюдаются слабость, озноб, головная боль.
Становится затруднительно кормить ребенка, наблюдаются слабость, озноб, головная боль.
Гнойный мастит у женщин проявляется нагноением участка груди и сопровождается повышением температуры тела от 39 С и выше, сильнейшими болями в молочной железе и увеличением лимфатических узлов в подмышечной области.
При нелактационном мастите также наблюдаются болезненность в области груди, выраженное покраснение кожи, выделение гноя из соска, повышение температуры тела и интоксикация организма.
ОН КЛИНИК медицинские центры в Москве
Диагностика мастита
Диагностика мастита основывается на опросе пациентки маммологом и пальпации (ощупывания) молочной железы. Также может потребоваться анализ крови, а для определения типа бактерий, поразивших организм кормящей матери, и их чувствительности к различным антибиотикам производят бактериологическое исследование молока. Для правильной постановки диагноза применяется и УЗИ.
Кормление грудью в этот период следует прекратить, но при этом не забывать о сцеживании, чтобы молочные железы освобождались от инфицированного бактериями молока.
Как лечить мастит
Лечение как лактационного, так и нелактационного мастита должно проходить только в медицинском учреждении, под руководством опытного врача.
Ни в коем случае нельзя заниматься самолечением и следовать советам, найденным на просторах интернета: это чревато развитием осложнений вплоть до сепсиса – инфекционного заболевания крови, которое может привести к летальному исходу!
Лечение мастита у кормящих матерей должно начаться как можно раньше, при появлении первых симптомов, не дожидаясь, пока мастит станет гнойным. Опытные маммологи Международного медицинского центра ОН КЛИНИК на первом же приеме подскажут, что нужно делать при послеродовом или нелактационном мастите, как его вылечить, каким образом можно избежать осложнений и как при необходимости сохранить грудное вскармливание.
Основными лекарственными средствами в лечении мастита являются антибиотики. Гнойные формы этого заболевания в большинстве случаев требуют хирургического лечения.
Лечение мастита у женщин в ОН КЛИНИК проходит по авторским разработкам и методикам, признанным в ведущих клиниках Европы и США. Чтобы избавиться от мастита, необходимо своевременно обращаться к маммологам ОН КЛИНИК, что позволит получить необходимые навыки ухода за молочной железой и избежать деформации формы груди, образования свищей и развития других осложнений.
Автор статьи
Поделиться
Подпишитесь на рассылку
И получайте полезную информацию о здоровье на email, раз в неделю
Нажимая на кнопку подписаться вы соглашаетесь с правилами обработки персональной информации.
Другие заболевания
Внутрипротоковая папиллома
Гинекомастия
Доброкачественные опухоли молочной железы
Злокачественные опухоли молочной железы
Киста молочной железы
Листовидная фиброаденома
Мастит
Мастопатия
Фиброаденома молочной железы
Острый мастит — StatPearls — Книжная полка NCBI
Непрерывное обучение
Мастит можно разделить на лактационные и нелактационные причины. Хотя причины мастита, не связанные с лактацией, встречаются реже, лактационный мастит является распространенным заболеванием, поражающим женщин, кормящих грудью. В этом упражнении рассматривается оценка, диагностика и лечение различных форм мастита, а также подчеркивается роль межпрофессиональной команды в оценке и лечении пациентов с этими состояниями.
Хотя причины мастита, не связанные с лактацией, встречаются реже, лактационный мастит является распространенным заболеванием, поражающим женщин, кормящих грудью. В этом упражнении рассматривается оценка, диагностика и лечение различных форм мастита, а также подчеркивается роль межпрофессиональной команды в оценке и лечении пациентов с этими состояниями.
Цели:
Объясните патофизиологию лактационного мастита.
Определите факторы риска развития лактационного мастита.
Опишите клиническую картину пациента с идиопатическим гранулематозным маститом.
Объясните важность сотрудничества и общения между межпрофессиональной командой для улучшения результатов лечения пациентов с лактационным маститом.
Получите доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Введение
Мастит — это воспаление ткани молочной железы, которое можно разделить на лактационный и нелактационный мастит. Лактационный мастит является наиболее распространенной формой мастита. Два типа нелактационного мастита включают перидуктальный мастит и идиопатический гранулематозный мастит (ИГМ).
Лактационный мастит является наиболее распространенной формой мастита. Два типа нелактационного мастита включают перидуктальный мастит и идиопатический гранулематозный мастит (ИГМ).
Лакционный мастит, также известный как послеродовой мастит, обычно возникает из-за длительного наполнения молочных протоков инфекционными компонентами из-за проникновения бактерий через повреждения кожи. У пациентов может развиться очаговая эритема, боль и отек, а также сопутствующие системные симптомы, включая лихорадку. Чаще всего это происходит в первые шесть недель грудного вскармливания, но может произойти в любое время во время лактации, причем в большинстве случаев исчезает через 3 месяца.[1]
Перидуктальный мастит — это доброкачественное воспалительное заболевание, поражающее субареолярные протоки и чаще всего встречающееся у женщин репродуктивного возраста. Идиопатический гранулематозный мастит — это редкое доброкачественное воспалительное заболевание, которое может клинически имитировать рак молочной железы. [1] Заболевание возникает в основном у рожавших женщин, чаще всего в течение 5 лет после родов.[1]
[1] Заболевание возникает в основном у рожавших женщин, чаще всего в течение 5 лет после родов.[1]
Этиология
Лактационный мастит чаще всего вызывается бактериями, колонизирующими кожу, Staphylococcus aureus является наиболее распространенным. Метициллин-резистентный S. aureus (MRSA) становится все более распространенной причиной мастита, и следует учитывать факторы риска для MRSA. Другие возбудители включают виды Streptococcus pyogenes , Escherichia coli , Bacteroides и коагулазоотрицательные стафилококки. Факторы риска лактационного мастита включают мастит в анамнезе, трещины и трещины на сосках, неадекватное выделение молока, материнский стресс, недостаток сна, тесные бюстгальтеры и использование противогрибковых кремов для сосков.[2][3]
Причина перидуктального мастита не ясна. Однако многие предполагают, что курение может быть связано с развитием этого состояния путем прямого повреждения протоков и последующего воспаления. Бактерии выделяют в культурах у 62-85% пациентов с перидуктальным маститом, и наиболее распространенными возбудителями являются Staphylococcus aureus , Pseudomonas aeruginosa , Enterococcus , Bacteroides 1 и Proteus 20094. ] Ожирение и сахарный диабет также считаются возможными факторами риска.[5]
Бактерии выделяют в культурах у 62-85% пациентов с перидуктальным маститом, и наиболее распространенными возбудителями являются Staphylococcus aureus , Pseudomonas aeruginosa , Enterococcus , Bacteroides 1 и Proteus 20094. ] Ожирение и сахарный диабет также считаются возможными факторами риска.[5]
Этиология идиопатического гранулематозного мастита (ИГМ) остается неясной. Возможными причинами могут быть аутоиммунные заболевания, травмы, лактация, использование оральных противозачаточных таблеток и гиперпролактинемия. Также может быть связь с Corynebacterium , особенно у пациентов с гистологическими данными кистозного нейтрофильного гранулематозного мастита (CNGM) [7].
Эпидемиология
Во всем мире лактационный мастит встречается у 2-30% кормящих женщин.[8] В Соединенных Штатах зарегистрированная заболеваемость составляет от 7% до 10%.[2][9].] Заболеваемость является самой высокой в первые три недели после родов.[10]
Пациенты с перидуктальным маститом чаще всего являются женщинами репродуктивного возраста, и это почти исключительно связано с употреблением табака. [10] Перидуктальный мастит встречается у 5-9 % женщин во всем мире.[11]
[10] Перидуктальный мастит встречается у 5-9 % женщин во всем мире.[11]
IGM встречается очень редко, и его истинная распространенность неизвестна.[12] IGM возникает у рожавших женщин, обычно в течение пяти лет после родов. Большинство затронутых пациентов сообщают о грудном вскармливании в анамнезе и у них развиваются симптомы от шести месяцев до двух лет после прекращения грудного вскармливания[13]. Средний возраст начала заболевания – от 32 до 34 лет.[13] Несколько исследований показали более высокую частоту IGM в латиноамериканском населении.
Патофизиология
Лактационный мастит возникает из-за сочетания неадекватного оттока молока и внедрения бактерий. Распространенные сценарии, приводящие к плохому оттоку молока, включают нечастое кормление, избыток молока, быстрое отлучение от груди, болезни матери или ребенка и закупорку молочных протоков.[3] Неадекватно слитое молоко застаивается, и в нем размножаются микроорганизмы, что приводит к инфекции. Считается, что бактерии (обычно изо рта младенца или с кожи матери) попадают в молоко через трещины в соске. [2]
[2]
Патофизиология перидуктального мастита остается неясной. Считается, что курение играет роль в патогенезе, прямо или косвенно повреждая протоки, что приводит к последующему некрозу и инфекции. Плоскоклеточная метаплазия является находкой у пациентов с этим заболеванием, и считается, что десквамированные метапластические клетки могут образовывать пробку, ведущую к закупорке протока и последующей инфекции [18]. Одно недавнее исследование показало активацию IFN-γ, и IL-12A у пациентов с перидуктальным маститом по сравнению с контрольной группой.[5] Это цитокины, секретируемые клетками Th2, которые играют роль в эрадикации чужеродных патогенов. Активация этих цитокинов предполагает, что иммунный ответ может играть роль в патогенезе перидуктального мастита.
Патофизиология IGM остается неясной, но наиболее широко распространенная теория указывает на аутоиммунную деструкцию, инициированную специфическим триггером, таким как травма, бактерии или экстравазатное молоко. [14] Это вызывает просачивание выделений из протоков в ткань молочной железы, а воспалительные клетки инфильтрируют и вызывают гранулематозную реакцию.[19]
[14] Это вызывает просачивание выделений из протоков в ткань молочной железы, а воспалительные клетки инфильтрируют и вызывают гранулематозную реакцию.[19]
Гистопатология
Идиопатический гранулематозный мастит (ИГМ) характеризуется неказеозными гранулемами с эпителиоидными гистиоцитами и многоядерными гигантскими клетками в дольках молочной железы. В подтипе CNGM классическими гистологическими признаками являются неказеозные гранулемы с характерными кистозными пространствами, выстланными нейтрофилами, содержащими грамположительные кокки. Важно отметить, что биопсия обычно не рекомендуется для оценки перидуктального мастита или лактационного мастита.
Анамнез и физикальное исследование
Лактационному маститу часто предшествует нагрубание или фокальная закупорка протока. Пациенты могут сообщить об этих сопутствующих симптомах в анамнезе до развития классических признаков мастита. Лактационный мастит характеризуется очаговой, плотной, эритематозной, опухшей и болезненной областью одной молочной железы, а также лихорадкой (выше или равной 100,4 градусам по Фаренгейту). Пациенты часто испытывают системные симптомы, такие как озноб, миалгии и недомогание.
Пациенты часто испытывают системные симптомы, такие как озноб, миалгии и недомогание.
Признаки перидуктального мастита включают периареолярное или субареолярное образование, которое может сопровождаться болью и эритемой. Пациенты могут иметь инверсию сосков, густые выделения из сосков, абсцесс молочной железы или дренирующие свищи.
IGM чаще всего проявляется плотным односторонним образованием молочной железы. Другие признаки могут включать втягивание соска, утолщение кожи, подмышечную лимфаденопатию, изъязвление и образование абсцесса.[23] Многие из этих признаков совпадают с признаками злокачественного новообразования молочной железы, и иногда это может быть ошибочно диагностировано на ранней стадии. Пациенты с IGM также могут испытывать экстрамаммарные проявления, включая артралгии, эписклерит и кожные изменения [24].
Оценка
Диагноз лактационного мастита основывается на анамнезе и клинических данных. Если есть опасения, что у пациентки может быть абсцесс молочной железы, можно сделать УЗИ молочных желез. При наличии абсцесса будут видны гипоэхогенные участки гнойного содержимого. Для пациентов с тяжелой инфекцией, которая не реагирует на первоначальную антибактериальную терапию, культура грудного молока может быть полезна для выбора подходящего антибиотика. Однако в этом нет необходимости. Точно так же, если есть подозрение на бактериемию у пациента с тяжелым маститом, следует получить посев крови. Однако они не являются частью рутинного обследования.[11]
При наличии абсцесса будут видны гипоэхогенные участки гнойного содержимого. Для пациентов с тяжелой инфекцией, которая не реагирует на первоначальную антибактериальную терапию, культура грудного молока может быть полезна для выбора подходящего антибиотика. Однако в этом нет необходимости. Точно так же, если есть подозрение на бактериемию у пациента с тяжелым маститом, следует получить посев крови. Однако они не являются частью рутинного обследования.[11]
Перидуктальный мастит — это прежде всего клинический диагноз. Если имеется отделяемое из соска, необходимо провести окрашивание по Граму и посев для выявления любых ассоциированных организмов. Если есть сопутствующее образование и подозрение на злокачественность, следует провести ультразвуковое исследование или маммографию.[11]
Поскольку клинические признаки IGM совпадают с признаками рака молочной железы, для постановки этого диагноза необходимо провести биопсию. Биопсия толстой иглы или эксцизионная биопсия являются жизнеспособными вариантами. Из-за предполагаемой связи между гиперпролактинемией и IGM может быть отправлен уровень пролактина. Ультразвук и маммография недостаточны для того, чтобы отличить IGM от злокачественной опухоли молочной железы.[13]
Из-за предполагаемой связи между гиперпролактинемией и IGM может быть отправлен уровень пролактина. Ультразвук и маммография недостаточны для того, чтобы отличить IGM от злокачественной опухоли молочной железы.[13]
Лечение/управление
Первоначальное лечение лактационного мастита – симптоматическое лечение.[25] Было показано, что продолжение полного опорожнения груди снижает продолжительность симптомов у пациентов, получавших лечение как антибиотиками, так и без них. Пациентов следует поощрять к продолжению грудного вскармливания, молокоотсоса или ручного сцеживания.[19][8][9] Если больной перестанет выделять молоко, произойдет дальнейший стаз, и инфекция будет прогрессировать. Для контроля боли можно использовать нестероидные противовоспалительные препараты (НПВП). Тепло, приложенное к груди непосредственно перед опорожнением, может помочь увеличить выделение молока и облегчить опорожнение. [25] Холодные компрессы, прикладываемые к груди после опорожнения, могут помочь уменьшить отек и боль.
Если симптомы лактационного мастита сохраняются более 12–24 часов, следует ввести антибиотики.[8][9] Поскольку S. aureus является наиболее распространенной причиной, антибактериальная терапия должна быть подобрана соответствующим образом. В условиях легкой инфекции без факторов риска MRSA амбулаторное лечение можно начинать с диклоксациллина или цефалексина. Если у пациента аллергия на пенициллин, можно использовать эритромицин. Если у пациента есть факторы риска заражения MRSA, варианты лечения включают триметоприм-сульфаметоксазол (TMP-SMX) или клиндамицин. TMP-SMX следует избегать у женщин, кормящих грудью детей в возрасте до 1 месяца, а также у детей с желтухой или недоношенных. Если пациенту требуется госпитализация, следует начинать эмпирическое лечение ванкомицином до восстановления посева и чувствительности. Недостаточно исследований по соответствующей продолжительности амбулаторного лечения, но большинство источников рекомендуют 10-14-дневный курс [10].
Перидуктальный мастит лечится эмпирически амоксициллином-клавуланатом. Альтернативные варианты включают диклоксациллин плюс метронидазол или цефалексин плюс метронидазол. При наличии абсцесса предпочтительной стратегией лечения является аспирация иглой под ультразвуковым контролем в сочетании с антибактериальной терапией [11]. Перидуктальный мастит часто является рецидивирующим заболеванием. Если у пациента есть рецидивирующие инфекции, может потребоваться хирургическое иссечение воспаленных протоков.[26]
Альтернативные варианты включают диклоксациллин плюс метронидазол или цефалексин плюс метронидазол. При наличии абсцесса предпочтительной стратегией лечения является аспирация иглой под ультразвуковым контролем в сочетании с антибактериальной терапией [11]. Перидуктальный мастит часто является рецидивирующим заболеванием. Если у пациента есть рецидивирующие инфекции, может потребоваться хирургическое иссечение воспаленных протоков.[26]
Лечение IGM остается спорным. Современные стратегии лечения сильно различаются и могут включать наблюдение, кортикостероиды, иммунодепрессанты, антибиотики и хирургическое вмешательство.[23] IGM — это доброкачественное состояние, которое обычно проходит без лечения в среднем через 5 месяцев. Недавнее исследование показало, что время до разрешения симптомов не различалось у пациентов, получавших медикаментозное лечение, и у пациентов, получавших наблюдение и поддерживающую терапию.[23] Хирургическое иссечение является вариантом, но сообщается о 10% рецидивах, даже при хирургическом лечении. Если IGM осложняется вторичной инфекцией, антибиотики следует выбирать на основе посева и чувствительности.
Если IGM осложняется вторичной инфекцией, антибиотики следует выбирать на основе посева и чувствительности.
Дифференциальный диагноз
Дифференциальный диагноз трех форм мастита существенно различается. Обычные дифференциальные диагнозы для каждого следующие:
Лактационный мастит
Перидуктальный мастит
Duct Ectasia
Abscess
CARCINOMA
CARCINOMA
MURDATIST
9003
9000 9000 9004
. пациентов с маститом выздоровеет при соответствующем лечении. Частота рецидивов для каждого типа мастита варьируется следующим образом:
Лактационный мастит: 8–30 % [27][28]
Перидуктальный мастит: 4–28 % [17]
Идиопатический гранулематозный мастит 30]
В одном исследовании сообщалось, что 38% пациентов с IGM сообщили о значительных рубцах, а 29% сообщили о длительной боли. [30]
[30]
Осложнения
Одним из наиболее частых осложнений лактационного мастита является раннее прекращение грудного вскармливания. Заболевание молочной железы и связанная с ним боль являются одними из наиболее часто упоминаемых причин раннего прекращения грудного вскармливания.[25][31] Абсцесс молочной железы является еще одним осложнением лактационного мастита и встречается у 3–11 % пациентов.[32][25] Развитие абсцесса молочной железы более распространено, если мастит не лечить на ранней стадии.
Перидуктальный мастит и ВГМ могут осложняться образованием абсцесса или свища. Обе формы нелактационного мастита связаны с рецидивами и могут привести к рубцеванию и деформации ткани молочной железы.
Сдерживание и обучение пациентов
Лактационный мастит обычно развивается после периода неполного дренирования и застоя молока. Важно информировать пациентов о том, как ограничить этот застой, чтобы предотвратить мастит. Вопросы, которые следует обсудить, могут включать в себя подходящую частоту кормления и правильную технику прикладывания ребенка к груди. Боль в сосках является распространенной жалобой кормящих женщин и может привести к менее частым кормлениям. Это увеличивает застой молока, тем самым увеличивая риск развития мастита. Важно консультировать пациентов о том, как справиться с болью и уменьшить ее. Пациенты с лактационным маститом могут чувствовать склонность к прекращению грудного вскармливания в период болезни, возможно, из-за сочетания дискомфорта и боли, а также опасения передачи инфекции их ребенку. Медицинские работники должны гарантировать пациентке, что грудное вскармливание с маститом безопасно и что при желании им следует продолжать это делать.[33] Если пациентка не хочет продолжать кормить грудью, ее следует проконсультировать о важности опорожнения груди и обучить альтернативным методам, таким как использование молокоотсоса или ручное сцеживание.
Боль в сосках является распространенной жалобой кормящих женщин и может привести к менее частым кормлениям. Это увеличивает застой молока, тем самым увеличивая риск развития мастита. Важно консультировать пациентов о том, как справиться с болью и уменьшить ее. Пациенты с лактационным маститом могут чувствовать склонность к прекращению грудного вскармливания в период болезни, возможно, из-за сочетания дискомфорта и боли, а также опасения передачи инфекции их ребенку. Медицинские работники должны гарантировать пациентке, что грудное вскармливание с маститом безопасно и что при желании им следует продолжать это делать.[33] Если пациентка не хочет продолжать кормить грудью, ее следует проконсультировать о важности опорожнения груди и обучить альтернативным методам, таким как использование молокоотсоса или ручное сцеживание.
Помимо обучения пациентов, не менее важным является обучение медицинских работников. Одно небольшое исследование показало, что некоторые медицинские работники дезинформируют пациентов с маститом о том, что они должны прекратить грудное вскармливание во время инфицирования. [28] Это не только увеличивает вероятность развития абсцесса у пациентки, но также способствует раннему прекращению грудного вскармливания, что лишает как пациентку, так и младенца связанных с этим преимуществ.[33]
[28] Это не только увеличивает вероятность развития абсцесса у пациентки, но также способствует раннему прекращению грудного вскармливания, что лишает как пациентку, так и младенца связанных с этим преимуществ.[33]
Перидуктальный мастит встречается почти исключительно у курильщиков. Поощрение отказа от курения имеет важное значение и может помочь снизить риск повторного воспаления.
Жемчуг и другие предметы
Баллы на вынос
Одним из наиболее важных соображений при лечении лактационного мастита является необходимость продолжать опорожнять молочные железы. Поощряйте пациенток продолжать кормить грудью, если они этого хотят, а если нет, поощряйте использование молокоотсоса или ручного сцеживания.
Лакционный мастит можно лечить консервативно с поддерживающими мерами в течение первых 12–24 часов. Если симптомы не улучшаются по истечении этого периода, следует начать прием антибиотиков.
Если симптомы лактационного мастита не улучшаются в течение 24–28 часов, рассмотрите возможность абсцесса молочной железы и сделайте УЗИ.

Идиопатический гранулематозный мастит — редкое заболевание, которое часто принимают за рак молочной железы. Биопсия должна быть сделана, чтобы диагностировать это состояние и исключить более серьезную патологию.
Большинство пациентов с маститом могут лечиться амбулаторно. Примеры сценариев, при которых пациенту может потребоваться госпитализация, включают следующее: гемодинамическая нестабильность, непереносимость перорального приема пищи, тяжелое обезвоживание и рецидивирующая инфекция, не поддающаяся амбулаторному лечению.
Улучшение результатов работы команды здравоохранения
Лакционный мастит является распространенным заболеванием среди кормящих женщин. В этой статье обсуждается несколько поддающихся изменению факторов риска, таких как слишком редкое кормление, использование определенных кремов для сосков, неправильная техника захвата груди и тесные бюстгальтеры, которые предрасполагают женщин к этому заболеванию. Просвещение вскоре после родов с целью повышения осведомленности матерей об этих факторах риска потенциально может привести к снижению заболеваемости маститом. При обучении таких женщин следует использовать межпрофессиональный командный подход. Вклад врача, медперсонала и консультанта по грудному вскармливанию должен быть объединен в общие усилия, направленные на снижение заболеваемости этим заболеванием.
Просвещение вскоре после родов с целью повышения осведомленности матерей об этих факторах риска потенциально может привести к снижению заболеваемости маститом. При обучении таких женщин следует использовать межпрофессиональный командный подход. Вклад врача, медперсонала и консультанта по грудному вскармливанию должен быть объединен в общие усилия, направленные на снижение заболеваемости этим заболеванием.
Хотя пациенты с лактационным маститом могут обратиться за помощью к своему акушеру, нередко эти пациенты обращаются в учреждения неотложной помощи, отделения неотложной помощи или к семейным врачам для обследования. По этой причине важно, чтобы врачи в каждом из этих условий знали о надлежащем лечении этого состояния. Весь медицинский персонал, ухаживающий за пациентами с маститом, должен знать о рекомендации продолжать грудное вскармливание этих пациентов и о том, что внезапное прекращение грудного вскармливания увеличивает риск образования абсцесса.[Уровень 3][33]
Пациентам, обращающимся за помощью в отделение неотложной помощи, часто приходится долго ждать, и в это время может потребоваться сцеживание или уход. В некоторых больницах есть помпы, которые можно проверить у пациентов в отделении неотложной помощи. Врачи скорой помощи должны знать правила своей больницы, чтобы получить помпу, если она необходима. Часто это можно скоординировать либо с консультационной группой по грудному вскармливанию, либо с командой акушеров.
В некоторых больницах есть помпы, которые можно проверить у пациентов в отделении неотложной помощи. Врачи скорой помощи должны знать правила своей больницы, чтобы получить помпу, если она необходима. Часто это можно скоординировать либо с консультационной группой по грудному вскармливанию, либо с командой акушеров.
Если врач не уверен, безопасен ли антибиотик, который он прописывает, во время грудного вскармливания, он может нанять опытного фармацевта, чтобы убедиться, что пациентка получает лекарство, которое позволит ей продолжать кормить ребенка грудью.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Алтинтопрак Ф., Кивилчим Т., Озкан О.В. Этиология идиопатического гранулематозного мастита. Мировые дела J Clin. 2014 г., 16 декабря; 2(12):852-8. [Бесплатная статья PMC: PMC4266833] [PubMed: 25516860]
- 2.
Фоксман Б., Д’Арси Х., Гиллеспи Б., Бобо Дж. К., Шварц К. Лакционный мастит: возникновение и лечение среди 946 кормящих женщин в США. Am J Эпидемиол. 2002 г., 15 января; 155 (2): 103–14. [PubMed: 117
]
- 3.
Fetherston C. Факторы риска лактационного мастита. Дж. Гум Лакт. 1998 июнь; 14 (2): 101-9. [PubMed: 9775842]
- 4.
Бандред, Нью-Джерси, Диксон Дж.М., Ламсден А.Б., Рэдфорд Д., Худ Дж., Майлз Р.С., Четти Ю., Форрест А.П. Являются ли очаги эктазии протоков стерильными? Бр Дж Сур. 1985 г., октябрь; 72 (10): 844-5. [PubMed: 4041720]
- 5.
Liu L, Zhou F, Wang P, Yu L, Ma Z, Li Y, Gao D, Zhang Q, Li L, Yu Z. Перидуктальный мастит: воспалительное заболевание, связанное с бактериальной инфекцией и последующим иммунным ответом? Медиаторы воспаления. 2017;2017:5309081. [Бесплатная статья PMC: PMC5274658] [PubMed: 28182101]
- 6.
Бутон М.Е., Винтон Л.М., Ганди С.Г., Джаярам Л.
 , Патель П.Н., О’Нил П.Дж., Коменака И.К. Временное разрешение идиопатического гранулематозного мастита с возобновлением терапии бромокриптином при пролактиноме. Отчет по делу Int J Surg, 2015; 10:8-11. [Бесплатная статья PMC: PMC4429849] [PubMed: 25781920]
, Патель П.Н., О’Нил П.Дж., Коменака И.К. Временное разрешение идиопатического гранулематозного мастита с возобновлением терапии бромокриптином при пролактиноме. Отчет по делу Int J Surg, 2015; 10:8-11. [Бесплатная статья PMC: PMC4429849] [PubMed: 25781920]- 7.
Johnstone KJ, Robson J, Cherian SG, Wan Sai Cheong J, Kerr K, Bligh JF. Кистозный нейтрофильный гранулематозный мастит, ассоциированный с Corynebacterium, включая Corynebacterium kroppenstedtii. Патология. 2017 июнь;49(4):405-412. [PubMed: 28442140]
- 8.
Schoenfeld EM, McKay MP. Мастит и метициллин-резистентный золотистый стафилококк (MRSA): затишье перед бурей? J Emerg Med. 2010 май;38(4):e31-4. [В паблике: 19232875]
- 9.
Spencer JP. Лечение мастита у кормящих женщин. Ам семейный врач. 2008 г., 15 сентября; 78(6):727-31. [PubMed: 18819238]
- 10.
Boakes E, Woods A, Johnson N, Kadoglou N. Инфекция молочной железы: обзор методов диагностики и лечения.
 Eur J Здоровье груди. 2018 июль; 14 (3): 136-143. [Бесплатная статья PMC: PMC6092150] [PubMed: 30123878]
Eur J Здоровье груди. 2018 июль; 14 (3): 136-143. [Бесплатная статья PMC: PMC6092150] [PubMed: 30123878]- 11.
Стахс А., Стуберт Дж., Реймер Т., Хартманн С. Доброкачественная болезнь молочной железы у женщин. Dtsch Arztebl Int. 201909 августа; 116 (33-34): 565-574. [Бесплатная статья PMC: PMC6794703] [PubMed: 31554551]
- 12.
Сарагоса Сарагоса C, Hostalet Robles F, Kosny P, Morcillo Rodenas MÁ. [Идиопатический гранулематозный мастит: состояние без окончательного лечения]. Cir Esp. 2013 ноябрь; 91 (9): 615-6. [PubMed: 22717103]
- 13.
Плугес-Турулл К.В., Наньес Дж. Э., Кинтеро К.Дж., Ализай Х., Майс Д.Д., Кист К.А., Дорнблут, Северная Каролина. Идиопатический гранулематозный мастит: проявления мультимодальной визуализации и подводные камни. Рентгенография. 2018 март-апрель;38(2):330-356. [В паблике: 29528819]
- 14.
Шрипати С., Аячит А., Бала А., Кадавигере Р., Кумар С. Идиопатический гранулематозный мастит: диагностическая дилемма для рентгенолога молочной железы.
 Инсайты. 2016 авг; 7 (4): 523-9. [Бесплатная статья PMC: PMC4956625] [PubMed: 27164916]
Инсайты. 2016 авг; 7 (4): 523-9. [Бесплатная статья PMC: PMC4956625] [PubMed: 27164916]- 15.
Barreto DS, Sedgwick EL, Nagi CS, Benveniste AP. Гранулематозный мастит: этиология, визуализация, патология, лечение и клинические данные. Лечение рака молочной железы. 2018 Октябрь; 171 (3): 527-534. [В паблике: 29971624]
- 16.
Джозеф К.А., Луу X, Мор А. Гранулематозный мастит: опыт государственной больницы Нью-Йорка. Энн Сург Онкол. 2014 Декабрь; 21 (13): 4159-63. [PubMed: 25008030]
- 17.
Zhang Y, Zhou Y, Mao F, Guan J, Sun Q. Клинические характеристики, классификация и хирургическое лечение перидуктального мастита. Дж. Торак Дис. 2018 апр;10(4):2420-2427. [Бесплатная статья PMC: PMC5949503] [PubMed: 29850148]
- 18.
Таффурелли М., Пеллегрини А., Сантини Д., Занотти С., Ди Симоне Д., Серра М. Рецидивирующий перидуктальный мастит: хирургическое лечение. Операция. 2016 Декабрь;160(6):1689-1692.
 [PubMed: 27616631]
[PubMed: 27616631]- 19.
Thomsen AC, Espersen T, Maigaard S. Течение и лечение застоя молока, неинфекционного воспаления груди и инфекционного мастита у кормящих женщин. Am J Obstet Gynecol. 1984 г., 01 июля; 149 (5): 492-5. [PubMed: 6742017]
- 20.
Wang Y, LeGolvan M, Chapin K, Mainiero M. Кистозный нейтрофильный гранулематозный мастит с коринебактериями и стафилококками, имитирующими карциному молочной железы. Clin Case Rep. 2018 Nov;6(11):2208-2210. [Бесплатная статья PMC: PMC6230645] [PubMed: 30455922]
- 21.
Goulabchand R, Hafidi A, Van de Perre P, Millet I, Maria ATJ, Morel J, Quellec AL, Perrochia H, Guilpain P. Мастит при аутоиммунных заболеваниях: обзор литературы, диагностика Путь и патофизиологические ключевые игроки. Дж. Клин Мед. 30 марта 2020 г.; 9(4) [бесплатная статья PMC: PMC7231219] [PubMed: 32235676]
- 22.
Dixon JM. Перидуктальный мастит/эктазия протоков.
 Мир J Surg. 1989 ноябрь-декабрь; 13(6):715-20. [PubMed: 2696225]
Мир J Surg. 1989 ноябрь-декабрь; 13(6):715-20. [PubMed: 2696225]- 23.
Дэвис Дж., Кокко Д., Мац С., Хсу Ч., Браун М.Дж., Ли Дж., Бутон М.Е., Карузо Д.М., Коменака И.К. Повторная оценка того, остается ли наблюдение лучшим методом лечения идиопатического гранулематозного мастита. Операция. 2019 декабрь; 166(6):1176-1180. [PubMed: 31400951]
- 24.
Махмодлу Р., Дадха Н., Аббаси Ф., Насири Дж., Вализаде Р. Идиопатический гранулематозный мастит: дилеммы диагностики и лечения. Электронный врач. 9(9) сентября 2017 г.: 5375-5379. [Бесплатная статья PMC: PMC5633240] [PubMed: 2
- 24]
- 25.
Abou-Dakn M, Richardt A, Schaefer-Graf U, Wöckel A. Воспалительные заболевания молочной железы во время лактации: застой молока, послеродовой мастит, абсцессы молочной железы и злокачественные опухоли — текущие и фактические данные -Основа стратегии диагностики и терапии. Уход за грудью (Базель). 2010 март;5(1):33-37. [Бесплатная статья PMC: PMC3357165] [PubMed: 22619640]
- 26.

Lannin DR. Двадцатидвухлетний опыт лечения рецидивирующего субареолярного абсцесса и свища млечного протока у одного хирурга-маммолога. Am J Surg. 2004 г., октябрь; 188 (4): 407-10. [В паблике: 15474436]
- 27.
Фогель А., Хатчисон Б.Л., Митчелл Э.А. Мастит в первый год после родов. Рождение. 1999 декабрь; 26 (4): 218-25. [PubMed: 10655826]
- 28.
Скотт Дж. А., Робертсон М., Фитцпатрик Дж., Найт С., Малхолланд С. Возникновение лактационного мастита и медикаментозное лечение: проспективное когортное исследование в Глазго. Int Breastfeed J. 2008, 25 августа; 3:21. [Бесплатная статья PMC: PMC2542350] [PubMed: 18721487]
- 29.
Oltean HN, Soliman AS, Omar OS, Youssef TF, Karkouri M, Abdel-Aziz A, Hablas A, Blachley T, Tahri A, Merajver SD. Факторы риска хронического мастита в Марокко и Египте. Int J Inflam. 2013;2013:184921. [Бесплатная статья PMC: PMC3847959] [PubMed: 24327928]
- 30.
Néel A, Hello M, Cottereau A, Graveleau J, De Faucal P, Costedoat-Chalumeau N, Rondeau-Lutz M, Lavigne C , Chiche L, Hachulla E, Seiberras S, Cabane J, Tournemaine N, Hamidou M. Долгосрочные результаты идиопатического гранулематозного мастита: западное многоцентровое исследование. QJM. 2013 май; 106(5):433-41. [PubMed: 23407345]
- 31.
Schwartz K, D’Arcy HJ, Gillespie B, Bobo J, Longeway M, Foxman B. Факторы, связанные с отлучением от груди в первые 3 месяца после родов. Дж. Фам Практ. 2002 май; 51 (5): 439-44. [PubMed: 12019051]
- 32.
Кауфманн Р., Фоксман Б. Мастит у кормящих женщин: возникновение и факторы риска. соц. мед. 1991;33(6):701-5. [PubMed: 1957190]
- 33.
Амир Л.Х., Комитет протокола Академии грудного вскармливания. Клинический протокол ABM № 4: мастит, пересмотренный в марте 2014 г., грудное вскармливание. 2014 июнь;9(5):239-43. [Бесплатная статья PMC: PMC4048576] [PubMed: 24911394]
Мастит крупного рогатого скота — репродуктивная система
За некоторыми исключениями, мастит возникает, когда микробы попадают в сосок через сосковый канал. Почти любой микроб может оппортунистически проникнуть в сосковый канал и вызвать мастит. Однако большинство инфекций вызывается различными видами стрептококков (или подобных грамположительных кокков), стафилококками и грамотрицательными палочками, особенно ферментирующими лактозу микроорганизмами кишечного происхождения, обычно называемыми кишечными палочками . С эпидемиологической точки зрения первичные резервуары инфекции для большинства патогенов можно рассматривать как контагиозные или экологические, хотя это разделение может быть неоднозначным для некоторых патогенов.
Почти любой микроб может оппортунистически проникнуть в сосковый канал и вызвать мастит. Однако большинство инфекций вызывается различными видами стрептококков (или подобных грамположительных кокков), стафилококками и грамотрицательными палочками, особенно ферментирующими лактозу микроорганизмами кишечного происхождения, обычно называемыми кишечными палочками . С эпидемиологической точки зрения первичные резервуары инфекции для большинства патогенов можно рассматривать как контагиозные или экологические, хотя это разделение может быть неоднозначным для некоторых патогенов.
За исключением Mycoplasma spp, которые могут передаваться от коровы к корове воздушно-капельным путем и проникать в вымя после бактериемии, заразное распространение патогенов происходит во время доения через такие пути, как руки дояра или вкладыши доильного аппарата Ед. изм. Виды, которые в основном используют этот путь передачи, включают Staphylococcus aureus , Streptococcus agalactiae и Corynebacterium bovis . Большинство других видов являются условно-патогенными микроорганизмами из окружающей среды коровы, хотя другие стрептококки и стафилококки также могут иметь контагиозный компонент.
Большинство других видов являются условно-патогенными микроорганизмами из окружающей среды коровы, хотя другие стрептококки и стафилококки также могут иметь контагиозный компонент.
Кроме того, контагиозная передача патогенов, обычно связанных с резервуарами в окружающей среде, происходит нечасто, например, за счет развития адаптированных к хозяину факторов вирулентности ( Escherichia coli ) или выделения подавляющего числа бактерий из инфицированного вымени ( Trueperella [ранее Arcanobacterium ] pyogenes и Lactococcus spp.). Контагиозная передача также была определена как возможный путь заражения водорослей 9.0041 Prototheca zopfii .
Подстилка, используемая для содержания крупного рогатого скота, является основным источником патогенов из окружающей среды, но зараженные растворы для обработки сосков, интрамаммарные инфузии, вода, используемая для подготовки вымени перед доением, водяные пруды или грязевые ямы, повреждения кожи, травмы сосков и мухи — все это инкриминируется как источники инфекции.
Интрамаммарные инфекции (ИМИ) часто описывают как субклинический или клинический мастит. Субклинический мастит — наличие инфекции без явных признаков местного воспаления или системного поражения. Хотя могут появляться преходящие эпизоды аномального молока, субклинический мастит в большинстве случаев протекает бессимптомно. Если инфекция сохраняется в течение как минимум двух месяцев, инфекция называется хронической. Однажды установленные, многие из этих инфекций сохраняются в течение всей лактации или жизни коровы, хотя это зависит от возбудителя.
Выявление субклинического мастита лучше всего проводить путем анализа молока на количество соматических клеток (ПСК) (преимущественно лейкоцитов) с использованием Калифорнийского теста на мастит или автоматических методов, предоставляемых организациями по улучшению молочного стада. ПКР положительно коррелируют с наличием инфекции. Воспалительные изменения и снижение качества молока могут начаться при уровне SCC всего 100 000 клеток/мл. Несмотря на вариабельность (особенно при определении в одном анализе), SCC ≥200 000 клеток/мл у коровы указывает на высокую вероятность инфекции. Аналогичным образом, чем выше SCC в резервуаре для хранения стада, тем выше распространенность инфекции в стаде. Стадные SCC
Несмотря на вариабельность (особенно при определении в одном анализе), SCC ≥200 000 клеток/мл у коровы указывает на высокую вероятность инфекции. Аналогичным образом, чем выше SCC в резервуаре для хранения стада, тем выше распространенность инфекции в стаде. Стадные SCC
Удои снижаются у коров с субклиническим маститом. Потери молока из-за воспалений прямо пропорциональны SCC индивидуальной коровы; по мере увеличения SCC производство молока снижается. Эти потери могут быть особенно значительными, если ИМИ возникает в начале лактации и сохраняется в виде хронической инфекции на протяжении всей лактации.
Клинический мастит — это воспалительная реакция на инфекцию, вызывающая явно ненормальное молоко (например, цвет, сгустки фибрина). По мере увеличения степени воспаления могут также проявляться изменения в вымени (отек, жар, боль, покраснение). Клинические случаи, которые включают только местные признаки, относятся к легким или умеренным. Если воспалительная реакция включает системное поражение (лихорадка, анорексия, шок), случай называется тяжелым. Если начало очень быстрое, как это часто бывает при тяжелых клинических случаях, это называется острым или тяжелым маститом. У коров с более тяжелым поражением обычно наблюдаются серозные выделения в пораженной четверти.
Если начало очень быстрое, как это часто бывает при тяжелых клинических случаях, это называется острым или тяжелым маститом. У коров с более тяжелым поражением обычно наблюдаются серозные выделения в пораженной четверти.
Хотя при субклиническом мастите одновременно может быть заражено любое количество четвертей, обычно клинический мастит проявляется только у одной четверти. Однако клинические эпизоды, вызванные Mycoplasma , нередко поражают несколько кварталов. Гангренозный мастит Клинический мастит За некоторыми исключениями мастит возникает, когда микробы попадают в сосок через сосковый канал. Почти любой микроб может оппортунистически проникнуть в сосковый канал и вызвать мастит. Тем не менее, большинство инфекций… читать далее также могут возникать, особенно при субклинических, хронических инфекциях S. aureus становятся тяжелыми во время иммунной дисфункции (например, во время родов). Как и в случае субклинического мастита, посев образцов молока, взятых из пораженных четвертей, является единственным надежным методом определения этиологии клинических случаев.
Размер стада и доля молока, производимого большими стадами, увеличивается в молочной промышленности США и во всем мире. Таким образом, зависимость от наемных работников, а также от иммигрантов для выполнения важнейших задач, таких как доение коров, также увеличивается. Кроме того, многие менеджеры молочной фермы, вероятно, имеют ограниченные знания в области управления персоналом и опыт управления. Таким образом, они, как правило, не воспринимают себя как тренеров сотрудников; это часто приводит к разочарованию из-за дрейфа протоколов и ощущению, что сотрудники не заинтересованы в том, чтобы участвовать в успехе фермы сверх предписанных инструкций. В совокупности это привело к разрыву между потребностями в человеческих ресурсах, возникающими в отрасли, и возможностями производителей и менеджеров по их удовлетворению.
Хотя обширные исследования и клинические испытания определили основы борьбы с маститом, знания этих концепций у сотрудников часто отсутствуют по сравнению с управляющими стадом. Наилучшие протоколы качества молока потерпят неудачу, если протоколы будут соблюдаться непоследовательно. Вопреки распространенному мнению, большинство сотрудников заявили в опросах, что они хотят узнать больше не только о том, как следует выполнять протоколы, но и о том, почему они важны. Таким образом, ветеринары имеют возможность помогать в обучении и обучении сотрудников и выступать в качестве «учителей естественных наук на ферме».
Наилучшие протоколы качества молока потерпят неудачу, если протоколы будут соблюдаться непоследовательно. Вопреки распространенному мнению, большинство сотрудников заявили в опросах, что они хотят узнать больше не только о том, как следует выполнять протоколы, но и о том, почему они важны. Таким образом, ветеринары имеют возможность помогать в обучении и обучении сотрудников и выступать в качестве «учителей естественных наук на ферме».
Во всех молочных стадах есть коровы с субклиническим маститом; однако распространенность инфицированных коров колеблется от 5% до 75%, а в кварталах от 2% до 40%. Многие различные возбудители могут вызвать хроническую инфекцию, при которой клинические признаки мастита проявляются лишь изредка. Исторически борьба с субклиническим маститом была сосредоточена на инфекционных патогенах S agalactiae и S aureus , а также на других грамположительных кокках, в первую очередь на Streptococcus dysgalactiae (который также может быть заразным или патогенным из окружающей среды) 9. 0041 Streptococcus uberis , энтерококки и множество других ненауреусных стафилококков (ранее называвшихся коагулазонегативными стафилококками), в том числе Staphylococcus hyicus , S epidermidis , S xylosus 900 S 1 и 9004. Были идентифицированы стада со значительным субклиническим маститом, вызванным грамотрицательными палочками, такими как Klebsiella sp, Serratia marcescens , Pseudomonas aeruginosa , и другими атипичными патогенами, такими как Candida spp. и Prototheca zopfii . Из-за увеличения размера стад в молочной промышленности и более частых перемещений крупного рогатого скота между стадами и географическими районами, Mycoplasma spp, особенно M bovis , был признан частым патогеном в некоторых стадах, при этом у коров проявляются как субклинические, так и клинические признаки.
0041 Streptococcus uberis , энтерококки и множество других ненауреусных стафилококков (ранее называвшихся коагулазонегативными стафилококками), в том числе Staphylococcus hyicus , S epidermidis , S xylosus 900 S 1 и 9004. Были идентифицированы стада со значительным субклиническим маститом, вызванным грамотрицательными палочками, такими как Klebsiella sp, Serratia marcescens , Pseudomonas aeruginosa , и другими атипичными патогенами, такими как Candida spp. и Prototheca zopfii . Из-за увеличения размера стад в молочной промышленности и более частых перемещений крупного рогатого скота между стадами и географическими районами, Mycoplasma spp, особенно M bovis , был признан частым патогеном в некоторых стадах, при этом у коров проявляются как субклинические, так и клинические признаки.
В отношении инфекционных патогенов наибольшему риску заражения подвергается взрослый лактирующий крупный рогатый скот. Первичным резервуаром инфекции является молочная железа; передача инфекции происходит при доении либо руками дояра, либо доильным оборудованием, выступающим в роли фомита. Сообщалось, что первородящие телки заражаются стафилококками и стрептококками до отела, хотя распространенность сильно различается в разных стадах и географических регионах. Дерматит конца соска, вызванный роговой мухой, Haematobia irritans , который может содержать S aureus , был связан с повышенным риском заражения телок, особенно в более теплом климате.
Сообщалось, что первородящие телки заражаются стафилококками и стрептококками до отела, хотя распространенность сильно различается в разных стадах и географических регионах. Дерматит конца соска, вызванный роговой мухой, Haematobia irritans , который может содержать S aureus , был связан с повышенным риском заражения телок, особенно в более теплом климате.
Для S. agalactiae, S. aureus, и не-aureus стафилококков сезонные колебания заболеваемости незначительны или отсутствуют.
Терапия субклинического мастита проводится исходя из того, что затраты на лечение будут перевешиваться приростом производства после ликвидации инфекции, и что профилактика всегда предпочтительнее. Также иммунная функция лейкоцитов в лактирующей железе нарушена по сравнению с другими тканями, например, легкими. По этим причинам ожидания и необходимость лечения ИМИ следует тщательно взвесить, а у лактирующих коров вообще избегать. Это особенно актуально, если при лечении не учитываются возбудитель или продолжительность инфекции.
В случае контагиозных возбудителей элиминация может привести к уменьшению резервуара инфекции у ранее неинфицированных коров. Никаких существенных экономических потерь не произойдет в результате отсрочки терапии до тех пор, пока не будет завершена бактериальная культура. Однако многие субклинические ИИМ являются хроническими, и, особенно в случае S. aureus , прогнозирование терапевтического исхода с помощью тестирования in vitro ненадежно. Распределение препарата после интрамаммарного введения может быть неадекватным из-за обширного фиброза и образования микроабсцессов в железе. Коровы с длительной инфекцией (> 3 месяцев), зараженные более чем на четверть или инфицированные патогенами, устойчивыми к противомикробным препаратам, обычно используемым для интрамаммарных инфузий, вероятно, будут невосприимчивы к терапии.
С S agalactiae открывается необычная возможность успешного лечения субклинического ИИМ. Распространенность ИМИ, вызванного этим возбудителем, можно быстро снизить, обработав противомикробными препаратами всех инфицированных коров в стаде. Все четыре четверти инфицированных коров должны быть пролечены, чтобы обеспечить элиминацию возбудителя и предотвратить возможное перекрестное заражение незараженной четверти. Показатели излечения часто колеблются от 75% до 90%. Предпочтение отдается помеченным коммерческим препаратам для внутригрудного введения, содержащим амоксициллин, пенициллин или цефалоспорины. Употребление наркотиков, происходящих из многодозовые флаконы (с маркировкой для системной терапии) следует использовать для интрамаммарной терапии , а не , поскольку коммерческие препараты для интрамаммарной терапии имеют более высокие стандарты контроля качества в отношении стерильности и более высокую надежность для прогнозирования периодов воздержания от молока и мяса после лечения . Крайне важно применять строгие асептические методы (например, использование пропитанных спиртом прокладок для подготовки кончиков сосков) всякий раз, когда вводится какой-либо продукт для инфузии интрамаммарно.
Все четыре четверти инфицированных коров должны быть пролечены, чтобы обеспечить элиминацию возбудителя и предотвратить возможное перекрестное заражение незараженной четверти. Показатели излечения часто колеблются от 75% до 90%. Предпочтение отдается помеченным коммерческим препаратам для внутригрудного введения, содержащим амоксициллин, пенициллин или цефалоспорины. Употребление наркотиков, происходящих из многодозовые флаконы (с маркировкой для системной терапии) следует использовать для интрамаммарной терапии , а не , поскольку коммерческие препараты для интрамаммарной терапии имеют более высокие стандарты контроля качества в отношении стерильности и более высокую надежность для прогнозирования периодов воздержания от молока и мяса после лечения . Крайне важно применять строгие асептические методы (например, использование пропитанных спиртом прокладок для подготовки кончиков сосков) всякий раз, когда вводится какой-либо продукт для инфузии интрамаммарно.
Стада, проходящие экстенсивную терапию против S agalactiae , должны контролироваться SCC и последующим посевом молока для дальнейшего выявления коров, не пролеченных или вылеченных во время первоначальной терапии. Обычно 30-дневные интервалы мониторинга успешны. Небольшой процент коров не будет реагировать на терапию, и их лучше отделить или выбраковать. Кроме того, неиспользование окунания сосков после доения и обработки сухостойных коров под одеялом для предотвращения новых инфекций в конечном итоге приведет к повторному заражению стада.
Большинство других стрептококков также проявляют in vitro чувствительность к многочисленным противомикробным препаратам, особенно бета-лактамным препаратам. Несмотря на эту очевидную восприимчивость, многие стрептококковые инфекции не так легко излечиваются, как инфекции, вызванные S agalactiae . Как правило, субклинические инфекции, вызванные S uberis и S dysgalactiae , следует предпочтительно лечить в конце лактации с помощью внутригрудных вливаний коммерческих сухостойных коровьих продуктов. Показатели излечения в это время могут превышать 75%. Другие стрептококкоподобные организмы, такие как Лактококки и Энтерококки часто не поддаются терапии.
Показатели излечения в это время могут превышать 75%. Другие стрептококкоподобные организмы, такие как Лактококки и Энтерококки часто не поддаются терапии.
Интрамаммарные инфекции, вызванные S. aureus , вызывают глубокие абсцессы. Терапия затруднена, поскольку резистентность к противомикробным препаратам (особенно к бета-лактамам) встречается чаще, чем при стрептококковых инфекциях, а S. aureus может сохраняться внутриклеточно после фагоцитоза. Интрамаммарные инфузии могут вылечить только 20–40% инфекций и меньше при хронических инфекциях.
Показатель успешности терапии хронического субклинического ИИМ, вызванного S. aureus может повышаться при использовании как парентеральной, так и интрамаммарной терапии. Тем не менее, системная терапия включает использование препаратов, не указанных в этикетке, и необходимо определить периоды воздержания от молока и мяса. Кроме того, терапию следует проводить достаточно долго (7–10 дней), чтобы обеспечить эффективную элиминацию возбудителя. Терапия сухостойных коров более экономична и с наименьшей вероятностью приводит к образованию остатков в молоке по сравнению с терапией лактирующих коров. В зависимости от теста на чувствительность липофильные противомикробные препараты, которые хорошо распределяются в тканях молочной железы, такие как окситетрациклин (11 мг/кг/день), являются лучшими кандидатами для системного введения, хотя несколько исследований показали, что окситетрациклин (вводимый в течение 4 дней или меньше) быть неэффективным. Показатели излечения могут быть ненамного выше, чем при спонтанном излечении, и излечение должно быть определено критически (т.е. долгосрочное влияние на плоскоклеточный рак и производство молока).
Терапия сухостойных коров более экономична и с наименьшей вероятностью приводит к образованию остатков в молоке по сравнению с терапией лактирующих коров. В зависимости от теста на чувствительность липофильные противомикробные препараты, которые хорошо распределяются в тканях молочной железы, такие как окситетрациклин (11 мг/кг/день), являются лучшими кандидатами для системного введения, хотя несколько исследований показали, что окситетрациклин (вводимый в течение 4 дней или меньше) быть неэффективным. Показатели излечения могут быть ненамного выше, чем при спонтанном излечении, и излечение должно быть определено критически (т.е. долгосрочное влияние на плоскоклеточный рак и производство молока).
Иногда в хронически инфицированных помещениях возникает преждевременная агалактия. Выбраковка может быть практичным вариантом для этих коров. В качестве альтернативы обычно высушивают зараженную четверть и продолжают доить корову. Это может иметь некоторую пользу для генетически превосходных животных в стаде или для коров, которых необходимо содержать до отела. Цель состоит в том, чтобы устранить инфекцию, вызвав фиброз пораженной четверти, тем самым снизив риск заражения других коров. Кроме того, такие коровы больше не будут давать молоко с высоким содержанием SCC (из инфицированной четверти), что поможет сохранить качество продаваемого молока. Высушивание четвертей, выбраковка или терапия как средство снижения вклада SCC от инфицированных коров является паллиативным подходом к борьбе с маститом, который лучше решать путем профилактики инфекций.
Цель состоит в том, чтобы устранить инфекцию, вызвав фиброз пораженной четверти, тем самым снизив риск заражения других коров. Кроме того, такие коровы больше не будут давать молоко с высоким содержанием SCC (из инфицированной четверти), что поможет сохранить качество продаваемого молока. Высушивание четвертей, выбраковка или терапия как средство снижения вклада SCC от инфицированных коров является паллиативным подходом к борьбе с маститом, который лучше решать путем профилактики инфекций.
Сухой период лактационного цикла является критическим для здоровья вымени молочных коров. Молочная железа претерпевает выраженные биохимические, клеточные и иммунологические изменения. Инволюция паренхимы молочных желез начинается через 1–2 дня после окончания лактации и продолжается в течение 10–14 дней. В это время железа особенно уязвима для новых ИМИ. Однако инволюционная молочная железа представляет собой наиболее враждебную иммунную среду для бактериальных патогенов. Следовательно, сухостойный период является идеальным временем для достижения синергии между антимикробной терапией и иммунной функцией без значительных затрат, типичных для терапии лактирующих коров.
Для лечения сухостойных коров доступны многочисленные коммерческие продукты, в том числе пенициллин, клоксациллин, цефапирин, цефтиофур или новобиоцин. Достаточно одного тюбика на четверть, и его следует вводить сразу после последней дойки лактации. Терапию не следует повторять внутримаммарной инфузией; если существует потребность в продлении терапии, следует использовать системное введение в качестве дополнения к внутримаммарной инфузии. В дополнение к устранению существующих субклинических инфекций, одной из наиболее важных функций сухостойной терапии коров является предотвращение новых инфекций.
Внутренние герметики для сосков, используемые в качестве дополнительной инфузии после инфузий противомикробных препаратов при высыхании, служат физическим барьером, помогающим уменьшить количество новых инфекций. В некоторых случаях новые ИМИ во время сухостоя были дополнительно снижены на 50% по сравнению с только антимикробной терапией. Этот положительный эффект может быть частично обусловлен уровнем молочной продуктивности молочных коров в сухостойный период, который со временем значительно увеличился. Повышенная выработка молока при сухостойном периоде задерживает инволюцию и приводит к тому, что большая часть каналов соска остается открытой в течение всего сухостойного периода. Как и в случае с инфузиями лактирующим коровам, важно соблюдать строгую асептическую технику для любой инфузии в период откорма.
Повышенная выработка молока при сухостойном периоде задерживает инволюцию и приводит к тому, что большая часть каналов соска остается открытой в течение всего сухостойного периода. Как и в случае с инфузиями лактирующим коровам, важно соблюдать строгую асептическую технику для любой инфузии в период откорма.
Одеяло для сухостойных коров (BDCT; обработка всех четвертей всех коров при сухостойном кормлении) уже более 50 лет является основой борьбы с маститом. Однако, несмотря на высокую степень успеха BDCT в предотвращении и лечении IMI в засушливый период, картина мастита изменилась, включая более низкую распространенность S agalactiae и S aureus во многих стадах и более высокую распространенность экологических патогенов. . Кроме того, большинство сухостойных коровьих продуктов нацелены на грамположительные кокки, которые могут не быть преобладающими патогенами в конкретном стаде. Наконец, достижения в области содержания и подстилки, управления питанием и внутренних герметиков для сосков помогли снизить уровень IMI в сухостойный период. Таким образом, селективная терапия сухостойных коров (SDCT; лечение только коров, которые идентифицированы как инфицированные при сухостойном откорме) может рассматриваться как альтернатива BDCT. Самое большое предостережение при выборе BDCT по сравнению с SDCT заключается в том, что каждое стадо имеет уникальные проблемы и подходы к управлению их работой, поэтому программа терапии сухостойных коров должна быть адаптирована к их потребностям.
Таким образом, селективная терапия сухостойных коров (SDCT; лечение только коров, которые идентифицированы как инфицированные при сухостойном откорме) может рассматриваться как альтернатива BDCT. Самое большое предостережение при выборе BDCT по сравнению с SDCT заключается в том, что каждое стадо имеет уникальные проблемы и подходы к управлению их работой, поэтому программа терапии сухостойных коров должна быть адаптирована к их потребностям.
Стада, которым трудно справиться с базовым маститом (SCC > 200 000 клеток/мл), не являются лучшими кандидатами для SDCT. Кроме того, следует строго соблюдать как показатели исходов, так и протоколы отбора коров для сухостойной терапии. Алгоритмы, специфичные для стада, должны включать, по крайней мере, как клинический анамнез мастита, так и индивидуальный SCC коровы во время лактации перед сухостойным периодом и после отела. В США в меньшем количестве стад используется тестирование на SCC для улучшения молочного стада, и поэтому у них возникают трудности с мониторингом субклинического мастита. Кроме того, из-за повышенного внимания к так называемой эффективности доильного зала, т. е. скорости производства коров на многих крупных молочных фермах, способность операторов доения правильно идентифицировать клинический мастит, не говоря уже о том, чтобы сцедить молоко с сосков, вызывает сомнения.
Кроме того, из-за повышенного внимания к так называемой эффективности доильного зала, т. е. скорости производства коров на многих крупных молочных фермах, способность операторов доения правильно идентифицировать клинический мастит, не говоря уже о том, чтобы сцедить молоко с сосков, вызывает сомнения.
Таким образом, в некоторых стадах возможность определить эффективность программы лечения сухостойных коров, такой как новый и вылеченный ИМИ в течение периода сухостойных коров, а также клинический мастит в первые 30–60 дней лактации, будет невелика. Несмотря на то, что посев образцов молока, либо перед сушкой, либо после клинических случаев, является полезной частью любой программы борьбы с маститом в стаде, особенно для тех, кто выбирает SDCT, большинство производителей молока неохотно используют молочные культуры. Суть решения об использовании SDCT заключается в том, чтобы убедиться в наличии инструментов и готовности правильно выбирать коров и отслеживать изменения качества молока.
Рекомбинантный бычий гранулоцитарный колониестимулирующий фактор (rbG-CSF), ковалентно связанный с полиэтиленгликолем, вводимый дважды подкожно коровам до и в течение 24 часов после отела, увеличивает количество циркулирующих полиморфноядерных лейкоцитов. Предполагается, что эта индуцированная нейтрофилия обеспечивает более сильную и своевременную реакцию у коров, которые могут быть предрасположены к послеродовым инфекционным заболеваниям, включая мастит. Однако результаты последующих полевых испытаний на молочных фермах выявили непостоянное влияние на уровень клинического мастита в течение первых 30 дней после отела. Кроме того, rbG-CSF не влиял на субклинический мастит (SCC) у леченных коров по сравнению с нелеченными. Эта технология может помочь коровам в переходный период преодолеть иммунную дисфункцию, связанную с полиморфноядерными лейкоцитами, хотя существуют и другие пути послеродовой иммунной дисфункции (например, метаболический стресс), на которые этот подход может не повлиять. Клиническая польза может быть ограничена в стадах, в которых уже наблюдается низкая заболеваемость послеродовым клиническим маститом. Наконец, rbG-CSF не следует использовать в качестве замены другим рациональным методам содержания переходных коров, включая гигиену помещения и контроль метаболического и теплового стресса.
Клиническая польза может быть ограничена в стадах, в которых уже наблюдается низкая заболеваемость послеродовым клиническим маститом. Наконец, rbG-CSF не следует использовать в качестве замены другим рациональным методам содержания переходных коров, включая гигиену помещения и контроль метаболического и теплового стресса.
Большинство ИМИ у отелов телок вызываются стафилококковыми видами, отличными от S. aureus , которые имеют высокий уровень спонтанного излечения. Однако в некоторых условиях стада значительная часть телок имеет более трудноизлечимые инфекции, в том числе вызванные S. aureus . Потенциальные источники включают молоко (скармливаемое телятам) и участки тела, такие как миндалины и кожа. Существует также географический фактор риска: в патогенезе может играть роль дерматит укусов мух на конце соска, который ставит под угрозу этот важный физический барьер для инфекции.
Сообщалось, что внутригрудные инфузии бета-лактамных антибактериальных препаратов за 7–14 дней до предполагаемой даты отела снижают распространенность ИИМ при отёле. Тем не менее, было обнаружено, что долгосрочные преимущества в отношении SCC, молочной продуктивности и заболеваемости клиническим маститом во время лактации сильно варьируются в зависимости от стада и непостоянны. Перед инфузией следует провести строгую антисептику конца соска, чтобы предотвратить заражение; таким образом, работа с животными для лечения может быть обширной. Это не рекомендуемая программа управления для многих молочных ферм. Однако, если данные стада показывают, что распространенность IMI у животных первой лактации при отеле высока (> 20%), особенно при наличии стафилококков, этот режим можно рассмотреть.
Тем не менее, было обнаружено, что долгосрочные преимущества в отношении SCC, молочной продуктивности и заболеваемости клиническим маститом во время лактации сильно варьируются в зависимости от стада и непостоянны. Перед инфузией следует провести строгую антисептику конца соска, чтобы предотвратить заражение; таким образом, работа с животными для лечения может быть обширной. Это не рекомендуемая программа управления для многих молочных ферм. Однако, если данные стада показывают, что распространенность IMI у животных первой лактации при отеле высока (> 20%), особенно при наличии стафилококков, этот режим можно рассмотреть.
Новые инфекции можно предотвратить, если сосредоточить внимание на снижении присутствия патогенов на конце соска. Таким образом, чистая и сухая подстилка, чистое и сухое вымя во время доения, отказ от использования воды во время протоколов доения (за исключением поддержания гигиены доильных аппаратов), а также поддержание здоровья кончиков сосков положительно влияют на контроль.
В отношении заразных патогенов единственной наиболее важной практикой предотвращения передачи новых инфекций является использование эффективного гермицида в качестве средства для обработки сосков после доения . Эти продукты следует наносить раствором (а не распылением) сразу после доения. Другие методы, улучшающие гигиену сосков, включают использование индивидуальных полотенец для сушки сосков, перчаток для рук дояров, использование гермицидов перед доением (спрей или погружение), подсоединение устройств в нужное время после стимуляции сосков (60–120 секунд), а не передоение, очистка доильных аппаратов после доения инфицированной коровы или изоляция зараженных коров. Этот последний вариант может быть нереалистичным для крупного рогатого скота в свободном содержании, который обычно изолируется по причинам питания или воспроизводства. Следует проводить регулярные оценки доильного оборудования, чтобы убедиться, что вакуум на конце соска работает на надлежащем уровне и остается стабильным во время доения. Правильная работа пульсатора имеет решающее значение, и при необходимости следует заменять вкладыши и резиновые воздушные шланги.
Правильная работа пульсатора имеет решающее значение, и при необходимости следует заменять вкладыши и резиновые воздушные шланги.
Гигиена доения также снижает уровень заражения патогенами из окружающей среды. Однако, что более важно, коровы должны быть обеспечены сухими, чистыми помещениями. Неорганическая подстилка поддерживает меньший рост бактерий, чем материал на основе целлюлозы; таким образом, песок предпочтительнее опилок, соломы, переработанной бумаги или навоза. В частности, более высокая частота инфекций, вызванных Klebsiella , была связана с подстилкой из опилок. Однако количество бактерий может сильно различаться в зависимости от влажности и наличия органических веществ (например, в песке после переработки). Таким образом, борьба с экологическим маститом не должна основываться исключительно на выборе материала подстилки. Практики, которые имеют Положительное влияние на контроль мастита окружающей среды включает в себя:
Регулярная очистка или изменение постельных принадлежностей
РЕЗЕРТАЦИЯ ТЕПРАТ
- .
 коров путем регулирования потребления калия и натрия в питании
коров путем регулирования потребления калия и натрия в питании избегание мест скопления воды
уход за стойлами для правильного лежания
предотвращение обморожения и контакта с мухами
Когда баланс между защитой хозяина и вторжением патогенов вызывает выраженную воспалительную реакцию, клинические признаки становятся очевидными. Инфекции от любого патогена могут быть клиническими или субклиническими, в зависимости от продолжительности инфекции, иммунного статуса хозяина и вирулентности патогена. Борьба с клиническим маститом обычно направлена на профилактику и устранение патогенов, возникающих из резервуара окружающей среды. Таким образом, эпидемиология и профилактика клинического мастита аналогична борьбе с субклиническим маститом.
За исключением вспышек Mycoplasma , клинический мастит в большинстве молочных стад вызывается патогенами окружающей среды . Кроме того, многие клинические случаи мастита являются преходящими, особенно те, которые являются начальными эпизодами для коровы и четверти. Таким образом, оценка клинического мастита основана на заболеваемости, а не на распространенности.
Таким образом, оценка клинического мастита основана на заболеваемости, а не на распространенности.
Методы мониторинга субклинического мастита, т. е. рутинные ПКК и посев коров с повышенным ПКК, являются непостоянными предикторами случаев клинического мастита. У коров с высоким SCC, вызванным хроническими инфекциями, иногда может проявляться клинический мастит, хотя обычно он протекает в легкой форме. Однако коровы с низким уровнем соматических клеток также склонны к развитию клинического мастита.
История каждого случая коровы (например, сезон, возраст, стадия лактации и предыдущие эпизоды) должна быть зарегистрирована, чтобы помочь определить факторы риска. Образцы молока должны быть взяты из пораженных кварталов и, по возможности, проведены тесты на чувствительность к противомикробным препаратам. Для хорошо управляемых стад, в которых мастит, вызванный инфекционными патогенами, находится под контролем, целевым показателем заболеваемости клиническим маститом должно быть 1–2 случая на 100 дойных коров в месяц. Случаи тяжелого мастита должны быть в пределах 1-2 случаев на 100 дойных коров в год.
Случаи тяжелого мастита должны быть в пределах 1-2 случаев на 100 дойных коров в год.
Как правило, 30–40 % проб молока, взятых у пациентов с клиническими проявлениями мастита, не обнаруживают микроорганизмы при посеве. Однако в образцах, которые действительно выделяют микроорганизмы, 90–95% выделенных бактерий включают широкий спектр стрептококков, стафилококков или кишечных палочек. Если это не так, особенно если преобладают неколиформные, грамотрицательные палочки, грибковые или водорослевые ( Prototheca sp) патогены, следует рассмотреть точечный источник инфекции.
БГКП (грамотрицательные палочки семейства Enterobacteriaceae, ферментирующие лактозу) являются наиболее частой причиной этой формы мастита. Большинство колиформных инфекций выводятся из железы с незначительными или слабовыраженными клиническими признаками. Однако тяжелый мастит (системные признаки) возникает, когда концентрация бактерий в молоке увеличивается настолько, что стимулирует выраженный иммунный ответ.
Тяжелый мастит, вызванный кишечной палочкой, приводит к более высокой частоте падежа коров или выбраковки, связанной с агалактией (30–50 % случаев), чем мастит, вызванный другими патогенами (5–10 % случаев). Прогноз для случаев инфекции Klebsiella должен быть особенно осторожным, потому что пораженные коровы в два раза чаще выбраковываются или умирают, чем коровы, инфицированные другими колиформами. Таким образом, первичная терапия тяжелого клинического мастита должна быть направлена против колиформных организмов, хотя вторичное внимание должно быть уделено другим возбудителям. Поддерживающая терапия, включая жидкости, вероятно, является наиболее полезным компонентом терапевтического режима. Антимикробная терапия в идеале основана на идентификации возбудителя; однако это невозможно в течение нескольких часов после первоначального распознавания случая. Кроме того, схемы системного применения противомикробных препаратов, применяемые при тяжелом клиническом мастите, не маркируются FDA в США.
После заражения количество кишечных палочек в молоке быстро увеличивается, часто достигая максимальной концентрации в течение нескольких часов. Быстрое снижение количества бактерий следует за миграцией нейтрофилов в железу.
Воспалительные и системные изменения, возникающие при тяжелом колиформном мастите, вызваны высвобождением липополисахаридного (ЛПС) эндотоксина из бактерий и последующей активацией цитокинов и производных арахидоновой кислоты медиаторов воспаления; это вызывает реакцию острой фазы (сепсис). К моменту начала терапии большая часть воздействия ЛПС уже прошла. Таким образом, основной терапевтической задачей является лечение шока, вызванного ЛПС, с помощью жидкостей, электролитов и противовоспалительных препаратов. Внутривенный путь предпочтительнее в качестве начального метода введения жидкости.
При введении изотонического раствора необходимо 30–40 л в течение 4-часового периода, что может быть затруднительно в условиях фермы. Практической альтернативой является внутривенное введение 2 л 7% NaCl (гиперсолевого раствора).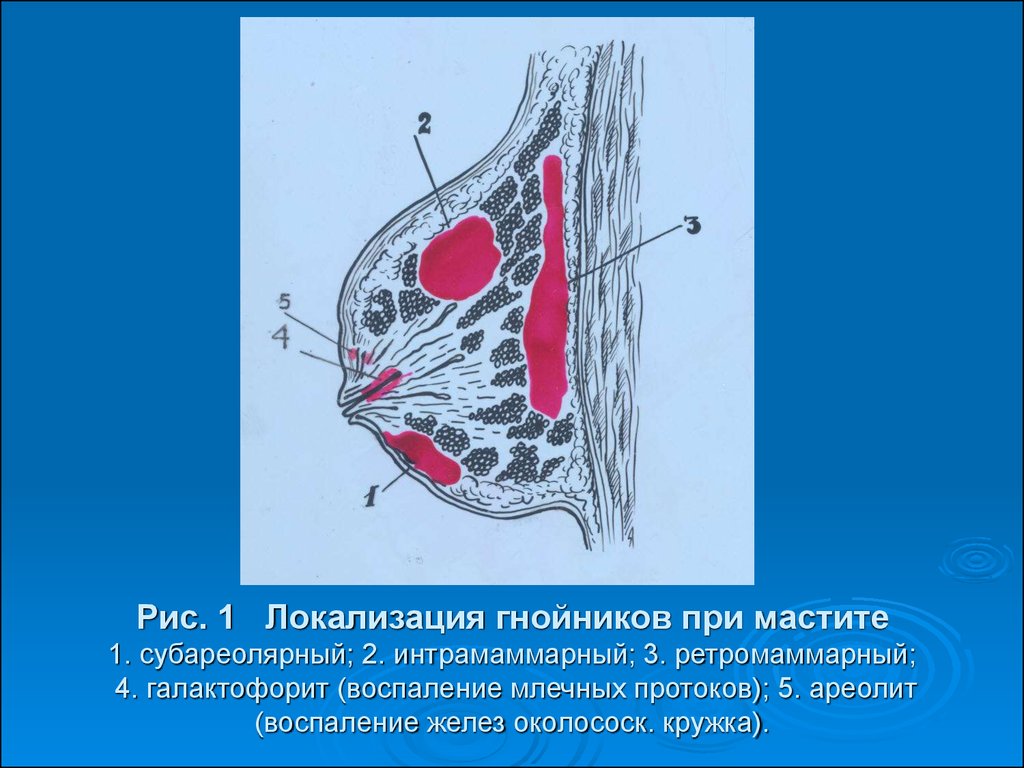 Это вызывает быстрое поглощение жидкости из компартментов тела в кровоток. Затем коровам следует предлагать пить воду по своему выбору, и если по крайней мере 8–10 галлонов не выпито, 5–7 галлонов следует закачивать в рубец. У многих коров с эндотоксическим шоком отмечается незначительная гипокальциемия; таким образом, 500 мл бороглюконата кальция следует вводить подкожно (во избежание возможных осложнений при внутривенном введении). В качестве альтернативы можно назначать кальциевые гели с быстрой абсорбцией, предназначенные для перинатальной гипокальциемии. Если корова остается в шоке, следует продолжать инфузионную терапию перорально или внутривенно в виде изотонических, а не гипертонических жидкостей.
Это вызывает быстрое поглощение жидкости из компартментов тела в кровоток. Затем коровам следует предлагать пить воду по своему выбору, и если по крайней мере 8–10 галлонов не выпито, 5–7 галлонов следует закачивать в рубец. У многих коров с эндотоксическим шоком отмечается незначительная гипокальциемия; таким образом, 500 мл бороглюконата кальция следует вводить подкожно (во избежание возможных осложнений при внутривенном введении). В качестве альтернативы можно назначать кальциевые гели с быстрой абсорбцией, предназначенные для перинатальной гипокальциемии. Если корова остается в шоке, следует продолжать инфузионную терапию перорально или внутривенно в виде изотонических, а не гипертонических жидкостей.
Глюкокортикоиды, назначенные на ранних стадиях заболевания, могут быть полезны в случаях мастита, вызванного кишечной палочкой, продуцирующей эндотоксин. Эти соединения ингибируют многие провоспалительные пути, связанные с острофазовым ответом. Сообщалось, что введение дексаметазона (30 мг, в/м) молочным коровам сразу после введения E coli в молочную железу уменьшает отек молочной железы и улучшает перистальтику рубца. Следует соблюдать осторожность при назначении этих препаратов беременным животным; однако тяжелый клинический мастит сам по себе может вызвать потерю беременности у крупного рогатого скота.
Следует соблюдать осторожность при назначении этих препаратов беременным животным; однако тяжелый клинический мастит сам по себе может вызвать потерю беременности у крупного рогатого скота.
Опубликовано мало исследований по применению глюкокортикоидов при мастите, вызванном грамположительными бактериями. Разумно ожидать, что грамположительные инфекции с меньшей вероятностью получат пользу от противовоспалительной активности глюкокортикоидов и даже могут быть неблагоприятно затронуты. Интрамаммарное введение глюкокортикоидов для уменьшения местного воспаления рассматривалось как терапевтический вариант. Хотя в Европе существуют продукты, сочетающие противомикробные и глюкокортикоидные препараты для внутригрудного введения, неясно, достигается ли клиническая польза по сравнению с только противомикробной терапией. Как правило, лечение глюкокортикоидами следует проводить только в тяжелых случаях грамотрицательного мастита с однократным введением дозы на ранних стадиях заболевания.
НПВП широко используются для лечения острого мастита. Флуниксин, меглумин, флурбипрофен, карпрофен, мелоксикам и кетопрофен использовались для лечения экспериментального колиформного мастита или эндотоксин-индуцированного мастита. Системное применение этих препаратов предпочтительнее перорального приема аспирина, который, скорее всего, не достигнет эффективной концентрации в тканях или не приведет к положительным результатам. Использование анальгина у сельскохозяйственных животных строго запрещено FDA. Фенилбутазон запрещен для молочного скота старше 20 месяцев; уровень толерантности для фенилбутазона равен нулю, и обнаружение любой концентрации является незаконным остатком. Таким образом, эти два препарата не следует использовать для противовоспалительной терапии мастита крупного рогатого скота.
Кетопрофен доступен в качестве ветеринарного препарата для применения у лошадей, имеет высокий терапевтический индекс, благоприятную фармакокинетику для использования у лактирующего молочного скота и одобрен для применения у крупного рогатого скота в некоторых странах; однако в США он не предназначен для использования в пищевых целях. Банк данных по предотвращению пищевых отходов животного происхождения (FARAD) рекомендует интервалы отмены в 7 дней для убоя и 24 часа для молока, с внутривенным или внутримышечным введением, для доз до 3,3 мг/кг/день, на срок до 3 дней.
Банк данных по предотвращению пищевых отходов животного происхождения (FARAD) рекомендует интервалы отмены в 7 дней для убоя и 24 часа для молока, с внутривенным или внутримышечным введением, для доз до 3,3 мг/кг/день, на срок до 3 дней.
Флуниксин меглюмин предназначен для мясного и молочного скота. Это единственный НПВП, разрешенный для использования у крупного рогатого скота в США, и поэтому он является наиболее логичным выбором для лечения тяжелого клинического мастита. В полевых исследованиях не было продемонстрировано повышения выживаемости и увеличения производства молока после лечения клинического острого мастита флуниксином меглумина в дозе 1,1 мг/кг. Однако в исследованиях экспериментального мастита флуниксин меглюмин уменьшал тяжесть клинических признаков, таких как лихорадка, депрессия, частота сердечных сокращений и дыхания, а также боль в вымени. Утвержденные FDA интервалы отмены составляют 4 дня для убоя и 36 часов для молока при внутривенном введении, как указано на этикетке. Из-за длительных и непредсказуемых периодов отмены этот препарат следует , а не следует вводить внутримышечно. Как и глюкокортикоиды, НПВП могут облегчать симптомы и улучшать самочувствие. Введение на ранних стадиях инфекции, вероятно, увеличит клиническую пользу.
Из-за длительных и непредсказуемых периодов отмены этот препарат следует , а не следует вводить внутримышечно. Как и глюкокортикоиды, НПВП могут облегчать симптомы и улучшать самочувствие. Введение на ранних стадиях инфекции, вероятно, увеличит клиническую пользу.
Антимикробная терапия может иметь второстепенное значение по сравнению с немедленным поддерживающим лечением эндотоксического шока, но она остается неотъемлемой частью терапевтического режима. Иногда колиформные инфекции приводят к хроническому маститу. Бактериемия встречается более чем в 50% тяжелых случаев кишечной палочки. Кроме того, многие другие патогены, в том числе грамположительные кокки, вызывают тяжелый клинический мастит, который бывает трудно отличить от случаев, вызванных кишечной палочкой при начальных проявлениях.
Выбор подходящего противомикробного препарата для лечения тяжелого колиформного мастита зависит в первую очередь от чувствительности организма к выбранному лекарственному средству и способности поддерживать эффективные концентрации на первичной фармакологической мишени (которой в случае колиформного мастита является плазменный отсек коровы).
Коровы, подвергшиеся экспериментальному заражению E coli и получавшие 500 мг гентамицина интрамаммарно два раза в день, не имели более низких пиковых концентраций бактерий в молоке, продолжительности инфекции, выздоравливающих SCC или концентрации сывороточного альбумина в молоке, а также ректальной температуры по сравнению с контрольными коровами, не получавшими лечения. Кроме того, гентамицин легко диффундирует через молочно-гематический барьер, в результате чего остатки препарата в почках могут сохраняться более 18 месяцев. Из-за нулевой толерантности к остаткам аминогликозидов при убое использование этого класса препаратов у молочного скота нецелесообразно.0041 не рекомендуется .
Окситетрациклин (11 мг/кг/день, внутривенно) улучшал исход у коров с клиническим колиформным маститом (не обязательно тяжелым) по сравнению с коровами, которые не получали системные антибактериальные препараты. Цефтиофур натрия (2,2 мг/кг/день, внутримышечно) снижал смертность и процент выбраковки коров с тяжелым колиформным маститом, а также улучшал восстановление молочной продуктивности. Этот препарат плохо распределяется в молочной железе, что подтверждает важность целенаправленной терапии бактериемии в дополнение к молочной железе.
Этот препарат плохо распределяется в молочной железе, что подтверждает важность целенаправленной терапии бактериемии в дополнение к молочной железе.
Коровам с тяжелым клиническим маститом следует вводить внутригрудную инфузию противомикробных препаратов. Это лечение, возможно, не повлияет на исходы в случаях колиформных инфекций, но, вероятно, улучшит исходы в случаях, вызванных грамположительными кокками. Следует критически оценить необходимость продолжения антимикробной терапии у коров с явно ненормальным молоком, но с улучшенным аппетитом, поведением и молочной продуктивностью. Ненужное продление терапии в этих случаях приводит к увеличению расходов на выбрасываемое молоко и риску наличия остатков противомикробных препаратов в товарном молоке.
Как указывалось ранее, микроорганизмы не выделяются из 30-40% бактериологических культур образцов молока, взятых у коров с клиническим маститом. Многие легкие случаи мастита, которые не дают бактерий в культуре, представляют собой колиформные интрамаммарные инфекции, которые разрешаются до того, как необходимо лечение. Кроме того, многочисленные легкие клинические случаи мастита являются временными нарушениями баланса между защитой возбудителя и хозяина, который возникает при хроническом ИИМ.
Кроме того, многочисленные легкие клинические случаи мастита являются временными нарушениями баланса между защитой возбудителя и хозяина, который возникает при хроническом ИИМ.
Здравый смысл и индивидуальный анамнез стада должны определять курс терапии при легких клинических случаях мастита в молочных стадах. Наилучшим вариантом является использование одобренных коммерческих внутригрудных инфузий. Основой успеха является бактериологическое излечение, но более практически оно будет основано на возвращении к нормальному молоку. Частоту рецидивов следует контролировать как лучший показатель терапевтической эффективности, потому что многие случаи будут считаться успешно вылеченными в краткосрочной перспективе, но рецидивы возникнут позже в период лактации. Если мастит регулярно рецидивирует в пораженных частях тела при отсутствии системных признаков, повторное лечение того, что теперь стало хроническим ИМИ, не оправдано.
Кроме того, аугментация парентеральной терапией в этих случаях не продемонстрировала свою эффективность и вряд ли позволит компенсировать затраты на выбрасываемое молоко, другие связанные с этим затраты на лечение и повышенный риск остаточных количеств в молоке и мясе. Клинические случаи в анамнезе («рецидивисты»), длительная продолжительность инфекции (о чем свидетельствует высокий уровень отдельных SCC или длительные периоды увеличения SCC) и инфекции, вызванные невосприимчивыми патогенами, являются наибольшими факторами риска плохого терапевтического результата. Практикующие врачи должны разработать протокол для молочных клиентов, чтобы уменьшить количество ненужного лечения в случаях низкого риска, как указано выше, и не полагаться на продолжение безуспешной терапии или поиск «лучшего лекарства».
Клинические случаи в анамнезе («рецидивисты»), длительная продолжительность инфекции (о чем свидетельствует высокий уровень отдельных SCC или длительные периоды увеличения SCC) и инфекции, вызванные невосприимчивыми патогенами, являются наибольшими факторами риска плохого терапевтического результата. Практикующие врачи должны разработать протокол для молочных клиентов, чтобы уменьшить количество ненужного лечения в случаях низкого риска, как указано выше, и не полагаться на продолжение безуспешной терапии или поиск «лучшего лекарства».
Если стандартные схемы не дают желаемых результатов, было бы лучше продлить начальную терапию на длительный период, а не переходить на другие противомикробные препараты или увеличивать количество каждой дозы. Исследования показали улучшение показателей излечения грамположительных кокков, особенно коагулазонегативных стафилококков и стрептококков, когда инфицированные четверти обрабатывались интрамаммарными инфузиями в течение 8 дней по сравнению с 2 днями. Однако результаты будут варьироваться в зависимости от бактериологии стада. Особую осторожность следует проявлять при асептической подготовке соска для продолжительной терапии из-за повышенного риска внутрибольничных инфекций.
Однако результаты будут варьироваться в зависимости от бактериологии стада. Особую осторожность следует проявлять при асептической подготовке соска для продолжительной терапии из-за повышенного риска внутрибольничных инфекций.
Наиболее эффективное использование противомикробной терапии и лучший способ сократить ненужное использование — это применение «культуральной терапии» для принятия решений в рамках терапевтического протокола на ферме. Лечение пораженной четверти (легкий клинический мастит) прекращается до тех пор, пока не будут получены результаты бактериологического посева образца молока, обычно в течение 24–48 часов. Решения о лечении, зависящие от посева, могут варьироваться от фермы к ферме, но в целом противомикробная терапия не улучшает исходы в случаях отсутствия микроорганизмов, грамотрицательных микроорганизмов и необычных патогенов (например, 9).0041 Pseudomonas spp.). Таким образом, исключая случаи, которые дают такие результаты посева, молочное стадо может сократить использование противомикробных препаратов для легкой клинической терапии на 50–75%.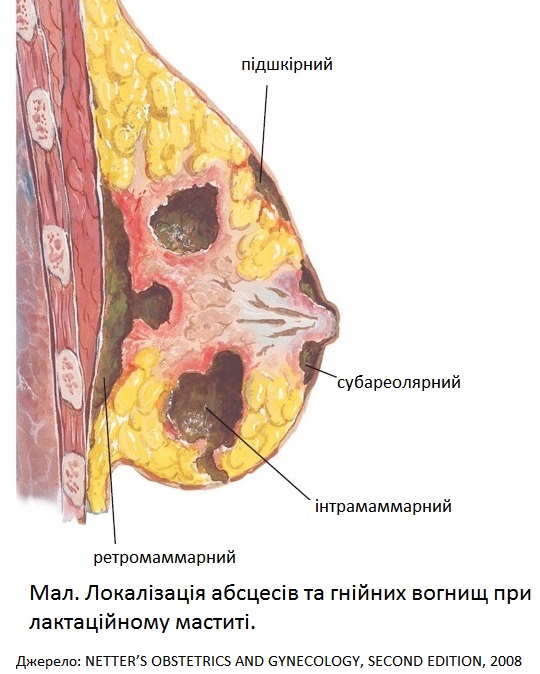
Кроме того, «период ожидания» между клиническим началом и принятием решения о лечении (после результатов посева) не оказывает неблагоприятного влияния на бактериальное лечение, рецидивы, надои или SCC у коров, выбранных для лечения. Простая бактериология молока, позволяющая идентифицировать грамположительных от грамотрицательных возбудителей, а также не выделяющая их, может проводиться в ветеринарных клиниках или при должной подготовке на ферме.
Pseudomonas aeruginosa может вызывать вспышки клинического мастита. Как правило, возникает персистирующая инфекция, которая может характеризоваться перемежающимися острыми или подострыми обострениями. Организм встречается в почвенно-водной среде, характерной для молочных ферм. Сообщалось о стадных инфекциях после обширного контакта с загрязненной водой для мытья в доильном зале, со вкладышами доильных стаканов или после интрамаммарных процедур, проводимых доярками. Неиспользование асептических методов обработки вымени или использование загрязненного доильного оборудования может привести к P. aeruginosa IMI. У одних коров может наблюдаться тяжелый сверхострый мастит с токсемией и высокой смертностью, тогда как у других могут возникать субклинические инфекции. Микроорганизм сохраняется в железе в течение пяти лактаций, но может произойти спонтанное выздоровление. Помимо поддерживающей терапии при тяжелых эпизодах, терапия не имеет большого значения. Выбраковка рекомендуется для коров с устойчивыми симптомами.
aeruginosa IMI. У одних коров может наблюдаться тяжелый сверхострый мастит с токсемией и высокой смертностью, тогда как у других могут возникать субклинические инфекции. Микроорганизм сохраняется в железе в течение пяти лактаций, но может произойти спонтанное выздоровление. Помимо поддерживающей терапии при тяжелых эпизодах, терапия не имеет большого значения. Выбраковка рекомендуется для коров с устойчивыми симптомами.
Trueperella (ранее Arcanobacterium ) pyogenes часто встречается при нагноительных процессах у крупного рогатого скота и свиней и вызывает характерный мастит у телок и сухостойных коров. Иногда он поражает лактирующее вымя после травмы соска и может быть вторичным возбудителем. Воспаление характеризуется образованием обильного, зловонного, гнойного экссудата. Мастит из-за T pyogenes распространен среди сухостойных коров и телок, которые в летние месяцы выпасаются на полях и имеют доступ к прудам или влажным участкам. Переносчиком инфекции от животного к животному является муха Haematobia irritans . Борьба с инфекциями достигается за счет ограничения возможности стоять в воде и борьбы с мухами. Терапия редко бывает успешной, и зараженная четверть обычно теряется в производстве. Инфицированные коровы могут иметь системные заболевания, и коров с абсцессами обычно следует убивать. (Также см. Актиномикоз Актиномикоз.)
Борьба с инфекциями достигается за счет ограничения возможности стоять в воде и борьбы с мухами. Терапия редко бывает успешной, и зараженная четверть обычно теряется в производстве. Инфицированные коровы могут иметь системные заболевания, и коров с абсцессами обычно следует убивать. (Также см. Актиномикоз Актиномикоз.)
Mycoplasma spp может вызывать тяжелую форму мастита, которая может быстро распространяться в стаде с серьезными последствиями. M bovis является наиболее распространенной причиной. Другие важные виды включают M californicum , M canadense и M bovigenitalium . Начало быстрое, и источник инфекции часто является эндогенным после вспышек респираторных заболеваний у телок или коров. Болезнь часто наблюдается в стадах, подвергающихся расширению, в которые были добавлены животные из внешних источников. Как правило, интродуцированные животные будут бессимптомными носителями, а затем выделяют микроорганизм в результате респираторной или интрамаммарной передачи. Некоторые или все кварталы становятся вовлеченными. Выпадение продукции часто резкое, и секреция вскоре сменяется серозным или гнойным экссудатом. Вначале в материале, взятом из инфицированных желез, можно увидеть характерный мелкозернистый или хлопьевидный осадок.
Некоторые или все кварталы становятся вовлеченными. Выпадение продукции часто резкое, и секреция вскоре сменяется серозным или гнойным экссудатом. Вначале в материале, взятом из инфицированных желез, можно увидеть характерный мелкозернистый или хлопьевидный осадок.
Несмотря на сильное местное воздействие на ткани вымени, у коров обычно не проявляются признаки системного поражения. Инфекция может сохраняться в течение сухого периода. Идентификация всех инфицированных коров в стаде может быть затруднена из-за частой склонности этих коров к бессимптомному носительству и периодическому выделению микроорганизма с молоком.
Поскольку удовлетворительного лечения не существует, больных коров следует изолировать во время активных вспышек. Регулярный осмотр наливного резервуара и молочных трубок может помочь выявить наличие инфицированных коров. Тем не менее, молочная культура коров с клиническим маститом или недавно отелившихся коров обеспечивает наиболее надежное наблюдение. Если у коров продолжают проявляться клинические признаки мастита или системные признаки, их следует выбраковывать. Санитарные меры должны строго соблюдаться, особенно при доении и в больничных/лечебных помещениях. Молоко от Инфицированных микоплазмой коров нельзя скармливать телятам, так как это может привести к пневмонии или среднему отиту. Заменитель молока или пастеризованное молоко, а не отработанное молоко, следует скармливать телятам в стадах с Mycoplasma .
Санитарные меры должны строго соблюдаться, особенно при доении и в больничных/лечебных помещениях. Молоко от Инфицированных микоплазмой коров нельзя скармливать телятам, так как это может привести к пневмонии или среднему отиту. Заменитель молока или пастеризованное молоко, а не отработанное молоко, следует скармливать телятам в стадах с Mycoplasma .
Nocardia asteroides вызывает деструктивный мастит, характеризующийся острым началом, высокой температурой, анорексией, быстрым истощением и выраженным отеком вымени. Как правило, возникает гранулематозное воспаление вымени, которое приводит к обширному фиброзу и образованию пальпируемых узелков. Инфицирование вымени может быть связано с несоблюдением асептики при интрамаммарном лечении распространенных форм мастита. Для зараженных коров рекомендуется убой.
Мастит, вызванный Serratia , может возникнуть в результате загрязнения молочных шлангов, сосков, источников воды или другого оборудования, используемого в процессе доения.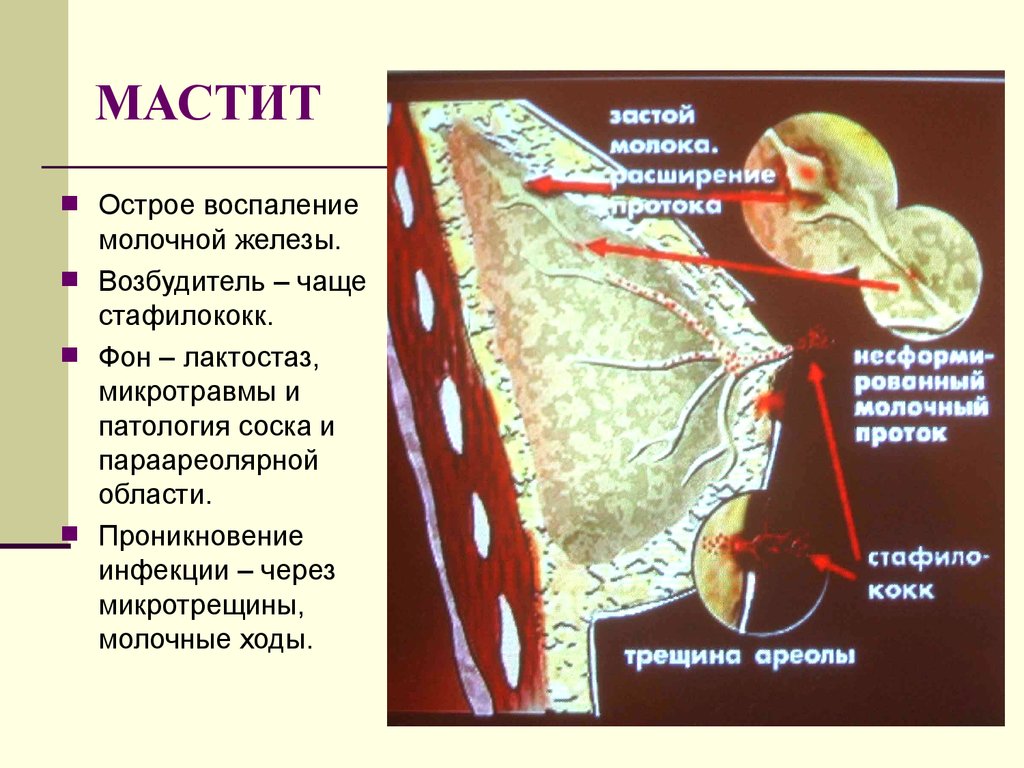 Организм устойчив к дезинфицирующим средствам. Коров с этой формой мастита, у которых продолжают проявляться клинические признаки, следует выбраковывать.
Организм устойчив к дезинфицирующим средствам. Коров с этой формой мастита, у которых продолжают проявляться клинические признаки, следует выбраковывать.
Мастит, вызванный различными грибковыми микроорганизмами (дрожжами), появился в молочных стадах, особенно после применения пенициллина в сочетании с длительным повторным применением противомикробных инфузий у отдельных коров. Дрожжи хорошо растут в присутствии пенициллина и некоторых других противомикробных препаратов; они могут заноситься во время инфузии антибиотиков в вымя, размножаться и вызывать мастит. Тем не менее, у телок, которые никогда не получали инфузии интрамаммарно, может развиться дрожжевой мастит. Признаки могут быть тяжелыми, с лихорадкой, за которой следует либо спонтанное выздоровление примерно через 2 недели, либо, реже, хронический деструктивный мастит. Другие дрожжевые инфекции вызывают минимальное воспаление и проходят самостоятельно. При подозрении на мастит, вызванный дрожжами, терапию антибиотиками следует немедленно прекратить.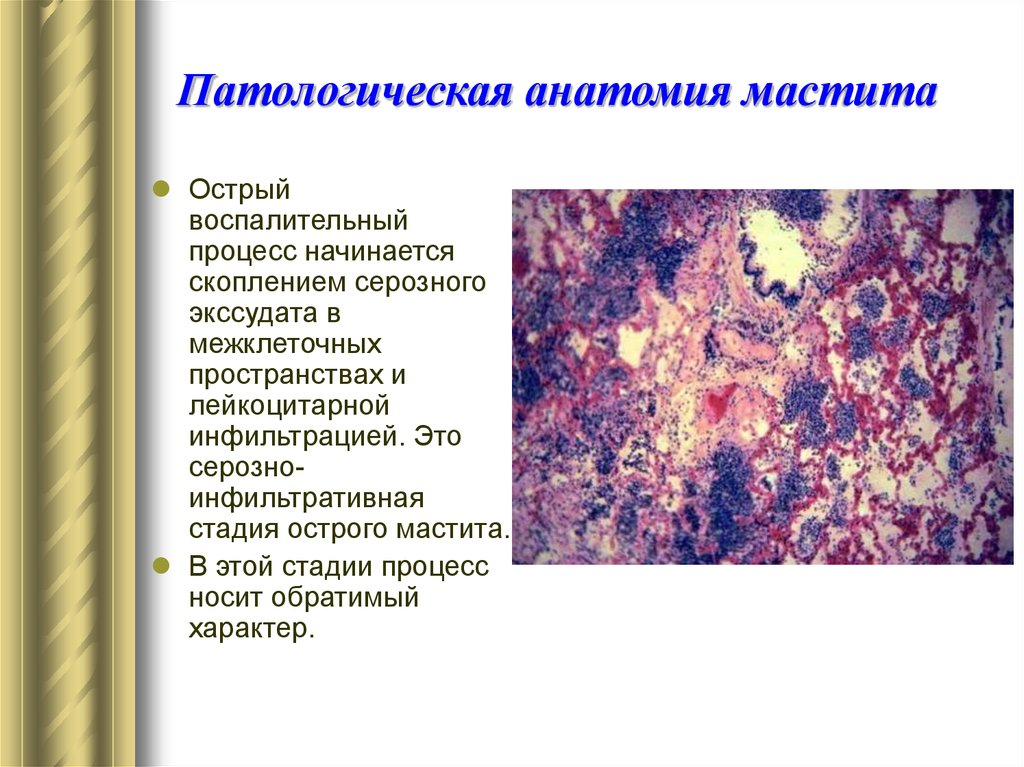
Сообщалось, что хронический мастит, подобный маститу, вызванному туберкулезной палочкой, вызывается кислотоустойчивыми Mycobacterium spp. M phlei , когда такие микроорганизмы вводятся в железу вместе с антибиотиками (особенно пенициллином) в масляных или «домашних средствах». В противном случае эти организмы склонны к сапрофитам и исчезают из зараженных кварталов, по крайней мере, к следующей лактации. Между тем мастит обычно протекает умеренно. Отдельные вспышки случаются, и было зарегистрировано несколько, особенно с М фортуитум и М смегматис .
Prototheca sp — это непигментированные одноклеточные водоросли, обычно встречающиеся во влажной среде, такой как ручьи, стоячие пруды и морские воды, особенно во влажных средах обитания с органическими веществами в почве. На молочных фермах они особенно многочисленны на грязных или влажных открытых площадках или участках, в местах отдыха, на дорожках, по которым прогоняют животных, и на пастбищах, загрязненных навозной жижей. Возможно заражение в сухостойный период, особенно у коров, находящихся на подстилке с навозом или на открытом воздухе. Кроме того, со вспышками были связаны плохая асептика инфузии и использование многодозовых противомикробных препаратов, не предназначенных для интрамаммарной инфузии. Сообщения о случаях заболевания предполагают, что если IMI в стаде достигнет критического уровня, заразная передача Прототека во время доения также может возникнуть.
Возможно заражение в сухостойный период, особенно у коров, находящихся на подстилке с навозом или на открытом воздухе. Кроме того, со вспышками были связаны плохая асептика инфузии и использование многодозовых противомикробных препаратов, не предназначенных для интрамаммарной инфузии. Сообщения о случаях заболевания предполагают, что если IMI в стаде достигнет критического уровня, заразная передача Прототека во время доения также может возникнуть.
Прототекальный мастит у молочного скота часто протекает хронически и бессимптомно с увеличением SCC, хотя спорадические тяжелые инфекции встречаются. Инфекции могут спонтанно разрешаться, но обычно длительное носительство с периодическим выделением. После первоначального возникновения клинического мастита инфекции могут не обнаруживаться культуральным исследованием молока в течение нескольких месяцев, чтобы рецидивировать только во время последующей лактации, особенно вскоре после отела. Терапевтические вмешательства бесполезны.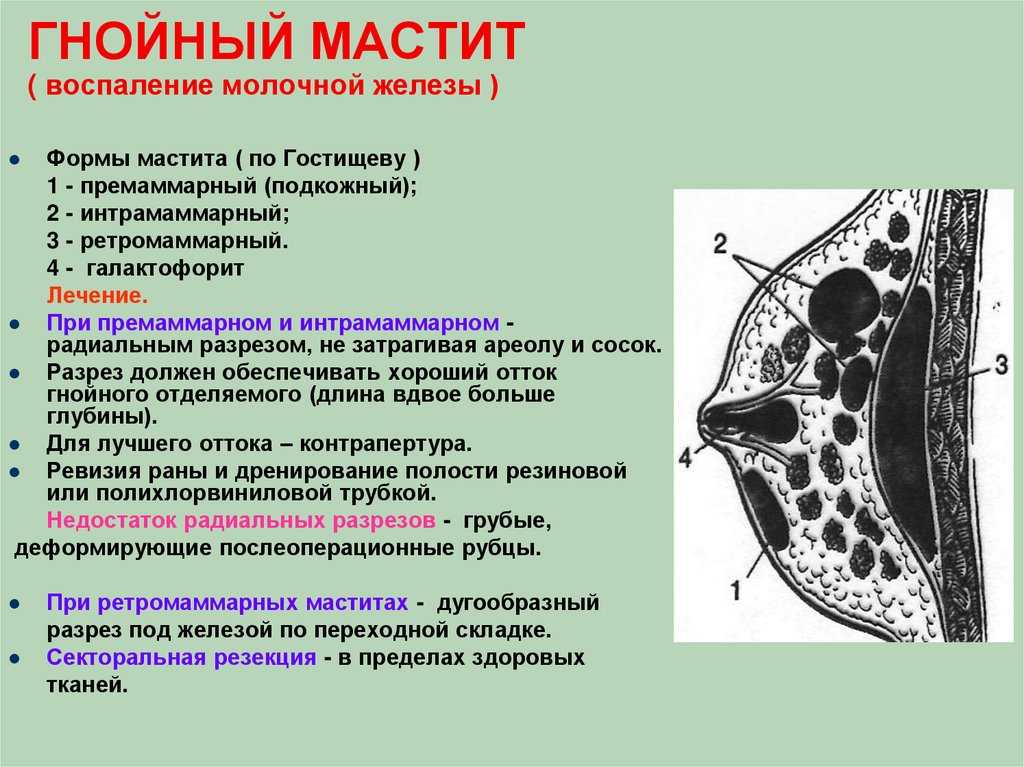 Таким образом, производители молочных продуктов имеют ограниченные возможности прогнозировать прогрессирование или влиять на исход прототекального мастита и ограничены вариантами лечения, аналогичными тем, которые используются для лечения хронического мастита, вызванного другими патогенами. Таким образом, профилактика является первостепенной задачей, а не смягчением последствий инфекций. Чтобы уменьшить воздействие возбудителя на других неинфицированных коров в стаде, коров с хроническим маститом часто выбраковывают.
Таким образом, производители молочных продуктов имеют ограниченные возможности прогнозировать прогрессирование или влиять на исход прототекального мастита и ограничены вариантами лечения, аналогичными тем, которые используются для лечения хронического мастита, вызванного другими патогенами. Таким образом, профилактика является первостепенной задачей, а не смягчением последствий инфекций. Чтобы уменьшить воздействие возбудителя на других неинфицированных коров в стаде, коров с хроническим маститом часто выбраковывают.
Первичный возбудитель прототекального мастита крупного рогатого скота был идентифицирован как P zopfii . В других сообщениях ставится под сомнение абсолютная исключительность P zopfii как этиологического агента прототекального мастита, но на практике коров, у которых выявлен мастит, вызванный Prototheca sp, лечат аналогичным образом, независимо от вида или генотипа. Часто Prototheca ошибочно идентифицируются при рутинном молочном культивировании, и следует использовать либо селективные среды, либо использование окраски по Граму для идентификации крупных организмов (по сравнению с типичными бактериями).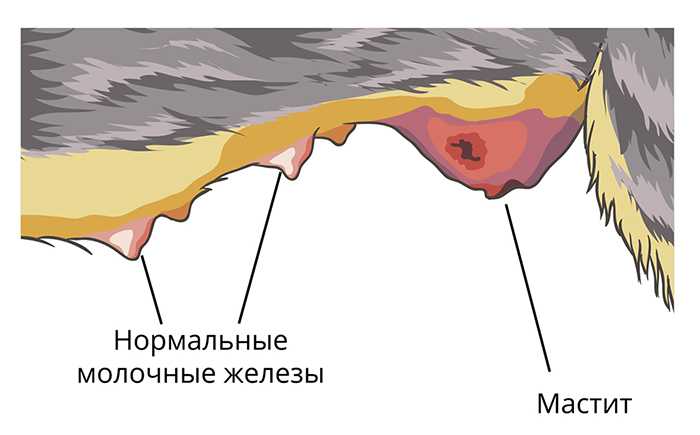
Мастит, вызванный Bacillus spp., имеет то же происхождение, клиническую картину и методы профилактики, что и другие необычные патогены. Как и в случае с другими микроорганизмами этой категории, лечение обычно не приводит к успеху.
Профилактика клинического мастита практически идентична профилактике субклинического мастита, т. е. снижение воздействия микробов на соски. Поскольку большинство случаев клинического мастита вызывается возбудителями преимущественно из окружающей среды, крайне важно уменьшить воздействие на подстилку, жилище или на открытых участках и пастбищах. Тем не менее, надлежащая гигиена перед доением, чтобы убедиться, что соски чистые и сухие перед установкой доильного аппарата, включая использование гермицидов (обмакивание сосков перед доением), является полезным.
За исключением бактеринов, которые воздействуют на грамотрицательные патогены, в частности на кишечные палочки, иммунизация для уменьшения последствий мастита была в основном безуспешной или, в лучшем случае, непостоянной. Технология сердцевинного антигена на основе мутанта J5 E coli может помочь уменьшить тяжесть клинического мастита, вызванного кишечной палочкой. Иммунизация этими бактеринами должна включать как минимум многократные дозы в сухостойный период для снижения случаев клинического колиформного мастита, часто связанного с ранней лактацией. Протоколы для увеличенного количества иммунизаций этими бактеринами могут быть оправданы в стадах с высокими показателями тяжелого мастита после 60 дней в молоке, потому что защита часто ослабевает через 50–60 дней после последней иммунизации. Важно отметить, что эти бактерины уменьшают тяжесть клинических случаев мастита, вызванного только грамотрицательными возбудителями. Кроме того, хотя тяжесть клинических признаков может быть уменьшена, эти бактерины не предотвращают инфекции.
Технология сердцевинного антигена на основе мутанта J5 E coli может помочь уменьшить тяжесть клинического мастита, вызванного кишечной палочкой. Иммунизация этими бактеринами должна включать как минимум многократные дозы в сухостойный период для снижения случаев клинического колиформного мастита, часто связанного с ранней лактацией. Протоколы для увеличенного количества иммунизаций этими бактеринами могут быть оправданы в стадах с высокими показателями тяжелого мастита после 60 дней в молоке, потому что защита часто ослабевает через 50–60 дней после последней иммунизации. Важно отметить, что эти бактерины уменьшают тяжесть клинических случаев мастита, вызванного только грамотрицательными возбудителями. Кроме того, хотя тяжесть клинических признаков может быть уменьшена, эти бактерины не предотвращают инфекции.
Успех кор-антигенных бактеринов зависит от пяти фундаментальных принципов :
Подтверждение того, что кишечные палочки являются основной причиной тяжелого клинического мастита в стаде, путем посева образцов молока.

Определите, составляет ли заболеваемость тяжелым колиформным маститом >1% поголовья каждый год.
Опишите животных, подверженных риску, например, количество дней в молоке и период лактации.
Уменьшить другие факторы риска колиформного мастита в стаде, такие как неподходящие подстилки.
Разработайте протокол вакцинации для животных из группы риска.
Недавно вакцина, нацеленная на Klebsiella spp. путем иммунизации против сидерофорных (захватывающих железо) белков, которые являются важным фактором вирулентности для грамотрицательных патогенов, продемонстрировала перспективность снижения тяжести клинического мастита, вызванного этой подгруппой патогены.
Достижения в подходах к лечению и лечению мастита крупного рогатого скота: всесторонний обзор
- DOI:10.1080/01652176.2021.1882713
- Идентификатор корпуса: 231758120
@article{Sharun2021AdvancesIT,
title={Достижения в подходах к лечению и лечению мастита крупного рогатого скота: всесторонний обзор},
автор={Кхан Шарун и Кулдип Дхама и Ручи Тивари и Мудасир Башир Гугджу и Мохд.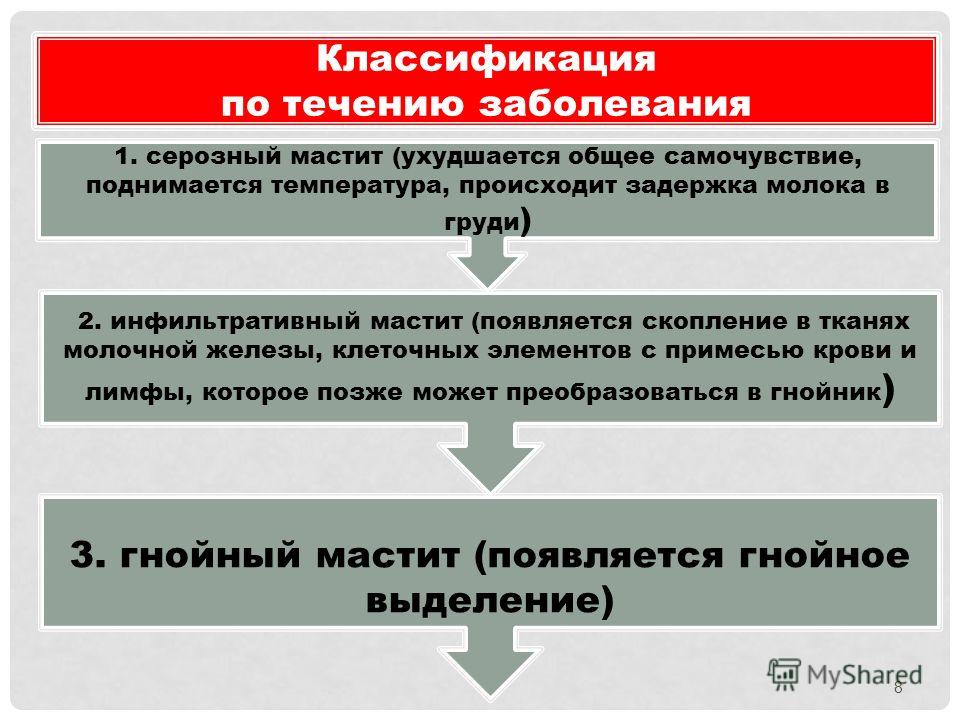 Икбал Яту и Шайлеш Кумар Патель и Мамта Патхак и Кумарагурубаран Картик и Сандип Кумар Кхурана и Рахул Сингх и Бхавани Пуввала и Амарпал и Раджендра Сингх и Карам Пал Сингх и Ванпен Чайкумпа},
journal={Ежеквартальный ветеринарный журнал},
год = {2021},
объем = {41},
страницы={107–136}
}
Икбал Яту и Шайлеш Кумар Патель и Мамта Патхак и Кумарагурубаран Картик и Сандип Кумар Кхурана и Рахул Сингх и Бхавани Пуввала и Амарпал и Раджендра Сингх и Карам Пал Сингх и Ванпен Чайкумпа},
journal={Ежеквартальный ветеринарный журнал},
год = {2021},
объем = {41},
страницы={107–136}
} - K. Sharun, K. Dhama, W. Chaicumpa
- Опубликовано 1 января 2021 г.
- Medicine
- The Veterinary Quarterly
Abstract влияя на благополучие животных, а также нанося огромные экономические убытки молочной промышленности из-за снижения производственных показателей и увеличения показателей выбраковки. Мастит крупного рогатого скота – это воспаление молочных желез/вымени крупного рогатого скота, в большинстве случаев вызываемое бактериальными возбудителями. Рутинная диагностика основана на клинических и субклинических формах…
Посмотреть на Taylor & Francis
tandfonline.com
Терапевтическая эффективность бактериофагового препарата Фагомаст при клиническом мастите коров
Фаготерапия является эффективным и безопасным способом лечения инфекционных заболеваний, вызванных различными видами бактерий, в том числе мастита у коров. Тем не менее, количество исследований фагов in vivo для лечения…
Тем не менее, количество исследований фагов in vivo для лечения…
Влияние артемизинина на индуцированный Escherichia coli мастит в эпителиальных клетках молочной железы крупного рогатого скота и мышах
- Zhaoming Li, Jiaqing Hu, Jianzhu Liu
Медицина
Ветеринария
- 2022
Показано, что артемизинин обладает защитным действием против мастита, вызванного Escherichia coli, что обеспечивает практический подход к клиническому контролю мастита.
Эффективность растительного препарата при маститах крупного рогатого скота
- Аминова А., Юмагузин И., Субханкулов Нияз, Седых Т.
Медицина
Аграрный вестник
- 2021
Оптимальная дозировка для ежедневного внутритканевого введения при серозном мастите составила 5 мл и 10 мл при катаральном мастите, а сравнение терапевтического действия фитопрепаратов Райдо и Рипосол выявило более высокую эффективность ежедневного применения Райдо в этих дозировках .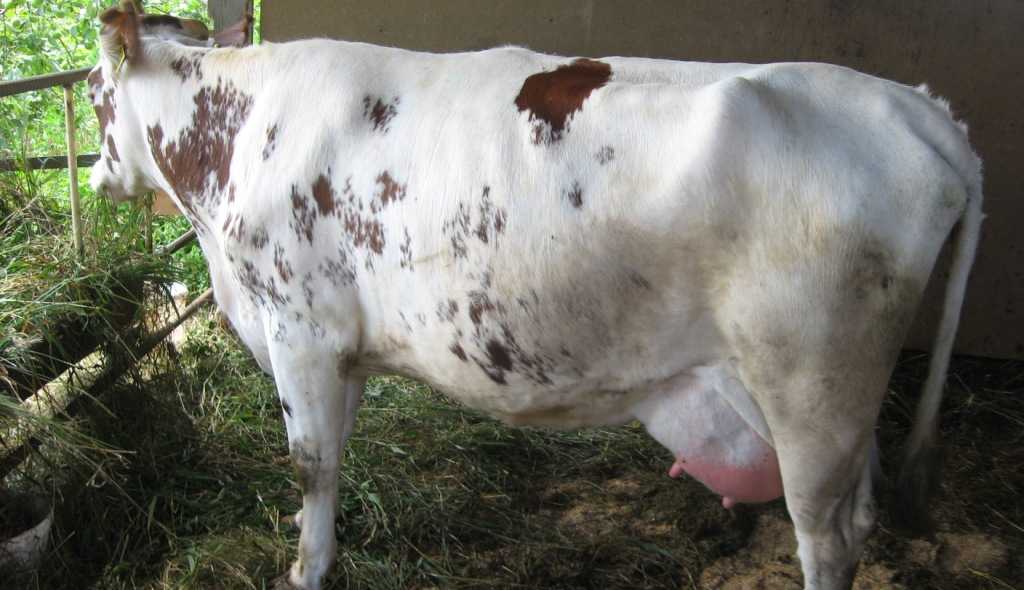
Профилактика мастита у повторнородящих молочных коров с маститом в анамнезе путем перорального кормления пробиотиком Bacillus subtilis.
Мастит — очень распространенное воспалительное заболевание молочной железы молочных коров, приводящее к снижению надоев и качества молока. Пробиотики могут служить альтернативой антибиотикам для…
Профилактика мастита крупного рогатого скота с помощью вакцинации.
- Жылкайдар А., Орынтаев К., Алтенов А., Кылпыбай Э., Чайхмет Э.
Медицина
Архив Института Рази
- 2021
- Косенко Ю., Остапив Н., Зарума Л., Пономарова С.А. Целью данного исследования было продолжение выполнения рекомендаций МЭБ по мониторингу объемов продаж противомикробных ветеринарных лекарственных средств.
 Предметом исследования были…
Предметом исследования были…ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ ПРЕПАРАТА НА ОСНОВЕ ЙОДА ПРИ МАСТИТЕ У КОРОВ
- Фотина Т., Нахорна Л., Нестерук В.С.
- 2021
препарат на основе йода для лечения различных форм мастита коров в хозяйстве по производству…
Химический состав, антиоксидантная и антибактериальная активность двух различных эфирных масел в отношении возбудителей, ассоциированных с маститом
- Д. Томанич, Б. Божин, З. Ковачевич
Acta Veterinaria
- 2022
Резюме Мастит является одним из наиболее распространенных и дорогостоящих заболеваний молочных коров во всем мире. Поскольку устойчивость к антибиотикам стала глобальной угрозой как для здоровья животных, так и для человека, она становится…
Оценка терапевтической эффективности наночастиц меди в модели мастита крыс, вызванного Staphylococcus aureus
Сделан вывод, что CuNPs могут обеспечить потенциальную альтернативную терапевтическую схему для лечения мастита крупного рогатого скота и в дальнейшем демонстрируют раннее выздоровление, снижение бактериальной нагрузки и улучшение показателей окислительного стресса.

Распространенность и факторы риска стафилококкового субклинического мастита у молочных животных Читвана, Непал
Субклинический мастит (СКМ), бессимптомное воспаление ткани молочной железы, является наиболее распространенной формой мастита у домашнего скота. Распространенность СКМ и факторы риска у молочных животных в Западном Читване,…
ПОКАЗАНЫ 1-10 ИЗ 297 ССЫЛОК
СОРТИРОВАТЬ ПОРелевантность Наиболее влиятельные документыНедавность
Борьба с маститом крупного рогатого скота: старые и современные терапевтические подходы
Непрерывный поиск новых терапевтических альтернатив, эффективных для контроля и лечения мастита крупного рогатого скота, является неотложным, и в этом обзоре будет представлен обзор некоторых традиционных и новых подходов к лечению инфекций, вызванных маститом b крупного рогатого скота.
Мастит крупного рогатого скота: оценка его альтернативного лечения травами.
Обзор симпозиума: особенности патогенеза мастита, вызванного Staphylococcus aureus, которые определяют стратегии разработки вакцин.

Целью данного обзора является обобщение ключевых концепций, связанных с патогенезом Staph.
Эффективность и фармакокинетика бактериофаговой терапии при лечении субклинического мастита, вызванного золотистым стафилококком, у лактирующих молочных коров
Концентрация фага в молоке свидетельствует о значительной деградации или инактивации введенного фага в железах молочной железы крупного рогатого скота, что является серьезная проблема для молочной промышленности из-за его устойчивости к лечению антибиотиками и склонности к хроническому рецидивированию.
Терапевтическое действие низина Z на субклинический мастит у лактирующих коров
Активность NAGазы в образцах молока и количество молочных четвертей с количеством соматических клеток в молоке ≥500 000/мл были значительно снижены после лечения низином, в то время как в контрольной группе существенных изменений не произошло.

Безопасность и эффективность интрамаммарной терапии мезенхимальными стволовыми клетками у молочных коров с экспериментально индуцированным клиническим маститом, вызванным Staphylococcus aureus
- O. Peralta, C. Carrasco, C. Torres
Medicine
Scientific Reports
- 2020
Предоставлены первоначальные доказательства безопасности и эффективности аллогенной интрамаммарной терапии на основе МСК для лечения мастита крупного рогатого скота за счет снижения количества бактерий в молоке коров с клиническим маститом, вызванным S. aureus, по сравнению с коровами, не получавшими лечения.
Технологические вмешательства и достижения в диагностике внутригрудных инфекций у животных с акцентом на популяции крупного рогатого скота — обзор
В этом обзоре обобщены различные диагностические тесты, доступные для выявления мастита, включая диагностику с помощью общих и специальных технологических вмешательств и достижений.

в современном животноводстве. Зарегистрировано поражение практически повсеместно, с учетом субклинической формы от 30% до 50%…
