Септический шок у детей: ДИАГНОСТИКА И ЛЕЧЕНИЕ СЕПСИСА И СЕПТИЧЕСКОГО ШОКА У ДЕТЕЙ | Тепаев
Септический шок. Что такое Септический шок?
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
R57.2
- Причины
- Патогенез
- Классификация
- Симптомы септического шока
- Осложнения
- Диагностика
- Лечение септического шока
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.
Септический шок
Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
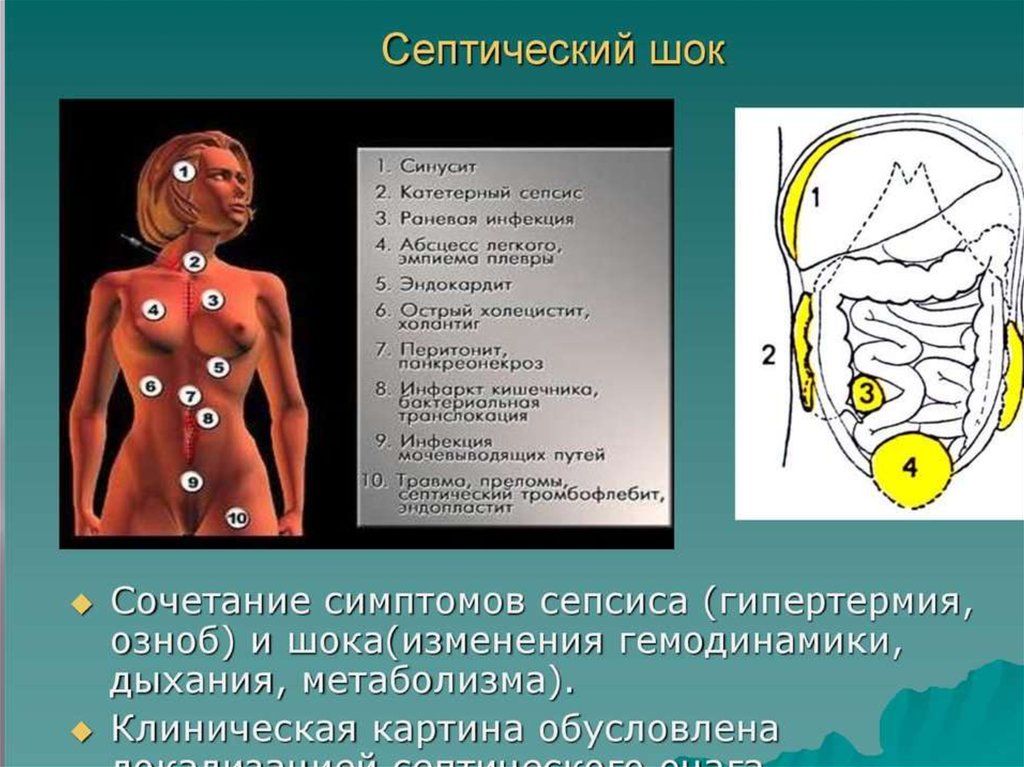
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока.
 Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок. - Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов.
 В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила). - СПИД. ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Шоковое состояние классифицируется по патогенетическому и клиническому принципу. Патогенетически болезнь может быть «теплой» и «холодной». Тёплый шок характеризуется увеличением сердечного выброса на фоне снижения общего сосудистого тонуса, эндогенной гиперкатехоламинемией и расширением внутрикожных сосудов. Явления органной недостаточности выражены умеренно. Холодная разновидность проявляется снижением сердечного выброса, резким ослаблением тканевой перфузии, централизацией кровообращения и тяжелой ПОН. По клиническому течению септический шок подразделяется на следующие разновидности:
 Артериальное давление незначительно снижено, уровень САД не меньше 90 мм ртутного столба. Выявляется тахикардия (PS <100 уд/мин). Субъективно пациент ощущает слабость, головокружение, головную боль и снижение мышечного тонуса.
Артериальное давление незначительно снижено, уровень САД не меньше 90 мм ртутного столба. Выявляется тахикардия (PS <100 уд/мин). Субъективно пациент ощущает слабость, головокружение, головную боль и снижение мышечного тонуса.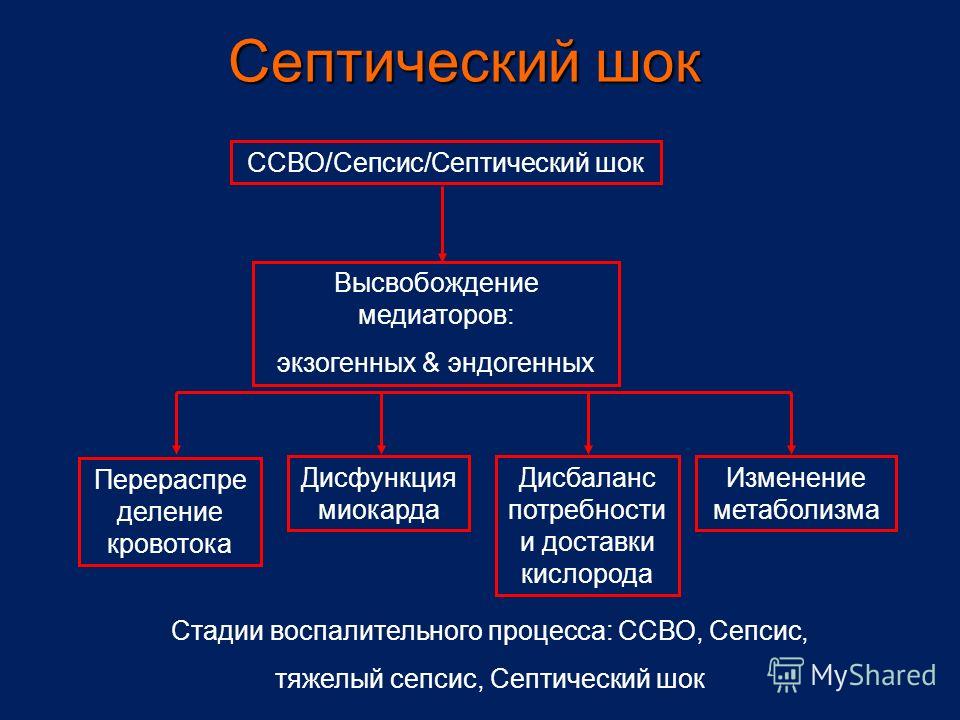 Сознание отсутствует, кожа мраморного оттенка или серая, покрытая синюшными пятнами. Дыхание патологическое по типу Биота или Куссмауля, ЧДД снижается до 8-10 раз/минуту, иногда дыхание полностью прекращается. САД менее 50 мм рт. столба. Мочеотделение отсутствует. Пульс с трудом пальпируется даже на центральных сосудах.
Сознание отсутствует, кожа мраморного оттенка или серая, покрытая синюшными пятнами. Дыхание патологическое по типу Биота или Куссмауля, ЧДД снижается до 8-10 раз/минуту, иногда дыхание полностью прекращается. САД менее 50 мм рт. столба. Мочеотделение отсутствует. Пульс с трудом пальпируется даже на центральных сосудах.Симптомы септического шока
Один из определяющих признаков ИТШ – артериальная гипотония. Восстановить уровень АД не удается даже при адекватном объеме инфузии (20-40 мл/кг). Для поддержания гемодинамики необходимо использовать прессорные амины (допамин). Отмечается острая олигурия, диурез не превышает 0,5 мл/кг/час. Температура тела достигает фебрильных значений – 38-39° C, плохо снижается с помощью антипиретиков. Для предупреждения судорог, вызванных гипертермией, приходится применять физические методы охлаждения.
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
Диагноз устанавливается врачом анестезиологом-реаниматологом. Предположение строится на клинических данных, однако с точностью определить имеющееся состояние можно только при наличии результатов аппаратного и лабораторного исследований. При подозрении на септический шок все анализы делаются в экстренном режиме, «по cito». Реанимационные мероприятия следует начинать, не дожидаясь окончания работы вспомогательных служб. Комплексное обследование, необходимое для определения и подтверждения ИТШ, включает в себя:
- Осмотр и физикальное исследование.
 Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг. - Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов.
 У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (<100 × 10⁹/л). При прогрессирующей анемии эритроциты составляют 1,5-2,5 миллиона в 1 мм3, гемоглобин ниже 90 г/л. pH венозной крови <7,3 (метаболический ацидоз).
У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (<100 × 10⁹/л). При прогрессирующей анемии эритроциты составляют 1,5-2,5 миллиона в 1 мм3, гемоглобин ниже 90 г/л. pH венозной крови <7,3 (метаболический ацидоз).
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение.
 При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования. - Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.

Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
Источники
- Реанимация и интенсивная терапия// Жданов Г.Г., Зильбер А.П. – 2007.
- Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.

- Сепсис и септический шок/ Кузьков В.В. – 2015.
- Настоящая статья подготовлена по материалам сайта: https://www.krasotaimedicina.ru/
ВАЖНО
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Различные стратегии инфузионной терапии сепсиса и септического шока
Вопрос обзора
Мы стремились выяснить, может ли либеральная терапия жидкостями привести к более благоприятным или повреждающим эффектам по сравнению с консервативной инфузионной терапией взрослых и детей с тяжелым сепсисом или септическим шоком. Мы в основном оценили различное влияние этих двух вмешательств на риск смерти и возникновения неблагоприятных событий.
Актуальность
Сепсис и септический шок являются осложнениями инфекции. Это состояние с большей вероятностью развивается у пациентов в отделениях интенсивной терапии (ОИТ), чем у других. При септическом шоке у пациентов развивается дисфункция органов, которая в некоторых случаях может привести к смерти. Терапия жидкостями часто используется в качестве важного вмешательства для начального лечения сепсиса у взрослых и детей.
Это состояние с большей вероятностью развивается у пациентов в отделениях интенсивной терапии (ОИТ), чем у других. При септическом шоке у пациентов развивается дисфункция органов, которая в некоторых случаях может привести к смерти. Терапия жидкостями часто используется в качестве важного вмешательства для начального лечения сепсиса у взрослых и детей.
Результаты
Мы провели поиск в электронных базах данных 16 января 2018 года. Мы не обнаружили ни одного исследования у взрослых, которое соответствовало бы нашим критериям включения. Мы включили три испытания с участием 3402 детей. Мы определили три «текущих» (или продолжающихся) испытания, которые еще не были опубликованы. Объединенные результаты двух исследований (с участием 3288 детей) показывают, что либеральная терапия жидкостями может повысить риск смерти в стационаре на 38%, а риск смерти при четырехнедельном наблюдении на 39%. Это означает, что на каждые 34 ребенка, получающих терапию жидкостями, в группе либеральной инфузионной терапии будет на одну внутрибольничную смерть больше, чем в группе консервативной терапии. Аналогично, на четвертой неделе наблюдения в группе либеральной инфузионной терапии будет на одну смерть больше, чем в группе консервативной инфузионной терапии на каждые 29 детей, получающих терапию жидкостями. Одно небольшое исследование сообщило о неубедительных результатах по риску внутрибольничной смерти. У нас нет определённости, есть ли разница в неблагоприятных эффектах (например, развитии гепатомегалии, аллергических реакций и неврологических последствий, необходимости вентиляции легких) между пациентами, получающими либеральную или консервативную терапию жидкостями.
Аналогично, на четвертой неделе наблюдения в группе либеральной инфузионной терапии будет на одну смерть больше, чем в группе консервативной инфузионной терапии на каждые 29 детей, получающих терапию жидкостями. Одно небольшое исследование сообщило о неубедительных результатах по риску внутрибольничной смерти. У нас нет определённости, есть ли разница в неблагоприятных эффектах (например, развитии гепатомегалии, аллергических реакций и неврологических последствий, необходимости вентиляции легких) между пациентами, получающими либеральную или консервативную терапию жидкостями.
В одном исследовании (с участием 101 ребенка) сообщили, что консервативная терапия жидкостями может сократить пребывание в отделении интенсивной терапии и длительность вентиляции лёгких. Однако, у нас очень мало уверенности в этих результатах из-за малого размера выборки. Мы не нашли исследований с участием взрослых с сепсисом или септическим шоком.
Выводы
Доказательства низкого и высокого качества показывают, что либеральная терапия жидкостями может повысить уровень смертности среди детей с сепсисом или септическим шоком. За исключением этих результатов, у нас нет определённости относительно влияния либеральной и консервативной терапии жидкостями на риск неблагоприятных событий. У нас также нет определённости относительно влияния этих двух вмешательств у взрослых с сепсисом или септическим шоком из-за отсутствия данных. Ожидаются будущие испытания, посвященные сепсису или септическому шоку у взрослых в других условиях с более широким спектром патогенных микроорганизмов. После публикации и оценки, эти три выявленные продолжающиеся исследования могут изменить выводы этого обзора.
За исключением этих результатов, у нас нет определённости относительно влияния либеральной и консервативной терапии жидкостями на риск неблагоприятных событий. У нас также нет определённости относительно влияния этих двух вмешательств у взрослых с сепсисом или септическим шоком из-за отсутствия данных. Ожидаются будущие испытания, посвященные сепсису или септическому шоку у взрослых в других условиях с более широким спектром патогенных микроорганизмов. После публикации и оценки, эти три выявленные продолжающиеся исследования могут изменить выводы этого обзора.
Заметки по переводу:
Перевод: Потапов Александр Сергеевич. Редактирование: Зиганшина Лилия Евгеньевна. Координация проекта по переводу на русский язык: Кокрейн Россия — Cochrane Russia, Cochrane Geographic Group Associated to Cochrane Nordic. По вопросам, связанным с этим переводом, пожалуйста, обращайтесь к нам по адресу: [email protected]
Педиатрия: лечение септического шока
1. Weiss SL, Fitzgerald JC, Pappachan J, et al. Глобальная эпидемиология тяжелого сепсиса у детей: исследование распространенности сепсиса, исходов и методов лечения. Am J Respir Crit Care Med. 2015;191(10):1147–1157. doi: 10.1164/rccm.201412-2323OC. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Глобальная эпидемиология тяжелого сепсиса у детей: исследование распространенности сепсиса, исходов и методов лечения. Am J Respir Crit Care Med. 2015;191(10):1147–1157. doi: 10.1164/rccm.201412-2323OC. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2. Hon K, Leung AK, Wong JC. Распространение синдромов и аббревиатур в педиатрической реанимации: мы более или менее запутались? Hong Kong Med J. 2020;26(3):260–262. дои: 10.12809/hkmj198059. [PubMed] [CrossRef] [Google Scholar]
3. Seymour CW, Liu VX, Iwashyna TJ, et al. Оценка клинических критериев сепсиса. ДЖАМА. 2016;315(8):762–774. doi: 10.1001/jama.2016.0288. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Singer M, Deutschman CS, Seymour CW, et al. Третье международное консенсусное определение сепсиса и септического шока (сепсис-3) JAMA. 2016;315(8):801–810. doi: 10.1001/jama.2016.0287. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
5. Шанкар-Хари М., Филлипс Г. С., Леви М.Л. и соавт. Разработка нового определения и оценка новых клинических критериев септического шока. ДЖАМА. 2016;315(8):775–787. doi: 10.1001/jama.2016.0289. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
С., Леви М.Л. и соавт. Разработка нового определения и оценка новых клинических критериев септического шока. ДЖАМА. 2016;315(8):775–787. doi: 10.1001/jama.2016.0289. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
6. Rhodes A, Evans LE, Alhazzani W, et al. Кампания по выживанию при сепсисе: международные рекомендации по лечению сепсиса и септического шока: 2016 г. Intensive Care Med. 2017;43(3):304–377. doi: 10.1007/s00134-017-4683-6. [PubMed] [CrossRef] [Академия Google]
7. Brun-Buisson C, Doyon F, Carlet J, et al. Заболеваемость, факторы риска и исход тяжелого сепсиса и септического шока у взрослых: многоцентровое проспективное исследование в отделениях интенсивной терапии. J Am Med Assoc. 1995;274(12):968–974. [PubMed] [Google Scholar]
8. Kaukonen K-M, Bailey M, Pilcher D, Cooper DJ, Bellomo R. Критерии синдрома системной воспалительной реакции в определении тяжелого сепсиса. N Engl J Med. 2015;372(17):1629–1638. doi: 10.1056/nejmoa1415236. [PubMed] [CrossRef] [Академия Google]
9. Ангус Д.К., Ван дер Полл Т. Тяжелый сепсис и септический шок. N Engl J Med. 2013;369(9):840–851. doi: 10.1056/NEJMra1208623. [PubMed] [CrossRef] [Google Scholar]
Ангус Д.К., Ван дер Полл Т. Тяжелый сепсис и септический шок. N Engl J Med. 2013;369(9):840–851. doi: 10.1056/NEJMra1208623. [PubMed] [CrossRef] [Google Scholar]
10. Gustot T. Полиорганная недостаточность при сепсисе: прогноз и роль системной воспалительной реакции. Curr Opin Crit Care. 2011;17(2):153–159. doi: 10.1097/MCC.0b013e328344b446. [PubMed] [CrossRef] [Google Scholar]
11. Goldstein B, Giroir B, Randolph A. Международная консенсусная конференция по педиатрическому сепсису: определения сепсиса и органной дисфункции в педиатрии. Pediatr Crit Care Med. 2005;6(1):2–8. дои: 10.1097/01.ПКС.0000149131.72248.Е6. [PubMed] [CrossRef] [Google Scholar]
12. Weiss SL, Peters MJ, Alhazzani W, et al. Международные рекомендации по лечению септического шока и связанной с сепсисом органной дисфункции у детей в рамках кампании по борьбе с сепсисом. Интенсивная терапия Мед. 2020; 46 (Приложение 1): 10–67. doi: 10.1007/s00134-019-05878-6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
13. Menon K, Schlapbach LJ, Akech S, et al. Детское определение сепсиса — протокол систематического обзора Целевой группы по определению педиатрического сепсиса. Исследование критического ухода. 2020;2(6):e0123. дои: 10.1097/cce.0000000000000123. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Menon K, Schlapbach LJ, Akech S, et al. Детское определение сепсиса — протокол систематического обзора Целевой группы по определению педиатрического сепсиса. Исследование критического ухода. 2020;2(6):e0123. дои: 10.1097/cce.0000000000000123. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
14. Leclerc F, Leteurtre S, Duhamel A, et al. Суммарное влияние органных дисфункций и септического состояния на смертность детей в критическом состоянии. Am J Respir Crit Care Med. 2005;171(4):348–353. doi: 10.1164/rccm.200405-630OC. [PubMed] [CrossRef] [Google Scholar]
15. Хьюстон К.А., Джордж Э.К., Мейтленд К. Значение лечения шока у детей в условиях ограниченных ресурсов: взгляд из исследования FEAST. Критический уход. 2018;22(1):119. doi: 10.1186/s13054-018-1966-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Davis AL, Carcillo JA, Aneja RK, et al. Параметры клинической практики Американского колледжа медицины критических состояний для гемодинамической поддержки педиатрического и неонатального септического шока. Крит Уход Мед. 2017;45(6):1061–1093. doi: 10.1097/CCM.0000000000002425. [PubMed] [CrossRef] [Google Scholar]
Крит Уход Мед. 2017;45(6):1061–1093. doi: 10.1097/CCM.0000000000002425. [PubMed] [CrossRef] [Google Scholar]
17. Brierley J, Carcillo JA, Choong K, et al. Параметры клинической практики для гемодинамической поддержки педиатрического и неонатального септического шока: обновление 2007 г. от Американского колледжа медицины критических состояний. Крит Уход Мед. 2009 г.;37(2):666–688. doi: 10.1097/CCM.0b013e31819323c6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
18. Morin L, Ray S, Wilson C, et al. Рефрактерный септический шок у детей: определение Европейского общества педиатрической и неонатальной интенсивной терапии. Интенсивная терапия Мед. 2016;42(12):1948–1957. doi: 10.1007/s00134-016-4574-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
19. Brun-Buisson C. Эпидемиология системного воспалительного ответа. Интенсивная терапия Мед. 2000; 26 (S1): S064–S074. doi: 10.1007/s001340051121. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
20. Дельгадо И., Рашински А., Тотапалли Б.Р., Хон К.Л.Э. Инотропы, абсолютное количество моноцитов и выживаемость детей с септическим шоком. HK J Педиатр. 2016;21(1):22–26. [Google Scholar]
Дельгадо И., Рашински А., Тотапалли Б.Р., Хон К.Л.Э. Инотропы, абсолютное количество моноцитов и выживаемость детей с септическим шоком. HK J Педиатр. 2016;21(1):22–26. [Google Scholar]
21. Rudd KE, Johnson SC, Agesa KM, et al. Глобальная, региональная и национальная заболеваемость и смертность от сепсиса, 1990–2017 гг.: анализ для исследования глобального бремени болезней. Ланцет. 2020;395(10219):200–211. doi: 10.1016/S0140-6736(19)32989-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. де Соуза Д.С., Шие Х.Х., Баррейра Э.Р., Вентура АМС, Буссо А., Тростер Э.Дж. Эпидемиология сепсиса у детей, поступивших в отделения интенсивной терапии в Южной Америке. Pediatr Crit Care Med. 2016;17(8):727–734. doi: 10.1097/PCC.0000000000000847. [PubMed] [CrossRef] [Google Scholar]
23. Hartman ME, Linde-Zwirble WT, Angus DC, Watson RS. Тенденции в эпидемиологии тяжелого сепсиса у детей. Pediatr Crit Care Med. 2013;14(7):686–693. doi: 10.1097/PCC.0b013e3182917fad. [PubMed] [CrossRef] [Академия Google]
[PubMed] [CrossRef] [Академия Google]
24. Деллинджер Р.П., Леви М.М., Родс А. и соавт. Кампания по выживанию при сепсисе: международные рекомендации по лечению тяжелого сепсиса и септического шока, 2012 г. Intensive Care Med. 2013;41(2):165–228. doi: 10.1097/CCM.0b013e31827e83af. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
25. Huang C-T, Tsai YJ, Tsai P-R, Yu CJ, Ko WJ. Тяжелый сепсис и септический шок. Шок. 2016;45(5):518–524. doi: 10.1097/SHK.0000000000000540. [PubMed] [CrossRef] [Google Scholar]
26. Drumheller BC, Agarwal A, Mikkelsen ME, et al. Факторы риска смертности, несмотря на раннюю протоколированную реанимацию при тяжелом сепсисе и септическом шоке в отделении неотложной помощи. J Крит Уход. 2016;31(1):13–20. doi: 10.1016/j.jcrc.2015.10.015. [PubMed] [CrossRef] [Академия Google]
27. Церцвадзе А., Ройл П., Сидат Ф., Купер Дж., Кросби Р., Маккарти Н. Внебольничный сепсис и его бремя для общественного здравоохранения: систематический обзор. Системная редакция 2016; 5(1):81. doi: 10.1186/s13643-016-0243-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Системная редакция 2016; 5(1):81. doi: 10.1186/s13643-016-0243-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Estenssoro E, Dubin A, Laffaire E, et al. Заболеваемость, клиническое течение и исход у 217 пациентов с острым респираторным дистресс-синдромом. Крит Уход Мед. 2002;30(11):2450–2456. doi: 10.1097/00003246-200211000-00008. [PubMed] [CrossRef] [Академия Google]
29. Синель И., Опал С.М. Молекулярная биология воспаления и сепсиса: учебник для начинающих. Крит Уход Мед. 2009;37(1):291–304. doi: 10.1097/CCM.0b013e31819267fb. [PubMed] [CrossRef] [Google Scholar]
30. Hotchkiss RS, Karl IE. Патофизиология и лечение сепсиса. N Engl J Med. 2003;348(2):138–150. doi: 10.1056/NEJMra021333. [PubMed] [CrossRef] [Google Scholar]
31. Schwarz MA. Острое повреждение легких: клеточные механизмы и нарушения. Pediatr Respir Respir. 2001; 2 (1): 3–9.. doi: 10.1053/prrv.2000.0095. [PubMed] [CrossRef] [Google Scholar]
32. Коллеф М.Х., Шустер Д. П. Острый респираторный дистресс-синдром. N Engl J Med. 1995;332(1):27–37. doi: 10.1056/NEJM199501053320106. [PubMed] [CrossRef] [Google Scholar]
П. Острый респираторный дистресс-синдром. N Engl J Med. 1995;332(1):27–37. doi: 10.1056/NEJM199501053320106. [PubMed] [CrossRef] [Google Scholar]
33. Vaishnavi C. Транслокация кишечной флоры и ее роль при сепсисе. Индийская J Med Microbiol. 2013;31(4):334–342. doi: 10.4103/0255-0857.118870. [PubMed] [CrossRef] [Google Scholar]
34. Kinross J, von Roon A, Penney N, et al. Микробиота кишечника как мишень для улучшения хирургического результата и улучшения ухода за пациентами. Курр Фарм Дез. 2009 г.;15(13):1537–1545. doi: 10.2174/138161209788168119. [PubMed] [CrossRef] [Google Scholar]
35. Kothari N, Bogra J, Kohli M, et al. Роль молекул активного азота в развитии септического шока. Acta Anaesthesiol Scand. 2012;56(3):307–315. doi: 10.1111/j.1399-6576.2011.02607.x. [PubMed] [CrossRef] [Google Scholar]
36. Crouser ED. Митохондриальная дисфункция при септическом шоке и синдроме полиорганной дисфункции. Митохондрия. 2004;4(5–6):729–741. doi: 10.1016/j.mito.2004. 07.023. [PubMed] [CrossRef] [Академия Google]
07.023. [PubMed] [CrossRef] [Академия Google]
37. Леви М., тен Кейт Х., ван дер Полл Т., ван Девентер С.Дж. Патогенез диссеминированного внутрисосудистого свертывания крови при сепсисе. ДЖАМА. 1993;270(8):975–979. http://www.ncbi.nlm.nih.gov/pubmed/8345649. [PubMed] [Google Scholar]
38. Landry DW, Oliver JA. Патогенез вазодилататорного шока. В: Эпштейн Ф.Х., редактор. N Engl J Med. 8. Том. 345. 2001. стр. 588–595. [PubMed] [CrossRef] [Google Scholar]
39. Papathanassoglou ED, Moynihan JA, Ackerman MH. Играет ли роль запрограммированная гибель клеток (апоптоз) в развитии полиорганной дисфункции у пациентов в критическом состоянии? Обзор и теоретическая основа. Крит Уход Мед. 2000; 28(2):537–549.. doi: 10.1097/00003246-200002000-00042. [PubMed] [CrossRef] [Google Scholar]
40. Коцоволис Г., Калларас К. Роль эндотелия и эндогенных вазоактивных веществ при сепсисе. Гиппократия. 2010;14(2):88–93. http://www.ncbi.nlm.nih.gov/pubmed/20596262. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Bone RC, Balk RA, Cerra FB, et al. Определения сепсиса и органной недостаточности и рекомендации по использованию инновационных методов лечения сепсиса. Грудь. 1992;101(6):1644–1655. doi: 10.1378/сундук.101.6.1644. [PubMed] [CrossRef] [Академия Google]
Bone RC, Balk RA, Cerra FB, et al. Определения сепсиса и органной недостаточности и рекомендации по использованию инновационных методов лечения сепсиса. Грудь. 1992;101(6):1644–1655. doi: 10.1378/сундук.101.6.1644. [PubMed] [CrossRef] [Академия Google]
42. Shankar-Hari M, Bertolini G, Brunkhorst FM, et al. Оценка качества текущих определений и критериев септического шока. Критический уход. 2015;19:445–1164. doi: 10.1186/s13054-015-1164-6. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Brink M, Cronqvist J, Fagerberg A, et al. Новое определение и диагностические критерии сепсиса — шведское использование Сепсиса-3. Лакартинген. 2018;115:E3W9. [PubMed] [Google Scholar]
44. Чамейдес Л., Самсон Р., Шекснайдер С., Хазински М. Руководство по расширенному жизнеобеспечению в педиатрии. Американская Ассоциация Сердца; 2016. Признание шока. [Академия Google]
45. Майр Ф.Б., Йенде С., Ангус Д.С. Эпидемиология тяжелого сепсиса. Вирулентность. 2014;5(1):4–11. doi: 10.4161/viru.27372. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.4161/viru.27372. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
46. Machowicz R, Janka G, Wiktor-Jedrzejczak W. Похожие, но не одинаковые: дифференциальная диагностика ГЛГ и сепсиса. Crit Rev Oncol Hematol. 2017; 114:1–12. doi: 10.1016/j.critrevonc.2017.03.023. [PubMed] [CrossRef] [Google Scholar]
47. Wacker C, Prkno A, Brunkhorst FM, Schlattmann P. Прокальцитонин как диагностический маркер сепсиса: систематический обзор и метаанализ. Ланцет Infect Dis. 2013;13(5):426–435. дои: 10.1016/S1473-3099(12)70323-7. [PubMed] [CrossRef] [Google Scholar]
48. Schlapbach LJ, MacLaren G, Festa M, et al. Прогноз детской смертности от сепсиса в течение 1 часа после поступления в реанимацию. Интенсивная терапия Мед. 2017;43(8):1085–1096. doi: 10.1007/s00134-017-4701-8. [PubMed] [CrossRef] [Google Scholar]
49. Хименес М.Ф., Маршалл Дж.К. Контроль источника в лечении сепсиса. Интенсивная терапия Мед. 2001;27(14):S49–S62. doi: 10.1007/PL00003797. [PubMed] [CrossRef] [Google Scholar]
50. Абрахам Э., Сингер М. Механизмы органной дисфункции, вызванной сепсисом. Крит Уход Мед. 2007;35(10):2408–2416. дои: 10.1097/01.СКМ.0000282072.56245.91. [PubMed] [CrossRef] [Google Scholar]
Абрахам Э., Сингер М. Механизмы органной дисфункции, вызванной сепсисом. Крит Уход Мед. 2007;35(10):2408–2416. дои: 10.1097/01.СКМ.0000282072.56245.91. [PubMed] [CrossRef] [Google Scholar]
51. Dellinger RP, Levy MM, Carlet JM, et al. Кампания по выживанию при сепсисе: международные рекомендации по лечению тяжелого сепсиса и септического шока: 2008 г. Crit Care Med. 2008;36(1):296–327. doi: 10.1097/01.CCM.0000298158.12101.41. [PubMed] [CrossRef] [Google Scholar]
52. Левинсон А.Т., Кассерли Б.П., Леви М.М. Снижение смертности при тяжелом сепсисе и септическом шоке. Семин Крит Уход Мед. 2011;32(2):195–205. doi: 10.1055/s-0031-1275532. [PubMed] [CrossRef] [Академия Google]
53. Риверс Э., Нгуен Б., Хавстад С. и др. Ранняя целенаправленная терапия при лечении тяжелого сепсиса и септического шока. N Engl J Med. 2001;345(19):1368–1377. doi: 10.1056/nejmoa010307. [PubMed] [CrossRef] [Google Scholar]
54. Общество реаниматологии. Алгоритм начальной реанимации у детей. [По состоянию на 16 марта 2021 г.]. Опубликовано в 2020 г.
[По состоянию на 16 марта 2021 г.]. Опубликовано в 2020 г.
55. Севранский Ю.Э., Леви М.М., Марини Ю.Дж. Механическая вентиляция легких при остром повреждении легких/остром респираторном дистресс-синдроме, вызванном сепсисом: обзор, основанный на доказательствах. Крит Уход Мед. 2004; 32 (Приложение 11): S548–S553. [PubMed] [Google Scholar]
56. Dugar S, Choudhary C, Duggal A. Сепсис и септический шок: лечение на основе рекомендаций. Клив Клин J Med. 2020;87(1):53–64. doi: 10.3949/ccjm.87a.18143. [PubMed] [CrossRef] [Google Scholar]
57. Alobaidi R, Morgan C, Basu RK, et al. Связь между балансом жидкости и исходами у детей в критическом состоянии. JAMA Педиатр. 2018;172(3):257–268. doi: 10.1001/jamapediatrics.2017.4540. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
58. Emrath ET, Fortenberry JD, Travers C, McCracken CE, Hebbar KB. Реанимация с использованием сбалансированных жидкостей связана с улучшением выживаемости при тяжелом сепсисе у детей. Крит Уход Мед. 2017;45(7):1177–1183. doi: 10.1097/CCM.0000000000002365. [PubMed] [CrossRef] [Google Scholar]
Крит Уход Мед. 2017;45(7):1177–1183. doi: 10.1097/CCM.0000000000002365. [PubMed] [CrossRef] [Google Scholar]
59. Бил Р. Дж., Холленберг С. М., Винсент Дж. Л., Паррильо Дж. Э. Вазопрессорная и инотропная поддержка при септическом шоке: обзор, основанный на доказательствах. Крит Уход Мед. 2004;32(11):S455–S465. doi: 10.1097/01.CCM.0000142909.86238.Б1. [PubMed] [CrossRef] [Google Scholar]
60. Patel GP, Grahe JS, Sperry M, et al. Эффективность и безопасность дофамина по сравнению с норадреналином при лечении септического шока. Шок. 2010;33(4):375–380. doi: 10.1097/SHK.0b013e3181c6ba6f. [PubMed] [CrossRef] [Google Scholar]
61. Nathan CR, Lang E, Dowling S. Дофамин против норадреналина при лечении шока. CJEM. 2011;13(6):395–397. doi: 10.2310/8000.2011.110297. [PubMed] [CrossRef] [Google Scholar]
62. De Backer D, Biston P, Devriendt J, et al. Сравнение дофамина и норадреналина при лечении шока. N Engl J Med. 2010;362(9): 779–789. doi: 10.1056/NEJMoa0907118. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
63. Morin L, Kneyber M, Jansen NJG, et al. Трансляционный пробел в лечении септического шока у детей: точка зрения ESPNIC. Энн Интенсивная терапия. 2019;9(1):73. doi: 10.1186/s13613-019-0545-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
64. Ventura AMC, Shieh HH, Bousso A, et al. Двойное слепое проспективное рандомизированное контролируемое исследование допамина по сравнению с адреналином в качестве вазоактивных препаратов первой линии при септическом шоке у детей. Крит Уход Мед. 2015;43(11):2292–2302. doi: 10.1097/CCM.0000000000001260. [PubMed] [CrossRef] [Google Scholar]
65. Мартин Г.С. Сепсис, тяжелый сепсис и септический шок: динамика заболеваемости, возбудители и исходы. Expert Rev Anti Infect Ther. 2012;10(6):701–706. doi: 10.1586/eri.12.50. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
66. Patregnani JT, Sochet AA, Klugman D. Кратковременные периферические вазоактивные инфузии в педиатрии. Pediatr Crit Care Med. 2017;18(8):e378–e381. doi: 10.1097/PCC.0000000000001230. [PubMed] [CrossRef] [Академия Google]
Pediatr Crit Care Med. 2017;18(8):e378–e381. doi: 10.1097/PCC.0000000000001230. [PubMed] [CrossRef] [Академия Google]
67. Briegel J, Forst H, Haller M, et al. Стрессовые дозы гидрокортизона обращают гипердинамический септический шок: проспективное, рандомизированное, двойное слепое, одноцентровое исследование. Крит Уход Мед. 1999;27(4):723–732. [PubMed] [Google Scholar]
68. Циммерман Дж. Дж. Кортикостероиды при септическом шоке у детей бесполезны. Крит Уход Мед. 2018;46(4):637–639. doi: 10.1097/CCM.0000000000002980. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
69. Alejandria MM, Lansang MAD, Dans LF, Mantaring JB. Внутривенный иммуноглобулин для лечения сепсиса, тяжелого сепсиса и септического шока. Cochrane Database Syst Rev. 2013; 2013(9)):CD001090. doi: 10.1002/14651858.CD001090.pub2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
70. Sandrock C, Albertson T. Противоречия в лечении сепсиса. Semin Respir Crit Care Med. 2010;31(1):66–78. doi: 10.1055/s-0029-1246290. [PubMed] [CrossRef] [Google Scholar]
2010;31(1):66–78. doi: 10.1055/s-0029-1246290. [PubMed] [CrossRef] [Google Scholar]
71. Bernard GR, Vincent J-L, Laterre PF, et al. Эффективность и безопасность рекомбинантного человеческого активированного протеина С при тяжелом сепсисе. N Engl J Med. 2001;344(10):699–709. doi: 10.1056/NEJM200103083441001. [PubMed] [CrossRef] [Академия Google]
72. Alharthy A, Faqihi F, Memish ZA, et al. Непрерывная заместительная почечная терапия с добавлением картриджа CytoSorb ® у пациентов в критическом состоянии с COVID-19 плюс острая почечная недостаточность: серия случаев. Артиф Органы. 2020 г.: 10.1111/aor.13864. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Wei T, Chen Z, Li P, et al. Раннее использование oXiris для поглощения эндотоксина при абдоминальном септическом шоке: клинический случай. Медицина (Балтимор) 2020;99(28):e19632. дои: 10.1097/MD.0000000000019632. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
74. Bottari G, Guzzo I, Marano M, et al. Гемоперфузия с цитосорбом у детей с септическим шоком: ретроспективное обсервационное исследование. Int J Artif Organs. 2020;43(9):587–593. doi: 10.1177/03913988209. [PubMed] [CrossRef] [Google Scholar]
Bottari G, Guzzo I, Marano M, et al. Гемоперфузия с цитосорбом у детей с септическим шоком: ретроспективное обсервационное исследование. Int J Artif Organs. 2020;43(9):587–593. doi: 10.1177/03913988209. [PubMed] [CrossRef] [Google Scholar]
75. Консенсусная конференция педиатрической группы по острой легочной травме. Педиатрический ОРДС: консенсусные рекомендации педиатрической консенсусной конференции по острому повреждению легких. Pediatr Crit Care Med. 2015;16(5):428–439. doi: 10.1097/PCC.0000000000000350. [Статья PMC бесплатно] [PubMed] [CrossRef] [Google Scholar]
76. Oberender F, Ganeshalingham A, Fortenberry JD, et al. Веноартериальная экстракорпоральная мембранная оксигенация по сравнению с традиционной терапией при тяжелом педиатрическом септическом шоке. Pediatr Crit Care Med. 2018;19(10):965–972. doi: 10.1097/PCC.0000000000001660. [PubMed] [CrossRef] [Google Scholar]
77. Бликли Г., Коул М. Распознавание и лечение сепсиса: роль медсестры. Бр Дж Нурс. 2020;29(21): 1248–1251. doi: 10.12968/bjon.2020.29.21.1248. [PubMed] [CrossRef] [Google Scholar]
2020;29(21): 1248–1251. doi: 10.12968/bjon.2020.29.21.1248. [PubMed] [CrossRef] [Google Scholar]
78. Сун Дж., Сони Н. Сепсис: распознавание и лечение. Clin Med J. 2012;12(3):276–280. doi: 10.7861/clinmedicine.12-3-276. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
79. Straney L, Clements A, Parslow RC, et al. Педиатрический индекс смертности 3. Pediatr Crit Care Med. 2013;14(7):673–681. doi: 10.1097/PCC.0b013e31829760cf. [PubMed] [CrossRef] [Google Scholar]
80. Olaechea PM, Quintana JM, Gallardo MS, Insausti J, Maraví E, Alvarez B. Прогностическая модель подхода к лечению внебольничной пневмонии у пациентов, нуждающихся в госпитализации в отделение интенсивной терапии. Интенсивная терапия Мед. 1996;22(12):1294–1300. doi: 10.1007/BF01709541. [PubMed] [CrossRef] [Google Scholar]
81. Джексон Дж. К., Хопкинс Р. О., Миллер Р. Р., Гордон С. М., Уиллер А. П., Эли Э. В. Острый респираторный дистресс-синдром, сепсис и снижение когнитивных функций: обзор и тематическое исследование. South Med J. 2009;102(11):1150–1157. doi: 10.1097/SMJ.0b013e3181b6a592. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
South Med J. 2009;102(11):1150–1157. doi: 10.1097/SMJ.0b013e3181b6a592. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
82. Chuang Y-Y, Huang Y-C, Lin T-Y. Синдром токсического шока у детей. Педиатр Наркотики. 2005;7(1):11–25. doi: 10.2165/00148581-200507010-00002. [PubMed] [CrossRef] [Академия Google]
83. Ames SG, Workman JK, Olson JA, et al. Инфекционная этиология и исходы при педиатрическом септическом шоке. J Pediatric Infect Dis Soc. 2017;1(6):80–86. doi: 10.1093/jpids/piv108. [PubMed] [CrossRef] [Google Scholar]
Сепсис – оценка и лечение
См. также
Антибиотики
Лихорадка у детей
Фебрильная нейтропения
Калькулятор лекарств и жидкостей для неотложной помощи
Инвазивные контакты Стрептококковые инфекции группы А: лечение бытовых0003
Ключевые моменты
- Сепсис определяется как опасная для жизни дисфункция органов, вызванная нерегулируемой реакцией хозяина на инфекцию
- Важно быстро диагностировать сепсис, но не допускать гипердиагностики.
 У большинства детей с лихорадкой (с очагом или без него) нет
У большинства детей с лихорадкой (с очагом или без него) нет
сепсис (см. раздел оценки ниже) - Септический шок — это сепсис с признаками дисфункции сердечно-сосудистых органов; гипотензия является поздним признаком
- Быстрый сосудистый доступ, раннее начало эмпирической антибиотикотерапии и тщательно подобранная инфузионная терапия жизненно необходимы
- Инотропы и вазопрессоры можно безопасно вводить через периферическую канюлю или внутрикостный доступ (ВК) у детей во время начальной реанимации
История вопроса
- основная причина заболеваемости и смертности у детей
- Помощь, оказанная в первый час после выявления сепсиса, имеет решающее значение
Группы высокого риска включают:
- новорожденных
- детей с ослабленным иммунитетом
- детей с центральным венозным доступом
- аборигенов и жителей островов Торресова пролива
<2 месяцев:
- Escherichia coli
- Группа B Streptococcus
- Listeria monocytogenes встречается редко
- HSV infection should be considered in differential diagnosis of sepsis
Major pathogens in older children:
- Neisseria meningitidis
- Streptococcus pneumoniae
- Staphylococcus aureus (MSSA or MRSA)
- Group A Streptococcus (GAS)
Оценка
Сепсис или септический шок следует подозревать у пациента с подозреваемой или подтвержденной бактериальной инфекцией и любой из следующих
- Изменение сознания (вялость, раздражительность, вялость, слабый крик)
- Нездоровый вид ± сыпь без побледнения кожа, длительное время наполнения центральных капилляров (CRT>2), тахикардия, снижение диуреза (<1 мл/кг/ч) или узкое пульсовое давление
- холодовой шок: узкое пульсовое давление, длительное наполнение капилляров (чаще у новорожденных/младенцев )
- теплый шок: широкое пульсовое давление, скачкообразный пульс, гиперемия кожи с быстрым наполнением капилляров (чаще встречается у детей старшего возраста/подростков и часто не распознается)
- Необъяснимая боль
- Лихорадка или гипотермия (температура может быть нормальной у новорожденных или лиц с ослабленным иммунитетом)
Токсин-опосредованный сепсис: вызван суперантигенами токсин-продуцирующих штаммов S. aureus или GAS
aureus или GAS
- Клинические признаки могут включать лихорадку, рвоту, диарею, миалгию, инъекцию конъюнктивы, спутанность сознания, коллапс и распространенную эритематозную сыпь
Настораживающие признаки
- в течение 48 часов
- Клиническое ухудшение, несмотря на лечение
- Недавно перенесенная операция или ожоги
Ведение
Основные принципы лечения тяжелого сепсиса или септического шока
- Early recognition/seeking senior help
- Assess airway and breathing and administer oxygen if required
- Rapid vascular access
- Empiric antibiotic therapy
- Carefully titrated fluid resuscitation
- Early назначение инотропов
- Раннее привлечение служб интенсивной терапии
- Контроль источника
- Частая переоценка
Подход к управлению
Рассмотрите возможность консультации с местной педиатрической бригадой
Любой ребенок с подозрением на сепсис
Рассмотрите возможность перевода в отделение интенсивной терапии, когда
- Признаки шока сохраняются, несмотря на введение 40 мл/кг жидкости
- Потребность в инотропных препаратах
- Стойкий лактат венозной сыворотки >3 ммоль/л
- Нейтропения (<1000/мм 3 ), не связанная с химиотерапией (большой околоушной белый выпот
- вне гемиторакса)
- Коагулопатия (МНО >1,6, АЧТВ >60, Фиб.

