Глпс у детей: Геморрагическая лихорадка с почечным синдромом
Геморрагическая лихорадка с почечным синдромом
Геморрагическая лихорадка с почечным синдромом — острая инфекционная природно-очаговая болезнь, которая вызывается вирусом, характеризуется поражением преимущественно мелких сосудов, лихорадкой , геморрагическим синдромом и проявлениями недостаточности почек.
Исторические данные гемморагической лихорадки
На Дальнем Востоке болезнь регистрируется с 1913 г. Вирусную природу ее доказал в 1940 г. А. С. Смородинцев, а в 1956 г. подтвердил М. П. Чумаков. От больного человека вирус впервые выделили в 1978 г. в Корее P. Lee и Н. Lee. Название «геморрагическая лихорадка с почечным синдромом» была предложена в 1954 p. М. П. Чумаковым и рекомендована в 1982 г. ВОЗ, чтобы ликвидировать многочисленные синонимы, которые болезнь имела в разных странах.
Эпидемиология геморрагической лихорадки
Источником инфекции являются грызуны (полевые и лесные мыши, лемминги и др. ). И некоторые насекомоядные животные. Грызуны выделяют вирус преимущественно с мочой, экскрементами, реже со слюной. Среди животных наблюдается трансмиссивная передача инфекции. В природных очагах заражение человека происходит преимущественно аэрогенным путем при вдыхании пыли, содержащей инфицированные экскременты грызунов, а также алиментарным (овощи) и контактным путем (при соприкосновении с больными грызунами, инфицированными предметами). Спорадические случаи заболевания развиваются в течение всего года, преимущественно среди сельских жителей. Групповые заболевания наблюдаются летом и осенью, что связано с миграцией грызунов в населенные пункты и более частым пребыванием людей в природных очагах. Болеют чаще мужчины (70-80% случаев). Хотя вирус выделяется с мочой, заражение ГЛПС от больного человека не описано.
). И некоторые насекомоядные животные. Грызуны выделяют вирус преимущественно с мочой, экскрементами, реже со слюной. Среди животных наблюдается трансмиссивная передача инфекции. В природных очагах заражение человека происходит преимущественно аэрогенным путем при вдыхании пыли, содержащей инфицированные экскременты грызунов, а также алиментарным (овощи) и контактным путем (при соприкосновении с больными грызунами, инфицированными предметами). Спорадические случаи заболевания развиваются в течение всего года, преимущественно среди сельских жителей. Групповые заболевания наблюдаются летом и осенью, что связано с миграцией грызунов в населенные пункты и более частым пребыванием людей в природных очагах. Болеют чаще мужчины (70-80% случаев). Хотя вирус выделяется с мочой, заражение ГЛПС от больного человека не описано.
Клиника геморрагической лихорадки
Инкубационный период длится от 8 до 45 дней, в среднем 20 дней. Болезнь характеризуется цикличностью.
В ее клиническом течении различают четыре стадии:
- начальную (1-4-й день болезни)
- олигурическую (с 3-4-го по 8-12-й день),
- полиурическую (с 9-13-го по 21-25-й день)
- реконвалесценции.

Начальная (лихорадочная) стадия
Болезнь начинается остро, температура тела повышается с ознобом до С-40 ° С и удерживается несколько дней. После ее снижения до нормы она снова может повышаться до субфебрильной. Больные жалуются на сильную головную боль, боль в мышцах, сухость во рту. Лицо и шея гиперемированы, сосуды склер и конъюнктивы инъецированы, слизистая оболочка зева ярко-красного цвета. На 3-4-й день болезни появляются признаки геморрагического синдрома — геморрагическая энантема на мягком небе, петехиальная сыпь в подмышечных областях, под и над ключицами, лопатками, на внутренних поверхностях плеч, иногда на шее, лице. Сыпь может располагаться в виде цепей, полос («удар бича»).
Олигурическая стадия
В олигурической стадии, несмотря на снижение температуры тела, состояние больного ухудшается, головная боль и геморрагические проявления усиливаются, возможны обширные кровоизлияния в кожу, склеры, носовые, легочные, желудочные, маточные кровотечения. Одновременно развивается почечный синдром. Возникает боль в области поясницы, симптом Пастернацкого положительный, количество мочи уменьшается до 200-400 мл в сутки, она может иметь розовый или красный оттенок, иногда приобретает цвет мясных помоев. Возможно развитие анурии. Вследствие нарушения выделительной функции почек прогрессирует азотемия, иногда развивается уремия, а в тяжелых случаях — кома. Патогномоничным является массивная протеинурия, которая достигает З0-90 г / л.
Одновременно развивается почечный синдром. Возникает боль в области поясницы, симптом Пастернацкого положительный, количество мочи уменьшается до 200-400 мл в сутки, она может иметь розовый или красный оттенок, иногда приобретает цвет мясных помоев. Возможно развитие анурии. Вследствие нарушения выделительной функции почек прогрессирует азотемия, иногда развивается уремия, а в тяжелых случаях — кома. Патогномоничным является массивная протеинурия, которая достигает З0-90 г / л.
Оказывается гипоизостенурия, гематурия, цилиндрурия. Отеки возникают редко.
Поражение нервной системы характеризуется заторможенностью, нередко менингеальные симптомы, анизорефлексия, иногда пирамидными знаками, инфекционным делирием. При спинномозговой пункции ликвор вытекает под повышенным давлением, количество белка повышена. Со стороны органов кровообращения — брадикардия, умеренная артериальная гипотензия, которая изменяется гипертензией. Язык сухой, живот умеренно вздут, болезненный в эпигастральной области.
При исследовании крови выявляется нейтрофильный лейкоцитоз до , плазмоцитоз до 5-25%, тромбоцитопения, значительно увеличенная СОЭ.
Полиурическая стадия
С 9-13-го дня болезни состояние больного улучшается, суточный диурез увеличивается до 5-8 л, появляется никтурия. Уменьшается боль в пояснице и животе, появляется аппетит, жажда, но еще долгое время остается слабость, умеренная боль в пояснице, сердцебиение, гипоизостенурия. Постепенно нормализуются биохимические показатели крови.
Стадия реконвалесценции может продолжаться до 3-6 месяцев, характеризуется медленной нормализацией функции почек, лабильностью функции органов кровообращения.
Осложнения геморрагической лихорадки
Возможны инфекционно-токсический шок, азотемическая кома и отек легких, недостаточность кровообращения, эклампсия, разрыв почек, кровоизлияния в мозг, надпочечники, миокард и другие органы, а также пневмония, флегмона, абсцесс.
Прогноз при легком и среднетяжелом течении болезни благоприятный. В тяжелых случаях летальность составляет 1 -10%.
В тяжелых случаях летальность составляет 1 -10%.
Специфическая диагностика геморрагической лихорадки
Вирус выделяют путем внутри-мозгового заражения кровью больного мышей поросят, идентифицируют в РН на мышах и культурах клеток. Для выявления антител против вируса ГЛПС применяют РНИФ, ИФА, РИА. Получения концентрированных и очищенных вирусных препаратов позволило использовать РТГА и РСК. Серологические исследования проводят в динамике болезни (метод парных сывороток).
Дифференциальный диагноз геморрагической лихорадки
ГЛПС следует дифференцировать с другими геморрагическими лихорадками, сыпным тифом, лептоспирозом, сепсисом, энцефалитом, капилляротоксикозом, острым гломерулонефритом, недостаточностью почек токсико-аллергической природы, иногда с хирургическими заболеваниями брюшной полости.
Профилактика геморрагической лихорадки
В эндемичных очагах обязательными являются мероприятия по уничтожению мышевидных грызунов, предотвращения инфицирования продуктов питания и воды, соблюдение санитарно-противоэпидемического режима жилья и окружающей территории
Всё о ГЛПС: опасна ли геморрагическая лихорадка с почечным синдромом?
Всё о ГЛПС: опасна ли геморрагическая лихорадка с почечным синдромом?
Геморрагическая лихорадка с почечным синдромом (ГЛПС) – тяжелое, смертельно опасное инфекционное заболевание с поражением мелких кровеносных сосудов, почек, легких и других органов человека. Заболевание широко распространяется благодаря высокой численности носителей вируса ГЛПС в природе – лесных грызунов, в особенности рыжей полевки. Вирус ГЛПС попадает во внешнюю среду с выделениями зараженных зверьков. Основной путь передачи инфекции – воздушно-пылевой (до 85 %), при котором пыль, содержащая высохшие выделения грызунов, а, следовательно, и вирус попадают в организм человека.
Заболевание широко распространяется благодаря высокой численности носителей вируса ГЛПС в природе – лесных грызунов, в особенности рыжей полевки. Вирус ГЛПС попадает во внешнюю среду с выделениями зараженных зверьков. Основной путь передачи инфекции – воздушно-пылевой (до 85 %), при котором пыль, содержащая высохшие выделения грызунов, а, следовательно, и вирус попадают в организм человека.
Реже встречается контактно-бытовой (курение и прием пищи грязными руками или непосредственный контакт со зверьками) и алиментарный (употребление в пищу продуктов питания, которые до этого грызли инфицированные животные, без их термической обработки). Заболевание от человека к человеку не передаётся.
У человека абсолютная восприимчивость к возбудителю. В большинстве случаев характерна осеннее-зимняя сезонность.
Если в летний и осенний период заражения происходят при посещении лесов, на садоводческих массивах, то зимой регистрируются случаи заражения в быту и на производстве. Связано это с заселением лесными грызунами, в частности рыжей полёвкой, жилых и производственных помещений. В период резких колебаний температуры воздуха, недостаточного снежного покрова грызуны мигрируют из леса в близлежащие постройки и при высокой их численности заселяют жилые помещения.
Связано это с заселением лесными грызунами, в частности рыжей полёвкой, жилых и производственных помещений. В период резких колебаний температуры воздуха, недостаточного снежного покрова грызуны мигрируют из леса в близлежащие постройки и при высокой их численности заселяют жилые помещения.
При первом после зимнего перерыва посещении садов и дач необходимо помнить, что длительно непосещаемые людьми постройки, как правило, заселяются грызунами. Первым делом нужно хорошо проветрить помещения, желательно, в отсутствии людей. Затем, обязательно защитив органы дыхания респиратором или ватно-марлевой повязкой и надев резиновые перчатки, провести тщательную влажную уборку с добавлением дезинфицирующих средств, при их отсутствии – тёплым мыльно-содовым раствором. Постельные принадлежности можно просушить на солнце в течение 3–5 часов.
Как развивается ГЛПС?
Входные ворота инфекции — слизистая дыхательных путей и пищеварительной системы, где либо гибнет (при хорошем местном иммунитете) либо начинает размножаться вирус (что соответствует инкубационному периоду). Затем вирус попадает в кровь (виремия), что проявляется инфекционно-токсическим синдромом у больного (чаще этот период соответствует 4-5 дням болезни). В последствие он оседает на внутренней стенке сосудов (эндотелии), нарушая ее функцию, что проявляется у пациента геморрагическим синдромом (проявляется в виде сыпи на теле, кровоизлияния в склеры) Выделяется вирус с мочой, поэтому поражаются и сосуды почек (воспаление и отек ткани почек), последующее развитие почечной недостаточности (затруднение выделения мочи). Именно тогда может наступить неблагоприятный исход. Этот период длится до 9 дня болезни. Затем происходит обратная динамика — рассасывание кровоизлияний, уменьшение почечного отека, восстановление мочеиспускания (до 30 дня заболевания).
Затем вирус попадает в кровь (виремия), что проявляется инфекционно-токсическим синдромом у больного (чаще этот период соответствует 4-5 дням болезни). В последствие он оседает на внутренней стенке сосудов (эндотелии), нарушая ее функцию, что проявляется у пациента геморрагическим синдромом (проявляется в виде сыпи на теле, кровоизлияния в склеры) Выделяется вирус с мочой, поэтому поражаются и сосуды почек (воспаление и отек ткани почек), последующее развитие почечной недостаточности (затруднение выделения мочи). Именно тогда может наступить неблагоприятный исход. Этот период длится до 9 дня болезни. Затем происходит обратная динамика — рассасывание кровоизлияний, уменьшение почечного отека, восстановление мочеиспускания (до 30 дня заболевания).
С момента заражения до появления первых признаков заболевания проходит 7–10 дней (максимально до 40 дней). Начало заболевания похоже на обычную острую респираторную инфекцию – повышается температура, появляются головная боль, боли в мышцах, общая слабость, потеря аппетита, иногда тошнота и рвота. У некоторых больных отмечаются катаральные явления (заложенность носа, сухой кашель, гиперемия зева), кратковременное ухудшение зрения (туман в глазах). На 45 день к перечисленным симптомам присоединяются боли в пояснице и животе, иногда на коже появляется сыпь. Нарушается функция почек, беспокоит жажда, сухость во рту, икота. Возникают кровотечения – почечные, желудочные, носовые и др.
У некоторых больных отмечаются катаральные явления (заложенность носа, сухой кашель, гиперемия зева), кратковременное ухудшение зрения (туман в глазах). На 45 день к перечисленным симптомам присоединяются боли в пояснице и животе, иногда на коже появляется сыпь. Нарушается функция почек, беспокоит жажда, сухость во рту, икота. Возникают кровотечения – почечные, желудочные, носовые и др.
При любых проявлениях заболевания необходимо как можно быстрее обратиться в поликлинику по месту жительства. Лечение проводится только в стационаре, самолечение опасно!
Для ГЛПС отсутствуют меры специфической профилактики, то есть не существует вакцины или специфического иммуноглобулина против этой болезни. Предупреждение заболеваний ГЛПС сводится к общесанитарным мероприятиям и борьбе с грызунами.
В целях профилактики:
– во время работы при большом количестве пыли (снос старых строений, погрузка сена, соломы, травы, разборка штабелей досок, брёвен, куч хвороста, уборка помещений и т. п.) необходимо использовать рукавицы и респиратор или ватно-марлевую повязку;
п.) необходимо использовать рукавицы и респиратор или ватно-марлевую повязку;
– уборка помещений должна проводиться только влажным способом;
– продукты должны быть недоступными для грызунов, храниться в металлической, плотно закрывающейся таре. Поврежденные грызунами пищевые продукты нельзя использовать в пищу без термической обработки;
– строго запрещается курить и принимать пищу немытыми руками;
– ни в коем случае нельзя прикасаться к живым или мертвым грызунам без рукавиц или резиновых перчаток.
Врач-инфекционист Трофимова Е.Н.
Безопасность и эффективность агонистов рецепторов глюкагоноподобного пептида-1 у детей и подростков с ожирением: метаанализ
Метаанализ
. 2021 сен;236:137-147.e13.
doi: 10.1016/j.jpeds.2021.05.009.
Epub 2021 11 мая.
Пол М Райан
1
, Шон Зельцер
2
, Натаниэль Э. Хейворд
Хейворд
3
, Давид Авелар Родригес
4
, Райан Т Слесс
5
, Колин П. Хоукс
6
Принадлежности
- 1 Департамент педиатрии и детского здоровья, Университетский колледж Корка, Корк, Ирландия. Электронный адрес: [email protected].
- 2 Институт медицинских исследований леди Дэвис, Монреаль, Квебек, Канада.
- 3 Кафедра педиатрии, Университет штата Юта, Солт-Лейк-Сити, Юта.
- 4 Кафедра педиатрии, Университет Торонто, Торонто, Онтарио, Канада.
- 5 Медицинский факультет Университета Торонто, Торонто, Онтарио, Канада.

- 6 Кафедра педиатрии и детского здоровья, Университетский колледж Корка, Корк, Ирландия; Отделение эндокринологии и диабета Детской больницы Филадельфии, Пенсильвания; Медицинская школа Перельмана, Пенсильванский университет, Пенсильвания.
PMID:
33984333
DOI:
10.1016/j.jpeds.2021.05.009
Бесплатная статья
Мета-анализ
Paul M Ryan et al.
J Педиатр.
2021 Сентябрь
Бесплатная статья
. 2021 сен;236:137-147. e13.
e13.
doi: 10.1016/j.jpeds.2021.05.009.
Epub 2021 11 мая.
Авторы
Пол М Райан
1
, Шон Зельцер
2
, Натаниэль Э. Хейворд
3
, Давид Авелар Родригес
4
, Райан Т Слесс
5
, Колин П. Хоукс
6
Принадлежности
- 1 Департамент педиатрии и детского здоровья, Университетский колледж Корка, Корк, Ирландия. Электронный адрес: [email protected].
- 2 Институт медицинских исследований леди Дэвис, Монреаль, Квебек, Канада.

- 3 Кафедра педиатрии, Университет штата Юта, Солт-Лейк-Сити, Юта.
- 4 Кафедра педиатрии, Университет Торонто, Торонто, Онтарио, Канада.
- 5 Медицинский факультет Университета Торонто, Торонто, Онтарио, Канада.
- 6 Кафедра педиатрии и детского здоровья, Университетский колледж Корка, Корк, Ирландия; Отделение эндокринологии и диабета Детской больницы Филадельфии, Пенсильвания; Медицинская школа Перельмана, Пенсильванский университет, Пенсильвания.
PMID:
33984333
DOI:
10.
 1016/j.jpeds.2021.05.009
1016/j.jpeds.2021.05.009
Абстрактный
Цели:
Определить вес, индекс массы тела (ИМТ), кардиометаболические и желудочно-кишечные эффекты агонистов рецептора глюкагоноподобного пептида-1 (ГПП-1) у детей с ожирением.
Дизайн исследования:
Базы данных Web of Science, PubMed/MEDLINE и Scopus от 01.01.1994-01/01/2021 для рандомизированных контролируемых исследований по изучению массы тела, ИМТ, кардиометаболических или желудочно-кишечных эффектов агонистов рецептора GLP-1 у детей и подростков с ожирением. Данные были извлечены двумя независимыми исследователями, и для метаанализа общих результатов обратной дисперсии была применена модель случайных эффектов. Первичные исходы были связаны с массой тела и кардиометаболическим профилем, а вторичные исходы, представляющие интерес, представляли собой нежелательные явления, связанные с желудочно-кишечным трактом и возникшие во время лечения.
Полученные результаты:
Было выявлено девять исследований с участием 574 человек, из которых 3 касались эксенатида и 6 — лираглутида. Использование агонистов рецептора GLP-1 вызвало умеренное снижение массы тела (средняя разница [MD] -1,50 [-2,50, -0,50] кг, I 2 64%), ИМТ (MD -1,24 [-1,71, -0,77]). кг/м 2 , I 2 0%), и показатель ИМТ z (MD -0,14 [-0,23, -0,06], I 2 43%). Гликемический контроль был улучшен у детей с доказанной резистентностью к инсулину (среднее значение гликированного гемоглобина A1c -1,05 [-1,93,-0,18] %, I 2 76%). Хотя улучшения липидного профиля отмечено не было, было обнаружено умеренное снижение систолического артериального давления (РС -2,30 [-4,11, -0,49] мм рт. ст.; I 2 0%). Наконец, анализ побочных эффектов со стороны желудочно-кишечного тракта, возникших после лечения, выявил повышенный риск тошноты (соотношение рисков 2,11 [1,44, 3,09]; I 2 0%), без значительного усиления других желудочно-кишечных симптомов.
Выводы:
Этот метаанализ показывает, что агонисты рецептора GLP-1 безопасны и эффективны для умеренного снижения веса, ИМТ, гликированного гемоглобина A1c и систолического артериального давления у детей и подростков с ожирением в клинических условиях, хотя и с повышенной частотой тошноты.
Идентификатор Просперо:
CRD42020195869.
Ключевые слова:
ГПП-1; инкретин; детское ожирение.
Copyright © 2021 Автор(ы). Опубликовано Elsevier Inc. Все права защищены.
Похожие статьи
Эффективность и безопасность агонистов рецептора глюкагоноподобного пептида-1 при диабете 2 типа: систематический обзор и сравнительный анализ смешанного лечения.

Htike ZZ, Zaccardi F, Papamargaritis D, Webb DR, Khunti K, Davies MJ.
Htike ZZ и др.
Сахарный диабет Ожирение Metab. 2017 апр;19(4): 524-536. дои: 10.1111/дом.12849. Epub 2017 17 февраля.
Сахарный диабет Ожирение Metab. 2017.PMID: 27981757
Обзор.
Влияние терапии агонистами рецепторов глюкагоноподобного пептида-1 на индекс массы тела у подростков с тяжелым ожирением: рандомизированное плацебо-контролируемое клиническое исследование.
Келли А.С., Рудсер К.Д., Натан Б.М., Фокс К.К., Метциг А.М., Кумбс Б.Дж., Фитч А.К., Бомберг Э.М., Абуззахаб М.Дж.
Келли А.С. и соавт.
JAMA Педиатр. 2013 г., апрель; 167(4):355-60. doi: 10.1001/jamapediatrics.2013.1045.
JAMA Педиатр. 2013.PMID: 23380890
Бесплатная статья ЧВК.Клиническое испытание.
Влияние агонистов рецептора глюкагоноподобного пептида-1 на гликемический контроль и антропометрические профили у пациентов с диабетом с неалкогольной жировой болезнью печени: систематический обзор и метаанализ рандомизированных контролируемых исследований.

Новрузи-Сохраби П., Резаи С., Джалали М., Ашурпур М., Ахмадипур А., Кешаварз П., Акбари Х.
Новрузи-Сохраби П. и соавт.
Евр Дж Фармакол. 2021 15 февраля; 893:173823. doi: 10.1016/j.ejphar.2020.173823. Epub 2020 19 декабря.
Евр Дж Фармакол. 2021.PMID: 33352183
Эффективность и безопасность агонистов рецепторов глюкагоноподобного пептида-1 длительного действия по сравнению с эксенатидом два раза в день и ситаглиптином при сахарном диабете 2 типа: систематический обзор и метаанализ.
Пинелли Н.Р., Хуррен К.М.
Пинелли Н.Р. и соавт.
Энн Фармакотер. 2011 июль; 45 (7-8): 850-60. doi: 10.1345/aph.1Q024. Epub 2011 5 июля.
Энн Фармакотер. 2011.PMID: 21730278
Обзор.
Агонисты рецепторов глюкагоноподобного пептида-1 по сравнению с инсулином гларгином при сахарном диабете 2 типа: систематический обзор и метаанализ рандомизированных контролируемых исследований.

Li WX, Gou JF, Tian JH, Yan X, Yang L.
Li WX и др.
Curr Ther Res Clin Exp. 2010 авг; 71 (4): 211-38. doi: 10.1016/j.curtheres.2010.08.003.
Curr Ther Res Clin Exp. 2010.PMID: 24688145
Бесплатная статья ЧВК.Обзор.
Посмотреть все похожие статьи
Цитируется
Влияние агонистов рецептора глюкагоноподобного пептида-1 на кардиометаболические факторы риска среди лиц с ожирением/избыточным весом, получающих антипсихотические препараты: обновленный систематический обзор и метаанализ рандомизированных контролируемых исследований.
Патулиас Д., Михайлидис Т., Димосиари А., Фрагакис Н., Це Г., Риццо М.
Патулиас Д. и соавт.
Биомедицины. 2023 22 февраля; 11 (3): 669. doi: 10.3390/biomedicines11030669.
Биомедицины. 2023.
PMID: 36979648
Бесплатная статья ЧВК.Обзор.
Возможное влияние длительного использования агонистов рецепторов глюкагоноподобного пептида-1 (GLP-1RA) на Hba1c и профиль липидов при сахарном диабете 2 типа: ретроспективное исследование в KAUH, Джидда, Саудовская Аравия.
Аджабнур Г.М.А., Хашим К.Т., Альзахрани М.М., Алсухейли А.З., Альхарби А.Ф., Альхозали А.М., Энани С., Эльдахны Б., Эльсамануди А.
Аджабнур ГМА и др.
Болезни. 2023 14 марта; 11(1):50. дои: 10.3390/болезни11010050.
Болезни. 2023.PMID: 36975599
Бесплатная статья ЧВК.
Типы публикаций
термины MeSH
вещества
FDA одобряет применение эксенатида один раз в неделю для детей с диабетом 2 типа
Регина Шаффер
Взгляд Кэролайн М. Аповян, доктора медицины
Аповян, доктора медицины
Источник/раскрытие информации
Опубликовано:
Источник:
пресс-релиз
Раскрытие информации:
Пангалос является исполнительным вице-президентом по исследованиям и разработкам AstraZeneca BioPharmaceuticals. Healio не смог определить соответствующие финансовые раскрытия для Tamborlane перед публикацией.
Регина Шаффер
Взгляд Кэролайн М. Аповян, доктора медицины
Источник/раскрытие информации
Опубликовано:
Источник:
пресс-релиз
Раскрытие информации:
Пангалос является исполнительным вице-президентом по исследованиям и разработкам AstraZeneca BioPharmaceuticals. Healio не смог определить соответствующие финансовые раскрытия для Tamborlane перед публикацией.
Healio не смог определить соответствующие финансовые раскрытия для Tamborlane перед публикацией.
Вы успешно добавили оповещения. Вы получите электронное письмо, когда будет опубликован новый контент.
Щелкните здесь, чтобы управлять оповещениями по электронной почте
Нам не удалось обработать ваш запрос. Пожалуйста, повторите попытку позже. Если у вас по-прежнему возникает эта проблема, свяжитесь с нами по адресу [email protected].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило агонист рецептора ГПП-1 эксенатид для детей в возрасте от 10 до 17 лет с диабетом 2 типа, первый инъекционный препарат для приема один раз в неделю, одобренный для педиатрического применения в Соединенных Штатах, согласно отраслевому пресс-релизу.
Утверждение эксенатида пролонгированного действия (Bydureon BCise, AstraZeneca) было получено после положительных данных фазы 3, представленных на научных сессиях Американской диабетической ассоциации и опубликованных Healio, продемонстрировавших, что подростки с диабетом 2 типа с большей вероятностью достигают целевых показателей HbA1c через 24 недели эксенатида один раз в неделю по сравнению с плацебо.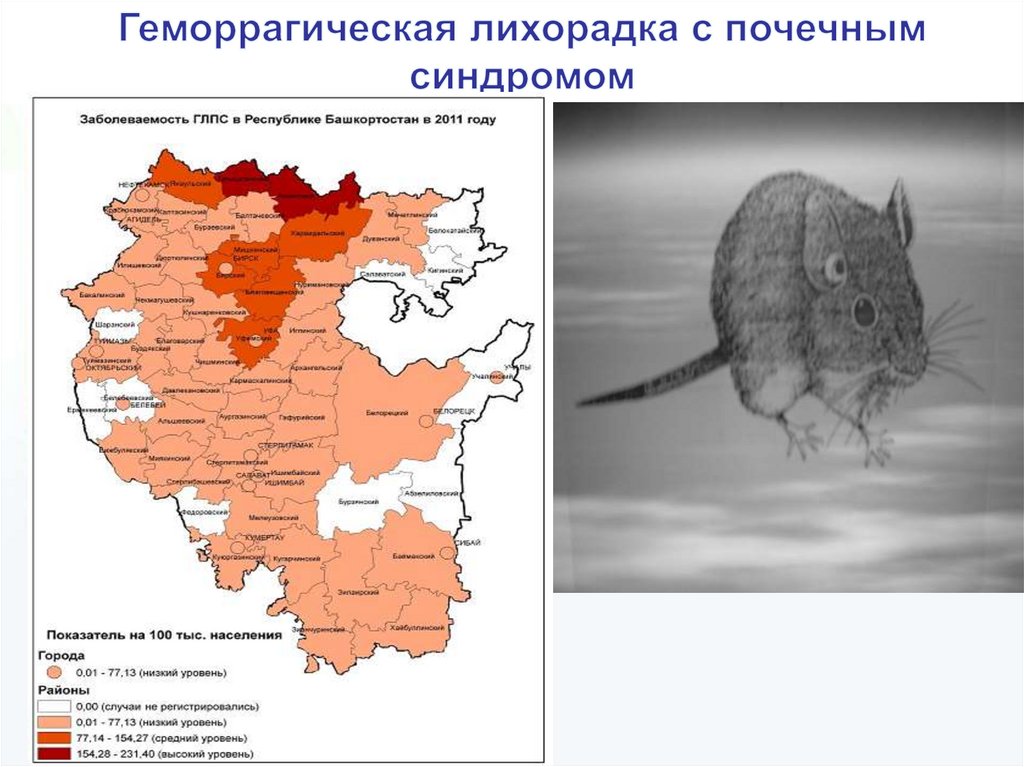 Исследователи также отметили тенденцию к снижению уровня глюкозы в плазме натощак и уменьшению массы тела.
Исследователи также отметили тенденцию к снижению уровня глюкозы в плазме натощак и уменьшению массы тела.
Источник: Adobe Stock
«Одобрение FDA США является важной вехой в лечении детей с диабетом 2 типа», Уильям Тамборлейн, доктор медицины, профессор и руководитель детской эндокринологии в Йельской школе медицины в Нью-Хейвене, Коннектикут, и международный исследователь-координатор эксенатида испытания, говорится в выпуске. «Bydureon BCise предлагает врачам, ухаживающим за детьми с этим хроническим заболеванием, новый важный терапевтический вариант, который может привести к серьезным долгосрочным проблемам, если его не лечить должным образом».
Для исследования фазы 3 83 подростка в возрасте не менее 10 лет с диабетом 2 типа, с инсулином или терапией сульфонилмочевиной или без них, были рандомизированы в соотношении 5:2 один раз в неделю по 2 мг эксенатида (n = 59) или плацебо (n = 59). 24) в течение 24 недель с последующей 28-недельной открытой фазой продления. Первичной конечной точкой эффективности было изменение по сравнению с исходным уровнем HbA1c на 24-й неделе; вторичными конечными точками эффективности были изменения уровня глюкозы натощак, массы тела и систолического артериального давления. Исследователи также оценили частоту нежелательных явлений.
Первичной конечной точкой эффективности было изменение по сравнению с исходным уровнем HbA1c на 24-й неделе; вторичными конечными точками эффективности были изменения уровня глюкозы натощак, массы тела и систолического артериального давления. Исследователи также оценили частоту нежелательных явлений.
Через 24 недели эксенатид один раз в неделю превосходил плацебо в снижении уровня HbA1c (среднее изменение по методу наименьших квадратов, 0,36% против 0,49% соответственно), с разницей между группами 0,85 процентных пункта ( P = ,012). ).
Исследователи также отметили недостоверные различия средних значений методом наименьших квадратов от исходного уровня до 24 недель в пользу эксенатида по уровню глюкозы натощак (21,6 мг/дл; 95% ДИ от 49 до 5,7), систолическому АД (2,8 мм рт. ст.; 95% ДИ от 8 до 2,4). и масса тела (1,22 кг; 95% ДИ от 3,59 до 1,15).
Во время исследования наблюдалась низкая частота гипогликемии, несмотря на использование инсулина, и хорошая переносимость со стороны желудочно-кишечного тракта, даже при отсутствии титрования эксенатида при назначении лечения. Это испытание было первым для применения агониста рецептора ГПП-1 один раз в неделю у детей с диабетом 2 типа.
Это испытание было первым для применения агониста рецептора ГПП-1 один раз в неделю у детей с диабетом 2 типа.
«Это решение является важной вехой в лечении этой более молодой группы пациентов, предоставляя удобный вариант лечения один раз в неделю», Mene Pangalos , исполнительный вице-президент по исследованиям и разработкам AstraZeneca BioPharmaceuticals, говорится в пресс-релизе. «Данные фазы 3, подтверждающие это одобрение, продемонстрировали, что безопасность и переносимость эксенатида пролонгированного действия у молодых пациентов аналогичны доказанному профилю безопасности этого препарата у взрослых».
Эксенатид с пролонгированным высвобождением был одобрен в США в октябре 2017 г. в качестве автоинъекционного устройства для однократного введения один раз в неделю для взрослых с диабетом 2 типа, у которых уровень глюкозы остается неконтролируемым при приеме одного или нескольких пероральных лекарств от диабета в дополнение к диете и физическим упражнениям.
