Гипоксия левого желудочка: Диагностика и лечение гипоксии миокарда
Признаки патологии сердца у новорожденных, перенесших гипоксию
В последнее время уделяется большое внимание изменениям со стороны сердечно — сосудистой системы у новорожденных, перенесших перинатальную гипоксию. Возникающие нарушения вызывают изменения в энергетическом обмене миокарда, приводя к быстрому снижению его сократительной функции. В генезе поражения важную роль играют дисэлектролитные изменения, гипогликемия и тканевой ацидоз, которые приводят к различным нарушениям: от незначительных гемодинамических расстройств до выраженных некротических повреждений, включая некрозы миокарда.
На базе Самаркандского областного детского многопрофильного медицинского центра было проведено комплексное обследование 58 новорожденных детей, перенесших гипоксию.
Авторы разделили пациентов на II группы:
· I — 30 новорожденных, родившихся в состоянии острой гипоксии;
· II — 28 новорожденных, родившихся на фоне хронической внутриутробной гипоксии плода.
Анализ соматического статуса матерей новорожденных пациентов показал, что женщины имели экстрагенитальную патологию различного характера и степени тяжести, при этом частота проявлений была выше во II группе. Особое значение приобретает наличие у беременной артериальной гипертензии, заболеваний почек, эндокринной системы и других заболеваний, в основе которых лежит эндотелиальная дисфункция. По мнению авторов, именно эти заболевания являются факторами риска развития кардиальной патологии при гипоксических состояниях у новорожденных
При клиническом анализе было выявлено, что у детей сравниваемых групп наблюдалось расширение границ сердца — в левую сторону у 6 новорожденных I группы и 13 II группы; влево и вправо у 2 и 5 пациентов в I и II группе соответственно. При определении верхушечного толчка было определено, что при пальпации сердца в 6 и 12 случаях I и II группы он был ослаблен или не определялся. У 2 новорожденных в I группы и 4 II группы отмечались повторные эпизоды брадикардии. При аускультации выслушивался систолический шум функционального характера у 4 детей с острой гипоксией, и шум органического характера у 1 ребенка с ДМПП, тогда как в группе с хронической внутриутробной гипоксией плода — у 6 детей наблюдался ДМПП и ДМЖП, у 5 отмечался функциональный систолический шум. ДМПП можно было расценить как персистирование фетальных коммуникаций, так как зачастую незакрытое овальное окном диагностируют как ДМПП.
При аускультации выслушивался систолический шум функционального характера у 4 детей с острой гипоксией, и шум органического характера у 1 ребенка с ДМПП, тогда как в группе с хронической внутриутробной гипоксией плода — у 6 детей наблюдался ДМПП и ДМЖП, у 5 отмечался функциональный систолический шум. ДМПП можно было расценить как персистирование фетальных коммуникаций, так как зачастую незакрытое овальное окном диагностируют как ДМПП.
Глухость сердечных тонов, как одно из проявлений позднего дезадаптационной кардиомиопатии наблюдался – у 10 детей I группы и 21 ребненка II группы. Тахикардия в покое — у 10 новорожденных I группы и 14 новорожденных II группы. Средняя частота сердечных сокращений у детей с в группах составила 162,2±3,5 ударов в мин в I группе и достоверно больше в 178,0±4,3 во второй группе. Увеличение частоты дыхания наблюдалось у 13 детей с острой гипоксией и 17 новорожденных родившихся на фоне хронической гипоксии, средняя частота дыхания в 1 минуту составила 67,0±2,7 в I и 73,5±3,17 во II группе соответственно.
При аускультации легких застойные хрипы в виде рассеянных мелкопузырчатых хрипов наблюдалась у 6 и 8 больных детей сравниваемых групп. Признаки недостаточности кровообращения в виде тахикардии и одышки, что соответствовало сердечной недостаточности различной степени тяжести по левожелудочковому типу наблюдалось в 8 случаев I группе и 14 во II группе.
При электрокардиографическом исследовании, авторами было выявлено, что среди нарушений ритма сердца и проводимости у обследованных новорожденных синусовая тахикардия регистрировались в 12 случаях в I группе и в 19 во II; синусовой аритмии – в 2 и 3 соответственно. На ЭКГ также были обнаружены снижение вольтажа комплекса QRS у 2 новорожденных I группы и 2 II группы. У подавляющего числа детей как I так и II группы отмечено нарушение процессов реполяризации. Наджелудочковая экстрасистолия была установлена у 2 детей I группы II группы соответственно. Удлинение интервала QT отмечено у 2 новорожденных I группы, укорочение интервала PQ, так же как и его удлинение — у 1 ребенка I группы и 3 детей II группы. Синдром WPW был обнаружен у одного ребенка II группы.
Синдром WPW был обнаружен у одного ребенка II группы.
На эхокардиографическом исследовании определили дилатация левого желудочка у 3 детей I группы и 7 детей II группы, тогда как дилатация левого и правого желудочка — 2 в I группе и 5 во II группе. У всех этих пациентов наблюдалась гипокинезия межжелудочковой перегородки и задней стенки левого желудочка, у 5 детей родившихся в состоянии хронической внутриутробной гипоксии выявлено снижение фракции выброса, увеличение конечно-систолического и конечно — диастолического размеров левого желудочка, тогда как во I группе данные признаки наблюдались всего в 1 случае.
Таким образом, авторами выявлены клинико-инструментальные и лабораторные критерии патологии сердца у новорожденных перенесших гипоксию, а также факторы риска кардиальной патологии: наличие в анамнезе у матерей заболевания почек, бронхиальная астма, хроническая патология сердечно — сосудистой системы и тяжелая анемия.
Источник: «Факторы риска, клинико-инструментальные и лабораторные признаки патологии сердца, перенесших гипоксию у новорожденных»
Лим В. И., Аллаёрова Х.А., Шавази М.Н., Муродова Д.А., Абдухалик-Заде Г.А.
И., Аллаёрова Х.А., Шавази М.Н., Муродова Д.А., Абдухалик-Заде Г.А.
https://scientifictext.ru/home/arkhiv-zhurnala-dostizheniya-nauki-i-obrazovaniya.html
Выпуск № 57 2020 год, стр. 98-103
Метки: научные исследования, неонатология
15.04.2020
РОЛЬ ИНДУЦИРУЕМОГО ГИПОКСИЕЙ ФАКТОРА-1 (HIF-1) В РЕАЛИЗАЦИИ ЦИТОПРОТЕКТИВНОГО ЭФФЕКТА ИШЕМИЧЕСКОГО И ФАРМАКОЛОГИЧЕСКОГО ПОСТКОНДИЦИОНИРОВАНИЯ | Щербак
1. Shlyakhto EV, Galagudza MM, Syrenskij AV, et al. Ischemic postconditioning infarction: a new way to protect the heart from reperfusion injury. Terapevticheskij arhiv. 2005; 77(5): 77–80. Russian (Шляхто Е. В., Галагудза М. М., Сыренский А. В.и др. Ишемическое посткондиционирование миокарда: новый способ защиты сердца от реперфузионного повреждения. Терапевтический архив. 2005; 77(5): 77-80).
2. Maslov LN, Mrochek AG, Hanush L, et al. The phenomenon of ischemic postconditioning of the heart. Rossijskij fiziologicheskij zhurnal im. I. M. Sechenova. 2012; 98(8): 943-61.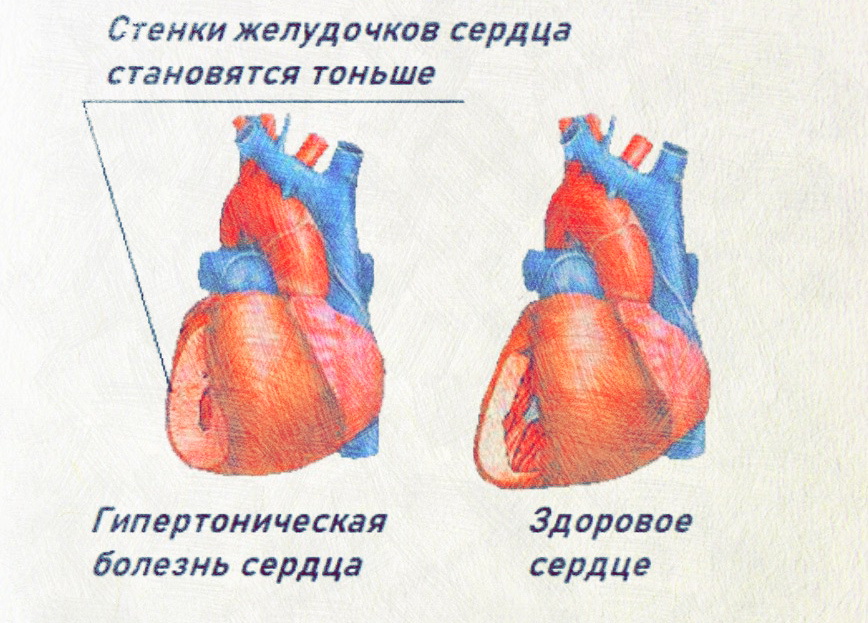 Russian (Маслов Л. Н., Мрочек А. Г., Хануш Л., и соавт. Феномен ишемического посткондиционирования сердца. Российский физиологический журнал им. И. М. Сеченова. 2012; 98(8): 943-61).
Russian (Маслов Л. Н., Мрочек А. Г., Хануш Л., и соавт. Феномен ишемического посткондиционирования сердца. Российский физиологический журнал им. И. М. Сеченова. 2012; 98(8): 943-61).
3. de Rougemont O, Lehmann K, Clavien PA. Preconditioning, organ preservation, and postconditioning to prevent ischemia-reperfusion injury to the liver. Liver Transpl. 2009; 15(10): 1172-82. doi: 10.1002/lt.21876.
4. Zhao ZQ, Corvera JS, Halkos ME, et al. Inhibition of myocardial injury by ischemic postconditioning during reperfusion: comparison with ischemic preconditioning. Am J Physiol Heart Circ Physiol. 2003; 285: 579-88.
5. Huang H, Zhang L, Wang Y, et al. Effect of ischemic post-conditioning on spinal cord ischemic-reperfusion injury in rabbits. Can J Anaesth. 2007; 54: 42-8.
6. Santos CHM, Gomes OM, Pontes JCDV, et al. The ischemic preconditioning and postconditioning effect on the intestinal mucosa of rats undergoing mesenteric ischemia/ reperfusion process. Acta Cir Bras. 2008; 23: 22-8.
7. Zhang WL, Zhao YL, Liu XM, et al. Protective role of mitochondrial K-ATP channel and mitochondrial membrane transport pore in rat kidney ischemic postconditioning. Chin Med J (Engl). 2011; 124(14): 2191-5.
8. Shcherbak N, Popovetsky M, Galagudza M, et al. The infarct-limiting effect of cerebral ischemic postconditioning in rats depends on the middle cerebral artery branching pattern. Int J Exp Pathol. 2013; 94(1): 34-8.
9. Wang GL, Jiang BH, Rue EA, et al. Hypoxia-inducible factor 1 is a basic-helix-loop-helix-PAS heterodimer regulated by cellular O2 tension. Proc Natl Acad Sci USA. 1995; 92(5): 510-4.
10. Loor G, Schumacker PT. Role of hypoxia-inducible factor in cell survival during myocardial ischemia-reperfusion. Cell Death Differ. 2008; 15(4): 686-90.
11. Correia SC, Carvalho C, Cardoso S, et al., Mitochondrial preconditioning: a potential neuroprotective strategy. Front Aging Neurosci. 2010; 26(2): 138.
12. Hollmann M, Hartley M, Heinemann S.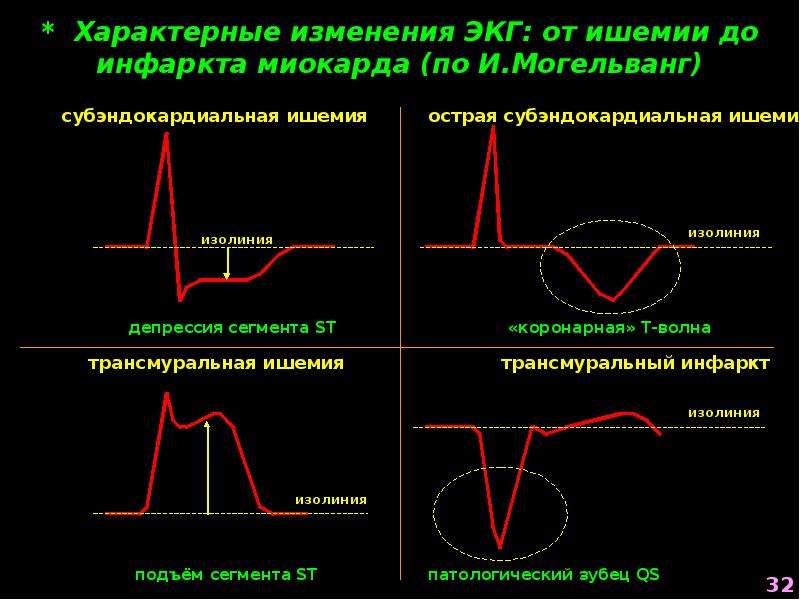 Ca2+ permeability of KA-AMPAgated glutamate receptor channels depends on subunit composition. Science. 1991; 252(5007): 851-3.
Ca2+ permeability of KA-AMPAgated glutamate receptor channels depends on subunit composition. Science. 1991; 252(5007): 851-3.
13. Iyer NV, Kotch LE, Agani F, et al. Cellular and developmental control of O2 of hypoxiainducible factor 1. Genes & Dev. 1998; 12: 149-62.
14. Masson N, Ratcliffe PJ. HIF prolyl and asparaginyl hydroxylases in the biological response to intracellular O(2) levels. J Cell Sci. 2003; 116(Pt 15): 3041-9.
15. Plamondon H, Blondeau N, Heurteaux C, et al. Mutually protective actions of kainic acid epileptic preconditioning and sublethal global ischemia on hippocampal neuronal death: involvement of adenosine A1 receptors and KATP channels. J Cereb Blood Flow Metab. 1999; 19: 1296-308.
16. Pugh CW, Ratcliffe PJ. Regulation of angiogenesis by hypoxia: role of the HIF system. Nat Med. 2003; 9(6): 677-84.
17. Tanaka H, Grooms SY, Bennett MV, et al. The AMPAR subunit GluR2: still front and centerstage. Brain Res. 2000; 886(1-2): 190-207.
18. Fang LQ, Xu H, Sun Y, et al. Induction of inducible nitric oxide synthase by isoflurane postconditioning via hypoxia inducible factor-1α during tolerance against ischemic neuronal injury. Brain Res. 2012; 1451: 1-9. doi: 10.1016/j.brainres.2012.02.055.
Fang LQ, Xu H, Sun Y, et al. Induction of inducible nitric oxide synthase by isoflurane postconditioning via hypoxia inducible factor-1α during tolerance against ischemic neuronal injury. Brain Res. 2012; 1451: 1-9. doi: 10.1016/j.brainres.2012.02.055.
19. Ye Z, Guo Q, Xia P, et al. Sevoflurane postconditioning involves an up-regulation of HIF-1α and HO-1 expression via PI3K/Akt pathway in a rat model of focal cerebral ischemia. Brain Res. 2012; 1463: 63-74. doi: 10.1016/j.brainres.2012.04.050.
20. Panahian N, Yoshiura M, Maines MD. Overexpression of heme oxygenase-1 is neuroprotective in a model of permanent middle cerebral artery occlusion in transgenic mice. J. Neurochem. 1999; 72: 1187-203.
21. Stocker R, Yamamoto Y, McDonagh AF, et al. Bilirubin is an antioxidant of possible physiological importance. Science. 1987; 235: 1043-6.
22. Volti GL, Sacerdoti D, Sangras B, et al. Carbonmonoxide signaling in promoting angiogenesis in human microvessel endothelial cells. Antioxid. Redox Signal. 2005; 7: 704-10.
Antioxid. Redox Signal. 2005; 7: 704-10.
23. Yang Y, Chen J, Li L, et al. Effect of different mild hypoxia manipulations on kainic acidinduced seizures in the hippocampus of rats. Neurochem Res. 2013; 38(1): 123-32. doi: 10.1007/s11064-012-0899-6.
24. Leconte C, Tixier E, Freret T, et al. Delayed hypoxic postconditioning protects against cerebral ischemia in the mouse. Stroke. 2009; 40(10): 3349-55.
25. Lee M, Ryu JK, Piao S, et al. Efficient gene expression system using the RTP801 promoter in the corpus cavernosum of high-cholesterol diet-induced erectile dysfunction rats for gene therapy. J Sex Med. 2008; 5: 1355-64.
26. Zhu XY, Rodriguez-Porcel M, Bentley MD, et al. Antioxidant intervention attenuates myocardial neovascularization in hypercholesterolemia. Circulation 2004; 109: 2109-15.
27. Zhao H, Wang Y, Wu Y, et al. Hyperlipidemia does not prevent the cardioprotection by postconditioning against myocardial ischemia/reperfusion injury and the involvement of hypoxia inducible factor-1alpha upregulation. Acta Biochim Biophys Sin (Shanghai). 20 09; 41(9): 745-53.
Acta Biochim Biophys Sin (Shanghai). 20 09; 41(9): 745-53.
28. Knudsen AR, Kannerup AS, Grønbæk H, et al. Effects of ischemic preand postconditioning on HIF-1α, VEGF and TGF-β expression after warm ischemia and reperfusion in the rat liver. Comp Hepatol. 2011; 10(1): 3. doi: 10.1186/1476-5926-10-3.
29. Song X, Zhang N, Xu H, et al. Combined preconditioning and postconditioning provides synergistic protection against liver ischemic reperfusion injury. Int J Biol Sci. 2012; 8(5): 707-18. doi: 10.7150/ijbs.4231.
30. Guo JY, Yang T, Sun XG, et al. Ischemic postconditioning attenuates liver warm ischemiareperfusion injury through Akt-eNOS-NO-HIF pathway. J Biomed Sci. 2011; 18: 79. doi: 10.1186/1423-0127-18-79.
31. Yingjia G, Tong Y, Jun L, et al. Rb1 postconditioning attenuates liver warm ischemia– reperfusion injury through ROS-NO-HIF pathway. Life Sciences. 2011; 88: 598-605.
32. Li F, Sonveaux P, Rabbani ZN, et al. Regulation of HIF-1alpha stability through S-nitrosylation. Mol Cell. 2007; 26: 63-74.
Mol Cell. 2007; 26: 63-74.
33. Mateo J, Garcia-Lecea M, Cadenas S, et al. Regulation of hypoxia-inducible factor-1 and independent pathways. Biochem J 2003; 376: 537-44.
34. Metzen E, Zhou J, Jelkmann W, et al. Nitric oxide impairs normoxic degradation of HIF- 1alpha by inhibition of prolyl hydroxylases. Mol Biol Cell. 2003; 14: 3470-81.
35. Lefer DJ. Induction of HIF-1alpha and iNOS with siRNA: a novel mechanism for myocardial protection. Circ Res. 2006; 98: 10-1.
36. Kasuno K, Takabuchi S, Fukuda K, et al. Nitric oxide induces hypoxia-inducible factor 1 activation that is dependent on MAPK and phosphatidylinositol 3-kinase signaling. J Biol Chem. 2004; 279: 2550-8.
37. Sandau KB, Faus HG, Brune B. Induction of hypoxia-inducible-factor 1 by nitric oxide is mediated via the PI 3 K pathway. Biochem Biophys Res Commun. 2000; 278: 263-7.
38. Wang T, Leng YF, Zhang Y, et al. Oxidative stress and hypoxia-induced factor 1α expression in gastric ischemia. World J Gastroenterol. 2011; 17(14): 1915-22.
2011; 17(14): 1915-22.
39. Liang H, Yu F, Tong Z, et al. Effect of ischemia post-conditioning on skeletal muscle oxidative injury, mTOR, Bax, Bcl-2 proteins expression, and HIF-1α/β-actin mRNA, IL-6/ β-actin mRNA and caveolin-3/β-actin mRNA expression in ischemia-reperfusion rabbits. Mol Biol Rep. 2013; 40(1): 507-14. doi: 10.1007/s11033-012-2087-9.
Влияние острой гипоксии на функцию левого желудочка при нагрузке
Сохранить цитату в файл
Формат:
Резюме (текст)PubMedPMIDAbstract (текст)CSV
Добавить в коллекции
- Создать новую коллекцию
- Добавить в существующую коллекцию
Назовите свою коллекцию:
Имя должно содержать менее 100 символов
Выберите коллекцию:
Не удалось загрузить вашу коллекцию из-за ошибки
Повторите попытку
Добавить в мою библиографию
- Моя библиография
Не удалось загрузить делегатов из-за ошибки
Повторите попытку
Ваш сохраненный поиск
Название сохраненного поиска:
Условия поиска:
Тестовые условия поиска
Электронная почта:
(изменить)
Который день?
Первое воскресеньеПервый понедельникПервый вторникПервая средаПервый четвергПервая пятницаПервая субботаПервый деньПервый рабочий день
Который день?
ВоскресеньеПонедельникВторникСредаЧетвергПятницаСуббота
Формат отчета:
РезюмеРезюме (текст)АбстрактАбстракт (текст)PubMed
Отправить не более:
1 шт. 5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
5 шт. 10 шт. 20 шт. 50 шт. 100 шт. 200 шт.
Отправить, даже если нет новых результатов
Необязательный текст в электронном письме:
Создайте файл для внешнего программного обеспечения для управления цитированием
Полнотекстовые ссылки
Спрингер
Полнотекстовые ссылки
Сравнительное исследование
. 2007 г., июнь; 100 (3): 261-5.
doi: 10.1007/s00421-007-0427-6.
Epub 2007 24 февраля.
Бин Ян
1
, Ян Ху, Хуншу Цзи, Дапэн Бао
принадлежность
- 1 Колледж спортивных наук Пекинского спортивного университета, Пекин 100084, Китай.

PMID:
17323069
DOI:
10.1007/s00421-007-0427-6
Сравнительное исследование
Бинг Ян и др.
Eur J Appl Physiol.
2007 июнь
. 2007 г., июнь; 100 (3): 261-5.
doi: 10.1007/s00421-007-0427-6.
Epub 2007 24 февраля.
Авторы
Бин Ян
1
, Ян Ху, Хуншу Цзи, Дапэн Бао
принадлежность
- 1 Колледж спортивных наук Пекинского спортивного университета, Пекин 100084, Китай.

PMID:
17323069
DOI:
10.1007/s00421-007-0427-6
Абстрактный
Влияние острой гипоксии на функцию левого желудочка человека при физической нагрузке оценивали с помощью двухмерной и доплеровской эхокардиографии на 11 здоровых студентах мужского пола. Каждый испытуемый выполнял 6-минутные упражнения на велосипеде средней интенсивности (100 Вт) в положении лежа на спине в условиях нормоксии и гипоксии соответственно. Концентрацию вдыхаемого O(2) регулировали так, чтобы поддерживать концентрацию артериального гемоглобина O(2) (SpO(2)) на уровне 88–9.2% при гипоксии. Полученные допплеровские показатели сравнивали между нормоксией и гипоксией. Диастолическая функция миокарда левого желудочка была увеличена при физической нагрузке в условиях гипоксии по сравнению с нормоксией. Пиковая скорость волны раннего наполнения увеличивалась в покое (P < 0,05) и при нагрузке (P < 0,05 на второй минуте и P < 0,01 на шестой минуте) в условиях гипоксии. Частота сердечных сокращений (P < 0,01) и сердечный выброс (P < 0,001) были заметно повышены в покое во время гипоксии. Показатели систолической функции левого желудочка, такие как ударный объем, фракция выброса и конечный систолический объем, были относительно неизменны при гипоксии по сравнению с нормоксией. Результаты показывают, что острая гипоксия увеличивает диастолическую функцию миокарда левого желудочка во время упражнений на велосипеде умеренной интенсивности, не влияя на систолическую функцию.
Пиковая скорость волны раннего наполнения увеличивалась в покое (P < 0,05) и при нагрузке (P < 0,05 на второй минуте и P < 0,01 на шестой минуте) в условиях гипоксии. Частота сердечных сокращений (P < 0,01) и сердечный выброс (P < 0,001) были заметно повышены в покое во время гипоксии. Показатели систолической функции левого желудочка, такие как ударный объем, фракция выброса и конечный систолический объем, были относительно неизменны при гипоксии по сравнению с нормоксией. Результаты показывают, что острая гипоксия увеличивает диастолическую функцию миокарда левого желудочка во время упражнений на велосипеде умеренной интенсивности, не влияя на систолическую функцию.
Похожие статьи
Экспериментальная острая гипоксия у здоровых лиц: оценка систолической и диастолической функции левого желудочка в покое и при нагрузке с помощью эхокардиографии.
Кульмер Т., Кнайсль Г., Катова Т.
 , Кроненбергер Х., Урхаузен А., Киндерманн В., Мерц В., Мейер-Сюдов Й.
, Кроненбергер Х., Урхаузен А., Киндерманн В., Мерц В., Мейер-Сюдов Й.Кульмер Т. и соавт.
Eur J Appl Physiol Occup Physiol. 1995;70(2):169-74. дои: 10.1007/BF00361545.
Eur J Appl Physiol Occup Physiol. 1995.PMID: 7768240
Клиническое испытание.
Улучшение работы левого желудочка у пожилых мужчин, тренирующихся на выносливость.
Seals DR, Hagberg JM, Spina RJ, Rogers MA, Schechtman KB, Ehsani AA.
Силс Д.Р. и др.
Тираж. 1994 г., январь; 89 (1): 198–205. doi: 10.1161/01.cir.89.1.198.
Тираж. 1994.PMID: 8281647
Исследование DEFIANT функции левого желудочка и работоспособности после острого инфаркта миокарда. Доплеровский поток и эхокардиология при функциональной сердечной недостаточности: оценка исследовательской группы по терапии низолдипином.

Льюис, Б.С., Пул-Уилсон, Пенсильвания.
Льюис Б.С. и соавт.
Сердечно-сосудистые препараты Ther. 1994 г., май; 8 Приложение 2: 407-18. дои: 10.1007/BF00877325.
Сердечно-сосудистые препараты Ther. 1994.PMID: 7947383
Клиническое испытание.
Оценка размеров и функций левого желудочка у спортсменов и лиц, ведущих малоподвижный образ жизни, в покое и при физической нагрузке с помощью эхокардиографии, допплерографии и радионуклидной вентрикулографии.
Хуонкер М., Кениг Д., Кеул Дж.
Хуонкер М. и соавт.
Int J Sports Med. 17 ноября 1996 г. Приложение 3: S173-9. doi: 10.1055/s-2007-972920.
Int J Sports Med. 1996.PMID: 9119539
Обзор.
Клинические аспекты диастолической функции левого желудочка, оцененные с помощью допплерэхокардиографии после острого инфаркта миокарда.

Поульсен С.Х.
Поульсен Ш.
Дэн Мед Булл. 2001 ноябрь; 48(4):199-210.
Дэн Мед Булл. 2001.PMID: 11767125
Обзор.
Посмотреть все похожие статьи
Цитируется
Влияние острой умеренной гипоксии по сравнению с нормоксией на метаболическую и сердечную функцию и оксигенацию скелетных мышц во время упражнений на выносливость при одинаковом уровне частоты сердечных сокращений.
Park HY, Jung WS, Kim SW, Seo J, Sun Y, Choi JH, Kim J, Lim K.
Парк Х.И. и др.
Метаболиты. 2022 15 октября; 12 (10): 975. дои: 10.3390/метабо12100975.
Метаболиты. 2022.PMID: 36295877
Бесплатная статья ЧВК.Острая физическая нагрузка с умеренной гипоксией снижает сатурацию артериального кислорода и церебральную оксигенацию, не влияя на гемодинамику у физически активных мужчин.

Муллири Г., Маньяни С., Роберто С., Гиани Г., Сечи Ф., Фанни М., Марини Э., Стаги С., Лай Ю., Ринальди А., Изола Р., Варгиу Р., Спрангер М.Д., Крисафулли А.
Муллири Г. и др.
Общественное здравоохранение Int J Environ Res. 2022 10 апр; 19(8):4558. дои: 10.3390/ijerph29084558.
Общественное здравоохранение Int J Environ Res. 2022.PMID: 35457425
Бесплатная статья ЧВК.Систолическая и диастолическая функции после кратковременного острого приступа легкой физической нагрузки при нормобарической гипоксии.
Маньяни С., Муллири Г., Роберто С., Сечи Ф., Гиани Г., Сайнас Г., Нухеду Г., Варгиу Р., Бассарео П.П., Крисафулли А.
Маньяни С. и др.
Фронт Физиол. 2021 23 апр;12:650696. doi: 10.3389/fphys.2021.650696. Электронная коллекция 2021.
Фронт Физиол. 2021.PMID: 33967823
Бесплатная статья ЧВК.Влияние агонистов и антагонистов адренорецепторов на сердечно-легочную функцию при нормобарической гипоксии у крыс.

Белтер С., Габриэль П., Аппельт П., Саламе А., Ширле К., Расслер Б.
Белтер С. и др.
Фронт Физиол. 2019 5 июля; 10:860. doi: 10.3389/fphys.2019.00860. Электронная коллекция 2019.
Фронт Физиол. 2019.PMID: 31333500
Бесплатная статья ЧВК.Влияние различных острых гипоксических состояний на метаболические параметры и функцию сердца при физической нагрузке и восстановлении.
Moon HW, Sunoo S, Park HY, Lee DJ, Nam SS.
Мун Х.В. и др.
Спрингерплюс. 2016 8 августа; 5 (1): 1294. doi: 10.1186/s40064-016-2952-4. Электронная коллекция 2016.
Спрингерплюс. 2016.PMID: 27547668
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Рекомендации
Медицинские спортивные упражнения.
 2003 сен; 35 (9): 1471-6
2003 сен; 35 (9): 1471-6—
пабмед
Медицинские спортивные упражнения. 1994 сент; 26 (9): 1116-21
—
пабмед
Медицинские спортивные упражнения. 2005 Январь; 37 (1): 138-46
—
пабмед
J Sci Med Sport.
 2006 май; 9 (1-2): 177-80
2006 май; 9 (1-2): 177-80—
пабмед
High Alt Med Biol. Лето 2002 г .; 3 (2): 177–93.
—
пабмед
Типы публикаций
термины MeSH
вещества
Полнотекстовые ссылки
Спрингер
Укажите
Формат:
ААД
АПА
МДА
НЛМ
Отправить по телефону
Изменения функции левого желудочка и скорости коронарного кровотока при изокапнической гипоксии: магнитно-резонансная томография сердца | Журнал кардиоваскулярного магнитного резонанса
Изменения функции левого желудочка и скорости коронарного кровотока при изокапнической гипоксии: магнитно-резонансная томография сердца
Скачать PDF
Скачать ePub
Скачать PDF
Скачать ePub
Том 18, Приложение 1
- Постерная презентация
- Открытый доступ
- Опубликовано:
- Глен Э Фостер 1 ,
- Цзысин Дэн 2 ,
- Линдси М Буле 1 ,
- Пуджа К Мехта 3 ,
- Джанет Вэй 3 ,
- Чжаоян Фан 2 ,
- C Ноэль 1 ,
- Бэйри Мерц 3 ,
- Дебиао Ли 2 и
- …
- Майкл Д Нельсон 2,3
9 0009 Рохан Дхармакумар 2 ,
Журнал кардиоваскулярного магнитного резонанса
том 18 , Номер статьи: P126 (2016)
Процитировать эту статью
758 доступов
Сведения о показателях
История вопроса
Кардиологическое стресс-тестирование является стандартом диагностики ишемической болезни сердца. Традиционное нагрузочное тестирование включает физическую или фармакологическую нагрузку, чтобы вызвать гиперемию и/или увеличить потребность миокарда в кислороде. Однако физический стресс невозможен в 100% случаев, а фармакологический стресс сопряжен с редким, но серьезным риском. Мы спросили, можно ли использовать острую изокапническую гипоксию в качестве альтернативного сердечно-сосудистого стресс-теста.
Традиционное нагрузочное тестирование включает физическую или фармакологическую нагрузку, чтобы вызвать гиперемию и/или увеличить потребность миокарда в кислороде. Однако физический стресс невозможен в 100% случаев, а фармакологический стресс сопряжен с редким, но серьезным риском. Мы спросили, можно ли использовать острую изокапническую гипоксию в качестве альтернативного сердечно-сосудистого стресс-теста.
Методы
Восемь здоровых мужчин-добровольцев (31 + 4 года) подверглись воздействию изокапнической гипоксии с использованием динамической системы искусственного дыхания в конце выдоха. Функцию левого желудочка и скорость кровотока в коронарных артериях измеряли с помощью МРТ (3Т, Siemens). Парциальное давление кислорода в конце выдоха поддерживали на уровне 43 ± 0,3 мм рт. ст., а парциальное давление углекислого газа в конце выдоха контролировали на исходном уровне. Фракция выброса левого желудочка оценивалась с использованием кинопоследовательности при свободном дыхании (TE/TR = 1,08/46,74 мс; пространственное разрешение в плоскости = 2,5 × 2,5 мм 9 ). 0069 2 ; толщина среза = 8 мм). Скорость коронарного кровотока измеряли в левой передней нисходящей (LAD), левой огибающей (LCX) и левой основной (LM) коронарных артериях с использованием свободной последовательности декартовой двухмерной фазово-контрастной (ПК) МРТ с навигатором. (временное разрешение = 26,4 мс; пространственное разрешение в плоскости = 0,88 × 0,88 мм 2 ; толщина среза = 7 мм; VENC = 40-80 см/с в направлении z). Площадь поперечного сечения коронарных артерий была оценена у 3 из 8 пациентов (все в левой передней нисходящей коронарной артерии, LAD) с использованием 2D сбалансированной стационарной последовательности свободной прецессии (запускаемая ЭКГ и стробируемая навигатором; сбор данных только в фазе покоя; плоскостное пространственное разрешение = 0,85 × 0,85 мм 2 ; толщина среза = 7 мм).
0069 2 ; толщина среза = 8 мм). Скорость коронарного кровотока измеряли в левой передней нисходящей (LAD), левой огибающей (LCX) и левой основной (LM) коронарных артериях с использованием свободной последовательности декартовой двухмерной фазово-контрастной (ПК) МРТ с навигатором. (временное разрешение = 26,4 мс; пространственное разрешение в плоскости = 0,88 × 0,88 мм 2 ; толщина среза = 7 мм; VENC = 40-80 см/с в направлении z). Площадь поперечного сечения коронарных артерий была оценена у 3 из 8 пациентов (все в левой передней нисходящей коронарной артерии, LAD) с использованием 2D сбалансированной стационарной последовательности свободной прецессии (запускаемая ЭКГ и стробируемая навигатором; сбор данных только в фазе покоя; плоскостное пространственное разрешение = 0,85 × 0,85 мм 2 ; толщина среза = 7 мм).
Результаты
Во время гипоксии сатурация артериального оксигемоглобина снижалась до 79 ± 1%, а частота сердечных сокращений и систолическое давление увеличивались на 47% и 4% соответственно (все Р < 0,05). Гипоксия увеличивала фракцию выброса левого желудочка с 66 + 1 до 74 + 1% (p < 0,01) и произведение скорости давления с 7057 + 639 до 10340 + 801 мм рт. ст./уд/мин (P < 0,01). Средняя скорость коронарного кровотока значительно увеличилась у семи из восьми субъектов (5 LAD, увеличение с 17,9+ 2,1 до 25,6 + 1,2 см/с; 1 LCX, увеличение с 20,1 до 38,8 см/с; и 1 лм, увеличиваясь с 18,6 до 40,0 см/с). Плохое качество изображения не позволило провести анализ скорости коронарного кровотока у 1 субъекта. Изменение скорости коронарного кровотока было пропорционально изменению потребности миокарда в кислороде (P = 0,26). Площадь поперечного сечения коронарных артерий была измерена у трех субъектов и оказалась неизменной (22,3 + 4,5 против 22,4 + 5,3 мм 2 , p = ns, исходный уровень по сравнению с гипоксией, соответственно).
Гипоксия увеличивала фракцию выброса левого желудочка с 66 + 1 до 74 + 1% (p < 0,01) и произведение скорости давления с 7057 + 639 до 10340 + 801 мм рт. ст./уд/мин (P < 0,01). Средняя скорость коронарного кровотока значительно увеличилась у семи из восьми субъектов (5 LAD, увеличение с 17,9+ 2,1 до 25,6 + 1,2 см/с; 1 LCX, увеличение с 20,1 до 38,8 см/с; и 1 лм, увеличиваясь с 18,6 до 40,0 см/с). Плохое качество изображения не позволило провести анализ скорости коронарного кровотока у 1 субъекта. Изменение скорости коронарного кровотока было пропорционально изменению потребности миокарда в кислороде (P = 0,26). Площадь поперечного сечения коронарных артерий была измерена у трех субъектов и оказалась неизменной (22,3 + 4,5 против 22,4 + 5,3 мм 2 , p = ns, исходный уровень по сравнению с гипоксией, соответственно).
Выводы
Это первое исследование МРТ для одновременной оценки функции сердца и коронарного кровотока в ответ на острую изокапническую гипоксию с использованием динамического форсирования в конце выдоха. Результаты подтверждают использование гипоксии в качестве уникального сердечно-сосудистого стресс-теста. Необходимы дальнейшие исследования для определения целесообразности и эффективности его использования у целевых групп пациентов.
Результаты подтверждают использование гипоксии в качестве уникального сердечно-сосудистого стресс-теста. Необходимы дальнейшие исследования для определения целесообразности и эффективности его использования у целевых групп пациентов.
Информация об авторе
Авторы и организации
Центр здоровья сердца, легких и сосудов, Университет Британской Колумбии, Келоуна, Британская Колумбия, Канада
Glen E Foster, Lindsey M Boulet и C Noel
Научно-исследовательский институт биомедицинской визуализации, Медицинский центр Cedars-Sinai, Лос-Анджелес, Калифорния, США
Zixin Deng, Zhaoyang Fan, Rohan Dharmakumar, Debiao Li & Майкл Д Нельсон
Институт сердца, Медицинский центр Cedars-Sinai, Лос-Анджелес, Калифорния, США
Puja K Mehta, Janet Wei, Bairey Merz & Michael D Nelson
Авторы
9019 8
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Академия
Посмотреть публикации автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar
Просмотр публикаций автора
Вы также можете искать этого автора в
PubMed Google Scholar

