Энцефалопатия у новорожденных что это такое: Энцефалопатия новорожденных: что это такое, причины, симптомы и способы лечения
Психологический центр
В «Академии здоровья» ведет прием Наталья Малова, детский психоневролог, кандидат медицинских наук, врач высшей категории, специалист с 25- летним стажем, ведущий сотрудник неврологического отделения областной детской больницы.
Психоневролог: что это за врач, и какие проблемы он решает?
Мы смотрим умственное и двигательное развитие ребенка, мышечный тонус на соответствие возрастным нормам. Это и задержки речевого развития, заикание, невнятная речь, энурез (ночное недержание мочи), различные судорожные и бессудоржные состояния, нарушения психологического развития. В возрасте до года – перинатальная энцефалопатия. Если такой диагноз поставлен, такие дети впоследствии, как правило, имеют проблемы. Поэтому вместе с родителями мы наблюдаем, смотрим, как развивается малыш и помогаем.
Когда мама должна затревожиться? и понять, что ее чаду необходима помощь психоневролога?
— Настораживающих симптомов много, начиная с самого рождения: беспокойное поведение, частое срыгивание, плохой сон. Самое главное – то, что мама замечает отставание в развитии ребенка по срокам от сверстников: позже начинает держать голову, переворачиваться, сидеть, стоять и говорить. Если у вашего ребенка есть такие симптомы, то необходима наша помощь. В более старшем возрасте – это задержка речи. Когда ребенок позже начинает говорить или плохо говорит, когда не понимает упрощенную речь.Это и нарушение сна, и возникновение непроизвольных движений – тиков: а именно-учащенное моргание, подергивание мышц плечевого пояса.Все эти признаки свидетельствуют о патологии нервной системы.
Самое главное – то, что мама замечает отставание в развитии ребенка по срокам от сверстников: позже начинает держать голову, переворачиваться, сидеть, стоять и говорить. Если у вашего ребенка есть такие симптомы, то необходима наша помощь. В более старшем возрасте – это задержка речи. Когда ребенок позже начинает говорить или плохо говорит, когда не понимает упрощенную речь.Это и нарушение сна, и возникновение непроизвольных движений – тиков: а именно-учащенное моргание, подергивание мышц плечевого пояса.Все эти признаки свидетельствуют о патологии нервной системы.
Но речь – это традиционно логопед?
Речь – одна из сторон психической деятельности человека. Если наблюдается ее задержка, значит, есть патология с этой стороны. Поэтому мы и называемся психоневрологи. Как правило, задержка речи никогда не бывает изолированной, у ребенка страдают и другие функции.
Что такое перинатальная энцефалопатия?
— Данный диагноз выставляется в том случае, если были факторы, которые неблагоприятно воздействовали на нервную систему. Это два последних месяца внутриутробного развития и первый месяц после рождения. Сюда входят как травматические повреждения, например, родовые травмы, так и патологические состояния, которые были у матери во время беременности, оказавшие роль на формирование плода и на дальнейшее его развитие. Неблагоприятные факторы – это токсикозы беременных, анемия, хроническая внутриутробная гипоксия плода. Все это в свою очередь вызывает поражения в той или мере нервной системы и вызывает множество синдромов: гидроцефальный (водянка головного мозга), гипертензионный, синдром мышечной дистонии.
Это два последних месяца внутриутробного развития и первый месяц после рождения. Сюда входят как травматические повреждения, например, родовые травмы, так и патологические состояния, которые были у матери во время беременности, оказавшие роль на формирование плода и на дальнейшее его развитие. Неблагоприятные факторы – это токсикозы беременных, анемия, хроническая внутриутробная гипоксия плода. Все это в свою очередь вызывает поражения в той или мере нервной системы и вызывает множество синдромов: гидроцефальный (водянка головного мозга), гипертензионный, синдром мышечной дистонии.
Чем это обусловлено?
— Гипоксией, в ответ на которую реакция организма однотипна. Желудочки головного мозга начинают продуцировать излишнее количество жидкости, что в свою очередь, повышает внутричерепное давление. Появляется синдром повышенного внутричерепного давления (гипертензионный) и гидроцефальный синдром – излишнее накопление жидкости в полостях головного мозга. Вследствие гипоксического повреждения коры головного мозга у детей проявляется пирамидная недостаточность: повышение мышечного тонуса, сухожильных рефлексов и задержка двигательного развития. Такие дети внешне скованы, они позднее начинают сидеть, стоять, ходить. Ходят они неловко, неуклюже, часто с опорой на передний свод стопы (на носочках). Вовремя начатое лечение обычно компенсирует эти проблемы.
Вследствие гипоксического повреждения коры головного мозга у детей проявляется пирамидная недостаточность: повышение мышечного тонуса, сухожильных рефлексов и задержка двигательного развития. Такие дети внешне скованы, они позднее начинают сидеть, стоять, ходить. Ходят они неловко, неуклюже, часто с опорой на передний свод стопы (на носочках). Вовремя начатое лечение обычно компенсирует эти проблемы.
Какое лечение?
— Как правило, самое простое, но его необходимо вовремя назначить: массаж, гимнастика, иногда медикаментозная терапия. И тогда к году, как и положено, ребенок пойдет, потом заговорит и т.д. А если не лечить, такие дети попадают в группу риска. По мере их роста и взросления могут возникать всевозможные проблемы. Это гипервозбудимость, гиперактивность. Таким детям выставляется диагноз — минимальная мозговая дисфункция. Потом они доставляют массу хлопот и в детских учреждениях, и окружающим за счет своих поведенческих нарушений. Они не могут нормально учиться в школе из-за своей неусидчивости, невнимательности. Интеллект у таких детей, как правило, сохранен. Из-за своей неусидчивости они не могут впитывать информацию, а отсюда и проблемы с учебой.
Они не могут нормально учиться в школе из-за своей неусидчивости, невнимательности. Интеллект у таких детей, как правило, сохранен. Из-за своей неусидчивости они не могут впитывать информацию, а отсюда и проблемы с учебой.
Перинатальные патологии ведут к задержке речи. Ребенку 3-4 года, а он говорит несколько слов и у него отсутствует фразовая речь. Это серьезная задержка, свидетельствующая о нарушении умственного развития. Поэтому мы дифференцируем простые задержки от серьезных нарушений, то есть от умственной отсталости. Врачи-психоневрологи находятся на стыке: куда дальше определить ребенка? То ли он выйдет в норму, или ему потребуется коррекция.
Многие продвинутые мамочки сами назначают лечение свои детям, основываясь на отзывах других мамаш, или обращаются к самому доступному и известному доктору – интернет. Так можно делать?
— Категорически против самолечения. Приведу простой пример. С года до двух у ребенка формируются нормальные фазы сна. И все дети в этом возрасте плохо спят – это физиологическая абсолютная норма. Мамочки начинают пичкать таблетками, которые сами же прописывают. А ведь все препараты имеют свои побочные действия и противопоказания. В итоге потом приходят к нам, и мы лечим последствия. Лекарства назначаем в случае крайней необходимости, когда нет возможности обойтись ЛФК, массажем, закаливающими процедурами, соблюдением режимных моментов.
И все дети в этом возрасте плохо спят – это физиологическая абсолютная норма. Мамочки начинают пичкать таблетками, которые сами же прописывают. А ведь все препараты имеют свои побочные действия и противопоказания. В итоге потом приходят к нам, и мы лечим последствия. Лекарства назначаем в случае крайней необходимости, когда нет возможности обойтись ЛФК, массажем, закаливающими процедурами, соблюдением режимных моментов.
Массаж всем показан?
— Любому ребенку с месячного возраста рекомендуется массаж. Здоровому ребенку – общеукрепляющий. Но родители не могут сами ставить диагнозы. Если у ребенка пирамидная недостаточность – это один вид лечебного массажа, если у малыша миотонический синдром – это совсем другая история, сначала надо разбираться в причинах. И это определяет детский психоневролог, которого нужно посещать в первый год жизни каждые три месяца. Поле деятельности у нас огромное! В помощь нам и современные методы диагностики, и обследования. И все это есть в «Академии здоровья».
Перинатальная энцефалопатия: причины, симптомы и лечение
Перинатальная энцефалопатия — целый ряд заболеваний (отклонений в работе) центральной нервной системы у новорожденных. Заболевание может проявляться по-разному, а потому его весьма непросто диагностировать, особенно у младенцев. С этим и связан тот факт, что симптомы энцефалопатии зачастую расцениваются педиатрами как признаки совсем других заболеваний. В итоге лечению заболевания не уделяется необходимого внимания в раннем возрасте, когда наиболее велика вероятность полного выздоровления. Прогрессирующее заболевание при взрослении ребенка зачастую также диагностируется симптоматически, и лечение назначается соответствующее.
Избавление от ПЭП без остеопатического воздействия на первопричины возникновения заболевания, если не полностью невозможно (все-таки организм является саморегулирующей системой, которая вполне способна справиться с рядом серьезных заболеваний), то существенно затруднено.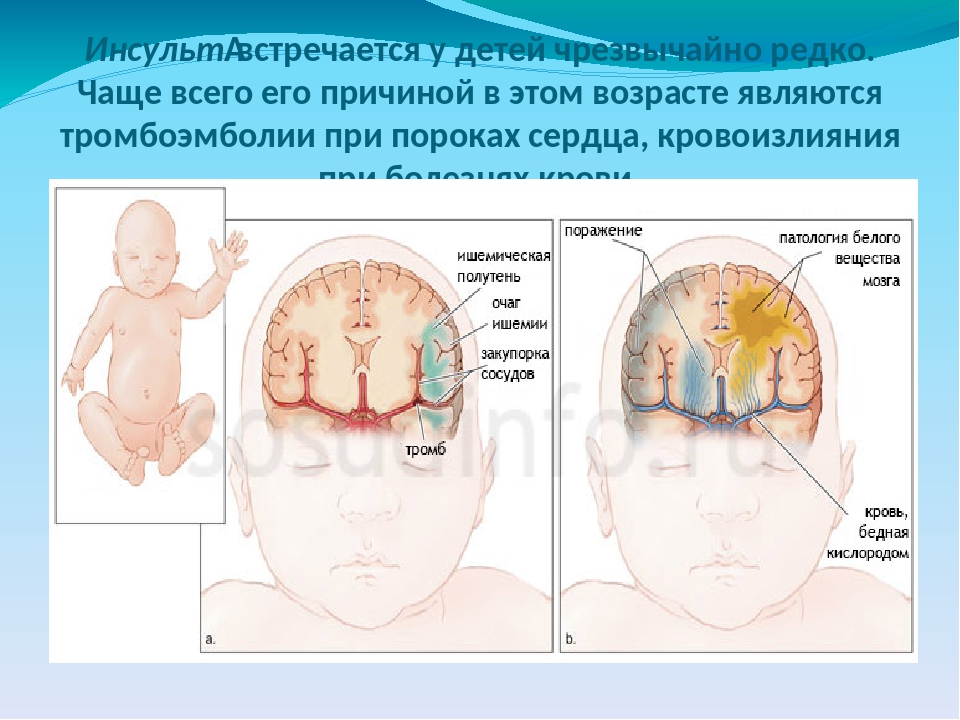 Конечно, не следует пренебрегать и другими методами лечения — как показывает практика, наиболее эффективны как раз комплексные процедуры.
Конечно, не следует пренебрегать и другими методами лечения — как показывает практика, наиболее эффективны как раз комплексные процедуры.
Симптомы и последствия перинатальной энцефалопатии
Симптомы заболевания проявляются по-разному в различные периоды жизни ребенка. Для простоты классификации и улучшения диагностики принято выделять три основных периода ПЭП: острый (в течение первого месяца жизни), восстановительный (до 1 года, реже до 2 лет — в основном у недоношенных детей) и исход заболевания. Существует вероятность, что организм ребенка — как саморегулирующая система, с точки зрения остеопатии, — может полностью восстановиться и нейтрализовать симптомы болезни, адаптировавшись к ним. Это не означает полного выздоровления, так как последствия ПЭП могут проявиться в более позднем возрасте. Поэтому при возникновении подозрений на заболевание необходимо сразу же показать ребенка врачу-остеопату, который сможет поставить правильный диагноз и назначить грамотное адекватное лечение, направленное на избавление организма не от последствий, а от причин болезни.
Основные симптомы перинатальной энцефалопатии
В острый период развития заболевания наблюдаются:
- синдром угнетения ЦНС. Характеризуется общей вялостью новорожденных, сниженной реакцией на внешние раздражители, наличием спонтанных двигательных рефлексов;
- коматозный синдром. Обычно развивается быстро и внезапно, вызывая бессознательное состояние у ребенка. Может проявляться в остром нарушении жизненно важных функций организма;
- повышенная нервно-рефлекторная возбудимость. Проявляется в виде тремора конечностей и ненормально-возбужденной реакцией на внешние раздражители;
- повышенное черепное давление с последующим гипертензионно-гидроцефальным синдромом и непропорциональным увеличением размера черепа;
- судороги.
В восстановительный период к этим симптомам могут добавляться:
- двигательные нарушения. Проявляются по-разному, но общим является то, что ребенок полностью или частично не контролирует свои движения;
- задержка психомоторного развития (ЗПР).
 Проявляется в замедленном развитии, проблемах с речью, нарушении памяти, проблемах с вниманием и т.д.;
Проявляется в замедленном развитии, проблемах с речью, нарушении памяти, проблемах с вниманием и т.д.; - эпилептические припадки.
Признаки заболевания могут проявляться как комбинированно, так и поодиночке. Причем в разном возрасте. При обнаружении хотя бы одного симптома рекомендуется обратиться к специалисту-остеопату для проведения более детального обследования.
Исходом заболевания могут быть:
- выздоровление;
- минимальная мозговая дисфункция;
- умственное недоразвитие;
- ДЦП;
- невротические заболевания;
- эпилепсия;
- гидроцефалия.
Как показывает практика, при легких формах перинатальной энцефалопатии вероятность полного выздоровления достаточно велика. Особенно при правильном остеопатическом лечении, которое может сочетаться с другими методами воздействия на детский организм.
При более тяжелой форме понадобится более длительное лечение, которое в силу различных факторов может не иметь стопроцентной результативности. Некоторые проблемы с памятью, вниманием, координацией движений у ребенка могут сохраняться как в течение длительного периода, так и на протяжении всей жизни. Но остеопатия способствует если и не полному излечению, то существенной минимизации симптомов перинатальной энцефалопатии.
Некоторые проблемы с памятью, вниманием, координацией движений у ребенка могут сохраняться как в течение длительного периода, так и на протяжении всей жизни. Но остеопатия способствует если и не полному излечению, то существенной минимизации симптомов перинатальной энцефалопатии.
Факторы риска
К факторам риска, повышающим опасность возникновения заболевания, относятся:
- хронические болезни матери. Зачастую они не передаются ребенку напрямую, так как не являются наследственными, но на генетическом уровне обуславливают проявления различных патологий и отклонений в развитии плода и уже родившегося ребенка;
- инфекционные заболевания, перенесенные во время беременности. Очень опасны недолеченные патологии, которые могут проявиться на фоне общего ослабления иммунитета организма из-за беременности;
- неправильное питание. В период вынашивания плода организм матери должен получать весь необходимый набор белков, витаминов и минеральных веществ.
 Питание должно быть сбалансированным и согласовываться с врачом — во избежание возникновения пищевой аллергии и расстройств органов пищеварения;
Питание должно быть сбалансированным и согласовываться с врачом — во избежание возникновения пищевой аллергии и расстройств органов пищеварения; - слишком молодой возраст матери. Организм девушки может быть просто неготовым к вынашиванию полноценного и здорового ребенка. В случае слишком юного возраста или недостаточного физического развития будущей матери она должна находиться под постоянным контролем специалиста в течение всего периода беременности и после родов;
- нарушение обмена веществ в организме матери. Так как ее организм тесно взаимосвязан с организмом будущего ребенка, любые нарушения отражаются на питании и здоровье плода. Поэтому столь важно правильное питание, о котором говорилось ранее, а также безотказная работа органов, отвечающих за обмен веществ в организме;
- патологии во время беременности. Очень опасны ранние и поздние токсикозы, стрессы, физические нагрузки и другие факторы, которые могут привести к прерыванию и ненормальному течению беременности;
- неблагоприятная экологическая обстановка.
 К сожалению, сегодня этот фактор опаснее многих других, ведь избежать воздействия вредных внешних проявления зачастую невозможно. Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды;
К сожалению, сегодня этот фактор опаснее многих других, ведь избежать воздействия вредных внешних проявления зачастую невозможно. Рекомендуется обратиться к специалистам (в том числе и остеопату), которые помогут в значительной мере нейтрализовать неблагоприятное воздействие окружающей среды; - недоношенность или переношенность плода.
- Таким образом, большинство факторов риска связаны
именно со здоровьем матери. Поэтому в период беременности она должна тщательно следить за своим самочувствием, прислушиваясь к совету хорошего врача. Параллельно с другими специалистами рекомендуется регулярно посещать остеопата, который также будет следить за ходом протекания беременности и сможет скорректировать вероятные отклонения остеопатическими методами, без применения лекарств, способных навредить будущему ребенку.
Опасность перинатальной энцефалопатии
Как и многие другие младенческие заболевания, не будучи вылеченной на ранних стадиях, перинатальная энцефалопатия прогрессирует с возрастом и может проявляться в виде самых различных нарушений, которые на первый взгляд покажутся не связанными:
- синдром частой заболеваемости.
 Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.;
Это могут быть как частые простуды, так и периодические недомогания, связанные с плохим самочувствием, повышенной утомляемостью, головными болями и т.д.; - хронические заболевания дыхательной системы. Могут проявляться на фоне частых ОРЗ, постепенно переходя в хроническую форму. При отсутствии грамотного остеопатического лечения с возрастом могут перерасти в астму и другие не менее опасные заболевания;
- отставание в развитии. Могут проявляться в не очень явной форме, как затруднения в учебе, особенно в точных науках и творческих дисциплинах;
- нарушения осанки. Незаметные родовые травмы и нарушения в работе ЦНС, возникшие еще на этапе беременности, в дальнейшем нередко приводят к искривлению позвоночника и появлению таких серьезных заболеваний, как сколиоз, со всеми вытекающими из него последствиями, влекущими опускание внутренних органов и их частичную или полную дисфункцию;
- нарушения в работе внутренних органов, системы обмена веществ и системы кровообращения.
 Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.
Обычно эти нарушения неизменно влекут за собой другие заболевания, так как из-за нарушенного кровотока различные участки организма начинают недополучать кислород, что приводит к гибели клеток и дисфункции.
Как расценивают перинатальную энцефалопатию специалисты-остеопаты
С точки зрения остеопатии весь комплекс заболеваний ЦНС, объединяемых под этим термином, является последствием механических нарушений в теле плода новорожденного ребенка. Причем возникнуть они могут еще на этапе беременности или позже — при сложных родах и/или кесаревом сечении. Причинами, приводящими к появлению заболевания, являются:
- дисфункция позвоночного столба или отдельных его участков;
- нарушения в работе внутренних органов;
- продолжительное кислородное голодание;
- нарушение кровообращения.
Но даже в том случае, если во время беременности плод развивался нормально, существует большая вероятность получения повреждения во время родов, так как, проходя между костями таза, плод поворачивается на 360 градусов, что может вызвать нарушения в структуре скелета, мышечных тканях. Наиболее часто наблюдается нарушения в положении шейных позвонков. В большинстве случаев в первые недели роста ребенка последствия повреждений полностью нейтрализуются организмом самостоятельно. Но так бывает далеко не всегда, любые изменения или отклонения в развитии могут привести к осложнениям, которые впоследствии спровоцируют нарушения кровоснабжения мозга и проявление перинатального расстройства.
Наиболее часто наблюдается нарушения в положении шейных позвонков. В большинстве случаев в первые недели роста ребенка последствия повреждений полностью нейтрализуются организмом самостоятельно. Но так бывает далеко не всегда, любые изменения или отклонения в развитии могут привести к осложнениям, которые впоследствии спровоцируют нарушения кровоснабжения мозга и проявление перинатального расстройства.
Как диагностируется перинатальная энцефалопатия у новорожденных и младенцев
Существует ряд безопасных методов исследования головного мозга, которым могут подвергаться новорожденные. Они позволяют составить полную клиническую картину, определить наличие заболевания, его степень, характер течения. Наиболее информативной и эффективной является нейросонография, которая точно выявляет наличие поврежденных участков в мозгу младенца. Дополнительно к ней можно провести доплерографию — для оценки кровотока в сосудах головного мозга.
В случае выявления отклонений в развитии рекомендуется пройти электроэнцефалографическое обследование, направленное на определение степени задержки в развитии. Эта процедура также позволяет выявить очаги эпилептического поражения и оценить степень их активности и опасности для организма.
Эта процедура также позволяет выявить очаги эпилептического поражения и оценить степень их активности и опасности для организма.
В некоторых случаях также рекомендуется осмотр окулиста, который поможет выяснить степень поражения путем оценки состояния зрительных нервов и анализа глазного дна.
Лечение энцефалопатии остеопатическими методами
Хороший врач-остеопат способен диагностировать ранние симптомы заболевания и составить полную картину его течения. Это дает возможность назначить грамотное лечение, способствующее адаптации организма к новым условиям, запуску и стимуляции его функций саморегулирования.
Воздействия остеопата — в зависимости от течения и сложности заболевания — направляются, в первую очередь, на пораженные участки тела, чтобы снять болевые ощущения и спазмы, образующиеся в результате неправильного развития и нарушений в системе кровообращения. Параллельно с этим специалист осуществляет комплекс процедур с целью нормализации работы мозга. Обычно для этого применяются различные техники мышечно-энергетического воздействия, которые позволяют мануальным путем восстановить равновесие натяжения внутричерепных оболочек. Это способствует восстановлению микропульсаций костей черепа и самого мозга, нормализации кровообращения.
После нормализации мозговой деятельности организм получает мощный стимул к саморегуляции и избавлению от энцефалопатии. Дальнейшие действия остеопата заключаются в том, чтобы помочь телу малыша справиться с болезнью. Для этого применяется мануальная терапия, массаж, лечебная физкультура и другие методики, которые, по мнению специалиста, смогут помочь скорейшему выздоровлению.
Как показывает практика, перинатальная энцефалопатия у новорожденных излечивается полностью в 30% случаев — при раннем обнаружении и грамотном лечении. Еще примерно в 20–30% — обычно при тяжелых и среднетяжелых случаях течения — новорожденные излечиваются не полностью. Какие-то симптомы при этом остаются, но зачастую часть из них удается скорректировать комплексной терапией, включающей как ЛФК, остеопатию, массажные техники, так и особое воспитание, обучение и т.д.
К сожалению, во многих случаях, когда перинатальная энцефалопатия проявляется в форме серьезного поражения клеток коры головного мозга, избавиться от заболевания невозможно. Причина в гибели клеток мозга и нарушении нейронных связей, которые не могут быть восстановлены из-за недостатка или отсутствия физических носителей в мозге ребенка. Даже в этих случаях остеопатия может помочь снять некоторые неврологические симптомы, но полное восстановление мозговой деятельности оказывается невозможным.
Важно, чтобы возможная энцефалопатия новорожденных диагностировалась на самых ранних стадиях развития — в первые месяцы жизни ребенка. Чтобы поспособствовать этому, рекомендуется посетить остеопата на 3 месяце жизни, для проведения полного обследования. Специалист назначит необходимые анализы и проведет самостоятельные осмотр, что в комплексе позволит обнаружить симптомы и выявить возможное наличие заболевания.
Нередко при обнаружении ПЭП врачи-педиатры советуют начинать медикаментозное лечение. Причем делать это необходимо с раннего младенческого возраста. Каждый родитель должен осознавать, что такой подход далеко не всегда действенен и способен скорее навредить ребенку. Дело в том, что организм новорожденного достаточно слаб, но при этом сбалансирован и способен к адаптации и саморегуляции. Воздействие на него сильнодействующих лекарств приводит к необратимым изменениям, которые даже остеопат не сможет нейтрализовать. Поэтому, если у ребенка диагностирована перинатальная энцефалопатия или имеются серьезные подозрения на ее наличие, рекомендуется пройти обследование также и у остеопата. Остеопатические техники более тонкие и деликатные, а потому — эффективные. Они точечно воздействуют на участки тела и мозга, нервную систему ребенка, приводя ее в нормальное состояние.
Профилактика заболевания
Наиболее действенным методом профилактики является соблюдение матерью режима в период беременности. В большинстве случаев новорожденные отличаются хорошим здоровьем, если мама заботится о своем организме (а значит, и о малыше). Также рекомендуется регулярное посещение врача-остеопата, который поможет следить за здоровьем в предродовой период.
Очень важно и внимание к здоровью и состоянию ребенка в первые недели и месяцы его жизни. Любые отклонения в развитии, аномалии и патологии должны выявляться и фиксироваться специалистом для точной диагностики и лечения.
Энцефалопатия новорожденного — хотя и очень серьезный диагноз, но еще не приговор. Это заболевание вполне эффективно лечится.
процедуры связанные с заболеванием
Перинатальная гипоксическая энцефалопатия | Бондаренко Е.С., Зыков В.П.
Перинатальная гипоксическая энцефалопатия является частым осложнением патологии беременности и родов и диагносцируется у новорожденных до 5% случаев [1]. Перинатальные повреждения мозга составляют более 60% всей патологии нервной системы детского возраста, непосредственно участвуют в развитии таких заболеваний, как детский церебральный паралич, эпилепсия, минимальная мозговая дисфункция.
Факторы риска. Этиология и патогенез гипоксической энцефалопатии
Для распознавания клинических признаков перинатальной гипоксии необходимо учитывать факторы риска, предрасполагающие к ее развитию [8]:
• Пограничный возраст матери (моложе 20 и старше 35 лет)
• Преждевременная отслойка плаценты
• Предлежание плаценты
• Преэклампсия
• Преждевременные или поздние роды
• Окрашивание околоплодных вод меконием
• Брадикардия, тахикардия плода, приглушение тонов сердца плода
• Многоплодие
• Длительный безводный промежуток
• Диабет матери
• Любые заболевания матери во время беременности
• Прием матерью потенциально опасных для плода препаратов
Среди причин нарушений вентиляции легких и оксигенации крови выделяют периферическую и центральную гипоксию. В периферической гипоксии принимает участие патология дыхательных путей или альвеолярного кровотока, в центральной гипоксии основой является нарушение функции дыхательного центра.
Этиология гипоксии
| Периферическая | Центральная |
| 1. Респираторный | 1. Пониженное давление |
| дистресс-синдром | у матери |
| 2. Аспирация околоплодных | 2. Анемия матери |
| вод | |
| 3. Пневмоторакс | 3. Артериальная гипертензия |
| (с родовой травмой) | |
| 4. Бронхолегочная | 4. Плацентарная |
| дисплазия | недостаточность |
| 5. Врожденные аномалии (синдром Пьера — Робена) | 5. Пороки развития мозга |
Гипоксия приводит к нарушению окислительных процессов, развитию ацидоза, снижению энергетического баланса клетки, избытку нейромедиаторов, нарушению метаболизма глии и нейронов. Ацидоз увеличивает проницаемость сосудистой стенки с развитием межклеточного отека и нарушением церебральной гемодинамики. В условиях гипоксии нарушается перекисное окисление липидов с накоплением агрессивных свободных радикалов, гидроперекисей, которые оказывают деструктивное действие на мембраны нейронов. Нарушения церебральной гемодинамики ишемическо-геморрагического характера являются следствием тяжелой гипоксии мозга.
В антенатальном периоде основным этиологическим фактором гипоксии является плацентарная недостаточность [2,9]. Трофическая недостаточность протекает с нарушением всасываемости и усвоением питательных веществ через плаценту, дефицитом транспорта кислорода и углекислоты, что проявляется синдромом задержки развития плода, внутриутробной гипотрофией, незрелостью легких и сурфактанта. Установлено, что снижение маточно-плацентарного кровотока служит объективным показателем гипоксического поражения мозга [4]. Дефицит сурфактанта и дыхательная аноксия служат основными патогенетическими факторами церебральной гипоксии недоношенных и новорожденных от больных диабетом матерей. В патогенезе дефицита сурфактанта новорожденных лежит вторичный гиперинсулинизм плода, который развивается в ответ на гликемию матери. Инсулин тормозит синтез лецитина — основного элемента сурфактанта, недостаток которого препятствует разлипанию альвеол, что и приводит к нарушению вентиляции легких.
Таким образом, компенсация диабета беременных является профилактикой дыхательного дисстресс-синдрома новорожденных и гипоксической энцефалопатии [15]. В неонатальном периоде причиной церебральной гипоксии и ишемии может быть выраженный интрапульмональный шунт. В патогенезе гипоксии мозга значительную роль играют гипоксическая кардиопатия новорожденных и надпочечниковая недостаточность. Гипогликемия и дефицит запаса гликогена рассматриваются как факторы, обусловливающие повышенную ранимость мозговой ткани к гипоксии новорожденных, особенно недоношенных с низкой массой тела.
Морфология гипоксической энцефалопатии
Головной мозг в норме поглощает пятую часть кислорода, поступающего в организм. У детей раннего возраста доля мозга в использовании кислорода составляет почти половину, что обеспечивает высокий уровень метаболизма окислительных процессов. В зависимости от длительности гипоксии в мозге развиваются изменения от локального отека до некрозов с геморрагическим пропитыванием. В ряде исследований было показано, что имеется различная чувствительность мозговых структур к гипоксии, которая зависит от особенностей метаболизма и кровоснабжения. Наиболее чувствительными к гипоксии являются зона Зоммера аммонова рога и перивентрикулярная область смежного кровоснабжения между передней, средней и задней мозговыми артериями. При сочетании гипоксии и ишемии возникают очаги некрозов в коре, зрительном бугре, полосатом теле, мозжечке. Выделяют следующие стадии морфологических гипоксических изменений в головном мозге: I стадия — отечно-геморрагическая, II стадия — энцефальный глиоз, III стадия — лейкомаляция (некроз), IV стадия — лейкомаляция с кровоизлиянием. Первые две стадии острой гипоксии являются курабельными, имеется возможность восстановления метаболизма нейронов и глии, III и IV стадии ведут к необратимой гибели нейронов. При антенатальной гипоксии наблюдаются дистрофия нейронов, пролиферация глии, явления склерозирования, кистозные полости на местах мелких очагов некрозов.
Клиника гипоксической энцефалопатии
В клинической картине гипоксической энцефалопатии выделяют три периода — острый (1-й месяц жизни ребенка), восстановительный (с 1-го месяца до 1 года, а у недоношенных незрелых детей до 2 лет) и исход [12].
В остром периоде по степени тяжести выделяются легкая форма поражений нервной системы, отражающая преходящие нарушения гемоликвородинамики; форма средней тяжести с отечно-геморрагическими изменениями, глиозом, единичными лейкомаляциями; тяжелая форма, характерная для генерализованного отека мозга, множественных лейкомаляций и кровоизлияний. Для определения степени тяжести и выраженности нарушений мозгового кровообращения применяется шкала Апгар.
В остром периоде выделяют 5 клинических синдромов: повышение нервно-рефлекторной возбудимости, судорожный, гипертензионно-гидроцефальный, синдром угнетения, коматозный. Обычно наблюдается сочетание нескольких синдромов. Особенностью острого периода является доминирование общемозговых нарушений без выраженных локальных симптомов. При легкой форме поражения мозга (оценка по шкале Апгар 6 — 7 баллов) характерным является синдром повышенной нервно-рефлекторной возбудимости. Основными проявлениями синдрома являются усиление спонтанной двигательной активности, беспокойный поверхностный сон, удлинение периода активного бодрствования, трудность засыпания, частый немотивированный плач, оживление безусловных врожденных рефлексов, мышечная дистония, повышение коленных рефлексов, тремор конечностей и подбородка. У недоношенных синдром нервно-рефлекторной возбудимости в 94% случаев является клиническим признаком понижения порога судорожной готовности, что подтверждается данными электроэнцефалографии (ЭЭГ) [12]. Больные, у которых, по данным ЭЭГ, имеется снижение порога судорожной готовности, должны рассматриваться в группе риска по судорожному синдрому.
Среднетяжелая форма гипоксической энцефалопатии (оценивается по шкале Апгар 4 — 6 баллов) проявляется гипертензионно-гидроцефальным синдромом и синдромом угнетения.
Для гипертензионно-гидроцефального синдрома характерным является увеличение размеров головы на 1 — 2 см по сравнению с нормой (или окружностью грудной клетки), раскрытие сагитального шва более 0,5 см, увеличение и выбухание большого родничка. Типичной является брахиоцефалическая форма головы с увеличенными лобными буграми или долихоцефалическая — с нависающим кзади затылком. Отмечается симптом Грефе, симптом «заходящего солнца», непостоянный горизонтальный нистагм, сходящее косоглазие. Выявляется мышечная дистония, больше в дистальных отделах конечностей в виде симптома «тюленьих лапок» и «пяточных стопок». У большинства детей, особенно в первые дни жизни, эти явления сочетаются с пароксизмами вздрагиваний, спонтанным рефлексом Моро, нарушением сна, симптомом Арлекино, общим и локальным цианозом. Развитие гипертензионно-гидроцефального синдрома на 3 — 5-й день жизни может являться признаком перивентрикулярного кровоизлияния. Гипертензионно-гидроцефальный синдром может быть изолированным, но чаще сочетается с синдромом угнетения или коматозным синдромом. Синдром угнетения проявляется вялостью, гиподинамией, снижением спонтанной активности, общей мышечной гипотонией, гипорефлексией, угнетением рефлексов новорожденных, снижением рефлексов сосания и глотания. Наблюдаются локальные симптомы в виде расходящегося и сходящегося косоглазия, нистагм, асимметрия и отвисание нижней челюсти, асимметрия мимической мускулатуры, бульбарные и псевдобульбарные симптомы. Синдром характеризует течение острого периода гипоксической энцефалопатии и в конце первого месяца жизни обычно исчезает. В остром периоде синдром угнетения может являться предвестником отека мозга и развития коматозного синдрома.
Коматозный синдром является проявлением тяжелого состояния новорожденного, по шкале Апгар оценивается 1 — 4 балла. В клинической картине выявляются выраженная вялость, адинамия, мышечная гипотония до атонии, врожденные рефлексы не выявляются, зрачки сужены, реакция на свет незначительная или отсутствует. Нет реакции на болевые раздражители, «плавающие» движения глазных яблок, горизонтальный и вертикальный нистагм, сухожильные рефлексы угнетены. Дыхание аритмичное, с частыми апное, брадикардия, тоны сердца глухие, пульс аритмичный, артериальное давление низкое. Могут отмечаться приступы судорог с преобладанием тонического компонента. Тяжелое состояние сохраняется 10 — 15 дней, отсутствуют рефлексы сосания и глотания. Появление в остром периоде гидроцефалии с выбуханием и напряжением большого родничка, расхождением черепных швов, протрузией глазных яблок, быстрым ростом головы свидетельствует о внутричерепном кровоизлиянии.
Судорожный синдром в остром периоде, как правило, сочетается с синдромом угнетения или коматозным. Возникает в результате гипоксического отека мозга, гипогликемии, гипомагнемии или внутричерепных кровоизлияний. Проявляется в первые дни жизни тонико-клоническими или тоническими судорогами. Наряду с этим наблюдаются локальные клонические судороги или гемиконвульсии. Судорожные припадки у новорожденных отличаются кратковременностью, внезапным началом, отсутствием закономерности повторения и зависимости от состояния сна или бодрствования, режима кормления и других факторов. Судороги наблюдаются в виде мелкоамплитудного тремора, кратковременной остановки дыхания, тонического спазма глазных яблок по типу пареза взора вверх, имитации симптома «заходящего солнца», нистагма, автоматических жевательных движений, пароксизмов клонуса стоп, вазомоторных реакций. Эти судороги по своему характеру иногда напоминают спонтанные движения ребенка, что затрудняет диагностику.
Восстановительный период гипоксической энцефалоратии включает следующие синдромы: повышение нервно-рефлекторной возбудимости, гипертензионно-гидроцефальный, вегетовисцеральных дисфункций, двигательных нарушений, задержки психомоторного развития, эпилептический.
Синдром повышенной нервно-рефлекторной возбудимости в восстановительном периоде имеет два варианта течения. При благоприятном варианте течения отмечается исчезновение или уменьшение выраженности симптомов повышенной нервно-рефлекторной возбудимости в сроки от 4 — 6 месяцев до 1 года. При неблагоприятном варианте, особенно у недоношенных, может развиться эпилептический синдром.
Гипертензионно-гидроцефальный синдром имеет два варианта течения:
1) гипертензионно-гидроцефальный синдром с благоприятным течением, при котором наблюдается исчезновение гипертензионных симптомов при задержке гидроцефальных;
2) неблагоприятный вариант гипертензионно-гидроцефального синдрома, входящий в симптомокомплекс органического церебрального синдрома.
Исходы гипертензионно-гидроцефального синдрома:
1. Нормализация роста окружности головы к 6 месяцам.
2. Компенсированный гидроцефальный синдром в 8 — 12 месяцев.
3. Развитие гидроцефалии.
Синдром вегето-висцеральных дисфункций начинает проявляться после 1 — 1,5 месяца жизни на фоне повышения нервно-рефлекторной возбудимости и гипертензионно-гидроцефального синдрома. В клинической картине отмечаются упорные срыгивания, стойкая гипотрофия, нарушение ритма дыхания и апное, изменение окраски кожных покровов, акроцианоз, пароксизмы тахи- и брадипное, расстройства терморегуляции, дисфункция желудочно-кишечного тракта, височное облысение.
Эпилептический синдром может проявляться в любом возрасте (как продолжение судорог после рождения или на фоне соматической инфекции). У новорожденных и грудных детей он имеет так называемое возрастное лицо, т. е. судорожные пароксизмы имитируют те двигательные возможности, которыми ребенок к моменту их появления обладает.
У новорожденных и грудных детей (особенно у недоношенных) судорожный синдром характеризуется многообразием клинических форм припадков. Наблюдаются генерализованные судорожные припадки (тонико-клонические, клонические, тонические), абортивные, фокальные, гемиконвульсивные, полиморфные припадки, простые и сложные абсансы. По частоте преобладают полиморфные формы припадков. У недоношенных детей с перинатальной энцефалопатией пропульсивные и импульсивные пароксизмы в изолированном виде не встречаются, а наблюдаются только в составе полиморфных припадков. Наибольшую трудность в диагностике представляют абортивные и бессудорожные формы пароксизмов.
Наблюдается имитация безусловных двигательных рефлексов в виде пароксизмально возникающих проявлений шейно-тонического симметричного рефлекса с наклоном головы и тоническим напряжением рук и ног; шейно-тонического асимметричного рефлекса с поворотом головы в сторону и разгибанием одноименной руки и ноги; первой фазы рефлекса Моро с раскрытием ручек. Бывают пароксизмы в виде спазма взора и нистагмом, имитацией «симптома заходящего солнца». Нередко наблюдаются приступы покраснения и побледнения кожных покровов с усиленным потоотделением, иногда срыгиваниями. После 3 — 4 месяцев жизни, по мере появления способности удерживать голову, появляются «кивки», «кливки», а с 6 — 7 месяцев — «поклоны» (сгибание туловища вперед-назад).
Такие особенности судорожного синдрома у недоношенных детей, как нестабильность клинических проявлений с преобладанием полиморфных судорог, наличие абортивных форм припадков, а также сложных абсансов с имитацией безусловных рефлексов новорожденных (первой фазы рефлекса Моро, асимметричного шейно-тонического рефлекса) являются, вероятно, следствием незрелости структур головного мозга. Однако увеличение частоты припадков, нарастание полиморфизма их проявлений, резистентность к противосудорожной терапии должны настораживать в отношении формирования грубых органических форм поражения мозга.
Полиморфизм приступов, их резистентность к терапии является прогностически неблагоприятным признаком.
Синдром двигательных нарушений выявляется с первых недель жизни, может протекать с мышечной гипотонией или гипертонией. При появлении синдрома двигательных нарушений с мышечной гипотонией отмечается снижение спонтанной двигательной активности, угнетение сухожильных рефлексов и врожденных безусловных рефлексов новорожденных. Синдром двигательных нарушений с мышечной гипотонией встречается изолированно, а также в сочетании с гипертензионно-гидроцефальным синдромом, синдром повышенной нервно-рефлекторной возбудимости с понижением порога судорожной готовности. Неблагоприятно сочетание синдрома двигательных нарушений и судорожного синдрома.
Нарастание мышечной гипертонии у доношенных детей, появление сторонности очаговых симптомов должны настораживать в плане развития детского церебрального паралича.
Синдром задержки психомоторного развития начинает проявляться с 1 — 2 месяцев. В структуре синдрома отмечается нарушение редукции безусловных врожденных рефлексов. Большую диагностическую роль приобретает шейно-тонические симметричный и асимметричный рефлексы, задержка формирования выпрямительных лабиринтных цепных тонических рефлексов. При наличии в структуре данного синдрома задержки психического развития у детей к месячному возрасту наблюдается недостаточно устойчивая фиксация взгляда, кратковременное прослеживание с быстрым истощением. Нет реакции на голос матери, слухового сосредоточения. К 2 — 3-месячному возрасту наблюдается недостаточное оживление при общении, крик маловыразителен, гуление отсутствует, дети отыскивают источник звука глазами без поворота головы, появляется редкая, трудно вызываемая улыбка. К полугоду — недостаточно активно интересуются игрушками и окружающими предметами, недостаточно реагируют на присутствие матери, гуление малоактивное и непродолжительное, манипуляции с предметами задержаны, нет активного внимания. Если задержка развития является «темповой», она при правильном выхаживании начинает исчезать. Данная группа детей в 4 — 5 месяцев как бы «скачком» становится активнее, причем психическое развитие опережает моторное. Появляются эмоциональная реакция на окружающих, интерес к игрушкам.
Возрастные двигательные функции начинают активно компенсироваться после 6 — 7 месяцев и, как правило, восстанавливаются к 1 — 1,5 годам. Прогностически неблагоприятна длительная задержка психического развития.
Диагностика
Исследование глазного дна в остром периоде легкой гипоксической энцефалопатии отклонений не выявляет, реже наблюдают умеренное полнокровие вен. При среднетяжелой степени отмечают расширение вен, отек, отдельные геморрагии. При тяжелой степени повреждения на фоне выраженного отека расширения сосудов отмечается стушеванность границ диска зрительного нерва, кровоизлияния. В дальнейшем у таких детей может обнаружиться атрофия сосков зрительных нервов.
В спинномозговой жидкости изменения выявляются при наличии внутричерепного кровоизлияния. В этих случаях в ликворе имеются свежие и выщелочные эритроциты. После 7 — 10-го дня жизни подтверждением перенесенного кровоизлияния является наличие в ликворе макрофагов.
Нейросонография — двухмерное ультразвуковое исследование анатомических структур мозга через большой родничок — позволяет установить перивентрикулярное кровоизлияние, очаги лейкомаляции, расширение желудочковой системы — вентрикуломегалию [5, 10]. Нейросонография позволяет провести дифференциальную диагностику с пороками головного мозга. Признаки гипоплазии мозга: увеличение субарахноидальных пространств, расширение межполушарной щели, вентрикуломегалия, повышение плотности в области паренхимы мозга без четкой дифференциации извилин, порэнцефалия. Галопрозэнцефалия — увеличение одного желудочка, тени, повышение эхоплотности от стволовых структур мозга, снижение плотности от паренхимы мозга [7]. При клинико-нейросонографических сопоставлениях выявляется корреляция числа лейкомаляций и неврологических исходов. Множественные лейкомаляции в обоих полушариях, обнаруживаемые у больных по данным нейросонографии в остром периоде заболевания, сочетаются с синдромом двигательных нарушений и грубой задержкой психомоторного развития в восстановительном периоде. Компьютерная томография головного мозга помогает объективизировать гипоксические изменения мозговой ткани в структурах мозжечка и ствола мозга, которые недостаточно четко выявляются при нейросонографии.
Электроэнцефалографическое (ЭЭГ) исследование выявляет очаги медленноволновой активности, очаги редукции корковой ритмики, очаги эпилептической активности. Большое значение ЭЭГ-исследование имеет для выделения группы риска по судорожному синдрому и диагностики клинически «немых» приступов. Косвенным подтверждением судорожного синдрома, а также признаком понижения порога судорожной готовности у больных является наличие пароксизмальных изменений ЭЭГ. Повторные припадки могут приводить к усилению выраженности пароксизмальной активности на ЭЭГ.
Из биохимических исследований в остром периоде показателем глубины гипоксических нарушений является оценка ацидоза от смешанного до выраженного декомпенсированного метаболического. При тяжелой гипоксии нарастает осмотическое давление плазмы крови, увеличивается уровень лактатдегидрогеназы. Лактатдегидрогеназа и другие ферменты гликолиза коррелируют с тяжестью состояния детей и отражают выраженность гипоксии в остром периоде перинатальной энцефалопатии.
Рентгенография легких используется для диагностики врожденных ателектазов, пневмопатии и воспалительных изменений легких.
Лечение острого периода
В остром периоде необходима своевременная коррекция респираторного дыхательного дисстресс-синдрома и адекватная вентиляция легких. У недоношенных проводится эндотрахеальное введение колфосцерила пальмитата 5 мл/кг. Использование аналогов сурфактанта приводит к значительному регрессу неврологических синдромов гипоксической энцефалопатии.
1. Коррекция гомеостаза и гиповолемии: свежезамороженная плазма 5 — 10 мл/кг, 10% альбумин 5 — 10 мл/кг, реополиглюкин 7 — 10 мл/кг, гемодез 10 мл/кг.
2. Снижение проницаемости сосудов: 12,5% раствор этамзилата внутримышечно или внутривенно, 1% викасол 0,1 мл/кг.
3. Метаболическая и антиоксидантная терапия: пирацетам 50 мг/кг, 10% глюкоза 10 мл/кг, актовегин внутривенно, 5% витамин Е 0,1 мл в день. В качестве антиоксиданта используется соевое масло 2 — 3 мл 4 — 6 дней на кожу живота [11].
4. Сосудистая терапия: винпоцетин 1мг/кг внутривенно.
5. Дегидратационная терапия: гидрокортизон 3 — 10 мг/кг, преднизолон 1 — 2 мг/кг, 25% магния сульфат 0,2 мл/кг.
6. Улучшение тканевого метаболизма сердечной мышцы: кокарбоксилаза 8 мг/кг, АТФ 10 мг/кг.
7. Антиконвульсантная терапия: диазепам 1мг/кг внутримышечно или внутривенно, ГОМК 50 мг/кг, барбитураты, когда бензодиазепины не эффективны, 5 мг/кг [14].
Лечение восстановительного периода
Лечение восстановительного периода проводится по синдромологическому принципу.
1. При синдроме повышенной нервно-рефлекторной возбудимости с проявлениями вегетовисцеральных дисфункций показаны седативные препараты: диазепам 0,001 г 2 раза в день, тазепам 0,001 г 2 раза в день, микстура с цитралью — раствор цитраля 2,0, магния сульфат 3,0, 10% раствор глюкозы 200,0 — по чайной ложке 3 раза в день; с 2-месячного возраста назначаются успокоительный коктейль из трав (корень валерианы, пустырник, шалфей) по 1 чайной ложке 3 раза в день.
2. При гипертензионно-гидроцефальном синдроме целесообразно назначать фуросемид 0, 002 г/кг в сутки с панангином, глицерол по 1 чайной ложке 3 раза в день. При выраженных проявлениях гипертензионно-гидроцефального синдрома используют ацетазоламид по 0,02 г/кг в сутки однократно по схеме: 3 дня — прием, 1 день перерыв, курс от 3 нед до 1 — 1,5 мес с панангином.
3. При синдроме двигательных нарушений: витамин В6 5 мг, витамин В1 2 мг, АТФ 0,5 мл 10 — 12 инъекций, пиритинол 10 — 20 капель на 1 кг массы тела 2 раза в день в первой половине дня 1 — 3 мес. Массаж. Лечебная гимнастика, проводится обучение матери навыкам реабилитации.
4. При синдроме задержки психомоторного развития: пирацетам 30 — 50 мг/кг в 3 приема, пиритинол. С 6 месяцев церебролизин 0,5 мл № 20 (противопоказан при судорожном синдроме), витамины В6, В1. Гамма-аминобутировая кислота по 0,06 г 2 — 3 раза в день.
5. При судорожном синдроме: вальпроат натрия 20 — 50 мг/кг, клоназепам до 1 — 2 мг в сутки, фенобарбитал 1 — 2 мг/кг. При резистентных судорогах ламотригин 1 — 2 мг/кг.
6. Хирургическое лечение применяется при сочетанных перивентрикулярных кровоизлияниях и развитии постгеморрагической гидроцефалии, проводится вентрикулярное шунтирование.
Терапевтические мероприятия в дальнейшем индивидуализируются в зависимости от исхода процесса. К годовалому возрасту у большинства зрелых детей с появлением вертикализации и речевых функций можно выявить исходы перинатальной гипоксической энцефалопатии. Выздоровление наступает у 15 — 20% детей. Частыми последствиями перенесенной энцефалопатии являются минимальная мозговая дисфункция, гидроцефальный синдром. Наиболее тяжелыми исходами являются детский церебральный паралич и эпилепсия.
Безусловно, успехи перинатальной медицины, адекватное ведение родов и острого периода гипоксической энцефалопатии позволят снизить психоневрологические исходы заболевания.
Литература:
1.Балан П.В., Маклакова А.С., Крушинская Я.В., Соколова Н.Л., Кудаков Н.И. Сравнительный анализ устойчивости к острой гипобарической гипоксии новорожденных и взрослых экспериментальных животных. Акуш. и гин. 1998;3:20-3.
2. Громыко Ю.Л. Оценка эффективности нового антиоксидантного препарата -актовегина для лечения плацентарной недостаточности и отставания в размерах плода. Материалы 1 съезда Российской ассоциации специалистов перинатальной медицины, 32.
3. Ивановская Т.Е., Покровская Л.Я. Основная патология перинатального периода по современным патологическим данным. Педиатрия 1987;4:11-7.
4. Кулаков В.И. Пренатальная медицина и репродуктивное здоровье женщины. Акуш. и гин. 1997;5:19-22.
5. Кузнецова Л.М, Дворяковский И.В., Мордова Н.А. Корреляция клинических и ультразвуковых признаков при ликвородинамических нарушениях у детей раннего возраста. Материалы научно-практической конференции. Калуга, 1980;34.
6. Миленин О.Б., Ефимов М.С. Применение синтетического сурфактанта экзосорфа в лечении и профилактике респираторного дисстресс-синдрома у новорожденных детей. Акуш. и гин. 1998;3:5-9.
7. Орлова Н.С., Мачинская Е.А., Фишкина Е.В. Нейросонография в диагностике некоторых пороков развития головного мозга. Материалы научно-практической конференции. Калуга. 1982;35.
8. Педиатрия (пер. англ.) / Под ред. Н.Н.Володина. М.,1996;125-70.
9. Федорова М.В. Плацентарная недостаточность. Акуш. и гин. 1997;5:40-3.
10. Фишкина Е.В., Симушин Г.П., Рубцова И.И. и др. Возможности нейросонографии в диагностике поражений центральной нервной системы
у новорожденных детей. Материалы научно-практической конференции. Калуга. 1980;43.
11. Шарипов Р.Х. Применение препаратов мембраннотропного действия в комплексном лечении недоношенных детей с перинатальной энцефалопатией. Тезисы докладов научно-практической конференции. Самара. 1993;1:63.
12. Эдельштейн Э.А., Бондаренко Е.С., Быкова Л.И. Перинатальные гипоксические синдромы. Учебное пособие. М., 1988;38.
13. De Volder AG, Joffinet AM, Bol A, et al. Brain glucose metabolism in postanoxic syndrome. Arch Neurol 1990;47(2):197-204.
14. Carlier G, Guidi О, Dubru JM. Le traitement des convulsions d’enfant. Rev/med/ Liege. 1989;257-62.
15. J. VoIpe Neurology of the Newborn, coundres company. 1987;715.
.
Диагностика энцефалопатии при помощи МРТ – МЕДСИ
Содержание
Что такое энцефалопатия и какая она бывает
Энцефалопатия – это группа заболеваний, синдром, который связан с дегенеративными изменениями в тканях головного мозга. Она проявляется на фоне других нарушений в состоянии организма и поражает как взрослых, так и детей.
Некоторые хронические недуги или иные недомогания могут привести к ухудшению кровоснабжения и питания кислородом мозговых клеток. По этой причине возникает дистрофия тканей данного органа, что ведет к гибели нейронов.
Развитие энцефалопатии можно предотвратить, даже если все предпосылки к ее возникновению уже появились. Для этого необходимо проходить регулярное обследование в клинике МЕДСИ, такие как МРТ мозга при энцефалопатии, наблюдаться у врача и неукоснительно соблюдать его рекомендации.
Виды недуга
Выделяют два типа классификации данного заболевания – по характеру появления и по его причине.
По характеру болезнь может быть:
- Врожденная
- Приобретенная
Первый вид проявляется у новорожденных и может быть диагностирован в период беременности или в первую неделю после родов.
У подростков же и у взрослых людей это заболевание приобретенное. И в данном случае оно может проявиться по таким причинам:
- Нарушения в сосудах и кровоснабжении
- Патологические и атипические изменения в тканях мозга (дисцикуляторные), которые делятся на типы:
- Венозный
- Атеросклеротический
- Гипертонический
- Смешанный
- Травматическая
- Алкогольная
- Токсическая
- Лучевая
Стадии заболевания
В современной медицине насчитывают четыре стадии энцефалопатии:
- Начальную
- Умеренную
- Выраженную
- Тяжелую
В первом случае симптомов может не быть. Во втором – они не всегда очевидны и характеры. В третьем симптоматика проявляется гораздо сильнее и нарастает по мере ухудшения состояния. На последней же стадии происходит серьезное поражение тканей головного мозга.
Причины и симптомы
Появление энцефалопатии связано с нарушениями кровотока и снабжения тканей мозга кислородом на фоне иных патологий и проблем в жизнедеятельности организма.
Причинами такого состояния являются:
- Атеросклеротические изменения в сосудах (в таком случае их стенки уплотняются, и на них появляются различного рода бляшки)
- Желтуха или иное тяжелое инфекционное заболевание, при которых вырабатывается и не утилизируется чрезмерное количество билирубина
- Кислородная недостаточность в течение долгого времени из-за проблем с давлением, прерыванием дыхания и другого
- При врожденной форме – прием матерью во время беременности некоторых лекарств, вредных веществ (алкоголь, никотин)
- Сердечно-легочная недостаточность (чаще всего проявляется у пожилых пациентов)
- Сахарный диабет
- Постоянное использование токсических веществ и алкоголя
- Слишком низкий уровень сахара в крови, плохое питание
- Опухоль мозга
- Облучение
- Очень часто меняющееся внутричерепное давление
- Регулярные стрессы
- Наследственные заболевания – сердечно-сосудистые, нервно-дегенеративные
Многие из данных нарушений можно выявить, когда врач назначит МРТ головного мозга при энцефалопатии.
Симптоматика заболевания
Подозрение на энцефалопатию той или иной природы возникает в следующих случаях:
- Затяжная депрессия, тревожность, маниакальность
- Слабость, нетрудоспособность
- Замедленная реакция, проблемы с памятью, когнитивные нарушения
- Спазмы, боли, головокружения
- Нарушения двигательной активности конечностей
- Проявление психических заболеваний
- Ухудшение зрения или слуха
На последней стадии возможно впадение в кому, паралич, а также инфаркт и инсульт.
Основные методы диагностики энцефалопатии
Чтобы выявить данное заболевание, недостаточно только провести лабораторные анализы. Необходимо провести и другие типы обследований:
- Собрать анамнез. Выяснить у больного, были у него хронические недуги, которые могли бы повлиять на ткани мозга
- Провести внешний осмотр. Определить симптомы, на которые жалуется больной, выяснить, нет ли очевидных физических отклонений
- Направить пациента на ряд тестов. Они помогут определить когнитивную активность, нарушения памяти, поведения или наличие психических отклонений
- Провести лабораторные анализы и исследования. МРТ мозга считается при диагностировании энцефалопатии одним из наиболее точных
Виды лабораторных исследований
Существует несколько типов анализов с использованием различных приборов, которые помогают выявить энцефалопатию:
- Магнитно-резонансная томография. Позволяет увидеть одновременно несколько частей и отделов головного мозга и найти нарушения в их развитии
- УЗИ с применением эффекта Доплера. Оно позволяет увидеть сосуды на всем их протяжении, а также рассмотреть изменения в них даже при минимальном диаметре исследуемого объекта
- Реоэнцефалография. Исследует сосуды на основе пропускания слабого тока и изменения величин электрического сопротивления тканей
- Компьютерная томография – тип рентгенологического анализа, который позволяет увидеть признаки перенесенного инсульта и иных патологий
- ЭЭГ. Запись потенциалов, связанных с общей электрической активностью мозга. Он показывает изменения функций коры данного органа и его более глубоких образований
Также врач прописывает и другие обследования:
- Общий анализ крови
- Динамика изменения давления
- Анализ на содержание аутоантител – появляются вследствие аутоимунных нарушений
- Обследование на содержание токсинов (таких, как алкоголь)
- Наличие метаболических отходов – они не могут использоваться органами
Что способна выявить МРТ
МРТ головного мозга при энцефалопатии позволяет рассмотреть детали развития различных отделов мозга, шейной части позвоночника и сосудов. Оно дает наиболее полное, четкое и контрастное изображение в разных плоскостях, что позволяет определить даже незначительные изменения на самой первой стадии появления заболеваний, когда никаких симптомов еще не возникло.
Благодаря данному обследованию можно выявить:
- Уменьшение мозгового объема – происходит уничтожение клеток, а также связей между нервными волокнами и нейронами, сопровождается нарушениями в работе коры и подкорки
- Атрофию коры мозга – проявляется в виде появления тромбов, вызывает гипоксию затылочной и теменной части
- Разреженность белого вещества – может вызвать психические отклонения
- Увеличение пространства между мягкой и паутинной оболочками – в нормальном состоянии оно заполнено ликвором, который обеспечивает питание клеток, в патологическом же состоянии может вызвать гидроцефалию или водянку. Обычно эти заболевания проявляются у младенцев. У взрослых же данный симптом может обозначать наличие гематомы или опухоли
- Атеросклероз мозга – хроническая болезнь, которая характеризуется образованием жировых отложений в виде бляшек на стенках сосудов, в которых затем появляется соединительная ткань и соли кальция. Из-за этого диаметр сосуда сужается, что ведет к дефициту кислорода и питательных веществ в органах
- Изменение боковых отделов мозга
- Множество инсультных мелких очагов – ишемический тип недуга, который ведет к появлению инфаркта
- Чрезмерная активность мозговых желудочков
- Нарушения строения лобной доли – может привести к ухудшению процесса мышления, речи, поведения
- Вестибулярные и вегетативные недуги – головокружения, тошнота, нарушение координации движения
При необходимости может быть использовано исследование с применением контрастного вещества. Это позволяет определить скорость поступления крови как в сосуды, так и в части мозга, в которых питание слишком мало. Также данным способом можно диагностировать наличие других путей снабжения клеток кровью, которые конструирует мозг при дефиците питания.
Все заболевания такого рода способствуют появлению энцефалопатического синдрома. Поэтому необходимо проходить периодические обследования, особенно если проявился хотя бы один из возможных симптомов.
Преимущества МРТ при диагностике заболевания
При использовании МРТ головного мозга энцефалопатия может быть определена с высокой точностью. Четкость изображения позволяет увидеть любые возможные нарушения в лобной, височной, затылочной и теменной зонах, а также в области шейных позвонков.
Магнитно-резонансная томография обладает рядом преимуществ перед иными методами исследований:
- Высокая степень информативности, возможность отследить динамические изменения в структурах тканей мозга
- Безопасность, безболезненность и не инвазивность – не нарушается целостность кожных покровов, не используется рентгенологического излучения
- Возможность обнаружения заболевания на самой первой стадии, в отсутствие симптомов и иных признаков
- Обследование происходит с разных сторон, томограмма включает в себя несколько срезовых изображений, но пациенту не нужно двигаться или переворачиваться
- Данное исследование можно проводить многократно для отслеживания результатов лечения или хирургического вмешательства, динамики протекания заболевания без нанесения вреда организму
- Результат записывается на электронный носитель и распечатывается, а скорость его появления – не более часа с момента проведения процедуры
- В отличие от некоторых иных методов МРТ можно применять для диагностики беременных женщин (но не рекомендуется делать этого в первом триместре)
Так как данный метод основан на явлении магнитного резонанса, то существуют и некоторые противопоказания для его использования:
- Наличие сердечных клапанов, кардиостимуляторов и подобных приборов, вступающих во взаимодействие с магнитным полем
- Установленные электронные приборы в некоторых частях тела (таких, как ушные протезы)
- Присутствие в организме металлических имплантатов или осколков
- Для приборов закрытого типа вес пациента должен быть не более 130 килограмм, а обхват – до 120 сантиметров
- Для пациентов с выраженной фобией закрытого пространства нахождение в трубе аппарата также будет затруднительно
- Психически нездоровым пациентам сложно находиться неподвижно в течение длительного времени
- В первом триместре беременности (если от данного исследования не зависит жизнь и здоровье) этот метод не используют
- Если необходимо обследование с контрастом, у пациента не должно быть аллергии на его компоненты
- Наличие сильных болей, мешающих неподвижно лежать на спине
Во всех иных случаях МРТ-анализ проводить можно.
Наличие аппаратов открытого типа за счет их открытой по бокам конструкции позволяет проводить магнитно-резонансное исследование людям с клаустрофобией и большим весом (до 200 килограмм, диаметр тела неважен). Он же помогает проводить такое обследование детям, пожилым людям и пациентам с психическими отклонениями за счет возможности контроля за процессом.
На стандартном туннельном аппарате для беспокойных или боящихся пациентов можно использовать наркоз.
Преимущества проведения процедуры в МЕДСИ
- Сеть клиник МЕДСИ предлагает своим пациентам проведение МРТ мозга при энцефалопатии на различных современных томографах с регулируемым напряжением, которые подходят для пациентов любых возрастных категорий
- Врачи-рентгенологи высшей квалификационной категории качественно расшифровывают результаты, назначают дополнительные анализы и необходимое в каждом конкретном случае лечение
- МЕДСИ предлагает срочное обследование в случае травмы или иных оперативных показаний
- Здесь более двадцати клиник по всей Москве и тридцать типов магнитно-резонансного обследования
- Есть условия для пациентов с боязнью замкнутых пространств, а также больных с психическими отклонениями, в том числе наиболее щадящий наркоз
- Используются аппараты, безопасные для беременных женщин и детей
- Чтобы узнать подробности, необходимо позвонить по телефону 8 (495) 7-800-500
Нервная система младенца
Проблема детского здоровья всегда являлась одной из главных в системе государственных приоритетов. Многогранность ее состоит не только в рождении здорового ребенка, но и создание благоприятных условий для его роста и развития. Большое значение придается разработке системы профилактики и лечения больных детей, в том числе детей с врожденной патологией.
В связи с этим особое внимание уделяется нарушениям, возникающим в антенатальном и перинатальном периодах развития. Необходимо отметить, что значительно расширились технические возможности диагностической медицины (в том числе ДНК – диагностика), методы визуализации плода, в связи с чем стала возможной ранняя диагностика заболеваний и пороков развития. Патология раннего детского возраста и особенно новорожденных представляет повышенную сложность для диагностического процесса. В большей степени это относится к неврологическому обследованию. В этом возрасте на первый план выступают общие симптомы, связанные с незрелостью центральной нервной системы. Морфологическая незрелость центральной нервной системы проявляется особенностью ее функционирования, что характеризуется недифференцированностью ответа на различные раздражители, отсутствием стабильности неврологических реакций и их быстрой истощаемостью.
При оценке полученных данных необходимо учитывать состояние матери как в период беременности, так и в процессе родов.
Нарушения в здоровье матери могут привести к угнетению общего состояния ребенка, ослаблению двигательной активности, угнетению или ослаблению условных или безусловных рефлексов.
Состояние новорожденного может значительно изменяться при внутриутробной задержке развития. Кроме того, при осмотре ребенка необходимо учитывать состояние окружающей обстановки: освещенность, шум, температуру воздуха в помещении и др. Для окончательной постановки диагноза проводится неоднократное обследование, так как неврологические симптомы, выявляемые в первый раз, могут исчезнуть при повторном осмотре, или, симптомы, расцененные в первый раз как легкие признаки нарушения ЦНС, в последующим могут стать более значимыми. Оценка неврологического статуса детей первого года жизни, в том числе и новорожденных, имеет ряд особенностей. Так, отмечается преобладание общих реакций вне зависимости от характера раздражающих факторов, а некоторые симптомы, расцениваемые у более старших детей и взрослых как безусловно патологические, у новорожденных и детей грудного возраста являются нормой, отражая степень зрелости определенных структур нервной системы и этапы функционального морфогенеза. Обследование начинают с визуального наблюдения за ребенком. Обращают внимание на положение головы, туловища, конечностей. Оценивают спонтанные движения рук и ног, определяют позу ребенка, анализируют объем активных и пассивных движений. У новорожденного ребенка руки и ноги находятся в постоянном движении. Спонтанная двигательная активность и крик усиливаются перед кормлением и ослабевают после него. Новорожденный хорошо сосет и глотает.
При церебральных нарушениях отмечается резкое снижение спонтанной двигательной активности. Резко снижены или отсутствуют сосательные и глотательные рефлексы. Низкоамплитудный высокочастотный тремор подбородка, ручек при крике или возбужденном состоянии новорожденного относится к физиологическим проявлениям. Новорожденный доношенный ребенок и младенец первых месяцев жизни удерживает преимущественно флексорную позу конечностей, т.е. тонус мышц в сгибателях конечностей преобладает над тонусом в разгибателях, причем тонус в руках выше, чем в ногах и он симметричен. Изменения мышечного тонуса проявляется мышечной гипотонией, дистонией, гипертонией.
Мышечная гипотония – один из наиболее часто обнаруживаемых синдромов у новорожденных детей. Она может быть выражена с рождения и носить диффузный или ограниченный характер в зависимости от характера патологического процесса. Встречается при: врожденных формах нервно-мышечных заболеваний, асфиксии, внутричерепной и спинальной родовой травме, поражении периферической нервной системы, хромосомных синдромах, наследственных нарушениях обмена веществ, а также у недоношенных. Поскольку мышечная гипотония часто сочетается с другими неврологическими нарушениями (судороги, гидроцефалия, парезы черепных нервов и др.), последние могут модифицировать характер задержки развития. Следует также отметить, что качество самого синдрома мышечной гипотонии и его влияние на задержку развития будут варьировать в зависимости от заболевания. Дети с пониженной возбудимостью, с синдромом гипотонуса вяло сосут, часто срыгивают.
Синдром мышечной гипертонии характеризуется увеличением сопротивления пассивным движениям, ограничением спонтанной и произвольной двигательной активности. При синдроме мышечной гипертонии следует приложить определенные усилия, чтобы раскрыть кулачки или разогнуть конечности. Причем дети достаточно часто реагируют на это плачем. Синдром гипертонуса встречается при: повышении внутричерепного давления, гнойном менингите, билиарной энцефалопатии, внутриутробной инфекции с поражением ЦНС, после внутричерепного кровоизлияния. У детей с гипертонусом часто возникают трудности с кормлением, так как некоординированы акты сосания и глотания. Отмечаются срыгивания и аэрофагии. Однако надо заметить, что физиологическая гипертония отмечается у детей первых месяцев жизни. Она возникает вследствие отсутствия угнетающего влияния пирамидной системы на спинномозговые рефлекторые дуги. Но, если по мере взросления грудного ребенка, отмечается нарастание мышечной гипертонии и появление односторонних симптомов, то это должно насторожить в плане возможного развития ДЦП. Синдром двигательных расстройств у новорожденных детей может сопровождаться мышечной дистонией (состояние сменяющихся тонусов – мышечная гипотония чередуется мышечной гипертонией). Дистония – проходящее повышение мышечного тонуса то в сгибателях, то в разгибателя. В покое у этих детей при пассивных движениях выражена общая мышечная дистония. При попытке выполнить какое-либо движение, при положительных или эмоциональных реакциях мышечный тонус резко нарастает. Такие состояния называются дистоническими атаками. Синдром легкой преходящей мышечной дистонии не оказывает существенного влияния на возрастное моторное развитие ребенка. Оценить состояние мышечного тонуса может только врач, педиатр и невропатолог, поэтому родители должны помнить, что своевременное обращение к врачу, динамическое наблюдение ребенка специалистами, в срок проведенные необходимые обследования, и выполнение назначений лечащего врача, способны предотвратить развитие каких-либо серьезных нарушений со стороны ЦНС. При оценке неврологического статуса у детей после исследования мышечного тонуса необходимо произвести осмотр головы, измерение ее окружности и сопоставления ее размеров с размерами груди.
Гидроцефалия характеризуется увеличением размеров головы, что связано с расширением желудочковых систем мозга и субарохноидальных пространств за счет избыточного количества цереброспинальной жидкости.
Макроцефалия – увеличение размеров головы, сопровождающееся увеличением массы и размеров головного мозга. Может быть врожденным пороком развития мозга, встречается у детей с фамакозами, болезнями накопления, может быть семейной особенностью. Микроцефалия- уменьшение размеров головы в следствие малых размеров мозга. Врожденная микроцефалия наблюдается при генетических заболеваниях, встречается при перенесенной внутриутробной нейроинфекции, алкогольной фетопатиии, пороках развития мозга и других заболеваниях.
Микрокрания – уменьшение размеров головы вследствие замедленного роста костей черепа и быстрой их оссификацией, с ранним закрытием швов и родничков. Нередко микрокрания является наследственно-конституциональной особенностью. Краниостеноз – врожденный порок развития черепа, который ведет к формированию неправильной формы головы с изменением ее размеров, характеризуется сращением швов, нарушение роста отдельных костей черепа. Краниостеноз обнаруживается уже на первом году жизни и проявляется различными деформациями черепа – башенный, ладьевидный, треугольный и т.д. Очень важно оценивать состояние родничков. При рождении определяется передний (большой) и задний (малый) роднички. Размеры родничка индивидуальны и колеблются от 1 до 3 см. Закрывается большой родничок, как правило, к 1,5 годам. Задержка закрытия родничка может быть связана с высоким внутричерепным давлением, особенностями онтогенеза черепа. Обращают внимание также на наличие гематом, отечности тканей головы, состояние подкожной венозной сети. Нередко у детей первых суток жизни при пальпации обнаруживается отек мягких тканей головы (родовая опухоль), который не ограничен одной костью и отражает физиологическую травму кожи и подкожной клетчатки в родах.
Кефалогематома – кровоизлияние под надкостницу, которое всегда расположено в пределах одной кости. Большие кефалогематомы удаляют, малые рассасываются сами.
Расширенная подкожная венозная сетка на голове свидетельствует о повышенном внутричерепном давлении как за счет ликворного компонента, так и за счет нарушений венозного оттока. Наличие или отсутствие выше перечисленных симптомов может оценить только врач (педиатр или невропатолог), после тщательного осмотра. В случае найденных им изменений, ребенку, возможно, будет назначено необходимое обследование (НСГ, ЭЭГ, доплероисследование сосудов головного мозга и др.), а также лечение. После общего осмотра новорожденного ребенка, оценки его сознания, двигательной активности, мышечного тонуса, состояние костей черепа и мягких тканей головы педиатр и невропатолог оценивают состояние черепно-мозговых нервов, безусловные и сухожильные рефлексы. О состоянии черепно-мозговых нервов у новорожденного можно судить по особенностям его мимики, крику, акту сосания и глотания, реакции на звук. Особое внимание уделяют органу зрения, так как внешние изменения глаз в ряде случаев позволяют заподозрить наличие врожденного или наследственного заболевания, гипоксического или травматического повреждения ЦНС. Врачи-специалисты (педиатр, невролог, офтальмолог) при оценке органа зрения обращают внимание на размеры и симметричность глазных щелей, состояние радужки, наличие кровоизлияния, на форму зрачка, наличие экзофтальма, нистагма, птоза и косоглазия. Состояние более глубоких структур глаза (хрусталика, стекловидного тела, сетчатки) может оценить только врач-офтальмолог. Поэтому, так важно, чтобы уже на первом месяце жизни ребенок был осмотрен не только педиатром и неврологом, но и врачом-офтальмологом.
Таким образом, чтобы вовремя диагностировать и в дальнейшем предотвратить серьезные нарушения со стороны центральной нервной системы, родителями должны соблюдаться ряд правил:
- Обязательная диспансеризация – это консультации педиатра (в течение первого месяца жизни 4 раза в месяц), далее ежемесячно и регулярные осмотры невролога: в 1 месяц, 3 месяца и в год; если возникает в том необходимость, то чаще. Консультации офтальмолога в 1 месяц, 3 месяца и в 1 год, если возникает в том необходимость, то чаще. Проведение скрининг исследования центральной нервной системы (нейросонографии) и проведение других исследований, если есть к этому показания. Неукоснительное соблюдение назначений врачей, наблюдающих ребенка.
- Рациональное вскармливание.
- Соблюдение санитарно-гигиенического режима.
- Физическое воспитание (массаж, гимнастика, закаливание).
причины, симптомы, лечение в Москве – Консультация и обследование при энцефалопатии – Неврология в Клинике № 1
Обследование и лечение
Дисциркуляторная энцефалопатия – неврологическое заболевание с медленным прогрессированием. Оно характеризуется недостатком кровоснабжения сосудов головного мозга. В результате его функции нарушаются в области пораженных очагов. Болезнь встречается как у пожилых, так и у молодых пациентов. Чем раньше будет начато лечение, тем выше шансы на полное восстановление.
Пройдите диагностику дискуляторной энцефалопатии в Клинике №1:
- МРТ
- Консультация офтальмолога
- ЭЭГ, РЭГ
- УЗД сосудов
- Дуплексное сканирование
При единовременной оплате услуг – скидка 20%
Позвонить
Причины развития заболевания
Ткани мозга в очень высокой степени зависят от поступления в них кислорода. Без постоянного кровоснабжения клетки погибают не позднее чем через шесть минут после прекращения питания. Основными причинами дисциркуляторной энцефалопатии являются:
- Атеросклероз.
- Скачки давления при гипертонической болезни, поликистозе почек, гламерулонефрите, болезни Кушинга.
- Шейный остеохондроз.
- Травмы шеи.
- Пороки развития артерий.
- Вегетососудистая дистония.
- Диабет.
- Аритмия.
- Воспалительные процессы в сосудах.
- Вредные привычки.
- Заболевания эндокринной системы.
- Тромбы в церебральных артериях.
- Частые стрессы.
Симптомы и стадии развития
Симптомы заболевания различаются в зависимости от степени поражения:
- При первой степени ДЭП появляется тревога, ранимость, раздражительность, частая смена настроения. Больной быстро утомляется, периодически жалуется на головную боль. Память ухудшается, наблюдается усталость после физических нагрузок. Может проявляться неустойчивость, неуверенная походка, тошнота.
- Вторая стадия характеризуется более серьезными признаками, появляются явные когнитивные нарушения, двигательные расстройства. Головная боль становится частой, больной ощущает шум в голове, вялость, плохо спит. Могут быть трудности с глотанием, нарушается координация, речь, слух, появляется тремор головы и рук, судороги. Могут возникать вспышки света перед глазами.
- Третья степень сопровождается серьезным нарушением координации и по сути является сосудистой деменцией. Зрение, слух и речь нарушаются, поведение больного неадекватное. Наблюдается шаркающая походка, постоянный тремор головы и рук, недержание кала и мочи, судороги.
Виды заболевания
Виды дисциркуляторной энцефалопатии разделяются в зависимости от причин ее возникновения:
- Гипертоническая.
- Венозная.
- Атеросклеротическая.
- Смешанная.
К какому врачу обратиться?
Дисциркуляторная энцефалопатия относится к неврологическим нарушениям. При появлении тревожных симптомов необходимо как можно скорее обратиться к врачу неврологу. Специалист проведет обследование, поставит точный диагноз и назначит адекватное лечение. Чем раньше будет оказана помощь – тем более оптимистичный прогноз для пациента
Пройдите диагностику дискуляторной энцефалопатии в Клинике №1:
- МРТ
- Консультация офтальмолога
- ЭЭГ, РЭГ
- УЗД сосудов
- Дуплексное сканирование
При единовременной оплате услуг – скидка 20%
Позвонить
Диагностика
Своевременная точная постановка диагноза крайне важна для проведения сосудистой терапии и восстановления нормального кровоснабжения мозга. Выявить заболевания на ранней стадии поможет посещение плановых осмотров у невролога. Особенно пациентам старшего возраста это необходимо делать регулярно. Также профилактические осмотры показаны пациентам из группы риска: гипертоникам, диабетикам, больным, страдающим атеросклерозом. Выявить когнитивные нарушения, которые поначалу незаметны для окружающих и самого пациента, позволяют специальные тесты. Невролог может попросить пациента нарисовать циферблат, повторить слова, произнесенные ранее.
Также для постановки диагноза используются:
- МРТ (позволяет выявить очаги немых инфарктов – наиболее достоверный признак ДЭП).
- Консультация офтальмолога.
- ЭЭГ, РЭГ.
- Ультразвуковая диагностика сосудов.
- Дуплексное сканирование.
Лечение
При лечении патологии применяется комплексная этиопатогенетическая терапия. Она направлена на компенсацию заболевания, нормализацию циркуляции крови, защиту нервных клеток от кислородного голодания и ишемии. Применяются препараты для снижения уровня сахара в крови, нормализации давления, холестерина. Корректируется питание, пациенту назначается специальная диета.
Операция может быть назначена в том случае, когда патология вызвана сужением просвета артерии, прогрессирует быстро и сопровождается серьезными осложнениями.
В качестве меры профилактики используется нормализация липидного обмена. Нарушение этого процесса влечет отложения на внутренней поверхности сосудов, которые сужают просвет и мешают нормальной циркуляции крови. Также важна борьба с атеросклерозом, поддержание нормального уровня сахара у пациентов с сахарным диабетом.
Записаться на консультацию к неврологу
Пройти грамотную консультацию невролога предлагает «Клиника №1» в Москве. Многопрофильный медицинский центр расположен в непосредственной близости от станции метро Люблино. Клиника располагает всеми современными техническими возможности для успешной диагностики и лечения множества заболеваний. Записаться на прием можно по телефону или через наш сайт.
г. Москва, ул. Краснодарская, дом. 52, корп. 2
+7 (495) 152-33-19
Работаем в будние дни и выходные с 8.00 до 21.00
Цены на консультацию и прием врача невролога
|
Название услуги |
Стоимость |
|
Бесплатная консультация врача после МРТ/КТ |
0,00 |
|
Первичный прием невролога (консультация) |
1270,00 |
|
Повторная консультация невролога |
810,00 |
|
Вызов врача на дом |
5180,00 |
Перинатальная энцефалопатия (ПЭП)
Перинатальная энцефалопатия – различные поражения центральной нервной системы, возникшие в период внутриутробного развития, во время родов или в раннем неонатальном периоде. Перинатальная энцефалопатия может заявлять о себе синдромом угнетения или гипервозбудимости ЦНС, двигательными нарушениями, гипертензионно-гидроцефальным, судорожным, вегето-висцеральным синдромом, задержкой темпов моторного, психического и речевого развития. Диагностика перинатальной энцефалопатии включает нейросонографию, допплерографию, МРТ и КТ головного мозга, ЭЭГ. Лечение перинатальной энцефалопатии предполагает проведение посиндромной медикаментозной терапии, повторных курсов массажа, ЛФК, логопедической коррекции.
Перинатальная энцефалопатия (ПЭП) – мозговая дисфункция, вызванная гипоксическим, травматическим, инфекционным, токсико-метаболическим воздействием на ЦНС плода и новорожденного. Использование собирательного термина «перинатальная энцефалопатия» в детской неврологии и педиатрии обусловлено схожестью клинической картины, развивающейся при различных механизмах повреждения головного мозга. Поэтому, строго говоря, формулировка «перинатальная энцефалопатия» не является диагнозом и требует дальнейшего синдромологического анализа. В структуре патологии нервной системы детского возраста перинатальная энцефалопатия составляет более 60%. Последствия перинатальной энцефалопатии у детей могут варьировать от минимальной мозговой дисфункции и вегето-сосудистой дистонии до гидроцефалии, ДЦП и эпилепсии.
Причины перинатальной энцефалопатии
Ведущей причиной повреждения головного мозга плода и новорожденного в перинатальном периоде выступает внутриутробная гипоксия. Т. о., перинатальная энцефалопатия может являться следствием отягощенного соматического анамнеза беременной (пороки сердца, сахарный диабет, пиелонефрит, бронхиальная астма, гипертоническая болезнь и др.), неблагополучного протекания беременности (угроза выкидыша, внутриутробные инфекции, гемолитическая болезнь плода, гестоз, фетоплацентарная недостаточность) и родов (узкий таз, преждевременные роды, затяжные или стремительные роды, слабость родовой деятельности и пр.). Повреждающее действие на плод могут оказывать вредные привычки беременной (курение, употребление алкоголя и наркотических веществ), прием потенциально опасных для плода лекарственных препаратов, профессиональные вредности, экологическое неблагополучие.
Кроме этого, перинатальная гипоксическая энцефалопатия может развиваться и в первые дни после рождения, например, при синдроме дыхательных расстройств, врожденных пороках сердца, сепсисе новорожденных и т. д.
Независимо от непосредственной причины, во всех случаях гипоксического поражения ЦНС пусковым механизмом служит недостаток кислорода. Другие дисметаболические нарушения (ацидоз, гипогликемия, гипо-/гипернатриемия, гипо-/гипермагниемия, гипокальциемия) обычно возникают вслед за гипоксическим поражением ЦНС.
Внутричерепные родовые травмы, как причина перинатальной энцефалопатии, главным образом связаны с механическим воздействием — использованием травмирующих плод акушерских пособий, родами в тазовом предлежании, неправильным вставлением головки, тракцией за головку и т. д.
Классификация перинатальной энцефалопатии
В течении перинатальной энцефалопатии выделяют острый период (первый месяц жизни), ранний восстановительный (до 4-6 месяцев) и поздний восстановительный периоды (до 1-2-х лет) и период остаточных явлений.
К основным клиническим синдромам перинатальной энцефалопатии относятся синдром двигательных расстройств, синдром повышенной нервно-рефлекторной возбудимости (синдром гипервозбудимости), синдром угнетения ЦНС, гипертензионно-гидроцефальный синдром, судорожный синдром, вегето-висцеральный синдром.
При определении степени тяжести перинатальной энцефалопатии учитывается оценка состояния новорожденного по шкале АПГАР:
легкая степень — 6 — 7 баллов. Проявлением легкой формы перинатальной энцефалопатии служит синдром повышенной нервно-рефлекторной возбудимости. Недоношенные дети с легкой формой перинатальной энцефалопатии составляют группу повышенного риска по развитию судорожного синдрома.
среднетяжелая степень — 4 — 6 баллов. Перинатальная энцефалопатия обычно протекает с синдромом угнетения ЦНС и гипертензионно-гидроцефальным синдромом.
тяжелая степень – 1-4 балла. Тяжелая форма перинатальной энцефалопатии характеризуется прекоматозным или коматозным состоянием.
Симптомы перинатальной энцефалопатии
Ранние признаки перинатальной энцефалопатии могут быть выявлены неонатологом сразу после рождения ребенка. К ним относятся слабый или поздний крик новорожденного, длительный цианоз, отсутствие сосательного рефлекса, изменения двигательной активности и др.
Клиника легкой формы перинатальной энцефалопатии включает повышенную спонтанную двигательную активность новорожденного, трудности засыпания, поверхностный беспокойный сон, частый плач, мышечную дистонию, тремор подбородка и конечностей. Перечисленные нарушения обычно обратимы и регрессируют в течение первого месяца жизни.
Синдром угнетения ЦНС при среднетяжелой форме перинатальной энцефалопатии протекает с вялостью, гипорефлексией, гиподинамией, диффузной мышечной гипотонией. Типично наличие очаговых неврологических расстройств: анизокории, птоза, сходящегося косоглазия, нистагма, нарушения сосания и глотания, асимметрии носогубных складок, асимметрии сухожильно-надкостничных рефлексов. Гипертензионно-гидроцефальный синдром характеризуется напряжением и выбуханием большого родничка, расхождением швов, увеличением окружности головы, нарушением сна, пронзительными вскрикиваниями. Неврологические расстройства при среднетяжелой перинатальной энцефалопатии частично регрессируют к позднему восстановительному периоду.
Тяжелая степень перинатальной энцефалопатии сопровождается адинамией, мышечной гипотонией вплоть до атонии, отсутствием врожденных рефлексов, реакции на болевые раздражители, горизонтальным и вертикальным нистагмом, аритмичным дыханием и пульсом, брадикардией, артериальной гипотонией, приступами судорог. Тяжелое состояние ребенка может сохраняться от нескольких недель до 2-х месяцев. Исходом тяжелой перинатальной энцефалопатии, как правило, является та или иная форма неврологической патологии.
В раннем и позднем восстановительном периодах перинатальной энцефалопатии встречаются синдромы: церебрастенический (астеноневротический), двигательных нарушений, судорожный, вегегативно-висцеральный, гипертензионно-гидроцефальный.
Синдром двигательных нарушений может проявляться мышечным гипо-, гипертонусом или дистонией, гиперкинезами, парезами и параличами. Астеноневротическому синдрому соответствуют нарушения сна, эмоциональная лабильность, двигательное беспокойство ребенка.
Судорожный синдром в восстановительном периоде перинатальной энцефалопатии может выражаться не только непосредственно судорогами, но и мелкоамплитудным дрожанием, автоматическими жевательными движениями, кратковременной остановкой дыхания, спазмом глазных яблок и т. д.
Вегето-висцеральная дисфункция при перинатальной энцефалопатии проявляется микроциркуляторными нарушениями (бледностью и мраморностью кожных покровов, преходящим акроцианозом, холодными конечностями), желудочно-кишечными дискинезиями (срыгиванием, диспепсией, кишечными коликами и др.), лабильностью сердечно-сосудистой системы (тахикардией, брадикардией, аритмией) и т. д.
Исходом перинатальной энцефалопатии у детей может являться выздоровление, темповая задержка развития (ЗПР, ЗРР), минимальная мозговая дисфункция, синдром дефицита внимания и гиперактивности (СДВГ), грубые органические поражения ЦНС (ДЦП, эпилепсия, олигофрения, прогрессирующая гидроцефалия).
Диагностика перинатальной энцефалопатии
Признаки перинатальной энцефалопатии обычно выявляются при осмотре и объективном обследовании ребенка педиатром или детским неврологом. При этом важно учитывать данные о течении беременности, родов, состоянии ребенка сразу после рождения. Однако для определения характера поражения головного мозга и оценки степени тяжести перинатальной энцефалопатии требуется проведение дополнительных лабораторных и инструментальных исследований.
В целях изучения показателей метаболизма проводится определение КОС и газового состава крови, уровня глюкозы, электролитов, анализ состава спинномозговой жидкости.
Самую первую диагностическую информацию, позволяющую косвенным образом судить о наличии перинатальной энцефалопатии, получают с помощью ультразвукового исследования анатомических структур мозга — нейросонографии через большой родничок.
Для уточнения гипоксически-ишемических изменений мозговой ткани, обнаруженных при НСГ, проводится КТ или МРТ головного мозга ребенку. С целью оценки кровоснабжения головного мозга выполняется допплерография сосудов шеи ребенку и дуплексное сканирование артерий головы. ЭЭГ ребенку представляет наибольшую ценность в диагностике перинатальной энцефалопатии, протекающей с судорожным синдромом. При необходимости обследование ребенка может дополняться ЭхоЭГ, РЭГ, электронейромиографией, рентгенографией шейного отдела позвоночника.
Ребенку с перинатальной энцефалопатией необходима консультация окулиста с исследованием глазного дна. При задержке психического и речевого развития показана консультация детского психолога и логопеда.
Лечение перинатальной энцефалопатии
В остром периоде лечение ребенка с перинатальной энцефалопатией осуществляется в отделении патологии новорожденных. Ребенку показан щадящий режим, оксигенотерапия, при необходимости – зондовое питание.
Медикаментозная терапия назначается с учетом преобладающих синдромов перинатальной энцефалопатии. Для уменьшения внутричерепной гипертензии проводится дегидратационная терапия (маннитол), вводятся кортикостероиды (преднизолон, дексаметазон и др.), выполняются лечебные спинномозговые пункции.
С целью нормализации метаболизма нервной ткани и повышения ее устойчивости к гипоксии осуществляется инфузионная терапия – введение растворов глюкозы, калия, кальция, аскорбиновой кислоты, препаратов магния и т. д. Для борьбы с судорогами используется фенобарбитал, диазепам и др. В рамках терапии перинатальной энцефалопатии показано назначение препаратов, улучшающих кровообращение и метаболизм головного мозга (винпоцетина, пирацетама, кортексина, депротеинизированного гемодеривата крови телят и др.).
В восстановительном периоде лечение ребенка с перинатальной энцефалопатией, как правило, осуществляется амбулаторно или в условиях дневного стационара. Проводятся повторные курсы лекарственной терапии ноотропными препаратами и ангиопротекторами, лечебная физкультура, плавание, массаж, физиопроцедуры (амплипульстерапия, электрофорез), гомеопатическая терапии, фитотерапия, остеопатия.
При нарушениях речи — ЗРР, синдромах алалии и дизартрии показаны коррекционные логопедические занятия.
Профилактика перинатальной энцефалопатии
Полное выздоровление, как исход легкой степени перинатальной энцефалопатии наступает у 20-30 % детей. В остальных случаях в резидуальном периоде развиваются те или иные неврологические синдромы. Серьезность последствий зависит от характера и тяжести повреждения, своевременности и полноты оказания лечебной помощи. Высокая пластичность ЦНС у детей обусловливает большой резерв для восстановления нарушенных функций в первые месяцы жизни, поэтому крайне важно начать лечение как можно раньше даже при минимальных проявлениях перинатальной энцефалопатии.
Профилактика перинатальной энцефалопатии включает минимизацию факторов риска при беременности и родоразрешении. Основной задачей будущей мамы и акушеров-гинекологов на этапе ведения беременности служит предупреждение внутриутробной гипоксии, что может быть достигнуто терапией хронических заболеваний, коррекцией патологического течения беременности. Во время родов необходимо проводить профилактику интранатального травматизма плода.
Источник: http://www.krasotaimedicina.ru/diseases/children/perinatal-encephalopathy
ГИЭ — гипоксическая ишемическая энцефалопатия
Перинатальная гипоксически-ишемическая энцефалопатия (ГИЭ) — один из наиболее серьезных и опасных для жизни типов повреждения головного мозга младенцев, которое может возникнуть во время родов. ГИЭ возникает, когда поступление кислорода и крови в мозг ребенка ограничено или прервано во время родов (перинатальная асфиксия), что приводит к гибели клеток мозга через короткие промежутки времени.
Что такое гипоксическая ишемическая энцефалопатия (ГИЭ)?
ГИЭ — это очень серьезный тип повреждения мозга младенца, который возникает во время родов, когда мозг ребенка лишен крови и кислорода.Из-за недостатка крови и кислорода клетки головного мозга ребенка умирают в считанные минуты.
Энцефалопатия — это медицинское слово, которое используется для обозначения различных родственных состояний, возникающих в результате травмы головного мозга. Гипоксическая ишемическая энцефалопатия (ГИЭ) — это особый тип повреждения головного мозга, вызванный комбинацией (1) гипоксии — нарушения циркуляции кислорода; и (2) ишемия — ограничение кровотока. Перинатальный ГИЭ возникает, когда кровь и кислород, поступающие в мозг, одновременно снижаются или прекращаются во время родов или сразу после них.ГИЭ — относительно редкое событие, которое происходит примерно у 3 из 1000 рождений.
Что вызывает гипоксическую ишемическую энцефалопатию (ГИЭ)?
ГИЭ вызывается острой потерей притока крови и кислорода к мозгу ребенка во время родов или во время беременности. Недостаток кислорода и крови приводит к тому, что клетки развивающегося мозга ребенка быстро разлагаются, а затем умирают. Кислородная недостаточность, вызывающая ГИЭ, обычно вызвана акушерскими осложнениями во время родов и родоразрешения, но также может быть результатом пренатальных осложнений или событий.Осложнения, которые могут вызвать ГИЭ, включают:
Роды и Осложнения при родах:
Осложнения новорожденных:
Последствия ГИЭ
ГИЭ — чрезвычайно серьезный тип черепно-мозговой травмы. Несмотря на то, что это происходит менее чем в 0,05% всех рождений, ГИЭ является одной из ведущих причин младенческой смертности в США каждый год.
Помимо опасности для жизни, ГИЭ вызывает необратимое повреждение головного мозга. Примерно 15-20% новорожденных с диагнозом ГИЭ умрут в первую неделю.Из оставшихся выживших 25% получат необратимые повреждения головного мозга различной степени тяжести. Повреждения головного мозга в результате ГИЭ часто приводят к физическим недостаткам и когнитивным нарушениям.
У меньшего процента детей с ГИЭ хорошие результаты. Эти дети полностью выздоравливают и испытывают лишь легкие симптомы неврологической травмы, если таковые имеются. Нет данных о продолжительности жизни 80-85% детей с ГИЭ, как выживают в первую неделю жизни. Но очевидно, что в тяжелых случаях это влияет на прогнозируемую продолжительность жизни.
Симптомы ГИЭ
Симптомы ГИЭ сразу после рождения будут существенно различаться, в основном, в зависимости от тяжести основного повреждения головного мозга:
Легкая ГИЭ
- Сухожильные рефлексы ненормальны, а мышцы жесткие в первые несколько дней
- Сильная раздражительность, проблемы с кормлением, чрезмерный плач или сон
- Симптомы легкой ГИЭ часто проходят в течение нескольких недель
Умеренная ГИЭ
- Отсутствие мышечного тонуса (синдром гибкого ребенка) с отсутствием рефлексов
- Невозможно схватка и плохой сосательный рефлекс
- Спорадическое апноэ
- Припадки (обычно в течение первого дня)
Тяжелая ГИЭ
- Экстремальные приступы, которые учащаются в первые 2 дня
- Не реагируют на внешние раздражители
- Нерегулярное дыхание
- Крайняя гипотония (как тряпичная кукла)
- Abn нормальный контроль глаз или движение с расширенными зрачками
- Аномальная частота сердечных сокращений и артериальное давление
- Кардиореспираторная недостаточность (часто со смертельным исходом)
Лечение ГИЭ
Основным лечением ГИЭ, которое набирает обороты в последние годы, является охлаждение тела и головы.Это лечение обычно называют терапевтическим переохлаждением. Лечебная гипотермия направлена на снижение температуры тела ребенка ниже нормы сразу после рождения. Это эффективно замедляет процессы распада и повреждения клеток в головном мозге. Замедляя этот процесс, терапия гипотермии направлена на минимизацию долгосрочного воздействия ГИЭ. К сожалению, повреждение мозга от гипоксии новорожденного носит постоянный характер и не может быть просто исправлено хирургическим вмешательством или лекарствами. Итак, ОТО — это постоянная травма.Варианты лечения включают терапию и лекарства, которые помогают справиться с последствиями любого повреждения головного мозга. Младенцы с тяжелыми травмами ГИЭ часто нуждаются в пожизненной поддержке и приспособлении.
Но есть и удивительные истории выздоровления от ГИЭ, когда ребенок получил необратимую травму с фантастическим исходом. Истории успеха после HIE не редкость. В конце концов, масштабы травмы ребенка, а это не утешение для родителей, часто не до конца понимают, пока ребенок не станет намного старше.
Scientific Sources
Yıldız, et al. «Неонатальная гипоксическая ишемическая энцефалопатия: обновленная информация о патогенезе заболевания и лечении». Экспертный обзор нейротерапии 17.5 (2017): 449-459.
Моллой, Элеонора Дж. И Синтия Биэр. «Неонатальная энцефалопатия против гипоксически-ишемической энцефалопатии». (2018): 574-574.
Finder, Mikael, et al. «Двухлетние исходы развития нервной системы после легкой гипоксической ишемической энцефалопатии в эпоху терапевтического гипотермии.» JAMA pediatrics 174.1 (2020): 48-55.
Greco, P., et al.» Патофизиология гипоксически-ишемической энцефалопатии: обзор прошлого и взгляд в будущее «. Acta Neurologica Belgica 120.2 (2020): 277-288.
Frontiers | Неонатальная энцефалопатия: необходимость распознавания множественных этиологий для оптимального ведения
Введение
Неонатальная энцефалопатия (NE) — сложное заболевание новорожденного, характеризующееся изменением уровня сознания, судорогами, плохим тонусом, неспособностью инициировать или поддерживать дыхание (1) и связано с полиорганной дисфункцией (2).Заболеваемость NE оценивается в 3 случая на 1000 живорождений (3). NE может быть результатом широкого спектра причин и является клиническим термином, не определяющим этиологию. Единственное доступное лечение — это терапевтическая гипотермия (ТГ) с максимальной пользой, если начать в первые 6 часов жизни (4). Существует несколько причин НЭ, таких как гипоксическая ишемическая энцефалопатия (ГИЭ), перинатальные инфекции, аномалии плаценты, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных (рис. 1). Однако более чем в половине случаев причина НЭ остается неустановленной (5).
Рисунок 1 . Многофакторная этиология неонатальной энцефалопатии. Многие факторы предрасполагают к возникновению неонатальной энцефалопатии по отдельности или в комбинации, включая (A) Факторы риска до зачатия, (B) Сопутствующие заболевания или события у матери до родов / во время родов, (C) Патология плаценты, (D) Гипоксия-ишемия, (E) Перинатальная инфекция, (F) Неонатальный инсульт или тромбофилия, (G) Метаболические нарушения и (H) Генетические и эпигенетические аномалии.ПРОМ, длительный разрыв плодных оболочек; ЗВУР, ограничение внутриутробного развития.
Использование термина NE vs. HIE противоречиво. Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных событий (6, 7). Трудно доказать наличие гипоксической ишемии головного мозга, за исключением моделей на животных и частных случаев неонатального инсульта. Все текущие параметры, включая pH и судороги, неспецифичны (7). Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE (7).Несколько опубликованных популяционных исследований показали, что факторы риска до родов и неасфиксии связаны с НЭ (6). Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ (1). Поэтому в этом обзоре мы использовали термин NE, и мы стремились изучить различные этиологии, связанные с NE.
Материнские факторы
Материнская гипертензия (16%) была важным фактором дородового риска НЭ в реестре неонатальной энцефалопатии Оксфордской сети штата Вермонт ( n = 4 165).Также была более высокая частота клинического хориоамнионита, длительного разрыва плодных оболочек и гипотиреоза матери. Хотя острый асфиксический эпизод был зарегистрирован в 15% случаев, связь с воспалением была обнаружена у 24% (5).
Популяционное исследование в Западной Австралии показало, что социально-экономический статус, семейный анамнез судорог, неврологические проблемы и зачатие после лечения бесплодия были независимыми факторами риска до зачатия для NE ( n = 164) (8).Заболевание щитовидной железы матери, кровотечение во время беременности, вирусные заболевания, преэклампсия, аномальная плацента, задержка внутриутробного развития и переношенность были другими важными факторами риска в дородовой период (8). Идентифицируемые дородовые факторы риска НЭ были обнаружены в 69% случаев, внутриродовые факторы риска — в 5%, как дородовые, так и во время родов — в 24% и отсутствие фактора риска — в 2%. Только в 4% случаев внутриродовая гипоксия была выявлена без каких-либо факторов риска до родов или до зачатия (9). Было обнаружено, что ограничение роста в развитых странах и беременность двойней в развивающихся странах связаны с НЭ.Заболевание щитовидной железы у матери, дородовое наблюдение, инфекция, роды и тактика ведения родов должны быть важными модификаторами в исследовании 27 новорожденных с NE и 100 контрольных детей (3). Дородовые (74 против 18%), внутриродовые (67 против 19%) и острые внутриродовые события (33 против 2%) более вероятны у младенцев с НЭ по сравнению с контрольной группой. Следовательно, в неонатальном клиническом анамнезе подробный материнский анамнез важен и может быть путем к профилактическим стратегиям в будущем.
Из 45 новорожденных с NE 36% имели дозорное событие, 40% имели хориоамнионит и 11% имели оба этих симптома.Если данные о дозорных событиях были исключены, то возраст матери> 35 лет (ОР 2,5; 95% ДИ 1,1–5,6) и инфекция мочевыводящих путей во время беременности (ОР 2,6; 95% ДИ 1,0–6,5) были потенциальными дородовыми факторами риска NE (10).
Гипоксия-ишемия
Хотя концепция гипоксии-ишемии четко обозначена в моделях на животных, она может не подходить для использования во всех случаях неонатальной NE у человека. «Дозу» и продолжительность гипоксии, а также степень ишемии можно непосредственно измерить на животной модели.Однако у новорожденных людей это неизвестно, если нет контрольного события и впоследствии используются суррогатные маркеры гипоксии. Badawi et al. показали, что асфиксия во время родов считается сопутствующим фактором в 29% случаев НЭ и самостоятельным фактором только в 4% случаев (9). Было обнаружено, что внутриродовая гипоксия-ишемия является одним из факторов, способствующих развитию НЭ в 30% случаев в развитых и 60% в развивающихся странах (3). Американский колледж акушеров и Американская академия педиатрии определили дозорное событие в своем документе о неонатальной энцефалопатии и неврологическом исходе (Obstet Gynecol 2014).Следующее соответствует острому пери- или интранатальному событию: дозорное гипоксическое или ишемическое событие, возникающее непосредственно перед или во время родов и родоразрешения, например разрыв матки или тяжелая отслойка плаценты; паттерны пульсометра плода, соответствующие острым послеродовым или интранатальным событиям; время и тип паттернов черепно-мозговых травм, основанные на исследованиях изображений, согласующихся с этиологией острого послеродового или внутриродового события, и отсутствуют доказательства других проксимальных или дистальных факторов, которые могли бы быть способствующими факторами.Кроме того, сочетание низких баллов по шкале Апгарса, ацидемии, аномального кардиотокографа, изменений МРТ, согласующихся с гипоксией-ишемией и полиорганной дисфункцией, — все это связано с гипоксически-ишемической этиологией, но в равной степени может быть изменено сепсисом или другими причинами NE. Асфиксичные родовые явления и воспаление присутствовали только в 12,6% случаев церебрального паралича (11). У новорожденных с NE ( n = 405) следующие независимо были связаны с NE ( p -значение = 0,001), включая: только 1 дородовой период (гестационный возраст> 41 недели) и 7 внутриродовых факторов, включая длительный разрыв плодных оболочек, аномальные кардиотокограф, густой меконий, дозорные события, дистоция плеча, тугая затылочная пуповина и отказ вакуума (12).В когорте из 26 новорожденных с дозорными событиями NE (ОР 74,9, 95% ДИ 11,9-бесконечность, p <0,001) и отслеживание ЧСС плода категории 3 (28,0% против 4,0%, p = 0,002) были сильно выражены. связанный с NE (13). В когорте из 45 новорожденных у 36% были дозорные события, а у 11% были как дозорные события, так и хориоамнионит (10).
Нейровизуализация с использованием магнитно-резонансной томографии, традиционной, диффузионной и спектроскопии от 24 до 96 часов жизни дает полезные рекомендации относительно возможных сроков церебрального инсульта, особенно диффузных аномалий.Аномалии, вызванные травмой головного мозга, становятся наиболее очевидными через 7 дней при использовании качественной МРТ, диффузии и спектроскопии. Глубокое ядерное серое вещество или водораздел кортикального повреждения развиваются по четко определенному типу повреждения мозга и типичны для гипоксически-ишемического повреждения мозга у новорожденного. Генетические и метаболические причины могут быть исследованы, если на МРТ существует другая картина травмы головного мозга или эволюция травмы. Признаки того, что послеродовая гипоксия-ишемия не была причиной НЭ, предлагаются на МРТ: порэнцефалия, очаговый артериальный инфаркт, венозный инфаркт, изолированное внутрипаренхиматозное или внутрижелудочковое кровоизлияние или атипичные паттерны метаболических энцефалопатий.
При NE, связанном с острым дозорным событием (HIE), типичная картина повреждения на МРТ показала вовлечение базальных ганглиев, таламуса с ассоциированной задней конечностью внутренней капсулы и, в тяжелых случаях, вовлечение ствола мозга (14). При NE без задокументированного дозорного события вовлечение базальных ганглиев или таламуса (BGT) также связано с изменениями белого вещества в 50% случаев (14). BGT с обширным повреждением белого вещества (WM) был обнаружен в 14%, BGT с WM от легкой до умеренной — в 56%, изолированное таламическое повреждение — в 5%, умеренное повреждение WM — только у 2% и легкое WM или нормальное — у 23% в 48%. младенцы с ГИЭ.Внутренняя капсула была аномальной у 93% пациентов с умеренным и тяжелым повреждением WM и была связана со смертью и ХП у 86% пациентов (15).
Характер повреждения головного мозга может указывать на возможную причину, например, повреждение коркового вещества и белого вещества (очаговое / мультифокальное) может быть связано с плацентарной недостаточностью и хориоамнионитом. Ранняя категоризация пациентов в соответствии с типом травмы головного мозга может привести к другому терапевтическому подходу, поскольку на животных моделях было показано, что разные уровни гипотермии защищают от повреждения коры головного мозга или глубокого серого вещества, поэтому для получения максимальной пользы могут потребоваться специфические для пациента протоколы гипотермии.Точно так же в моделях на животных разные режимы охлаждения, системное и селективное, приводят к разной температуре мозга (16).
Трудно окончательно установить наличие, продолжительность и степень гипоксии и ишемии у новорожденных, поэтому использовались суррогатные маркеры, такие как pH и судороги (7). Следовательно, биомаркеры мультиорганного поражения могут быть полезны для диагностики или оценки тяжести гипоксической ишемии и прогнозирования исхода при NE. Сердечный тропонин является маркером ишемии миокарда у новорожденных и детей и высвобождается из миоцитов после повреждения их мембраны.Сердечный тропонин I (cTnI) был значительно выше у новорожденных с ГИЭ в первые 48 часов по сравнению с контрольной группой ( p <0,0005) (17). Сердечный TnI был повышен у новорожденных с более высокой степенью НЭ и у тех, кому потребовались инотропы (18). Пороговое значение <0,22 нг / мл для нормотермических и <0,15 нг / мл для гипотермических младенцев с NE предсказывало нормальный исход развития нервной системы (19).
Гипоксия приводит к усилению эритропоэза и выбросу незрелых ядерных эритроцитов (nRBC) в кровоток (20).ЯРБК пуповинной крови были значительно выше у новорожденных, подвергшихся асфиксии, по сравнению с контрольной группой, а также коррелировали с апгаром через 1 мин, pH и развитием NE (20). Количество ядерных эритроцитов на 100 лейкоцитов было выше у новорожденных с НЭ по сравнению с контрольной группой, младенцев с НЭ средней / тяжелой и легкой степени ( p = 0,016) и у новорожденных с плохим исходом нервного развития ( p = 0,03) ( 21). Следовательно, стандартизованное измерение воздействия клинической гипоксии было бы полезным с использованием комбинации этих маркеров и могло бы помочь в определении времени инсульта и корреляции с доклиническими моделями на животных.
Инфекция
Риск спастического церебрального паралича (ДЦП) и квадриплегического ДЦП повышался при сочетании инфекции и асфиксии (22). Уровни интерлейкина (ИЛ) -6 через 6 часов связаны с отклонениями от нормы неврологического обследования (23). NE, инотропная поддержка, судороги без менингита, потребность в интубации и более низкий 5-минутный апгар были более вероятны у новорожденных с ХП при наличии инфекции у матери по сравнению с ХП без инфекции (22).
Инфекции матери и новорожденные с ранним началом представляют собой диагностическую проблему.Ведутся споры о том, может ли скрытая инфекция, не обнаруживаемая обычными методами культивирования, быть связана с неврологическим повреждением во всех возрастных группах. Полимеразная цепная реакция (ПЦР) выявила 11 случаев бактериемии у энцефалопатических новорожденных в Африке, у которых был отрицательный посев крови (NE n = 201). ПЦР в сочетании с посевом крови привела к обнаружению бактериальных продуктов в 8,9% случаев НЭ по сравнению с 3,1% при использовании одного посева крови (24). В метаанализе стрептококк группы B (GBS) был связан с NE в 0.58% случаев и смертность были выше при использовании СГБ плюс НЭ по сравнению с одним НЭ (25). В когорте из 45 новорожденных 40% имели хориоамнионит и 11% имели как дозорные события, так и хориоамнионит (10).
Терапевтическая гипотермия задерживает рост и пик ответа с-реактивного белка (СРБ), а также приводит к снижению количества лейкоцитов и нейтрофилов по сравнению с нормотермными новорожденными (26). Это влияние гипотермии на задержку развития естественных воспалительных маркеров следует учитывать при выборе лечения антибиотиками и продолжительности лечения новорожденных с НЭ.
Следовательно, полное обследование на сепсис имеет важное значение у всех детей с НЭ. Стандартных рекомендаций по выполнению люмбальной пункции во всех случаях НЭ не существует, и их можно выбирать в каждом конкретном случае. Кандидатами могут быть младенцы с повышенным WCC и CRP или факторами риска септического риска. Существуют также технические и практические проблемы для поясничной пункции у младенцев с НЭ, которые являются ригидными из-за ТГ, а также часто изначально имеют отек головного мозга при УЗИ черепа.
Аномалии плаценты
Поражение пуповины, хориоамнионит, васкулит плода, меконий хориональной пластинки и тромботическая васкулопатия плода часто встречались в плацентарных поражениях у пациентов с NE ( n = 23) (27).Поражения плаценты, указывающие на тромбоз и снижение фетоплацентарного кровотока, являются значимыми и независимыми факторами риска НЭ ( n = 93) (28). Наличие более одного поражения плаценты увеличивает вероятность НЭ, но не было корреляции между патологией плаценты и картиной повреждения на МРТ ( n = 56) (29). Аномальная патология плаценты была обнаружена у 29% новорожденных с дозорными событиями и у 73% младенцев без дозорных событий ( p = 0,0001), перенесших терапевтическую гипотермию (30).Воспалительные поражения плаценты чаще наблюдались у новорожденных без дозорных событий ( p = 0,002) (30). Хронический виллит был связан с повреждением базальных ганглиев (BGT), тогда как присутствие ядерных эритроцитов, снижение созревания плаценты и хронический виллит также приводили к повреждению белого вещества / водораздела вместе с вовлечением BGT ( n = 95) (31).
Доказательства связи хориоамнионита с НЭ разнообразны. Предполагается, что время инфицирования и степень воспалительного ответа могут привести либо к прекондиционированию, либо к сенсибилизации и могут вызвать либо защитный эффект, либо дальнейшее усиление перинатального повреждения головного мозга, соответственно (32).Этот эффект был продемонстрирован на животных моделях. Липополисахарид (ЛПС), вводимый за 4–6 ч до 20 и 50 мин воздействия HI, приводил к усилению травм головного мозга. Однако введение LPS за 24 часа до 50-минутного воздействия HI привело к значительному ослаблению травм головного мозга (32). КА выявлена у 8 новорожденных с признаками перинатальной асфиксии (всего n = 23) (27). Младенцы с NE и TH имели более высокие шансы на наличие CA по сравнению с младенцами, которые не получали TH ( n = 98) (33).CA, васкулит и фунизит были связаны с NE степени I, виллитом с NE II и фунизитом с III степенью у 141 новорожденного с NE и 309 контрольных (29). CA был связан с более низким риском черепно-мозговой травмы и плохим когнитивным исходом по сравнению с не-CA (скорректированный OR 0,3; 95% CI 0,1–0,7, p = 0,004) у новорожденных с NE ( n = 258), хотя только У 20 новорожденных были гистологические доказательства СА. В той же когорте новорожденные с признаками сепсиса имели более высокие шансы на повреждение водораздела и аномальные нейромоторные показатели, чем у новорожденных без каких-либо клинических признаков ( p = 0.007) (34). У 120 младенцев с сочетанием перинатального ацидоза, NE и хориоамнионита с ответом плода или без него и пятнистый / диффузный хронический виллит были независимо связаны с тяжестью NE (35). Единственным индивидуальным предиктором патологического исхода нервного развития через 22-24 месяца после терапии гипотермией был диффузный хронический виллит. Гистологическая CA имела низкую прогностическую ценность для развития энцефалопатии и смерти при NE ( n = 51) (36), но материнская лихорадка ( n = 336) во время родов была независимым фактором для NE (скорректированное OR 4.72, 95% ДИ 1,28–17,4) (37). Клинический хориоамнионит был связан с более высокими уровнями IL-6, IL-8 в пуповинной крови и регулировался активацией нормальных Т-клеток, экспрессируемых и секретируемых (RANTES) в NE ( n = 61). В когорте из 67 новорожденных с хориоамнионитом NE, независимо от того, были ли клинические или гистологические данные связаны со стойким метаболическим ацидозом, можно предсказать плохой неврологический исход (38).
Патология плаценты была описана как «черный ящик» беременности. Стандартизированная классификация результатов патологии плаценты важна для дальнейшего определения этиологии NE (39).
Нарушения обмена веществ
Нарушения обмена веществ являются редкими причинами НЭ, но их всегда следует учитывать. Врожденные нарушения метаболизма (ВЭМ) присутствуют в неонатальном периоде после нормального периода выздоровления и отсутствия признаков перинатальной асфиксии, но неврологические и полиорганные поражения могут проявляться как НЭ (40). Митохондриальные нарушения также являются важной причиной НЭ (41).
Амплитудная интегрированная электроэнцефалограмма (аЭЭГ) была ненормальной у 27 новорожденных с ВЭМ, причем наиболее устойчивыми признаками были аномальная фоновая активность и судороги.Не было различий в аЭЭГ для энцефалопатии, связанной с IEM или NE, и дифференцировать можно было только на основании клинического подозрения (42). Единственное метаболическое расстройство с диагностической ЭЭГ — это некетотическая гиперглицинемия с первоначальным паттерном «подавление-всплеск», переходящим в гипсаритмию в раннем или среднем младенчестве и диагностируемое путем измерения уровня глицина в спинномозговой жидкости (42). Имеются также отдельные сообщения о случаях ИЭМ, таких как дефицит сульфитоксидазы и цитохрома С, проявляющийся как НЭ (43, 44).
Результаты МРТ
могут варьироваться в зависимости от типа врожденной ошибки метаболизма (IEM) и могут варьироваться от поражения белого вещества до поражения глубоких серых ядер. Митохондриальные энцефалопатии имеют симметричное двустороннее распределение и изначально могут быть диагностированы как NE (45). Следует учитывать метаболические нарушения, если нет явных явлений во время родов, стойкий лактоацидоз и / или гипогликемия (45) и начато обследование. Различные паттерны повреждений на МРТ головного мозга могут помочь отличить метаболические нарушения от НЭ.Поражение Globus Pallidus часто встречается при IEM по сравнению с NE, хотя картина повреждения при дефиците сульфитоксидазы и дефиците фактора молибдена может имитировать NE (46).
Изолированные приступы связаны с такими расстройствами, как: судороги, связанные с пиридоксином, некетотическая гиперглицинемия (NKH), дефицит дигидропиримидиндегидрогеназы, дефицит сульфитоксидазы (либо изолированный, либо как часть дефицита кофактора молибдена), 4-аминобутират аминотрансферазы (GABA). дефицит, судороги, связанные с фолиевой кислотой, дефицит 3-фосфоглицератдегидрогеназы, дефицит гуанидиноацетатметилтрансферазы (GAMT) и дефицит переносчика глюкозы (GLUT-1).У младенцев с полиорганными поражениями, судорогами, метаболическим ацидозом, молочной железой, гипераммониемией могут быть: органическая ацидемия, дефекты цикла мочевины, пероксисомальные нарушения (например, синдром Зеллвегера) или митохондриальные нарушения.
Подробный семейный анамнез для установления факторов риска, таких как родство родителей или ранее пораженный ребенок, важен, поскольку большинство врожденных нарушений метаболизма имеют аутосомно-рецессивное или материнское наследование. Базовые исследования, такие как электролиты, аммиак, сывороточные аминокислоты, лактат, ацилкарнитин и органическая кислота мочи, могут быть рассмотрены при NE (40).Есть проблемы с метаболическим тестированием, так как их может потребоваться повторить, если ребенок очень плохо себя чувствует с полиорганной дисфункцией во время отбора образцов (46). Недавние исследования показали большой потенциал метаболомики как биомаркеров NE. Было показано, что содержание сукцината повышено у детей с НЭ, которые серьезно пострадали (47).
Тромбофилия и неонатальный инсульт
Асфиксия (в 4% случаев) участвует в патогенезе инсульта новорожденных (48). Фокальные клонические приступы являются наиболее частым проявлением неонатального инсульта (49), и 6 младенцев с инсультом были обнаружены в когорте NE ( n = 124) (50).Эти дети обычно страдали судорогами и имели худшие исходы с точки зрения нервного развития, чем остальная часть когорты. Нарушения свертывания крови, такие как полицитемия, лейденский фактор V, нарушения гемоглобина и мутации протромбина, не были обнаружены у 4 из 6 обследованных пациентов (50).
В моделях на животных повышенные уровни гомоцистеина приводили к увеличению провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNFα), интерлейкин 1 бета (IL-1β) и IL-6 в гиппокампе и коре головного мозга.Это провоспалительное состояние может быть ответственным за нейрональные и цереброваскулярные эффекты, наблюдаемые у взрослых (51). Роль гомоцистеина или полиморфизмов в гене метилентетрагидрофолатредуктазы в возникновении неонатального повреждения головного мозга неясна (52). Было обнаружено, что в когорте из 118 новорожденных с НЭ повреждение белого вещества / водораздела с большей вероятностью связано с гипогликемией, полиморфизмом метилентетрагидрофолатредуктазы (MTHFR) и уровнями гомоцистеина в плазме в верхнем квартиле нормы (52).
Генетические и эпигенетические аномалии
Отсутствуют опубликованные данные, связывающие генетическую предрасположенность к развитию NE. У 40 пациентов с NE генетическая изменчивость протромбических факторов, таких как протромбин G20210A, фактор V Leiden G1691A и метилентетрагидрофолатредуктаза [MTHFR] C677T, и ген фактора некроза опухоли не повлияли на оценку NE, ЭЭГ, смерть, краниальное УЗИ (США) , неврологический исход при выписке через 6 и 12 месяцев. Полиморфизм гена интерлейкина-6 (IL-6 174GC) имел защитный эффект и был связан с нормальной ЭЭГ, краниальным УЗИ и неврологическим обследованием при выписке (53).В ретроспективном исследовании «случай-контроль» с участием 11 новорожденных с NE у матерей была обнаружена более высокая частота полиморфизма MTHFR (7 гомозиготных и 4 гетерозиготных) по сравнению с контрольной группой (54). Генетический полиморфизм может увеличивать риск или тяжесть неонатального повреждения головного мозга при NE, и его следует учитывать (53).
В рамках лонгитюдного исследования родителей и детей, проведенного Avon, было проведено генотипирование 7611 доношенных детей, и мерами воздействия было наличие одного или нескольких минорных аллелей в одном из 3 SNP (rs2284411, rs2498804, rs1835740).Первичным результатом была необходимость реанимации при рождении, что было связано с rs1835740 (55). Требуются более крупные международные совместные исследования для определения необходимого количества пациентов для изучения генетических связей и разделения пациентов по этиологии.
Еще одна категория младенцев с генетической причиной неонатальной энцефалопатии — это дети с миопатиями и энцефалопатиями новорожденных. Пациенты, унаследовавшие миопатию (центронуклеарную миопатию), могут иметь неонатальный дистресс, гипотонию и признаки, указывающие на ГИЭ (56).Врожденная миотоническая дистрофия 1 типа характеризуется гипотонией и тяжелой генерализованной слабостью при рождении, часто с дыхательной недостаточностью, умственной отсталостью и ранней смертью. Это вызвано экспансией тринуклеотидного повтора CTG в некодирующей области DMPK .
В будущем подробное генотипирование, включая более легкий доступ к методам микроматрицы в клинических условиях, предоставит больше информации, чтобы позволить индивидуальный уход и потенциально классифицировать младенцев по генотипу.
Нейровизуализация
На МРТ можно увидеть различные модели травм, но это не исключает HIE как причины травмы. Характер повреждения зависит от тяжести, продолжительности и повторяемости гипоксической ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных сочетаниях (1). При глубокой гипоксии преобладает повреждение более глубоких серых структур, то есть базальных ганглиев и таламуса. Объясняется это тем, что эти участки миелинизированы и имеют более высокую скорость метаболизма.Состояния, которые уменьшают, а не вызывают полное прекращение кровотока, такие как анемия и гиповолемия, связаны с повреждением коры головного мозга и сохранением более глубоких серых структур (57). В когорте из 245 пациентов с NE 197 (80%) результаты МРТ соответствовали острому перинатальному инсульту. МРТ у 40 младенцев (16%) были нормальными. У 9 младенцев (4%) помимо гипоксического ишемического инсульта на МРТ были выявлены признаки тромбоза / инфаркта, генетических нарушений, антенатального инсульта и митохондрий (дефицит комплекса I).Нейровизуализация у 8 (3%) младенцев с клиническим диагнозом НЭ показала либо врожденную ошибку метаболизма, нервно-мышечное расстройство, либо отсутствие диагноза, и эти результаты не соответствовали гипоксической ишемии (48). Плацентарный виллит высокой степени неизвестной этиологии ( n = 4) был обнаружен в когорте из 36 пациентов, связанных с повреждением белого вещества, вторичным по отношению к воспалению / окислительному стрессу в перинатальном периоде (58).
Значение для терапии
Не все младенцы с NE могут не получать одинаковую пользу от гипотермии.Следовательно, выявление точной этиологии в каждом случае NE имеет значение для лечения, поскольку есть некоторые излечимые причины, которые требуют быстрого определения для оптимального лечения. Использование бактериальной ПЦР для выявления инфекции у новорожденных с NE может быть более полезным, чем только посев крови с низким выходом бактерий, а также гипотермия может уменьшить воспалительную реакцию. Гистология плаценты отражает внутриматочную среду и может прояснить основную этиологию. Все новорожденные с риском IEM должны быть обследованы на предмет метаболических нарушений, так как этим пациентам могут быть полезны специфические методы лечения, а не гипотермия.Точно так же скрининг на тромбофилию следует рассматривать у пациентов из группы риска, таких как пациенты с инсультом, семейный анамнез тромбофилии. Подробная оценка этиологии NE важна для выявления излечимых причин и категоризации этой гетерогенной группы новорожденных, чтобы можно было подобрать соответствующее лечение в соответствии с этиологией и улучшением отдаленных результатов. Точно так же будет полезно стратифицировать большие многоцентровые когорты младенцев с NE по этиологии, чтобы полностью понять этиологию, реакцию на лечение гипотермии и отдаленные результаты.
Взносы авторов
SA: основной автор; ТС: помогал с поиском релевантных статей и рисунка; ЭМ: автор-руководитель.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
2. Шах П., Рип Хаген С., Бейен Дж., Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch Dis Child Fetal Neonatal Ed . (2004) 89: F152 – F155. DOI: 10.1136 / adc.2002.023093
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Куринчук Дж. Дж., Уайт-Конинг М., Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Ранний Хум Дев . (2010) 86: 329–38. DOI: 10.1016 / j.earlhumdev.2010.05.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Джейкобс С.Е., Берг М., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г.Охлаждение новорожденных с гипоксической ишемической энцефалопатией. База данных Cochr Syst Rev . (2013) 1: CD003311 DOI: 10.1002 / 14651858.CD003311.pub3
CrossRef Полный текст | Google Scholar
5. Нельсон К. Б., Бингхэм П., Эдвардс Е. М., Хорбар Д. Д., Кенни М. Дж., Индер Т. и др. Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети штата Вермонт. Педиатрия . (2012) 130: 878–86. DOI: 10.1542 / peds.2012-0714
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7.Dammann O, Ferriero D, Gressens P. Неонатальная энцефалопатия или гипоксически-ишемическая энцефалопатия? Соответствующая терминология имеет значение Pediatr Res . (2011) 70: 1-2. DOI: 10.1203 / PDR.0b013e318223f38d
CrossRef Полный текст | Google Scholar
8. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ . (1998) 317: 1549–53. DOI: 10.1136 / bmj.317.7172.1549
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Бадави Н., Куринчук Дж. Дж., Кио Дж. М., Алессандри Л. М., О’Салливан Ф., Бертон П. Р. и др. Факторы риска внутриутробной энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ . (1998) 317: 1554–8. DOI: 10.1136 / bmj.317.7172.1554
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Паркер SJ, Kuzniewicz M, Niki H, Wu YW. Факторы дородового и внутриродового риска гипоксически-ишемической энцефалопатии в когорте новорожденных в США. J Педиатр . (2018) 203: 163–9. DOI: 10.1016 / j.jpeds.2018.08.028
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11. Адамсон С.Дж., Алессандри Л.М., Бадави Н., Бертон П.Р., Пембертон П.Дж., Стэнли Ф. Предикторы неонатальной энцефалопатии у доношенных детей. BMJ . (1995) 311: 598–602 DOI: 10.1136 / bmj.311.7005.598
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Мартинес-Биарге М., Диез-Себастьян Дж., Вустхофф С.Дж., Меркури Е., Коуэн FM.Дородовые и внутриродовые факторы, предшествующие неонатальной гипоксически-ишемической энцефалопатии. Педиатрия . (2013) 132: e952 – e959 doi: 10.1542 / peds.2013-0511
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Торбенсон В.Е., Толчер М.К., Несбитт К.М., Колби К.Э., Эль-Нашар С.А., Гостоут Б.С. и др. Внутриродовые факторы, связанные с неонатальной гипоксической ишемической энцефалопатией: исследование случай-контроль. BMC Беременность и роды . (2017) 17: 415 DOI: 10.1186 / s12884-017-1610-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14.Резерфорд М., Маламатениу С., МакГиннесс А., Оллсоп Дж., Биардж М.М., Конселл С. Магнитно-резонансная томография при гипоксически-ишемической энцефалопатии. Ранний Хум Дев . (2010) 86: 351–60. DOI: 10.1016 / j.earlhumdev.2010.05.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Окереафор А., Оллсоп Дж., Конселл С.Дж., Фицпатрик Дж., Аззопарди Д., Резерфорд М.А. и др. Характер черепно-мозговой травмы у новорожденных, подвергшихся перинатальным дозорным событиям. Педиатрия .(2008) 121: 906–14. DOI: 10.1542 / педс.2007-0770
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Мецлер М., Говиндан Р., Аль-Шаргаби Т., Везина Г., Андескавадж Н., Ван Й. и др. Характер черепно-мозговой травмы и снижение вариабельности сердечного ритма у новорожденных с гипоксической ишемической энцефалопатией. Педиатр Рес . (2017) 82: 438–43. DOI: 10.1038 / pr.2017.94
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Симович А.М., Игрутинович З., Обрадович С., Ристич Д., Вулетич Б., Раданович М.Значение сердечного тропонина I второго поколения в раннем скрининге гипоксически-ишемической энцефалопатии после перинатальной асфиксии. SRP Arh Celok Lek . (2012) 140: 600–5.
PubMed Аннотация | Google Scholar
18. Шастри А.Т., Самарасекара С., Мунираман Х., Кларк П. Концентрации сердечного тропонина I у новорожденных с гипоксически-ишемической энцефалопатией. Acta Paediatr . (2012) 101: 26–9. DOI: 10.1111 / j.1651-2227.2011.02432.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19.Лю X, Chakkarapani E, Stone J, Thoresen M. Влияние компрессий сердца и лечения гипотермии на сердечный тропонин I у новорожденных с перинатальной асфиксией. Реанимация . (2013) 84: 1562–7. DOI: 10.1016 / j.resuscitation.2013.07.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Гош Б., Миттал С., Кумар С., Дадхвал В. Прогнозирование перинатальной асфиксии с ядросодержащими эритроцитами в пуповинной крови новорожденных. Int J Gynaecol Obstet .(2003) 81: 267–71. DOI: 10.1016 / S0020-7292 (03) 00124-3
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Уолш Б.Х., Бойлан Г.Б., Мюррей Д.М. Ядерные эритроциты и ранняя ЭЭГ: прогнозирование стадии Сарната и двухлетнего исхода. Ранний Хум Дев . (2011) 87: 335–9. DOI: 10.1016 / j.earlhumdev.2011.01.041
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Нельсон К. Б., Гретер Дж. К.. Потенциально удушающие состояния и спастический церебральный паралич у младенцев с нормальной массой тела при рождении. Am J Obstet Gynecol . (1998) 179: 507–13. DOI: 10.1016 / S0002-9378 (98) 70387-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
23. Шалак Л.Ф., Лапток А.Р., Джафри Х.С., Рамило О., Перлман Дж. Клинический хориоамнионит, повышенные цитокины и травмы головного мозга у доношенных детей. Педиатрия . (2002) 110: 673–80. DOI: 10.1542 / педс.110.4.673
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Танн CJ, Nkurunziza P, Nakakeeto M, Oweka J, Kurinczuk JJ, Were J, et al.Распространенность патогенов кровотока выше в случаях неонатальной энцефалопатии по сравнению с контрольной группой, использующей новую панель ПЦР-анализов в реальном времени. PLOS ONE . (2014) 9: e97259. DOI: 10.1371 / journal.pone.0097259
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Танн С.Дж., Мартинелло К.А., Саду С., Лаун Дж.Э., Сил А.С., Вега-Поблете М. и др. Группа исследователей неонатальной энцефалопатии GBS. неонатальная энцефалопатия со стрептококками группы b во всем мире: систематический обзор, наборы данных исследовательских групп и метаанализ. Clin Infect Dis . (2017) 65 (Suppl_2): S173–89. DOI: 10.1093 / cid / cix662
CrossRef Полный текст | Google Scholar
26. Chakkarapani E, Davis J, Thoresen M. Терапевтическая гипотермия задерживает ответ C-реактивного белка и подавляет количество лейкоцитов и тромбоцитов у младенцев с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed . (2014) 99: F458 – F463. DOI: 10.1136 / archdischild-2013-305763
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27.Wintermark P, Boyd T, Gregas MC, Labrecque M, Hansen A. Патология плаценты у новорожденных с асфиксией, отвечающая критериям терапевтической гипотермии. Am J Obstet Gynecol . (2010) 203: 579.e1–9. DOI: 10.1016 / j.ajog.2010.08.024
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28. Макдональд Д.Г., Келехан П., Макменамин Дж.Б., Горман В.А., Мэдден Д., Тоббия И.Н. и др. Плацентарная тромботическая васкулопатия плода связана с неонатальной энцефалопатией. Хум Патол .(2004) 35: 875–80 DOI: 10.1016 / j.humpath.2004.02.014
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Hayes BC, Cooley S, Donnelly J, Doherty E, Grehan A, Madigan C и др. Плацента у младенцев> 36 недель беременности с неонатальной энцефалопатией: исследование случай-контроль. Arch Dis Child Fetal Neonatal Ed . (2013) 98: F233–9. DOI: 10.1136 / archdischild-2012-301992
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30.Чанг Т., Рейес Т.Дж., Пласетек Дж., Массаро А.Н., Нельсон КБ. Неонатальная энцефалопатия, дозорные явления и плацента. J Неонатальная перинатальная медицина . (2012) 5: 41–8. DOI: 10.3233 / NPM-2012-54211
CrossRef Полный текст | Google Scholar
31. Хартеман Дж. С., Никкельс П. Г., Бендерс М. Дж., Кви А., Грюнендал Ф., де Фрис Л. С.. Патология плаценты у доношенных детей с гипоксически-ишемической неонатальной энцефалопатией и ассоциация с магнитно-резонансной томографией повреждения головного мозга. J Педиатр .(2013) 163: 968–995 DOI: 10.1016 / j.jpeds.2013.06.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32. Эклинд С., Маллард С., Арвидссон П., Хагберг Х. Липополисахарид вызывает как первичную, так и вторичную фазу сенсибилизации в развивающемся мозге крысы. Педиатр Рес . (2005) 58: 112–6 DOI: 10.1203 / 01.PDR.0000163513.03619.8D
PubMed Аннотация | CrossRef Полный текст | Google Scholar
33. Нельсон Д.Б., Лаке А.М., Макинтайр Д.Д., Санчес П.Дж., Левено К.Дж., Чалак Л.Ф.Акушерские предшественники лечения новорожденного с помощью охлаждения тела. Am J Obstet Gynecol. (2014) 211: 155.e1–6. DOI: 10.1016 / j.ajog.2014.02.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
34. Йенстер М., Бонифачо С.Л., Рюэль Т., Роджерс Э.Е., Там Э.У., Партридж Дж.С. и др. Инфекция матери или новорожденного: связь с исходами неонатальной энцефалопатии. Педиатр Рес . (2014) 76: 93–9. DOI: 10.1038 / pr.2014.47
CrossRef Полный текст | Google Scholar
35.Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф. Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol . (2015) 213: 849.e1–7. DOI: 10.1016 / j.ajog.2015.09.072
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36. Шалак Л., Джонсон-Велч С., Перлман Дж. М.. Хориоамнионит и неонатальная энцефалопатия у доношенных детей с ацидемией плода: гистопатологические корреляции. Педиатр Нейрол . (2005) 33: 162–5. DOI: 10.1016 / j.pediatrneurol.2005.04.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Импи Л., Гринвуд К., Маккуиллан К., Рейнольдс М., Шейл О. Лихорадка во время родов и неонатальная энцефалопатия: проспективное когортное исследование. БЖОГ . (2001) 108: 594–7. DOI: 10.1111 / j.1471-0528.2001.00145.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Джонсон, CT, Бурд I, Рагхунатан Р., Нортингтон Ф.Дж., Грэм Э.М.Перинатальное воспаление / инфекция и его связь с коррекцией метаболического ацидоза при гипоксически-ишемической энцефалопатии. Дж Перинатол . (2016) 36: 448–52. DOI: 10.1038 / jp.2015.221
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39. Кларк П., Мунираман Х., Гарднер Д., Венкатеш В., Керли А., Виктор С. и др. Исследование неонатальной энцефалопатии: часто теряемый плацентарный «черный ящик». Педиатр Дев Патол . (2015) 18: 343–4. DOI: 10.2350 / 15-02-1611-LET.1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
40. Tan ES. Врожденные нарушения обмена веществ, проявляющиеся как неонатальная энцефалопатия: практические советы врачам. Энн Акад Мед Сингапур . (2008) 37 (12 Suppl.): 94–3.
PubMed Аннотация | Google Scholar
42. Олишар М., Шани Э., Айгюн С., Аззопарди Д., Хант Р.В., Тоет М.С. и др. Амплитудно-интегрированная электроэнцефалография у новорожденных с врожденными нарушениями обмена веществ. Неонатология .(2012) 102: 203–11. DOI: 10.1159 / 000339567
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Hobson EE, Thomas S, Crofton PM, Murray AD, Dean JC, Lloyd D. Изолированная недостаточность сульфитоксидазы имитирует признаки гипоксической ишемической энцефалопатии. Eur J Pediatr . (2005) 164: 655–9. DOI: 10.1007 / s00431-005-1729-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44. Уиллис Т.А., Дэвидсон Дж., Грей Р.Г., Поултон К., Рамани П., Уайтхаус В.Дефицит цитохромоксидазы, проявляющийся в виде асфиксии при рождении. Дев Мед Детский Нейрол . (2000) 42: 414–7. DOI: 10.1017 / S0012162200000761
PubMed Аннотация | CrossRef Полный текст | Google Scholar
46. Enns GM. Врожденные нарушения обмена веществ, маскирующиеся под гипоксически-ишемическую энцефалопатию. NeoReviews . (2005) 12: e549 – e558. DOI: 10.1542 / neo.6-12-e549
CrossRef Полный текст | Google Scholar
47. Уолш Б.Х., Бродхерст Д.И., Мандал Р., Вишарт Д.С., Бойлан Г.Б., Кенни Л.К. и др.Метаболомный профиль пуповинной крови при гипоксической ишемической энцефалопатии новорожденных. PLOS ONE . (2012) 7: e50520. DOI: 10.1371 / journal.pone.0050520
PubMed Аннотация | CrossRef Полный текст | Google Scholar
48. Коуэн Ф., Резерфорд М., Грюнендал Ф., Экен П., Меркури Э., Байддер Г.М. и др. Происхождение и сроки поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет . (2003) 361: 736–42 DOI: 10.1016 / S0140-6736 (03) 12658-X
PubMed Аннотация | CrossRef Полный текст | Google Scholar
50.Рамасвами В., Миллер С.П., Баркович А.Дж., Партридж Дж.С., Ферриеро Д.М. Перинатальный инсульт у доношенных детей с неонатальной энцефалопатией. Неврология . (2004) 62: 2088–91. DOI: 10.1212 / 01.WNL.0000129909.77753.C4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51. Scherer EB, Loureiro SO, Vuaden FC, da Cunha AA, Schmitz F, Kolling J, et al. Легкая гипергомоцистеинемия увеличивает уровни ацетилхолинэстеразы мозга и провоспалительных цитокинов в различных тканях. Мол Нейробиол .(2014) 50: 589–96. DOI: 10.1007 / s12035-014-8660-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
52. Хартеман Дж. С., Грюнендал Ф., Бендерс М. Дж., Хьюсман А., Блом Х. Дж., Де Фрис Л. С.. Роль тромбофильных факторов у доношенных детей с неонатальной энцефалопатией. Педиатр Рес . (2013) 73: 80–6. DOI: 10.1038 / pr.2012.150
PubMed Аннотация | CrossRef Полный текст | Google Scholar
53. Цалкавур С., Акису М., Олюкман О., Балим З., Бердели А., Чакмак Б. и др.Генетические факторы, влияющие на краткосрочный исход развития нервной системы у доношенных новорожденных с гипоксически-ишемической энцефалопатией. J Int Med Res . (2011) 39: 1744–56. DOI: 10.1177 / 147323001103
PubMed Аннотация | CrossRef Полный текст | Google Scholar
54. Додельсон де Кремер Р., Гроссо С. Материнская мутация 677C> T в гене метилентетрагидрофолатредуктазы, связанная с тяжелым повреждением головного мозга у потомства. Clin Genet . (2005) 67: 69–80.
PubMed Аннотация | Google Scholar
55.Odd D, Váradi A, Rajatileka S, Molnár E, Luyt K. Связь между реанимацией новорожденных и однонуклеотидным полиморфизмом rs1835740. Acta Paediatr . (2016) 105: e307–12. DOI: 10.1111 / apa.13421
PubMed Аннотация | CrossRef Полный текст | Google Scholar
56. Bruyland M, Liebaers I, Sacre L, Vandeplas Y, De Meirleir L, Martin JJ. Неонатальная миотубулярная миопатия с вероятным X-сцепленным наследованием: наблюдения за новой семьей с обзором литературы. Дж. Нейрол . (1984) 231: 220–2. DOI: 10.1007 / BF00313942
PubMed Аннотация | CrossRef Полный текст | Google Scholar
57. Баркович А.Дж., Вестмарк К., Партридж К., Сола А., Ферриеро Д.М. Перинатальная асфиксия: результаты МРТ в первые 10 дней. AJNR Am J Нейрорадиол . (1995) 16: 427–38.
PubMed Аннотация | Google Scholar
58. Barrett MJ, Donoghue V, Mooney EE, Slevin M, Persaud T, Twomey E, et al. Изолированное острое некистозное повреждение белого вещества у доношенных детей с неонатальной энцефалопатией. Arch Dis Child Fetal Neonatal Ed . (2013) 98: F158 – F160. DOI: 10.1136 / archdischild-2011-301505
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Неонатальная энцефалопатия и гипоксико-ишемическая энцефалопатия (ГИЭ)
Неонатальная энцефалопатия (NE) — это широкий термин, обозначающий неврологическую дисфункцию у младенца. Неонатальная энцефалопатия может быть вызвана множеством причин (1). Кислородная недостаточность при рождении (асфиксия при рождении) — одна из наиболее частых причин неонатальной энцефалопатии.Медицинские работники могут использовать термины гипоксически-ишемическая энцефалопатия (ГИЭ), перинатальная асфиксия , асфиксия во время родов и асфиксия при рождении взаимозаменяемо с неонатальной энцефалопатией, хотя это несколько разные состояния.
Что такое неонатальная энцефалопатия (NE)?
«Неонатальная энцефалопатия» включает любую форму дисфункции центральной нервной системы, вызванную повреждением головного мозга. Этот термин используется при обсуждении травм у детей, рожденных на сроке беременности 35 недель или позже (дети, которые либо родились поздно, либо доношены) (1, 2).По оценкам, неонатальная энцефалопатия встречается примерно у двух-девяти из 1000 живорождений (2) и может быть вызвана множеством факторов. К ним относятся следующие (3):
Заболевания, связанные с неонатальной энцефалопатией
У младенцев с неонатальной энцефалопатией или гипоксически-ишемической энцефалопатией могут быть другие связанные диагнозы, в том числе:
Что означает диагноз неонатальной энцефалопатии?
Диагноз неонатальной энцефалопатии может означать многое.В простейшем случае это означает, что у ребенка определенная степень дисфункции мозга. Иногда из-за травмы внутри головного мозга возникает отек. Во многих случаях у ребенка не остается необратимых повреждений или долгосрочных последствий, особенно если энцефалопатия своевременно распознается и лечится.
К сожалению, в некоторых случаях последствия неонатальной энцефалопатии выявляются в более позднем возрасте; когда ребенок достигает четырех-пяти лет и начинает пропускать важные вехи в развитии (4).Неонатальная энцефалопатия может привести к долгосрочным состояниям, таким как церебральный паралич, задержка в развитии или нарушение обучаемости.
Признаки и симптомы неонатальной энцефалопатии
Энцефалопатия новорожденных может быть легкой, средней или тяжелой степени в зависимости от ее симптомов. Признаки и симптомы энцефалопатии могут включать следующие (2):
- Низкая Оценка по шкале Апгар
- Слабый или отсутствующий плач при рождении / родах
- Изъятия
- Требуется реанимация
- Аномальный уровень сознания: Ребенок гиперактивен, раздражителен, апатичен, заторможен (не очень внимателен).
- Нарушения тонуса и рефлекса: Такие, как гипотония (вялые или гибкие конечности) и / или гипертонус (жесткие или спастические мышцы).
- Отсутствие примитивных рефлексов
- Апноэ : Периоды, при которых ребенок перестает дышать на 20 секунд или более.
- Проблемы с кормлением
- Респираторные проблемы
- Лихорадка
- Жесткость шеи: Часто встречается при менингите или менингоэнцефалите.
- Гипотония
- Органная недостаточность
- Гипер- или гипогликемия
Судороги у новорожденных являются одним из наиболее частых признаков неонатальной энцефалопатии . Важно отметить, что припадки у младенцев не выглядят так же, как припадки у взрослых; Признаки судорог у младенцев обычно менее заметны. У некоторых детей с припадками наблюдаются повторяющиеся подергивания или циклические движения конечностей, или им может казаться, что они тупо смотрят в пространство.Эти эпизоды могут повлиять на сознание ребенка. Эти припадки необходимо быстро диагностировать с помощью ЭЭГ и лечить, чтобы предотвратить ухудшение состояния мозга (5).
Лечение неонатальной энцефалопатии
Все средние и тяжелые случаи неонатальной энцефалопатии требуют лечения, которое проводится в отделении интенсивной терапии новорожденных (NICU) (2). Поскольку существует множество различных основных механизмов, которые могут вызвать неонатальную энцефалопатию, лечение и лечение травмы в высшей степени индивидуализировано.Некоторые виды энцефалопатии необходимо лечить с помощью терапевтической гипотермии (охлаждения мозга). Однако не все типы энцефалопатии лечатся одинаково. Например, энцефалопатия, вызванная бактериями или вирусом, лечится путем борьбы с основной инфекцией. Ключевые методы лечения включают (2):
- Вентиляция: Младенцев с энцефалопатией из-за респираторных заболеваний можно поместить на вентилятор, чтобы регулировать их дыхание и обеспечить адекватную оксигенацию.Медицинские работники должны избегать гипероксии и гипоксемии (слишком много или слишком мало кислорода).
- Приступы : Частью лечения неонатальной энцефалопатии является борьба с приступами. Некоторые лекарства можно использовать для лечения судорог. Кроме того, для регулярного наблюдения за приступами следует использовать мониторинг ЭЭГ.
- Лечение, связанное с кровью: Младенцам с мозговым кровотечением можно давать продукты крови (например, эритроциты и свежезамороженную плазму) или физиологический раствор для устранения проблем с кровяным давлением.Следует поддерживать перфузию мозга и органов и избегать гипертонии, гипотонии и гипервязкости.
- IV: Младенцам, перенесшим инсульт, можно вводить жидкости и лекарства внутривенно для предотвращения проблем со свертыванием крови.
- Лекарство: Младенцам с энцефалопатией из-за инфекции могут быть назначены противовирусные препараты или антибиотики для контроля инфекции (в зависимости от типа инфекции).
Причины неонатальной энцефалопатии
Неонатальная энцефалопатия может быть вызвана широким спектром осложнений во время или во время родов, включая следующие.
Асфиксия при рождении (недостаток кислорода в головном мозге)
В утробе матери младенцы получают кислород из крови, которая проходит от матери к плаценте и пуповине. Все, что мешает этому пути, может вызвать у ребенка недостаток кислорода (7). Вот некоторые примеры причин асфиксии при рождении:
Основные состояния материнского здоровья
Определенные состояния здоровья могут повысить риск беременности. Эти состояния здоровья несут с собой более высокий риск родовой травмы, что требует более тщательного наблюдения и более частых посещений дородового наблюдения.Эти условия включают (8):
Рождение с травмой
Очень важно, чтобы младенцы рожали опытные акушеры, гинекологи или другой медицинский персонал, обладающий необходимыми знаниями методов и процедур для сложных родов. Если медицинский персонал рожает ребенка способом, не отвечающим стандартам ухода, у ребенка могут быть травматические роды (8). Последствия травматических родов не всегда очевидны — внешнего кровотечения может и не быть.Иногда возникает внутреннее кровотечение (мозговое кровотечение). У младенцев могут сразу же появиться признаки неврологической дисфункции — например, в виде судорог — или — в некоторых случаях — неврологическая дисфункция у ребенка проявляется только по мере роста и пропускания основных этапов развития. Причины травматических родов могут включать:
Профилактика неонатальной энцефалопатии (NE)
Многие состояния, вызывающие неонатальную энцефалопатию (NE), имеют известные факторы риска. Это означает, что медицинский персонал может предотвратить неблагоприятные исходы, должным образом следя за здоровьем матери и ребенка и при необходимости проводя вмешательства.
Многие из этих событий влияют на ребенка во время схваток и родов. Из-за рисков, связанных с родами, частота сердечных сокращений ребенка должна постоянно контролироваться с помощью монитора сердечного ритма плода (9). Этот монитор предупредит медицинскую бригаду, если у ребенка начнется недостаток кислорода, что будет проявляться как неутешительное исследование сердца (дистресс плода). Если происходит дистресс плода, врач должен сразу же родить ребенка, часто с помощью кесарева сечения (самый быстрый и безопасный способ родить ребенка в бедственном положении).
Одним из ключевых моментов, которые очень важны для предотвращения неонатальной энцефалопатии у младенцев, является правильная техника для использования вакуумных экстракторов или щипцов , если это необходимо . Не должно быть ни перекручивания головы или шеи, ни чрезмерного натяжения, ни тяги более 20 минут (10). Если во время использования вакуум-экстрактор сработает 3 раза, врач должен перейти к кесареву сечению (11). Эти инструменты должны использоваться только врачами, которые соблюдают стандарты оказания медицинской помощи, в том числе обладающие высокой квалификацией.
Если у ребенка кровоизлияние в мозг в результате родов или родоразрешения, кровотечение необходимо незамедлительно распознать и лечить, чтобы можно было избежать энцефалита и таких необратимых состояний, как церебральный паралич. Это может включать:
- Лекарства, помогающие остановить или замедлить кровотечение
- Лекарства для повышения артериального давления и объема крови
- ИВЛ для ребенка (дыхательный аппарат)
- Лекарства от воспаления
- Тщательный мониторинг внутричерепного артериального давления
Беременные женщины должны проходить регулярные дородовые осмотры, которые оценивают как их здоровье, так и здоровье их ребенка.Пренатальные тесты включают нестрессовые тесты и биофизические профили (BPP). Если у матери беременность высокого риска, следует чаще проводить пренатальные анализы и направлять ее к специалисту по беременности и родам. Эти пренатальные тесты, если их провести правильно, могут выявить основные состояния здоровья, которые могут означать, что ребенок подвергается более высокому риску получения родовой травмы.
Во время дородовых посещений врачи должны уделять пристальное внимание результатам анализов, особенно сердцебиению ребенка. Эти записи вместе с результатами УЗИ предупредят медицинскую бригаду о проблемах со здоровьем, которые могут быть у ребенка, в том числе если ребенок лишен кислорода.Если это происходит, мать может быть госпитализирована, чтобы медицинская бригада могла внимательно наблюдать за ребенком. Иногда ребенка приходится рожать раньше, чтобы предотвратить необратимое повреждение мозга из-за недостатка кислорода и / или питательных веществ.
Юридические центры ABC: поверенные по неонатальной энцефалопатии
Если у вашего ребенка неонатальная энцефалопатия, рассмотрите возможность рассмотрения вашего дела адвокатом по родовым травмам. Некоторым детям с неонатальной энцефалопатией требуется круглосуточный уход, медицинская помощь, реабилитация и терапия и другие услуги.Иск о родовой травме может помочь покрыть расходы по уходу за вашим ребенком.
Свяжитесь с адвокатом по травмам при родах в юридических центрах ABC (Reiter & Walsh, P.C.), чтобы получить бесплатную 100% конфиденциальную оценку дела. Мы фокусируем только на родовых травмах, в отличие от других фирм, которые говорят, что они сосредотачиваются только на родовых травмах, но имеют списки случаев, полные укусов собак, автомобильных аварий и неисправностей медицинских устройств.
Родовая травма требует глубоких знаний медицины, юридических вопросов, проблем радиологии и планирования ухода в связи с детской инвалидностью.Адвокаты по травмам при родах в юридических центрах ABC имеют почти 100-летний опыт работы.
Вы бы не доверили врачу широкого профиля деликатную микрохирургию. Зачем доверять дело о родовой травме специалисту по травмам?
Бесплатный обзор случая | Доступно 24/7 | Никаких комиссий, пока мы не выиграем
Телефон (бесплатный): 888-419-2229
Нажмите кнопку Live Chat в своем браузере
Заполните нашу онлайн-форму для связи
Видео: Адвокаты по неонатальной энцефалопатии обсуждают гипоксически-ишемическую энцефалопатию (ГИЭ)
Источники:
- Краткое содержание: неонатальная энцефалопатия и неврологический исход, второе издание.Отчет Рабочей группы Американского колледжа акушеров и гинекологов по неонатальной энцефалопатии. Obstet Gynecol 2014; 123: 896.
- Wu, Y. (10 июля 2019 г.). Клиника, диагностика и лечение энцефалопатии новорожденных. Получено 4 октября 2019 г. с сайта https://www.uptodate.com/contents/clinical-features-diagnosis-and-treatment-of-neonatal-encephalopathy/print.
- Тан, С., и Ву, Ю. (27 июля 2018 г.). Этиология и патогенез неонатальной энцефалопатии. Получено 8 октября 2019 г. с сайта https: // www.uptodate.com/contents/etiology-and-pathogenesis-of-neonatal-encephalopathy?topicRef=6216&source=see_link.
- Задержки развития и родовые травмы: юридические центры ABC. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/types-of-birth-injuries/signs-milestones-developmental-delays/.
- Судорожные припадки у новорожденных (неонатальные припадки): поверенные по родовым травмам. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/neonatal-birth-injuries/seizures/.
- Терапия гипотермией: лечение гипоксико-ишемической энцефалопатии. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/treatments-and-therapies-for-birth-injuries/hypothermia-cooling/.
- Гипоксическая ишемическая энцефалопатия Адвокаты: асфиксия при рождении. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/prenatal-birth-injuries/fetus-or-newborn-medical-problems/hypoxic-ischemic-encephalopathy/birth-asphyxia-hypoxic-ischemic. -энцефалопатии-поверенные /.
- Беременность с повышенным риском: поверенные по родовым травмам. (нет данных). Получено 9 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/prenatal-birth-injuries/maternal-medical-conditions/high-risk-pregnancy/.
- Адвокаты в области родовой травмы: Адвокаты по церебральному параличу. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/types-of-birth-injuries/birth-trauma/.
- Адвокаты по травмам при родах: неправильный мониторинг плода. (нет данных). Получено 8 октября 2019 г. с сайта https: // www.abclawcenters.com/practice-areas/prenatal-birth-injuries/labor-and-delivery-complications-and-errors/improper-fetal-monitoring/.
- Адвокаты в штате Мичиган по травмам при рождении: травмы с помощью вакуумного экстрактора. (нет данных). Получено 8 октября 2019 г. с сайта https://www.abclawcenters.com/practice-areas/prenatal-birth-injuries/traumatic-birth-injuries/forceps-and-vacuum-extractor-injuries/.
- Али, У. А., и Норвиц, Э. Р. (2009). Вагинальные роды с использованием вакуума. Обзоры по акушерству и гинекологии , 2 (1), 5–17.
Что такое гипоксико-ишемическая энцефалопатия (ГИЭ)?
Что такое гипоксически-ишемическая энцефалопатия (ГИЭ)?
Гипоксически-ишемическая энцефалопатия (ГИЭ) — это тип повреждения головного мозга новорожденных, вызванный кислородной недостаточностью и ограниченным кровотоком. ГИЭ представляет собой тип родовой травмы ; это широкий термин, используемый для обозначения любого вреда, который ребенок испытывает во время или незадолго до рождения. Другие термины, используемые для HIE, включают асфиксию при рождении , перинатальную асфиксию и неонатальную энцефалопатию .
В некоторых случаях терапевтическая гипотермия может предотвратить или минимизировать необратимое повреждение головного мозга, хотя ее следует назначать в течение нескольких часов после рождения ребенка / травмы, вызванной кислородным голоданием (дополнительную информацию см. В разделе «Лечение ГИЭ»). Однако при терапевтической гипотермии и без нее у многих младенцев с ГИЭ развиваются постоянные состояния здоровья и расстройства. К ним относятся церебральный паралич (ДЦП), когнитивные нарушения, эпилепсия, нарушения слуха и зрения и многое другое.
Полная степень повреждения от ГИЭ обычно не проявляется сразу после рождения по двум основным причинам:
- Повреждение мозга в результате ГИЭ — это развивающийся процесс. Когда кровоток к частям мозга прекращается, клетки начинают разрушаться, умирать и выделять вещества, токсичные для других клеток. Затем эти клетки начинают отмирать и продолжают цепную реакцию, которая вызывает повреждение головного мозга в течение нескольких часов или дней. Разрушить эту цепную реакцию может терапевтическое переохлаждение.
- Повреждение от ГИЭ может иногда не проявляться до тех пор, пока у ребенка не появится задержка в развитии. Например, влияние на подвижность может быть незаметно до тех пор, пока ребенок не преодолеет такие важные вехи, как ползание или ходьба.
При необратимом повреждении головного мозга нет лекарства от ГИЭ. Однако существует множество методов лечения и терапии, которые могут улучшить симптомы и улучшить функции у детей с ГИЭ.
Каковы причины ГИЭ?
ГИЭ может быть вызвано различными медицинскими осложнениями во время родов.Во многих случаях врачебная халатность также играет роль. Например, врачи могут не следить должным образом за здоровьем матери и ребенка и выявлять потенциальные проблемы. С другой стороны, они могут распознавать проблемы, но не воспринимать их достаточно серьезно / не вмешиваться. Узнайте больше о связи между HIE и злоупотреблением служебным положением, а также о юридических вариантах.
Следующие проблемы со здоровьем и небрежные действия могут привести к ГИЭ (это лишь несколько примеров; дополнительную информацию см. На этой странице):
- Неправильное ведение беременности с высоким риском : Женщины с такими состояниями, как преэклампсия и гестационный диабет требуют более тщательного наблюдения и лечения.
- Осложнения пуповины : Пуповина подобна спасательному кругу между матерью и младенцем, снабжая кислородом и питательными веществами и удаляя отходы плода. Все, что сжимает пуповину или снижает ее функцию, подвергает ребенка риску ГИЭ.
- Плацентарные или маточные осложнения: Плацента и матка также играют очень важную роль в обеспечении ребенка насыщенной кислородом кровью. Примеры проблем с плацентой и маткой, которые могут вызвать ГИЭ, включают:
- Отслойка плаценты: когда плацента отделяется от матки до рождения ребенка
- Предлежание плаценты: когда плацента прикрепляется слишком близко к шейке матки; это может вызвать опасное кровотечение и кислородную недостаточность во время родов
- Плацентарная недостаточность: когда плацента не может доставить достаточно крови к ребенку
- Разрыв матки: когда матка разрывается частично или полностью
- Инфекции: инфекции у матери может передаваться ребенку во время схваток и родов, особенно если медицинская бригада не примет адекватных мер предосторожности (например, не проведет обследование на наличие инфекции и при необходимости назначит антибиотики).
- Неправильный мониторинг сердца плода: Если ребенок показывает признаки дистресса плода на мониторе сердечного ритма плода, врачи и медсестры часто могут вмешаться, чтобы восстановить его кислородное снабжение. При необходимости это может включать экстренное кесарево сечение. Однако, если мониторинг носит спорадический характер или не проводится, важные признаки опасности могут быть упущены.
- Неспособность предотвратить преждевременные роды: Недоношенные дети подвергаются более высокому риску ГИЭ и других родовых травм, поскольку их легкие настолько недоразвиты.Поэтому очень важно, чтобы врачи делали все возможное для предотвращения преждевременных родов, например, выполняли шейный серкляж (шов, накладываемый на шейку матки, чтобы она не открылась слишком рано) или обеспечивали лечение прогестероном.
- Продолжение продолжительных родов: роды вызывают стресс у младенцев, потому что сокращения матки сжимают плаценту и пуповину, которые снабжают их кислородом. Если что-то препятствует прогрессированию родов, а врачи не предлагают вмешательство (например, экстренное кесарево сечение), это халатность.Затяжные роды более вероятны, если ребенок крупнее обычного или таз матери меньше нормального.
- Проблемы с лекарствами: Иногда врачи прописывают лекарства, такие как Pitocin и Cytotec, чтобы вызвать или усилить роды. К сожалению, эти лекарства также могут стать причиной того, что сокращения матки станут настолько сильными и частыми, что ребенок будет опасно лишен кислорода.
- Неправильное ведение неонатального состояния: Гипоксико-ишемическое повреждение может быть вызвано осложнениями в неонатальном периоде, т.е.е. первый месяц жизни ребенка. Такие проблемы, как респираторный дистресс, желтуха и неонатальная гипогликемия, могут способствовать диагностике ГИЭ, особенно при неправильном лечении.
Каковы признаки и симптомы ГИЭ?
Младенцы с ГИЭ могут демонстрировать любой из следующих признаков (среди прочего):
- Проблемы с дыханием
- Проблемы с кормлением
- Отсутствие рефлексов (например, ребенок не реагирует на громкие звуки)
- Судороги
- Низкий Апгар баллов
- Низкий или высокий мышечный тонус
- Измененный уровень сознания (например,грамм. без предупреждения)
Как вы произносите «гипоксически-ишемическая энцефалопатия» (ГИЭ)?
Лечение ГИЭ
ГИЭ проводится с помощью лечения, называемого терапевтической гипотермией, при котором мозг или тело ребенка охлаждают до температуры ниже нормальной, чтобы замедлить каскадный эффект, вызывающий обширные повреждения. Это позволяет мозгу ребенка восстановиться и снижает уровень инвалидности, который может быть у него в процессе роста. Согласно действующим руководствам, лечение следует проводить в течение шести часов после родов, хотя есть некоторые данные, позволяющие предположить, что лечение может быть полезным при продолжении до 24 часов.
Лечебная гипотермия длится около 72 часов, что позволяет замедлить метаболизм ребенка. Это предотвращает дальнейшее повреждение, известное как реперфузионное повреждение , которое возникает, когда нормальная оксигенация и кровоток восстанавливаются слишком быстро в клетках мозга. Хотя может показаться нелогичным, что быстрое восстановление кровотока может вызвать дальнейшее повреждение, клетки мозга по-разному реагируют на быструю оксигенацию после кислородного голодания. После травмы, вызванной кислородным голоданием, быстрое насыщение кислородом может вызвать усиление воспаления и выделение определенных вредных соединений.Лечение гипотермии стабилизирует клетки мозга и предотвращает или ограничивает повреждающее воспаление.
В дополнение к терапевтическому переохлаждению медицинский персонал должен оказывать поддерживающую терапию, которая может означать помощь ребенку в дыхании, контроль и предотвращение судорог и низкого уровня сахара в крови, уменьшение отека мозга и многое другое. В долгосрочной перспективе младенцам с повреждением головного мозга в результате ГИЭ может быть полезен широкий спектр методов лечения и терапии. Хотя они не являются лечебными, они могут минимизировать симптомы и улучшить функцию.Для получения дополнительной информации нажмите здесь.
Типы и формы ГИЭ
Если они подозревают ГИЭ, медицинский персонал может провести визуализацию мозга, такую как УЗИ и МРТ, чтобы увидеть, насколько сильно повреждены ткани в головном мозге. Воспитатели также проводят анализ газов крови, чтобы определить pH крови ребенка, который также может предоставить некоторую информацию об уровне кислорода в крови ребенка.
Тяжесть ГИЭ определяется с использованием стадирования Sarnat, которое учитывает клиническую картину, результаты обследования, наличие приступов и продолжительность заболевания.Легкая ГИЭ классифицируется как степень I по Сарнату, а степень тяжести увеличивается до максимальной степени III (1).
Распространенность и частота ГИЭ
ГИЭ оценивается от 2 до 9 случаев на 1000 живорождений. Появление терапевтической гипотермии значительно снизило уровень смертности и инвалидности, но результаты все еще могут быть тяжелыми. В одном исследовании почти половина новорожденных с ГИЭ либо умерли, либо имели серьезные нарушения развития нервной системы в течение 18 месяцев наблюдения. Однако 40 процентов детей в этом исследовании имели нормальное раннее развитие (2).
Ожидаемая продолжительность жизни людей с ГИЭ и церебральным параличом
Ожидаемая продолжительность жизни людей с гипоксически-ишемической энцефалопатией во многом зависит от степени их поражения и их доступа к лечению и терапии. По этой причине трудно определить «среднюю» продолжительность жизни людей с ГИЭ. Поскольку многим детям с ГИЭ также ставится диагноз церебральный паралич, может быть более полезно посмотреть на ожидаемую продолжительность жизни людей с церебральным параличом.
Ожидается, что люди с церебральным параличом очень легкой степени будут жить столько же, сколько их сверстники в общей популяции.В целом, ожидаемая продолжительность жизни человека с церебральным параличом зависит от степени его поражения:
- Продолжительность жизни легкого церебрального паралича : Для людей с довольно легким церебральным параличом (определяемым как ходьба без посторонней помощи) продолжительность жизни женщин оценивается в 70-80 лет, а у мужчин — в 66-76 лет.
- Продолжительность жизни тяжелого церебрального паралича : Для тех, кто более серьезно поражен (определяется как неспособность поднимать голову и получать питание через зонд), ожидаемая продолжительность жизни, по оценкам, будет короче как для женщин, так и для мужчин, в зависимости от качество полученной медицинской помощи.
Эти цифры продолжительности жизни были взяты из исследования 2008 г., проведенного в журнале Developmental Medicine and Child Neurology . Щелкните здесь, чтобы просмотреть статью, в которой содержится подробная таблица ожидаемой продолжительности жизни людей с церебральным параличом. Он учитывает возраст, пол, подвижность и механизм кормления (3).
Более подробная информация о HIE
Для получения дополнительной информации о HIE, пожалуйста, посетите наш раздел «Медицинская информация».
О Центре помощи HIE и Юридических центрах ABC
Центр помощи HIE находится в ведении ABC Law Centers, юридической фирмы, занимающейся врачебной халатностью, которая занимается исключительно случаями, связанными с HIE и другими родовыми травмами.Наши юристы имеют более чем 100-летний совместный опыт работы с этим типом права и защищают интересы детей с ГИЭ и связанными с ними нарушениями с момента основания фирмы в 1997 году. счета, потеря заработной платы (если один или оба родителя вынуждены пропускать работу, чтобы ухаживать за своим ребенком), вспомогательные технологии и другие предметы первой необходимости.
Если вы подозреваете, что причиной ГИЭ у вашего ребенка была халатность со стороны врача, свяжитесь с нами сегодня, чтобы узнать больше о расследовании дела.Мы предоставляем бесплатные юридические консультации, в ходе которых мы проинформируем вас о ваших юридических вариантах и ответим на любые ваши вопросы. Более того, вы не будете платить ничего на протяжении всего судебного процесса , если мы не добьемся благоприятного урегулирования.
Вы также можете обращаться к нам с вопросами, которые не связаны с злоупотреблением служебным положением. Мы не можем предоставить индивидуальные медицинские консультации, но мы будем рады найти для вас информационные ресурсы.
Цитаты
- Сарнат, Х.Б. и Сарнат М.С. (1976). Энцефалопатия новорожденных после дистресса плода: клиническое и электроэнцефалографическое исследование. Архив неврологии , 33 (10), 696-705.
- (нет данных). Получено 15 января 2019 г. с сайта https://www.uptodate.com/contents/clinical-features-diagnosis-and-treatment-of-neonatal-encephalopathy
- Strauss, D., Brooks, J., Rosenbloom, L. , & Шавелле Р. (2008). Ожидаемая продолжительность жизни при церебральном параличе: обновленная информация. Медицина развития и детская неврология , 50 (7), 487-493.
Ведение и исследование неонатальной энцефалопатии: обновление 2017 г.
Реанимация
Около 85% доношенных детей будут дышать спонтанно при рождении без посторонней помощи, 10% потребуют стимуляции, 3% потребуют неинвазивной вентиляции, 2% будут интубированы и 0,1% потребуют компрессии грудной клетки и / или введения адреналина.6 Важно, чтобы при родах присутствовал квалифицированный персонал, а в случае дородовых или интранатальных событий присутствовали сотрудники с продвинутыми навыками реанимации новорожденных и навыками прохождения дыхательных путей.Ключевым компонентом реанимации новорожденного, страдающего асфиксией, является установление функциональной остаточной емкости (FRC) и при этом обеспечение возможности восстановления спонтанного кровообращения (ROSC) и перехода. Аэрация ранее заполненных жидкостью легких необходима для снижения легочного сосудистого сопротивления (PVR) и увеличения легочного кровотока. Легочный кровоток имеет жизненно важное значение как для оксигенации, так и для сердечного выброса, поскольку он заменяет возврат пупочной вены в качестве источника предварительной нагрузки на левый желудочек.7
После пережатия пуповины у младенца с апноэ с устойчивым кровообращением происходит 50% Снижение сердечного выброса, вторичным по отношению к внезапному увеличению, является системным сосудистым сопротивлением и постоянством высокого ЛСС.Сердечный выброс восстанавливается с началом вентиляции.8 У ребенка, который уже находится в состоянии гипоксии, на этот раз до установления FRC может усугубить ишемическое повреждение. Было показано, что вентиляция перед пережатием пуповины улучшает колебания сердечного выброса и церебральной перфузии9, а Клюков и Хупер8 предлагают отсрочить пережатие пуповины до начала вентиляции. Это потребует значительных изменений в практике родильного отделения, что потребует тесного сотрудничества между акушерским и неонатальным персоналом.Текущие европейские и британские руководящие принципы неонатальной жизнеобеспечения (NLS) 2015 года, а также рекомендация Международного комитета по связям по реанимации (ILCOR) рекомендуют отсроченное пережатие пуповины продолжительностью не менее минуты у младенцев, не нуждающихся в реанимации; 6, 10 необходимы дальнейшие исследования, чтобы определить, есть ли Реанимация ребенка с асфиксией с незажатой пуповиной приносит пользу. Зачистка (или «доение») пуповины не рекомендуется в качестве рутинной меры, кроме как в контексте дальнейших рандомизированных исследований.
Оптимальная стратегия вентиляции для достижения FRC и последующего перехода в апноэ неясна. Европейские руководящие принципы рекомендуют использовать 5 3-секундных вдохов-выдохов, в то время как американские руководящие принципы поддерживают традиционную вентиляцию.10 Было показано, что более продолжительное (20-30 секунд) устойчивое надувное дыхание ускоряет ROSC и переходный период на модели животных с асфиксией по сравнению с традиционной или «короткие» устойчивые инфляции.11 Однако длительное инфляция приводила к более быстрому и большему увеличению доставки кислорода в мозг и была связана с увеличением церебральной экстравазации и разрушения кровеносных сосудов у ягнят, подвергшихся асфиксии.12 Таким образом, нет достаточных доказательств, подтверждающих использование длительной устойчивой инфляции для реанимации ребенка, страдающего асфиксией, и следует сделать 5 трехсекундных вдохов-выдохов10. Токсичность реанимации с использованием 100% кислорода теперь хорошо установлена. Метаанализ 2133 младенцев13 показал снижение смертности младенцев, реанимированных при помощи 21% кислорода по сравнению со 100% кислородом (относительный риск (ОР) 0.69, 95% ДИ от 0,54 до 0,88) и тенденцию к снижению ГИЭ. В моделях неонатальной асфиксии на животных реанимация с использованием 21% кислорода по сравнению со 100% приводила к сопоставимым или улучшенным исходам смерти, нейроповеденческой инвалидности и гибели клеток14. кровоток (это противоречит здравому смыслу, поскольку церебральная вазоконстрикция является типичной реакцией на кислород) .15 Гипоксический мозг, возможно, потерял способность к ауторегуляции и стал «пассивным по давлению», что увеличивает риск гипероксии и вызванного кровотоком повреждения мозга.Нет никаких клинических исследований, изучающих пользу дополнительного кислорода, начинающегося во время реанимации, для младенца, нуждающегося в обширных мерах, то есть в компрессии грудной клетки.6 Текущая рекомендация ILCOR6 заключается в том, чтобы реанимацию всех доношенных детей начинали на воздухе, и чтобы это было увеличивается для младенцев, не достигших ROSC с помощью активных мер. Рекомендуется снизить содержание кислорода, как только восстановится частота сердечных сокращений. Концентрация кислорода для введения неизвестна, и это область для текущих исследований.Европейские руководящие принципы NLS предлагают использовать пульсоксиметрию, особенно при родах, при которых ожидается, что у младенца будут проблемы; 10 на основе нормативных данных ниже приводится руководство по приемлемым целевым показателям предуктальной сатурации кислорода (SpO 2 ) во время реанимации — 2 мин. после рождения 60%, 3 мин. 70%, 4 мин. 80%, 5 мин. 85% и 10 мин. 90% .16
Обновленные европейские рекомендации NLS 2015 г. предполагают, что попытки аспирации мекония из носа и рта еще не родившегося ребенка , пока голова все еще находится на промежности, не рекомендуется, и нельзя откладывать начало инфляции легких в течение первой минуты жизни у недышащих или неэффективно дышащих младенцев.Разумно быстро осмотреть ротоглотку, чтобы удалить потенциальные препятствия, но интубация трахеи не должна быть рутинной при наличии мекония.10
Использование адреналина во время реанимации новорожденных считается стандартным уходом за младенцами с ЧСС <60 уд / мин. не отреагировал на адекватную вентиляцию и сжатие грудной клетки. Доказательства этой практики основаны на исторических сериях случаев и экстраполированы на педиатрические и взрослые исследования.17 Недавнее исследование на асфиксированных ягнятах поддерживает использование адреналина у новорожденных, демонстрируя, что одно только сжатие грудной клетки не привело к увеличению среднего каротидного кровотока. и что адреналин был необходим для повышения диастолического и среднего каротидного (и, вероятно, коронарного) артериального давления, а затем для достижения ROSC.18 Рекомендуемая внутривенная доза адреналина составляет 10 мкг / кг (0,1 мл / кг раствора 1:10 000). Если это неэффективно, можно попробовать дозу до 30 мкг / кг (0,3 мл / кг раствора 1:10 000 ).10 Эндотрахеальный адреналин в более высоких дозах (50–100 мкг / кг) можно использовать, когда внутривенный путь недоступен.10,17 Бикарбонат натрия не рекомендуется во время кратковременной реанимации. Если он используется во время длительных остановок, его следует вводить только после того, как будет установлена адекватная вентиляция и кровообращение (с компрессией грудной клетки).Доза бикарбоната натрия составляет от 1 до 2 ммоль бикарбоната / кг (2–4 мл / кг 4,2% раствора бикарбоната). Гипогликемия может возникнуть в родильном отделении и, как известно, усугубляет травму; следует учитывать глюкозу, если не было ответа на другие препараты, вводимые через центральный венозный катетер (доза глюкозы (10%) составляет 2,5 мл / кг (250 мг / кг)). 10
В прошлом предлагалось руководство Прекращение реанимации новорожденных через 10 мин у младенца с сохраняющейся асистолией, несмотря на адекватную реанимацию.Это было основано на данных, полученных в период до терапевтической гипотермии, которые показали высокую смертность и нарушения нервного развития у выживших с ROSC через 10 минут. В более поздних публикациях показано улучшение исходов для младенцев с 0 баллом по шкале Апгар через 10 мин как для охлажденных, так и для неохлаждаемых младенцев. Показатели выживаемости без инвалидности составляли от 20,5% (нормотермия) до 27% (охлаждение) через 24 месяца в недавнем метаанализе19 и 20,8% через 6-7 лет при последующем наблюдении за исследованием охлаждения NICHD.20 Консенсус ILCOR 2015 г. наука и европейские рекомендации NLS 2015 года по-прежнему поддерживают прекращение приема через 10 минут, хотя и рекомендуют индивидуальный подход к принятию решений с учетом адекватности реанимации, доступа к охлаждению и мнения родителей.6, 10
Для младенцев, нуждающихся в обширной реанимации и переживших ее, следует заранее подумать о терапевтической гипотермии, которая более подробно обсуждается ниже. Терапевтическая гипотермия наиболее эффективна, когда ее начинают как можно ближе к моменту гипоксически-ишемического события. Наша практика и рекомендации — поддерживать нормотермию (избегать гипертермии) до тех пор, пока старший врач не примет решение о лечении с помощью охлаждения. После этого можно как можно скорее запустить пассивное охлаждение, обычно в родильном зале, отключив лучистые обогреватели.Затем можно начать активное охлаждение в неонатальном отделении. Для младенцев, рожденных в центрах, не обеспечивающих интенсивной терапии, младенцев следует незамедлительно обсудить с неонатальным отделением третичного уровня. Охлаждение должно быть начато как можно скорее в справочном центре и / или транспортной службой. Доступно клиническое руководство по охлаждению при транспортировке.21 Недавнее клиническое испытание в условиях транспортировки продемонстрировало, что активное охлаждение с использованием устройства с сервоуправлением привело к достижению целевой температуры большим количеством детей, чем при пассивном охлаждении.22
С этого момента используется термин ГИЭ, поскольку предполагается, что другие возможные этиологии энцефалопатии исключены.
Поддерживающая терапия
Младенцы с ГИЭ могут иметь степень полиорганной дисфункции. Гипоксический плод инициирует рефлекс ныряния, чтобы сохранить приток крови к жизненно важным органам, включая мозг, сердце и надпочечники, за счет притока к коже, внутренним сосудам, печени и почкам. отделение должно отражать возможное гипоксическое повреждение органов и быть индивидуальным.
Часто встречаются острый некроз канальцев и синдром несоответствующего антидиуретического гормона, а также нарушение функции печени. Вначале следует ограничить парентеральное введение жидкости, поскольку у младенцев будет олигурия; мы обычно ограничиваем потребление жидкости до 40 мл / кг / день, пока диурез не начнет увеличиваться. Мы вводим парентеральное питание через центральный венозный катетер. Трофическое кормление можно начинать по мере поступления молозива; обычно объем корма не увеличивается по сравнению с трофическим кормлением до тех пор, пока после согревания ребенок не находится в состоянии меньшего успокоения.Лекарства, требующие метаболизма почек и печени, особенно с нефротоксичностью, следует применять с осторожностью. Следует избегать гипергликемии и гипогликемии, так как обе связаны с длительной нетрудоспособностью в возрасте 18 месяцев или смертью младенцев с ГИЭ средней и тяжелой степени.24 Некоторые исследования предполагают особую связь гипогликемии с неблагоприятным исходом25 и операционный порог для принятия мер по повышению уровень глюкозы в крови у младенцев с ГИЭ выше, чем у здоровых доношенных детей (> 2.5 ммоль / л против> 2,0 ммоль / л). Может возникнуть коагулопатия из-за гипоксически-ишемического повреждения печени и костного мозга. Кроме того, переохлаждение снижает агрегацию тромбоцитов, снижает ферментативную функцию в каскаде свертывания и может вызвать диссеминированное внутрисосудистое свертывание. Исследования коагуляции следует контролировать ежедневно во время охлаждения, поскольку лабораторные доказательства коагулопатии универсальны у детей с ГИЭ, подвергающихся охлаждению. Стратегии переливания для поддержания количества тромбоцитов> 130 × 10 9 / л, фибриногена> 1.5 г / л и МНО <2 могут предотвратить клиническое кровотечение26.
Гипотония наблюдается у 62% младенцев с ГИЭ; Инотропная поддержка ГИЭ была недавно рассмотрена.27 Сердечные тропонины I и Т являются признанными маркерами ишемии миокарда и сердечной недостаточности у взрослых, детей и новорожденных. Было показано, что при ГИЭ уровни тропонина Т достигают пика в первый день, остаются повышенными в течение первой недели и коррелируют с тяжестью ГИЭ.28 Терапевтическая гипотермия снижает сердечный выброс на 67%, и обычно требуется усиление поддержки. период охлаждения.27
Факторами, способствующими легочной дисфункции, являются нарушение центрального контроля дыхания, легочная травма, персистирующая легочная гипертензия (PPHN) и аспирация мекония. Следует внимательно следить за адекватностью вентиляции и поддерживать PaO 2 и парциальное давление углекислого газа в пределах нормы. Следует проводить коррекцию ацидоза и гипоксии, чтобы избежать дополнительных травм головного мозга и ПРГН; следует избегать гипероксии и гипокарбии, поскольку они пагубны для долгосрочного исхода29, 30
Управление припадками
Припадки — обычная черта ГИЭ; однако следует отметить, что около 34% неонатальных припадков имеют клинические признаки, которые можно увидеть, и только 27% из них были правильно идентифицированы неонатальным персоналом.Кроме того, более 70% того, что считается приступами, не связаны с эпилептиформными разрядами на электроэнцефалограмме (ЭЭГ), что подчеркивает важность нейрофизиологического мониторинга.31 При ГИЭ приступы обычно возникают в первый день, а приступы наблюдаются раньше, чем через 6 часов. возраст должен вызвать подозрение в более раннем внутриутробном инсульте. Судороги увеличивают метаболические потребности мозга, вызывают высвобождение возбуждающего нейромедиатора и вызывают кардиореспираторную нестабильность, усугубляя повреждение нейронов. Повышенная судорожная нагрузка была значительно независимо связана с более тяжелой травмой на МРТ (OR 5.00, 95% ДИ 1,47–17,05, p = 0,01) 32 и с более низкими оценками при последующем наблюдении за развитием нервной системы через 18 месяцев.33 Терапевтическая гипотермия снижает бремя судорог у младенцев с легкой или средней, но не тяжелой, HIE34. судороги можно увидеть при повторном согревании.32
Не существует универсальных руководств по ведению судорог при ГИЭ новорожденных со стратегиями, различающимися в разных центрах. Эпилептический статус и частые припадки следует лечить, хотя есть споры о том, следует ли лечить менее частые припадки или только электрографические (т. Е. Не клинически очевидные) припадки.В одном исследовании лечение электрографических приступов с использованием амплитудно-интегрированной ЭЭГ (аЭЭГ) по сравнению с лечением клинических приступов (скрытая аЭЭГ) было связано с более низкой судорожной нагрузкой и менее серьезными оценками повреждений при МРТ. Однако не было никакой разницы в исходах развития через 18 месяцев.33
Противосудорожным препаратом первой линии является фенобарбитон, 35 хотя он может контролировать судороги только у 50% новорожденных.36 Общие препараты второй линии включают фенитоин, бензодиазепины, а в Европе лидокаин.Учитывая потенциальную токсичность и ограниченную эффективность этих традиционно используемых лекарств, ведется поиск новых агентов. Имеется ограниченная информация о фармакокинетике, эффективности, токсичности и дозировке новых противосудорожных средств (например, леветирацетама и топирамата) для новорожденных — имеется недавний обзор37. биодоступность, отсутствие лекарственного взаимодействия и связывания с белками) и уже не по назначению в некоторых центрах.Важно установить безопасность и эффективность, о чем свидетельствует недавнее исследование аналогичного многообещающего агента, буметанида, которое показало низкую эффективность и увеличение слуха.38 Кокрановский обзор продемонстрировал отсутствие доказательств в поддержку использования профилактических средств. противосудорожные препараты после перинатальной асфиксии.39 Противосудорожные препараты обычно требуются только в первую неделю, потому что судороги являются «острыми симптоматическими» и со временем исчезают. Иногда у детей с тяжелыми заболеваниями требуется более длительная терапия.
Сравнение неонатальной энцефалопатии и гипоксико-ишемической энцефалопатии
Неонатальная энцефалопатия (NE) — комплексный синдром, характеризующийся судорогами, измененным уровнем сознания и / или неспособностью инициировать или поддерживать дыхание. 1 Хотя заболеваемость варьируется, по оценкам, поражаются до 3 случаев на 1000 живорождений. 2 Младенцы могут демонстрировать полиорганную, а также неврологическую дисфункцию. 3 NE — это «зонтичный» термин, не описывающий конкретную этиологию. Терапевтическая гипотермия — единственное одобренное лечение, кроме поддерживающей интенсивной терапии. 4 Хотя существует несколько причин NE, включая гипоксию-ишемию (приводящую к гипоксически-ишемической энцефалопатии (ГИЭ)), перинатальные инфекции, плацентарные аномалии, метаболические нарушения, коагулопатии и сосудистый инсульт новорожденных, более чем в половине случаев причина не установлена случаи. 5
Термины HIE и NE взаимозаменяемы в литературе при описании новорожденных людей и животных. Ранее бывшие редакторы Pediatric Research Олаф Дамманн и Пьер Грессенс призывали уточнить определение с помощью термина NE. Однако это уточнение не нашло отражения в литературе. Термин ГИЭ очень уместно использовать в модели на животных, где имеется четко очерченная подверженность гипоксии, ишемии или обоим. У младенцев-людей такие явления, как выпадение пуповины, разрыв матки или отслойка плаценты, могут быть явно связаны с ГИЭ, но часто ГИЭ является вторичным явлением.Следовательно, хотя гипоксия-ишемия может иметь место, известно, что она является единственным возбудителем энцефалопатии примерно у 7% младенцев с НЭ. 6 Реестр неонатальной энцефалопатии Оксфордской сети штата Вермонт обнаружил, что асфиксия составляла 15%, а воспаление — 24% случаев NE с другой материнской этиологией ( n = 4165). 5
Следовательно, все другие этиологии энцефалопатии охватываются термином NE, включая метаболические, септические, тромбоэмболические и генетические.Определенных биомаркеров ГИЭ у людей нет. Хотя были предложены суррогаты, такие как ядросодержащие эритроциты, pH пуповинной артериальной крови, тропонин, на животных моделях не было обнаружено корреляции с определенным измеренным воздействием гипоксии. Лечение таких состояний, как сепсис, и исследования по изменению генетических и метаболических причин могут быть затруднены из-за предположения, что диагноз — ГИЭ. Использование обобщающего термина NE позволяет клиницисту более точно изучить этиологию.
Было предложено использовать термин NE для доношенных и поздних недоношенных новорожденных, у которых не было выявленных дозорных явлений. 7,8 Трудно доказать наличие церебральной гипоксической ишемии, за исключением хорошо изученных моделей на животных и частных случаев неонатального инсульта. Все текущие параметры, включая pH пуповинной крови и судороги, неспецифичны. 7 Некоторые из паттернов черепно-мозговых травм, наблюдаемых у пациентов с NE, могут быть воспроизведены на животных моделях с помощью гипоксии-ишемии, но это не доказывает, что все NE вызваны HIE. 7 Несколько опубликованных популяционных исследований показали, что дородовые и неасфиксионные факторы риска связаны с НЭ. 8 Напротив, некоторые авторы утверждают, что ГИЭ является причиной НЭ в 50–80% случаев на основании клинических критериев, критериев ЭЭГ и МРТ. 1 На МРТ для HIE можно увидеть другую картину повреждения по сравнению с другими причинами NE, но это открытие не исключает HIE или других причин NE в качестве причины травмы. Характер повреждения при ГИЭ зависит от тяжести, продолжительности и повторяемости гипоксии-ишемии и может привести к поражению базальных ганглиев, таламуса, ствола мозга и / или белого вещества головного мозга в различных комбинациях. 1
Отсутствие общепринятого термина для описания младенцев с НЭ и другими причинами энцефалопатии влияет на улучшение их результатов, поскольку препятствует более широким сетям сотрудничества и будущему развитию мегаиспытаний. Мы полагаем, что для изучения NE в широком международном сотрудничестве, консенсус по названию состояния является существенным. Затем это позволит подразделить на различные группы по этиологии, которым могут быть полезны более индивидуализированные схемы лечения.
Ссылки
- 1.
Volpe, J. J. Неонатальная энцефалопатия: неадекватный термин для гипоксически-ишемической энцефалопатии. Ann. Neurol. 72 , 156–166 (2012).
Артикул
Google Scholar
- 2.
Куринчук Дж. Дж., Уайт-Конинг М. и Бадави Н. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии. Early Hum. Dev. 86 , 329–338 (2010).
Артикул
Google Scholar
- 3.
Шах П., Рип Хаген С., Бейен Дж. И Перлман М. Мультиорганная дисфункция у младенцев с постасфиксиальной гипоксически-ишемической энцефалопатией. Arch. Дис. Child Fetal Neonatal Ed. 89 , F152 – F155 (2004).
CAS
СтатьяGoogle Scholar
- 4.
Jacobs, S.E. et al. Охлаждение новорожденных с гипоксической ишемической энцефалопатией. Кокрановская база данных Syst. Ред. 1 , CD003311 (2013).
Google Scholar
- 5.
Nelson, K. B. et al. Антецеденты неонатальной энцефалопатии в реестре энцефалопатии Оксфордской сети штата Вермонт. Педиатрия 130 , 878–886 (2012).
Артикул
Google Scholar
- 6.
Badawi, N. et al. Факторы дородового риска энцефалопатии новорожденных: исследование случай-контроль в Западной Австралии. BMJ 317 , 1549–1553 (1998).
CAS
СтатьяGoogle Scholar
- 7.
Дамманн, О., Ферриеро, Д. и Грессенс, П. Энцефалопатия новорожденных или гипоксически-ишемическая энцефалопатия? Соответствующая терминология имеет значение. Pediatr. Res. 70 , 1-2 (2011).
Артикул
Google Scholar
- 8.
Нельсон, К. Б. Это он? И почему это важно. Acta Paediatr. 96 , 1113–1114 (2007).
Артикул
Google Scholar
Скачать ссылки
Информация об авторе
Место работы
Педиатрия, Академический центр, Таллахтский университет. Больница Тринити-колледжа Дублинского университета, Институт трансляционной медицины Тринити, больница Святого Джеймса, Дублин; Неонатология, Университетская больница Кумб для женщин и младенцев, Дублин; Неонатология, Детская больница Богоматери, Крамлин, Дублин, Ирландия
Элеонора Дж.Моллой
Кафедра педиатрии Медицинского факультета Университета Мэриленда, Балтимор, США
Синтия Беэрр
Авторы
- Элеонора Дж. Моллой
- Синтия Бэрэр
Автор, отвечающий за переписку
Элеонора Дж. Моллой.
Декларации этики
Конкурирующие интересы
Авторы заявляют об отсутствии конкурирующих интересов.
Дополнительная информация
Примечание издателя: Springer Nature сохраняет нейтралитет в отношении юрисдикционных претензий на опубликованных картах и институциональной принадлежности.
Об этой статье
Цитируйте эту статью
Моллой, Э.Дж., Бирер, К. Неонатальная энцефалопатия в сравнении с гипоксически-ишемической энцефалопатией.
Pediatr Res 84, 574 (2018). https://doi.org/10.1038/s41390-018-0169-7
Скачать цитату
Дополнительная литература
СОГЛАСОВАННОСТЬ: основные результаты при неонатальной энцефалопатии (протокол)
- Фиона А.Куирк
- , Патрисия Хили
- , Элейн Ни Бхраонаин
- , Мэнди Дейли
- , Линда Биести
- , Тим Херли
- , Карен Уокер
- , Ширин Мехер
- , Дэвид М. Хаас
- , Фрэнк Х. Блумфилд
- , Джейми Дж. Киркхэм
- , Элеонора Дж. Моллой
- и Деклан Девейн
Испытания
(2021 год)Перспективы Общества педиатрических исследований.Клинические испытания неонатальной энцефалопатии: развитие будущего
- Кристен Л. Беннингер
- , Терри Э. Индер
- , Эми М. Гудман
- , К. Майкл Коттен
- , Дуглас Р. Нордли
- , Тушар А. Шах
- , Джеймс К. Слотер
- И Натали Л. Мэтр
Педиатрические исследования
(2021 год)Циркулирующие белки плотных соединений являются потенциальными биомаркерами функции гематоэнцефалического барьера в модели неонатального гипоксического / ишемического повреждения головного мозга.
- E.Аксель Андерссон
- , Карина Маллард
- и К. Йоаким Эк
Жидкости и барьеры ЦНС
(2021 год)Лечение мелатонином новорожденных с гипоксической ишемической энцефалопатией
- Тим Херли
- , Мэри О’Ди
- , Сайма Аслам
- , Хани Али
- , Никки Робертсон
- и Элеонора Моллой
Кокрановская база данных систематических обзоров
(2020)Оценка этиологии неонатальной энцефалопатии и диагностика FIRS
Семинары по медицине плода и новорожденного
(2020)
Гипоксически-ишемическая энцефалопатия — Советчик по терапии рака
Более поздняя шкала Миллера и соавторов была утверждена в качестве простого прикроватного инструмента для прогнозирования 30-дневного исхода развития нервной системы.Эта шкала аналогична шкале Сарната и Сарната, но добавляет в оценку статус питания и дыхания. Также распознаются более тонкие градации аномалий со шкалой от 0 (отсутствие энцефалопатии) до 6 (тяжелая энцефалопатия). См. Таблицу II.
Таблица II.
| Оценка = 0 | Оценка = 1 | |
|---|---|---|
| Кормление | нормальный | Кормление через желудочный зонд, гастростомический зонд или непереносимость кормления |
| Предупреждение | Предупреждение | раздражительный, плохо реагирующий или коматозный |
| Тон | нормальный | Гипо- или гипертония |
| Респираторный статус | нормальный | Дыхательная недостаточность |
| Рефлексы | нормальный | Гипоррефлексия, гиперрефлексия или ее отсутствие |
| Изъятия | Нет | Подозреваемые или подтвержденные |
Какое другое заболевание / состояние имеет некоторые из этих симптомов?
Симптомы ГИЭ могут быть нечеткими и часто перекрывают многие неврологические и метаболические состояния новорожденного.Общие состояния в термине новорожденный, которые могут быть ошибочно приняты за ГИЭ, включают инфекцию (например, сепсис), метаболические нарушения или врожденные нарушения обмена веществ, другие судороги (структурные, метаболические, генетические), артериальный ишемический или геморрагический инсульт или венозный тромбоз синуса головного мозга. Из-за этой общности симптомов необходимо исключить опасные для жизни или излечимые причины этих симптомов.
Что послужило причиной развития этой болезни в это время?
Конечная патофизиология ГИЭ плохо изучена, несмотря на обилие исследований.Известно, что роды — это период высокого риска сосудистых нарушений головного мозга. Незрелость сосудистой сети головного мозга и ауторегуляция, наряду с повышенной уязвимостью белого вещества у новорожденных, способствуют развитию ишемической болезни. Воспаление, эксайтотоксичность и окислительный стресс — все это важные медиаторы ГИЭ и гибели клеток от апоптоза или некроза. Апоптоз, скорее всего, играет важную роль в неонатальном повреждении головного мозга, связанном с ГИЭ, а не некрозом. Апоптоз является важным элементом нормального развития мозга, сокращая и определяя клеточные пути и связи.Аберрантный апоптоз подвергает развивающийся мозг повышенному риску нарушения развития нервной системы.
Известно, что перинатальная асфиксия, гипотония или аноксия являются основными факторами риска ГИЭ. Однако у многих из этих младенцев нет четкого анамнеза перинатальной аспиксии, и, таким образом, весь механизм травмы до сих пор неизвестен.
Какие лабораторные исследования следует запросить для подтверждения диагноза? Как следует интерпретировать результаты?
Поскольку симптомы могут перекрывать многие неврологические и метаболические состояния новорожденного, необходимо исключить опасные для жизни или излечимые причины этих симптомов.Важные лабораторные исследования, которые необходимо заказать, чтобы исключить эти условия, включают следующее:
Общий анализ крови с дифференциалом
Помогает исключить заражение
Уровень тромбоцитов может быть низким при ГИЭ
Комплексная метаболическая панель, включая функциональные пробы печени (LFT) и определение аммиака и лактата
Помогает исключить нарушение обмена веществ
Повышенный уровень аммиака указывает на дефицит цикла мочевины и требует экстренного диализа
Уровень лактата может быть повышен при метаболическом заболевании или только при ГИЭ
LFT и уровни азота / креатинина мочевины в крови могут быть ненормальными при ГИЭ
Посев крови
Исключить сепсис
Люмбальная пункция (LP), включая подсчет клеток, культуру, уровни белка и глюкозы
Исключить инфекцию центральной нервной системы
Низкий уровень глюкозы может указывать на нарушение транспорта глюкозы
Повышенный уровень лактата может указывать на нарушение обмена веществ
Второй LP может потребоваться для дальнейшей оценки метаболизма или нейромедиатора
Могут ли быть полезны визуализирующие исследования? Если да, то какие?
Визуализация головы может быть особенно полезна как для диагностики, так и для прогнозирования ГИЭ.Магнитно-резонансная томография (МРТ) является предпочтительным методом визуализации головы (см. Ниже).
Ультразвуковое исследование черепа (УЗИ) часто является первым изображением головы новорожденного из-за простоты и доступности. CUS может исключить внутричерепное кровоизлияние и в руках опытного ультразвукового врача может выявить ишемию. Однако нормальное сканирование на CUS не исключает ишемию, поскольку большая часть ишемии пропускается при CUS.
МРТ головного мозга является предпочтительным методом визуализации. Это чрезвычайно полезно для выявления моделей ишемического повреждения.Однако МРТ не может полностью охарактеризовать степень повреждения при незрелой миелинизации. В центрах, где часто проводят МРТ новорожденных, седация не требуется. Что наиболее важно, МРТ может помочь в прогнозировании (см. Ниже).
Компьютерная томография головы не идеальна из-за радиации и высокого содержания воды в мозге новорожденных. Однако его можно заказать, если МРТ недоступно и есть опасения по поводу кровотечения. Обычное компьютерное томографическое сканирование головы не исключает ишемию, поэтому всегда следует проводить контрольную МРТ.
Если вы можете подтвердить, что у пациента есть это заболевание, какое лечение следует начать?
Доношенных новорожденных с ГИЭ следует переводить в отделение интенсивной терапии, учитывая их критический характер. Лечение можно разделить на немедленное / стационарное и долгосрочное.
Немедленное / больничное управление
Респираторная опора
Катетер артериальной линии / пупочной артерии для измерения артериального давления и газов артериальной крови
Катетер для забора крови в пупочную вену
Поддержание церебральной перфузии путем контроля гипотензии, брадикардии и / или апноэ
Коррекция ацидоза по необходимости
Поддержание эугликемии
Контроль температуры
Лекарства от конфискации
Лоразепам 0.5 мг внутривенно (в / в) при необходимости при припадке
Фенобарбитал 20 мг / кг внутривенно для стойких припадков / эпилептического статуса; поддерживающая доза обычно составляет около 5 мг / кг / сут, но новорожденные могут быстро ее усвоить, и для достижения эффекта может потребоваться более интенсивное измельчение дозы (с учетом побочных эффектов)
Леветирацетам 20-30 мг / кг внутривенно при стойких припадках / эпилептическом статусе; поддерживающая начальная доза 15 мг / кг внутривенно или перорально два раза в день
Гипотермия (см. Ниже)
Длительное лечение может включать:
При необходимости принять лекарство от судорог (в большинстве случаев приступы прекращаются через 3-4 дня после рождения)
Лечебная физкультура
Трудотерапия
Логопед
Поведенческая или когнитивная терапия
Специальное образование
Вспомогательные устройства (т.э., артоз голеностопного сустава, шина на запястье)
Какие побочные эффекты связаны с каждым вариантом лечения?
Любое лечение в отделении интенсивной терапии сопряжено с риском. Побочные эффекты, наблюдаемые при обычном лечении ГИЭ, включают следующее:
Пупочные катетеры
Тромбообразование
Лекарства от конфискации
Повышенная сонливость
Плохое питание вследствие сонливости
Гипотермия
Относительно безопасно в клинических исследованиях
Сердечные аритмии
Нарушения коагуляции
Каковы возможные исходы этого заболевания?
Как описано выше, исход ГИЭ зависит от степени энцефалопатии и области повреждения головного мозга.Энцефалопатия легкой степени связана с нормальным нейрокогнитивным и двигательным исходом. Тяжелая энцефалопатия приводит к ранней смерти; у тех новорожденных, которые выживают, остаются плохие нейрокогнитивные и моторные результаты.
Умеренная энцефалопатия является наиболее разнородной группой и поэтому связана с самым широким диапазоном как когнитивных, так и двигательных исходов. МРТ может быть особенно полезной для прогноза в этой популяции. Повреждение базальных ганглиев приводит к наиболее тяжелым когнитивным и двигательным последствиям, тогда как травма водораздела обычно приводит к изолированному когнитивному дефициту.Кроме того, нейрокогнитивные нарушения обычно не проявляются до школьного возраста. Следовательно, для раннего распознавания и вмешательства следует проводить постоянный нейропсихологический скрининг.
Что вызывает это заболевание и как часто оно встречается?
ГИЭ является довольно распространенным явлением и встречается примерно у 1-6 детей из 1000 живорожденных. Пятая часть детей с ГИЭ умирает в период новорожденности. ГИЭ также ассоциируется с высокой заболеваемостью; до четверти выживших продолжают иметь распознаваемые моторные и / или когнитивные нарушения.В настоящее время нет известной генетической предрасположенности к ГИЭ.
Известные факторы риска ГИЭ включают асфиксию при рождении или длительное снижение церебрального кровотока (например, отслойку плаценты или гипотензию). Однако во многих случаях ГИЭ в анамнезе нет явной асфиксии или нарушения мозгового кровотока. Из-за этого отсутствия связи некоторые поставщики предпочитают использовать термин «неонатальная энцефалопатия» или «NE» вместо HIE.
Как эти патогены / гены / воздействия вызывают болезнь?
Как описано выше, головной мозг новорожденного особенно подвержен травмам, особенно во время родов и родоразрешения.Избирательная уязвимость незрелых олигодендрий объясняет повреждение белого вещества, наблюдаемое при ГИЭ. Известно, что длительное снижение мозгового кровотока вызывает кислородную и глюкозную недостаточность. Снижение мозгового кровотока также затрудняет выведение токсичных субстратов (например, оксида азота). Воспаление, эксайтотоксичность и окислительный стресс дополнительно опосредуют повреждение и гибель клеток (апоптоз). Тем не менее, во многих случаях ГИЭ нет очевидного асфиксического / гипоксического инсульта, и поэтому точный механизм повреждения остается неясным.
Другие клинические проявления, которые могут помочь в диагностике и лечении
Непрерывный электроэнцефалографический мониторинг все чаще признается важным инструментом лечения и прогноза ГИЭ у новорожденных, получавших гипотермию. Нормальная электроэнцефалограмма (ЭЭГ) является прогностическим признаком нормального или слегка ненормального МРТ, тогда как устойчивая сильно аномальная ЭЭГ (подавление вспышек или чрезвычайно низкое напряжение) во время охлаждения дает плохой прогноз.Амплитудно-интегрированная электроэнцефалография может быть дополнительным критерием оценки результатов ГИЭ; исследования продолжаются.
Какие осложнения можно ожидать от болезни?
Осложнения за пределами нейроаксиса часто наблюдаются при ГИЭ. Выявленные осложнения (но не ограничиваясь ими):
Острый
Долгосрочные
Как можно предотвратить это заболевание?
В настоящее время не существует профилактического препарата или вмешательства, которое могло бы предотвратить ГИЭ. Терапевтическая гипотермия — это широко применяемая терапия, помогающая предотвратить острую травму головного мозга при ГИЭ.Хотя терапевтическая гипотермия не может предотвратить ГИЭ, было показано, что она снижает заболеваемость и неврологическую смертность в возрасте 18–24 месяцев.
Какие доказательства?
Миллер, С.П., Латал, Б., Кларк, Х., Барнуэлл, А. «Клинические признаки предсказывают 30-месячный исход развития нервной системы после неонатальной энцефалопатии». Am J Obstet Gynecol. об. 190. 2004. pp. 93-9. (Авторы предлагают новую шкалу энцефалопатии, которая включает дополнительные клинические характеристики для прогнозирования 30-дневного исхода у доношенных новорожденных с перинатальной асфиксией.Шестьдесят восемь доношенных новорожденных оценивались по бдительности, кормлению, тонусу, респираторному статусу, рефлексам и судорожной активности. Баллы варьируются от 0 (энцефалопатия отсутствует) до 6 (тяжелая энцефалопатия). Индекс умственного развития, двигательные исходы и смерть оценивались через 30 дней. Авторы обнаружили, что более высокий балл энцефалопатии коррелирует с худшим исходом.)
Shankaran, S, Laptook, AR, Ehrenkranz, RA. «Сеть неонатальных исследований Национального института детского здоровья и человеческого развития. Гипотермия всего тела новорожденных с гипоксически-ишемической энцефалопатией ». N Engl J Med. об. 353. 2005. С. 1574–84. (Это первое рандомизированное контролируемое клиническое испытание терапевтической гипотермии у доношенных новорожденных с асфиксией. Было обнаружено, что гипотермия всего тела снижает риск смерти и инвалидности у младенцев с энцефалопатией средней и тяжелой степени. Следует отметить, что существенной разницы не было. при церебральном параличе или средний индекс умственного развития всех выживших, независимо от гипотермии.)
Джейкобс, С.Е., Морли, С.Дж., Индер, Т.Э.«Сотрудничество по оценке охлаждения младенцев. Гипотермия всего тела для доношенных и недоношенных новорожденных с гипоксически-ишемической энцефалопатией: рандомизированное контролируемое исследование». Arch Pediatr Adolesc Med. 2011. (Авторы стремились определить безопасность и эффективность гипотермии всего тела для новорожденных с асфиксией в больницах без отделения интенсивной терапии новорожденных или оборудования для гипотермии. Новорожденные были рандомизированы на гипотермию по сравнению со стандартной медицинской помощью. грелка и применение холодных гелевых пакетов.Было обнаружено, что терапевтическая гипотермия снижает риск смерти или тяжелой инвалидности через 2 года. Авторы пришли к выводу, что этот метод гипотермии безопасен и эффективен, если применять его в течение 6 часов после рождения.)
Продолжающиеся споры относительно этиологии, диагностики и лечения
В настоящее время большинство крупных академических институтов и специализированных центров третичной медицинской помощи рассматривают терапевтическую гипотермию как стандарт лечения. Продолжаются исследования относительно полезности непрерывной амплитудно-интегрированной электроэнцефалографии или непрерывного обычного электроэнцефалографического мониторинга новорожденных с ГИЭ, а также полезности лечения субклинических припадков.
